Изобретение относится к аналитической химии, а именно к способу количественного определения суммы тритерпеновых кислот в экстракте древесной зелени Пихты Сибирской методом жидкостной хромато-масс-спектрометрии. Изобретение заключается в способе полуколичественного определения суммы тритерпеновых кислот в экстракте Пихты сибирской.
Экстракт Пихты сибирской обладает фунгицидными и стимулирующими рост свойствами, именно поэтому на данный момент актуально ведутся исследования, направленные на его применение в качестве средства защиты сельскохозяйственных растений. Основную стимулирующую активность по отношению к выращиваемым растениям проявляют тритерпеновые кислоты. Для разработки методов получения экстракта пихты с сохранением максимального количества тритерпеновых кислот в продукте, необходим контроль их содержания на каждой из стадий технологического процесса, позволяющий селективно определять их в присутствии жирных и смоляных кислот, также содержащихся в хвое.
Наиболее распространенным методом анализа тритерпеновых кислот является жидкостная хроматография. Чаще всего используются обращенно-фазовые сорбенты и УФ-детектор. Так, в работе [Ралдугин В. А. Тритерпеноиды пихты и высокоэффективный регулятор роста растений на их основе // Рос. хим. журн. – 2004. – Т. 86. – №. 3. – С. 84] рассматриваются способы анализа тритерпеноидов с применением смесей ацетонитрил – вода (91:9 по объему), ацетонитрил ─ 1,25% H3PO4 (86:14 по объему), ацетонитрил – вода, подкисленная фосфорной кислотой до 3 pH (90:10), метанол – 0,1%, муравьиная кислота (92:8), метанол – 0,03 М фосфатный буфер 2,8 pH (88:12 по объему), метанол – вода – тетрагидрофуран (94:5:1). Соединения детектируются на 206 нм, 210 нм, 212 нм, 220 нм. Однако данный способ определения не селективен, так как при данных длинах волн поглощают излучение любые соединения, обладающие хромофорными группами, в том числе жирные и смоляные кислоты перекрывающие пики тритерпеновых кислот.
В работе [Кучин А.В., Карманова Л.П., Хуршкайнен Т.В. Способ выделения биологически активной суммы кислот из древесной зелени пихты. Патент №2161149 РФ. 2000] описаны следующие условия анализа: микроколоночный жидкостный хроматограф «Милихром», колонка 6,3 х 0,2 см, сорбент «Лихросорб РП-18», зерно ─ 5 мкм, элюент ─ смесь 0,05 М водной ортофосфорной кислоты и метанола (15:85 по объему), УФ детекция при 200 и 240 нм. Однако, эта информация может подвергаться сомнению, так как в другом патенте [Патент РФ №2161149 C1, №2161149, кл. С 07 С 57/26, А 61 К 35/07, опубл. 27.12.2000 г.] при тех же условиях характерный максимум биологической суммы тритерпеновых кислот соответствует поглощению в области от 236 нм до 238 нм.
В работе [Ралдугин В. А. Тритерпеноиды пихты и высокоэффективный регулятор роста растений на их основе // Рос. хим. журн. – 2004. – Т. 86. – №. 3. – С. 84] описана методика анализа с применением более селективного метода ─ ВЭЖХ-ЯМР. В качестве подвижной фазы используют ацетонитрил-d3 ─ D2O (92:8). Данный метод требует использования дорогостоящих дейтерированных растворителей для приготовления подвижной фазы, а хроматографическая система не получила широкого использования и недоступна для лабораторий.
В работе [Pérez-Camino, M. C., & Cert, A. (1999). Quantitative Determination of Hydroxy Pentacyclic Triterpene Acids in Vegetable Oils. Journal of Agricultural and Food Chemistry, 47(4), 1558–1562 doi.org/10.1021/jf980881h] для количественного анализа тритерпеновых кислот использовали метод газовой хроматографии с пламенно-ионизационным детектором. Хроматографическое разделение проводили на газовом хроматографе Chrompack CP9000, оснащенном пламенно-ионизационным детектором, и капиллярной колонке SGL5 (25 м × 0,25 мм, 0,25 мкм), неподвижная фаза – фенилметилсилан (5%), (Sugelabor, Мадрид, Испания). Температурный режим: с 0 до 4 минут температура термостата колонки составляла 260 ℃, затем увеличивалась со скоростью 2 ℃/мин до 320 ℃. В качестве газа-носителя использовали водород. Условия пробоподготовки, описанные в работе, включают стадии жидкостно-жидкостной и твердофазной экстракции, а также дериватизации с использованием триметилхлорсилана в качестве дериватизирующего агента. Большое количество этапов пробоподготовки значительно увеличивает суммарное время анализа, а также снижает его точность, за счет возможных потерь исследуемых веществ. Помимо указанных недостатков, следует отметить, что в работе использовался только внутренний стандарт — бетулиновая кислота, а предварительная идентификация тритерпеновых кислот методом ГХ-МС (газовая хромато-масс-спектрометрия) не осуществлялась. В таком случае подвергается сомнению идентификация соединений (урсоловая, олеановая, маслиновая кислоты). Следует отметить, что дериватизации могут быть подвергнуты и другие соединения, содержащиеся в матрице; например, жирные и смоляные кислоты. Их времена удерживания могут совпадать с временами удерживания исследуемых кислот, что также понижает селективность анализа. Подобной неопределенности можно избежать, используя масс-спектрометрическое детектирование.
Прототипом является способ анализа, описанный в работе [Xiaoyan Liao, Fangli Hu & Zilin Chen (2019). A HPLC-MS method for profiling triterpenoid acids and triterpenoid esters in Osmanthus fragrans fruits. The Analyst doi.org/10.1039/C9AN01542F]. Для идентификации тритерпеновых кислот использован метод ВЭЖХ-МС/МС метод с использованием хроматографической системы LC-20AD (Shimadzu, Киото, Япония), совмещенной с масс-спектрометром API 4000 Qtrap, оснащенным источником электроспрей-ионизацией. Разделение проводилось на обращенно-фазовой колонке n Ultimate PAH геометрии 250×4.6 мм; 5 мкм (Welch Technologies, Shanghai, China) в градиентном режиме. Программа градиента: с 0 до 8 минут содержание фазы B возрастает с 65 до 71% B, с 48 до 62 минут – с 71 до 85% B, c 62 до 90 минут содержание B остается неизменным, после чего следует этап промывки и переуравновешивания колонки. Фаза A – 0,1% муравьиная кислота, фаза B – метанол для градиентной хроматографии. Объем инжекции – 5 мкл, температура термостата – 40oC, скорость потока – 0,8 мл/мин.
Несмотря на возможность различить структурные изомеры тритерпеновых кислот, у данного способа есть недостатки. Так, помимо тритерпеновых кислот, в пробе присутствуют и более гидрофобные соединения: терпены, жирные кислоты, церамиды и иные растительные липиды, которые могут приводить к загрязнению колонки. Также анализ одного образца занимает 90 минут, а для оптимизации масс-спектроскопических параметров необходимы стандартные образцы тритерпеновых кислот пихты, что увеличивает время стоимость анализа соответственно.
Техническая задача изобретения состоит в разработке способа полуколичественного определения суммы тритерпеновых кислот в экстрактах Пихты Сибирской методом жидкостной хромато-масс-спектрометрии.
Технический результат: достижение групповой селективности для тритерпеновых кислот, облегчение интегрирования пиков для определения суммы компонентов, сокращение времени анализа, отсутствие необходимости очистки экстрактов от более гидрофобных компонентов.
Технический результат достигается тем, что способ полуколичественного определения суммы тритерпеновых кислот в экстрактах Пихты Сибирской методом жидкостной хромато-масс-спектрометрии включает экстракцию ацетонитрилом и хроматографирование полученного раствора в анионообменном хроматографическом режиме смесью 0,1% раствора муравьиной кислоты и ацетонитрила для градиентного элюирования в соотношении 25 : 75 при объемной скорости потока 1,2 мл/мин, объеме инжекции 2 мкл, температуре термостата колонки 40 °С, детектированием с использованием масс-спектрометрического электроспрей-ионизационного детектора, работающего в режиме регистрации отрицательных ионов при следующих условиях напряжение на капилляре 3000 В, напряжение на сопле 1000 В, диапазон сканирования 150–550 m/z, Да, полуколичественное определение суммы тритерпеновых кислот по градуировочной зависимости в диапазоне от 0,05 до 0,50 мг/мл урсуловой или олеановой кислоты.
Заявленный способ полуколичественного определения суммы тритерпеновых кислот в экстрактах Пихты Сибирской методом жидкостной хромато-масс-спектрометрии состоит из следующих этапов:
1. Пробоподготовка
1.1 Исследуемые экстракты помещают в ультразвуковую ванну на 10 минут для повышения однородности пробы, вязкие образцы тщательно перемешивают.
1.2 Берут навеску 1 мг образца в эппендорф объемом 1,5 мл, и добавляют 1000 мкл ацетонитрила для градиентного элюирования и тщательно вортексируют. Эппендорф помещают в ультразвуковую ванну на 10 мин, затем повторно вортексируют в течение 20 секунд. Для отделения нерастворимого остатка образцы центрифугируют в течение 3 минут при 15000 оборотах в минуту. Надосадочную жидкость отбирают с помощью механического дозатора в чистый эппендорф вместимостью 1,5 мл. Экстракт высушивают в токе азота при комнатной температуре, остаток перерастворяют в 1 мл подвижной фазы.
2. Приготовление градуировочных растворов.
2.1 Строят многоточечную градуировочную зависимость в диапазоне от 0,05 до 0,50 мг/мл. В качестве внешнего стандарта используют урсоловую или олеановую кислоты. Для этого методом последовательного разбавления готовят сток-растворы в диапазоне концентраций от 0,1 до 10,0 (20,0) мг/мл, в качестве растворителя используют изопропиловый спирт. После чего в чистые эппендорфы добавляют по 50 мкл сток-растворов, 1000 мкл ацетонитрила и проводят пробоподготовку, аналогичную пробоподготовке реальных образцов. Остаток после осушения в токе азота перерастворяют в 1 мл подвижной фазы. При необходимости возможно расширить диапазон концентраций.
3. Анализ пробы: хроматографическое определение суммы тритерпеновых кислот проводят методом ВЭЖХ-МС высокого разрешения. Разделение веществ проводят на колонке YMC-Pack NH2 (150×4,6 мм; 5 мкм), в качестве элюента используют смесь 0,1% раствора муравьиной кислоты и ацетонитрила для градиентного элюирования в соотношении 25 : 75 (по объему) при объемной скорости потока 1,2 мл/мин; объеме инжекции – 2 мкл; температуре термостата колонки – 40 °С; детектирование осуществляют с использованием масс-спектрометрического электроспрей-ионизационного детектора, работающего в режиме регистрации отрицательных ионов. Напряжение на капилляре составляет 3000 В, напряжение на сопле – 1000 В, диапазон сканирования: 150–550 m/z, Да. Время анализа – 6 минут.
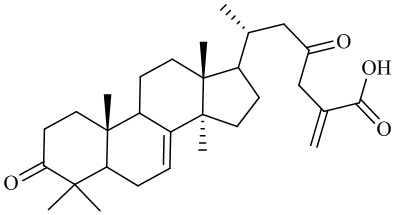
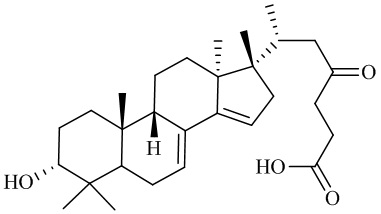
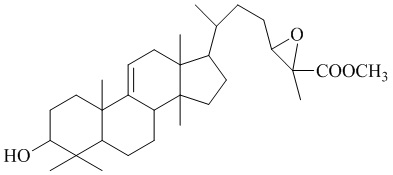
Разработанные хроматографические условия позволяют определить сумму тритерпеновых кислот с массой молекулярного иона 467,3; 469,3; 455,3; 481,3, а также ланостаноидов (метиловых эфиров тритерпеновых кислот) с массой молекулярного иона 485,3. Названия, структурные формулы веществ и соответствующие им массы молекулярных ионов представлены в таблице 1.
Таблица 1 – Тритерпеновые кислоты, содержащиеся в хвое пихты

мариесовая кислотаА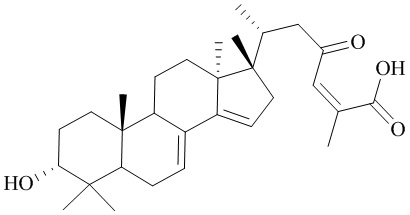
мариесовая кислота B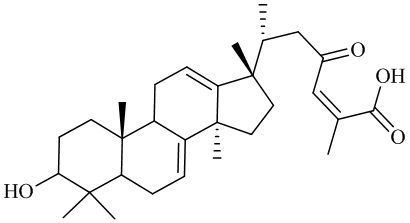







На фиг. 1 приведена хроматограмма образца экстракта лапок пихты "Образец 5" по выделенному ионному току.
Для стандартного образца (урсоловая или олеановая кислоты) определяют площадь хроматографического пика. Образец анализируют не менее двух раз. Полученную зависимость отношений массовой доли компонентов к массовой доле стандарта от отношения площадей хроматографического пика компонента к площади пика стандарта методом линейного регрессионного анализа интерполируют уравнением прямой. Градуировочная зависимость считается пригодной при коэффициенте корреляции не менее 0,90.
Массовую долю для каждой из групп изомерных кислот определяют по следующей формуле:
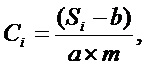
где Сi — концентрация компонента, мг/мл;
Si — площадь пиков по выделенному ионному току (EIC), соответствующих компонентам с одинаковой массой молекулярного иона, мВ×с;
a, b — коэффициенты градуировочной зависимости.
Суммарное содержание тритерпеновых кислот рассчитывают по формуле:

где C — суммарная концентрация компонентов, мг/мл;
Сi — концентрация компонента, мг/мл.
Ниже приведен пример осуществления изобретения.
Пример. Количественное определение суммы тритерпеновых кислот в образце пихтового масла «Образец 5»
Брали по 3 параллельных навески «Образца 5» в течение 3 дней, массы навесок приведены в таблице 2.
Таблица 2 – Массы навесок «Образца 5»
Навески образца помещали в чистые эппендорфы, добавляли 1000 мкл ацетонитрила, тщательно вортексировали, после чего помещали в ультразвуковую ванну Elma Panasonic P на 10 минут при частоте 37 кГц. Вортексировали повторно в течение 20 секунд, после чего центрифугировали при 15000 оборотах в минуту на микроцентрифуге CM-50. Супернатант переносили в чистый эппендорф и высушивали в токе азота с помощью концентратора NK-200. Остаток перерастворяли в подвижной фазе. Полученный раствор был гомогенным без видимых включений и опалесценции. Каждый раствор анализировали дважды.
Раствор хроматографировали по приведенным условиям. Также была построена градуировочная зависимость концентрации урсоловой кислоты от отношения площади хроматографического пика (табл.3). При реализации способа использовали оборудование Томского регионального центра коллективного пользования (Agilent 1260 и QTOF 6550).
Таблица 3 — Диапазон градуировочной зависимости
Результаты расчета содержания тритерпеновых кислот в образце приведен в таблице 4.
Таблица 4 – Результаты анализа образца 5
*Relative standard deviation (относительное стандартное отклонение)
RSD для всех полученных значений: 7,13%.
Список использованных источников
1. Ралдугин В. А. Тритерпеноиды пихты и высокоэффективный регулятор роста растений на их основе // Рос. хим. журн. – 2004. – Т. 86. – №. 3. – С. 84
2. Кучин А.В., Карманова Л.П., Хуршкайнен Т.В. Способ выделения биологически активной суммы кислот из древесной зелени пихты. Патент №2161149 РФ. 2000
3. Патент № 2 161 149 Российская Федерация, A61K 36/15, A61K 127/00, A61K 135/00, B01D 11/04, C07C 57/26. Способ выделения биологически активной суммы кислот из древесной зелени пихты : № 99115901/04 : опубл. 2000.12.27 / Кучин А.В., Карманова Л.П., Хуршкайнен Т.В. — 4 с.
4. Ралдугин В. А. Тритерпеноиды пихты и высокоэффективный регулятор роста растений на их основе // Рос. хим. журн. – 2004. – Т. 86. – №. 3. – С. 84.
5. Pérez-Camino, M. C., & Cert, A. (1999). Quantitative Determination of Hydroxy Pentacyclic Triterpene Acids in Vegetable Oils. Journal of Agricultural and Food Chemistry, 47(4), 1558–1562 doi.org/10.1021/jf980881h
6. Xiaoyan Liao, Fangli Hu & Zilin Chen (2019). A HPLC-MS method for profiling triterpenoid acids and triterpenoid esters in Osmanthus fragrans fruits. The Analyst doi.org/10.1039/C9AN01542F
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ контроля содержания противотуберкулёзных препаратов основного ряда и их токсичных метаболитов в плазме крови | 2018 |
|
RU2702998C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУММЫ ТРИТЕРПЕНОВЫХ КИСЛОТ | 1997 |
|
RU2108803C1 |
| Способ количественного определения амиодарона в плазме крови человека | 2024 |
|
RU2835337C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 2-ФЕНОКСИЭТАНОЛА В БИОЛОГИЧЕСКИХ СРЕДАХ | 2021 |
|
RU2776730C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 8-(ТРИФТОРМЕТИЛ)БЕНЗО[F][1,2,3,4,5]ПЕНТАТИЕПИН-6-АМИНА ГИДРОХЛОРИДА В БИОЛОГИЧЕСКИХ СРЕДАХ | 2018 |
|
RU2676487C1 |
| Способ количественного определения N-нитрозоаминов: N-диметилнитрозоамин, N-метилэтилнитрозоамин, N-диэтилнитрозоамин, N-дибутилнитрозоамин, N-дипропилнитрозоамин, N-пиперидиннитрозоамин, N-пирролидиннитрозоамин, N-морфолиннитрозоамин, N-дифенилнитрозоамин, в пробах копченых мясопродуктов методом хромато-масс-спектрометрии | 2017 |
|
RU2657822C1 |
| Способ количественного определения салицилатов в плазме крови | 2016 |
|
RU2622996C1 |
| Способ количественного определения дисульфирама в биологических средах | 2019 |
|
RU2701524C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУММЫ ТРИТЕРПЕНОВЫХ КИСЛОТ | 2000 |
|
RU2179393C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУММЫ ТРИТЕРПЕНОВЫХ КИСЛОТ | 2006 |
|
RU2303589C1 |

Изобретение относится к аналитической химии, а именно к способу полуколичественного определения тритерпеновых кислот в экстракте древесной зелени хвойных пород. Способ полуколичественного определения тритерпеновых кислот в экстрактах древесной зелени пихты сибирской методом жидкостной хромато-масс-спектрометрии характеризуется тем, что проводят экстракцию ацетонитрилом и хроматографирование полученного раствора в анионообменном хроматографическом режиме смесью 0,1% раствора муравьиной кислоты и ацетонитрила для градиентного элюирования в соотношении 25 : 75 при объемной скорости потока 1,2 мл/мин, объеме инжекции 2 мкл, температуре термостата колонки 40 °С. Осуществляют детектирование с использованием масс-спектрометрического электроспрей-ионизационного детектора, работающего в режиме регистрации отрицательных ионов при напряжении на капилляре 3000 В, напряжении на сопле 1000 В, диапазоне сканирования 150–550 m/z, Да. Проводят полуколичественное определение суммы тритерпеновых кислот по градуировочной зависимости в диапазоне от 0,05 до 0,50 мг/мл урсуловой или олеановой кислоты. Техническим результатом является достижение групповой селективности для тритерпеновых кислот, облегчение интегрирования пиков для определения суммы компонентов, сокращение времени анализа, отсутствие необходимости очистки экстрактов от более гидрофобных компонентов. 1 ил., 4 табл.
Способ полуколичественного определения тритерпеновых кислот в экстрактах древесной зелени пихты сибирской методом жидкостной хромато-масс-спектрометрии, характеризующийся тем, что проводят экстракцию ацетонитрилом и хроматографирование полученного раствора в анионообменном хроматографическом режиме смесью 0,1% раствора муравьиной кислоты и ацетонитрила для градиентного элюирования в соотношении 25 : 75 при объемной скорости потока 1,2 мл/мин, объеме инжекции 2 мкл, температуре термостата колонки 40°С, осуществляют детектирование с использованием масс-спектрометрического электроспрей-ионизационного детектора, работающего в режиме регистрации отрицательных ионов при напряжении на капилляре 3000 В, напряжении на сопле 1000 В, диапазоне сканирования 150–550 m/z, Да, проводят полуколичественное определение суммы тритерпеновых кислот по градуировочной зависимости в диапазоне от 0,05 до 0,50 мг/мл урсуловой или олеановой кислоты.
| LIAO, X., HU, F., CHEN, Z | |||
| "A HPLC-MS METHOD FOR PROFILING TRITERPENOID ACIDS AND TRITERPENOID ESTERS IN OSMANTHUS FRAGRANS FRUITS", THE ANALYST, V.144(23), PP.6981-6988, 2019 | |||
| СПОСОБ ВЫДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУММЫ КИСЛОТ ИЗ ДРЕВЕСНОЙ ЗЕЛЕНИ ПИХТЫ | 1999 |
|
RU2161149C1 |
| Способ определения тритерпеновых кислот | 1987 |
|
SU1525571A1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ СУММЫ ТРИТЕРПЕНОВЫХ КИСЛОТ | 1997 |
|
RU2108803C1 |
Авторы
Даты
2023-12-28—Публикация
2023-11-02—Подача