Область техники, к которой относится изобретение
Изобретение относится к области микробиологии и биотехнологии, а именно, к средству ветеринарного и медицинского назначения для профилактики и лечения дисбиозов сельскохозяйственных животных, вызванных нарушением колонизационного потенциала нормофлоры желудочно-кишечного тракта различной этиологии и способу его получения.
Уровень техники
Сельскохозяйственные организации по разведению продуктивных животных часто сталкиваются с бактериальными желудочно-кишечными заболеваниями у новорождённого молодняка. Убытки, вызванные вспышками болезней, катастрофичны для отрасли животноводства. Хотя диарея, несомненно, является наиболее распространенной проблемой, она способна вызывать широкий спектр заболеваний, оказывающих непосредственное влияние на обменные процессы и иммунную систему.
Функционирование системы нормофлоры желудочно-кишечного тракта организма животного имеет первостепенное значение в синтезирующих, регуляторных, дезинтоксикационных, ферментативных, защитных процессах, в то же время кишечная микрофлора и их метаболиты могут активно модулировать иммунную систему. Таким образом, существует острая необходимость в эффективном, экономичном и постоянном методе борьбы с неблагоприятными последствиями болезней сельскохозяйственных животных.
Для профилактики и лечения ряда патологических состояний с симптомом диареи у молодняка сельскохозяйственных животных, широкое применение получили природные сорбенты [патент РФ № RU 2 029 546 C1] автор утверждает что энтеросорбент, полученный по его заявленному способу, приобретает новое свойство - пригодность для экстренного применения: адсорбционная активность через 3 мин после прием.
Недостатки следующие.
1. Во-первых, используемые энтеросорбент не способны убрать источник, вызывающий эффекты экзо- и эндотоксикозов, как правило, они не селективны и влияют в основном на объём субстрата.
2. Во-вторых, некоторые из них способны оказывать негативное воздействие на организм по причине сорбции необходимых метаболитов.
3. В-третьих, они не обеспечивают коррекцию колонизационного потенциала микробиоценоза желудочно-кишечного тракта.
Для нормализации микробиоценоза желудочно-кишечного тракта в большей степени получили применение препараты и средства, разработанные на основе живых бактериальных микроорганизмов, обладающих высокой продуктивностью и способностью подавлять патогенную микрофлору. Известен биопрепарат - пробиотик и способ его получения для животных и птицы [патент РФ № RU 2 217 493 C2], при получении которого для культивирования штамма, питательную среду обогащают дрожжевым автолизатом, водным раствором витаминов и непредельными жирными кислотами.
Недостатки следующие.
1. Во-первых, отсутствие в составе компонента носителя уменьшает колонизационную способность бактерий, что снижает их потенциал для временной колонизации
2. Во-вторых, в процессе сушки большая часть метаболитов разрушается, в частности, ценные органические кислоты и что бы их снова нарастить необходимы питательные основы.
Наиболее близким по способу получения и технической сущности (прототипом), является комплексный препарат-пробиотик [патент РФ № RU 2 317 089 C2] включает носитель, представляющий собой пористый энтеросорбент СУМС-1 на основе оксида алюминия, и клетки бактерий-эубиотиков с питательной и защитной средами, иммобилизованные на указанном носителе - энтеросорбенте.
Недостатки следующие.
1. Во-первых, в следствии отсутствия стимулирующих добавок указанный препарат имеет недостаточную колонизационную активность входящих в состав бактериальных клеток.
2. Во-вторых, указанный препарат не имеет в своём составе антиоксидантов и других стабилизирующих добавок, что характеризуется низким сроком хранения (не более 1 года).
Раскрытие изобретения
Задачей предлагаемого изобретения является создание комплексного средства «Синафлор» ветеринарного и медицинского назначения в иммобилизованной форме на основе сбалансированного комплекса биологически активных веществ с длительным сроком хранения и оказывающее пролонгированное благоприятное влияние на колонизацию индигенной составляющей микрофлоры желудочно-кишечного тракта сельскохозяйственных животных.
Технический результат, который может быть достигнут с помощью предлагаемого изобретения заключается в защите кишечного барьера, угнетении избыточного роста патогенов, а также снижении бактериальной транслокации и предотвращении бактериального инфекционного процесса в организме животного.
Технический результат достигается с помощью лиофилизата иммобилизованного поликомпонентного синбиотического средства «Синафлор», включающего сорбент-носитель, который, вступает во взаимодействие с пробиотическими бактериальными клетками посредствам иммобилизации, причём дополнительно содержит целевые компоненты, в качестве биокатализатора пребиотик-Лактулозe и олигосахарид-раффинозу, стимулирующих кинетику роста входящих в состав штаммов пробиотических микроорганизмов Lactobacillus acidophilus (B-4107) K-1-T и Enterococcus faecium (B-4054) УДС 86 с титром клеток 108-1012 КОЕ/г, а также дополнительно содержит вещества антиоксиданты и защитную сахарозо-желатиновую среду в форме сухого мелкодисперсного порошка концентрата, при следующем соотношении компонентов в мас.%:
Технический результат достигается с помощью способа получения лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» по п.1 включающего процесс иммобилизации консорциума пробиотических микроорганизмов и их метаболитов на сорбенте-носителе, при этом используемый носитель дегидратированный цеолит стерилизуют, при температуре 120+2°С в течение 30 минут и охлаждают до комнатной температуры, для приготовления стабилизированной питательной основы раствора используют сухие вещества: пребиотик - лактулозу, раффинозу, глутаминоваю кислоту, вносят цистеин и перемешивают, в стерильные флаконы ФБУ20 (стекло) 20 кубов с учётом правил асептики, загружают сорбент-носитель дегидратированный цеолит в виде мелкодисперсного порошка/гранул/таблеток и консорциум депонированных пробиотических культур Lactobacillus acidophilus (B-4107) K-1-T и Enterococcus faecium УДС (B-4054) 86 ресуспендированных фосфатным буфером с титром 109 - 1012 КОЕ/мл, дополнительно включают компоненты питательной и защитной среды для иммобилизации клеток на сорбент-носитель, полученную субстанцию размещают в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 2 часов, каждые 30 минут перемешивают, конечный продукт промывают изотоническим раствором NaCl, если в растворе осталось не более 50% от исходного количества концентрации микрооргонизмов, то процесс иммобилизации считается завершённым, далее замораживают промытый продукт методом сверхмедленного охлаждения - менее 1°С/мин в низкотемпературном холодильнике при температуре минус 50°C не более 24 часов как в вертикальном, так и в наклонном положении под углом (60+15)°, кассеты с предварительно замороженным средством перегружают в сушильную камеру интенсивного нагрева, где высушивают со скоростью до 20°С/ч и камеру вакуумируют, готовое расфасованное средство «Синафлор» герметично закрывают резиновыми пробками UL1-UL2 и консервируют алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм, хранение разработанного средства при температуре +4°С в течение года не изменяет его характеристики.
В качестве сорбента-носителя использовали дегидратированный цеолит, представленный ажурной кристаллической структурой в мелкодисперсной форме. Размер частиц кристаллов колеблется от 1 до 10 мкм. Среднее значение радиуса частиц порошка (по весу) составляет 1,39 мкм [Брек Д. Цеолитовые молекулярные сита. - М.: Мир, 1976. - 782 с., ил.].
Средство в качестве бактерий-пробиотиков содержит штамм Lactobacillus acidophilus K-1-T, ВКПМ: B-4107 (1970 год) и штамм Enterococcus faecium УДС 86, ВКПМ: B-4054 (1984 год) депонированные во Всероссийской Коллекции Промышленных Микроорганизмов НИИ им. Кручатова.
В основу лиофилизата синбиотического средства включили важнейшие для живого организма аминокислоты, глутаминовую кислоту и цистеин, в свою очередь они обладают высокими антиоксидантными свойствами [Сыровая А.О., Шаповал Л.Г., Макаров В.А. и соавт. Аминокислоты глазами химиков, фармацевтов, биологов. т. Том 1 / - Х. «Щедра садиба плюс», 2014 - 228 с.].
Используемый биокатализатор для пробиотических микроорганизмов, пребиотик-дисахарид лактулоза (галактофруктоза) синтезируется из лактозы (галактоглюкозы) путем изомеризации глюкозы во фруктозу. Лактулоза метаболизируется и не всасывается в тонкой кишке и поступает в толстый кишечник в неизмененном виде, где в процессе бактериального разложения распадается на короткоцепочечные жирные кислоты. Эксперименты in vitro показали, что общее производство короткоцепочечных жирных кислот увеличивается в два - три раза за счет добавления лактулозы. Полученные в результате кишечной микробной ферментации неперевариваемых продуктов, короткоцепочечные жирные кислоты, являются основным источником энергии колоноцитов, что делает их критически важными для здоровья желудочно-кишечного тракта [Синельников Б.М., Храмцов А.Г., Евдокимов И.А. и соавт. Лактулоза и её производные. - СПб.: Профессия, 2007. - 768 с., ил., табл.].
Олигосахарид раффиноза в кристаллическом виде, выделенный из сахарной свеклы. Он усваиваем бифидо- и лактобактериями. Производство НИЦФ «Germeon» г. Санкт-Петербург.
Чертежи и иные материалы
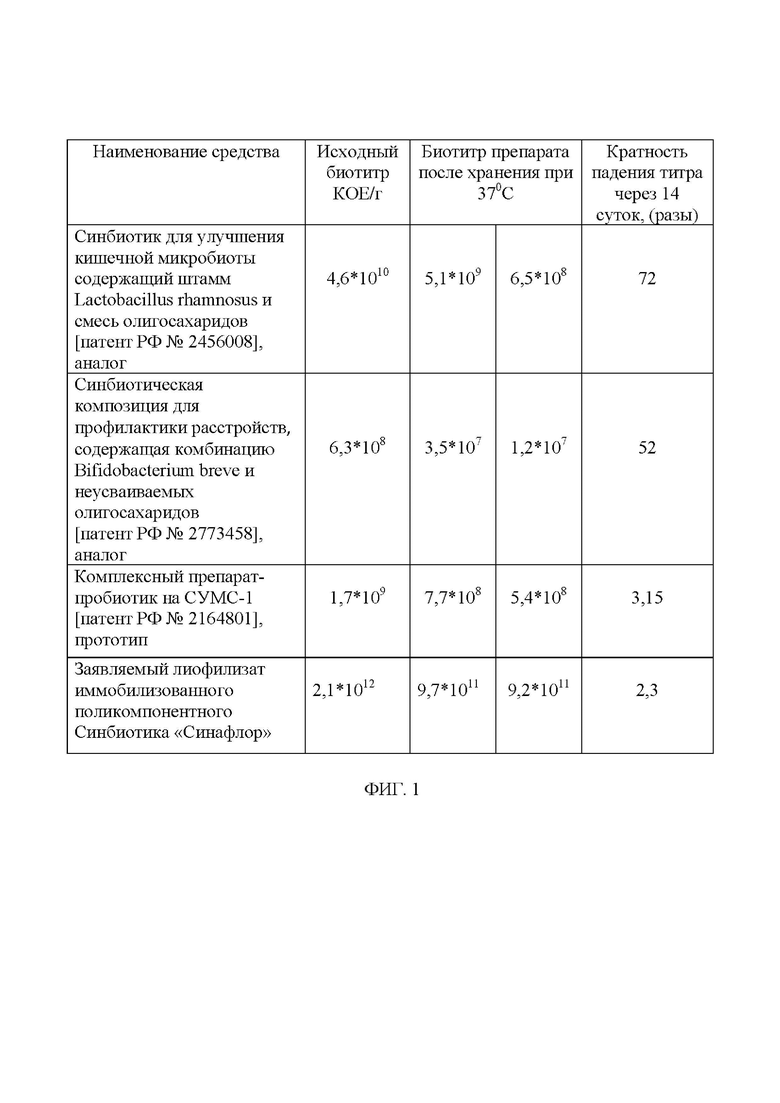
На фиг. 1 - Таблица 1 - Исследование влияния процедуры ускоренного хранения на биологическую активность (биотитр) заявленного средства и его аналогов.
На фиг. 2 - Паспорт штамма Lactobacillus acidophilus (B-4107) K-1-T, выдаваемого из коллекции.
На фиг. 3 - Паспорт штамма Enterococcus faecium (B-4054) УДС 86, выдаваемого из коллекции.
Осуществление изобретения
Способ получения лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» включает процесс иммобилизации консорциума пробиотических микроорганизмов и их метаболитов на сорбенте-носителе, используемый носитель дегидратированный цеолит стерилизуют согласно международным стандарт GMP, при температуре 120±2°С в течение 30 минут и охлаждают до комнатной температуры, для приготовления стабилизированной питательной основы раствора используют сухие вещества: пребиотик - лактулозу, раффинозу, глутаминоваю кислоту, цистеин смешивают в соответствии с п.1 формулы изобретения, перемешивают, в стерильные флаконы ФБУ20 (стекло) 20 кубов с учётом правил асептики, загружают сорбент-носитель дегидратированный цеолит в виде мелкодисперсного порошка/гранул/таблеток и консорциум депонированных пробиотических культур Lactobacillus acidophilus (B-4107) K-1-T и Enterococcus faecium УДС (B-4054) 86 ресуспендированных фосфатным буфером с титром 109 - 1012 КОЕ/мл, дополнительно включают компоненты питательной и защитной среды при указанных соотношениях в соответствии с п.1 формулы изобретения, для необходимой иммобилизации клеток на сорбент-носитель, полученную субстанцию размещают в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 2 часов, каждые 30 минут перемешивают (возможна автоматизация процесса), оценка качества проведённой иммобилизации полученного продукта осуществляют согласно МУК 4.2.577-96, продукт промывают изотоническим раствором NaCl, если в растворе осталось не более 50% от исходного количества концентрации микрооргонизмов, то процесс иммобилизации считается завершённым, далее замораживают промытый продукт методом сверхмедленного охлаждения (менее 1°С/мин) в низкотемпературном холодильнике при температуре минус 50°C не более 24 часов как в вертикальном, так и в наклонном положении под углом (60+15)°С, кассеты с предварительно замороженным средством перегружают в сушильную камеру интенсивного нагрева, где высушивают со скоростью до 20°С/ч и камеру вакуумируют, готовое расфасованное средство «Синафлор» герметично закрывают резиновыми пробками UL1-UL2 и консервируют алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм., массовая доля влаги составляет не более 1,3%, количество жизнеспособных клеток в готовом лиофилизате иммобилизованного поликомпонентного синбиотика составляет 108-1010 КОЕ/г, хранение разработанного средства при температуре +4°С в течение года не изменяет его характеристики.
Пример 1. Получение лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» осуществляли посредством иммобилизации консорциума пробиотических микроорганизмов и их метаболитов на сорбенте-носителе. Используемый сорбент-носитель дегидратированный цеолит стерилизовали согласно международным стандарт GMP, при температуре 120+2°С в течение 30 минут и охлаждали до комнатной температуры. Для приготовления стабилизированной питательной основы раствора использовали сухие вещества: пребиотик - лактулозу, раффинозу, глутаминоваю кислоту, цистеин смешивали в соответствии с п.1 формулы изобретения, перемешивали. В стерильные флаконы ФБУ20 (стекло) 20мл с учётом правил асептики, загружали сорбент-носитель дегидратированный цеолит в виде мелкодисперсного порошка/гранул/таблеток и консорциум депонированных пробиотических культур Lactobacillus acidophilus (B-4107) K-1-T и Enterococcus faecium (B-4054) УДС 86 ресуспендированных фосфатным буфером с титром 109 - 1012 КОЕ/мл, дополнительно включали компоненты питательной и защитной среды при указанных соотношениях в соответствии с п.1 формулы изобретения. Полученную субстанцию размещали в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 1 часа, каждые 30 минут перемешивали. После чего, продукт промывали изотоническим раствором NaCl и давали оценку качеству проведённой иммобилизации. Далее замораживали промытый продукт методом сверхмедленного охлаждения (менее 1°С/мин) в низкотемпературном холодильнике при температуре минус 50°C на протяжении 24 часов как в вертикальном, так и в наклонном положении под углом (60±15)°С. Кассеты с предварительно замороженным средством перегружали в сушильную камеру интенсивного нагрева, где высушивали со скоростью до 35°С/ч и камеру вакуумировали. Готовое расфасованное средство «Синафлор» герметично закрывали резиновыми пробками UL1-UL2 и консервировали алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм. Массовая доля влаги составила 1,05%.
По результатам оценки качества проведённой иммобилизации ресуспендированных пробиотических микроорганизмов установленном, что в смывах изотонического раствора NaCl, осталось 65% от исходного количества концентрации микрооргонизмов, а именно иммобилизация на носитель прошла не полностью, а именно количество жизнеспособных клеток в готовом лиофилизате иммобилизованного поликомпонентного синбиотика составило Lactobacillus acidophilus (B-4107) K-1-T - 106 КОЕ/г и Enterococcus faecium (B-4054) УДС 86 - 105 КОЕ/г. Таким образом необходимо увеличить время для более качественного процесса иммобилизации.
Пример 2. Получение лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» осуществляли согласно примеру 1, отличающееся тем, что полученную субстанцию размещали в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 2 часов, каждые 30 минут перемешивали. После чего, продукт промывали изотоническим раствором NaCl, в смывах раствора, осталось 25% от исходного количества концентрации микрооргонизмов. Далее замораживали промытый продукт методом сверхмедленного охлаждения (менее 1°С/мин) в низкотемпературном холодильнике при температуре минус 50°C на протяжении 24 часов как в вертикальном, так и в наклонном положении под углом (60±15)°С. Кассеты с предварительно замороженным средством перегружали в сушильную камеру интенсивного нагрева, где высушивали со скоростью до 35°С/ч и камеру вакуумировали. Готовое расфасованное средство «Синафлор» герметично закрывали резиновыми пробками UL1-UL2 и консервировали алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм. Массовая доля влаги составила 1,05%.
По результатам оценки количества жизнеспособных клеток в готовом лиофилизате иммобилизованного поликомпонентного синбиотика составило Lactobacillus acidophilus (B-4107) K-1-T - 108 КОЕ/г и Enterococcus faecium (B-4054) УДС 86 - 106 КОЕ/г. Таким образом, установлено, что интенсивный нагрев со скоростью до 35°С/ч, снизило количество жизнеспособных клеток пробиотических микроорганизмов входящих в состав разработанного средства, в связи с этим необходимо снизить скорость нагрева до 20°С/ч, что в свою очередь увеличит время сушки, однако сохранность клеток значительно повысится.
Пример 3. Получение лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» осуществляли согласно примеру 1, отличающееся тем, что полученную субстанцию размещали в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 2 часов, каждые 30 минут перемешивали. После чего, продукт промывали изотоническим раствором NaCl и давали оценку качеству проведённой иммобилизации. Далее замораживали промытый продукт методом сверхмедленного охлаждения (менее 1°С/мин) в низкотемпературном холодильнике при температуре минус 50°C на протяжении 24 часов как в вертикальном, так и в наклонном положении под углом (60±15)°С. Кассеты с предварительно замороженным средством перегружали в сушильную камеру интенсивного нагрева, где высушивали со скоростью до 35°С/ч и камеру вакуумировали. Готовое расфасованное средство «Синафлор» герметично закрывали резиновыми пробками UL1-UL2 и консервировали алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм. Массовая доля влаги составила 1,25%. Количество жизнеспособных клеток в готовом лиофилизате иммобилизованного поликомпонентного синбиотика составило Lactobacillus acidophilus (B-4107) K-1-T - 1010 КОЕ/г и Enterococcus faecium (B-4054) УДС 86 - 108 КОЕ/г.
Таким образом, предложенный метод сублимационной сушки по примеру 3 обеспечивает получение лиофилизата иммобилизованного поликомпонентного синбиотика без существенного негативного влияния на жизнеспособность бактериальных клеток входящих в состав предложенного средства.
Пример 4. Доклинические исследования лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» осуществляли согласно ГОСТ 32644-2014 на белых крысах (самцах) линии WISTAR (Свидетельство № 11742; Ветеринарное свидетельство №12125983222) серии 33-34, с массой тела 290-310 г., методом внутрижелудочного введения средства в предельной дозе, назначенной согласно руководству по проведению доклинических исследований лекарственных средств (2012).
По результатам клинико-физиологической оценки участвующих в исследованиях лабораторных животных, предложенное средство не вызывало побочных и непредвиденных нежелательных реакций, стимулировало процессы адаптации организма к неблагоприятным факторам внешней среды. По результатам доклинических исследований было установлено, динамика морфометрических показателей экспериментальных лабораторных животных в пределах физиологических норм в соответствии с популяционным стандартом. Анализ лабораторных исследований крови находились на должном физиологическом уровне. Итоги патологоанатомического вскрытия подтвердили состояние органов в норме.
Полученные результаты свидетельствуют о том, что лиофилизат иммобилизованного поликомпонентного синбиотика «Синафлор»комплексный успешно прошел доклинические испытания и предложенное средство можно отнести к V группе опасности по ГОСТ 32644-2014 или неклассифицированная.
Пример 5. Исследование биологической активности лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» в процессе их хранения проводили методом сравнения с аналогами и прототипом в процессе воздействия инактивирующих факторов внешней среды (температура, кислород воздуха, длительность воздействия и другие факторы). Для учёта используют стандартную процедуру ускоренного хранения биопрепарата при температуре 37°C. Результаты биотитрования стандартным методом путём посева последовательных 10-кратных разведений на агаризированные дифференциально-диагностические питательные среды в колонийобразующих единицах (КОЕ) на 1 г препарата (КОЕ/г) приведены в фиг. 1.
Анализ данных таблицы (фиг. 1) показывает, что по результатам ускоренного теста на хранение лиофилизата иммобилизованного поликомпонентного синбиотика «Синафлор» имеют биологическую активность в 1,5-2,0 раза выше, чем комплексный препарат-прототип и на 1-2 порядка выше, чем другие препараты-аналоги.
Хранение заявляемого препаратов в течение 1,5 лет при температуре не выше +4°C в условиях холодильника показало, что биологическая активность (в КОЕ/г) осталась практически неизменной несмотря на наличие атмосферного воздуха в средстве над флаконом. Это объясняется защитным антиокислительным действием имеющихся в лиофилизате иммобилизованного поликомпонентного синбиотика «Синафлор» аминокислот-антиоксидантов.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие преимущества:
1. Средство по изобретению обладает профилактическим потенциалом за счет разумного соотношения между иммобилизованными пробиотиками, пребиотиками и компонентами консервантами.
2. Входящие в состав средства важнейшие для живого организма аминокислоты, глутаминовая кислота и цистеин могут эффективно продлевать срок годности синбиотика, что не только оказывает положительное влияние на длительность эффекта, но также способствуют выживаемости пробиотиков в кишечнике.
3. Средство по настоящему изобретению может эффективно предупреждать нарушения пищеварительной системы, вызываемые антибиотиками. Синергетический эффект синбиотической композиции очевиден, ингредиенты безопасны и эффективны, а сырье подобрано в разумных пределах, выпускается в промышленных условиях, тем самым легкодоступно и недорого.
4. Изобретение способно восстановить барьер повреждённых участков слизистой оболочки кишечника и сохранить мембрану. Барьер ограничивает попадание вредных веществ, таких как бактерии и токсины в кишечник, в просвет кишечника, эффективно предотвращая проникновение токсинов в организм человека.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ непрямой регуляции иммунологических процессов у телят в период новорождённости для снижения риска развития желудочно-кишечных заболеваний | 2024 |
|
RU2833809C1 |
| Синбиотическое средство для повышения колонизационного потенциала нормофлоры желудочно-кишечного тракта молодняка крупного рогатого скота | 2021 |
|
RU2782031C1 |
| СИНБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ КОРРЕКЦИИ ДИСБИОТИЧЕСКИХ НАРУШЕНИЙ МИКРОБИОЦЕНОЗА ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2015 |
|
RU2592988C1 |
| СПОСОБ КОРМЛЕНИЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ | 2017 |
|
RU2652832C1 |
| Средство для лечения эшерихиоза и цитробактериоза молодняка крупного рогатого скота в раннем постнатальном онтогенезе | 2020 |
|
RU2758066C1 |
| Кормовая комплексная биологически активная добавка для животных и птиц | 2019 |
|
RU2708161C1 |
| Способ получения комплексной синбиотической композиции | 2023 |
|
RU2810586C1 |
| МЕТАБИОТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ОБЕСПЕЧЕНИЯ КОЛОНИЗАЦИОННОЙ РЕЗИСТЕНТНОСТИ МИКРОБИОЦЕНОЗА КИШЕЧНИКА ЧЕЛОВЕКА | 2015 |
|
RU2589818C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУХОГО ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 2008 |
|
RU2380107C1 |
| КОРМОВАЯ ДОБАВКА С ПРОБИОТИЧЕСКОЙ АКТИВНОСТЬЮ ДЛЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ, ПТИЦ, ЛОШАДЕЙ И РЫБ | 2017 |
|
RU2652836C1 |


Группа изобретений относится к биотехнологии. Предложены лиофилизат иммобилизованного поликомпонентного синбиотического средства для профилактики и лечения дисбиозов сельскохозяйственных животных, включающий сорбент-носитель и целевые компоненты: пребиотик - лактулозу и олигосахарид - раффинозу, штаммы пробиотических микроорганизмов Lactobacillus acidophilus К-1-Т ВКПМ В-4107 с титром 2⋅1012 КОЕ/г и Enterococcus faecium УДС 86 ВКПМ В-4054 с титром 2⋅108 КОЕ/г, глутаминовую кислоту, цистеин и защитную сахарозо-желатиновую среду в форме сухого мелкодисперсного порошка концентрата при заданном содержании исходных компонентов в мас.%, и способ его получения. Способ включает иммобилизацию пробиотических микроорганизмов на сорбенте-носителе в присутствии компонентов питательной и защитной среды, замораживание целевого продукта и сушку в сушильной вакуумированной камере в заданном режиме, фасовку. Изобретения обеспечивают расширение арсенала средств для профилактики и лечения дисбиозов сельскохозяйственных животных, вызванных нарушением колонизационного потенциала нормофлоры желудочно-кишечного тракта различной этиологии. 2 н.п. ф-лы, 3 ил., 5 пр.
1. Лиофилизат иммобилизованного поликомпонентного синбиотического средства для профилактики и лечения дисбиозов сельскохозяйственных животных, включающий сорбент-носитель, который вступает во взаимодействие с пробиотическими бактериальными клетками посредством иммобилизации, отличающийся тем, что содержит целевые компоненты: в качестве биокатализатора пребиотик - лактулозу и олигосахарид - раффинозу, штаммы пробиотических микроорганизмов Lactobacillus acidophilus К-1-Т ВКПМ В-4107 с титром 2⋅1012 КОЕ/г и Enterococcus faecium УДС 86 ВКПМ В-4054 с титром 2⋅108 КОЕ/г, а также содержит вещества антиоксиданты – глутаминовую кислоту, цистеин и защитную сахарозо-желатиновую среду в форме сухого мелкодисперсного порошка концентрата при следующем содержании исходных компонентов в мас.%:
2. Способ получения лиофилизата иммобилизованного поликомпонентного синбиотического средства по п.1, включающий процесс иммобилизации пробиотических микроорганизмов на сорбенте-носителе, при этом используемый носитель дегидратированный цеолит стерилизуют при температуре 120+2°С в течение 30 мин и охлаждают до комнатной температуры, для приготовления стабилизированной питательной основы раствора используют сухие вещества: пребиотик – лактулозу, раффинозу, глутаминовую кислоту, вносят цистеин и перемешивают, в стерильные флаконы ФБУ20 (стекло) 20 мл с учётом правил асептики загружают сорбент-носитель дегидратированный цеолит в виде мелкодисперсного порошка/гранул/таблеток и пробиотические культуры Lactobacillus acidophilus К-1-Т ВКПМ В-4107 с титром 2⋅1012 КОЕ/г и Enterococcus faecium УДС 86 ВКПМ В-4054 с титром 2⋅108 КОЕ/г, ресуспендированных фосфатным буфером, дополнительно включают компоненты питательной и защитной среды для иммобилизации клеток на сорбент-носитель, полученную субстанцию размещают в низкотемпературных шкафах под воздействием температуры на уровне +4°С в течение 2 ч, каждые 30 мин перемешивают, конечный продукт промывают изотоническим раствором NaCl, если в растворе осталось не более 50% от исходного количества концентрации микроорганизмов, то процесс иммобилизации считается завершённым, далее замораживают промытый продукт методом сверхмедленного охлаждения - менее 1°С/мин в низкотемпературном холодильнике при температуре минус 50°С не более 24 ч как в вертикальном, так и в наклонном положении под углом (60+15)°, кассеты с предварительно замороженным средством перегружают в сушильную камеру интенсивного нагрева, где высушивают со скоростью до 20°С/ч, и камеру вакуумируют, готовое расфасованное средство герметично закрывают резиновыми пробками UL1-UL2 и консервируют алюминиевыми колпачками с толщиной стенки 0,18-0,2 мм.
| КОМПЛЕКСНЫЙ ПРЕПАРАТ-ПРОБИОТИК В ИММОБИЛИЗОВАННОЙ И ЛИОФИЛИЗИРОВАННОЙ ФОРМЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2317089C2 |
| Синбиотическое средство для повышения колонизационного потенциала нормофлоры желудочно-кишечного тракта молодняка крупного рогатого скота | 2021 |
|
RU2782031C1 |
| ПРЕПАРАТ-ПРОБИОТИК В СУХОЙ ИММОБИЛИЗОВАННОЙ ФОРМЕ | 1999 |
|
RU2164801C1 |
| САМОЙЛЕНКО В.С | |||
| и др | |||
| "Влияние опытного образца синбиотического средства на биохимические показатели крови и иммунологический статус телят"; Вестник КрасГАУ, 2021, N 7, с.143-151. | |||
Авторы
Даты
2024-01-11—Публикация
2023-06-02—Подача