ОБЛАСТЬ ТЕХНИКИ
Целью настоящего изобретения являются производные хинолина для применения в лечении рака.
В связи с тяжестью заболевания существует постоянная необходимость в поиске новых лекарств для предупреждения и/или лечения рака и/или повышения эффективности существующих противораковых препаратов.
Также остается потребность в соединениях без побочных эффектов или с ограниченными побочными эффектами.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Некоторые производные хинолина описаны в следующих патентных заявках: WO 2010/143169, WO 2012/080953, WO 2016/009065 и WO 2016/009066 эффективны в лечении СПИДа или некоторых воспалительных заболеваний.
Дополнительно некоторые производные хинолина которые были раскрыты в WO 2010/143168, эффективны в лечении некоторых видов рака, и, более конкретно, эффективны против метастатической инвазии.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В рамках настоящего изобретения могут быть даны следующие определения:
• эффективное количество: количество фармацевтического соединения, которое оказывает воздействие на обрабатываемую опухоль и/или количество соединения настоящего изобретения, которое эффективно при предупреждении, уменьшении, устранении, лечении или контроле симптомов описанных в настоящем описании заболеваний и состояний, т.е. рака и/или дисплазии и, в частности, предракового состояния, рака на ранней стадии или неметастатического рака. Термин “эффективное количество” включает в себя “эффективное количество для профилактики”, а также “эффективное количество для лечения". Термин “эффективное количество для профилактики” относится к концентрации соединения данного изобретения, эффективной в ингибировании, предупреждении, снижении вероятности рака и/или дисплазии и, в частности, предракового состояния, рака на ранней стадии или неметастатического рака или в предупреждении отсроченного начала рака и/или дисплазии и, в частности, предракового состояния, рака на ранней стадии или неметастатического рака. Так же, термин “эффективное для лечения количество” относится к концентрации соединения, которое эффективно в лечении рака и/или дисплазии и, более конкретно, предракового состояния, рака на ранней стадии или неметастатического рака, например, ведет к уменьшению размера опухоли, опухолевой массы и/или числа опухолей предраковой опухоли, раннестадийной опухоли или неметастатической опухоли после осмотра при введении соединения после того, как возник (возникли) рак и/или дисплазия.
• раздельное введение лекарственной комбинации, одновременное введение или введение, распределенное во времени, означает, что элементарные составляющие комбинации могут быть введены одновременно, каждый за один прием в разные моменты времени, или многократно, или же в разные моменты, в частности во время циклов. Для этого элементарные составляющие могут быть разработаны в виде смесей, только если их вводят одновременно, или же разработаны отдельно для других схем введения;
• Используемый в настоящем документе термин "фармацевтически приемлемый" относится к тем соединениям, материалам, вспомогательным веществам, носителю, адъюванту, несущей лекарственное вещество среде, композициям или лекарственным формам, которые в рамках тщательной медицинской оценки подходят для контакта с тканями человека и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблемных осложнений, соизмеримых с разумным соотношением пользы/риска.
• Термин “пациент”, используемый в настоящем документе, означает животное, предпочтительно млекопитающее, и наиболее предпочтительно человека.
• “Комбинация” означает фармацевтическую композицию или набор, содержащий соединение, как определено в настоящем документе, или любой из его метаболитов или его фармацевтически приемлемых солей, в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин в любой форме, и по меньшей мере дополнительный противораковый или противоопухолевый активный агент.
• В контексте данного изобретения термин “обработка” или “лечение”, используемый в настоящем документе, означает регрессию, облегчение, ингибирование прогрессирования или предупреждение рака и/или дисплазии и, в частности, предракового состояния, раннестадийного рака или неметастатического рака.
• Термин "контроль" предназначен для обозначения всех процессов, где может происходить замедление, прерывание, купирование или остановка прогрессирования заболеваний и состояний, описанных в настоящем документе, но не обязательно означает полное устранение всех симптомов заболевания и состояния, и предполагается, что включает в себя профилактическое лечение.
• Термин “предупреждение”, используемый в настоящем документе, означает снижение риска возникновения или замедление возникновения данного явления, а именно в настоящем изобретении, рака и/или дисплазии и, в частности, предракового состояния, рака на ранней стадии или неметастатического рака. Используемый в настоящем документе термин «предупреждение» также включает в себя «снижение вероятности возникновения» или «снижение вероятности повторного возникновенияя».
Поэтому изобретение относится к производному хинолина формул (I), (I’), (I’’), (Ia), (Ib), (Ib’), (Ic), (Id), (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd), как определено в настоящем документе ниже, или его фармацевтически приемлемой соли для применения для лечения и/или придупреждения рака или дисплазии.
Как показано в экспериментальной части путем расчета IC50, соединения согласно настоящему изобретению, в частности соединения формулы (Ib’) или любой из их метаболитов или их фармацевтически приемлемая соль, эффективны для лечения и/или предупреждения рака, и в частности колоректального рака (прямой и толстой кишки), рака желудка, рака печени, рака легких и/или рака поджелудочной железы, в частности, у пациентов с предраковым состоянием, раком на ранней стадии или неметастатическим раком. Согласно одному варианту осуществления соединения формулы (Ib’) или любые из их метаболитов или их фармацевтически приемлемые соли не нацелены непосредственно на инвазию метастазов.
Дополнительно настоящее изобретение относится к соединениям формул (I), (I’), (I’’), (Ia), (Ib), (Ib’), (Ic), (Id), (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd), как определено ниже, или их фармацевтически приемлемой соли для применения в предупреждении и/или ингибировании и/или лечении рака или дисплазии, или метастаз рака или предопухолевых поражений.
Кроме того, настоящее изобретение относится к способу предупреждения, ингибирования или лечения рака или дисплазии, который включает, по меньшей мере, один этап, заключающийся во введении страдающему от этого пациенту эффективного количества соединения, определенного в формулах (I), (I’), (I’’), (Ia), (Ib), (Ib’), (Ic), (Id), (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd) ниже, или его фармацевтически приемлемой соли.
В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение уровня соединения, определенного в формулах (I), (I’), (I’’), (Ia), (Ib), (Ic), (Id) или (Ib’) в настоящем документе, или его фармацевтически приемлемой соли или его метаболита у пациента. В некоторых вариантах осуществления уровень соединения, определенного в формулах (I), (I’), (I’’), (Ia), (Ib), (Ic), (Id) или (Ib’), или его фармацевтически приемлемой соли, или его метаболита, измеряют в биологическом образце пациента. В некоторых вариантах осуществления биологический образец пациента представляет собой образец крови, плазмы, ткани, слюны и/или сыворотки. В некоторых вариантах осуществления способ настоящего изобретения дополнительно включает измерение уровня соединения формул (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение общего уровня соединений формул (I), (I’) или (I’’) и (IV) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает в себя измерение общего уровня соединений формул (Ia) и (IVa) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение общего уровня соединений формул (Ib) и (IVb) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение общего уровня соединений формул (Ib’) и (IVb’) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение общего уровня соединений формул (Ic) и (IVc) или их фармацевтически приемлемых солей у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение общего уровня соединений формул (Id) и (IVd) или их фармацевтически приемлемых солей у пациента.
В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение и/или мониторинг наличия и/или уровня биомаркера у пациента. В некоторых вариантах осуществления наличие и/или уровень биомаркера измеряется в биологическом образце пациента. В некоторых вариантах осуществления биологический образец пациента представляет собой образец крови. В некоторых вариантах осуществления биологический образец пациента представляет собой образец ткани. В некоторых вариантах осуществления биомаркером, измеряемым и/или контролируемым в способе настоящего изобретения, является miR-124, как описано в WO 2014/111892, все содержание которого включено в настоящий документ ссылкой. В некоторых вариантах осуществления способ или применнеие настоящего изобретения дополнительно включает измерение и/или мониторинг наличия и/или уровня экспрессии miR-124 у пациента до введения соединения или фармацевтически приемлемой соли или их композиции, как описано в настоящем документе. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает измерение и/или мониторинг присутствия и/или уровня экспрессии miR-124 у пациента во время курса лечения соединением или фармацевтически приемлемой солью или их композицией, как описано в настоящем документе. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает выбор пациента для лечения соединением или фармацевтически приемлемой солью или их композицией, как описано в настоящем документе, путем измерения и/или мониторинга наличия и/или уровня экспрессии miR-124 у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает исключение пациента из лечения соединением или фармацевтически приемлемой солью или их композицией, как описано в настоящем документе, путем измерения и/или мониторинга наличия и/или уровня экспрессии miR-124 у пациента. В некоторых вариантах осуществления способ или применение настоящего изобретения дополнительно включает корректировку (например, увеличение или уменьшение) режима дозирования (например, количества дозы и/или графика доз) соединения или его фармацевтически приемлемой соли или композиции, как описано в настоящем документе, для введения пациенту путем измерения и/или мониторинга наличия и/или уровня экспрессии miR-124 у пациента.
В некоторых вариантах осуществления способ или применение настоящего изобретения включает сравнение измеренного уровня экспрессии miR-124 у пациента с контрольным референсным значением. Контрольное референсное значение, которое будет использоваться для сравнения измеренного уровня экспрессии miR-124 у пациента, получают из контрольного образца. Контрольный образец может быть взят из различных источников. В некоторых вариантах осуществления контрольный образец берется у пациента до лечения или до заболевания (как например, архивный образец крови или образец ткани). В некоторых вариантах осуществления контрольный образец берется из набора нормальных, не больных членов популяции. В некоторых вариантах осуществления контрольный образец берется у пациента до лечения соединением или фармацевтически приемлемой солью или их композицией, как описано в настоящем документе. В некоторых вариантах осуществления на биологическом образце может быть проведен клеточный тест.
В некоторых вариантах осуществления модулированное наличие и/или уровень экспрессии miR-124 у пациента по сравнению с контрольным референсным значением указывает на рак. В некоторых вариантах осуществления модулированное наличие и/или уровень экспрессии miR-124 у пациента по сравнению с контрольным референсным значением указывает на эффективность лечения соединением или фармацевтически приемлемой солью или их композицией, как описано в настоящем документе, которое вводят пациенту. Термины “модуляция” или “модулированное наличие и/или уровень экспрессии” означают, что наличие или уровень экспрессии биомаркера либо индуцируется, или увеличивается, либо, альтернативно, подавляется, или уменьшается.
В некоторых вариантах осуществления измеренное сокращенное или супрессированное (подавленное) наличие или сниженный уровень экспрессии miR-124 относительно контрольного референсного значения указывает на рак. В некоторых вариантах осуществления измеренное индуцированное или повышенное наличие или повышенный уровень экспрессии miR-124 относительно контрольного референсного значения указывает на эффективность соединения или его фармацевтически приемлемой соли или их композиции, как описано в настоящем документе. В некоторых вариантах осуществления измеренный уровень экспрессии miR-124 у пациента, получающего соединение или фармацевтически приемлемую соль или их композицию, как описано в настоящем документе, представляет собой двукратное, четырехкратное, шестикратное, восьмикратное или десятикратное увеличение относительно контрольного референсного значения.
В настоящем документе также предусмотрено применение miR-124 in vitro или ex vivo в качестве биомаркера активности производного хинолина формулы (I), (I’) или (I’’) или любого из его метаболитов или фармацевтически приемлемой соли, как определено выше, в отношении рака.
Согласно одному варианту осуществления, применение и способы согласно данному изобретению могут, в частности, позволить определить рак у пациента и, в частности, последующее наблюдение за подобным раком.
Применение согласно настоящему изобретению может быть направлено на оценку реактивности пациента в лечении рака производным хинолина в соответствии с настоящим изобретением. Оно так же может быть дополнительно направлено на оценку эффективности лечения рака указанным производным хинолина или на оценку терапевтической эффективности указанного производного хинолина в качестве терапевтического средства для предупреждения и/или лечения рака.
Кроме того, оно может быть направлено на оценку комплаентности пациента противоопухолевому лечению указанным производным хинолина.
В некоторых вариантах осуществления настоящее изобретение предусматривает применение соединения формул (I), (I’), (I’’), (Ia), (Ib), (Ib’), (Ic), (Id), (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd) или его фармацевтически приемлемой соли, где измеряют наличие и/или уровень экспрессии miR-124 в крови и/или образце ткани для регулирования, дозирования или мониторинга ответа на лечение.
В некоторых вариантах осуществления настоящее изобретение предусматривает применение соединения формул (I), (I’), (I’’), (Ia), (Ib), (Ib’), (Ic), (Id), (IV), (IVa), (IVb), (IVb’), (IVc) или (IVd) или его фармацевтически приемлемой соли, где измеряют уровень метилирования miR-124 для регуляции терапии.
В некоторых вариантах осуществления настоящее изобретение обеспечивает алгоритм, сочетающий уровень miR-124 и уровень цитокина или другого биомаркера, или уровни соединений формулы (I) и/или (IV), как определено ниже, или их фармацевтически приемлемых солей, для мониторинга тяжести рака и/или для мониторинга эффективности лечения, включая без ограничений лечения, как описано в настоящем описании. В некоторых вариантах осуществления описанный в настоящем описании способ лечения включает использование алгоритма, сочетающего уровень miR-124 и уровень цитокина или другого биомаркера, или уровни соединений формулы (I) и/или (IV), как определено ниже, или их фармацевтически приемлемых солей, для мониторинга тяжести рака и/или для мониторинга эффективности лечения.
В настоящем изобретении дополнительно приведено производное хинолина формулы (I’) или любого из его метаболитов или фармацевтически приемлемой соли или любого из их энантиомеров или диастереоизомеров для применения согласно настоящему изобретению, где алгоритм, сочетающий уровень miR-124 и уровень цитокина или другого биомаркера, или уровни соединения формулы (I’), как определено ниже, или любого из его метаболитов или фармацевтически приемлемой соли или любого из их энантиомеров или диастереоизомеров, используют для мониторинга тяжести рака и/или для мониторинга эффективности лечения.
В настоящем документе дополнительно обеспечен алгоритм, который сочетает уровень miR-124 и уровень цитокина или другого биомаркера, или уровни соединения формулы (I’), как определено ниже, или любого из его метаболитов или фармацевтически приемлемой соли, или любого из их энантиомеров или диастереоизомеров для мониторинга эффективности лечения.
В настоящем документе также обеспчечено производное хинолина формулы (I), (I’) или (I’’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения в качестве противоопухолевого средства, предназначенного для пациентов, у которых наличие и/или уровень экспрессии miR-124 мониторируется в крови и/или образце ткани указанного пациента до и/или во время указанного применения противоопухолевого средства или лечения.
В настоящем документе также обеспчечено производное хинолина формулы (I), (I’) или (I’’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения в качестве противоопухолевого агента у пациентов, для которых наличие и/или уровень экспрессии miR-124 был измерен в крови и/или образце ткани указанного пациента до, во время и/или после введения.
Поэтому в настоящем документе обеспечен способ оценки активности производного хинолина формулы (I), (I’) или (I’’) для предупреждения и/или лечения рака у пациента, получающего указанное производное хинолина, включающий, по меньшей мере, этапы:
а - измерение наличия или уровня экспрессии по меньшей мере одной микроРНК (miRNA), причем по меньшей мере одной микроРНК, являющейся miR-124, в первом биологическом образце, ранее полученном от указанного пациента до введения указанного производного хинолина, и во втором биологическом образце, ранее полученном от указанного пациента после введения указанного производного хинолина; и
b - определение того, модулируется ли указанное наличие или уровень экспрессии во втором биологическом образце, полученном после лечения, по сравнению со вторым биологическим образцом, полученным до лечения;
где модулированное наличие или уровень экспрессии указанной микроРНК указывает на противоопухолевую активность указанного производного хинолина.
В некоторых вариантах осуществления способ или применение настоящего изобретения используется в сочетании с другим активным ингредиентом, в частности другим противоопухолевым агентом, как описано в настоящем документе.
В некоторых вариантах осуществления способ или применение настоящего изобретения используется в сочетании с другой терапией, как описано в настоящем документе. В некоторых вариантах осуществления другая терапия выбрана из химиотерапии, иммунотерапии, радиотерапии, хирургии, ультразвуковой терапии, моноклональных антител и вакцин против рака.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения
Соединения, описанные в настоящем документе, могут быть приготовлены согласно синтетическим подходам, описанными в WO 2010/143169, WO 2012/080953, WO 2016/009065 и WO 2016/009066, содержание которых включено в настоящий документ по ссылке полностью.
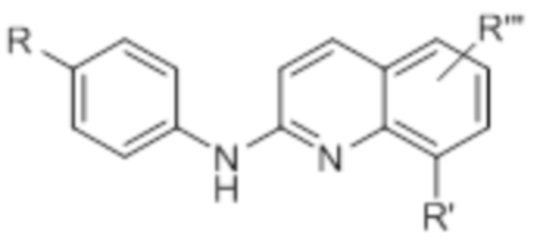
В одном аспекте соединение данного изобретения представляет собой соединение Формулы (I):
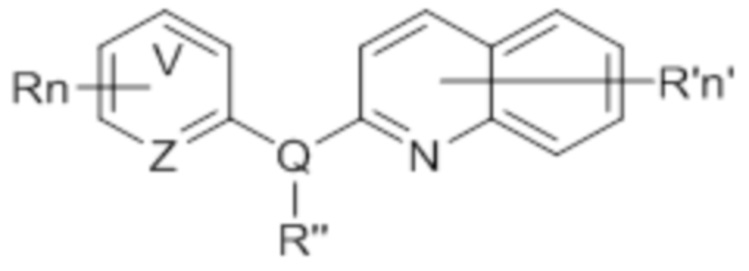
(I)
или его фармацевтически приемлемую соль, где:
Z представляет собой C или N;
V представляет собой C или N;
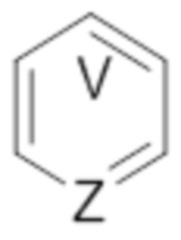 означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, то V находится в орто, мета или пара положении относительно Z;
означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, то V находится в орто, мета или пара положении относительно Z;
каждый R независимо представляет собой водород, галоген, -CN, гидроксил, (C1-C3)фторалкил, (C1-C3)фторалкокси, (C3-C6)циклоалкил, -NO2, -NR1R2, (C1-C4)алкокси, фенокси, -NR1-SO2-NR1R2, -NR1-SO2-R1, -NR1-C(=O)-R1, -NR1-C(=O)-NR1R2, -SO2-NR1R2, -SO3H, -O-SO2-OR3, -O-P(=O)-(OR3)(OR4), -O-CH2-COOR3, (C1-C3)алкил, причем указанный алкил необязательно моно - или дизамещен гидроксильной группой, группу формулы (IIa): 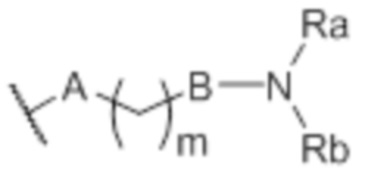 , или группу формулы (IIIa):
, или группу формулы (IIIa): 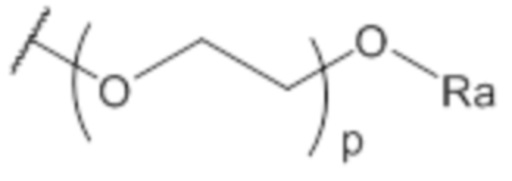 ;
;
Q представляет собой N или O, при условии, что R” не существует, когда Q представляет собой O;
каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил;
каждый из R3 и R4 независимо представляет собой водород,, Li+, Na+, K+, N+(Ra)4или бензил;
n представляет собой 1, 2 или 3;
n’ рав представляет собой но 1, 2 или 3;
каждый R’ независимо представляет собой водород, (C1-C3)алкил, гидроксил, галоген, -NO2, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3)фторалкил, (C1-C4)алкокси, -O-P(=O)-(OR3)(OR4), -CN, группу формулы (IIa): 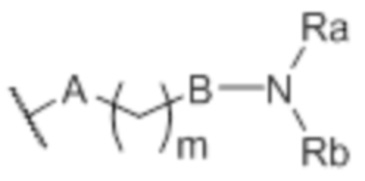 , или группу формулы (IIIa):
, или группу формулы (IIIa): 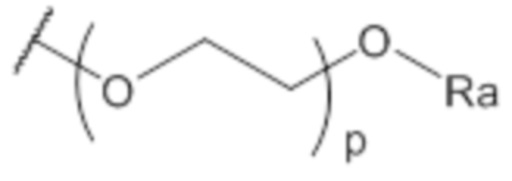 ;
;
А представляет собой ковалентную связь, кислород или NH;
B представляет собой ковалентную связ или NH;
m представляет собой 1, 2, 3, 4 или 5;
p представляет собой 1, 2 или 3;
каждый из Ra и Rb независимо представляет собой водород, (C1-C5)алкил или (C3-C6)циклоалкил, или
Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ является группой (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие R’ группы отличаются от указанной группы (IIa) или (IIIa); и
R” представляет собой водород, (C1-C4)алкил или группу формулы (IIa), как определено выше.
Как в целом определено выше, Z представляет собой C или N.
В некоторых вариантах осуществления Z представляет собой C. В некоторых вариантах осуществления Z представляет собой N.
В некоторых вариантах осуществления Z выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом определено выше, V представляет собой C или N.
В некоторых вариантах осуществления V представляет собой C. В некоторых вариантах осуществления V представляет собой N.
В некоторых вариантах осуществления V выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом определено выше, 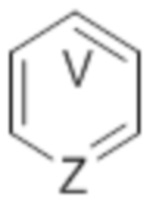 означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, то V находится в орто, мета или пара положении относительно Z.
означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, то V находится в орто, мета или пара положении относительно Z.
В некоторых вариантах осуществления 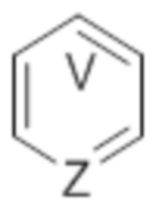 означает ароматическое кольцо, в котором V представляет собой C.
означает ароматическое кольцо, в котором V представляет собой C.
В некоторых вариантах осуществления 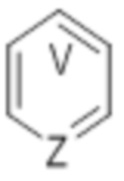 означает ароматическое кольцо, где V представляет собой N, а V находится в орто, мета или пара положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в орто положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в мета положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в пара положении относительно Z.
означает ароматическое кольцо, где V представляет собой N, а V находится в орто, мета или пара положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в орто положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в мета положении относительно Z. В некоторых вариантах осуществления V представляет собой N, и V находится в пара положении относительно Z.
В некоторых вариантах осуществления  представляет собой фенил. В некоторых вариантах осуществления
представляет собой фенил. В некоторых вариантах осуществления 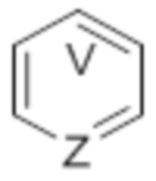 представляет собой пиридин. В некоторых вариантах осуществления
представляет собой пиридин. В некоторых вариантах осуществления  представляет собой пиридазин. В некоторых вариантах осуществления
представляет собой пиридазин. В некоторых вариантах осуществления 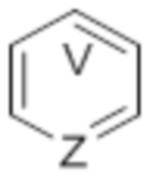 представляет собой пиримидин. В некоторых вариантах осуществления
представляет собой пиримидин. В некоторых вариантах осуществления  представляет собой пиразин.
представляет собой пиразин.
В некоторых вариантах осуществления  выбран из тех, которые изображены в таблицах 1-3 ниже.
выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, каждый R независимо представляет собой водород, галоген, -CN, гидроксил, (C1-C3)фторалкил, (C1-C3)фторалкокси, (C3-C6)циклоалкил, -NO2, -NR1R2, (C1-C4)алкокси, фенокси, -NR1-SO2-NR1R2, -NR1-SO2-R1, -NR1-C(=O)-R1, -NR1-C(=O)-NR1R2, -SO2-NR1R2, -SO3H, -O-SO2-OR3, -O-P(=O)-(OR3)(OR4), -O-CH2-COOR3, или (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой.
В некоторых вариантах осуществления R представляет собой водород. В некоторых вариантах осуществления R представляет собой галоген. В некоторых вариантах осуществления R представляет собой -CN. В некоторых вариантах осуществления R представляет собой гидроксил. В некоторых вариантах осуществления R представляет собой (C1-C3)фторалкил, причем указанный алкил необязательно моно- или дизамещен гидроксилом. В некоторых вариантах осуществления R представляет собой (C1-C3)фторалкокси. В некоторых вариантах осуществления R представляет собой (C3-C6)циклоалкил. В некоторых вариантах осуществления R представляет собой -NO2. В некоторых вариантах осуществления R представляет собой NR1R2. В некоторых вариантах осуществления R представляет собой (C1-C4)алкокси. В некоторых вариантах осуществления R представляет собой фенокси. В некоторых вариантах осуществления R представляет собой -NR1-SO2-NR1R2. В некоторых вариантах осуществления R является -NR1-SO2-R1. В некоторых вариантах осуществления R представляет собой -NR1-C(=O)-R1. В некоторых вариантах осуществления R представляет собой -NR1-C(=O)-NR1R2. В некоторых вариантах осуществления R представляет собой -SO2-NR1R2. В некоторых вариантах осуществления R представляет собой -SO3H. В некоторых вариантах осуществления R представляет собой -O-SO2-OR3. В некоторых вариантах осуществления R представляет собой -O-P(=O)-(OR3)(OR4). В некоторых вариантах осуществления R представляет собой -O-CH2-COOR3. В некоторых вариантах осуществления R представляет собой (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксилом.
В некоторых вариантах осуществления каждый R независимо представляет собой галоген, (C1-C3)фторалкил, (C1-C3)фторалкокси, -NR1R2, (C1-C4)алкокси, или (C1-C3)алкил.
В некоторых вариантах осуществления каждый R независимо представляет собой водород, метил, метокси, трифторметил, трифторметокси, амино, галоген или -O-P(=O)-(OR3)(OR4). В некоторых вариантах осуществления R представляет собой метил. В некоторых вариантах осуществления R представляет собой метокси. В некоторых вариантах осуществления R представляет собой трифторметил. В некоторых вариантах осуществления R представляет собой трифторметокси. В некоторых вариантах осуществления R представляет собой амино. В некоторых вариантах осуществления R представляет собой -O-P(=O)-(OR3)(OR4).
В некоторых вариантах осуществления каждый R независимо представляет собой метил, метокси, трифторметил, галоген, трифторметокси или амино.
В некоторых вариантах осуществления R выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, Q представляет собой N или O, при условии, что R" отсутствует, когда Q представляет собой O.
В некоторых вариантах осуществления Q представляет собой N. В некоторых вариантах осуществления Q представляет собой O, а R" отсутствует.
В некоторых вариантах осуществления Q выбран из тех, которые изображены в таблицах 1-3 ниже.
Как описано в целом выше, каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил.
В некоторых вариантах осуществления R1 представляет собой водород, R1 представляет собой (C1-C3)алкил. В некоторых вариантах осуществления R2 представляет собой водород. В некоторых вариантах осуществления R2 представляет собой (C1-C3)алкил.
В некоторых вариантах осуществления каждый из R1 и R2 выбран независимо от тех, которые изображены в таблицах 1-3 ниже.
Как описано в целом выше, каждый из R3 и R4 независимо представляет собой водород, Li+, Na+, K+, N+(Ra)4 или бензил.
В некоторых вариантах осуществления R3 представляет собой водород, R3 представляет собой Li+. В некоторых вариантах осуществления R3 представляет собой Na+. В некоторых вариантах осуществления R3 представляет собой K+. В некоторых вариантах осуществления R3 представляет собой N+(Ra)4. В некоторых вариантах осуществления R3 представляет собой бензил.
В некоторых вариантах осуществления R4 представляет собой водород, R4 представляет собой Li+. В некоторых вариантах осуществления R4 представляет собой Na+. В некоторых вариантах осуществления R4 представляет собой K+. В некоторых вариантах осуществления R4 представляет собой N+(Ra)4. В некоторых вариантах осуществления R4 представляет собой бензил.
В некоторых вариантах осуществления каждый из R3 и R4 независимо выбран от тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, n представляет собой 1, 2 или 3.
В некоторых вариантах осуществления n представляет собой 1 или 2. В некоторых вариантах осуществления n представляет собой 1. В некоторых вариантах осуществления n представляет собой 2. В некоторых вариантах n представляет собой 3.
В некоторых вариантах осуществления n выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, n’ представляет собой 1, 2 или 3.
В некоторых вариантах осуществления n’ представляет собой 1 или 2. В некоторых вариантах осуществления n’ представляет собой 1. В некоторых вариантах осуществления n’ представляет собой 2. В некоторых вариантах осуществления n’ представляет собой 3.
В некоторых вариантах осуществления n’ выбран из тех, которые изображены в таблицах 1-3 ниже.
Как описано в целом выше, каждый R’ независимо представляет собой водород, (C1-C3)алкил, гидроксил, галоген, -NO2, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3)фторалкил, ((C1-C4)алкокси, -O-P(=O)-(OR3)(OR4), -CN, группу формулы (IIa):  , или группу формулы (IIIa):
, или группу формулы (IIIa): 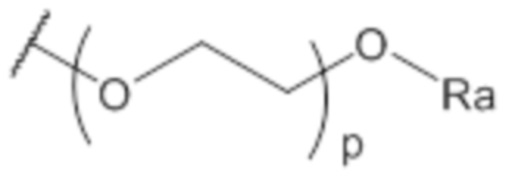 .
.
В некоторых вариантах осуществления R’ представляет собой водород. В некоторых вариантах осуществления R’ представляет собой (C1-C3алкил. В некоторых вариантах осуществления R’ м гидроксил. В некоторых вариантах осуществления R’ представляет собой галоген. В некоторых вариантах осуществления R’ представляет собой -NO2. В некоторых вариантах осуществления R’ представляет собой -NR1R2. В некоторых вариантах осуществления R’ представляет собой морфолинил. В некоторых вариантах осуществления R’ представляет собой морфолино. В некоторых вариантах осуществления R’ представляет собой N-метилпиперазинил. В некоторых вариантах осуществления R’ представляет собой (C1-C3)фторалкил. В некоторых вариантах осуществления R’ представляет собой (C1-C4)алкокси. В некоторых вариантах осуществления R’ представляет собой -O-P(=O)-(OR3)(OR4). В некоторых вариантах осуществления R’ представляет собой -CN. В некоторых вариантах осуществления R’ представляет собой группу формулы (IIa): 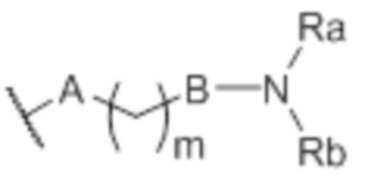 . В некоторых вариантах осуществления R’ представляет собой группу формулы (IIIa):
. В некоторых вариантах осуществления R’ представляет собой группу формулы (IIIa):  .
.
В некоторых вариантах осуществления R’ представляет собой амино. В некоторых вариантах осуществления R’ представляет собой метил. В некоторых вариантах осуществления R’ представляет собой группу формулы 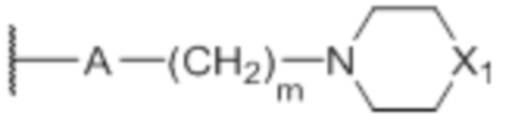 , где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3 при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3 при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления R’ представляет собой группу формулы 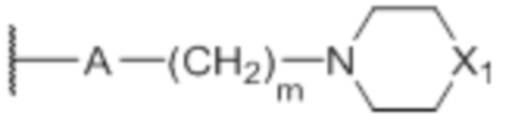 , где A представляет собой O или NH, m представляет собой 2 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группой, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группой, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления R’ представляет собой группу формулы 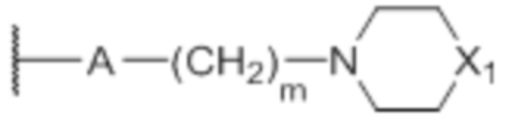 , где A представляет собой O или NH, m представляет собой 3, а X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 3, а X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления каждый R’ независимо представляет собой водород, галоген, амино, метил, -O-P(=O)-(OR3)(OR4), или группу формулы 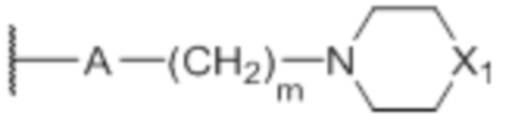 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления каждый R’ независимо представляет собой водород, галоген, метил или группу формулы 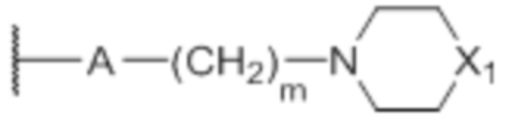 , где A представляет собой O или NH, m представляет собой 2 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления каждый R’ независимо представляет собой галоген, (C1-C3)алкил, гидроксил, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3)фторалкил, (C1-C4)алкокси или группу формул (IIa) или (IIIa), как описано в настоящем описании.
В некоторых вариантах осуществления R’ представляет собой галоген или метил.
В некоторых вариантах осуществления каждый R’ выбран независимо от тех, которые изображены в таблицах 1-3 ниже.
Как обычно описано выше, А представляет собой ковалентную связью, кислород или NH.
В некоторых вариантах осуществления А представляет собой ковалентную связь. В некоторых вариантах осуществления А представляет собой кислород. В некоторых вариантах осуществления A представляет собой NH.
В некоторых вариантах осуществления A выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, B представляет собой ковалентную связь или NH.
В некоторых вариантах осуществления B представляет собой ковалентную связь. В некоторых вариантах осуществления B является NH.
В некоторых вариантах осуществления B выбран из тех, которые изображены в таблицах 1-3 ниже.
Как в целом описано выше, m представляет собой 1, 2, 3, 4 или 5.
В некоторых вариантах осуществления m представляет собой 1. В некоторых вариантах осуществления m представляет собой 2. В некоторых вариантах осуществления m представляет собой 3. В некоторых вариантах осуществления m представляет собой 4. В некоторых вариантах осуществления m представляет собой 5.
В некоторых вариантах осуществления m выбран из тех, которые изображены в таблицах 1-3 ниже.
Как описано в целом выше, p представляет собой 1, 2 или 3.
В некоторых вариантах осуществления p представляет собой 1. В некоторых вариантах осуществления p представляет собой 2. В некоторых вариантах осуществления p представляет собой 3. В некоторых вариантах осуществления p представляет собой 4. В некоторых вариантах осуществления p представляет собой 5.
В некоторых вариантах осуществления p выбран из тех, которые изображены в таблицах 1-3 ниже.
Как описано в целом выше, каждый из Ra и Rb независимо представляет собой водород, ((C1-C5)алкил или (C3-C6)циклоалкил, или Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, причем указанный гетероцикл необязательно замещается одним или несколькими Ra, при условии, что, когда R’ представляет собой группу (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие группы R’ отличаются от указанной группы (IIa) или (IIIa).
В некоторых вариантах осуществления Ra представляет собой водород. В некоторых вариантах осуществления Ra представляет собой (C1-C5)алкил. В некоторых вариантах осуществления Ra представляет собой (C3-C6)циклоалкил. В некоторых вариантах осуществления Rb представляет собой водород. В некоторых вариантах осуществления Rb представляет собой (C1-C5)алкилом. В некоторых вариантах осуществления Rb представляет собой (C3-C6)циклоалкил.
В некоторых вариантах осуществления Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ представляет собой группу формул (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие группы R’ отличаются от указанной группы формул (IIa) или (IIIa). В некоторых вариантах осуществления насыщенный 5- или 6-членный гетероцикл, образованный Ra и Rb вместе с атомом азота, к которому они присоединены, как описано выше, необязательно имеет дополнительный гетероатом, выбранный из N, O и S.
В некоторых вариантах осуществления Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, имеющий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл замещен одним или более Ra, при условии, что, когда R’ является группой формул (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие группы R’ отличаются от указанной группы формул (IIa) или (IIIa).
В некоторых вариантах осуществления Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5-членный гетероцикл, при условии, что, когда R’ представляет собой группу формул (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие группы R’ отличаются от указанной группы формул (IIa) или (IIIa).
В некоторых вариантах осуществления Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 6-членный гетероцикл, при условии, что, когда R’ представляет собой группу формул (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие группы R’ отличаются от указанной группы формул (IIa) или (IIIa).
В некоторых вариантах осуществления Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, необязательно имеющий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ представляет собой группу (IIa) или (IIIa), n’ может представлять собой 2, только если другая группа R’ отличается от указанной группы (IIa) или (IIIa).
В некоторых вариантах осуществления каждый из Ra и Rb выбран независимо от тех, которые изображены в таблицах 1-3 ниже.
Как описано в общих чертах выше, R” представляет собой водород, (C1-C4)алкил или группу формулы (IIa), как определено выше.
В некоторых вариантах осуществления R” представляет собой водород или (C1-C4)алкил. В некоторых вариантах осуществления R” представляет собой водород. В некоторых вариантах осуществления R” представляет собой (C1-C4)алкил. В некоторых вариантах осуществления R” представляет собой группу формулы (IIa), как описано в настоящем документе.
В некоторых вариантах осуществления R” представляет собой группу формулы 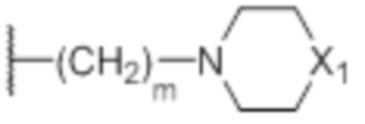 , где m представляет собой 2 или 3, а X1 представляет собой O, CH2, или N-CH3.
, где m представляет собой 2 или 3, а X1 представляет собой O, CH2, или N-CH3.
В некоторых вариантах осуществления R” выбран из тех, которые изображены в таблицах 1-3 ниже.
В некоторых вариантах осуществления n представляет собой 1; n’ представляет собой 1 или 2; R” представляет собой H; R выбран из метила, метокси, трифторметила, галогена, трифторметокси и амино; и каждый R’ независимо представляет собой галоген, метилом или группу 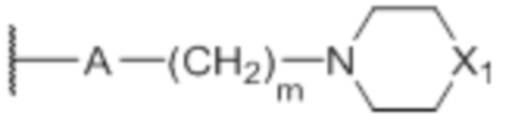 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
В некоторых вариантах осуществления n представляет собой 1; n’ представляет собой 1; R” представляет собой H; R выбран из метила, метокси, трифторметила, галогена и трифторметокси; и R’ представляет собой галоген или метил.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Ia):
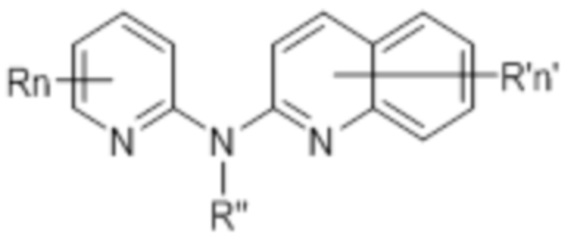 (Ia)
(Ia)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, R”, n и n’ независимо представляет собой как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Ib):
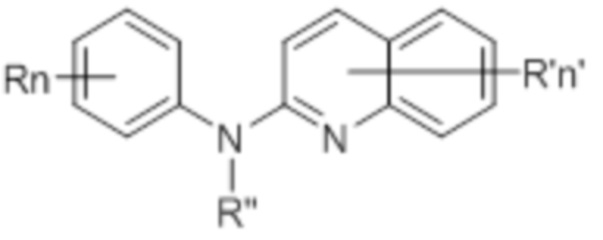 (Ib)
(Ib)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, R”, n и n’ независимо представляет собой как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Ic):
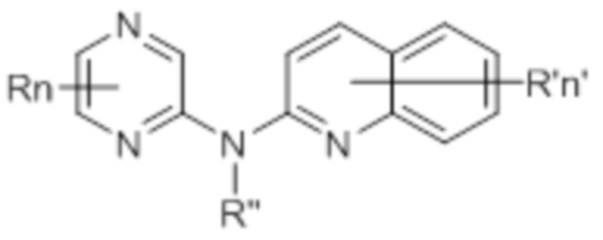 (Ic)
(Ic)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, R”, n и n’ независимо представляет собой как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (Ib’):
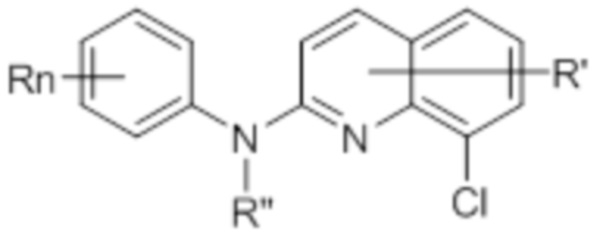 (Ib’)
(Ib’)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, R” и n независимо представляет собой как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (Ib) или его фармацевтически приемлемую соль, где:
каждый R независимо представляет собой галоген, (C1-C3)фторалкил, (C1-C3)фторалкокси, -NR1R2, (C1-C4)алкокси или (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой;
n представляет собой 1 или 2;
n’ представляет собой 1 или 2;
каждый из R1 и R2 независимо представляет собой водород или C1-C3)алкил;
каждый из R’ независимо представляет собой галоген, (C1-C3)алкил, гидроксил, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3фторалкил, C1-C4)алкокси или группу формул (IIa) или (IIIa), как описано в настоящем описании;
А представляет собой ковалентную связь, кислород или NH;
B представляет собой ковалентную связь или NH;
m представляет собой 1, 2, 3, 4 или 5;
p представляет собой 1, 2 или 3;
каждый из Ra и Rb независимо представляет собой водород, (C1-C5)алкил или (C3-C6)циклоалкил, или
Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, необязательно имеющий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ представляет собой группу (IIa) или (IIIa), n’ может представлять собой 2, только если другая группа R’ отличается от указанной группы (IIa) или (IIIa); и
R” представляет собой водород или (C1-C4)алкил.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Ib) или его фармацевтически приемлемую соль, где каждый R’ независимо представляет собой водород, галоген, (C1-C3)алкил или (C1-C4)алкоксигруппу, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой; R” представляет собой водород или (C1-C4)алкил; n представляет собой 1 или 2; n’ представляет собой 1 или 2; когда n представляет собой 1, R представляет собой (C1-C3)фторалкокси, NR1R2, или фенокси, где каждый из R1 и R2 независимо представляет собой (C1-C3)алкил; и когда n представляет собой 2, одна из двух R-групп представляет собой (C1-C3)фторалкокси, а другая R-группа представляет собой (C1-C3)алкил.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Ib) или его фармацевтически приемлемую соль, где каждый R независимо представляет собой (C1-C3)фторалкокси; каждый R’ независимо представляет собой водород, галоген, (C1-C3)алкил или (C1-C4)алкокси; R” представляет собой водород или (C1-C4)алкил; n представляет собой 1; и n’ представляет собой 1 или 2.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (Ib’) или его фармацевтически приемлемую соль, где каждый R независимо представляет собой водород, галоген, (C1-C3)алкил, -NR1R2, (C1-C3)фторалкокси, -NO2, фенокси или (C1-C4)алкокси, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой; каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил; R’ представляет собой водород, галоген, (C1-C3)алкил или (C1-C4)алкокси, с той оговоркой, что R’ отличается от метильной группы в положении 4 хинолиновой группы; R” представляет собой водород или (C1-C4)алкил; n представляет собой 1, 2 или 3; и n’ представляет собой 1 или 2.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (Id):
 (Id)
(Id)
или его фармацевтически приемлемую соль, где каждый из R и R’ независимо представляет собой, как определено выше и описано в вариантах осуществления в настоящем документе, как по отдельности, так и в комбинации, и R’” представляет собой водород или группу 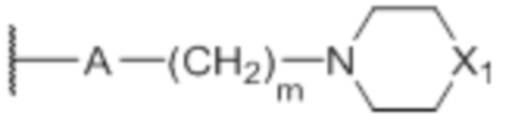 , где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3.
, где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (Id) или его фармацевтически приемлемую соль, где R представляет собой метил, метокси, трифторметил, галоген, трифторметокси или амино; R’ представляет собой галоген или метил, и R’’’ представляет собой водород или группу 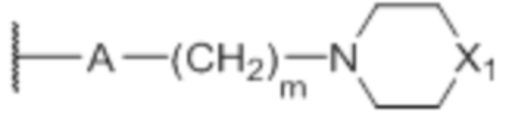 , где A представляет собой O или NH, m представляет собой 2 или 3, и X1 представляет собой O, CH2 или N-CH3.
, где A представляет собой O или NH, m представляет собой 2 или 3, и X1 представляет собой O, CH2 или N-CH3.
В некоторых вариантах осуществления R’’’ представляет собой водород. В некоторых вариантах осуществления R’’’ представляет собой группу 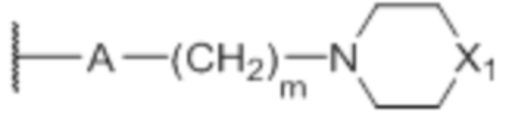 , где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3. В некоторых вариантах осуществления R’’’ представляет собой группу
, где A представляет собой O или NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3. В некоторых вариантах осуществления R’’’ представляет собой группу 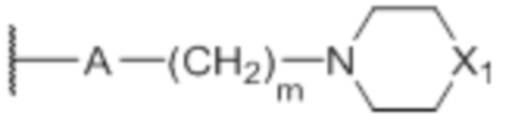 , где A представляет собой O, m представляет собой 2 или 3, и X1 представляет собой O, CH2 или N-CH3. В некоторых вариантах осуществления R’’’ представляет собой группу
, где A представляет собой O, m представляет собой 2 или 3, и X1 представляет собой O, CH2 или N-CH3. В некоторых вариантах осуществления R’’’ представляет собой группу 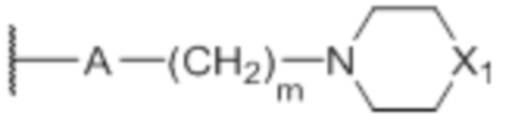 , где A представляет собой NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3.
, где A представляет собой NH, m представляет собой 2 или 3, а X1 представляет собой O, CH2 или N-CH3.
Кроме того, настоящее изобретение обеспчеивает производное хинолина формулы (I’)
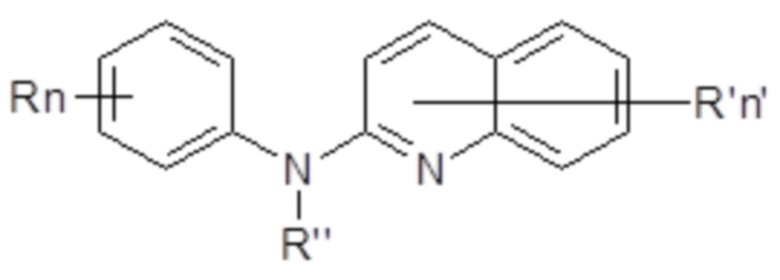 (I’),
(I’),
где:
R независимо представляет собой атом галогена или группу, выбранную из (C1-C3)фторалкильной группы, (C1-C3)фторалкоксигруппы, группы a -NR1R2 группы, (C1-C4)алкоксигруппы и (C1-C3)алкильной группы, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой,
n представляет собой 1 или 2,
n’ представляет собой 1 или 2,
R1 и R2 независимо представляют собой атом водорода или (C1-C3)алкильную группу,
R’ независимо представляет собой атом галогена или группу, выбранную из (C1-C3)алкильной группы, гидроксильной группы, группы -NR1R2, морфолинильной или морфолино группы, N-метилпиперазинильной группы, (C1-C3)фторалкильной группы и (C1-C4)алкоксигруппы, и дополнительно могут быть группой, выбранной из:
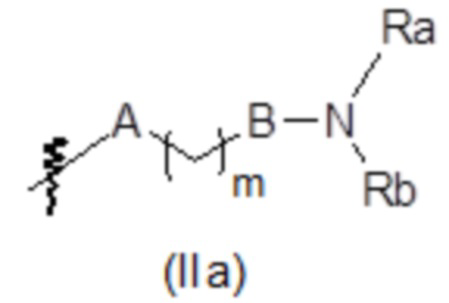 ,
,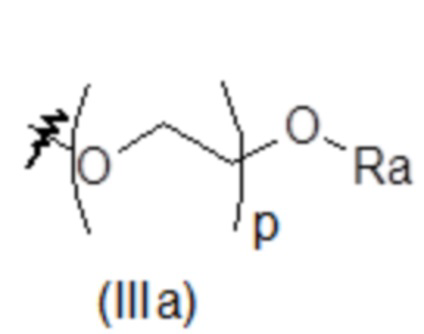 ,
,
А представляют собой ковалентную связь, атом кислорода или NH,
B - ковалентная связь или NH,
m представляют собой 2, 3 или 4,
p представляют собой 1, 2 или 3,
Ra и Rb независимо представляют собой атом водорода, (C1-C5)алкильную группу или (C3-C6)циклоалкильную группу,
Ra и Rb могут дополнительно образовывать вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, необязательно содержащий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл необязательно замещается одним или более Ra, при условии, что, когда R’ представляют собой (IIa) или (IIIa), n’ может представлять собой 2, только если другие группы R’ отличаются от указанной группы (IIa) или (IIIa).),
R’’ является атомом водорода или алкильной группой (C1-C4),
или любым из его метаболитов или фармацевтически приемлемой солью или любой из их энантиомеров или диастереоизомеров,
для применения для лечения или предупреждения рака или дисплазии.
Согласно одному аспекту настоящее изобретение обеспечивает производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемую соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где R независимо представляет собой метильную группу, метоксигруппу, трифторметильную группу, атом галогена и, в частности, атом фтора или хлора, трифторметоксигруппу и аминогруппу.
Согласно дополнительному аспекту, в настоящем документе представлено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где R’ независимо представляет собой атом галогена и, в частности, атом фтора или хлора, группу -NR1R2 и предпочтительно аминогруппу, гидроксильную группу, алкильную группу (C1-C3), предпочтительно метильную группу или группу 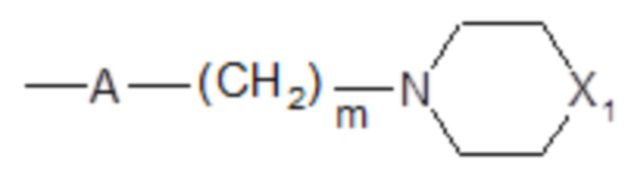 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ равно 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ равно 2, другая группа R’ отличается от указанной группы.
Согласно дополнительному аспекту, в настоящем документе представлено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где R’ независимо представляет собой атом галогена и, в частности, атом фтора или хлора, метильную группу или группу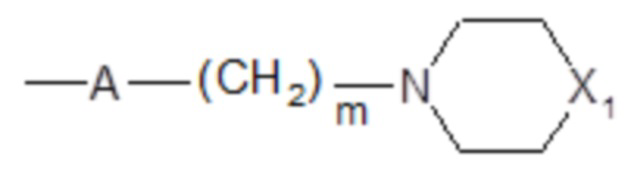 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда R’ представляет собой такую группу, n’ представляет собой 1 или 2, а когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
Согласно дополнительному аспекту, в настоящем документе представлено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где n представляет собой 1, n’ представляет собой 1 или 2, R” представляет собой H, R выбран из метильной группы, метоксигруппы, трифторметильной группы, атома галогена и, в частности, атома фтора или хлора, трифторметоксигруппы и аминогруппы, а R’ представляет собой атом галогена и, в частности, атом фтора или хлора, метильную группу или группу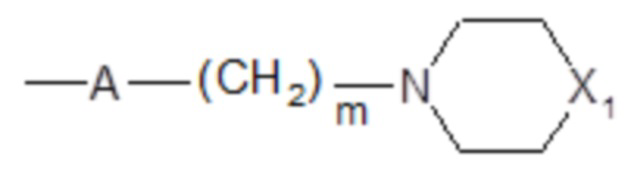 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, при условии, что, когда n’ представляет собой 2, другая группа R’ отличается от указанной группы.
Согласно дополнительному аспекту, в настоящем описании представлено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где n представляет собой 1, n’ представляет собой 1, R” представляет собой H, R выбран из метильной группы, метоксигруппы, трифторметильной группы, атома галогена и, в частности, атома фтора или хлора и трифторметоксигруппы, а R’ представляет собой атом галогена и, в частности, атом фтора или хлора или атом хлора или метильную группу.
Согласно дополнительному аспекту, в настоящем описании обеспечено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где оно определено формулой (I’)
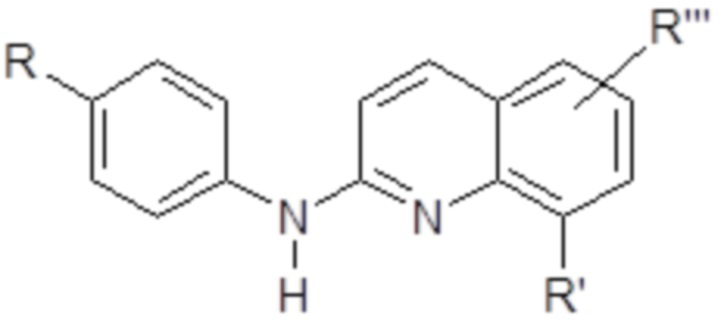 (I’’),
(I’’),
где
R выбран из метильной группы, метоксигруппы, трифторметильной группы, атома галогена и, в частности, атома фтора или хлора, трифторметоксигруппы и аминогруппы, и
R’ представляет собой атом галогена и, в частности, атом фтора или хлора или метильную группу, и
R’’ представляет собой атом водорода или группу 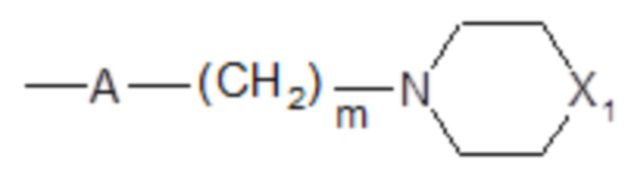 , где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, и, в частности, представляет собой атом водорода.
, где A представляет собой O или NH, m представляет собой 2 или 3 и X1 представляет собой O, CH2 или N-CH3, и, в частности, представляет собой атом водорода.
В некоторых вариантах осуществления соединение согласно настоящему изобретению представляет собой соединение формулы: 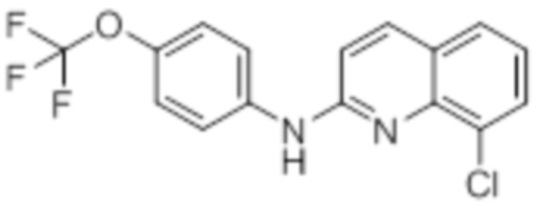 (“ABX464”) или его фармацевтически приемлемую соль. В некоторых вариантах осуществления соединение ABX464 или его фармацевтически приемлемая соль находится в аморфной форме. В некоторых вариантах осуществления соединение ABX464 или его фармацевтически приемлемая соль находится в кристаллизованной форме. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль имеет температуру плавления 120,5°C (±2°C). В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль показывает пики на XRPD (X-ray powder diffractogram - рентгеновская порошковая дифрактограмма) при углах 7,3, 14,6, 18,4 и 24,9. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль показывает один или более пиков XRPD при углах, выбранных из 18,0, 24,2, 28,3 и 29,5. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемой соли показывает один или несколько пиков XRPD под углами, выбранными из 18,6, 22,3, 23,0 и 23,5.
(“ABX464”) или его фармацевтически приемлемую соль. В некоторых вариантах осуществления соединение ABX464 или его фармацевтически приемлемая соль находится в аморфной форме. В некоторых вариантах осуществления соединение ABX464 или его фармацевтически приемлемая соль находится в кристаллизованной форме. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль имеет температуру плавления 120,5°C (±2°C). В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль показывает пики на XRPD (X-ray powder diffractogram - рентгеновская порошковая дифрактограмма) при углах 7,3, 14,6, 18,4 и 24,9. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемая соль показывает один или более пиков XRPD при углах, выбранных из 18,0, 24,2, 28,3 и 29,5. В некоторых вариантах осуществления кристаллизованная форма соединения ABX464 или его фармацевтически приемлемой соли показывает один или несколько пиков XRPD под углами, выбранными из 18,6, 22,3, 23,0 и 23,5.
Согласно дополнительному аспекту, в настоящем документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или их фармацевтически приемлемая соль для применения, как определено в настоящем документе, где указанное соединение представляет собой 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин и представляет собой кристаллическую полиморфную форму, характеризующуюся следующими основными пиками , выраженными как градус 2-тета углов при анализе XRPD: 7,3, 14,6, 23,5 и 28,4 (каждый раз ±0,2), и может дополнительно показывать следующие дополнительные пики, выраженные в виде градуса 2-тета углов при анализе XRPD: 12,1, 17,3, 18,4, 23,0; 24,2, 24,9, 27,4 и 29,1 (каждый раз ±0,2) и даже необязательно дополнительно следующие пики, выраженные в виде градуса 2-тета углов: 13,7, 16,3, 16,9, 18,1, 22,4, и 29,6 (каждый раз ±0,2).
В некоторых вариантах осуществления соединение изобретения выбрано из Таблицы 1:
Таблица 1 (соединения формулы Ia, как определено выше)
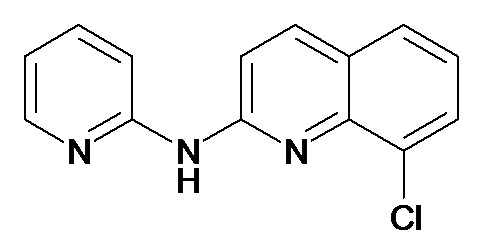
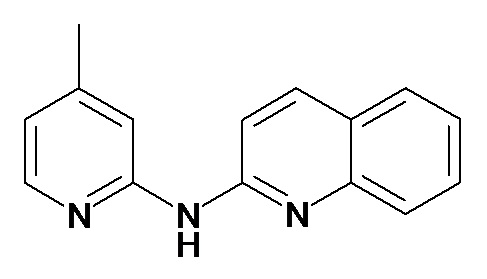
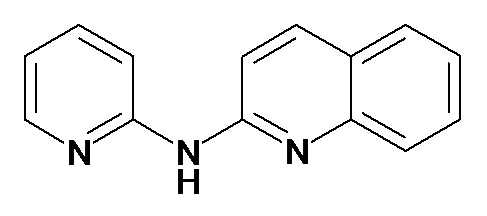
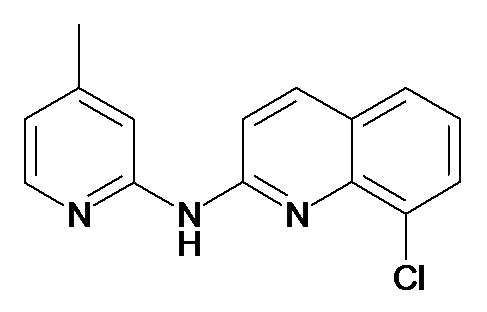
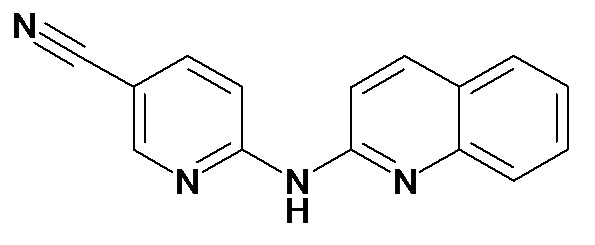
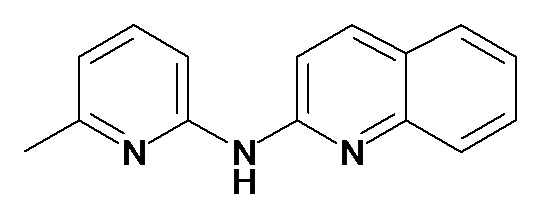
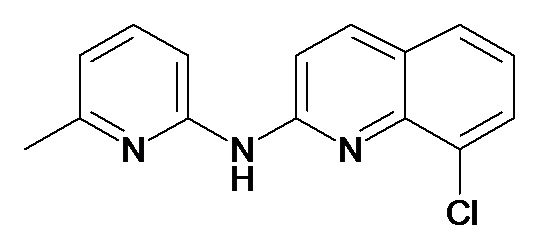
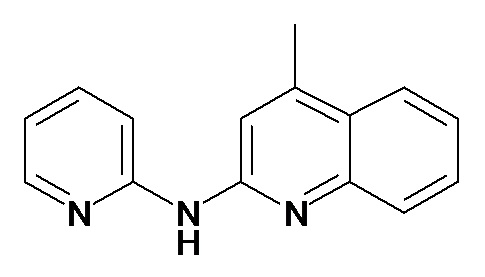
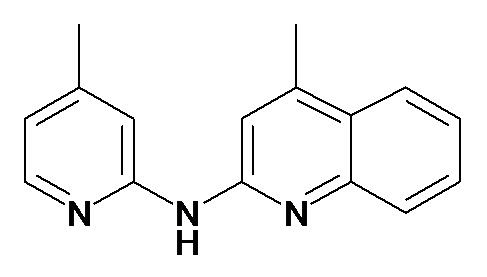
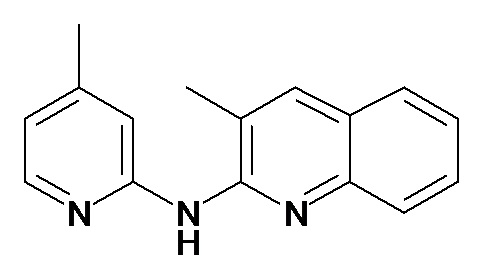
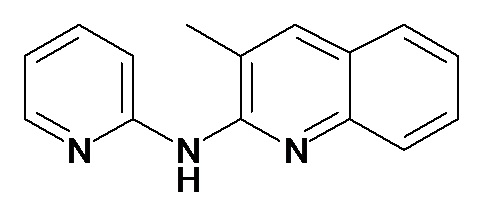
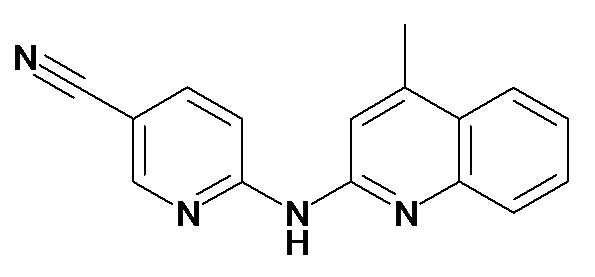
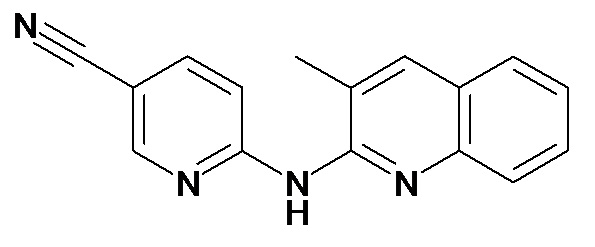
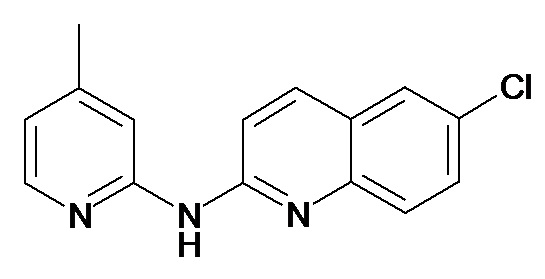
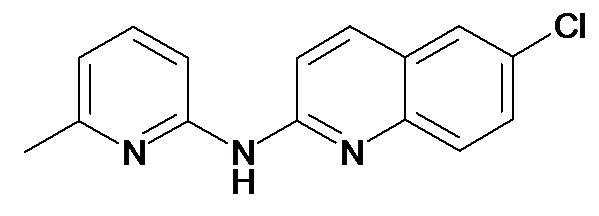
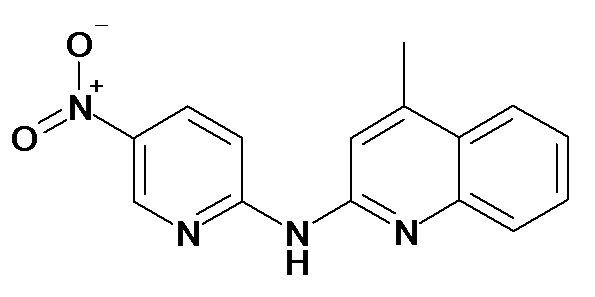
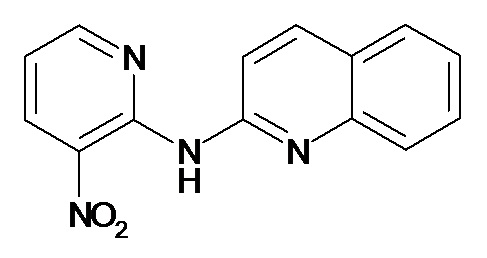
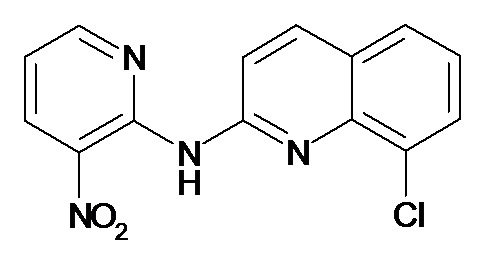
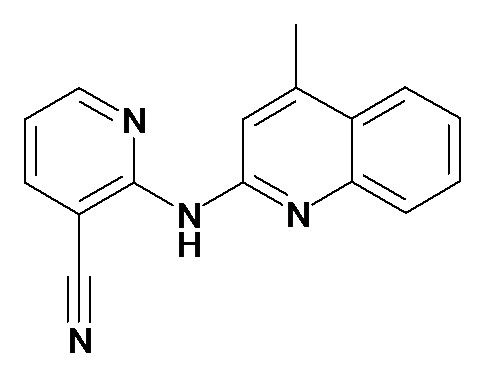
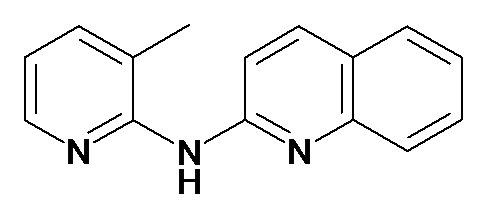
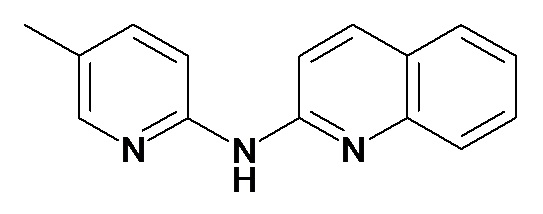
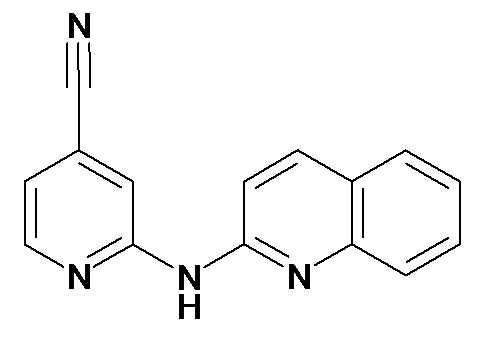
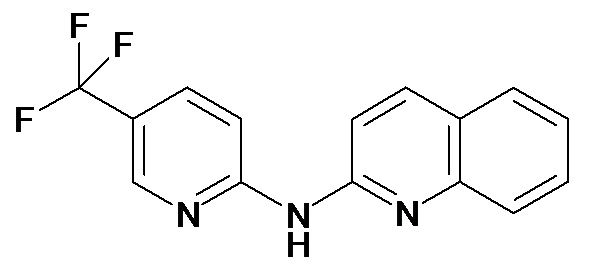
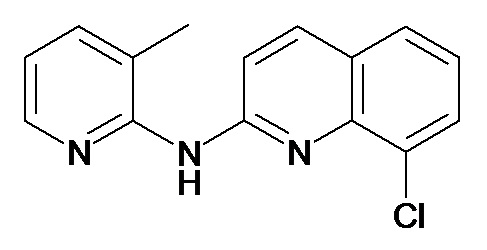
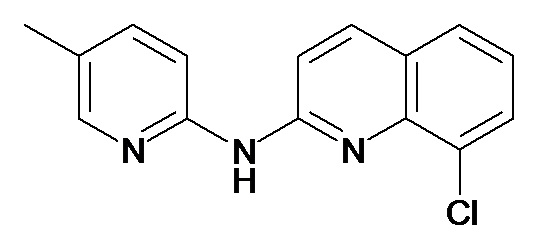
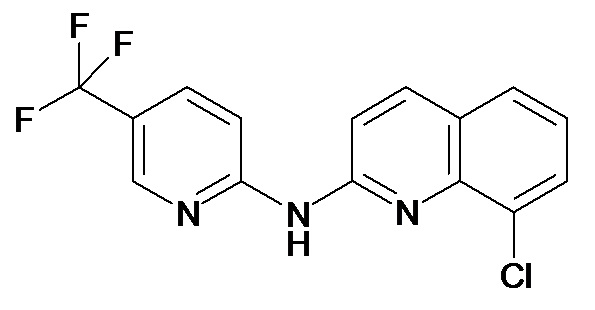
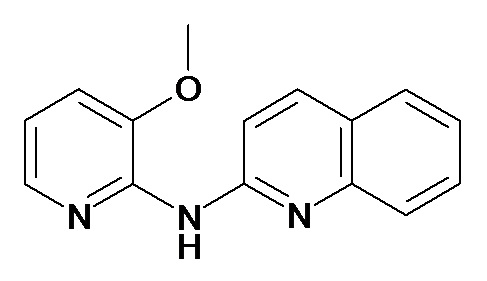
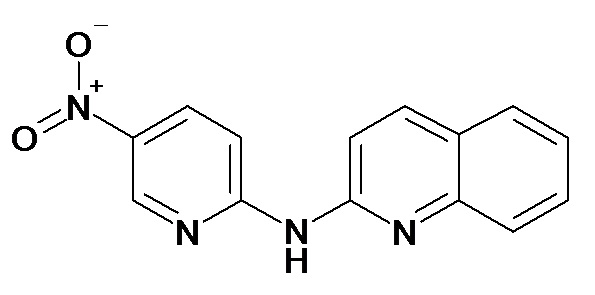
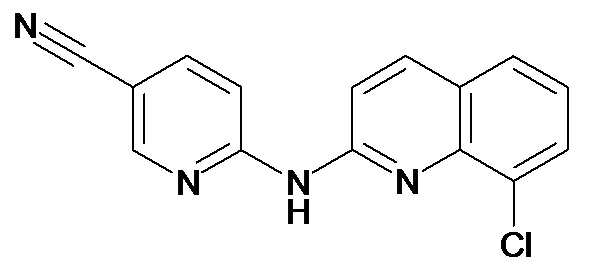
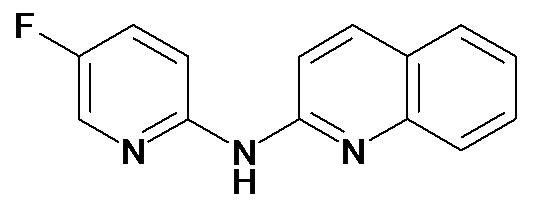
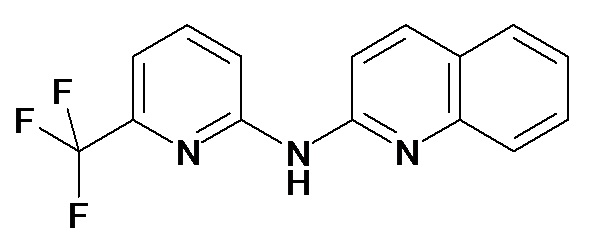
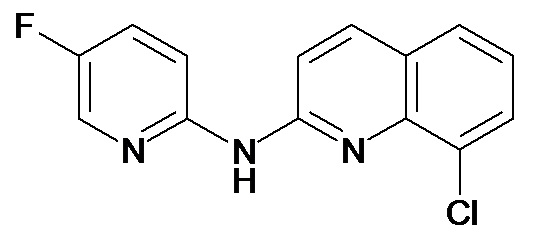
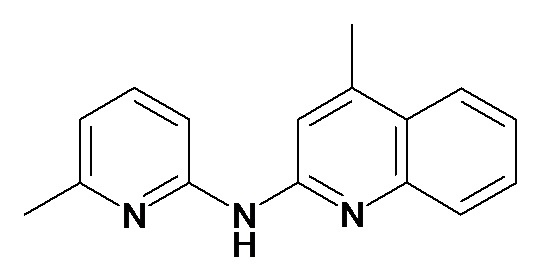
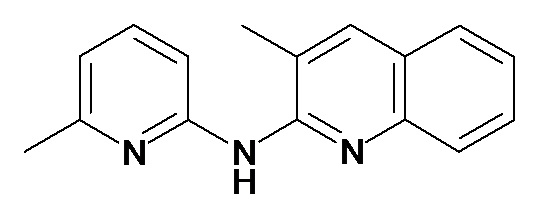
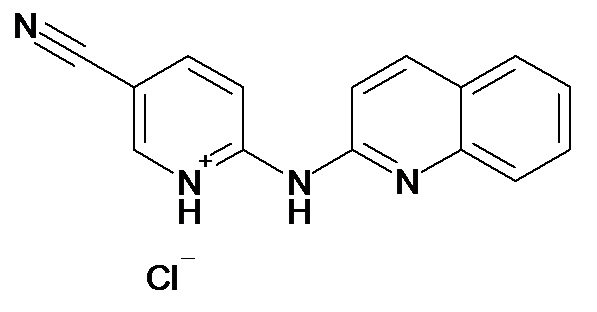
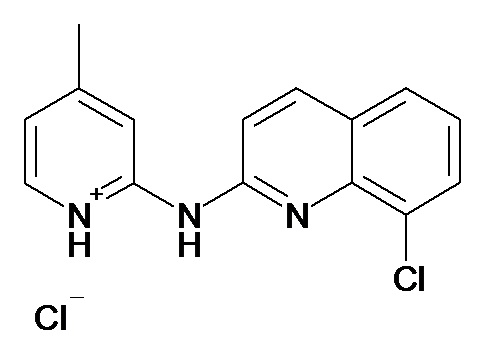
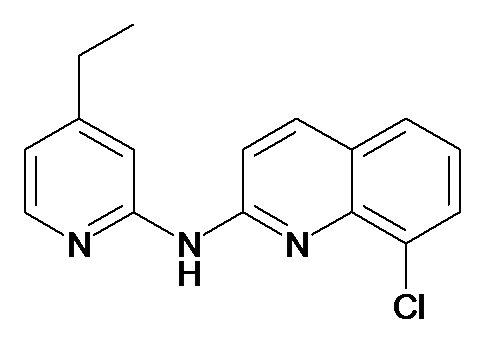
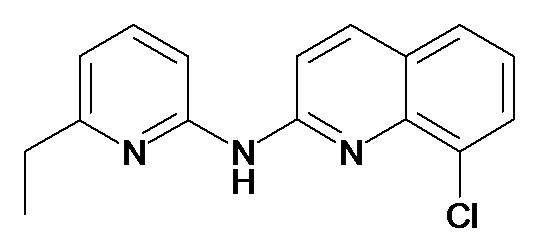
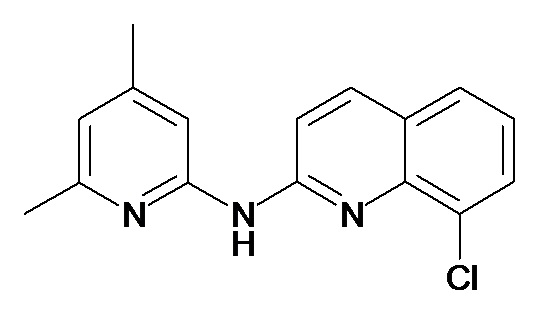
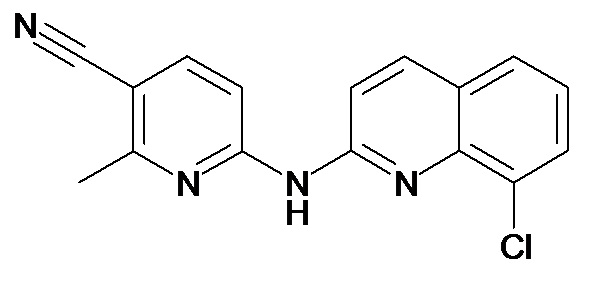
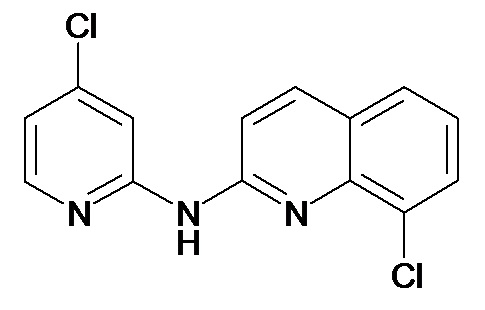
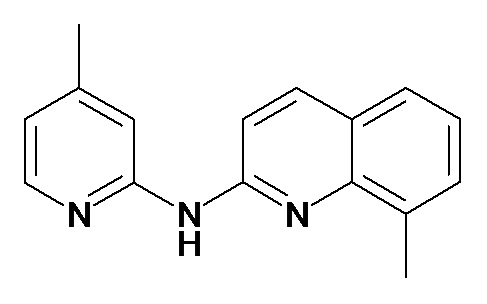
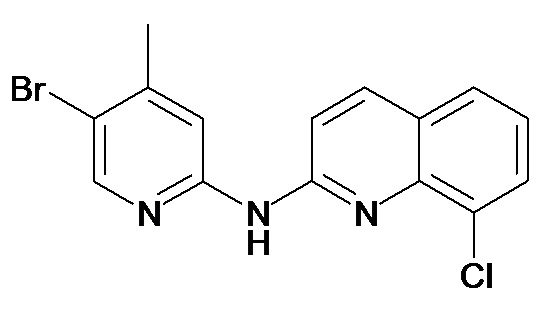
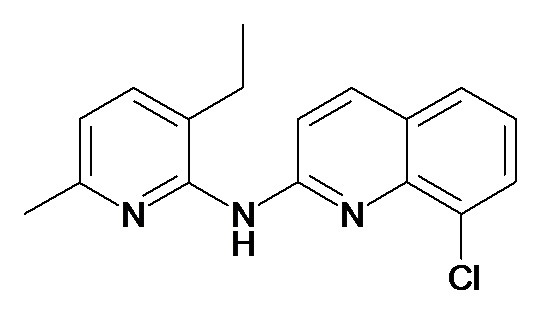
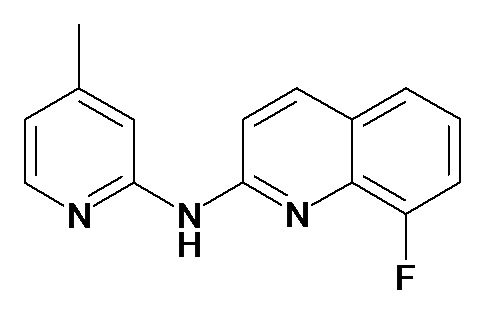
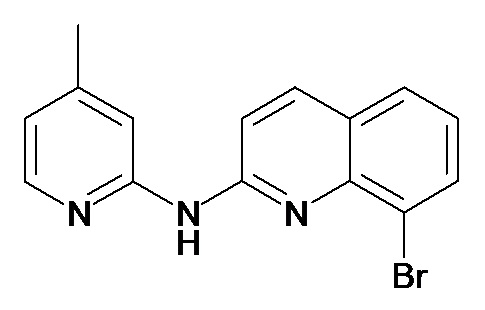
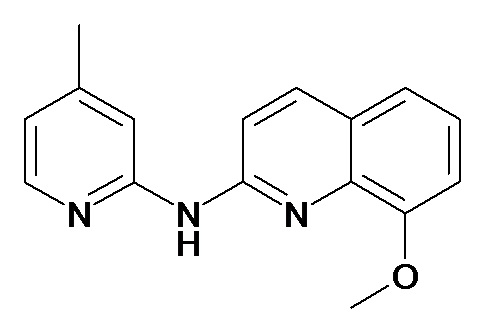
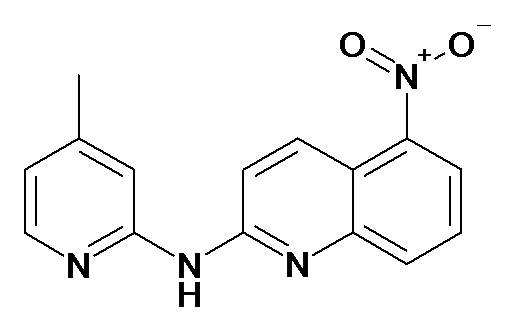
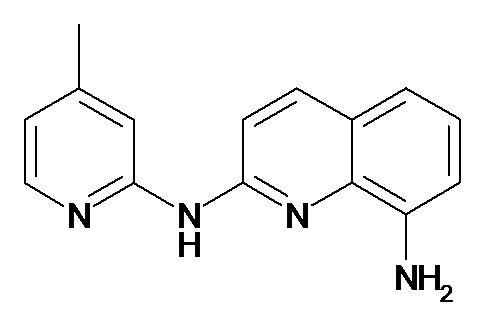
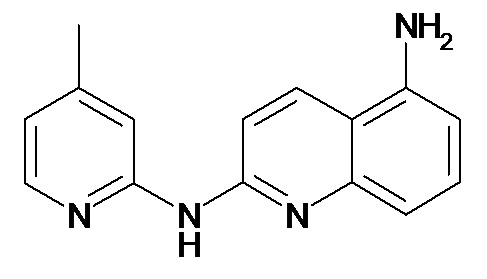
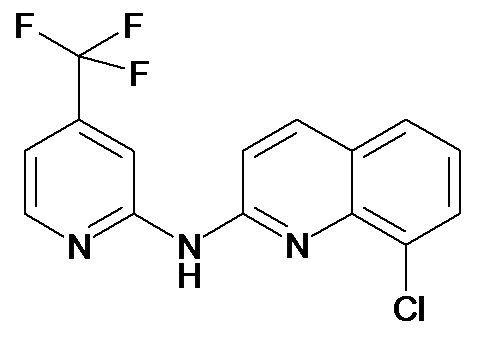
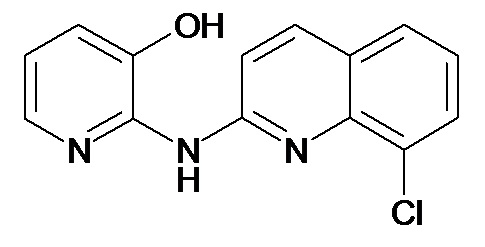
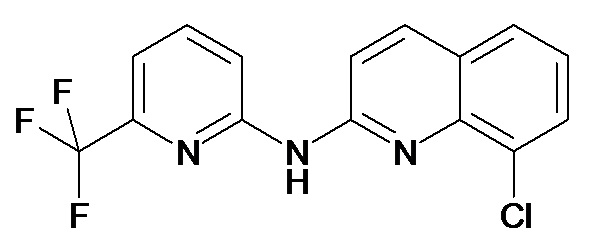
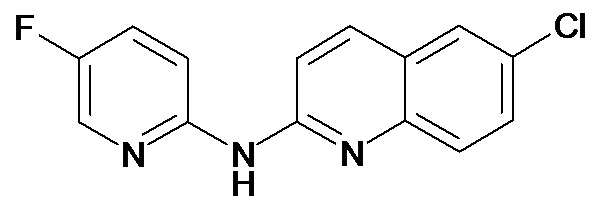
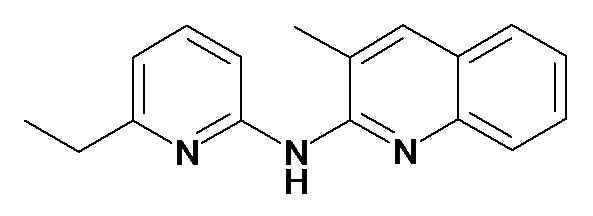
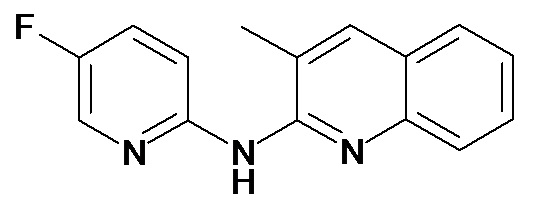
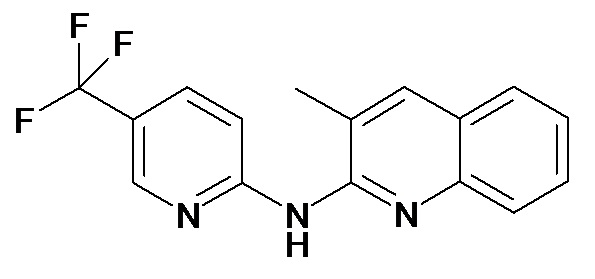
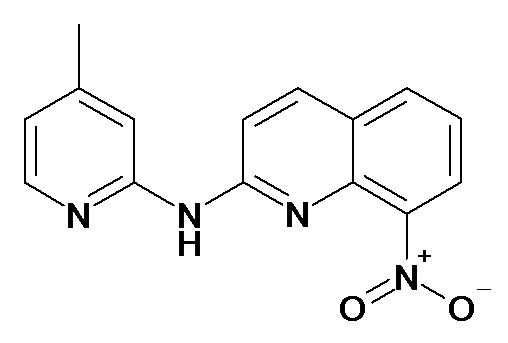
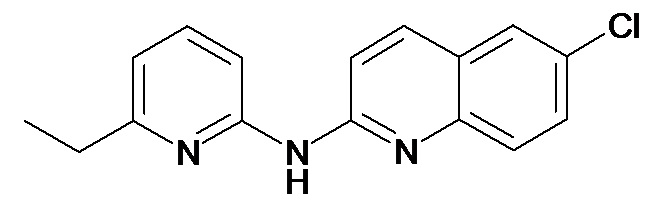
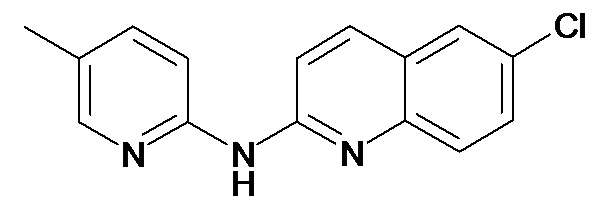
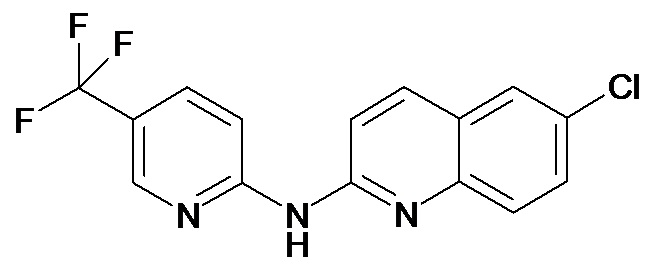
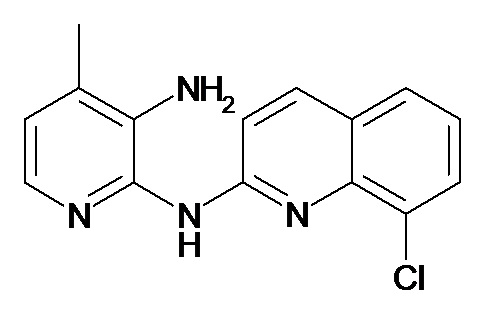

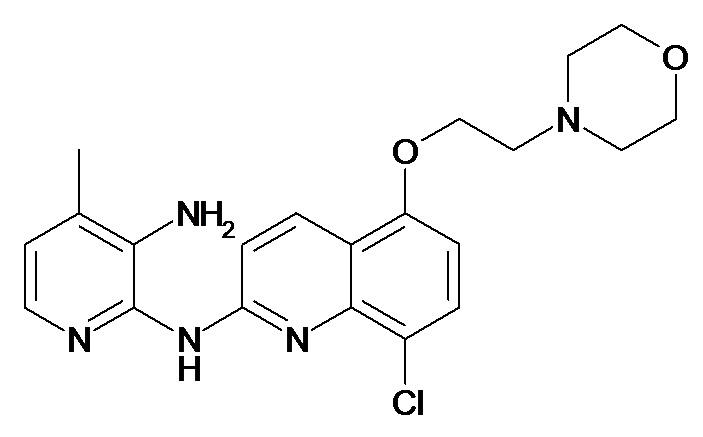
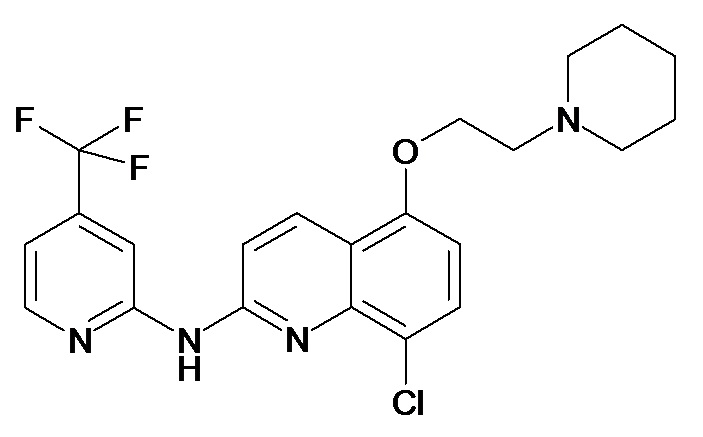
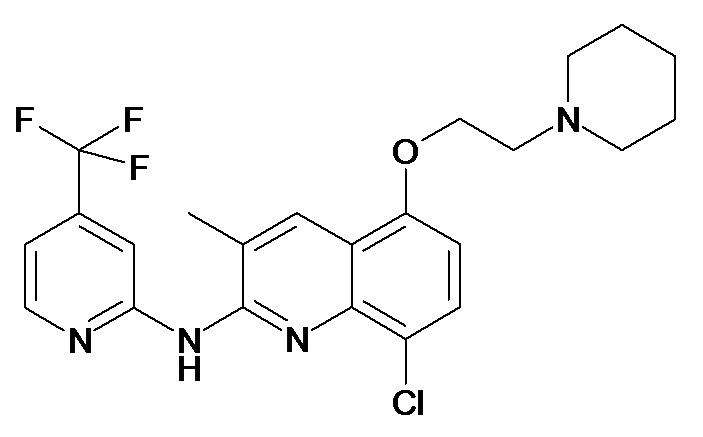
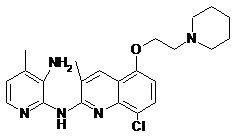
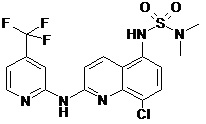
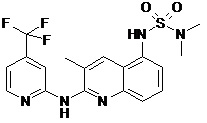
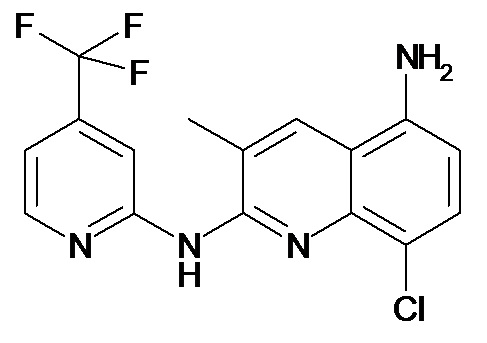
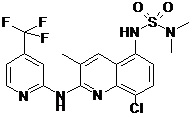
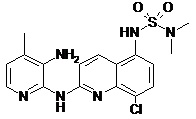
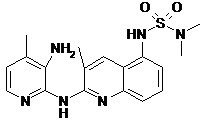
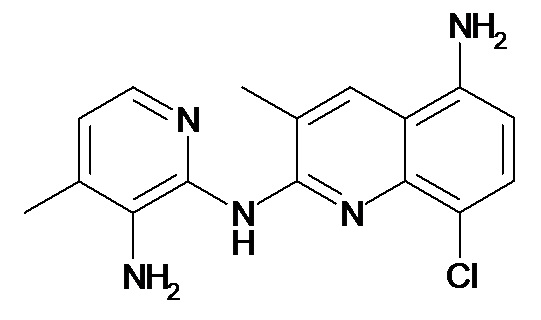
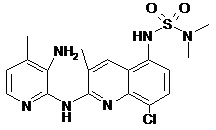
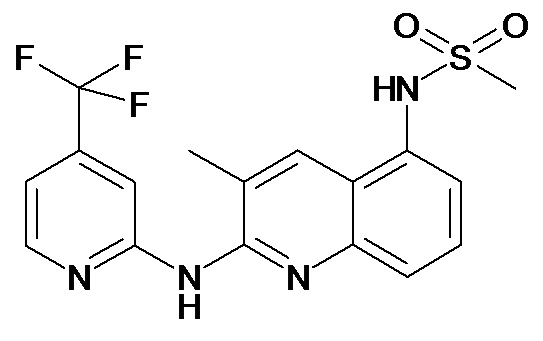
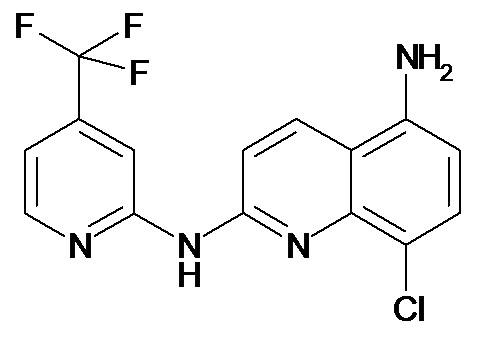
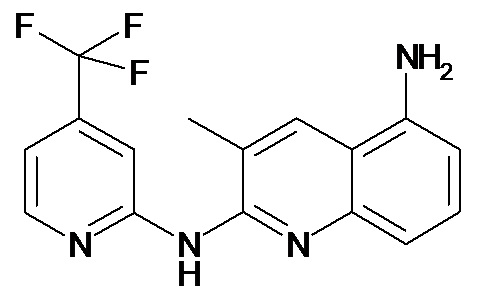
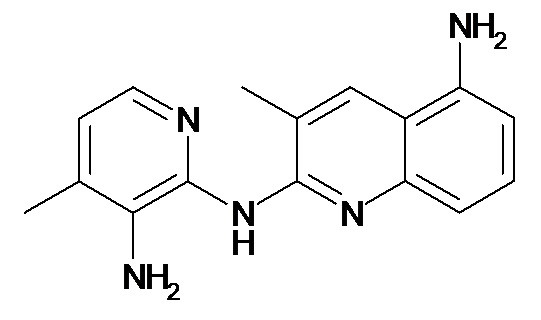
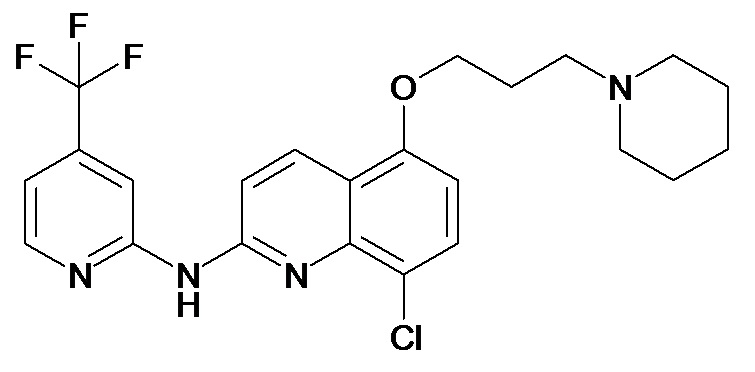
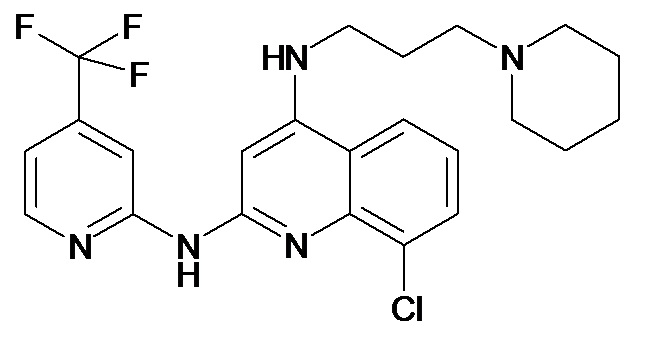
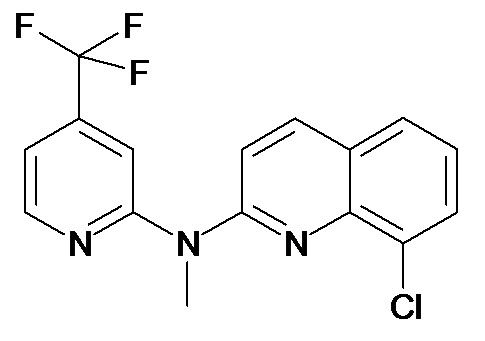
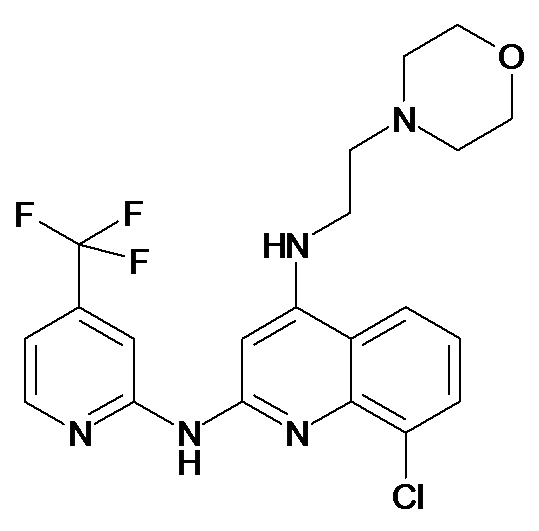
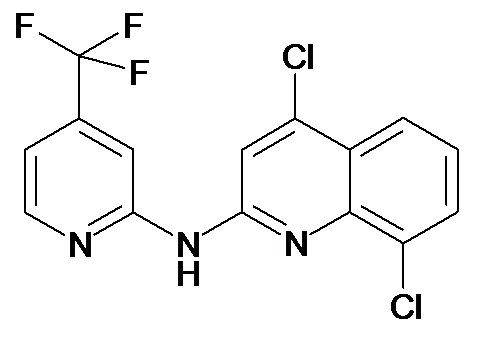
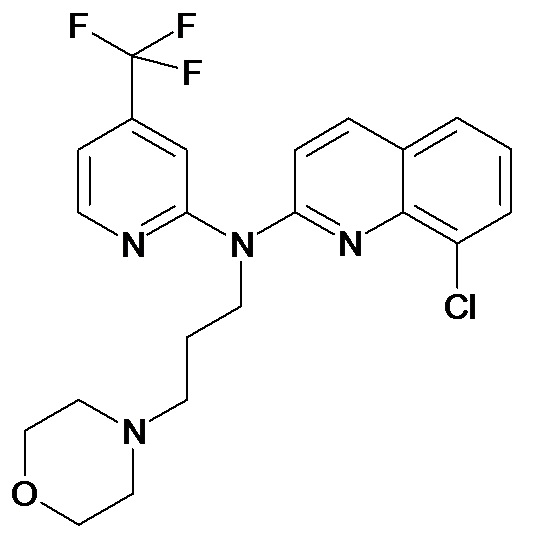
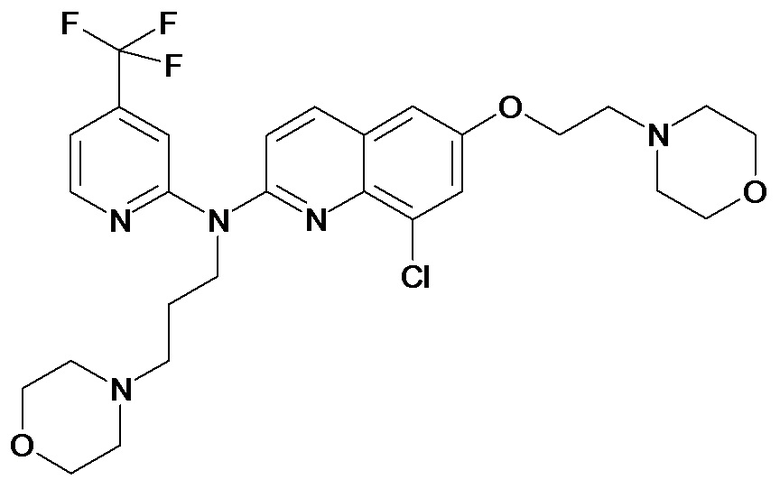
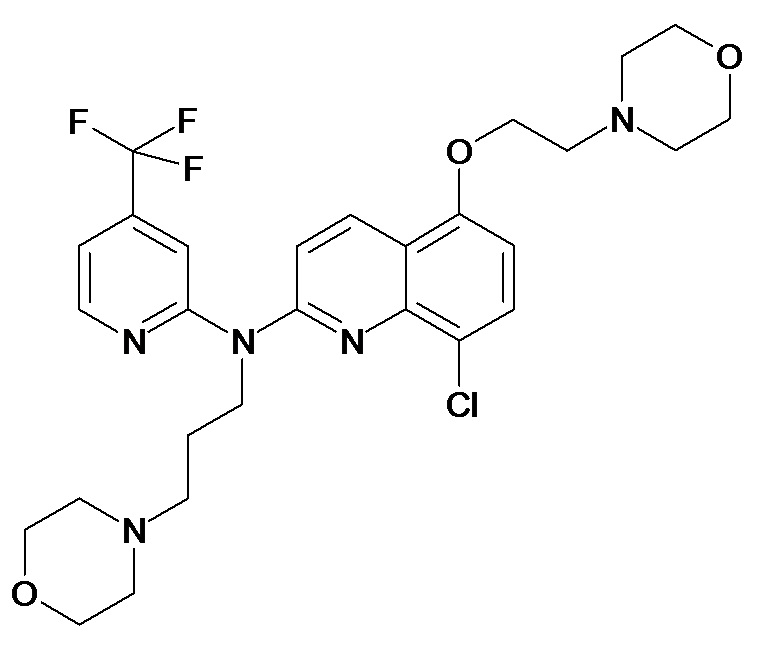
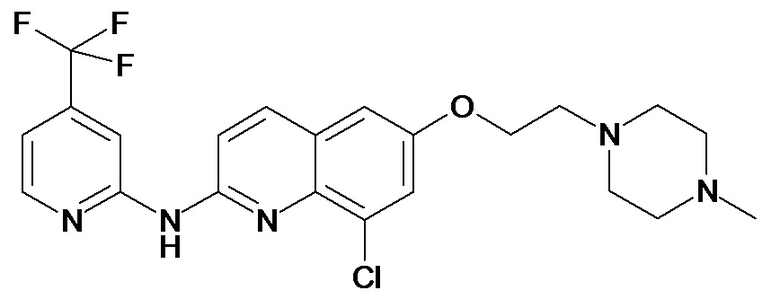
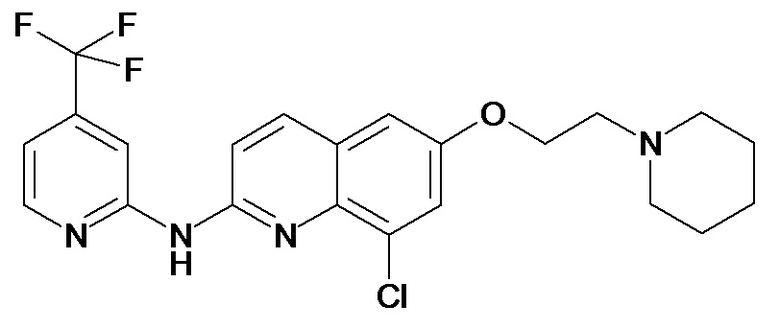
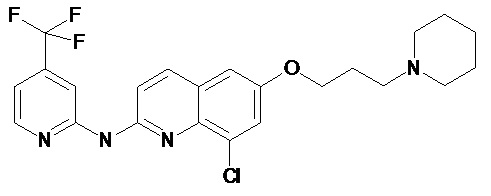
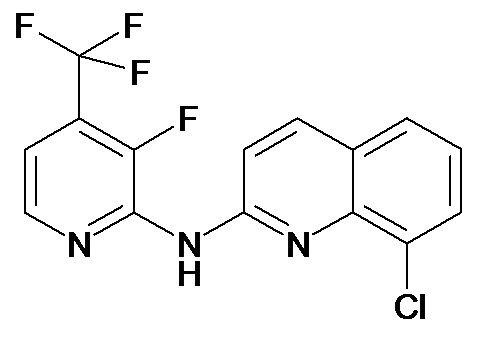
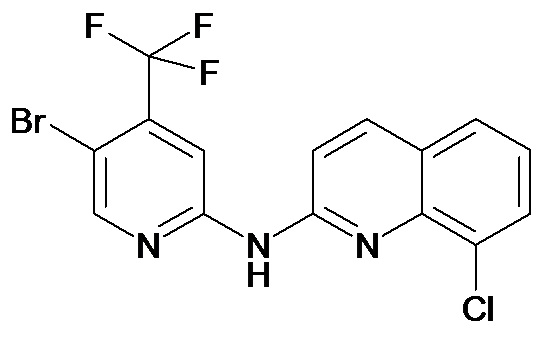
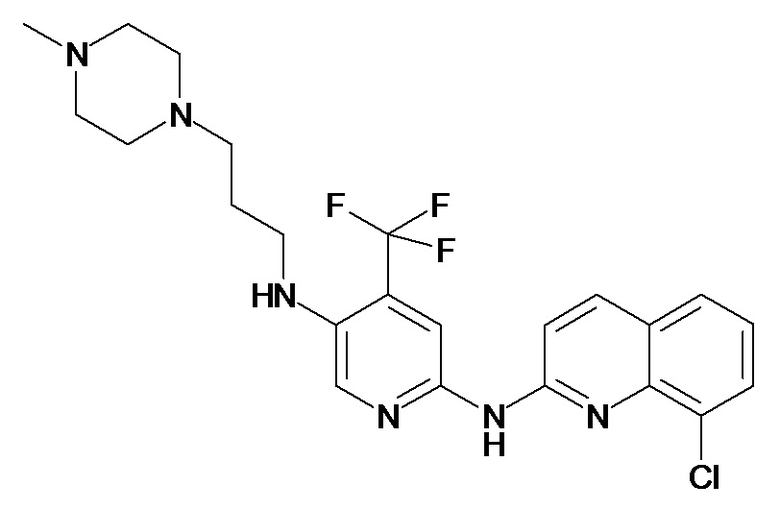
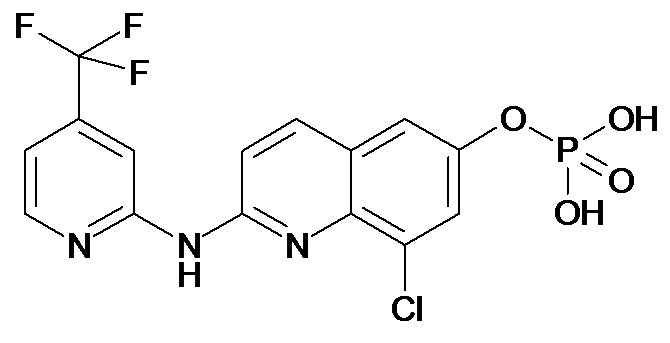
или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления соединение данного изобретения выбрано из Таблицы 2:
Таблица 2 (соединения формулы Ib, определенные выше)
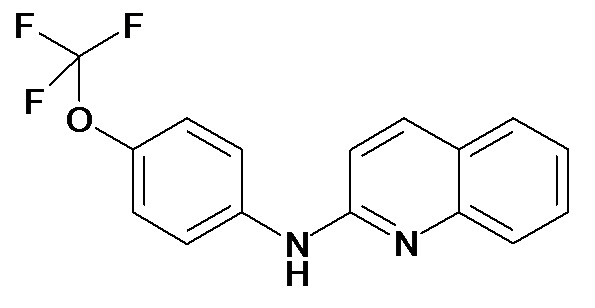
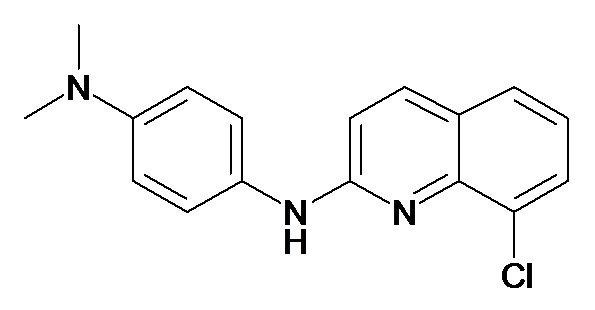
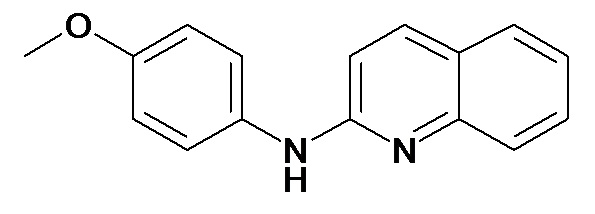
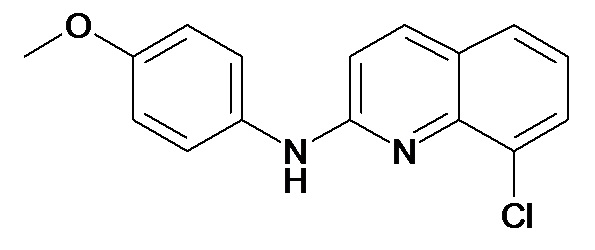
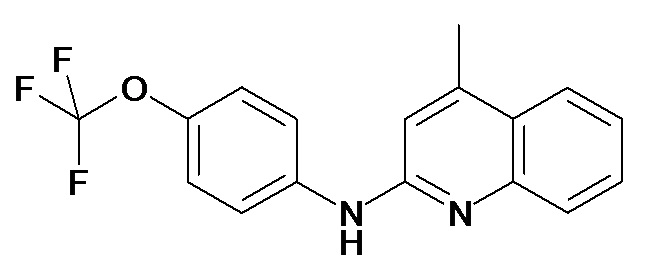
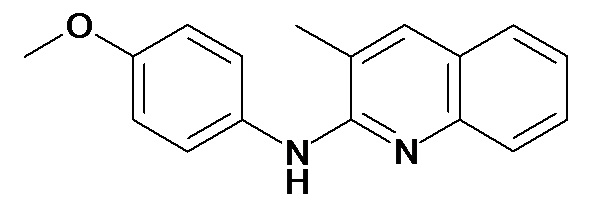
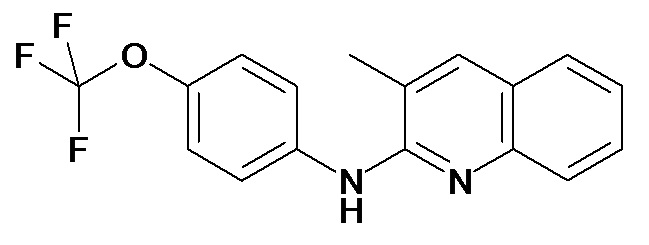
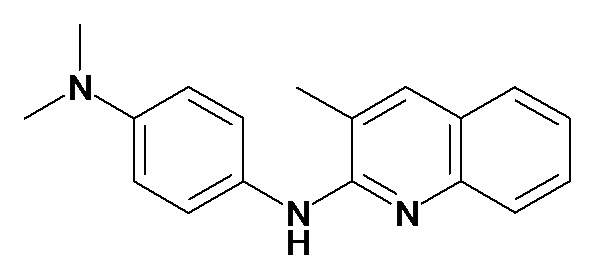
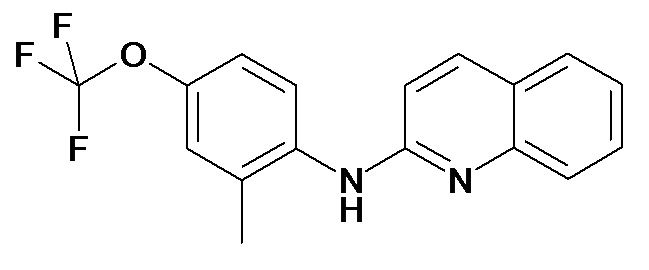
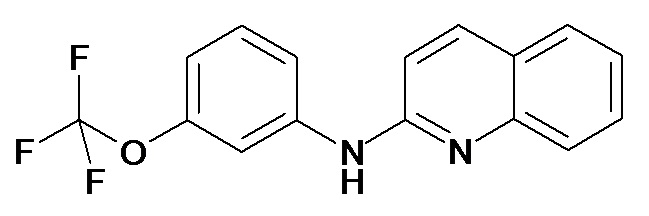
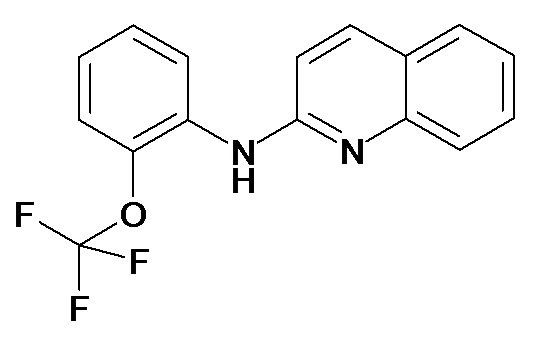
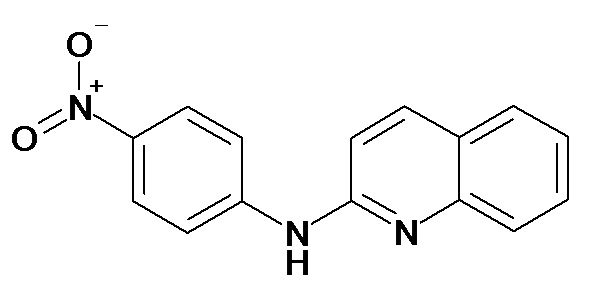
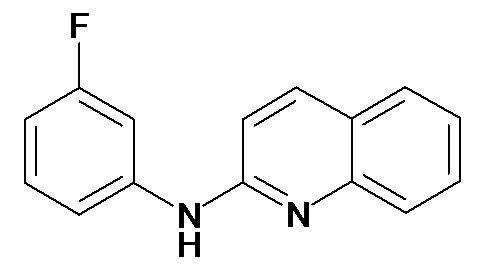
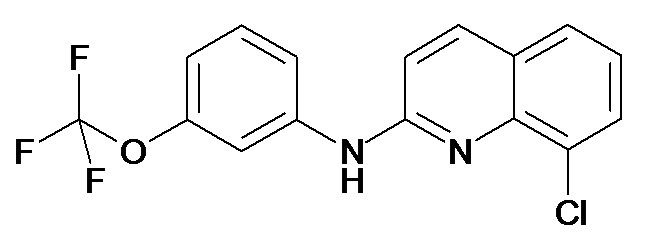
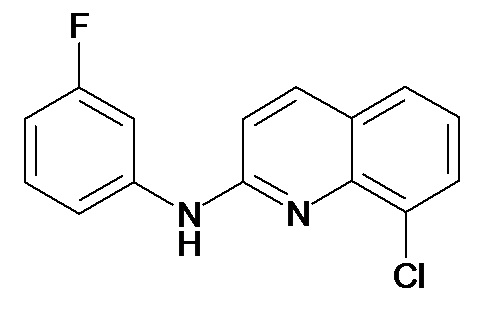
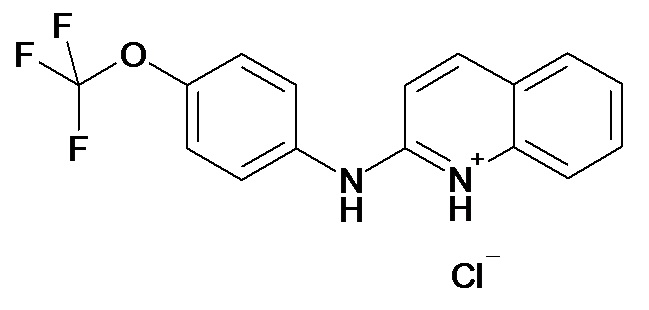
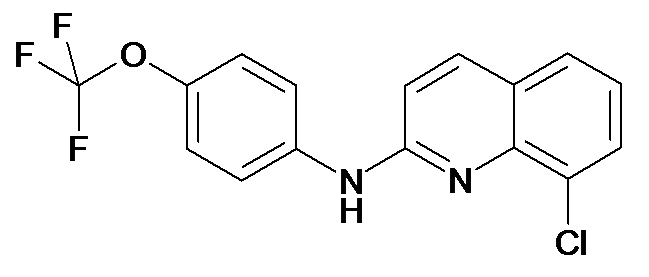
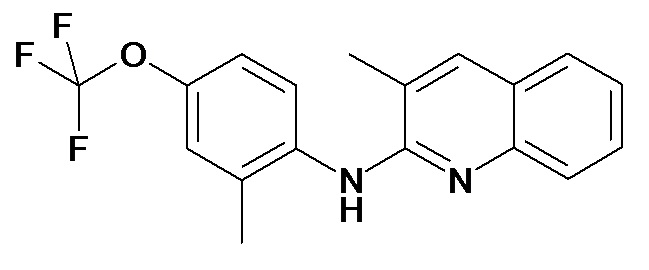
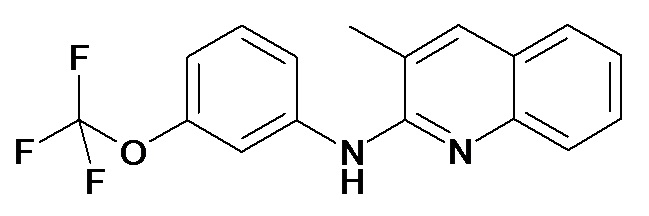
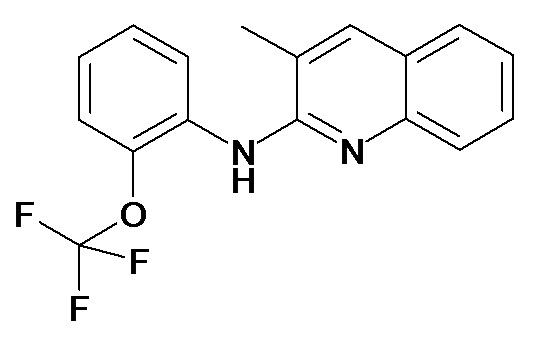
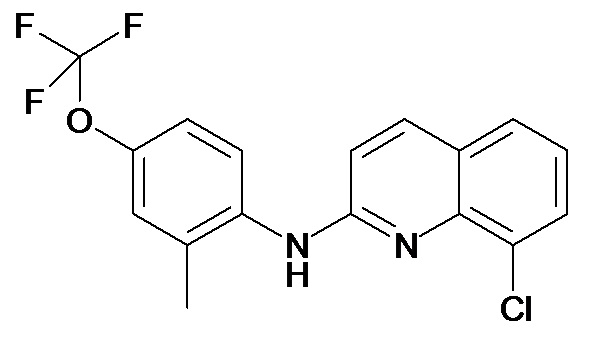
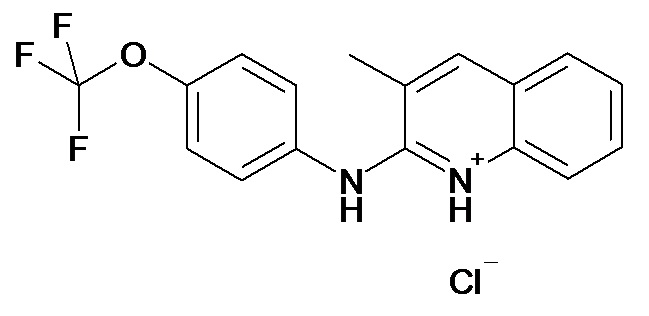
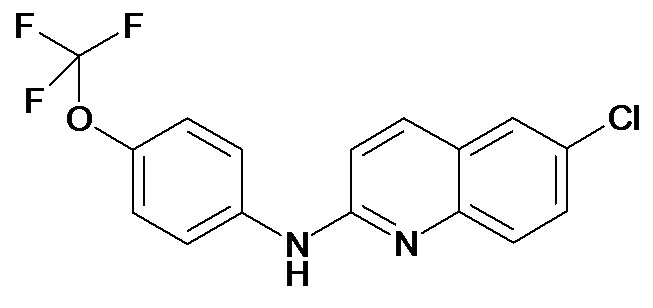
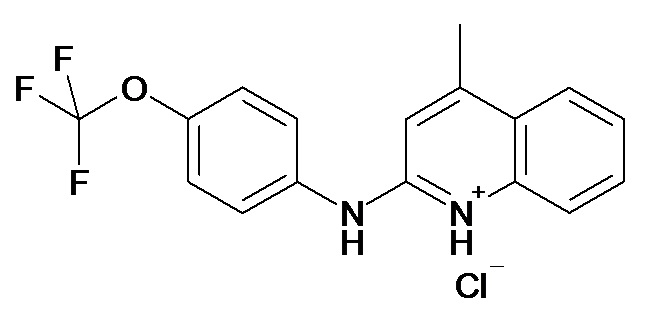
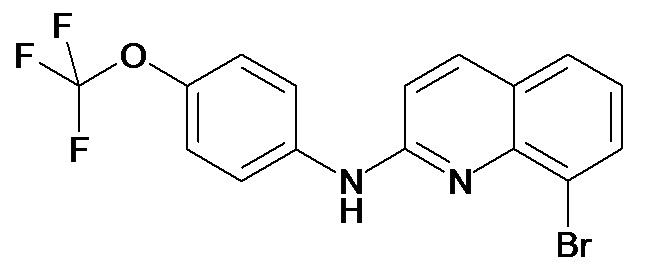
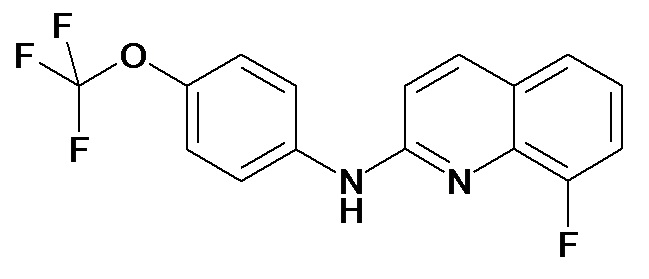
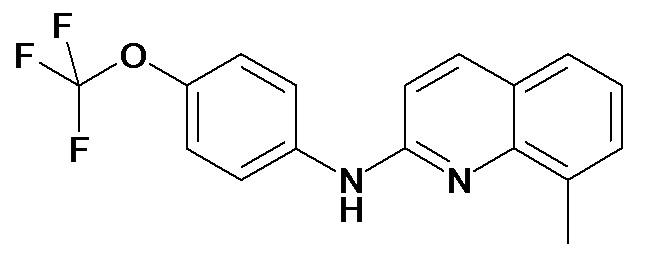
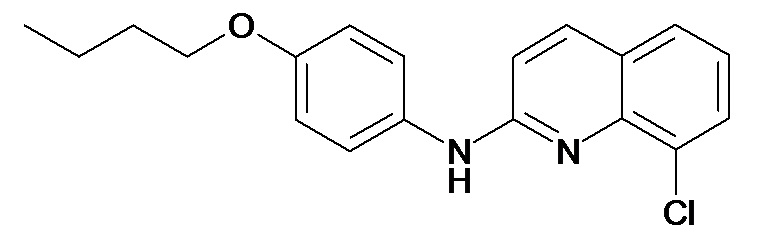
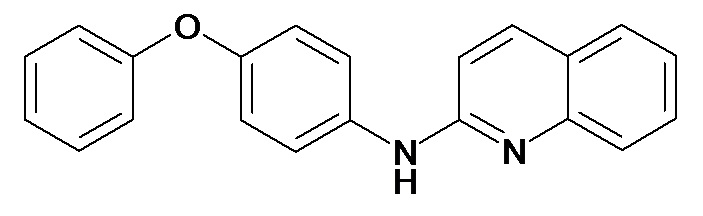
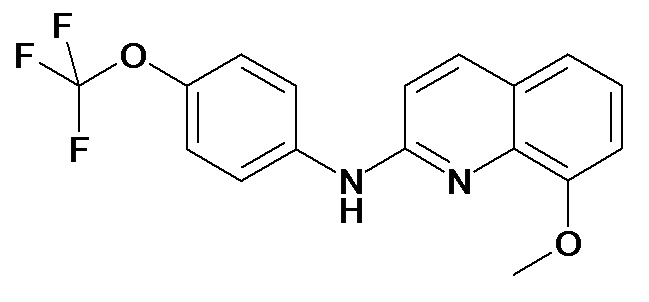
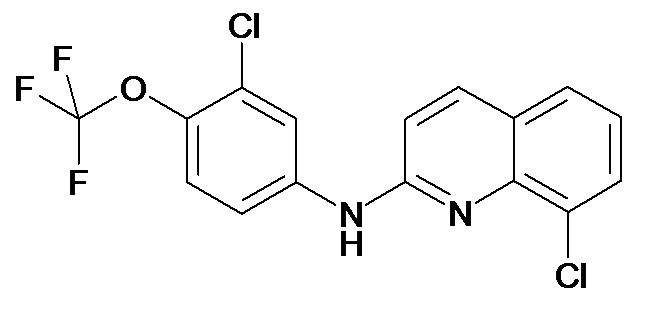
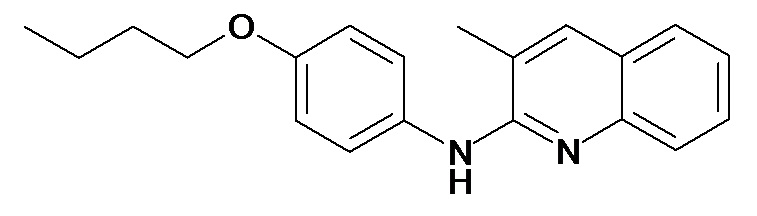
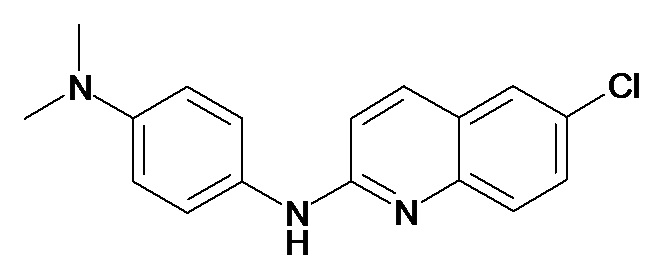
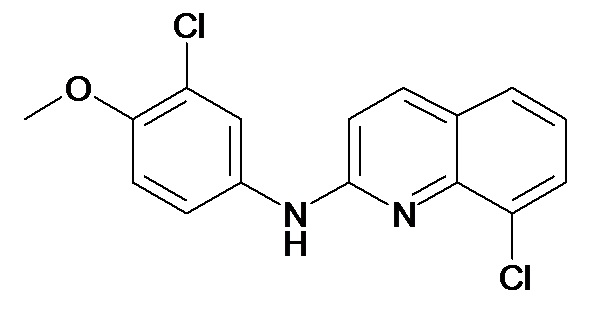
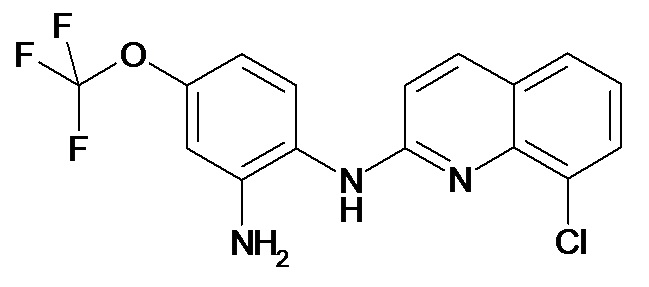
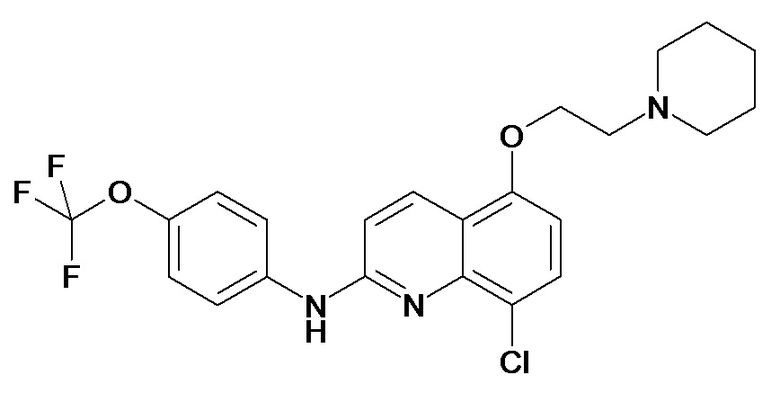
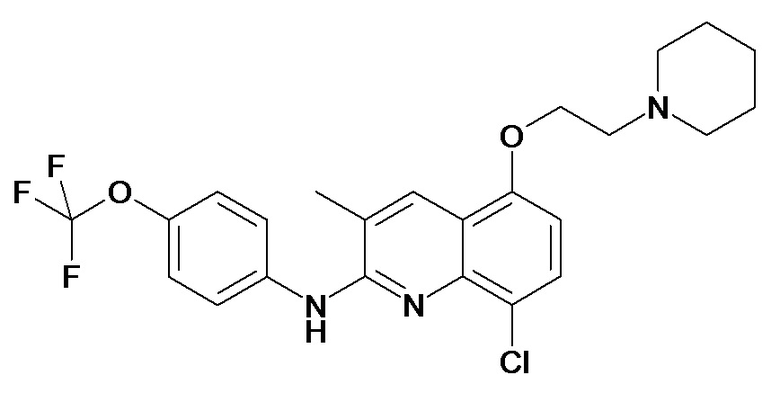
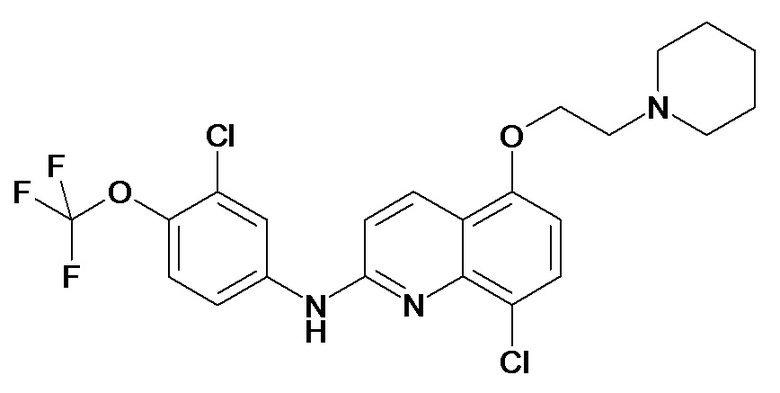
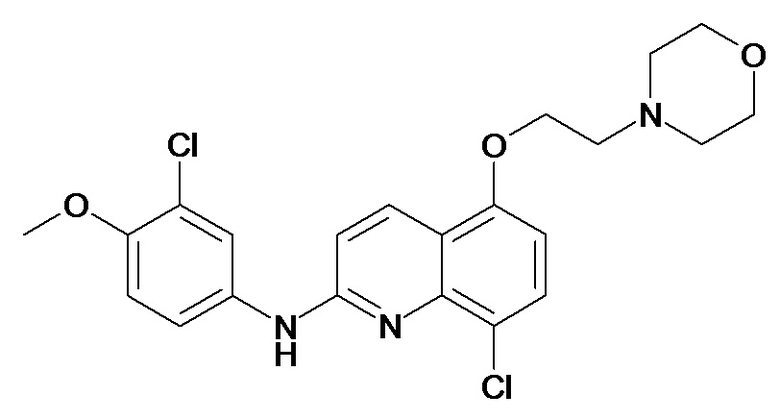
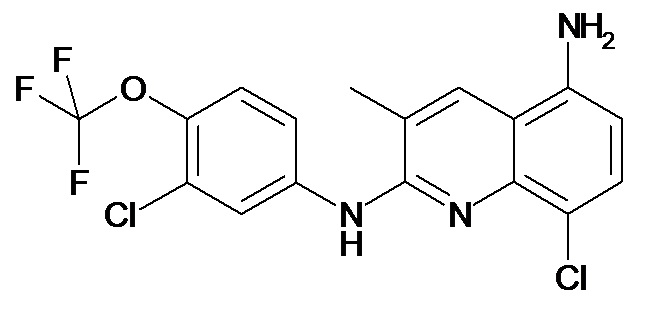
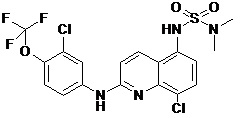
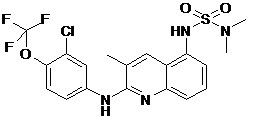
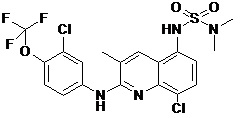
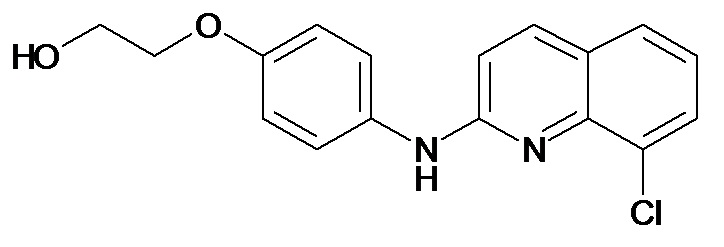
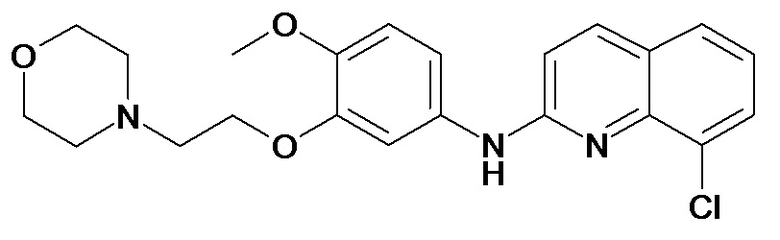
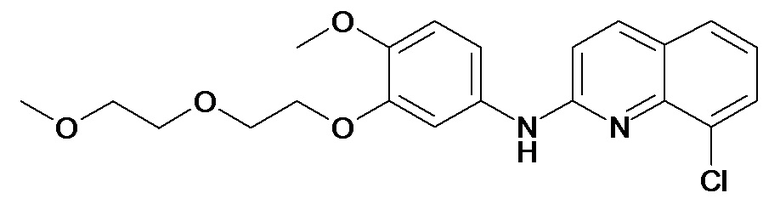
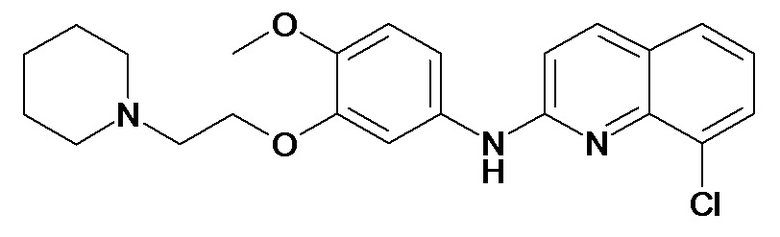
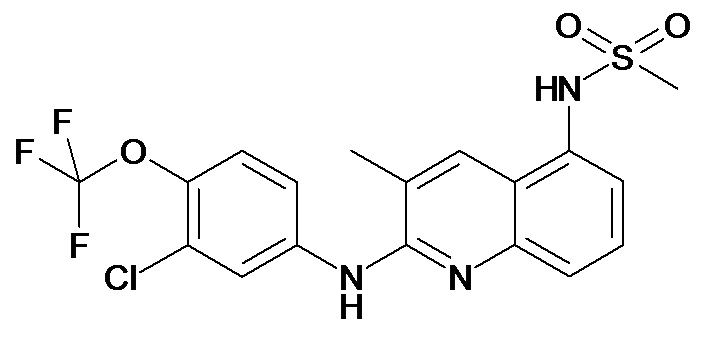
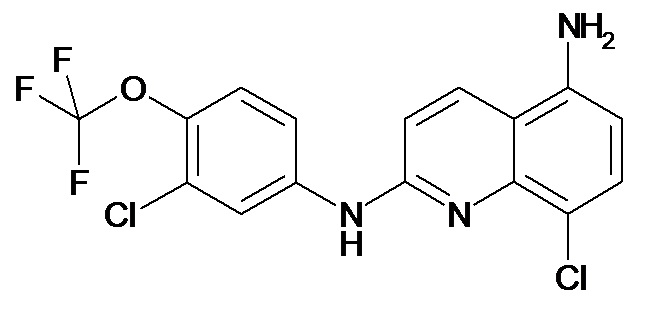
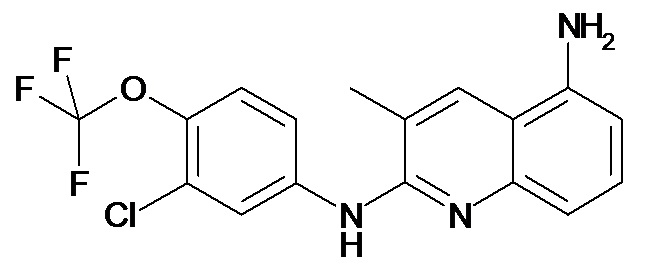
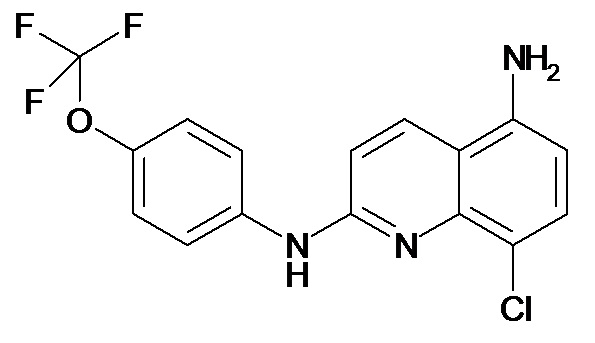
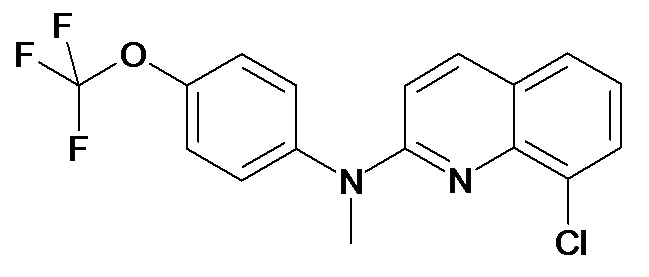
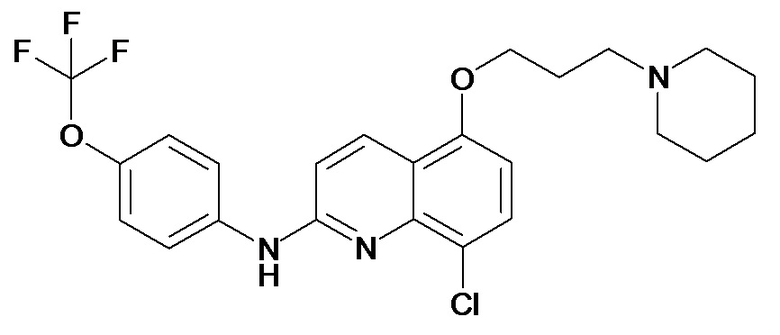
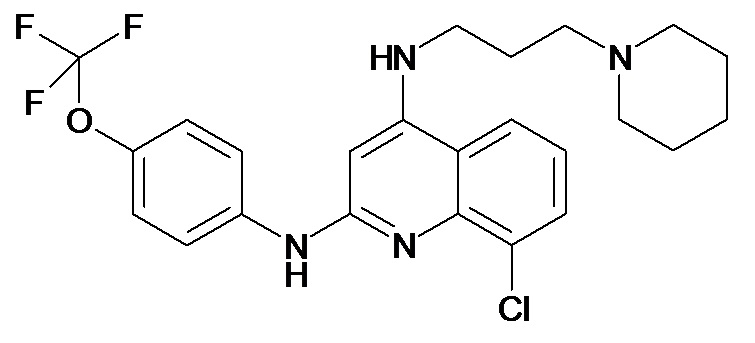
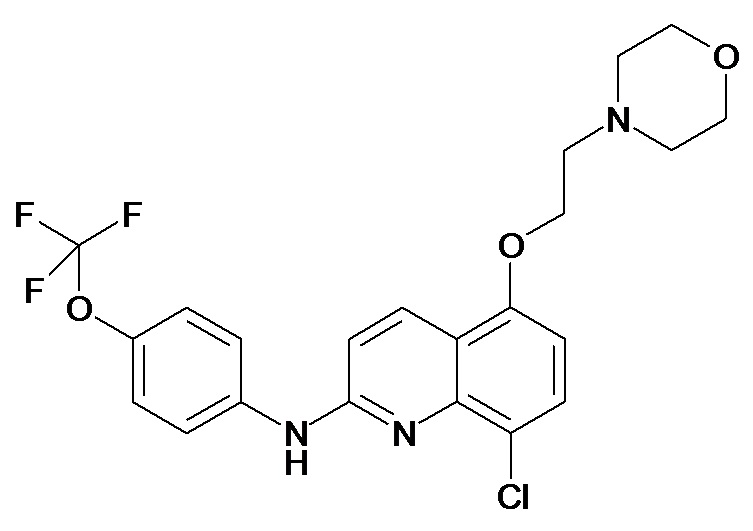
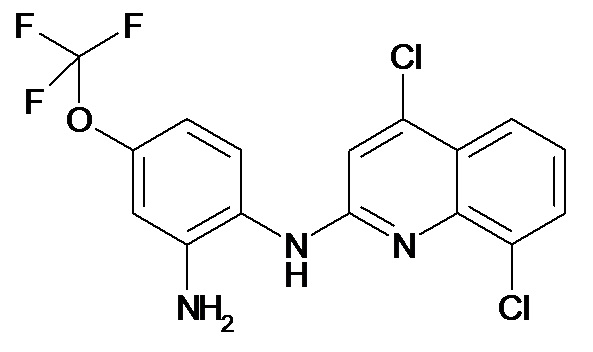
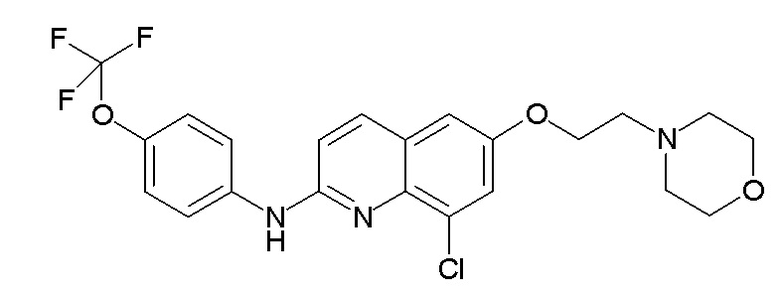
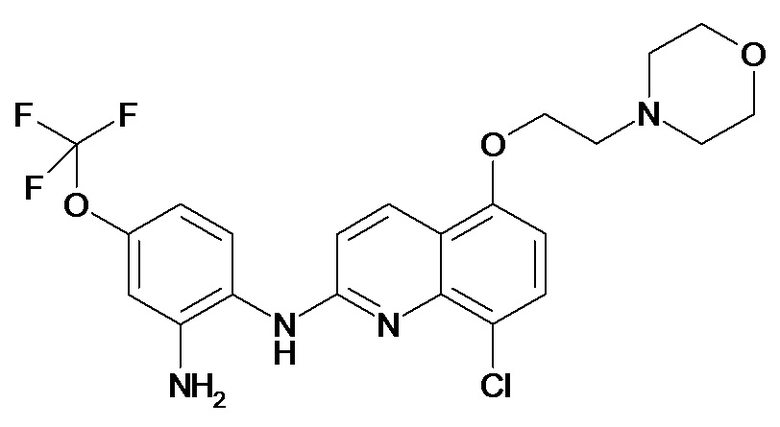
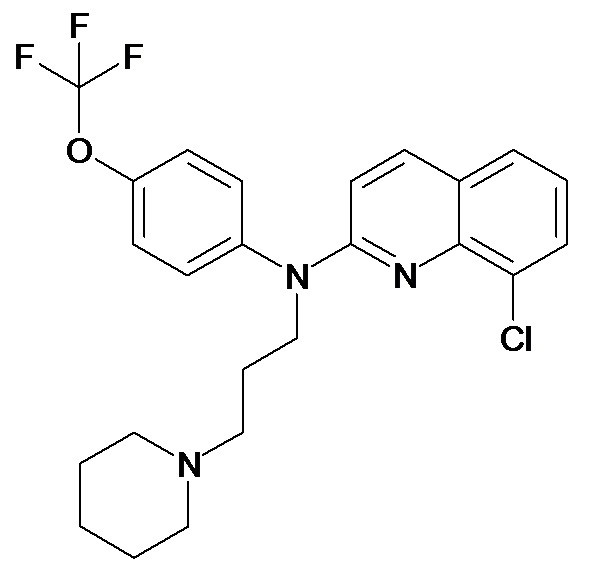
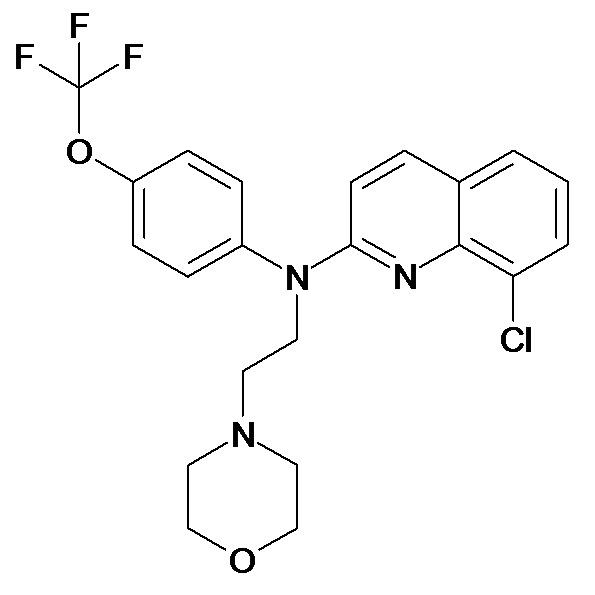

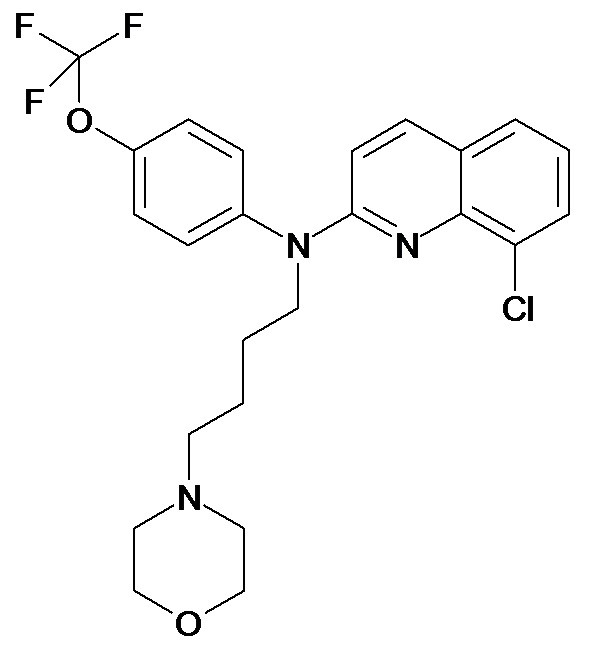
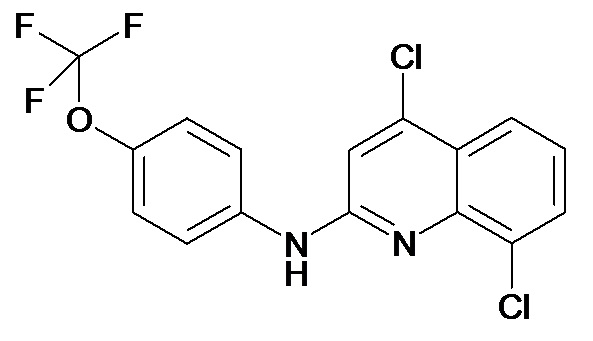
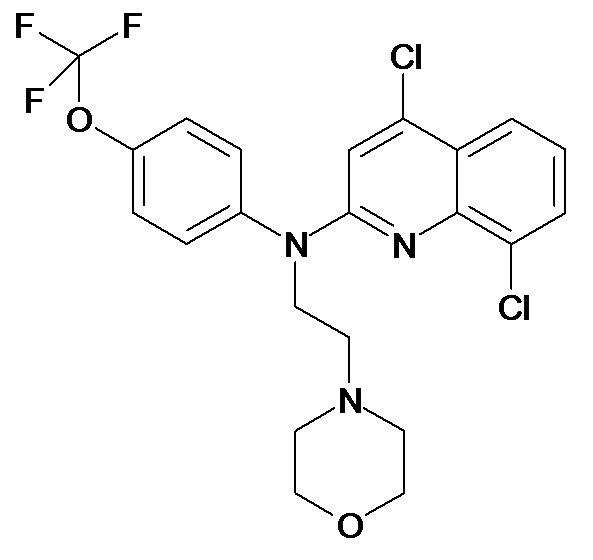
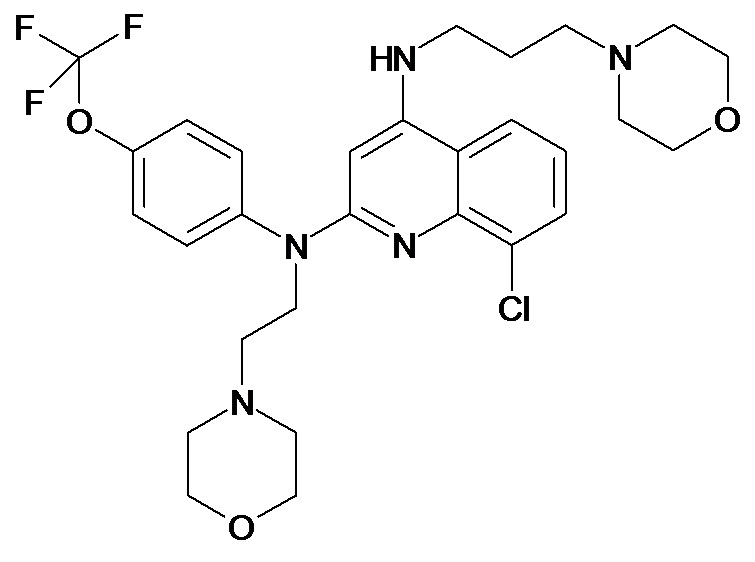
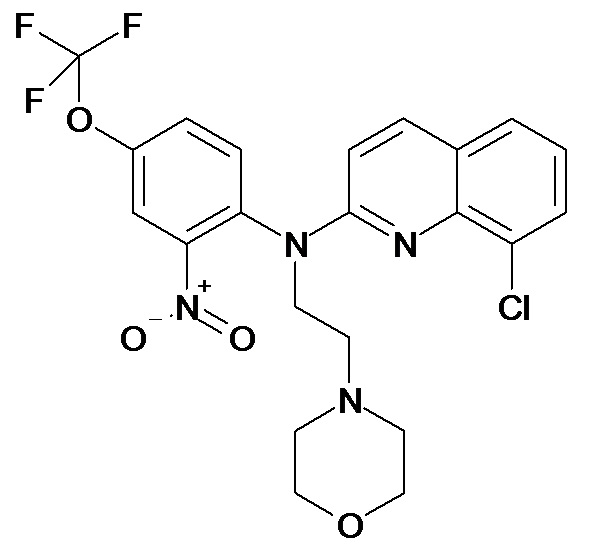
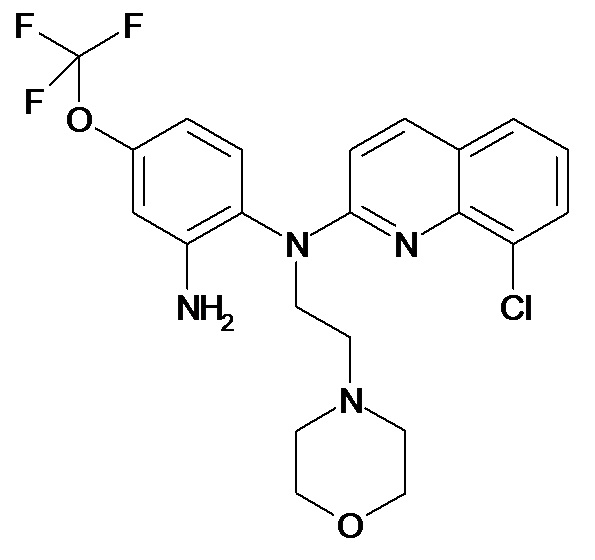
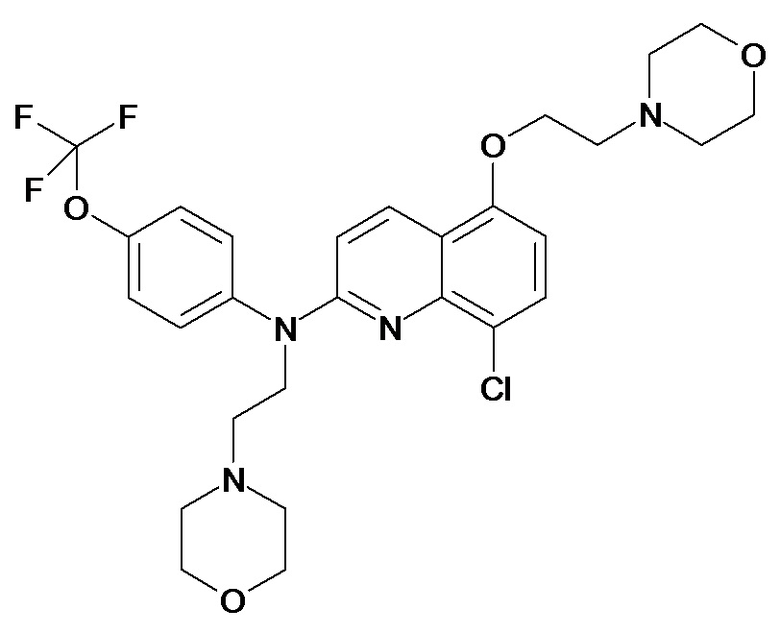
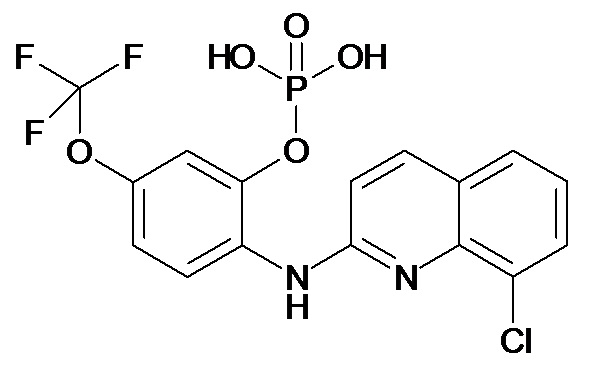
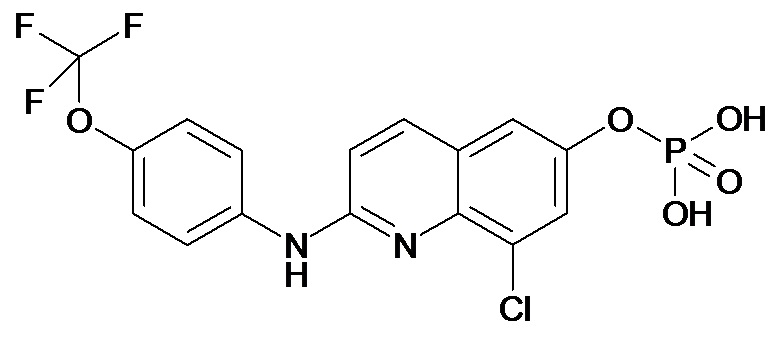
или их фармацевтически приемлемой соли.
В некоторых вариантах осуществления соединение изобретения выбрано из Таблицы 3:
Таблица 3 (Соединения формулы (I), отличные от соединений (Ia) и (Ib))

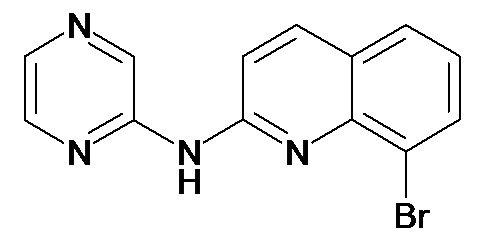
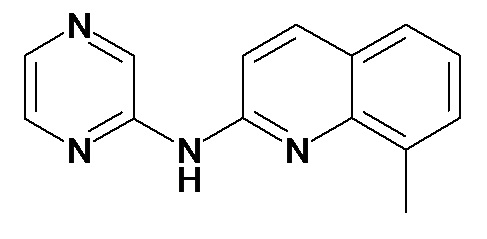
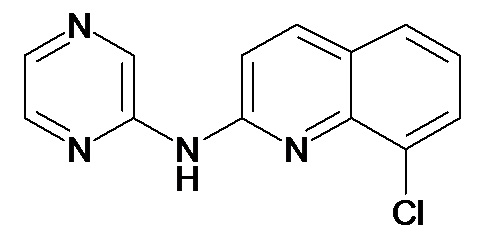
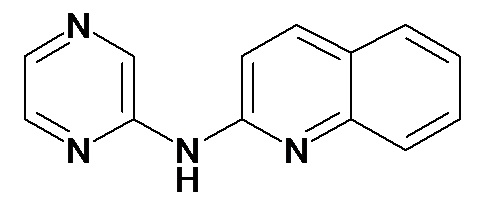
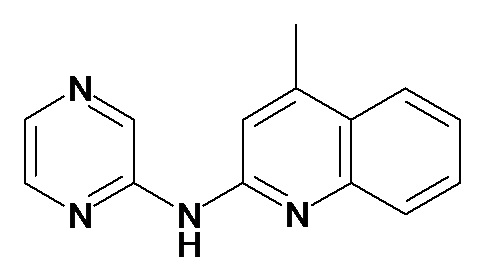
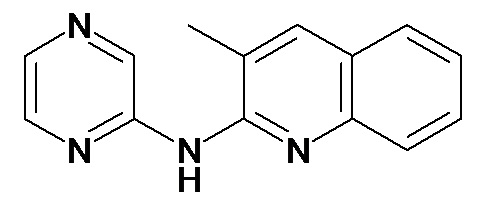
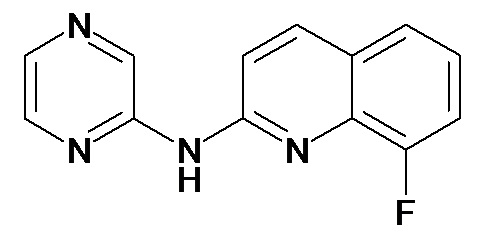
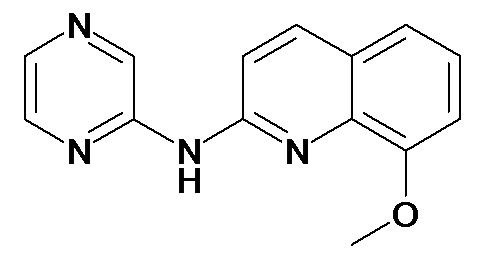
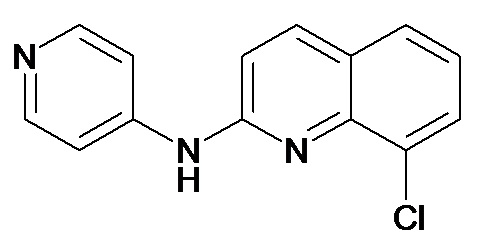
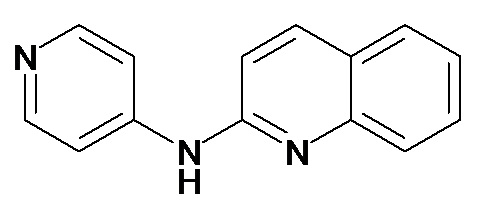
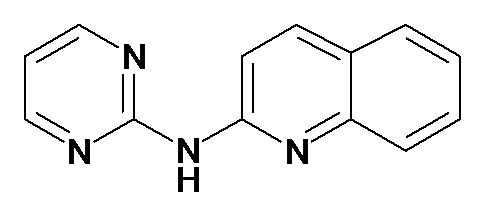
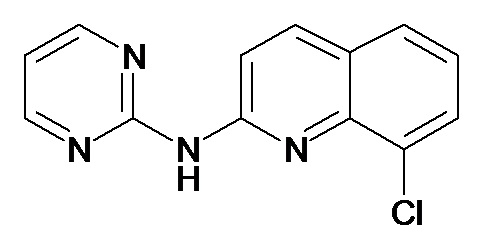
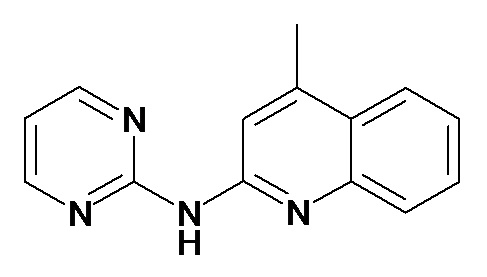
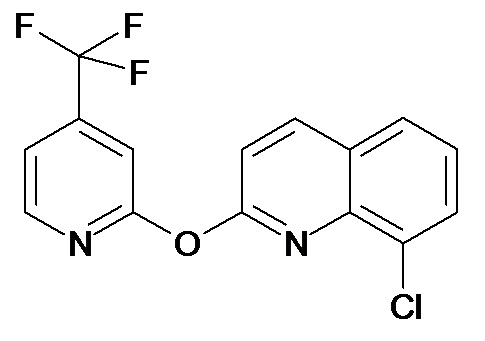
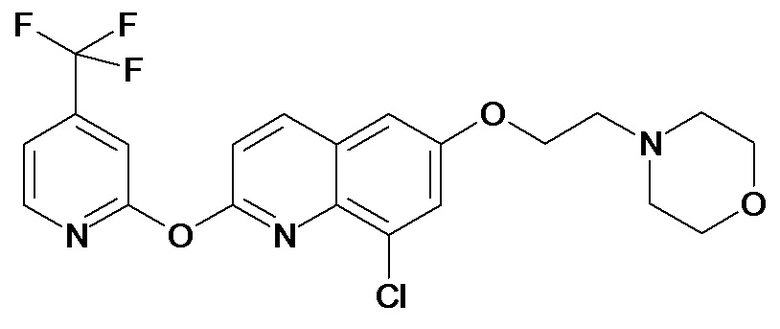
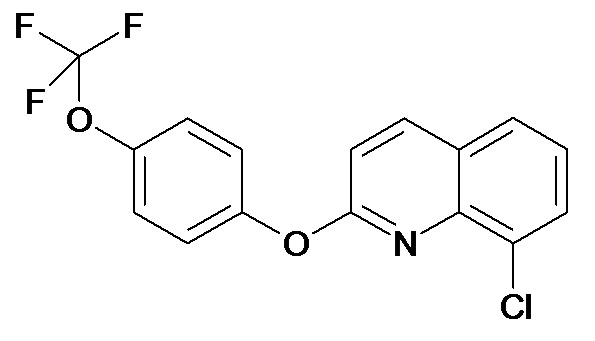
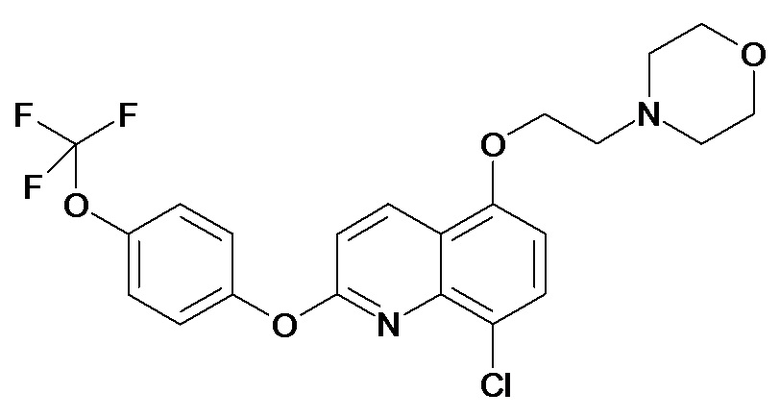
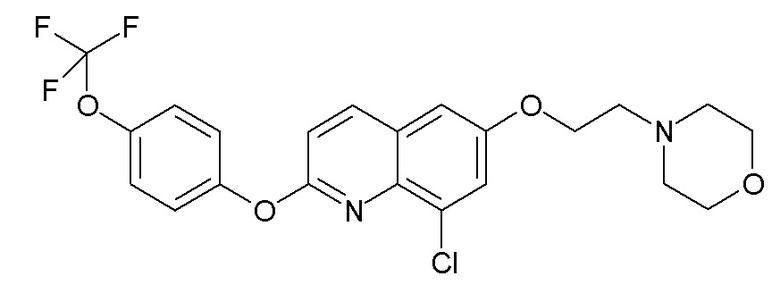
или их фармацевтически приемлемой соли.
Кроме того, настоящее изобретение обеспечивает соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемую соль для применения для лечения и/или предупреждения рака и/или дисплазии
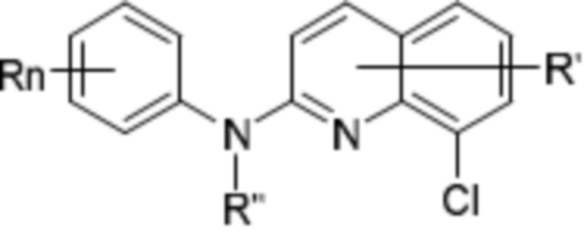
(Ib’),
где:
каждый R независимо представляет собой водород, галоген, -CN, гидроксил, (C1-C3)фторалкил, (C1-C3)фторалкокси, (C3-C6)циклоалкил, -NO2, -NR1R2, (C1-C4)алкокси, фенокси, -NR1-SO2-NR1R2, -NR1-SO2-R1, -NR1-C(=O)-R1, -NR1-C(=O)-NR1R2, -SO2-NR1R2, -SO3H, -O-SO2-OR3, -O-P(=O)(OR3)(OR4), -O-CH2-COOR3, (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой, группу -A-(CH2)m-B-NRaRb (формула IIa) или группу -(O-CH2-CH2)p-O-Ra (формула IIIa),
каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил,
каждый из R3 и R4 независимо представляет собой водород, Li+, Na+, K+, N+(Ra)4 или бензил,
n представляет собой 1, 2 или 3,
каждый R’ независимо представляет собой водород, (C1-C3)алкил, гидроксил, галоген, -NO2, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3) фторалкил, (C1-C4) алкокси, -O-P(=O)(OR3)(OR4), -CN, группу -NH-SO2-N(CH3)2, группу -A-(CH2)m-B-NRaRb (формула IIa) или группу -(O-CH2-CH2)p-O-Ra (формула IIIa),
A представляет собой ковалентную связь, кислородом или NH; B является ковалентной связь или NH;
m представляет собой 1, 2, 3, 4 или 5;
p представляет собой 1, 2 или 3;
каждый из Ra и Rb независимо представляет собой водород, (C1-C5)алкил или (C3-C6)циклоалкил, или
Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, необязательно содержащий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл необязательно замещен одним или несколькими Ra, и
R” представляет собой водород, (C1-C4)алкил или группу A-(CH2)m-B-NRaRb (формула IIa).
Согласно одному аспекту, в настоящем документе представлено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, где:
R независимо представляет собой атом галогена или группу, выбранную из группы (C1-C3)фторалкокси, группы -NR1R2, (C1-C4)алкоксигруппы, группы -O-P(=O)(OR3)(OR4), a (C1-C3)алкильной группы, NO2 группы, группы -A-(CH2)m-B-NRaRb (формула IIa) и группы -(O-CH2-CH2)p-O-Ra Ra (формула IIIa),
n представляет собой 1 или 2,
R’ представляет собой атом водорода, атом галогена или группу, выбранную из группы -NR1R2, группы -O-P(=O)(OR3)(OR4), группы -NH-SO2-N(CH3)2 и группы -A-(CH2)m-B-NRaRb (IIa),
R’ представляет собой атом водорода, алкильную группу (C1-C4) или группу -A-(CH2)m-B-NRaRb (формула IIa),
R1 и R2 независимо представляют собой атом водорода или (C1-C3)алкильную группу,
R3 и R4 независимо представляют собой водород, Li+, Na+, K+, N+(Ra)4 или бензил,
А представляет собой ковалентную связь, атом кислорода или NH,
B представляет собой ковалентную связь,
m представляет собой 2, 3 или 4,
p представляет собой 1, 2 или 3,
Ra и Rb независимо представляют собой атом водорода или алкильную группу (C1-C5),
Ra и Rb могут дополнительно образовывать вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, необязательно содержащий дополнительный гетероатом, выбранный из N, O и S, причем указанный гетероцикл необязательно замещен одним или несколькими Ra.
Согласно дополнительному аспекту, в данном документе представлено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения как определено в настоящем тексте, в котором:
R независимо представляет собой F, Cl, -NH2, -N(CH3)2, -OCH3, -O-(CH2)3-CH3, -OCF3, -CH3, -O-(CH2)2-OH, -O-(CH2)2-O-(CH2)2-OCH3, -NO2 группу, -O-P(=O)(OH)(OH) группу, -O-(CH2)2-морфолиновую группу или -O-(CH2)2-пиперидино группу,
n представляет собой 1 или 2,
R’ представляет атом водорода, Cl, -CH2-CH2-CH3, a -O-(CH2)2-морфолиновую группу, -O-(CH2)2-пиперидино группу, -O-(CH2)3-пиперидино группу, -N-(CH2)3-морфолиновую группу, группу -NH-SO2-N(CH3)2, NH2 или -O-P(=O)(OH)(OH) группу,
R’ представляет собой атом водорода, -CH3, -(CH2)3-пиперидино группу, -(CH2)2-морфолиновую группу, -(CH2)4-морфолиновую группу или -(CH2)2-пирролидино группу.
Согласно дополнительному аспекту, в настоящем документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения как определено в настоящем документе, где:
R представляет собой (C1-C3)фторалкоксильную группу, и
n представляет собой 1,
и R’, и R’’ определены в настоящем тексте.
Согласно дополнительному аспекту, в данном документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения как определено в настоящем документе, где:
R представляет собой (C1-C3)фторалкоксильную группу,
n представляет собой 1,
R’ представляет собой атом водорода, и
R’’ представляет собой атом водорода.
Согласно дополнительному аспекту, в настоящем документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения как определено в настоящем тексте, где:
R’ представляет собой атом водорода.
и R, n и R’ являются такими, как определено в настоящем тексте.
Согласно дополнительному аспекту, в настоящем документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения как определено в настоящем тексте, где указанное соединение выбрано из соединений 96, 98, 108, 109, 111, 115, 122, 125, 128, 129, 130, 132, 133, 135, 138-141, 143 и 145-164.
Согласно дополнительному аспекту, в настоящем документе обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем документе, где указанное соединение представляет собой 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин (соединение 111).
Как показано в экспериментальной части, соединения формулы (Ib’) или любые их метаболиты или их фармацевтически приемлемая соль, как определено в настоящем изобретении, в частности соединение ABX464, эффективны для лечения и/или предупреждения рака, в частности колоректального рака, рака желудка, рака печени, рака легких и/или рака поджелудочной железы (см. значения IC50), в частности у пациентов в предраковом состоянии, с раком на ранней стадии или неметастатическим раком. Согласно одному варианту осуществления соединения формулы (Ib’) или любой их метаболит или их фармацевтически приемлемая соль, подходящая для настоящего изобретения, не нацелены непосредственно на метатстатическую инвазию.
Кроме того, из результатов, раскрытых в экспериментальной части, следует, что соединения формулы (Ib’) или любой их метаболит или фармацевтически приемлемая соль неожиданно более эффективны для лечения и/или предупреждения рака, в частности у пациентов, имеющих предраковое состояние, рак на ранней стадии или неметастатический рак, чем сравниваемое соединение 26, которое относится к формуле (Ia), как определено в настоящем тексте и в WO 2010/143168.
Более того, в WO 2010/143168 соединение 26 соответствует соединению 37. И в WO 2010/143168 было продемонстрировано, что указанное соединение обладает антиинвазивным эффектом, предсказывающим его активность против рака. Следовательно, было неожиданно, что соединение 26, как оно определено в настоящем тексте, менее эффективно, чем соединения формулы (Ib’). Эти результаты также демонстрируют, что соединение, обладающее антиинвазивными свойствами, необязательно обладает столь же эффективной активностью против предракового состояния, рака на ранней стадии или неметастатического рака.
В некоторых вариантах осуществления описанное в настоящем документе соединение находится в форме соли, выбранной из сульфата, гидробромида, цитрата, трифторацетата, аскорбата, гидрохлорида, тартрата, трифлата, малеата, мезилата, формиата, ацетата, фумарата и сульфоната. В некоторых вариантах осуществления описанное в настоящем описании соединение находится в солевой форме в виде алкилсуфоната или арилсульфоната. В некоторых вариантах осуществления описанное в настоящем описании соединение находится в форме соли в виде мезилата, трифлата, эдизилата, безилата и тозилата.
В одном аспекте настоящее изобретение обеспечивает метаболит соединения, описанного в настоящем описании. В некоторых вариантах осуществления настоящее изобретение обеспечивает N-глюкуронидный метаболит соединения, описанного в настоящем описании.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (IV):
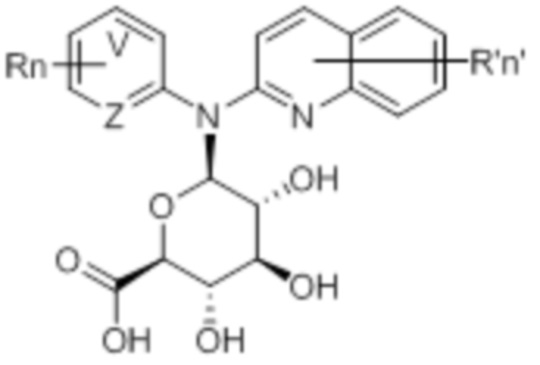 (IV)
(IV)
или его фармацевтически приемлемую соль, где каждая из переменных V, Z, R, R’, n и n’ является такой, как определено выше и описана в вариантах осуществления в настоящем описании, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение данного изобретения представляет собой соединение формулы (IVa):
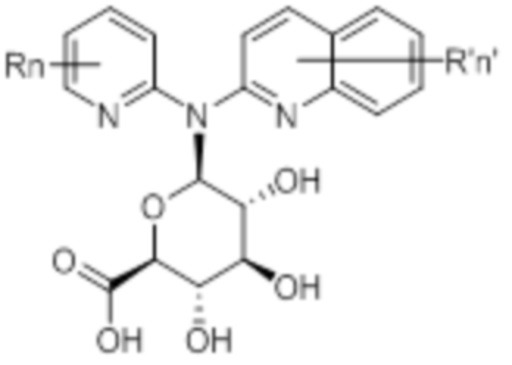 (IVa)
(IVa)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, n и n’ независимо является такой, как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (IVb):
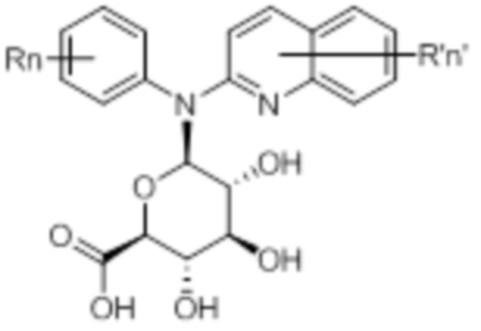 (IVb)
(IVb)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, n и n’ независимо является такой, как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (IVc):
 (IVc)
(IVc)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, n и n’ независимо является такрой, как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (IVb’):
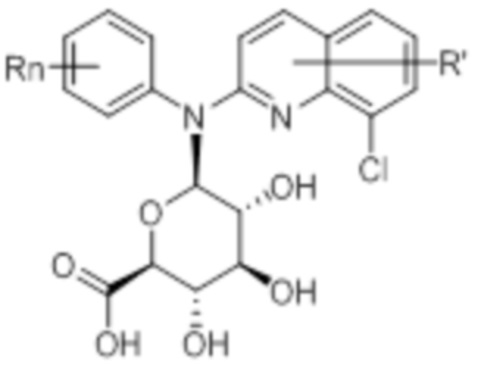 (IVb’)
(IVb’)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’ и n независимо является такой, как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
Таким образом, настоящее изобретение, кроме того, обеспечивает соединение формулы (IVb’) или его фармацевтически приемлемую соль для применения для лечения и/или предупреждения рака и/или дисплазии. Согласно одному варианту осуществления, указанные соединения формулы (IVb’) или их фармацевтически приемлемая соль не нацелены непосредственно на метастатическую инвазию.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы (IVd):
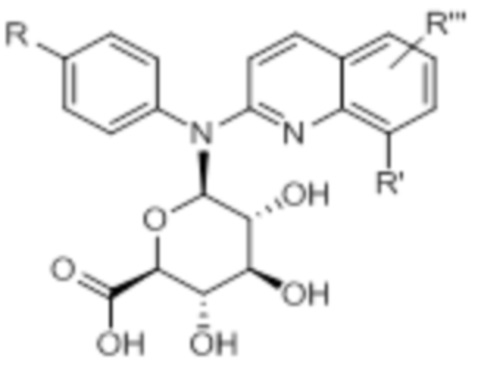 (IVd)
(IVd)
или его фармацевтически приемлемую соль, где каждая из переменных R, R’, R’” независима как определено выше и описано в вариантах осуществления в настоящем документе, как отдельно, так и в комбинации.
В некоторых вариантах осуществления настоящее изобретение предоставляет способ лечения воспалительного заболевания, расстройства или состояния, включающий введение нуждающемуся в этом пациенту соединения любой из формул (IV), (IVa), (IVb), (IVc), (IVb’) и (IVd)или его фармацевтически приемлемой соли.
В некоторых вариантах осуществления соединение изобретения представляет собой соединение формулы:
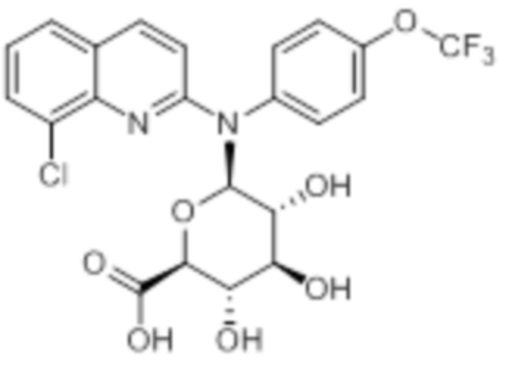
или их фармацевтически приемлемую соль.
Таким образом, согласно дополнительному аспекту, в настоящем документе предоставлено соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, где указанное соединение имеет следующую формулу:
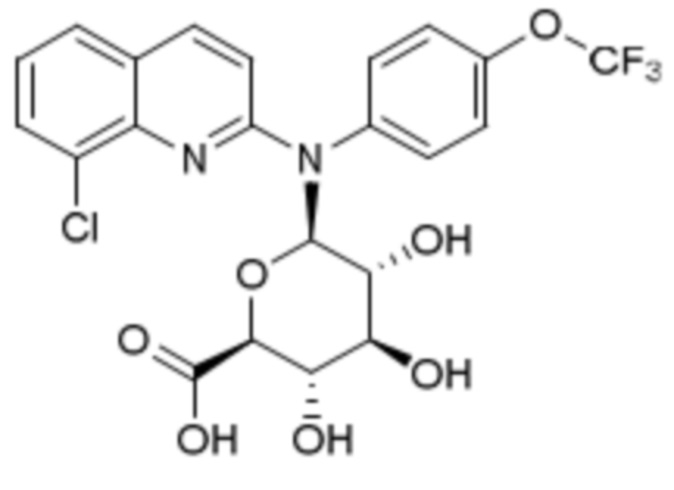 .
.
Соединения согласно настоящему изобретения могут существовать в форме свободных оснований или солей присоединения с фармацевтически приемлемыми кислотами. Подходящие физиологически приемлемые соли присоединения кислот соединений настоящего изобретения включают сульфат, гидробромид, цитрат, трифторацетат, аскорбат, гидрохлорид, трифлат, тартрат, малеат, формиат, ацетат, фумарат и сульфонат, в частности алкилсуфонат или арилсульфонат, и более конкретно мезилат, трифлат, эдизилат, безилат и тозилат.
Соединения настоящего изобретения и/или их соли могут образовывать сольваты или гидраты, и данное изобретение включает все подобные сольваты и гидраты. Термины "гидраты" и "сольваты" буквально означают, что соединения согласно данному изобретению могут быть в форме гидрата или сольвата, т.е. связаны или ассоциированы с одной или более молекулами воды или растворителя. Это только химическая характеристика подобных соединений, которая может быть применена ко всем органическим соединениям указанного типа.
Соединения настоящего изобретения могут содержать один или более асимметричных атомов углерода. Таким образом, они могут существовать в форме энантиомеров или диастереоизомеров. Эти энантиомеры, диастереоизомеры и их смеси, включая рацемические смеси, охватываются рамками настоящего изобретения.
В контексте настоящего изобретения термин:
- “галоген” понимается как хлор, фтор, бром или йод и, в частности, термин обозначает хлор, фтор или бром,
- “(C1-C5)алкил”, используемый в настоящем документе, соответственно, относится к нормальному, вторичному или третичному насыщенному углеводороду C1-C5. Примерами являются без ограничений метил, этил, 1-пропил, 2-пропил, бутил, пентил,
- “(C3-C6)циклоалкил”, используемый в настоящем документе, соответственно, относится к циклическому насыщенному углеводороду. Примерами являются, но не ограничиваются циклопропил, циклобутил, циклопентил, циклогексил,
- “(C1-C4)алкокси”, используемый в настоящем документе, соответственно, относится к O-(C1-C4)алкильной части, где алкил является тем, что определен выше. Примерами являются без ограничений, метокси, этокси, 1-пропокси, 2-пропокси, бутокси,
- “фторалкильная группа” и “фторалкоксильная группа” относятся, соответственно, к алкильной группе и алкоксигруппе как определено выше, причем указанные группы замещены по меньшей мере одним атомом фтора. Примерами являются перфторалкильные группы, такие как трифторметильная или перфторпропильная,
- “насыщенный 5- или 6-членный гетероцикл”, используемый в настоящем документе, соответственно, относится к насыщенному циклу, содержащему по меньшей мере один гетероатом. Примерами являются, но не ограничиваются ими, морфолин, пиперазин, тиоморфолин, пиперидин, пирролидин.
Используемый в настоящем документе термин “фармацевтически приемлемая соль” относится к тем солям, которые, в рамках тщательной медицинской оценки, подходят для применения в контакте с тканями человека и низших животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного и соизмеримы с разумным соотношением пользы/риска. Фармацевтически приемлемые соли хорошо известны в данной области. Например, S.M. Berge et al. подробно описывают фармацевтически приемлемые соли в J. Pharmaceutical Sciences, 1977, 66, 1-19, включенные в настоящем описании по ссылке
Фармацевтически приемлемые соли соединений настоящего изобретения включают соли, полученные из подходящих неорганических и органических кислот и оснований. Примерами фармацевтически приемлемых нетоксичных солей присоединения кислот являются соли аминогруппы, образованные неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и хлорная кислота, или органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с использованием других методов, используемых в данной области техники, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурилсульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, p-толуолсульфонат, ундеканоат, валератные соли и тому подобное.
Соли, полученные из соответствующих оснований, включают соли щелочных металлов, щелочноземельных металлов, аммонийные и соли N+(C1-4alkyl)4. Типичные соли щелочных или щелочноземельных металлов включают натрий, литий, калий, кальций, магний и подобные. Дополнительные фармацевтически приемлемые соли включают, при необходимости, нетоксичные катионы аммония, четвертичного аммония и аминные катионы, образованные с использованием противоионов, таких как галид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
Если не указано иное, структуры, изображенные в настоящем описании, также должны включать все изомерные (например, энантиомерные, диастереомерные и геометрические (или конформационные)) формы структуры; например, конфигурации R и S для каждого асимметричного центра, изомеры с двойной связью Z и E, а также конформационные изомеры Z и E. Поэтому отдельные стереохимические изомеры, так же как и энантиомерные, диастереомерные и геометрические (или конформационные) смеси настоящих соединений, входят в сферу применения изобретения. Если не указано иное, все таутомерные формы соединений данного изобретения входят в сферу действия изобретения. Кроме того, если не указано иное, структуры, изображенные в настоящем описании, также предназначены для включения соединений, которые отличаются только наличием одного или более обогащенных изотопами атомов. Например, соединения, имеющие настоящие структуры, включая замену водорода дейтерием или тритием, или замену углерода на 13C- или 14C-обогащенный углерод, входят в сферу действия настоящего изобретения. Такие соединения эффективны, например, в качестве аналитических инструментов, в качестве зондов в биологических анализах или в качестве терапевтических агентов согласно настоящему изобретению.
Формы рака
Соединение или любой из его метаболитов или их фармацевтически приемлемые соли, как определено выше, могут быть эффективны в лечении или предупреждении различных видов рака.
Используемый в настоящем документе термин “рак (раковое заболевание)”, и если не указано иное, то может относиться к любому нарушению, связанному с аномальным клеточным ростом, которое, таким образом, включает злокачественные опухоли и доброкачественные опухоли, метастатические опухоли и неметастатические опухоли, солидные опухоли и несолидные опухоли, такие как раки крови, которые, таким образом, могут включать лейкоз, лимфому и миелому; оно также может относиться к ракам центральной нервной системы (ЦНС) и ракам, не затрагивающим ЦНС. Если не указано иное, термин “рак (раковое заболевание)” также охватывает ювенильные и неювенильные виды рака, рецидивирующие и нерецидивирующие виды рака, а также рецидивы рака.
Когда рассматриваемый рак является раком крови, он может быть выбран из: мелкоклеточной лимфоцитарной лимфомы, неходжкинской лимфомы, индолентной неходжкинской лимфомы (iNHL - indolent non-Hodgkin's lymphoma), рефрактерной iNHL, мантийноклеточной лимфомы, фолликулярной лимфомы, лимфоплазмоцитарной лимфомы, лимфомы маргинальной зоны, иммунобластной крупноклеточной лимфомы, лимфобластной лимфомы, В-клеточной лимфомы маргинальной зоны селезенки (+/- моноцитоидных B клеток), лимфомы узловой маргинальной зоны (+/- моноцитоидных В-клеток), экстранодальной В-клеточной лимфомы маргинальной зоны MALT (лимфоидная ткань слизистых оболочек), кожной Т-клеточной лимфомы, экстранодальной Т-клеточной лимфомы, анапластической крупноклеточной лимфомы, ангиоиммунобластной Т-клеточной лимфомы, грибовидной гранулёмы, В-клеточной лимфомы, диффузной B-крупноклеточной лимфомы, средостенной B-крупноклеточной лимфомы, интраваскулярной B-крупноклеточной лимфомы, первичной эффузионной лимфомы, мелкоклеточной лимфома с нерассеченными ядрами, лимфомы Беркитта, множественной миеломы, плазмоцитомы, острого лимфоцитарного лейкоза, Т-клеточного острого лимфобластного лейкоза, В-клеточного острого лимфобластного лейкоза, В-клеточного пролимфоцитарного лейкоза, острого миелоидного лейкоза, хронического лимфоцитарного лейкоза, ювенильного миеломоноцитарного лейкоза, минимальной остаточной болезни, лейкоза ворсистых клеток, первичного миелофиброза, вторичного миелофиброза, хронического миелоидного лейкоза, миелодиспластического синдрома, миелопролиферативного заболевания или макроглобулинемии Вальденстрёма.
В других вариантах рак представляет собой рак поджелудочной железы, урологический рак, рак мочевого пузыря, колоректальный рак, рак толстой кишки, рак молочной железы, рак предстательной железы, рак почек, гепатоцеллюлярный рак, рак щитовидной железы, рак желчного пузыря, рак легких (например, немелкоклеточный рак легких, мелкоклеточный рак легких), рак яичников, рак шейки матки, рак желудка, рак эндометрия, рак пищевода, рак головы и шеи, меланому, нейроэндокринный рак, рак ЦНС, опухоли головного мозга (например, глиому, анапластическую олигодендроглиому, мультиформную глиобластому взрослых и анапластическую астроцитому взрослых), рак костей, саркому мягких тканей, ретинобластомы, нейробластомы, перитонеальные выпоты, злокачественные плевральные выпоты, мезотелиомы, опухоли Вильмса, трофобластические неоплазии, гемангиоперицитомы, саркомы Капоши, миксоидную карциному, круглоклеточную карциному, плоскоклеточную карциному, плоскоклеточную карциному пищевода, карциному ротовой полости, адренокортикальные раковые заболевания или опухоли, продуцирующие АКТГ.
Согласно одному варианту осуществления, рак выбран из рака головы и шеи, плоскоклеточной карциномы головы и шеи, плоскоклеточной карциномы шеи, острого лимфоцитарного лейкоза (ALL) взрослых или детей, острого миелоидного лейкоза (AML) у взрослых или детей, острого лимфобластного лейкоза, рака надпочечников, рака анального канала, астроцитарной глиомы, астроцитомы (I, II и III, или IV степени), B- или NK/Т-клеточной лимфомы, базального и плоскоклеточного рака кожи, рака желчных протоков, рака мочевого пузыря, рака костей, рака головного мозга, опухолей головного и спинного мозга взрослых, опухолей головного и спинного мозга детей, анапластической астроцитомы, рака молочной железы, рака желудочно-кишечного тракта, рака молочной железы у женщин, рака молочной железы у молодых женщин, рака молочной железы мужчин, рецидивирующего рака молочной железы, наследственного рака молочной железы, HER2-позитивного рака молочной железы, рака молочной железы с лимфогенным метастазированием, позитивного по ER (рецептор эстрогена) альфа рака молочной железы, рака у подростков, рака у детей, рака у молодых взрослых, рака неизвестной первичной локализации, болезни Кастлемана, рака шейки матки, интраэпителиальной неоплазии шейки матки, холангиокарциномы, хронического лимфоцитарного лейкоза (CLL), хронического миелоидного лейкоза (CML), хронического миеломоноцитарного лейкоза (CMML), колоректального рака, аденомы толстой кишки, плоскоклеточной карциномы кожи, рака эндометрия, эпителиального рака яичников, эпителиального рака яичников, ассоциированного с метастазами, рака пищевода, плоскоклеточного рака пищевода, саркомы Юинга, семейства опухолей Юинга, лимфобластного лейкоза (ALL), рака глаза, такого как меланома глаза и лимфома глаза, рака желчного пузыря, рака желудка, рака желудочно-кишечного тракта, желудочно-кишечных карциноидных опухолей, желудочно-кишечной стромальной опухоли (GIST), гестационной трофобластической болезни, глиобластомы, мультиформной глиобластомы (GBM), лейкоза ворсистых клеток, глиомы, глиомы высокой степени злокачественности, гепатоцеллюлярной карциномы, внутрипеченочной холангиокарциномы, инвазивной карциномы протоков молочной железы, лимфомы Ходжкина, саркомы капоши, рака почек, рака гортани и гипофаринкса, лейомиосаркомы, лейкоза, лейкоза у детей, рака печени, рака легких, карциноидной опухоли легких, лимфомы, лимфомы кожи, злокачественной мезотелиомы, мантийноклеточной лимфомы, медуллобластомы, меланомного рака кожи, злокачественной меланомы, менингиомы, рака кожи из клеток меркеля, множественной миеломы, множественной миеломы с остеонекрозом челюсти, миелодиспластического синдрома, рака полости носа и придаточных пазух носа, рака носоглотки, рецидивирующей или метастатической карциномы носоглотки, нейробластомы, нейроглиомы, неходжкинской лимфомы, неходжкинской лимфомы у детей, немелкоклеточного рака легких, устойчивого к гефитинибу немелкоклеточного рака легких, рака полости рта, рака полости рта и ротоглотки, остеосаркомы, легочной метастатической остеосаркомы, рака яичников, рака поджелудочной железы, карциномы щитовидной железы, папиллярной карциномы щитовидной железы, детской спинальной эпендимомы, рака полового члена, опухолей гипофиза, аденомы гипофиза, пронейральных опухолей, рака предстательной железы, ретинобластомы, рабдомиосаркомы, рака слюнных желез, рака кожи, мелкоклеточного рака легких, рака тонкой кишки, саркомы мягких тканей, плоскоклеточной карциномы языка, рака желудка, рака яичек, рака тимуса, рака щитовидной железы, саркомы матки, рака влагалища, рака вульвы, рака почек, ретинобластомы, макроглобулинемии Вальденстрёма и опухоли Вильмса.
Согласно одному частному варианту осуществления, в настоящем описании дополнительно обеспечено соединение или любой его метаболит или фармацевтически приемлемые соли, как определено в настоящем документе, и в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин для применения в предупреждении или лечении рака, выбранного из плоскоклеточной карциномы головы и шеи, плоскоклеточной карциномы шеи, острого лимфоцитарного лейкоза (ALL) взрослых или детей, острого миелоидного лейкоза (AML) у взрослых или детей, острого лимфобластного лейкоза, рака надпочечников, рака анального канала, астроцитарной глиомы, астроцитомы (I, II и III или IV степени), B- или NK/Т-клеточных лимфом, базального и плоскоклеточного рака кожи, рака желчных протоков, рака костей, рака головного мозга, опухолей головного и спинного мозга взрослых, опухолей головного и спинного мозга детей, анапластической астроцитомы, рака желудочно-кишечного тракта, рака молочной железы у женщин, рака молочной железы у молодых женщин, рака молочной железы мужчин, рецидивирующего рака молочной железы, наследственного рака молочной железы, HER2-позитивного рака молочной железы, рака молочной железы с лимфогенным метастазированием, позитивного по ER (рецептор эстрогена) альфа рака молочной железы, рака у подростков, рака у детей, рака у молодых взрослых, рака неизвестной первичной локализации, болезни Кастлемана, интраэпителиальной неоплазии шейки матки, холангиокарциномы, хронического лимфоцитарного лейкоза (CLL), хронического миелоидного лейкоза (CML), хронического миеломоноцитарного лейкоза (CMML), колоректальной аденомы, плоскоклеточной карциномы кожи, рака эндометрия, эпителиального рака яичников, эпителиального рака яичников, ассоциированного с метастазами, плоскоклеточной карциномы пищевода, саркомы Юинга, семейства опухолей Юинга, лимфобластного лейкоза (ALL), рака глаза, такого как меланома глаза и лимфома глаза, рака желудка, рака желудочно-кишечного тракта, желудочно-кишечных карциноидных опухолей, желудочно-кишечной стромальной опухоли (GIST), гестационной трофобластической болезни, глиобластомы, мультиформной глиобластомы (GBM), лейкоза ворсистых клеток, глиомы, глиомы высокой степени злокачественности, гепатоцеллюлярной карциномы, внутрипеченочной холангиокарциномы, инвазивной карциномы протоков молочной железы, лимфомы Ходжкина, саркомы Капоши, рака гортани и гипофаринкса, лейомиосаркомы, лейкоза, лейкоза у детей, карциноидной опухоли легких, лимфомы, лимфомы кожи, злокачественной мезотелиомы, мантийноклеточной лимфомы, медуллобластомы, злокачественной меланомы, менингиомы, рака кожи из клеток Меркеля, множественной миеломы, множественной миеломы с остеонекрозом челюсти, миелодиспластического синдрома, рака полости носа и придаточных пазух носа, рака носоглотки, рецидивирующей или метастатической карциномы носоглотки, нейробластомы, нейроглиомы, неходжкинской лимфомы, неходжкинской лимфомы у детей, устойчивого к гефитинибу немелкоклеточного рака легких, рака полости рта, рака полости рта и ротоглотки, остеосаркомы, легочной метастатической остеосаркомы, карциномы щитовидной железы, папиллярной карциномы щитовидной железы, детской спинальной эпендимомы, рака полового члена, опухолей гипофиза, аденомы гипофиза, пронейральных опухолей, ретинобластомы, рабдомиосаркомы, рака слюнных желез, рака кожи, мелкоклеточного рака легких, рака тонкой кишки, саркомы мягких тканей, плоскоклеточной карциномы языка, рака яичек, рака тимуса, саркомы матки, рака влагалища, рака вульвы, рака почек, ретинобластомы, макроглобулинемии Вальденстрёма и опухоли Вильмса.
Согласно другому варианту осуществления, метастазирование локализуется в головном мозге, голове или шее, легких, трахее, желудке, тонком кишечнике, толстой кишке, печени, костях, брюшине, яичниках, почках, мочевом пузыре, лимфатических узлах, мышцах или коже.
Согласно одному варианту осуществления соединение или любой из его метаболитов или его фармацевтически приемлемые соли, как определено в настоящем документе, и, в частности, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин, также называемый (8-хлор-хинолин-2-ил)-(4-трифторметокси-фенил)-амин, более конкретно предназначены для лечения или предупреждения любого метастазирования любого из вышеупомянутых видов рака в головном мозге, костях, печени, легких, почках, мышцах, брюшной полости или других тканях.
Согласно одному варианту осуществления, соединение или любой из его метаболитов или фармацевтически приемлемых солей, как описано в настоящем документе, и, в частности, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин, также называемый (8-хлор-хинолин-2-ил)-(4-трифторметокси-фенил)-амин, более конкретно предназначены для лечения или предупреждения следующих видов рака: рака головы и шеи, рака желудка, рака молочной железы, базального и плоскоклеточного рака кожи, рака печени, рака головного мозга, рака легких, рака поджелудочной железы, рака глаза, рака желудочно-кишечного тракта, колоректального рака, рака мочевого пузыря, рака костей и рака почек.
Согласно одному конкретному варианту осуществления, соединение или любой из его метаболитов, или их фармацевтически приемлемых солей, как описано в настоящем документе, и, в частности, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин, также называющийся (8-хлор-хинолин-2-ил)-(4-трифторметокси-фенил)-амин, в частности предназначены для лечения и предупреждения следующих видов рака: карциномы носоглотки (рецидивы и метастазы), астроцитарных глиом, рака, рака предстательной железы, немелкоклеточного рака легких (NSCLC), холангиокарциномы (с вовлечением лимфоузла и дистантным метастазированием), рака мочевого пузыря, плоскоклеточной карциномы головы и шеи (HNSCC), рака полости рта, саркомы Юинга, метастатической саркомы Юинга, устойчивого к гефитинибу немелкоклеточного рака легких, плоскоклеточной карциномы кожи, остеосаркомы, злокачественной меланомы, остеосаркомы связанной с легочными метастазами, колоректальной карциномы, рака молочной железы, колоректального рака (CRC), рака желудка (GC), мультиформной глиобластомы, глиомы, глиобластомы, ретинобластомы, карциномы носоглотки (NPC), колоректального рака, рака мочевого пузыря, острого миелоидного лейкоза, астроцитом (степени I-II-II-IV), B- или NK/Т-клеточных лимфом, рака мочевого пузыря (запущенная опухоль), дисплазия желудка, рака желудка, связанного с метастазами в лимфоузлы, глиомы, миелодиспластического синдрома, панкреатической аденокарциномы протоков (связанные с метастазами в лимфоузлы и/или опухоли, узла, метастазирования), HER2-позитивного рака молочной железы, аденокарциномы легких, медуллобластомы, немелкоклеточного рака легких (связанного с метастазами в лимфоузлы и/или опухолевых узлов метастазы), рака молочной железы (связанные с узла опухоли метастазы и метастазы лимфатических узлов), рака эндометрия, медуллобластомы, плоскоклеточной карциномы кожи, внутрипеченочной холангиокарциномы (ICC), рака желчного пузыря, колоректальной аденомы (CRA), острого лимфобластного лейкоза (ALL), мультиформной глиобластомы (GBM), аденокарциномы протоков поджелудочной железы (PDAC), рака мочевого пузыря (BC), рака яичников (OC), лейкоза, миелодиспластического синдрома (MDS), пронейральных опухолей, плоскоклеточной карциномы головы и шеи (HNSCC), первичной опухоли, почечно-клеточного рака (RCC), увеальной меланомы, злокачественного рака предстательной железы, плоскоклеточных карцином ротовой полости (OSCC), анапластических астроцитом, рака пищевода, астроцитом, холангиокарцином, рака молочной железы (связанного с метастазами в лимфоузлы), детской спинальной эпендимомы, рака поджелудочной железы, эпителиального рака яичников, рака молочной железы (связанные с костным метастазированием), гепатокарциномы, миелодиспластического синдрома, злокачественной меланомы (узловое метастазирование), нейроэндокринных новообразований тонкой кишки (SI-NEN), эпителиального рака яичников (связанные с метастазами в лимфоузлы, брюшину, и отдаленные органы), миелодиспластического синдрома, детской эпендимомы, карциномы желудка, рака молочной железы (ER-alpha позитивный), гепатоцеллюлярной карциномы (HCC), рака яичников, плоскоклеточного рака пищевода (ESCC), инвазивной карциномы протоков молочной железы (связанные с метастазами в лимфоузлы), лимфомы, миеломы (MM), лимфобластного лейкоза (ALL), хронического лимфоцитарного лейкоза (CLL), острого миелоидного лейкоза (AML), неходжкинской лимфомы (NHL), B- или NK/Т-клеточной лимфомы, карциномы шейки матки, карциносаркомы, рака шейки матки, интраэпителиальной неоплазии шейки матки (CIN2 и CIN3 классы), метахронного рака желудка, светлоклеточного рака почек, миелодиспластического синдрома (MDS), рака мочевого пузыря (BCA), рака поджелудочной железы, CCRCC (светлоклеточные раки почек), опухолевых тканей ульцеративного колита (UC) (рака, ассоциированного с колитом (CAC), дисплазии и спорадического колоректального рака (S-CRC)), интраэпителиальной неоплазии шейки матки, рака головы и шеи.
В соответствии с дополнительным вариантом осуществления, рак выбран из рака головы и шеи, плоскоклеточной карциномы головы и шеи, плоскоклеточной карциномы рака шеи, злокачественной меланомы, рака желудка, рака молочной железы, рака молочной железы у женщин, рака молочной железы у молодых женщин, базального и плоскоклеточного рака кожи, рака печени, рака головного мозга, анапластических астроцитом, рака легких, немелкоклеточного рака легких, устойчивого к гефитинибу немелкоклеточного рака легких, рака полости рта, рака глаза, рака желудка, рака желудочно-кишечного тракта, астроцитарных глиом, астроцитом (I, II, III, или IV степень), колоректального рака, колоректальной аденомы, плоскоклеточной карциномы кожи, рака мочевого пузыря, рака костей, рецидивирующего рака молочной железы, наследственного рака молочной железы, HER2-позитивного рака молочной железы, рака молочной железы, связанного с метастазами в лимфоузел, ER-альфа-положительного рака молочной железы, раак почек, интраэпителиальной неоплазии шейки матки, холангиокарциномы, лейомиосаркомы, хронического лимфоцитарного лейкоза (CLL), хронического миелоидного лейкоза (CML), хронического миеломоноцитарного лейкоза (CMML), острого миелоидного лейкоза (AML) у взрослых или детей, острого лимфобластного лейкоза, B- или NK/Т-клеточных лимфом, рака шейки матки, глиобластомы, мультиформной глиобластомы (GBM) лейкоза ворсистых клеток, глиомы, глиом высокой степени злокачественности, гепатоцеллюлярной карциномы, внутрипеченочной холангиокарциномы, инвазивного рака протоков молочной железы, рака почек, рака эндометрия, рака яичников, эпителиального рака яичников, эпителиального рака яичников связанного с метастазированием, рака пищевода, плоскоклеточного рака пищевода, саркома Юинга, лимфобластного лейкоза (ALL), лимфомы мантийных клеток, медуллобластомы, лимфомы, миелодиспластического синдрома, менингиомы, множественной миеломы (MM), множественной миеломы с остеонекрозом челюсти, рака носоглотки, рецидивирующего или метастатического рака носоглотки, нейробластомы, нейроглиомы, папиллярного рака щитовидной железы, детской спинальной эпендимомы, остеосаркомы, остеосаркомы с легочными метастазами, рака поджелудочной железы, рака щитовидной железы, саркомы, опухоли гипофиза, аденомы гипофиза, пронейральных опухолей, плоскоклеточной карциномы языка, ретинобластомы и рака предстательной железы.
В соответствии с дополнительным вариантом осуществления настоящего изобретения рак выбран из рака головы и шеи, плоскоклеточной карциномы головы и шеи, плоскоклеточной карциномы шеи, злокачественной меланомы, астроцитарной глиомы, глиомы, рака желудка, рака молочной железы, холангиокарциномы, рецидивирующей или метастатической карциномы носоглотки, базального и плоскоклеточного рака кожи, рака печени, рака головного мозга, анапластических астроцитом, рака легких, немелкоклеточного рака легких, устойчивого к гефитинибу немелкоклеточного рака легких, рака полости рта, глиобластомы, остеосаркомы, остеосаркомы с легочными метастазами, рака поджелудочной железы, рака глаза, рака желудочно-кишечного тракта, колоректального рака, колоректальной аденомы, плоскоклеточной карциномы кожи, рака эндометрия, эпителиального рака яичников, рака пищевода, саркомы Юинга, рака желудка, гепатоцеллюлярной карциномы, HER2-позитивного рака молочной железы, рака мочевого пузыря, рака костей, рака предстательной железы, ретинобластомы и рака почек.
В конкретном варианте осуществления раковые заболевания, которые рассматриваются в частности, выбраны из: анапластических астроцитом, астроцитарных глиом, рака мочевого пузыря, рака молочной железы, холангиокарциномы, колоректального рака, колоректальной аденомы, плоскоклеточной карциномы кожи, рака эндометрия, эпителиального рака яичников, рака пищевода, саркомы Юинга, рака желудка, устойчивого к гефитинибу немелкоклеточного рака легких, глиобластомы, глиомы, гепатоцеллюлярной карциномы, HER2-позитивного рака молочной железы, плоскоклеточной карциномы головы и шеи, злокачественной меланомы, карциномы носоглотки (рецидив или метастазирование), плоскоклеточной карциномы шеи, немелкоклеточного- рака легких, рака полости рта, остеосаркомы, остеосаркомы, связанной с легочным метастазированием, рака предстательной железы и ретинобластомы.
Согласно одному аспекту, настоящее изобретение относится к 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амину для применения в предупреждении и/или лечении рака, в частности, выбранного из рака головы и шеи, рака желудка, рака молочной железы, базального и плоскоклеточного рака кожи, рака печени, рака головного мозга, рака легких, рака глаза, рака желудочно-кишечного тракта, колоректального рака, рака мочевого пузыря, рака костей, рака почек, хронического лимфоцитарного лейкоза (CLL), хронического миелоидного лейкоза (CML), хронического миеломоноцитарного лейкоза (CMML), острого миелоидного лейкоза (AML), В- или NK/Т-клеточных лимфом, рака шейки матки, рака почек, рака эндометрия, рака яичников, рака пищевода, лимфобластного лейкоза (ALL), лимфомы, миелодиспластического синдрома, множественной миеломы (ММ), рака носоглотки, нейробластомы, остеосаркомы, остеосаркомы с легочным метастазиированием, рака поджелудочной железы, карциномы щитовидной железы, саркомы, опухолей гипофиза и рака предстательной железы.
Согласно частному варианту осуществления, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин может быть эффективен в лечении или предупреждении рака головы и шеи, рака желудка, рака молочной железы, базального и плоскоклеточного рака кожи, рака печени, рака головного мозга, рака легких, рака глаза, рака желудочно-кишечного тракта, колоректального рака, рака мочевого пузыря, рака костей или рака почек.
Рак включает, в одном варианте осуществления, без ограничения, лейкозы (например, острый лейкоз, острый лимфоцитарный лейкоз, острый миелоцитарный лейкоз, острый миелобластный лейкоз, острый промиелоцитарный лейкоз, острый миеломоноцитарный лейкоз, острый моноцитарный лейкоз, острый эритролейкоз, хронический лейкоз, хронический миелоцитарный лейкоз, хронический лимфоцитарный лейкоз), истинную полицитемию, лимфому (например, болезнь Ходжкина или неходжкинскую болезнь), макроглобулинемию Вальденстрёма, множественную миелому, болезнь тяжелых цепей и солидные опухоли, такие как саркомы и карциномы (например, фибросаркому, миксосаркому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиому, мезотелиому, опухоль Юинга, лейомиосаркому, рабдомиосаркому, рак толстой кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточная карцинома, базально-клеточная карцинома, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярную аденокарциному, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечно-клеточную карциному, гепатому, карциному желчных протоков, хориокарциному, семиному, эмбриональную карциному, опухоль Вильма, рак шейки матки, рак матки, рак яичек, карциному легких, мелкоклеточную карциному легких, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, мультиформную глиобластому (GBM, также известную как глиобластому), медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, акустическую невриному, олигодендроглиому, шванному, нейрофибросаркому, менингиому, меланому, нейробластому и ретинобластому).
В некоторых вариантах осуществления рак является глиомой, астроцитомой, мультиформной глиобластомой (GBM, также известной как глиобластома), медуллобластомой, краниофарингиомой, эпендимомой, пинеаломой, гемангиобластомой, акустической невриномой, олигодендроглиомой, шванномой, нейрофибросаркомой, менингиомой, меланомой, нейробластомой или ретинобластомой.
В некоторых вариантах осуществления рак является акустической невриномой, астроцитомой (например, I степень - Пилоцитарная астроцитома, II степень - астроцитома низшей степени, III степень - Анапластическая Астроцитома или IV степень - глиобластома (GBM)), хордомой, лимфомой ЦНС, краниофарингиомой, глиомой ствола головного мозга, эпендимомой, смешанной глиомой, глиомой зрительного нерва, субэпендимомой, медуллобластомой, менингиомой, метастатической опухолью головного мозга, олигодендроглиомой, опухолью гипофиза, примитивной нейроэктодермальной опухолью (PNET) или шванномой. В некоторых вариантах осуществления данный рак является типом, чаще встречающимся у детей, чем у взрослых, таким как глиома ствола головного мозга, краниофарингиома, эпендимома, ювенильная пилоцитарная астроцитома (JPA), медуллобластома, глиома зрительного нерва, опухоль эпифиза, примитивные нейроэктодермальные опухоли (PNET) или рабдоидная опухоль. В некоторых вариантах осуществления пациентом является взрослый человек. В некоторых вариантах осуществления пациентом является ребенок или педиатрический пациент.
Рак включает в себя в другом варианте осуществления без ограничения мезотелиому, гепатобилиарный рак (рак печени и желчного протока), рак костей, рак поджелудочной железы, рак кожи, рак головы или шеи, меланому кожи или меланому внутри глаза, рак яичников, рак толстой кишки, рак прямой кишки, рак анальной области, рак желудка, рак желудочно-кишечного тракта (желудочный, колоректальный и двенадцатиперстной кишки), рак матки, карциному фаллопиевых труб, карциному эндометрия, карциному шейки матки, карциному влагалища, карцинома вульвы, болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечников, саркому мягких тканей, рак уретры, рак полового члена, рак предстательной железы, рак яичек, хронический или острый лейкоз, хронический миелоидный лейкоз, лимфоцитарные лимфомы, рак мочевого пузыря, рак почки или мочеточника, почечно-клеточную карциному, карциному почечной лоханки, неходжкинскую лимфому, опухоли оси позвоночника, глиому ствола головного мозга, аденому гипофиза, рак коры надпочечников, рак желчного пузыря, множественную миелому, холангиокарциному, фибросаркому, нейробластому, ретинобластому или комбинации одного или более из вышеупомянутых видов рака.
В некоторых вариантах осуществления рак выбран из гепатоцеллюлярной карциномы, рака яичников, эпителиального рака яичников или рака фаллопиевых труб; папиллярной серозной цистаденокарциномы или папиллярной серозной карциномы матки (UPSC - uterine papillary serous carcinoma), рака предстательной железы, рака яичек, рака желчного пузыря, гепатохолангиокарциномы, синовиальной саркомы мягких тканей и костей, рабдомиосаркомы, остеосаркомы, хондросаркомы, саркомы Юинга, анапластического рака щитовидной железы, аденомы коры надпочечников, рак поджелудочной железы, карциномы протоков поджелудочной железы или аденокарциномы поджелудочной железы, рака желудочно-кишечного тракта/желудка (GIST), лимфомы, плоскоклеточной карциномы головы и шеи (SCCHN), рака слюнных желез, глиомы или рака головного мозга, ассоциированных с NF1 (NF1, нейрофиброматоз 1 типа), злокачественных опухолей оболочек периферических нервов (MPNST), макроглобулинемии Вальденстрёма или медуллобластомы.
В некоторых вариантах осуществления рак выбран из гепатоцеллюлярной карциномы (HCC), гепатобластомы, рака толстой кишки, рака прямой кишки, рака яичников, эпителиального рака яичников, рака фаллопиевой трубы, папиллярной серозной цистаденокарциномы, папиллярной серозной карциномы матки (UPSC), гепатохолангиокарциномы, синовиальной саркомы мягких тканей и костей, рабдомиосаркомы, остеосаркомы, анапластического рака щитовидной железы, аденомы коры надпочечников, рака поджелудочной железы, карциномы протоков поджелудочной железы, аденокарциномы поджелудочной железы, глиомы, ассоциированных с NF1 (NF1, нейрофиброматоз 1 типа), злокачественных опухолей оболочек периферических нервов (MPNST), макроглобулинемии Вальденстрёма или медуллобластомы.
Согласно другому варианту осуществления, рак выбран из анального рака, рака желчных протоков, рака желудочно-кишечного тракта, холангиокарциномы, колоректального рака, колоректальной аденомы, рака пищевода, плоскоклеточной карциномы пищевода, рака желудка, карциноидных опухолей желудочно-кишечного тракта, стромальной опухоли желудочно-кишечного тракта (GIST), гепатоцеллюлярной карциномы, внутрипеченочной холангиокарциномы, рака печени, рака легких, карциноидной опухоли легких, немелкоклеточного рака легких, устойчивого к гефитинибу немелкоклеточного рака легких, легочной метастатической остеосаркомы, рака желудка, рака поджелудочной железы, мелкоклеточного рака легких и рака тонкой кишки.
Согласно другому варианту осуществления, рак выбран из рака желудка, рака желудка, рака желудочно-кишечного тракта, колоректального рака, рака поджелудочной железы, рака легких и рака печени.
Согласно одному частному варианту осуществления, в настоящем описании дополнительно приведено соединение формулы (Ib’) или любого его метаболита или его фармацевтически приемлемой соли, и, в частности, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина, для применения в предупреждении и/или лечении рака, выбранного из рака анального канала, рака желчных протоков, рака желудочно-кишечного тракта, холангиокарциномы, колоректального, колоректальной аденомы, рака пищевода, плоскоклеточной карциномы пищевода, рака желудка, карциноидных опухолей желудочно-кишечного тракта, стромальной опухоли желудочно-кишечного тракта (GIST), гепатоцеллюлярной карциномы, внутрипеченочной холангиокарциномы, рака печени, рака легких, карциноидной опухоли легких, немелкоклеточного рака легких, устойчивого к гефитинибу немелкоклеточного рака легких, метастатической остеосаркомы легких, рака желудка, рака поджелудочной железы, мелкоклеточного рака легких и рака тонкой кишки.
Согласно другому частному варианту осуществления, в настоящем документе дополнительно обеспечено соединение формулы (Ib’) или любого его метаболита или его фармацевтически приемлемой соли, и в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин, для применения в предупреждении и/или лечении рака, выбранного из рака желудка, рака желудка, рака желудочно-кишечного тракта, колоректального рака, рака поджелудочной железы, рака легких и рака печени.
В некоторых вариантах осуществления настоящий документ предоставляет способ лечения рака, являющегося солидной опухолью, такой как саркома, карцинома или лимфома, включая этап введения раскрытого соединения или его фармацевтически приемлемой соли пациенту, нуждающемуся в этом. Солидные опухоли обычно представляют собой аномальную массу ткани, которая обычно не включает кисты или жидкие области. В некоторых вариантах осуществления рак выбран из почечно-клеточнй карциномы или рака почки; гепатоцеллюлярной карциномы (HCC) или гепатобластомы, или рака печени; меланомы; рака молочной железы; колоректальной карциномы или колоректального рака; рака толстой кишки; рака прямой кишки; рака анального канала; рака легких, такого как немелкоклеточный рака легких (NSCLC) или мелкоклеточный рака легких (SCLC); рака яичников, эпителиального рака яичников, карциномы яичников или рака фаллопиевых труб; папиллярной серозной цистаденокарциномы или папиллярной серозной карциномы матки (UPSC); рака предстательной железы; рака яичек; рака желчного пузыря; гепатохолангиокарциномы; синовиальной саркомы мягких тканей и костей; рабдомиосаркомы; остеосаркомы; хондросаркомы; саркомы Юинга; анапластического рака щитовидной железы; карциномы коры надпочечников; рака поджелудочной железы; карциномы протоков поджелудочной железы или аденокарциномы поджелудочной железы; рака желудочно-кишечного тракта/желудка (GIST); лимфомы; плоскоклеточного рака головы и шеи (SCCHN); рака слюнных желез; глиомы или рака головного мозга; ассоциированных с NF1 (нейрофиброматоз 1 типа), злокачественных опухолей оболочек периферических нервов (MPNST); макроглобулинемии Вальденстрёма; или медуллобластомы.
В некоторых вариантах осуществления рак выбран из почечно-клеточного рака, гепатоцеллюлярной карциномы (HCC), гепатобластомы, колоректальной карциномы, колоректального рака, рака толстой кишки, рака прямой кишки, рака анального канала, рака яичников, эпителиального рака яичников, карциномы яичников, рака фаллопиевых труб, папиллярной серозной цистаденокарциномы, папиллярной серозной карциномы матки (UPSC), гепатохолангиокарциномы, синовиальной саркомы мягких тканей и костей, рабдомиосаркомы, остеосаркомы, хондросаркомы, анапластического рака щитовидной железы, карциномы коры надпочечников, рака поджелудочной железы, карциномы протоков поджелудочной железы, аденокарциномы поджелудочной железы, глиомы, рака головного мозга, ассоциированного с NF1 (нейрофиброматоз 1 типа), злокачественных опухолей оболочек периферических нервов (MPNST), макроглобулинемии Вальденстрёма или медуллобластомы.
В некоторых вариантах осуществления рак выбран из гепатоцеллюлярной карциномы (HCC), гепатобластомы, рака толстой кишки, рака прямой кишки, рака яичников, эпителиального рака яичников, карциномы яичников, рака фаллопиевых труб, папиллярной серозной цистаденокарциномы, папиллярной серозной карциномы матки (UPSC), гепатохолангиокарциномы, синовиальной саркомы мягких тканей и костей, рабдомиосаркомы, остеосаркомы, анапластического рака щитовидной железы, карциномы коры надпочечников, рака поджелудочной железы, карциномы протоков поджелудочной железы, аденокарциномы поджелудочной железы, глиомы, ассоциированных с NF1 (NF1, нейрофиброматоз 1 типа), злокачественных опухолей оболочек периферических нервов (MPNST), макроглобулинемия Вальденстрёма или медуллобластомы.
В некоторых вариантах осуществления рак представляет собой гепатоцеллюлярную карциному (ГЦК). В некоторых вариантах осуществления раком является гепатобластома. В некоторых вариантах осуществления рак является раком толстой кишки. В некоторых вариантах осуществления рак является раком прямой кишки. В некоторых вариантах осуществления рак является раком яичников или карциномой яичников. В некоторых вариантах осуществления рак представляет собой эпителиальный рак яичников. В некоторых вариантах осуществления рак представляет собой рак фаллопиевых труб. В некоторых вариантах осуществления рак представляет собой папиллярную серозную цистаденокарциному. В некоторых вариантах осуществления рак представляет собой папиллярную серозную карциному матки (UPSC). В некоторых вариантах осуществления рак представляет собой гепатохолангиокарциному. В некоторых вариантах осуществления рак представляет собой синовиальную саркому мягких тканей и костей. В некоторых вариантах осуществления рак представляет собой рабдомиосаркому. В некоторых вариантах осуществления рак представляет собой остеосаркому. В некоторых вариантах осуществления рак представляет собой анапластический рак щитовидной железы. В некоторых вариантах осуществления рак представляет собой карциному коры надпочечников. В некоторых вариантах осуществления рак является раком поджелудочной железы или карциномой протоков поджелудочной железы. В некоторых вариантах осуществления рак представляет собой аденокарциному поджелудочной железы. В некоторых вариантах осуществления рак представляет собой глиому. В некоторых вариантах осуществления рак представляет собой злокачественные опухоли оболочек периферических нервов (MPNST). В некоторых вариантах осуществления рак представляет собой MPNST, ассоциированные с NF1 (NF1, нейрофиброматоз 1 типа). В некоторых вариантах рак является макроглобулинемией Вальденстрёма. В некоторых вариантах осуществления рак представляет собой медуллобластому.
Настоящее изобретение дополнительно демонстрирует способы и композиции для диагностики, прогностики и лечения раковых заболеваний, ассоциированных с вирусами, включая солидные опухоли, ассоциированные с вирусом иммунодефицита человека (ВИЧ), неизлечимые солидные опухоли позитивные по вирусу папилломы человека (ВПЧ)-16 и Т-клеточный лейкоз взрослых, вызванный вирусом Т-клеточного лейкоза человека типа I (HTLV-I) и являющийся высокоагрессивной формой CD4+ Т-клеточного лейкоза, характеризующейся клональной интеграцией HTLV-I в лейкозные клетки (см. https://clinicaltrials.gov/ct2/show/study/NCT02631746); а также вирус-ассоциированные опухоли при раке желудка, карциному носоглотки, рак шейки матки, рак влагалища, рак вульвы, плоскоклеточную карциному головы и шеи и карциному из клеток Меркеля. (см. https://clinicaltrials.gov/ct2/show/study/NCT02488759; см. также https://clinicaltrials.gov/ct2/show/study/NCT0240886; https://clinicaltrials.gov/ct2/show/NCT02426892).
В некоторых вариантах осуществления настоящее изобретение обеспечивает способ лечения опухоли у нуждающегося в этом пациента, включающий введение пациенту любого из данных соединений, солей или фармацевтических композиций, описанных в настоящем документе. В некоторых вариантах осуществления опухоль включает в себя любой из видов рака, описанных в настоящем описании. В некоторых вариантах осуществления опухоль представляет собой, в частности, рак меланому. В некоторых вариантах осуществления опухоль представляет собой, в частности, рак молочной железы. В некоторых вариантах осуществления опухоль представляет собой, в частности, рак легких. В некоторых вариантах осуществления опухоль представляет собой, в частности, мелкоклеточный рак легких (SCLC). В некоторых вариантах осуществления опухоль представляет собой, в частности, немелкоклеточный рак легких (NSCLC).
В некоторых вариантах данную опухоль лечат путем остановки дальнейшего роста опухоли. В некоторых вариантах осуществления опухоль лечат путем уменьшения размера (например, объема или массы) опухоли по меньшей мере на 5%, 10%, 25%, 50%, 75%, 90% или 99% относительно размера опухоли до начала лечения. В некоторых вариантах осуществления опухоли лечат путем уменьшения количества опухолей у пациента по меньшей мере на 5%, 10%, 25%, 50%, 75%, 90% или 99% относительно количества опухолей до лечения.
В настоящем тексте также описывается соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, или соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, где рак предствляет собой предраковое состояние, рак на ранней стадии или неметастатический рак.
Согласно одному варианту осуществления, соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, или соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, не нацелены непосредственно на метастатическую инвазию.
В настоящем документе также описывается соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем документе, или соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, где применение заключается в уменьшении или предупреждения возникновения предракового состояния, рака на ранней стадии или неметастатического рака у субъекта с раком в семейном анамнезе рака или наследственным синдромом рака, где у субъекта никогда не было клинически обнаруживаемого рака.
В настоящем тексте также описывается соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, или соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения, как определено в настоящем тексте, где для выбора пациента измеряют присутствие и/или уровень экспрессии miR-124 в крови и/или образце ткани.
Согласно другому варианту осуществления, в настоящем описании обеспечено соединение формулы (Ib’) или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем документе, или соединение формулы (IVb’) или его фармацевтически приемлемая соль для применения у пациента, как определено в настоящем тексте,
где у указанного пациента нет клинически обнаруживаемых метастазов, в частности, у указанного пациента предраковое состояние, рак на ранней стадии или неметастатический рак, или
где указанный пациент с клинически обнаруживаемыми метастазами, и указанные соединения формулы (Ib’) или формулы (IVb’) не направлены непосредственно на метастатическую инвазию.
Согласно частному варианту осуществления, в настоящем описании обеспечено ABX464 или любой из его метаболитов или его фармацевтически приемлемая соль для применения, как определено в настоящем документе, или соединение формулы 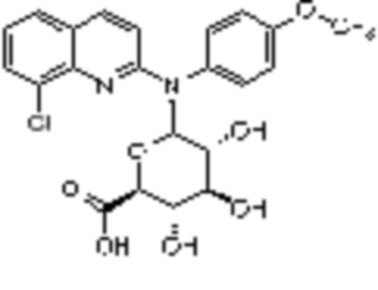 или его фармацевтически приемлемая соль для применения у пациента, как определено в настоящем документе,
или его фармацевтически приемлемая соль для применения у пациента, как определено в настоящем документе,
где у указанного пациента нет клинически обнаруживаемых метастазов, в частности, у указанного пациента предраковое состояние, рак на ранней стадии или неметастатический рак, или
где указанный пациент с клинически обнаруживаемыми метастазами, и указанный ABX464 или любой из его метаболитов, или его фармацевтически приемлемая соль, или указанное соединение формулы 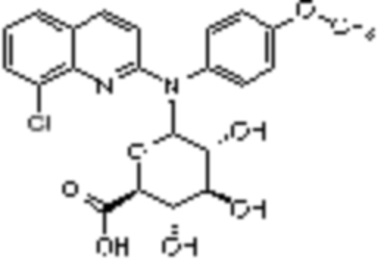 не нацелено непосредственно на метастатическую инвазию.
не нацелено непосредственно на метастатическую инвазию.
Как упоминалось выше, указанные соединения формул (Ib’) и (IVb’) могут быть использованы для предупреждения и/или лечения предракового состояния, рака на ранней стадии или неметастатического рака. Указанные соединения также могут быть эффективны для предупреждения и/или снижения вероятности рецидива рака.
В некоторых вариантах осуществления введение указанных соединений предупреждает превращение предракового состояния, рака на ранней стадии или неметастатического рака в инвазивный или метастатический рак. Например, предраковое состояние, ранняя стадия рака или неметастатический рак могут быть стадией 0, стадией I или стадией II рака, и в некоторых вариантах осуществления введение указанных соединений предупреждает прогрессирование предракового состояния, рака на ранней стадии или неметастатического рака до следующей стадии (стадий), например, стадии I, стадии II, стадии III или стадии IV рака. В некоторых вариантах осуществления указанные соединения вводят в течение времени и в количестве, достаточном для лечения предраковой опухоли, опухоли на ранней стадии или неметастатической опухоли у субъекта или для предупреждает превращения предраковой опухоли, опухоли на ранней стадии или неметастатической опухоли в инвазивный или метастатический рак. В некоторых вариантах осуществления введение указанных соединений уменьшает размер опухоли, массу опухоли или количество опухолей предраковой опухоли, опухоли на ранней стадии или неметастатической опухоли. Указанные соединения также могут быть введены в количестве и в течение времени для снижения сосудистой плотности в предраковой опухоли, опухоли на ранней стадии или неметастатической опухоли.
Под терминами "рак на ранней стадии" или "опухоль на ранней стадии" подразумевают рак, не являющийся инвазивным или метастатическим или классифицирующийся как рак 0, I или II стадии.
Термин "предраковый" относится к состоянию или росту, которые обычно предшествуют или развиваются в рак. "Предраковый" рост будут иметь клетки, которые характеризуются аномальной регуляцией клеточного цикла, пролиферации или дифференцировки, которые могут быть определены маркерами регуляции клеточного цикла, клеточной пролиферации или дифференцировки.
Под "дисплазией" подразумевается любой аномальный рост или развитие ткани, органа или клеток. Предпочтительно, дисплазия представляет собой диспалазию высокой степени или предраковую.
Под "массой опухоли" подразумевается количество раковых клеток, размер опухоли или размер рака в организме. Масса опухоли также называется опухолевой нагрузкой.
Под "числом опухолей" подразумевается количество опухолей.
Под "метастазированием" подразумевается распространение рака из его первичной локализации в другие места в теле. Раковые клетки могут отделяться от первичной опухоли, проникать в лимфатические и кровеносные сосуды, циркулировать по кровотоку и расти в отдаленном очаге (метастазировать) в нормальных тканях в других частях тела. Метастазы могут быть локальными или отдаленными. Метастазирование является последовательным процессом, зависящим от отделения опухолевых клеток от первичной опухоли, перемещения по кровотоку и остановки в отдаленном месте. На новом месте клетки формируют кровоснабжение и могут расти, образуя угрожающую жизни массу. Как стимулирующие, так и ингибирующие молекулярные пути в опухолевой клетке регулируют данное поведение, и взаимодействия между опухолевой клеткой и клетками-хозяевами в отдаленном участке также являются значительными.
Под "неметастатическим" раком подразумевается раковая опухоль, которая является доброкачественной или остается в первичном месте локализации и не проникает в лимфатическую или в систему кровеносных сосудов или в ткани, отличные от первичной локализации. В целом, неметастатический рак представляет собой любой рак 0, I или II стадии.
Ссылка на опухоль или рак как на "Стадию 0", "Стадию I", "Стадию II", "Стадию III" или "Стадию IV" указывает на классификацию опухоли или рака по общей стадии, или методами стадирования римскими цифрами, известными из уровня техники. Хотя фактическая стадия рака зависит от типа рака, в целом, рак 0 стадии представляет собой in situ поражение, рак I стадии представляет собой небольшую локализованную опухоль, стадия II представляет собой локальную опухоль на поздней стадии, рак III стадии представляет собой инвазию лимфатических узлов или окружающих тканей, а рак IV стадии представляет собой метастатический рак. Конкретные стадии для каждого типа опухоли известны квалифицированному клиницисту.
Как правило, классификация злокачественных опухолей TNM (TNM, см. 8-е издание в 2017 году) является всемирно признанным стандартом для классификации степени распространения рака. Действительно, TNM является системой обозначений, которая описывает стадию рака, возникающего из солидной опухоли, с использованием буквенно-цифровых кодов:
• T описывает размер изначальной (первичной) опухоли и то, проникла ли она в близлежащие ткани,
• N описывает близлежащие (регионарные) вовлеченные лимфатические узлы,
• М описывает отдаленные метастазы (распространение рака из одной части тела в другую).
Термин "опухоль", используемый в настоящем документе, относится ко всему росту и пролиферации неопластических клеток, будь то злокачественных или доброкачественных, а также ко всем предраковым и раковым клеткам и тканям.
Под "первичной опухолью" или "первичным раком" подразумевается исходный рак, а не метастатическое поражение, расположенное в другой ткани, органе или месте в теле субъекта.
Термин "рецидив рака" в настоящем документе относится к возвращению рака после лечения и включает в себя возвращение рака в первичный орган, а также отдаленный рецидив, когда рак возвращается за пределы первичного органа.
Соединения и композиции, согласно способу настоящего изобретения, могут быть введены с использованием любого количества и любого способа введения, эффективного для лечения или уменьшения тяжести рака, аутоиммунного расстройства, первичного иммунодефицита, пролиферативного нарушения, воспалительного заболевания, нейродегенеративного или неврологического заболевания, шизофрении, заболевания, связанного с костями, заболевания печени или сердечного заболевания. Точное требуемое количество будет варьироваться от субъекта к субъекту в зависимости от вида, возраста и общего состояния субъекта, тяжести заболевания или состояния, конкретного агента, способа его введения и тому подобного. Соединения согласно настоящему изобретению предпочтительно разрабатываются в форме единицы дозирования для удобства введения и однородности дозирования. Выражение “форма единицы дозирования”, используемое в настоящем документе, относится к физически дискретной единице агента, подходящей для пациента, подлежащего лечению. Нужно понимать, тем не менее, что общее ежедневное использование соединений и композиций настоящего изобретения будет определяться лечащим врачом в рамках тщательной медицинской оценки. Конкретный эффективный уровень дозы для любого конкретного пациента или организма будет зависеть от множества факторов, включающих лечащееся заболевание и тяжесть заболевания; активность конкретного используемого соединения; конкретную используемую композицию; возраст, массу тела, общее состояние здоровья, пол и диету данного пациента; время введения, способ введения и скорость выведения конкретного используемого соединения; продолжительность лечения; лекарственные средства, используемые в комбинации или совпадающие с конкретным используемым соединением, и подобные факторы, хорошо известные в области медицины.
Фармацевтически приемлемые композиции согласно настоящему изобретения могут быть введены людям и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, внутрибрюшинно, местно (в виде порошков, мазей или капель), буккально, в виде перорального или назального спрея или тому подобного, в зависимости от тяжести лечащегося заболевания или нарушения.
Жидкие лекарственные формы для перорального введения содержат без ограничений фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным соединениям жидкие лекарственные формы могут содержать инертные растворители, обычно используемые в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковых семян, арахиса, кукурузы, зародышей, оливок, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот сорбитана и их смеси. Помимо инертных разбавителей, пероральные композиции могут также включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подслащивающие, исправляющие вкус и придающие запах агенты.
Инъекционные препараты, например, стерильные инъекционные водные или масляные суспензии, могут быть получены в соответствии с известным уровнем техники с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный инъекционный препарат может также представлять собой стерильный инъекционный раствор, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых несущих лекарственное вещество сред и растворителей, которые могут быть использованы, находятся вода, раствор Рингера, U.S.P. (US Pharmacopeia - фармакопея США)) и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно используются в качестве растворителя или суспендирующей среды. Для этой цели может быть использовано любое легкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, используются при приготовлении инъекционных растворов.
Инъекционные препараты могут быть простерилизованы, например, путем фильтрации через фильтр, удерживающий бактерии, или путем включения стерилизующих агентов в виде стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной среде для инъекций перед использованием.
Для того чтобы продлить действие соединения согласно настоящему изобретения, часто желательно замедлить всасывание соединения при подкожном или внутримышечном введении. Это может быть достигнуто путем применения жидкой суспензии кристаллического или аморфного материала с плохой растворимостью в воде. Скорость абсорбции данного соединения затем зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристалла и кристаллической формы. В альтернативном варианте отложенная абсорбция парентерально вводимой формы соединения достигается путем растворения или суспендирования соединения в масляной среде, несущей лекарственное вещество. Инъекционные депо-формы получают путем формирования микрокапсулирующих матриц соединения в биоразлагаемых полимерах, таких как полилактид-полигликолид. В зависимости от соотношения соединения к полимеру и природы конкретного используемого полимера скорость высвобождения соединения можно контролировать. Примеры других биоразлагаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъецируемые лекарственные формы депо также получают путем улавливания соединения в липосомах или микроэмульсиях, совместимых с тканями тела.
Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые могут быть получены путем смешивания соединений данного изобретения с подходящими не раздражающими вспомогательными веществами или носителями, такими как масло какао, полиэтиленгликоль или суппозиторный воск, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела и, следовательно, растворяются в прямой кишке или вагинальной полости и высвобождают активное соединение.
Твердые лекарственные формы для перорального применения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах активное соединение смешивают по меньшей мере с одним инертным, фармацевтически приемлемым вспомогательным веществом или носителем, таким как цитрат натрия или дикальцийфосфат, и/или а) наполнителями или разбавителями, такими как крахмал, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, б) связующими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидинон, сахароза и гуммиарабик, в) увлажнителями, такими как глицерин, г) разрыхлителями, такими как агар-агар, карбонат кальция, крахмал картофеля или тапиоки, альгиновая кислота, определенные силикаты и карбонат натрия, д) замедлители растворения, такие как парафин, е) ускорители абсорбции, такие как соединения четвертичного аммония, ё) смачивающие агенты, такие как, например, цетиловый спирт и глицеринмоностеарат, ж) абсорбенты, такие как каолин и бентонитовая глина, и з) смазывающие материалы, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и их смеси. В случае капсул, таблеток и таблеток лекарственная форма может также содержать буферные агенты.
Твердые композиции одинакового типа могут также использоваться в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких вспомогательных веществ, как лактоза, или молочный сахар, а также высокомолекулярные полиэтиленгликоли и тому подобное. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул могут быть получены с покрытиями и оболочками, такими как кишечнорастворимые покрытия и другие покрытия, хорошо известные в области фармацевтического производства. Они могут необязательно содержать замутняющие агенты, а также могут представлять собой композицию, в которй они высвобождают активный ингредиент(-ы) только или предпочтительно в определенной части кишечного тракта, необязательно с задержкой. Примеры заливочных композиций, которые могут быть использованы, включают в себя полимерные субстанции и воски. Твердые композиции одинакового типа могут также использоваться в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких вспомогательных веществ, как лактоза, или молочный сахар, а также высокомолекулярных полиэтиленгликолей и тому подобного.
Активные соединения также могут быть в микрокапсулированной форме с одним или более вспомогательными веществами, как указано выше. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул могут быть получены с покрытиями и оболочками, такими как кишечнорастворимыми покрытиями, покрытиями, которые контролируют высвобождение, и другими покрытиями, хорошо известные в области фармацевтического производства. В таких твердых лекарственных формах активное соединение может быть смешано по меньшей мере с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы могут также содержать, как это происходит в стандартной практике, дополнительные вещества, отличные от инертных разбавителей, например, смазывающие вещества для таблетирования и другие вспомогательные вещества для таблетирования, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль лекарственные формы могут также содержать буферные агенты. Они могут необязательно содержать замутняющие агенты, а также могут представлять собой композицию, в которой они высвобождают активный ингредиент(-ы) только или предпочтительно в определенной части кишечного тракта, необязательно с задержкой. Примеры заливочных составов, которые могут быть использованы, включают в себя полимерные субстанции и воски.
Лекарственные формы для местного или трансдермального введения соединения согласно настоящему изобретению включают в себя мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, летучие препараты или пластыри. Активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферами, которые могут требоваться. Офтальмологическая лекарственная форма, ушные и глазные капли также рассматриваются как входящие в объем настоящего изобретения. Также, настоящее изобретение рассматривает применение трансдермальных пластырей, которые имеют дополнительное преимущество в обеспечении контролируемой доставки соединения в организм. Такие лекарственные формы могут быть получены путем растворения или дозирования соединения в соответствующей среде. Усилители абсорбции также могут быть использованы для усиления прохождения соединения через кожу. Скорость может регулироваться либо путем предоставления контролирующей мембраны, либо путем диспергирования соединения в полимерной матрице или геле.
Лечение рака или дисплазии
Виды и способы применения рассматриваются в значении изобретения.
Изобретение дополнительно относится к способу лечения или предупреждения рака или дисплазии, включающему, по меньшей мере, этап введения нуждающемуся в этом пациенту эффективного количества соединения, как определено выше, или любого из его метаболитов или его фармацевтически приемлемой соли, или любого из их энантиомеров или диастереоизомеров, в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина.
Настоящее изобретение также относится к применению, по меньшей мере, соединения, как определено выше, или любого из его метаболитов или его фармацевтически приемлемой соли, или любого из его энантиомеров или диастереоизомеров, и в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина в аморфной или кристаллической форме, или одного из его метаболитов или его фармацевтически приемлемых солей, в частности N-глюкуронидного метаболита, как определено выше, согласно настоящему изобретению для получения фармацевтической композиции, предназначенной для лечения рака или дисплазии.
Настоящее изобретение дополнительно относится к способу лечения пациентов, страдающих от рака или дисплазии, который включает, по меньшей мере, этап введения страдающему от вышеупомянутого пациенту эффективного количества соединения, как определено выше, или любого из его метаболитов или его фармацевтически приемлемой соли, или любого из его энантиомеров или диастереоизомеров, и, в частности, 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина в аморфной или кристаллической форме, или одного из его метаболитов или их фармацевтически приемлемых солей, в частности N-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина в аморфной или кристаллической форме, или одного из его метаболитов или их фармацевтически приемлемых солей, в частности N-глюкуронидного метаболита, как определено выше.
Раковые клетки человека из различных раковых источников используются для оценки противоопухолевой активности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина в любой форме или в форме одной из его фармацевтически приемлемой соли, например, в отношении пролиферации клеток, жизнеспособности и инвазивной активности. Клетки культивируют в специфической среде для каждого типа раковых клеток в присутствии или без 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амина в любой форме или одной из его фармацевтически приемлемых солей в течение различных периодов времени, например 48 и 72 часа. В конце культивирования клеточная цитотоксичность, пролиферация и жизнеспособность может быть оценена с помощью люминесцентного или колориметрического теста, например, CellTiter-Glo или MTT. Способность к инвазивности раковых клеток может быть изучена путем теста на миграционную активность с помощью мембранных вставок или теста на заживление раны.
Дозы и схема лечения
Данное изобретение дополнительно относится к способу предупреждения и/или лечения рака или дисплазии, способ включает этап введения хозяину эффективного количества соединения, как определено выше, или его фармацевтически приемлемой соли, в частности, с различными частотами, в дозах от 10 до 1000 мг, в частности от 25 до 800 мг, или даже от 30 до 600 мг, и, например, от 30 до 200 мг.
Согласно одному варианту осуществления, частота лечения может составлять один или два раза в день, один раз в три дня, один раз в неделю, один раз в 2 недели или один раз в месяц.
В соответствии с частным вариантом осуществления лечение является продолжительным или непостоянным.
Термин “продолжительное лечение” означает длительное лечение, которое может осуществляться с различными частотами введения, например один раз в три дня, или один раз в неделю, или один раз в две недели, или один раз в месяц.
Период лечения, т.е. когда лечение является непостоянным, может варьироваться от 1 недели до трех лет, что включает в себя от 2 до 6 недель, 3 месяца, 6 месяцев, 1 год и три года.
Согласно одному варианту осуществления соединение или любую из его фармацевтически приемлемых солей, как описано в настоящем документе, вводят в дозе, варьирующейся от 25 до 300 мг, в частности от 25 до 200 мг, например, от 25 до 150 мг и, в частности, от 25 до 100 мг. Дозы в диапазоне от 25 до 300 мг включают в себя дозы около 25, 50, 75, 100, 150, 200, 250 и 300 мг.
Указанные дозы могут быть адаптированы в зависимости от того, является ли лечение продолжительным или непостоянным. Следует также понимать, что конкретная дозировка и режим лечения для любого конкретного пациента будет зависеть от множества факторов, включая активность конкретного используемого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время введения, скорость выведения, комбинацию лекарственных средств, а также усмотрение лечащего врача и тяжесть конкретного лечащегося заболевания. Количество хинолинового соединения настоящего изобретения в композиции также будет зависеть от конкретного соединения в композиции.
Все комбинации доз, частот и периода лечения охватываются в рамках настоящего изобретения.
Согласно конкретному варианту осуществления соединение согласно настоящему изобретению, и в частности 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или любая его фармацевтически приемлемая соль, может быть введена в различных дозировках и схеме лечения, в частности, один раз в день в дозах от 10 до 1000 мг, в частности от 25 до 800 мг и, в частности, от 25 до 400 мг при продолжительном лечении или в течение периода лечения.
Период лечения может варьировать от одной недели до трех лет, что включает в себя от 2 до 6 недель, 3 месяца, 6 месяцев, 1 год и три года.
Производное хинолина может быть введено каждый день, один раз в три дня, один раз в неделю, один раз в две недели или один раз в месяц.
Несколько примеров доз и схем лечения приведены ниже.
Более конкретно данное изобретение относится к дозировке и схеме лечения, где соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 25 мг один раз в день в течение периода лечения или при продолжительном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 50 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 75 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 100 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 150 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 300 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 400 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно данное изобретение относится к дозировке и схеме лечения, в которых соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и более конкретно 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин или его фармацевтически приемлемую соль, вводят по 600 мг один раз в день в течение периода лечения или при непрерывном лечении
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 50 мг один раз в день в течение периода лечения или при непрерывном лечении.
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 150 мг один раз в день в течение периода лечения или при непрерывном лечении.
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 300 мг один раз в день в течение периода лечения или при непрерывном лечении.
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 500 мг один раз в день в течение периода лечения или при непрерывном лечении.
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 700 мг один раз в день в течение периода лечения или при непрерывном лечении.
Более конкретно изобретение относится к дозировке и схеме лечения, где N-глюкуронидный метаболит формулы (1), как определено выше, или его фармацевтически приемлемую соль вводят по 1000 мг один раз в день в течение периода лечения или при непрерывном лечении.
Таким образом, соединение согласно настоящему изобретению может быть реализовано в фармацевтической композиции, которая может содержать эффективное количество соединения, как определено выше, или его метаболит во всех формах, как описано выше, и одно или более фармацевтически приемлемое вспомогательное вещество.
Композиция может содержать соединение настоящего изобретения или его фармацевтически приемлемую соль и фармацевтически приемлемое вспомогательное вещество, носитель, адъювант или несущую лекарственное вещество среду. В определенных вариантах осуществления композиция данного изобретения получают для введения пациенту, нуждающемуся в подобной композиции.
Вышеупомянутые вспомогательные вещества, носители, адъюванты или несущие лекарственное вещество среды выбраны в соответствии с лекарственной формой и желаемым способом введения.
Фармацевтически приемлемые носители, адъюванты или несущие лекарственное вещество среды, которые могут быть использованы в композициях данного изобретения, включают без ограничений: ионообменные вещества, окись алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, частичные глицеридные смеси насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, динатрий гидрофосфат, дикалия гидрофосфат, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрийкарбоксиметилцеллюлоза, полиакрилаты, воски, блок-сополимеры полиэтилена и полиоксипропилена, полиэтиленгликоль и ланолин.
Указанная фармацевтическая форма может быть введена перорально, парентерально, с помощью ингаляционного спрея, местно, ректально, назально, буккально, вагинально или через имплантированный резервуар. Термин "парентеральный", используемый в настоящем документе, включает в себя подкожные, внутривенные, внутримышечные, внутрисуставные, внутрисиновиальные, интрастернальные, интратекальные, внутрипеченочные, внутриочаговые и внутричерепные инъекции или инфузионные методы. Предпочтительно, чтобы композиции вводят перорально, интраперитонеально или внутривенно. Стерильные инъекционные формы композиций настоящего изобретения могут быть водной или масляной суспензией. Эти суспензии могут быть получены в соответствии с известными в данной области методами с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный инъекционный препарат может также представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых несущих лекарственное вещество сред и растворителей, которые могут быть использованы, находятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно используются в качестве растворителя или суспендирующей среды.
Для этой цели может быть использовано любое легкое нелетучее масло, включая синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, эффективны при получении инъекционных растворов, также как и натуральные фармацевтически приемлемые масла, такие как оливковое или касторовое масло, особенно в их полиоксиэтилированных вариантах. Данные масляные растворы или суспензии могут также содержать длинноцепочечный спиртовой разбавитель или диспергирующее вещество, такой как карбоксиметилцеллюлоза или подобные диспергирующие агенты, которые обычно используются в получении фармацевтически приемлемых лекарственных форм, включая эмульсии и суспензии. Другие обычно используемые сурфактанты, такие как Tweens, Spans и другие эмульгирующие агенты или усилители биодоступности, которые обычно используются в производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм, также могут использоваться в целях получения. Фармацевтическая форма, в частности, может быть пригодна для энтерального или парентерального введения в сочетании с соответствующими вспомогательными веществами, например, в виде простых таблеток или таблеток с покрытием, твердых желатиновых капсул, капсул в мягкой оболочке и других капсул, суппозиториев или пригодных для питья форм, таких как суспензии, сиропы или инъекционные растворы или суспензии.
Более конкретно, способ введения может быть пероральным или парентеральным (IM внутримышечный, SC подкожный, IV внутривенный) или внутриопухолевым или быть in-situ введением.
Могут быть использованы фармацевтические композиции с замедленным высвобождением.
Например, соединение или любой из его метаболитов или его фармацевтически приемлемая соль, как описано в настоящем документе, могут быть введены перорально, парентерально, внутривенно, трансдермально, внутримышечно, ректально, сублингвально, мукозально, назально или по-другиму. Кроме того, соединение или любой из его или метаболитов или его фармацевтически приемлемая соль, как описано в настоящем документе, могут бытьвведены в форме фармацевтической композиции и/или в форме единицы дозирования.
В частности, фармацевтические композиции данного изобретения могут вводиться перорально и/или парентерально.
Согласно одному иллюстративному варианту осуществления фармацевтические композиции данного изобретения могут быть введены перорально. Фармацевтически приемлемые композиции настоящего изобретения могут быть введены перорально в любой перорально приемлемой лекарственной форме, включая без ограничений капсулы, таблетки, водные суспензии или растворы. В случае таблеток для перорального применения обычно используемые носители включают в себя лактозу и кукурузный крахмал. Обычно также добавляют смазывающие вещества, такие как стеарат магния. Для перорального введения в форме капсул пригодные разбавители включают в себя лактозу и высушенный кукурузный крахмал. Когда для перорального применения требуются водные суспензии, активный ингредиент комбинируют с эмульгирующими и суспендирующими агентами. При необходимости можно также добавить определенные подслащивающие, вкусоароматические или красящие агенты.
В качестве альтернативы фармацевтически приемлемые композиции данного изобретения могут вводиться в форме суппозиториев для ректального введения. Они могут быть получены путем смешивания агента с подходящим нераздражающим вспомогательным веществом, являющимся твердым при комнатной температуре, но жидким при ректальной температуре и, следовательно, растоворяющимися в прямой кишке, чтобы высвободить лекарство. Подобные материалы включают в себя какао-масло, пчелиный воск и полиэтиленгликоли.
Фармацевтически приемлемые композиции настоящего изобретения также могут быть ввдены местно, особенно когда мишень для лечения включает области или органы, легко доступные для местного применения, включая заболевания глаз, кожи или нижних отделов кишечного тракта. Для каждой из этих областей или органов без труда изготавливаются подходящие местные лекарственные формы.
Местное нанесение для нижних отделов кишечного тракта может осуществляться в форме ректальных суппозиториев (см. выше) или в подходящей лекарственной форме клизмы. Также могут быть использованы местно-трансдермальные пластыри.
Для местного нанесения, предоставляемые фармацевтически приемлемые композиции могут быть получены в форме подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или более носителях. Носители для местного введения соединений данного изобретения включают в себя, но не ограничиваются ими: минеральное масло, жидкий вазелин, медицинский вазелин, пропиленгликоль, полиоксиэтилен, полиоксипропиленовое соединение, эмульгирующий воск и воду. В альтернативном варианте, предоставляемые фармацевтически приемлемые композиции могут быть изготовлены в подходящей форме лосьона или крема, содержащих активные компоненты, суспендированные или растворенные в одном или нескольких фармацевтически приемлемых носителях. Подходящие носители включают, но не ограничиваются ими: минеральное масло, сорбитанмоностеарат, полисорбат 60, воск цетиловых сложных эфиров, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
Для офтальмологического применения обеспечиваемые фармацевтически приемлемые композиции могут быть получены в виде тонкоизмельченных суспензий в изотоническом стерильном физиологическом растворе с подведенным рН или, предпочтительно, в виде растворов в изотоническом стерильном физиологическом растворе с отрегулированным рН, либо с консервантом, таким как бензилалкония хлорид, либо без него. Альтернативно, для офтальмологического применения фармацевтически приемлемые композиции могут быть получены в форме мази, такой как вазелин.
Фармацевтически приемлемые композиции настоящего изобретения также могут быть введены в виде назального аэрозоля или ингаляцией. Такие композиции получают в соответствии с методами, хорошо известными в области фармацевтического производства, и могут быть получены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, стимуляторов абсорбции для повышения биодоступности, фторуглеродов и/или других обычных солюбилизирующих или диспергирующих агентов.
Наиболее предпочтительно, если фармацевтически приемлемые композиции настоящего изобретения разработаны для перорального введения. Такие препараты можно вводить с пищей или без нее. В некоторых вариантах осуществления фармацевтически приемлемые композиции данного изобретения вводят без пищи. В других вариантах осуществления фармацевтически приемлемые композиции данного изобретения вводят с пищей.
Подходящие лекарственные формы включают в себя без ограничений: капсулы, таблетки (включая быстро растворяющиеся таблетки и таблетки с отсроченным высвобождением), порошок, сиропы, пероральные суспензии и растворы для парентерального введения, и, в частности, капсулы.
Фармацевтическая композиция может также содержать другое лекарственное средство для лечения рака, хорошо известное специалисту в данной области, в сочетании с соединением согласно настоящему изобретению.
Предпочтительно соединение или любой из его или метаболитов или его фармацевтически приемлемая соль, как описано в настоящем документе, могут быть введены в комбинации с одним или более другими противоопухолевыми препаратами и/или с радиотерапией.
Следовательно, настоящее изобретение дополнительно относится к фармацевтической комбинации формулы (I) или любого из ее метаболитов или фармацевтически приемлемой соли или любого из их энантиомеров или диастереоизомеров, как определено выше, и другого противоопухолевого лекарственного средства.
Когда соединение или любой из его метаболитов или его фармацевтически приемлемая соль, как описано в настоящем документе, вводят в комбинации с другим активным ингредиентом, таким как другое противоопухолевое лекарственное средство, оно может быть введено в уникальной лекарственной форме.
В альтернативном варианте, такая комбинация может быть введена раздельно или одновременно, например, болюсно. Согласно указанному конкретному варианту осуществления, указанная комбинация может быть в форме по меньшей мере двух фармацевтических препаратов. Другими словами, комбинация может быть в виде комбинированного набора или продукта. Форма таких комбинаций будет зависеть от способа введения каждого из соединений.
В таком варианте осуществления два фармацевтических препарата могут вводиться последовательно (в разное время) или одновременно (в одно и то же время).
Другими словами, введение соединения формулы (I) или (I’) или любого из его метаболитов или их фармацевтически приемлемой соли и указанной дополнительной противоопухолевой терапии является одновременным, раздельным или распределенным во времени.
Например, согласно некоторым вариантам осуществления, каждое соединение комбинации или его композиция вводится одним и тем же способом введения (т.е. строго перорально). Согласно другим вариантам осуществления, некоторые соединения вводят различными способами введения (т.е. перорально и парентерально).
Комбинацию можно вводить повторно за курс из нескольких циклов согласно протоколу, который зависит от характера и стадии рака предстательной железы, подлежащего лечению, а также от пациента, подлежащего лечению (возраст, вес, предыдущее лечение(-я) и т.д.). Протокол может быть определен любым практикующим врачом, специализирующимся в области онкологии.
Согласно конкретному варианту осуществления данного изобретения, радиотерапевтические процедуры лечения также могут проводиться одновременно или последовательно.
Среди других противоопухолевых препаратов можно привести следующие:
- Ингибиторы рецепторов андрогенов, такие как энзалутамид (Xtandi®, Astellas/Medivation), абиратерон (Zytiga®, Centocor/Ortho), антагонист рецепторов гонадотропин-рилизинг-гормона (GnRH), такие как дегараликс (Firmagon®, Ferring Pharmaceuticals)
- Антиапоптотические средства, такие как венетоклакс (Venclexta®, AbbVie/Genentech), блинатумомаб (Blincyto®, Amgen), навитоклакс (ABT-263, Abbott);
- Антипролиферативные и антимитотические средства, такие как алкалоиды барвинка (включающие винбластин, винкристин);
- Антибиотики, такие как дактиномицин, даунорубицин, доксорубицин, идарубицин, антрациклины, митоксантрон, блеомицины, пликамицин (митрамицин) и митомицин;
- L-аспарагиназа;
- Антитромбоцитарные средства;
- Антипролиферативные/антимитотические алкилирующие агенты, такие как азотистый иприт, циклофосфамид и аналоги (которые включают мелфалан, хлорамбуцил, гексаметилмеламин и тиотепа), алкил нитрозомочевины (которые включают кармустин) и аналоги, стрептозоцин и триазены (включающие дакарбазин);
- Антипролиферативные/антимитотические антиметаболиты, такие как аналоги фолиевой кислоты (которые включают метотрексат), ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; активные соединения микротрубочек; алкилирующие соединения; ингибиторы гистоновой деацетилазы; соединения, которые индуцируют процессы дифференцировки клеток; ингибиторы циклооксигеназы; ингибиторы MMP; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, нацеленные/снижающие белковую или липидную киназную активность и дополнительные антиангиогенные соединения; соединения, которые нацелены, снижают или ингибируют активность белковой или липидной фосфатазы; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; ингибиторы матриксной металлопротеиназы; бисфосфонаты; модификаторы биологического ответа; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеасом; соединения, используемые в лечении гематологических злокачественных новообразований; соединения, которые нацелены, снижают или ингибируют активность Flt-3; ингибиторы Hsp90, такие как 17-AAG (17-аллиламиногельданамицин, NSC330507), 17-DMAG (17-диметиламиноэтиламино-17-деметокси-гелданамицин, NSC707545), IPI-504, CNF1010, CNF2024, CNF1010 из Conforma Therapeutics; темозоломид (Temodal®); ингибиторы кинезинового белка веретена деления, такие как SB715992 или SB743921 из GlaxoSmithKline, или пентамидин/хлорпромазин от CombinatoRx; ингибиторы MEK, такие как ARRY142886 от Array BioPharma, AZd6244 от AstraZeneca, PD181461 от Pfizer и лейковорин;
- Антимиграционные агенты;
- Ингибиторы ангиогенеза, такие как TNP-470;
- Ингибиторы ароматазы, такие как летрозол и анастрозол, экземестан;
- Ангиотензин
- Антисмысловые олигонуклеотиды, такие как антисмысловые нуклеиновые кислоты против miR-124;
- Антикоагулянты, такие как гепарин, синтетические соли гепарина и другие ингибиторы тромбина;
- Ингибиторы аргинина, такие как AEB1102 (пегилированная рекомбинантная аргиназа, Aeglea Biotherapeutics) и CB-1158 (Calithera Biosciences);
- Ингибиторы резорбции костной ткани, такие как деносумаб (Xgeva®, Amgen), бисфосфонаты, такие как золедроновая кислота (Zometa®, Novartis);
- Ингибиторы CC рецептора хемокина 4 типа (CCR4), такие как могамулизумаб (Poteligeo®, Kyowa Hakko Kirin, Япония);
- Ингибиторы CDK, такие как ингибиторы CDK4/CDK6, такие как палбоциклиб (Ibrance®, Pfizer); рибоциклиб (Kisqali®, Novartis); абемациклиб (Ly2835219, Eli Lilly); и трилациклиб (G1T28, G1 Therapeutics);
- Ингибиторы клеточного цикла и индукторы дифференцировки, такие как третиноин;
- Кортикостероиды, такие как кортизон, дексаметазон, гидрокортизон, метилпреднизолон, преднизон и преднизолон;
- Повреждающие ДНК агенты, такие как актиномицин, амсакрин, бусульфан, карбоплатин, хлорамбуцил, цисплатин, циклофосфамид (CYTOXAN®), дактиномицин, даунорубицин, доксорубицин, эпирубицин, ифосфамид, мелфалан, мехлорэтамин, митомицин, митоксантрон, нитрозомочевина, прокарбазин, таксол, таксотер, тенипозид, этопозид и триэтилентиофосфорамид;
- Фибринолитические агенты, такие как активатор тканевого плазминогена, стрептокиназа, урокиназа, аспирин, дипиридамол, тиклопидин и клопидогрел;
- Антагонисты фолиевой кислоты;
- Ингибиторы рецепторв FLT3, такие как энзалутамид, абиратерон, апалутамид, эрлотиниб, кризотиниб, нирапариб, олапариб, осимертиниб, регорафениб, сунитиниб, лестауртиниб, мидостаурин, гилтеритиниб, семаксиниб, линифаниб, фостаматиниб, пексидартиниб, сорафениб, кабозантиниб, понатиниб, илорасертиб, пакритиниб, фамитиниб, пексидартиниб, квизартиниб;
- Ингибиторы глутаминазы, такие как CD-839 (Calithera Biosciences);
-Ингибиторы киназы трансдукции сигнала фактора роста;
- Ингибиторы фактора роста, такие как ингибиторы фактора роста эндотелия сосудов и ингибиторы фактора роста фибробластов, такие как оларатумаб (Lartrovo®; Eli Lilly), цетуксимаб (Erbitux®, Eli Lilly); нецитумумаб (Portrazza®, Eli Lilly), панитумумаб (Vectibix®, Amgen); и осимертиниб (действующий на активированный EGFR, Tagrisso®, AstraZeneca);
- Ингибиторы Hedgehog сигнального пути, такие как сонидегиб (Odomzo®, Sun Pharmaceuticals); и висмодегиб (Erivedge®, Genentech);
- Ингибиторы гистоновой деацетилазы (HDAC), такие как вориностат (Zolinza®, Merck); ромидепсин (Istodax®, Celgene); панобиностат (Farydak®, Novartis); белиностат (Beleodaq®, Spectrum Pharmaceuticals); энтиностат (SNDX-275, Syndax Pharmaceuticals) (NCT00866333); и хидамид (Epidaza®, HBI-8000, Chipscreen Biosciences, Китай);
- Гормоны и их аналоги, такие как эстроген, тамоксифен, гозерелин, бикалутамид и нилутамид);
- Ингибиторы изоцитратдегидрогеназы (IDH), такие как AG120 (Celgene; NCT02677922); AG221 (Celgene, NCT02677922; NCT02577406); BAY1436032 (Bayer, NCT02746081); IDH305 (Novartis, NCT02987010)
- Изофлавоны, такие как генистеин;
- Иммунодепрессанты, такие как такролимус, сиролимус, азатиоприн и микофенолат;
- Ингибиторы белков-супрессоров р53, таких как ALRN-6924 (Aileron);
- Ингибиторы трансформирующего фактора роста-бета (TGF-бета или TGFß), такие как NIS793 (Novartis), фрезолимумаб (GC1008; Sanofi-Genzyme), M7824 (Merck KGaA - ранее MSB0011459X);
- Агонисты клеток iNKT, такие как ABX196 (Abivax)
- Ингибиторы mTOR, такие как эверолимус (Afinitor®, Novartis); темсиролимус (Torisel®, Pfizer) и сиролимус (Rapamune®, Pfizer);
- Препараты, ингибирующие микротрубочки, такие как таксаны (которые включают паклитаксел, доцетаксел), винбластин, нокодазол, эпотилоны, винорелбин) (NAVELBINE®) и эпиподофиллотоксины (этопозид, тенипозид);
- Доноры оксида азота;
- Ингибиторы нуклеозидов, такие как трабектедин (гуанидин алкилирующий агент, Yondelis®, Janssen Oncology), мехлорэтамин (алкилирующий агент, Valchlor®, Aktelion Pharmaceuticals); винкристин (Oncovin®, Eli Lilly; Vincasar®, Teva Pharmaceuticals; Marqibo®, Talon Therapeutics); темозоломид (пролекарство к алкилирующему агенту 5-(3-метилтриазен-1-ил)-имидазол-4-карбоксамид (MTIC) Temodar®, Merck); инъекция цитарабина (ara-C, антиметаболическый аналог цитидина, Pfizer); ломустин (алкилирующий агент, CeeNU®, Bristol-Myers Squibb; Gleostine®, NextSource Biotechnology); азацитидин (пиримидиновый нуклеозидный аналог цитидина, Vidaza®, Celgene); омацетаксин мепесукцинат (эфир цефалотаксина) (ингибитор синтеза белка, Synribo®; Teva Pharmaceuticals); аспарагиназа Erwinia chrysanthemi (фермент для истощения аспарагина, Elspar®, Lundbeck; Erwinaze®, EUSA Pharma); эрибулина мезилат (ингибитор микротрубочек, антимитотик на основе тубулина, Halaven®, Eisai); кабазитаксел (ингибитор микротрубочек, антимитотик на основе тубулина, Jevtana®, Sanofi-Aventis); капацетрин (ингибитор тимидилатсинтазы, Xeloda®, Genentech); бендамустин (бифункциональное производное мехлорэтамина, предположительно образует поперечные связи между нитями ДНК, Treanda®, Cephalon/Teva); иксабепилон (полусинтетический аналог эпотилона В, ингибитор микротрубочек, антимитотик на основе тубулина, Ixempra®, Bristol-Myers Squibb); неларабин (пролекарство аналога дезоксигуанозина, нуклеозидный метаболический ингибитор, Arranon®, Novartis); клорафабин (пролекарство ингибитора рибонуклеотидной редуктазы, конкурентный ингибитор дезоксицитидина, Clolar®, Sanofi-Aventis); и трифлуридин и типирацил (нуклеозидный аналог на основе тимидина и ингибитор тимидиновой фосфорилазы, Lonsurf®, Taiho Oncology);
- Ингибиторы PI3K, такие как иделализиб (Zydelig®, Gilead), альпелизиб (BYL719, Novartis), тазелизиб (GDC-0032, Genentech/Roche); пиктилизиб (GDC-0941, Genentech/Roche); копанлизиб (BAY806946, Bayer); дувелизиб (ранее IPI-145, Infinity Pharmaceuticals); PQR309 (Piqur Therapeutics, Швейцария); и TGR1202 (ранее RP5230, TG Therapeutics);
- Координационные комплексы платины (такие, как цисплатин, оксилоплатин, карбоплатин, недаплатин, пикоплатин, прокарбазин, митотан, сатраплатин и аминоглютетимид);
- Ингибитор поли(АДФ-рибоза)-полимеразы (PARP), например, выбранный из: олапариба (Lynparza®, AstraZeneca); рукапариба (Rubraca®, Clovis Oncology); нирапариба (Zejula®, Tesaro); талазопариба (MDV3800/BMN 673/LT00673, Medivation/Pfizer/Biomarin); велипариба (ABT-888, AbbVie); и BGB-290 (BeiGene, Inc.);
- Ингибиторы протеасом, такие как эверолимус (Afinitor®, Novartis); темсиролимус (Torisel®, Pfizer); и сиролимус (Rapamune®, Pfizer), бортезомиб (Velcade®, Takeda); карфилзомиб (Kyprolis®, Amgen); и иксазомиб (Ninlaro®, Takeda);
- Аналоги пиримидина и пурина, такие как флоксуридин, капецитабин и цитарабин;
- Блокаторы рецепторов, Антисекреторные агенты, такие как бревельдин;
- Селективный модулятор рецепторов эстрогена (SERM - Selective estrogen receptor modulator), такой как ралоксифен (Evista®, Eli Lilly);
- Терапевтические антитела, например, выбранные из: антител к TNF, антител к VEGF, антител к EGFR, антител к PD-1, антител к HER2, антител к CD20, антител к IL17 и антител к CTLA4, антетел к PDL1, антител к CD25, антител к α4интегрин, антител к IL6R, антиител к C5, антител к IL1, антиител к TPO, антител к IL12/23, антител к EPCAM/CD3, антител к CD30, антител к CD80/86, антител к сибирской язве, антиел к CCR4, антител к CD6, антител к CD19, антител к α4β7, антител к IL6, антител к VEGFR-2, антител к SLAMF7, антител к GD2, антител к IL17A, антител к PCSK9, антител к IL5, антител к CD22, антител к IL4, антител к PDGFRα, антител к IL17RA и антител к TcdB, и такие как выбранные из: абаговомаба, абатацепта, абциксимаба, абитузумаба, абрилумаба, актоксумаба, адалимумаба, адекатумаба, адуканумаба, афлиберцепта, афутузимаба, алацизумаба, алефацепта, алемтузумаба, алирокумаба, альтумомаба, аматиксумаба, анатумомаба, анетумаба, анифромумаба, анрукинзумаба, аполизумаба, арцитумомаба, аскринвакумаба, азелизумаба, атезолизумаба, атинумаба, альтизумаба, аторолимумаба, бапинейзумаба, базиликсимаба, бавитуксимаба, бектумомаба, бегеломаба, белатацепта, белимумаба, бенрализумаба, бертилимумаба, бесилезомаба, бевацизумаба, безлотоксумаба, бицирумаба, бимагрумаба, бимекизумаба, биватузумаба, блинатумумаба, блосозумаба, бокоцизумаба, брентуксимаба, бриакимумаба, бродалумаба, бролуцизумаба, бронтицизумаба, канакинумаба, кантузумаба, каплацизумаба, капромаба, карлумаба, катумаксомаба, цеделизумаба, цетролизумаба, цетиксумаба, цитатузумаба, циксутумумаба, клазакизумаба, кленоликсимаба, кливатузумаба, кодритузумаба, колтуксимаба, конатумумаба, концизумаба, кренезумаба, дацетузумаба, даклизумаба, далотузумаба, дапиролизумаба, даратумимаба, дектрекумаба, демцизумаба, денинтузумаба, деносумаба, дерлотиксумаба, детумомаба, динутуксимаба, диридавумаба, дорлиномаба, дрозитумаба, дупилумаба, дурвалумаба, дузигитумаба, экромексимаба, экулизумаба, эдобакомаба, эдреколомаба, эфализумаба, эфунгумаба, элделумаба, элгемтумаба, элотузумаба, элсилимомаба, эмактузумаба, эмибетузумаба, энаватузумаба, энфортумаба, энлимомаба, эноблитузумаба, энокизумаба, энотикумаба, энситуксимаба, эпитумомаба, эпратозумаба, эрлизумаба, эртумаксомаба, этанерцепта, этарацизумаба, 'этролизумаба, эвинакумаба, эволокумаба, эксбивирумаба, фанолезомаба, фаралимомаба, фарлетузомаба, фазимумаба, фелвизумаба, фезкимумаба, фиклатузумаба, фигитумумаба, фиривумаба, фланвотумаба, флетикумаба, фонтолизумаба, форалумаба, форавирумаба, фрезолимумаба, фулрамумаба, футуксимаба, галиксимаба, ганитумаба, гантенерумаба, гавилимомаба, гемтузумаба, гевокизумаба, гирентуксимаба, глембатумумаба, голимумаба, гомиликсимаба, гуселькумаба, ибализумаба, ибритумомаба, икрукумаба, идаруцизумаба, иговомаба, ималумаба, имкиромаба, имгатузумаба, инклакумаба, индатуксимаба, индусатумаба, инфликсимаба, интетумумаба, инолимомаба, инотузумаба, ипилимумаба, иратумумаба, исатуксимаба, итолизумаба, иксекизумаба, келиксимаба, лабетузумаба, ламбролизумаба, лампализумаба, лебрикизумаба, лемалесомаба, лензилумаба, лерделимумаба, лексатумумаба, либивирумаба, лифастузумаба, лигелизумаба, лилотомаба, линтузумаба, лирилумаба, лодельцизумаба, локиветмаба, лорвотузумаба, лукатумумаба, лулизумаба, люмиликсимаба, лумретузумаба, мапатумумаба, маргетуксимаба, маслимомаба, маврилимумаба, матузумаба, меполизумаба, метелимумаба, милатузумаба, минэтумумаба, мирветуксимаба, митумомаба, могамулизумаба, моролимумаба, мотавизумаба, моксетумомаба, муромонаба CD3, наколомаба, намилумаба, наптумомаба, нарнатумаба, натализумаба, небацумаба, нецитузумаба, немолизумаба, нерелимомаба, несвакумаба, нимотузумаба, ниволумаба, нофетумомаба, обилтоксаксимаба, обинутузумаба, окаратузумаба, окрелизумаба, одулимомаба, офатумумаба, оларатумаба, олокизумаба, омализумаба, онартузумаба, онтуксизумаба, опицинумаба, опортузумаба, ореговомаба, ортикумаба, отеликсизумаба, олтертузумаба, окселумаба, озанезумаба, озорализумаба, пагибаксимаба, паливизумаба, панитумумаба, панкомаба, панобакумаба, парсатузумаба, пасколизумаба, пасотуксизумаба, патеклизумаба, патритумаба, пембролизумаба, пемтумомаба, перакизумаба, пертузумаба, пекселизумаба, пидилизумаба, пинатузумаба, пинтумомаба, полатузумаба, понезумаба, приликсимаба, притумумаба, квилизумаба, ракотумомаба, радретумаба, рафивирумаба, ралпанцизумаба, рамуцирумаба, ранибизумаба, раксибакумаба, рефанезумаба, регавирумаба, резлизумаба, рилонацепта, рилотумумаба, ринукумаба, ритуксимаба, робатумумаба, роледумаба, ромосозумаба, ронтализумаба, ровелизумаба, руплизумаба, сацитузумаба, самализумаба, сарилумаба, сатумомаба, секукимумаба, серибантумаба, сетоксаксимаба, севирумаба, сибротузумаба, сифалимумаба, силтуксимаба, сиплизумаба, сирукумаба, софитузумаба, соланезумаба, солитомаба, сонепцизумаба, сонтузумаба, стамулумаба, сулесомаба, сувизумаба, табалумаба, такатузумаба, тадоцизумаба, тализумаба, танезумаба, таплитумомаба, тарекстумаба, тефибазумаба, телимомаб аритокса, тенатумомаба, тенеликсимаба, теплизумаба, тезидолумаба, TGN 1412, тиклимумаба, тилдракизумаба, тигатузумаба, TNX-650, тоцилизумаба, торализумаба, тосатоксумаба, тоситимумаба, товетумаба, тралокимумаба, трастузумаба, ТРБС07, трегализумаба, тремелимумаба, тревогрумаба, тукотузумаба, тувирумаба, ублитуксимаба, улокуплумаба, урелумаба, уртоксазумаба, устекимумаба, вандортуцумаба, вандиктумаба, вануцизумаба, вапаликсимаба, варлимумаба, вателизумаба, ведолизумаба, велтузумаба, вепалимомаба, весенкумаба, визилизумаба, волоциксумаба, ворсетузумаба, вотумумаба, залутумимаба, занолимумаба, затуксимаба, зиралимумаба, зив-афлиберцепта и золимомаба;
- Ингибиторы топоизомеразы, такие как доксорубицин, даунорубицин, дактиномицин, энипозид, эпирубицин, этопозид, идарубицин, иринотекан, митоксантрон, топотекан и иринотекан;
- Токсины, такие как холерный токсин, рицин, экзотоксин из Pseudomonas, аденилатциклазный токсин из Bordetella pertussis, дифтерийный токсин и активаторы каспаз;
Ингибиторы киназы или VEGF, такие как регорафениб (Stivarga®, Bayer); вандетаниб (Caprelsa®, AstraZeneca); акситиниб (Inlyta®, Pfizer); и ленватиниб (Lenvima®, Eisai); ингибиторы Raf, такие как сорафениб (Nexavar®, Bayer AG и Onyx); дабрафениб (Tafinlar®, Novartis); и вемурафениб (Zelboraf®, Genentech/Roche); ингибиторы MEK, такие как кобиметаниб (Cotellic®, Exelexis/Genentech/Roche); траметиниб (Mekinist®, Novartis); ингибиторы тирозинкиназы Bcr-Abl, такие как иматиниб (Gleevec®, Novartis); нилотиниб (Tasigna®, Novartis); дазатиниб (Sprycel®, BristolMyersSquibb); босутиниб (Bosulif®, Pfizer); и понатиниб (Inclusig®, Ariad Pharmaceuticals); ингибиторы Her2 и EGFR, такие как гефитиниб (Iressa®, AstraZeneca); эрлотиниб (Tarceeva®, Genentech/Roche/Astellas); лапатиниб (Tykerb®, Novartis); афатиниб (Gilotrif®, Boehringer Ingelheim); осимертиниб (активированный EGFR, Tagrisso®, AstraZeneca); и бригатиниб (Alunbrig®, Ariad Pharmaceuticals); ингибиторы c-Met и VEGFR2, такие как кабозанитиб (Cometriq®, Exelexis); и мультикиназные ингибиторы, такие как сунитиниб (Sutent®, Pfizer); пазопаниб (Votrient®, Novartis); ингибиторы ALK, такие как кризотиниб (Xalkori®, Pfizer); церитиниб (Zykadia®, Novartis); и алектиниб (Alecenza®, Genentech/Roche); ингибиторы тирозинкиназы Брутона, такие как ибрутиниб (Imbruvica®, Pharmacyclics/Janssen); и ингибиторы рецепторов Flt3, такие как мидостаурин (Rydapt®, Novartis), тивозаниб (Aveo Pharmaecuticals); ваталаниб (Bayer/Novartis); луцитаниб (Clovis Oncology); довитиниб (TKI258, Novartis); Чиауаниб (Chipscreen Biosciences); CEP-11981 (Cephalon); линифаниб (Abbott Laboratories); нератиниб (HKI-272, Puma Biotechnology); радотиниб (Supect®, IY5511, Il-Yang Pharmaceuticals, S. Korea); руксолитиниб (Jakafi®, Incyte Corporation); PTC299 (PTC Therapeutics); CP-547,632 (Pfizer); форетиниб (Exelexis, GlaxoSmithKline); квизартиниб (Daiichi Sankyo) и мотесаниб (Amgen/Takeda);
Неограничивающим образом соединения данного изобретения могут быть объединены, по отдельности или в форме набора из частей, с одним или более из следующих противораковых препаратов или соединений: ABVD, AC, ACE, Абиратерон(Zytiga®), абраксан, абстрал, актиномицин D, актик, адриамицин, афатиниб (Giotrif®), афинитор, афлиберцепт(Zaltrap®), алдара, алдеслейкин (IL-2, пролейкин или интерлейкин 2), алемтузумаб (MabCampath), алкеран, амсакрин (Amsidine, m-AMSA), амсидин, анастрозол (Arimidex®), Ара C, аредия, аримидекс, аромазин, трехокись мышьяка (Trisenox®, ATO), аспарагиназа (Crisantaspase®, Erwinase®), акситиниб (Inlyta®), азацитидин (Vidaza®), BEACOPP, BEAM, бендамустин (Levact®), бевацизумаб (Avastin), бексаротен (Targretin®), бикалутамид (Casodex®), блеомицин, этопозид и платина (BEP), бортезомиб (Velcade®), босулиф, босутиниб (Bosulif), брентуксимаб (Adcetris®), бруфен, бусерелин (Suprefact®), бусильвекс, бусульфан (Myleran, Busilvex), CAPE-OX, CAPOX, CAV, CAVE, CCNU, CHOP, CMF, CMV, CVP, кабацитаксел (Jevtana®), кабозантимиб (Cometriq®), каэликс, калпол, кампто, капецитабин (Xeloda®), капрельса, карбо МВ (Carboplatin, methotrexate, vinblastin), карботаксол, карбоплатин, карбоплатин и этопозид, карбоплатин и паклитаксель, кармустин (BCNU, Gliadel®), казодекс, церитиниб (Zykadia®), церубидин, цетуксимаб (Erbitux®), ChlVPP, хлорамбуцил(Leukeran®), цисплатин, цисплатин и тейсуно, цисплатин и капецитабин (CX), цисплатин, этопозид и ифосфамид (PEI), цисплатин, фтотрурацил (5-FU) и трастузумаб, кладрибин (Leustat®, LITAK), кластеон, клофарабин (Evoltra®), ко-кодамол (Kapake®, Solpadol®, Тилекс®), кометрик, космеген, кризантаспаза, кризотиниб (Xalkori®), циклофосфамид, талидомид и дексаметазон (CTD), ципростат, ципротерон ацетат (Cyprostat®), цитарабин (Ara C, цитозина арабинозид), цитарабин в спинномозговую жидкость, цитозин арабинозид, DHAP, DTIC, дабрафениб (Tafinlar®), дакарбазин (DTIC), дакоген, дактиномицин (актиномицин D, Cosmegen®), дасатиниб (Sprycel), даунорубицин, De Gramont, декапептил SR, децитабин (Dacogen®), дегареликс (Firmagon®), деносумаб (Prolia®, Xgeva®), депоцит, дексаметазон, диаморфин, динатрия памидронат, диспрол, доцетаксел (Taxotere®), доцетаксел, цисплатин и фторурацил (TPF), доксифос, доксил, доксорубицин (адриамицин), доксорубицин и ифосфамид (Доксифос), дрогенил, дюрогезик, EC, ECF, EOF, EOX, EP, ESHAP, эффентора, эфудикс, элдизин, элоксатин, энзалутамид, эпирубицин (Pharmorubicin®), эпирубицин цисплатин и капецитабин (ECX), эпирубицин, карбоплатин и капецитабин (ECarboX), эпозин, эрбитукс, эрибулин (Halaven®), эрлотиниб (Tarceva®), эрвиназа, эстрацит, этопофос, этопозид (Eposin®, Etopophos®, Vepesid®), эверолимус (Afinitor®), эволтра, экземестан (Aromasin®), FAD, FEC, FEC-T хемотерапия, FMD, FOLFIRINOX, FOLFOX, фаслодекс, фемара, фентанил, фирмагон, флудара, флударабин (Fludara®), флударабин, циклофосфамид и ритуксимаб (FCR), фторурацил (5FU), флутамид, фолиновая кислота, фторурацил и иринотекан (FOLFIRI), фульвестрант(faslodex®), G-CSF, гефитиниб (Iressa), ГемКарбо (гемцитиниб и карбоплатин), ГемТаксол, гемцитабин (Gemzar), Гемцитабин и капецитабин (ГемКап), Гемцитабин и цисплатин (GC), Гемцитабин и паклитаксел (GemTaxol®), гемза, гиотриф, глиадел, гливек, гонапептил, депо, госерелин (Zoladex®), госерелин (Zoladex®, Novgos®), фактор стимулирующий гранулоцитарные колонии (G-CSF), галавен, герцептин, гикамтин, гидреа, гидроксикарбамид (Hydrea®), гидроксимочевина, I-DEX, ICE, IL-2, IPE, ибандроновая кислота, ибритумомаб (Zevalin®), ибрутиниб (Imbruvica®), ибупрофен (Brufen®, Nurofen®), иклюсиг, идарубицин (Zavedos®), идарубицин и дексаметазон, иделалисиб (Zydelig®), ифосфамид (Mitoxana®), иматиниб (Glivec®), крем имиквимод (Aldara®), имновид, инстанил, интерферон (Intron A), интерлейкин, интрон A, ипилимумаб (Yervoy®), Иресса, иринотекан (Campto®), иринотекан и капецитабин (Xeliri®), иринотекан де Грамона, иринотекан модифицированный де Грамоном, явлор, евтана, кадцила, капаке, кейтруда, ланреотид(Somatuline®), ланвис, лапатиниб (Tyverb®), леналидомид (Revlimid®), летрозол (Femara®), лейкеран, лейпрорелин (Prostap®, Lutrate®), лейстат, левакт, липосомальный доксорубицин, литак, ломустин (CCNU), линпарза, лизодрен, MIC, MMM, MPT, MST континус, MVAC, MVP, MabCampath, мабтера, макстрекс, медроксипрогестерон ацетат (Provera), мегейс, мегестрол ацетат(Megace®), мелфалан (Alkeran®), мепакт, меркаптопурин (Xaluprine®), метотрексат (Maxtrex), метил преднизолон, мифамуртид (Mepact®), митомицин C, митотан, митоксана, митоксантрон (Mitozantrone®), морфгесик СР, морфин, милеран, миоцет, Наб-паклитаксел, Наб-паклитаксел (Abraxane®), навелбин, неларабин (Atriance®), нексавар, нилотиниб(Tasigna®), нинтеданиб (Vargatef®), нипент, ниволумаб (Opdivo®), новгос, нурофен, обинутузумаб (Gazyvaro®), октреотид, офатумумаб (Arzerra®), олапариб (Lynparza®), онковин, онкотрон, опдиво, ораморф, оксалиплатин (Eloxatin), оксалиплатин и капецитабин (Xelox®), PAD, PC (паклитаксел и карбоплатин, карботаксол), PCV, PE, PMitCEBO, POMB/ACE, паклитаксел (Taxol®), паклитаксел и карбоплатини, памидронат, панадол, панитумумаб (Vectibix®), парацетамол, пазопаниб (Votrient®), пембролизумаб (Keytruda), пеметрексед (Alimta®), пеметрексед и карбоплатин, пеметрексед и цисплатин, пентостатин (Nipent®), перьета, пертузумаб (Perjeta®), пиксантрон (Pixuvri®), пиксуври, помалидомид (Imnovid®), понатиниб, потактазол, преднизолон, прокарбазин, пролейкин, пролиа, простап, провера, пуринетол, R-CHOP, R-CVP, R-DHAP, R-ESHAP, R-GCVP, RICE, ралоксифен, ралтитрексед (Tomudex®), регорафениб (Stivarga®), ревлимид, ритуксимаб, (Mabthera®), севердол, натрия клодронат (Bonefos®, Clasteon®, Loron®), солпадол, сорафениб (Nexavar®), стероиды (дексаметазон, преднизолон, метилпреднизолон), стрептозоцин (Zanosar®), сунитиниб (Sutent®), сутент, TAC, TIP, тафинлар, тамоксифен, тарцева, таргретин, тасигна, таксол, таксотер, таксотер и циклофосфамид (TC), темодал, темозоломид, (Temodal®), темсиролимус (Torisel®), тепадина, тейсуно, талидомид, тиотепа (Tepadina®), тиогуанин (тиогуанин®, 6-TG, 6-тиогуанин), томудекс, топотекан (гикамтин, протактазол), торисел, трабактедин (Yondelis), трастузумаб (Herceptin®), трастузумаб эмтанзин (Kadcyla®), тресульфан, третиноин (Vesanoid®, ATRA), трипторелин (Decapeptyl SR®, Gonapeptyl Depot®), трисенокс, тилекс, тиверб, VIDE, вандетаниб (Caprelsa®), варгатеф, VeIP, вектибикс, вельбе, велькаде, вемурафениб (Zelboraf®), вепесид, весаноид, видаза, винбластин (Velbe®), винкристин, винкристин, актиномицин D (dactinomycin®) и циклофосфамид (VAC), винкристин, актиномицин и ифосфамид (VAI), винкристин, доксорубицин и дексаметазон (VAD), виндезин (Eldisine®), винфлунин (Javlor®), винорелбин (Navelbine®), висмодегиб (Erivedge®), вотриент, кселокс, ксалкори, кселода, иксгева, исктанди, ервой, йонделис, Z-DEX, залтрап, заносар, заведос, зелбораф, зевалин, золадекс (рак молочной железы), золадекс (рак предстательной железы), золедроновая кислота (Zometa®), зомета, зоморф, зиделиг, зитига.
Согласно частному варианту осуществления, соединение или любой из его или метаболитов или его фармацевтически приемлемая соль, как описано в настоящем документе, могут быть объединены с различными видами терапии: химиотерапии, иммунотерапии (например, ингибиторами, моноклональными антителами), противоопухолевыми вакцинами, РНК-вакцинами, магнитными частицами, внутрисосудистыми микророботами, радиотерапией, хирургией, ультразвуковой или другими видами противоопухолевой терапии.
Следовательно, настоящее изобретение дополнительно обеспечивает соединение формулы (I) или (I’) или любой из его метаболитов или его фармацевтически приемлемую соль для применения в качестве противоопухолевого агента, предназначенного для пациентов, которые также проходят лечение любым способом из иммунотерапии, противоопухолевых вакцин, РНК-вакцин, радиотерапии, хирургии, ультразвуковой терапии или других противоопухолевых методов лечения.
Там, где обеспечен способ предупреждения и/или лечения, настоящее изобретение также обеспечивает соответствующее применение для предупреждения и/или лечения рака или дисплазии. Аналогичным образом, если обеспечено применение для предупреждения и/или лечения рака или дисплазии, настоящее изобретение также обеспечивает соответствующий способ предупреждения и/или лечения. В некоторых вариантах осуществления настоящее изобретение обеспечивает способ предупреждения и/или лечения рака или дисплазии, как описано в настоящем описании, включающий введение соединения или его фармацевтически приемлемой соли, как описано в настоящем описании. В некоторых вариантах осуществления настоящее изобретение обеспечивает способ предупреждения и/или лечения рака или дисплазии, как описано в настоящем документе, включающий измерение присутствия и/или уровня экспрессии miR-124, как описано в настоящем документе.
В настоящем документе дополнительно представлено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения в соответствии с настоящим изобретением, где применение предназначено для пациента, у которого уровень соединения формулы (I’) или его фармацевтически приемлемой соли в образцах крови, плазмы, ткани, слюны и/или сыворотки пациента измеряется во время применения.
В настоящем документе дополнительно обеспечено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения согласно настоящему изобретению, где применение предназначено для пациента, у которого уровень соединения формулы (IVa) или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента измеряется во время применения.
В настоящем документе дополнительно предложено производное хинолина формулы (I’) или любой из его метаболитов или фармацевтически приемлемая соль или любой из их энантиомеров или диастереоизомеров для применения согласно настоящему изобретению, где применение предназначено для пациента, у которого уровень соединения формул (I’) и (IVa) или их фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента измеряется во время применения.
Дополнительные примеры вариантов осуществления
1. Соединение Формулы (I):
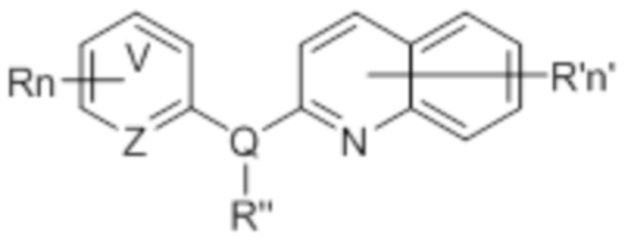 (I)
(I)
или его фармацевтически приемлемую соль, где:
Z представляет собой C или N;
V представляет собой C или N;
 означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, V находится в орто, мета или пара положении относительно Z;
означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, V находится в орто, мета или пара положении относительно Z;
каждый R независимо представляет собой водород, галоген, -CN, гидроксил, (C1-C3)фторалкил, (C1-C3)фторалкокси, (C3-C6)циклоалкил, -NO2, -NR1R2, (C1-C4)алкокси, фенокси, -NR1-SO2-NR1R2, -NR1-SO2-R1, -NR1-C(=O)-R1, -NR1-C(=O)-NR1R2, -SO2-NR1R2, -SO3H, -O-SO2-OR3, -O-P(=O)-(OR3)(OR4), -O-CH2-COOR3, (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой, группу формулы (IIa):  , или группу формулы (IIIa):
, или группу формулы (IIIa):  ;
;
Q представляет собой N или O, при условии, что R” отсутствует, когда Q представляет собой O;
каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил;
каждый из R3 и R4 независимо представляет собой водород, Li+, Na+, K+, N+(Ra)4 или бензил;
n представляет собой 1, 2 или 3;
n’ представляет собой 1, 2 или 3;
каждый R’ независимо представляет собой водород, (C1-C3)алкил, гидроксил, галоген, -NO2, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3)фторалкил, (C1-C4)алкокси, -O-P(=O)-(OR3)(OR4), -CN, группу формулы (IIa):  , или группу формулы (IIIa):
, или группу формулы (IIIa):  ;
;
А представляет собой ковалентную связь, кислород или NH;
B представляет собой ковалентную связь или NH;
m представляет собой 1, 2, 3, 4 или 5;
p представляет собой 1, 2 или 3;
каждый из Ra и Rb независимо представляет собой водород, (C1-C5)алкил или (C3-C6)циклоалкил, или
Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ представляет собой группу (IIa) или (IIIa), n’ может представлять собой 2 или 3, только если другие R’ группы отличаются от указанной группы (IIa) или (IIIa); и
R” представляет собой водород, (C1-C4)алкил или группу формулы (IIa), как определено в настоящем описании,
для применения для лечения или предупреждения рака или дисплазии.
2. Соединение варианта осуществления 1, где соединение имеет формулу (Ia):
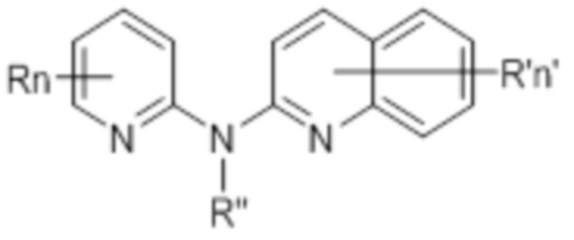 (Ia)
(Ia)
или его фармацевтически приемлемую соль.
3. Соединение варианта осуществления 1, где соединение имеет формулу (Ib):
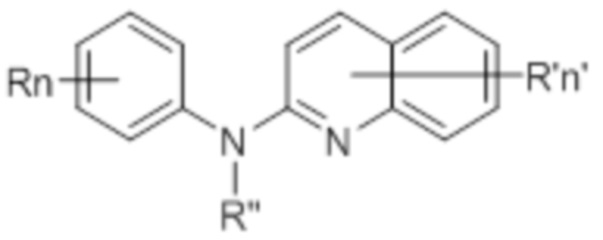 (Ib)
(Ib)
или его фармацевтически приемлемую соль.
4. Соединение варианта осуществления 1, где соединение имеет формулу (Ic):
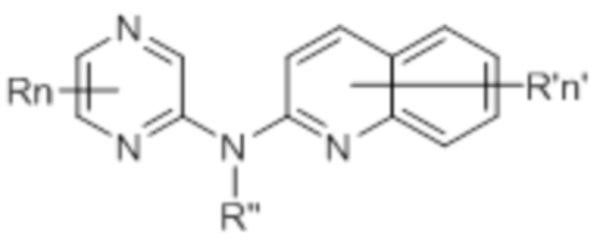 (Ic)
(Ic)
или его фармацевтически приемлемую соль.
5. Соединение варианта осуществления 1, где соединение имеет формулу (Ib’):
 (Ib’)
(Ib’)
или его фармацевтически приемлемую соль.
6. Соединение варианта осуществления 1, где соединение имеет формулу (Id):
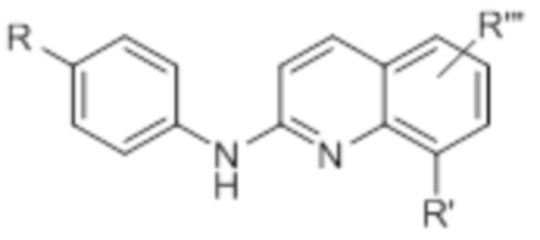 (Id)
(Id)
или его фармацевтически приемлемую соль.
7. Соединение формулы (IV):
 (IV)
(IV)
или его фармацевтически приемлемая соль, где каждая из переменных V, Z, R, R’, n и n’ является такой, как описано в варианте осуществления 1 для применения для лечения или предупреждения рака или дисплазии.
8. Соединение варианта осуществления 7, где соединение имеет формулу (IVa):
 (IVa)
(IVa)
или его фармацевтически приемлемая соль.
9. Соединение варианта осуществления 7, где соединение имеет формулу (IVb):
 (IVb)
(IVb)
или его фармацевтически приемлемая соль.
10. Соединение варианта осуществления 7, где соединение имеет формулу (IVc):
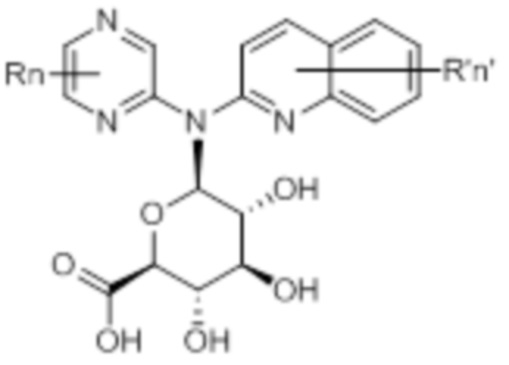 (IVc)
(IVc)
или его фармацевтически приемлемая соль.
11. Соединение варианта осуществления 7, где соединение имеет формулу (IVb’):
 (IVb’)
(IVb’)
или их фармацевтически приемлемую соль.
12. Соединение варианта осуществления 7, где соединение имеет формулу (IVd):
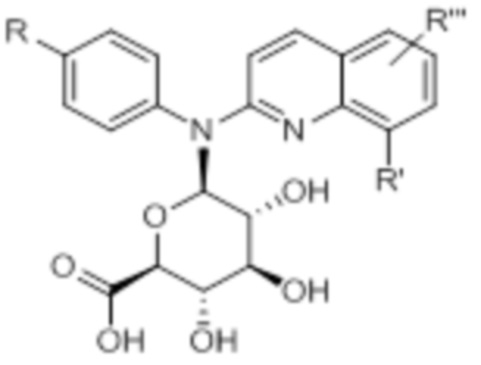 (IVd)
(IVd)
или его фармацевтически приемлемая соль.
13. Соединение для применения согласно люблму из вариантов осуществления 1-12, где применение предназначено для пациента, у которого уровень соединения формулы (I) или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента измеряют во время применения.
14. Соединение для применения в соответствии с любым из вариантов осуществления 1-13, где применение предназначено для пациента, у которого уровень соединения формулы (IV) или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента измеряют во время применения.
15. Соединение для применения в соответствии с любым из вариантов осуществления 1-14, где применение предназначено для пациента, у которого уровень соединений формулы (I) и (IV) или их фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента измеряют во время применения.
16. Соединение для применения в соответствии с любым из вариантов осуществления 1-15, где применение предназначено для пациента, у которого до и во время применения измеряют наличие и/или уровень экспрессии miR-124 в образце крови и/или ткани пациента.
17. Соединение для применения в соответствии с любым из вариантов осуществления 1-16, где применение предназначено для пациента, выбранного по измеренному наличию и/или уровню экспрессии miR-124 в образце крови и/или ткани пациента.
18. Соединение для применения в соответствии с любым из вариантов осуществления 1-17, где алгоритм, объединяющий уровень miR-124 и цитокиновый уровень или уровень другого биомаркера, используют для мониторинга тяжести заболевания, нарушения или состояния и/или для мониторинга эффективности применения.
19. Соединение для применения в соответствии с любым из вариантов осуществления 1-18, где алгоритм, сочетающий уровень miR-124 и цитокиновый уровень или уровень другого биомаркера, используют для отбора пациентов для применения.
20. Алгоритм, который объединяет уровень miR-124 и уровень цитокинов или другого биомаркера для мониторинга тяжести рака или дисплазии и/или для мониторинга эффективности лечения.
21. Способ лечения рака или дисплазии у пациента, нуждающегося в этом, включающий введение пациенту соединения формулы (I):
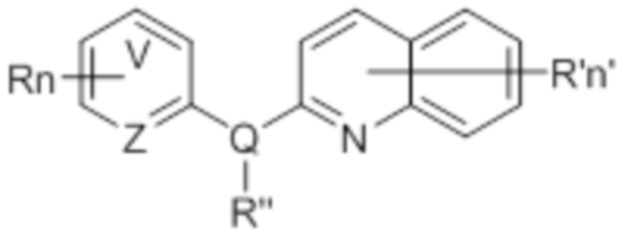 (I)
(I)
или его фармацевтически приемлемую соль, где:
Z представляет собой C или N;
V представляет собой C или N;
 означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, V находится в орто, мета или пара положении относительно Z;
означает ароматическое кольцо, где V представляет собой C или N, и когда V представляет собой N, V находится в орто, мета или пара положении относительно Z;
каждый R независимо представляет собой водород, галоген, -CN, гидроксил, (C1-C3)фторалкил, (C1-C3)фторалкокси, (C3-C6)циклоалкил, -NO2, -NR1R2, (C1-C4)алкокси, фенокси, -NR1-SO2-NR1R2, -NR1-SO2-R1, -NR1-C(=O)-R1, -NR1-C(=O)-NR1R2, -SO2-NR1R2, -SO3H, -O-SO2-OR3, -O-P(=O)-(OR3)(OR4), -O-CH2-COOR3, (C1-C3)алкил, причем указанный алкил необязательно моно- или дизамещен гидроксильной группой или группу формулы (IIa):  , или группу формулы (IIIa):
, или группу формулы (IIIa):  ;
;
Q представляет собой N или O, при условии, что R” отсутствует, когда Q представляет собой O;
каждый из R1 и R2 независимо представляет собой водород или (C1-C3)алкил;
каждый из R3 и R4 независимо представляет собой водород, Li+, Na+, K+, N+(Ra)4 или бензил;
n представляет собой 1, 2 или 3;
n’ представляет собой 1, 2 или 3;
каждый R’ независимо представляет собой водород, (C1-C3)алкил, гидроксил, галоген, -NO2, -NR1R2, морфолинил, морфолино, N-метилпиперазинил, (C1-C3)фторалкил, (C1-C4)алкокси, -O-P(=O)-(OR3)(OR4), -CN, группу формулы (IIa):  , или группу формулы (IIIa):
, или группу формулы (IIIa):  ;
;
А представляет собой ковалентную связь, кислород или NH;
B представляет собой ковалентную связь или NH;
m представляет собой 1, 2, 3, 4 или 5;
p представляет собой 1, 2 или 3;
каждый из Ra и Rb независимо представляет собой водород, (C1-C5)алкил или (C3-C6)циклоалкил, или
Ra и Rb образуют вместе с атомом азота, к которому они присоединены, насыщенный 5- или 6-членный гетероцикл, причем указанный гетероцикл необязательно замещен одним или более Ra, при условии, что, когда R’ представляет собой группу (IIa) или (IIIa), n’ может представляет собой 2 или 3, только если другие R’ группы отличаются от указанной группы (IIa) или (IIIa); и
R” представляет собой водород, (C1-C4)алкил или группу формулы (IIa), как определено в настоящем документе.
22. Способ осуществления 21, где соединение имеет формулу (Ia):
 (Ia)
(Ia)
или его фармацевтически приемлемая соль.
23. Способ осуществления 21, где соединение имеет формулу (Ib):
 (Ib)
(Ib)
или его фармацевтически приемлемую соль.
24. Способ осуществления 21, где соединение имеет формулу (Ic):
 (Ic)
(Ic)
или его фармацевтически приемлемая соль.
25. Способ осуществления 21, где соединение имеет формулу (Ib’):
 (Ib’)
(Ib’)
или его фармацевтически приемлемая соль.
26. Способ осуществления 21, где соединение имеет формулу (Id):
 (Id)
(Id)
или его фармацевтически приемлемая соль.
27. Способ лечения рака или дисплазии у пациента, нуждающегося в этом, включающий введение пациенту соединения формулы (IV):
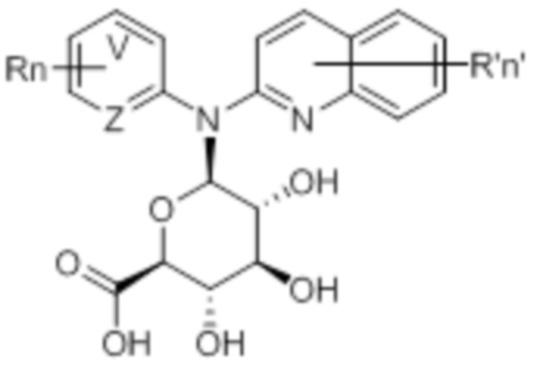 (IV)
(IV)
или его фармацевтически приемлемой соли, где каждая из переменных V, Z, R, R’, n и n’ является такой, как описано в варианте осуществления 21.
28. Способ осуществления 27, где соединение имеет формулу (IVa):
 (IVa)
(IVa)
или его фармацевтически приемлемая соль.
29. Способ осуществления 27, где соединение имеет формулу (IVb):
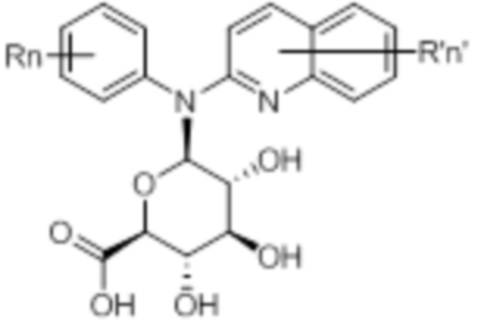 (IVb)
(IVb)
или его фармацевтически приемлемая соль.
30. Способ осуществления 27, где соединение имеет формулу (IVc):
 (IVc)
(IVc)
или его фармацевтически приемлемая соль.
31. Способ осуществления 27, где соединение имеет формулу (IVb’):
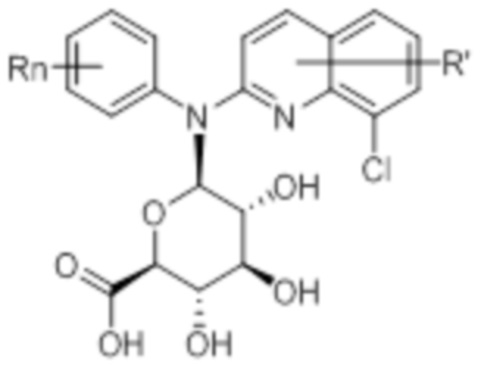 (IVb’)
(IVb’)
или его фармацевтически приемлемая соль.
32. Способ осуществления 27, в котором соединение имеет формулу (IVd):
 (IVd)
(IVd)
или его фармацевтически приемлемая соль.
33. Способ любого из вариантов осуществления с 21 по 32, дополнительно включающий измерение уровня соединения формулы I или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
34. Способ любого из вариантов осуществления с 21 по 33, дополнительно включающий измерение уровня соединения формулы IV или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
35. Способ любого из вариантов осуществления с 21 по 34, дополнительно включающий измерение общего уровня соединений формул I и IV или их фармацевтически приемлемых солей в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
36. Способ любого из вариантов осуществления с 21 по 35, дополнительно включающий измерение наличия и/или уровня экспрессии miR-124 в образце крови и/или ткани пациента до и во время лечения.
37. Способ любого из вариантов осуществления с 21 по 36, дополнительно включающий отбор пациента по измеренному наличию и/или уровню экспрессии miR-124 в образце крови и/или ткани пациента.
38. Способ любого из вариантов осуществления с 21 по 37, дополнительно включающий использование алгоритма, который сочетает уровень miR-124 и уровень цитокинов или другого биомаркера для мониторинга тяжести рака или дисплазии и/или для мониторинга эффективности лечения.
39. Способ любого из вариантов осуществления с 21 по 38, дополнительно включающий использование алгоритма, который сочетает уровень miR-124 и уровень цитокинов или другого биомаркера для отбора пациентов для лечения.
40. Алгоритм, который объединяет уровень miR-124 и уровень цитокинов или другого биомаркера для мониторинга тяжести рака или дисплазии и/или для мониторинга эффективности лечения.
41. Способ любого из вариантов с 21 по 40, дополнительно включающий измерение уровня соединения формулы (I) или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
42. Способ любого из вариантов осуществления с 21 по 40, дополнительно включающий измерение уровня соединения формулы (IV) или его фармацевтически приемлемой соли в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
43. Способ любого из вариантов осуществления с 21 по 40, дополнительно включающий измерение общего уровня соединений формул (I) и (IV) или их фармацевтически приемлемых солей в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
ПРИМЕРЫ
МАТЕРИАЛ И МЕТОДЫ
Материал и реагенты
Все клеточные линии являются первичными клеточными линиями человека, культивируемыми в среде DMEM/F12 + 10% FBS + дополнительные факторы роста при 37°C с 5% CO2, как объяснено ниже. Клеточные линии происходят из толстой кишки/прямой кишки, желудка, печени, легких или поджелудочной железы (см. таблицу ниже).
• DMEM/F12 (с высоким содержанием глюкозы) (Gibco, Cat#11320033)
• FBS (Cat#FND500, ExCell Bio)
• Люминесцентный анализ жизнеспособности клеток CellTiter-Glo® (Cat#G7571, Promega. температура хранения при -20°C).
• планшет 96 луночный (Cat#3610, Corning)
• DMEM/F12 medium (с низким содержанием глюкозы): смесь 1:1 среды DMEM (с низким содержанием глюкозы) (Gibco, Cat#11885076) и F-12K (Gibco, Cat#21127022)
Испытуемые соединения
1. Соединение 111 согласно изобретению:
Используют 20 мг соединения 111 (также называемого ABX464) (MW=338,7 г/моль, чистота = 100%). Данное соединение хранят при комнатной температуре (18-25°C), и растворителем был ДМСО.

2. Сравниваемое соединение 26: 8-хлор-N-(5-(трифторметил)пиридин-2-ил)хинолин-2-амин
Соединение 26 представляет собой соединение, которое относится к формуле (Ia), определенной в настоящем изобретении и в заявке WO 2010/143168 (под названием соединения 37).
Используют 20 мг соединения 26 (MW=323,71 г/моль, чистота = 100%). Данное соединение хранят при комнатной температуре (18-25°C), и растворителем был ДМСО.
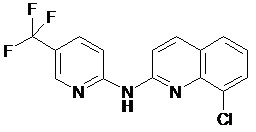
Для соединения 26 были протестированы два типа клеточных линий, а именно CR3085 (толстая кишка/колоректум) и GA0060 (желудок), как показано ниже.
Оборудование
BMRP004; CO2-инкубатор, SANYO Electric Co., Ltd (02100400059).
Инвертированный микроскоп, Chongguang XDS-1B, Chongqing Guangdian Corp. (TAMIC0200)
Многоканальный прибор Envision (TAREA0011)
Vi-Cell XR, Beckman Coulter (TACEL0030)
Способ
День 1: Засев клеток
1. Каждая лунка 96-луночного планшета содержит 90 мкл клеточной суспензии с клетками. Количество клеток для засева определяется на основе оптимизированного анализа плотности клеток.
2. Все 96-луночные планшеты с клетками помещают в инкубатор на ночь при 37°C с 5% CO2.
День 2: Обработка соединением
3. ABX464 разбавляют и добавляют 10 мкл/лунку ABX464 в указанных концентрациях (см. схему планшета ниже). Конечный объем составляет 100 мкл/лунку.
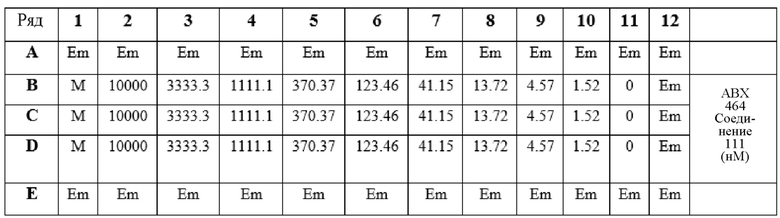
Em (Empty): Пустая лунка, содержащая PBS
M: Контроль среды (бланк)
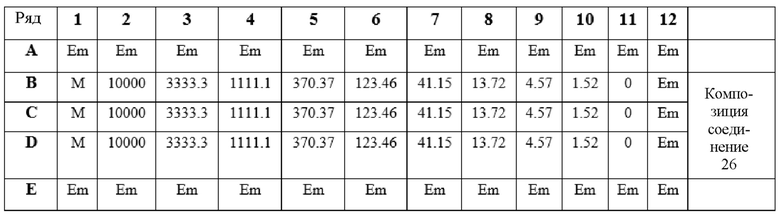
Em (Empty): Пустая лунка, содержащая PBS
M: Контроль среды (бланк)
День 5: Восполнение лекарственного средства/среды
4. Заменить старую среду предварительно подготовленной свежей средой с ABX464 в тех же указанных концентрациях. Конечный объем составляет 100 мкл/лунку.
День 9: Считывание планшета (7 дней обработки лекарственным средством)
5. Клетки наблюдают под микроскопом, убеждаясь в том, что клетки, обработанные контрольной средой, в хорошем состоянии.
6. Добавляют 50 мкл реагента CellTiter-Glo® в каждую лунку.
7. Смешивают содержимое в течение 2 минут на орбитальном шейкере для облегчения лизиса клеток.
8. Дают планшету инкубироваться при комнатной температуре в течение 10 минут для стабилизации люминесцентныых сигналов.
9. Записывают люминесценцию с помощью многоканального ридера EnVision.
Анализ данных
Анализ данных выполняется с помощью GraphPad Prism 7.0.
Для расчета IC50 кривая дозозависимого ответа генерируется с использованием нелинейной регрессионной модели с сигмовидным дозозависимым ответом. Формула выживаемости показана ниже, и IC50 будет автоматически сгенерирована программой GraphPad Prism 7.0.

Разница "Люм Необработ - ЛюмКонтрсреды" установлена как 100%.
Результаты:
ABX464
Сравниваемое соединение 26
Толстая кишка/толстая и прямая кишка (колоректум)
Толстая кишка/толстая и прямая кишка (колоректум)
Толстая кишка/толстая и прямая кишка (колоректум)
Желудок
Печень
Легкие
Легкие
Поджелудочная железа
Поджелудочная железа
Поджелудочная железа
Поджелудочная железа
Таким образом, соединения согласно настоящему изобретению, в частности, соединения формулы (Ib’) или любые их метаболиты или их фармацевтически приемлемые соли, эффективны для лечения и/или предупреждения рака, и в частности, колоректального рака, рака желудка, рака печени, рака легких и/или рака поджелудочной железы, в частности, у пациентов в предраковом состоянии, с раком на ранней стадии или неметастатическим раком. В частности, соединения формулы (Ib’) или любые их метаболиты или их фармацевтически приемлемая соль не нацелены непосредственно на метастатическую инвазию.
Кроме того, из данных результатов сверх того следует, что соединения согласно изобретению, в частности, соединения формулы (Ib’) или любые их метаболиты или их фармацевтически приемлемая соль, более эффективны для лечения и/или предупреждения рака, в частности у пациентов, имеющих предраковое состояние, рак на ранней стадии или неметастатический рак, чем сравниваемое соединение 26, принадлежащее к формуле (Ia) (для клеточной линии Толстой кишки/толстой и прямой кишки (колоректума) CR3085: IC50=0,08 против 0,17; а для клеточной линии желудка GA0060: IC50=0,6 против выше 10).
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОМАРКЕРЫ И ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ВИРУСНЫХ ИНФЕКЦИЙ, ВОСПАЛЕНИЙ ИЛИ РАКА | 2019 |
|
RU2820481C2 |
| СИСТЕМЫ ДОСТАВКИ ЛЕКАРСТВ НА ОСНОВЕ МАЙТАНЗИНОИДА | 2018 |
|
RU2783076C2 |
| КОМБИНАЦИОННАЯ ТЕРАПИЯ С ПРИМЕНЕНИЕМ ДИАРИЛЬНЫХ МАКРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 2018 |
|
RU2784853C2 |
| СПОСОБ ЛЕЧЕНИЯ РАКА С ИСПОЛЬЗОВАНИЕМ КОМБИНАЦИИ ИНГИБИТОРОВ СНК1 И ATR | 2015 |
|
RU2736219C2 |
| БЕНЗО[b]ТИОФЕНОВЫЕ АГОНИСТЫ STING ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2771811C2 |
| БЕНЗИМИДАЗОЛЫ, ПРИМЕНИМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2006 |
|
RU2415853C2 |
| ИНГИБИТОРЫ ДЕМЕТИЛАЗЫ LSD1 НА ОСНОВЕ АРИЛЦИКЛОПРОПИЛАМИНА И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2011 |
|
RU2611437C2 |
| СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБЫ ПРИГОТОВЛЕНИЯ СОЕДИНЕНИЙ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ ATR | 2019 |
|
RU2806857C2 |
| СОЕДИНЕНИЯ ПИРАЗОЛО[3,4-b]ПИРИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ ТАМ И МЕТ | 2019 |
|
RU2773611C1 |
| УМЕНЬШЕНИЕ МАССЫ ОПУХОЛИ ПУТЕМ ВВЕДЕНИЯ CCR1 АНТАГОНИСТОВ В КОМБИНАЦИИ С PD-1 ИНГИБИТОРАМИ ИЛИ PD-L1 ИНГИБИТОРАМИ | 2017 |
|
RU2745195C2 |
Изобретение относится к применению соединения формулы (Ib’) или его фармацевтически приемлемой соли для лечения рака, выбранного из рака желудка, рака желудочно-кишечного тракта, колоректального рака, рака поджелудочной железы, рака легких и рака печени у пациента, где у указанного пациента нет клинически обнаруживаемых метастазов или где у указанного пациента присутствуют клинически обнаруживаемые метастазы и указанное соединение формулы (Ib’) не направлено непосредственно против метастатической инвазии, причем указанное соединение представляет собой 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин. 5 з.п. ф-лы, 3 табл.
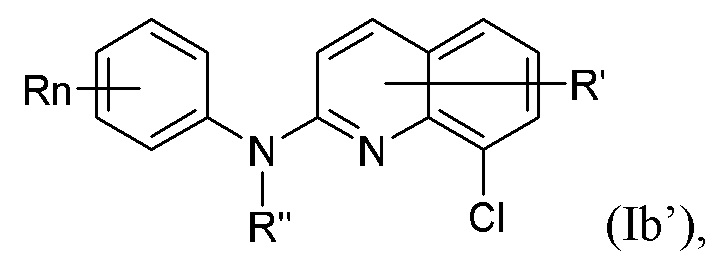
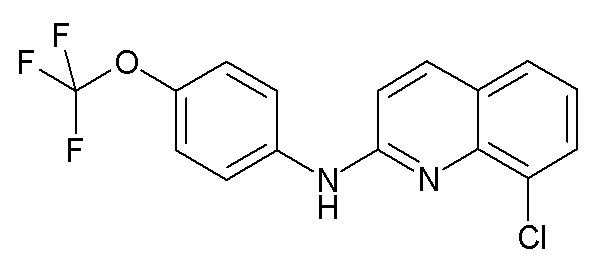
1. Применение соединения формулы (Ib’) или его фармацевтически приемлемой соли для лечения рака, выбранного из рака желудка, рака желудочно-кишечного тракта, колоректального рака, рака поджелудочной железы, рака легких и рака печени у пациента
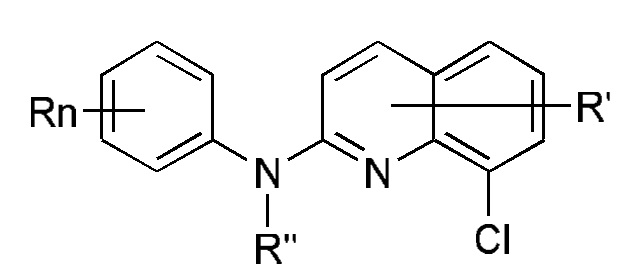
(Ib’),
где указанное соединение представляет собой 8-хлор-N-(4-(трифторметокси)фенил)хинолин-2-амин указанной ниже формулы или его фармацевтически приемлемую соль:
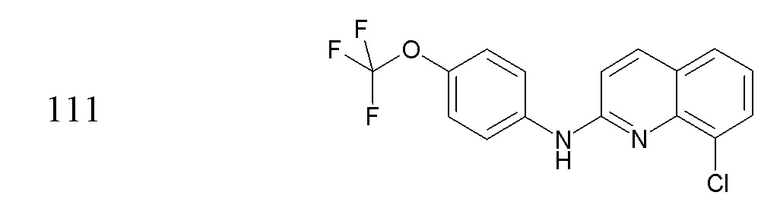
где у указанного пациента нет клинически обнаруживаемых метастазов, или
где у указанного пациента присутствуют клинически обнаруживаемые метастазы, и указанное соединение формулы (Ib’) не направлено непосредственно против метастатической инвазии.
2. Применение по п. 1,
где у указанного пациента нет клинически обнаруживаемых метастазов и указанный пациент имеет предраковое состояние, рак на ранней стадии или неметастатический рак.
3. Применение по п. 1, где измеряют наличие и/или уровень экспрессии miR-124 в образце крови и/или ткани пациента до и/или во время применения.
4. Применение по п. 1, где измеряют наличие и/или уровень экспрессии miR-124 в образце крови и/или ткани для регуляции дозы или мониторинга ответа на лечение.
5. Применение по п. 1, где для мониторинга тяжести рака и/или для мониторинга эффективности лечения используют алгоритм, сочетающий уровень miR-124 и уровень цитокинов или другого биомаркера или уровни соединения формулы (Ib’) или его фармацевтически приемлемой соли, как определено в п. 1.
6. Применение по п. 1, где во время применения у пациента измеряют уровень соединения формулы (Ib’) или его фармацевтически приемлемой соли, как определено в п. 1, в образце крови, плазмы, ткани, слюны и/или сыворотки пациента.
| WO 2010143168 A3, 16.12.2010 | |||
| ПЕРЕДАЧА ОБСЛУЖИВАНИЯ МЕЖДУ ТЕХНОЛОГИЯМИ РАДИОДОСТУПА | 2019 |
|
RU2757161C1 |
| EP 3059236 A1, 24.08.2016 | |||
| УПЛОТНИТЕЛЬНАЯ МАНЖЕТА | 2011 |
|
RU2465502C1 |
| WO 2016009065 A2, 21.01.2016 | |||
| ASHRAF KAREEM EL-DAMASY et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
2024-01-11—Публикация
2019-12-19—Подача