Настоящее изобретение относится к области медицины, фармацевтики и онкологии, а именно к новому химическому соединению к изопропиловому эфиру 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты, обладающему антипролиферативной активностью, опосредованной иммунными клетками человека, индукцией активности гена интерферона бета, активацией сигнального пути STING.
Предшествующий уровень техники
Роль иммунной системы в поддержании генетической стабильности организма является первостепенной. К основным факторам, приводящим к нарушениям генетического постоянства организма, относятся вторжение микроорганизмов и мутационная изменчивость собственных клеток, способная приводить к образованию злокачественных опухолей. Неудивительно, что иммунные реакции, направленные на уничтожение патогенов и на элиминацию злокачественных новообразований, могут пересекаться. Сигнальные пути, связанные с активацией синтеза интерферонов 1 типа, изначально считались компонентом врожденного иммунитета, направленного на уничтожение зараженных вирусами клеток и самих вирусов. Однако действие интерферонов 1 типа не ограничивается противовирусной активностью, антипролиферативное действие интерферонов позволяет рассматривать их в качестве противоопухолевых препаратов.
На сегодняшний день на отечественном рынке доступны несколько десятков препаратов с действующим веществом интерферон-альфа 2b и интерферон-бета, как для парэнтерального, так и для местного введения. Всего в России 14 фармацевтических компаний владеют регистрационными удостоверениями на препараты интерферонов альфа или бета. Показания для применения препаратов интерферона альфа - вирусные и онкологические заболевания; для препаратов интерферона бета - рассеянный склероз.
Интерфероны были открыты в 50-х годах прошлого века, когда два японских вирусолога Yasu-ichi Nagano и Yasuhiko Kojima работали в Токийском университете над созданием вакцины против оспы. Тогда ими было замечено, что после подкожного введения кроликам гомогената убитых вирусных частиц в дальнейшем на этих участках кожи вирус размножался хуже, чем на других участках, причем этот эффект распространялся не только на вирус оспы, но и на другие вирусы. Свои наблюдения ученые опубликовали в 1954 году во французском журнале "Journal de la Société de Biologie" [Nagano Y, Kojima Y (October 1954). "Pouvoir immunisant du virus vaccinal inactivé par des rayons ultraviolets" (in French). C. R. Seances Soc. Biol. Fil. 148 (19-20): 1700-2]. В то же время в Лондоне ученые Alick Isaacs и Jean Lindenmann наблюдали подобные явления с вирусом гриппа на куриных эмбрионах, о чем они рассказали в 1957 году в издании Proc. R. Soc. Lond., В, Biol. Sci. [Isaacs A, Lindenmann J (September 1957). "Virus interference. I. The interferon". Proc. R. Soc. Lond., B, Biol. Sci. 147 (927): 258-67], впервые назвав вещество, мешающее размножению вирусов, интерфероном. По-видимому, это вещество представляло собой смесь интерферонов I типа, куда относятся интерфероны альфа, бета и омега.
В настоящее время известно, по меньшей мере, 23 различные формы интерферона-альфа (ИФНа), представляющего собой белок молекулярной массы 19-26 кДа и длиной 156-172 аминокислотных остатков. Все типы ИФНа имеют консервативный участок 115-151 ак, тогда как N- и С- концы являются вариабельными. Многие типы ИФНа отличаются всего лишь по 1-2 аминокислотам. Дисульфидные связи в молекуле интерферона- альфа формируются между 1-98 и 29-138 аминокислотами. Дисульфидная связь между 29 и 138 аминокислотами является необходимой для биологической активности ИФНа, тогда как дисульфидная связь 1-98 может быть восстановлена без потери биологической активности. Все формы ИФН-а имеют потенциальный участок для гликозилирования, однако большинство из них не гликозилировано.
Для интерферона-бета (ИФНб) известна только одна природная форма, тогда как рекомбинантный интерферон-бета может быть как гликозилированный (интерферон-бета 1а), так и негликозилированный (интерферон-бета 1b). Негликозилированный ИФНб получают в клетках бактерий, и по активности он уступает гликозилированному интерферону из клеток млекопитающих [Алиев Т.К., Панина А.А., Свешников П.Г., Солопова О.Н. Способ количественного определения антипролиферативной активности интерферона-бета человека. Патент на изобретение РФ 2739261 С1, 22.12.2020]. Для гликозилированных форм интерферона-бета в антипролиферативных тестах на опухолевой линии НТ29 в присутствии мононуклеаров периферической крови человека (МПК) показатель полуингибирующей концентрации IC50 составил от 1.5×10-12 М для препарата Ребиф, до 2.0×10-12 М для препарата Синновекс, тогда как значения IC50 в подобных тестах для применяющихся в онкологии цитостатиков, например, цисплатина, лежат в микромолярном диапазоне. Антипролиферативная активность интерферона-бета, превышающая таковую цитостатиков на 5-7 порядков, делает его привлекательным агентом для разработки противоопухолевых средств.
Помимо прямого воздействия на опухоль, ИФНб запускает целый каскад местных иммунологических реакций: стимуляция Т-клеток, естественных киллеров (ЕК), дендритных клеток, врожденных лимфоидных клеток (ILCs); негативная регуляция супрессоров: миелоидных супрессорных клеток (MDSCs) и регуляторных Т-клеток (Treg); ингибирование пролиферации, модуляция апоптоза, дифференциация опухолевых клеток, экспрессия поверхностных антигенов, активация опухолевого супрессора Ecrg4, активация каспазы-8, индукция вторичных медиаторов (интерлейкинов) и др. [Belinda S. Parker, Jai Rautela & Paul J. Hertzog. Antitumour actions of interferons: implications for cancer therapy. Nature Reviews Cancer, 16,131-144(2016)].
Несмотря на значительные усилия [Dicitore A, Grassi ES, Borghi MO, Gelmini G, Cantone MC, Gaudenzi G, Persani L, Caraglia M, Vitale G.J. Antitumor activity of interferon-β1a in hormone refractory prostate cancer with neuroendocrine differentiation. Endocrinol Invest. 2017 Mar 1], [Iwamura T, Narumi H, Suzuki T, Yanai H, Mori K, Yamashita K, Tsushima Y, Asano T, Izawa A, Momen S, Nishimura K, Tsuchiyama H, Uchida M, Yamashita Y, Okano K, Taniguchi A novel pegylated IFN-β as strong suppressor of the malignant ascites in a peritoneal metastasis model of human cancer. T.Cancer Sci. 2017 Jan 27], [Rybchenko VS, Panina AA, Aliev TK, Solopova ON, Balabashin DS, Novoseletsky VN, Dolgikh DA, Sveshnikov PG, Kirpichnikov MP. Bispecific Antibodies for IFN-β Delivery to ErbB2+Tumors. Biomolecules. 2021 Dec 20;11(12): 1915. doi: 10.3390/biom11121915. PMID: 34944558; PMCID: PMC8699518], ни одного препарата на основе интерферона-бета для лечения онкологических заболеваний на сегодняшний день не зарегистрировано. Очевидное препятствие для применения интерферона-бета в практику лечения злокачественных новообразований - широкий спектр тяжелых побочных явлений при системном введении ИФНб. Локальное действие ИФНб на опухоль может быть достигнуто либо доставкой в опухоль вектора, несущего ген интерферона-бета, либо активацией интерфероновых сигнальных путей в опухолевом узле.
Первый подход, реализованный в препаратах для клинических исследований, пока не увенчался получением препарата, эффективность которого подтверждена клинически, но исследования в этом направлении продолжаются. NCT00107861, NCT00031083, NCT00299962, NCT00107861, NCT01628640], [Predina JD, Keating J, Venegas О, Nims S, Singhal S. Neoadjuvant intratumoral immuno-gene therapy for non-small cell lung cancer. Discov Med. 2016 Apr;21(116):275-81. PMID: 27232513].
Второй подход получил мощный толчок для развития с опубликованием в 2013 году патента «Use of STING agonist as cancer treatment)) [T.F. Gajewski, S. Woo, L. Corrales, Use of sting agonist as cancer treatment. Патент WO 2015077354 A1 https://patents.google.com/patent/WO2015077354A1/en]. Авторы патента экспериментально на мышиных моделях показали, что внутриопухолевая стимуляция интерферонового сигнального пути посредством активации белка STING приводит к полной и необратимой элиминации опухолевого узла. Основной фокус в данном патенте был сосредоточен на исследовании активности агонистов STING dimethylxanthone acetic acid (DMXAA) и ML RR-S2 CDA. Впоследствии было проведено несколько клинических испытаний DMXAA (NCT00863733, NCT00111618, NCT01057342, NCT01299415, NCT00003697 и др.), но клинического эффекта показано не было. Как оказалось, DMXAA специфичен к мышиному, но не к человеческому STING [Conlon J, Burdette DL, Sharma S, Bhat N, Thompson M, Jiang Z et al. (May 2013). "Mouse, but not human STING, binds and signals in response to the vascular disrupting agent 5,6-dimethylxanthenone-4-acetic acid". Journal of Immunology. 190 (10): 5216-25. doi:10.4049/jimmunol.1300097]. Кроме того, для достижения значимого противоопухолевого эффекта на мышиных моделях требовалось введение очень больших дозировок DMXAA: в экспериментах, описанных в указанном выше патенте и последующих работах, вводимые дозировки составляли 100-500 мкг на одно введение. Это побудило исследователей к поиску новых агонистов STING с максимальной активностью по отношению к человеческому STING. К 2019 году было известно уже несколько десятков молекул, их свойства подробно описаны в обзоре [11. Zhang Н, You QD, Xu XL. Targeting Stimulator of Interferon Genes (STING): A Medicinal Chemistry Perspective. J Med Chem. 2020 Apr 23;63(8):3785-3816. doi: 10.1021/acs.jmedchem.9b01039. Epub 2019 Dec 20. PMID: 31820978]. Соединение, описанное в этом обзоре под номером 62, а также в патенте WO 2018067423 - BENZO[B]THIOPHENE COMPOUNDS AS STING AGONISTS, было выбрано из 2,4 миллионов соединений путем скрининга на клетках и опубликовано в журнале Science под названием MSA-2. [Bo-Sheng Pan et al. An orally available non-nucleotide STING agonist with antitumor activity. Science369, eaba 6098(2020). DOI: 10.1126/science.aba6098].
Помимо соединения 62 или MSA-2 в обзоре [Zhang Н, You QD, Xu XL. Targeting Stimulator of Interferon Genes (STING): A Medicinal Chemistry Perspective. J Med Chem. 2020 Apr 23;63(8):3785-3816. doi: 10.1021/acs.jmedchem.9b01039. Epub 2019 Dec 20. PMID: 31820978] приводятся различные производные MSA-2, среди которых под номером 66 третбутиловый эфир, активность которого существенно ниже, чем у MSA-2: 16% от активности cGAMP, природного активатора STING, против 129% для MSA-2. Отсюда авторы делают заключение, что свободная карбоксильная группа имеет решающее значение для активности соединения.
На сегодняшний день активность MSA-2 показана во многих исследованиях, как в моно режиме, так и в сочетании с различными противоопухолевыми агентами, главным образом ингибиторами контрольных точек иммунитета. [Serrano R, Lettau М, Zarobkiewicz М, Wesch D, Peters С, Kabelitz D. Stimulatory and inhibitory activity of STING ligands on tumor-reactive human gamma/delta T cells. Oncoimmunology. 2022 Feb 1;11(1):2030021. doi: 10.1080/2162402X.2022.2030021.eCollection2022.], [14. Combination of oral STING agonist MSA-2 and anti-TGF-β/PD-L1 bispecific antibody YM101: a novel immune cocktail therapy for non-inflamed tumors. Yi M, Niu M, Wu Y, Ge H, Jiao D, Zhu S, Zhang J, Yan Y, Zhou P, Chu Q, Wu K. J Hematol Oncol. 2022 Oct 8;15(1):142. doi: 10.1186/sl3045-022-01363-8], [15. Lu Z, Chen J, Yu P, Atherton MJ, Gui J, Tomar VS, Middleton JD, Sullivan NT, Singhal S, George SS, Woolfork AG, Weljie AM, Hai T, Eruslanov EB, Fuchs SY. Tumor factors stimulate lysosomal degradation of tumor antigens and undermine their cross-presentation in lung cancer. Nat Commun. 2022 Nov 4;13(1):6623. doi: 10.1038/s41467-022-34428-w. PMID: 36333297; PMCID: РМС9636202].
Задачей настоящего изобретения является создание нового химического соединения, стимулирующего продукцию интерферона-бета человека.
Технический результат: получено и описано новое химическое соединение, стимулирующее продукцию интерферона-бета человека, и способ его получения.
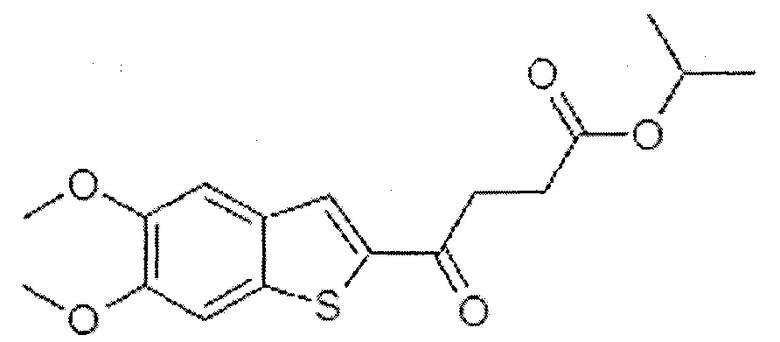
Технический результат достигается тем, что синтезирован изопропиловый эфир 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты, стимулирующий продукцию интерферона-бета формулы
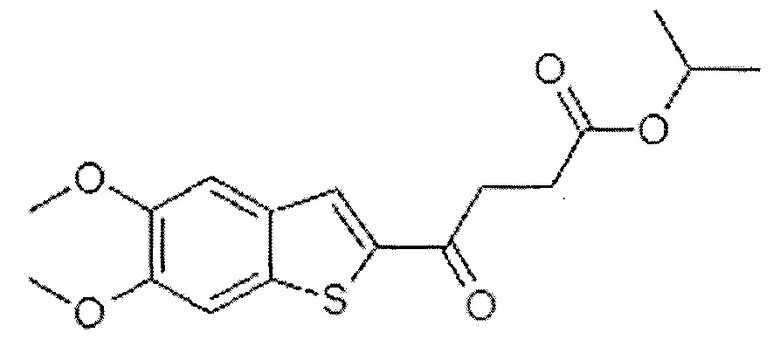
Получение соединения
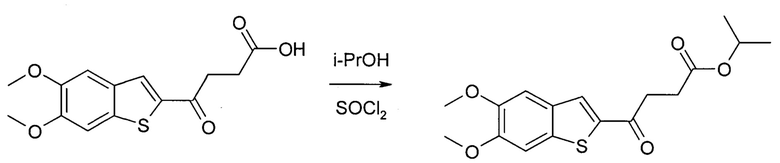
Синтез изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты:
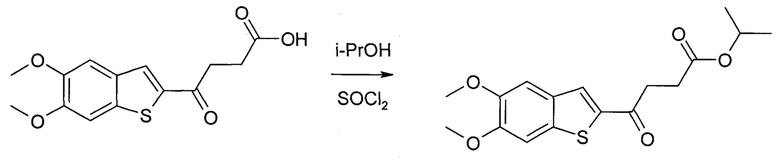
5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановую кислоту перемешивали в безводном изопропиловом спирте и добавляли по каплям хлористый тионил (1-5 экв.), не допуская повышения температуры выше 0°С. Затем перемешивали при комнатной температуре 12 часов.
После завершения реакции (контроль прохождения реакции по ТСХ до исчезновения исходной кислоты) растворитель упаривали до небольшого объема и, добавляя насыщенный раствор бикарбоната натрия, рН доводили примерно до 8, экстрагировали хлористым метиленом, органическую фазу собирали и очищали препаративной хроматографией. Выход 85-94%.
Физико-химические свойства изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты
Применяемые аналитические методы и оборудование
Аналитическую ВЭЖХ проводили на хроматографе Agilent 1260 Series. Спектры ESI-MS регистрировали на приборе "Agilent LC/MS 1200" при ионизации пробы электрораспылением в режиме регистрации положительных ионов.
Спектры ЯМР 1Н получены на Фурье ЯМР-спектрометре Bruker 600 МГц, внутренний стандарт - тетраметилсилан в дейтерохлороформе CDCl3. Химические сдвиги приведены в миллионных долях (δ), КССВ - в герцах. ТСХ проводили на пластинах Merck TLC Silica gel 60 F254, проявление в УФ и растворе перманганата калия.
Спектр 1Н ЯМР (CDCl3, δ м.д., J, Гц): 7.92 (уш.с, 1Н), 7.34-7.23 (м, 2Н), 5.06 (м, 1H), 3.98 (уш.с, 6Н), 3.33 (т, J=6.94, 2Н), 2.79 (т, J=6.94, 2Н), 1.28 (д, J=6.61, 6Н), ESI-MS, m/z 667,3 [2M+Na]+.
Изобретение иллюстрируется фигурами 1-3.
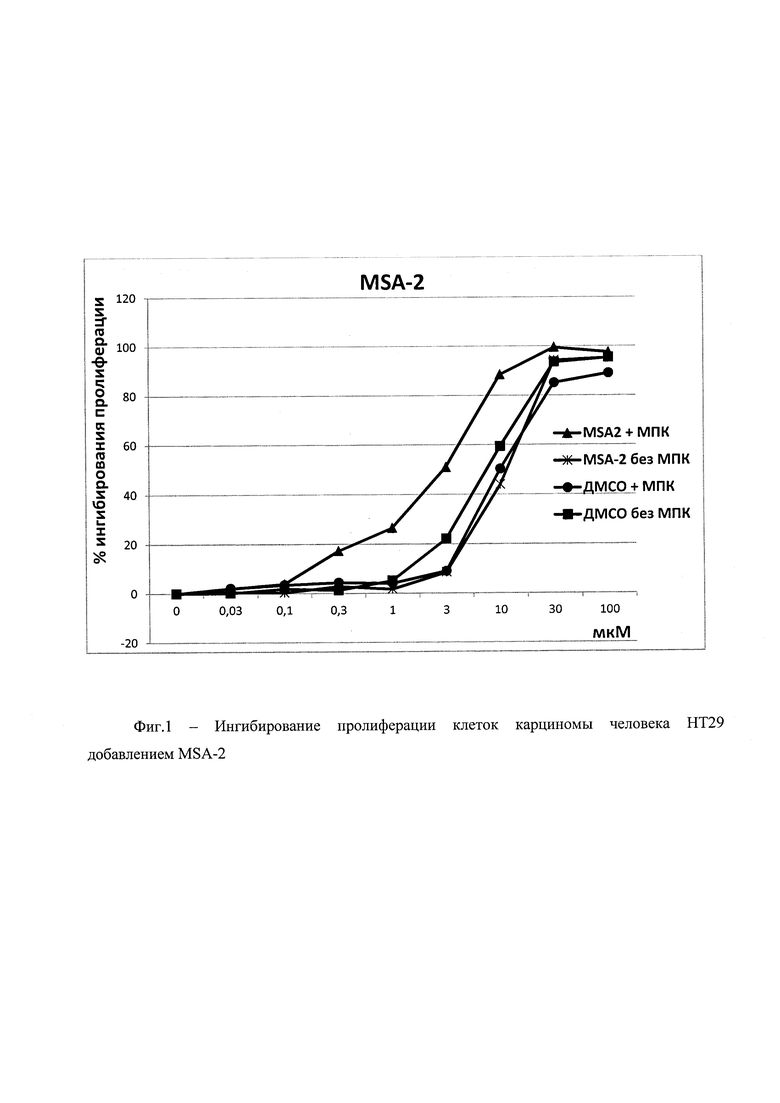
На фиг. 1 представлены графики зависимости уровня ингибирования пролиферации клеток карциномы человека НТ29 от концентрации MSA-2 или эквимолярной концентрации растворителя ДМСО в присутствии или в отсутствие мононуклеаров периферической крови человека.
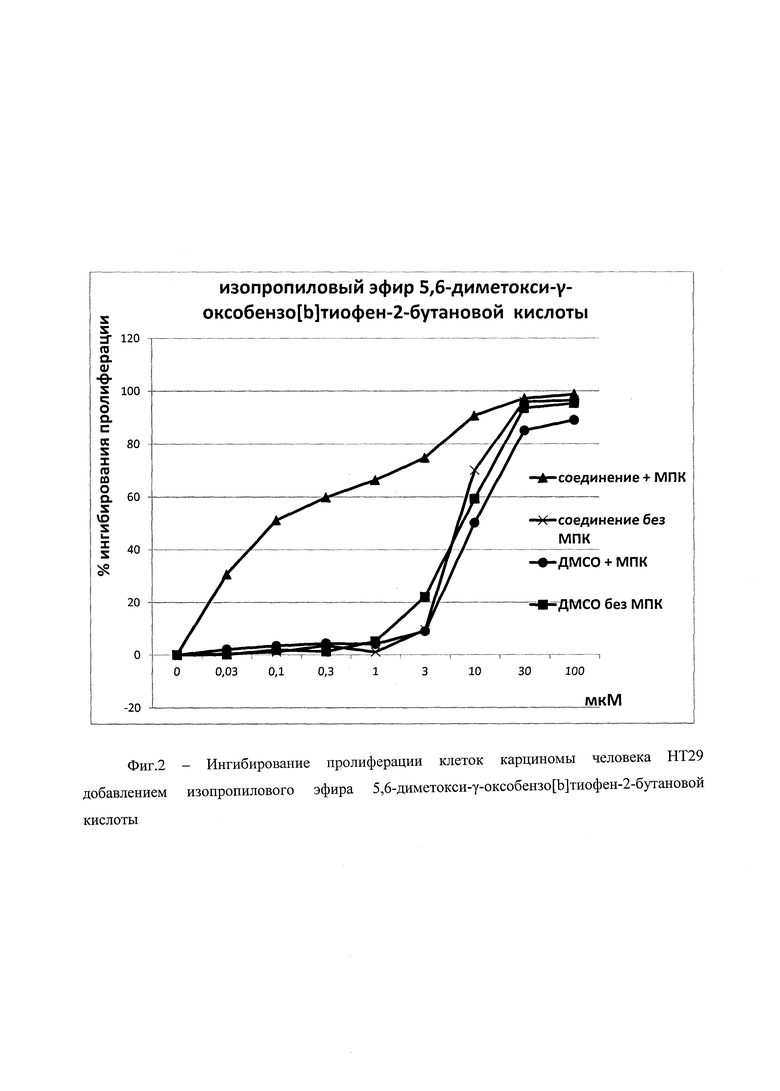
На фиг. 2 - представлены графики зависимости уровня ингибирования пролиферации клеток карциномы человека НТ29 от концентрации изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты или эквимолярной концентрации растворителя ДМСО в присутствии или в отсутствие мононуклеаров периферической крови человека.
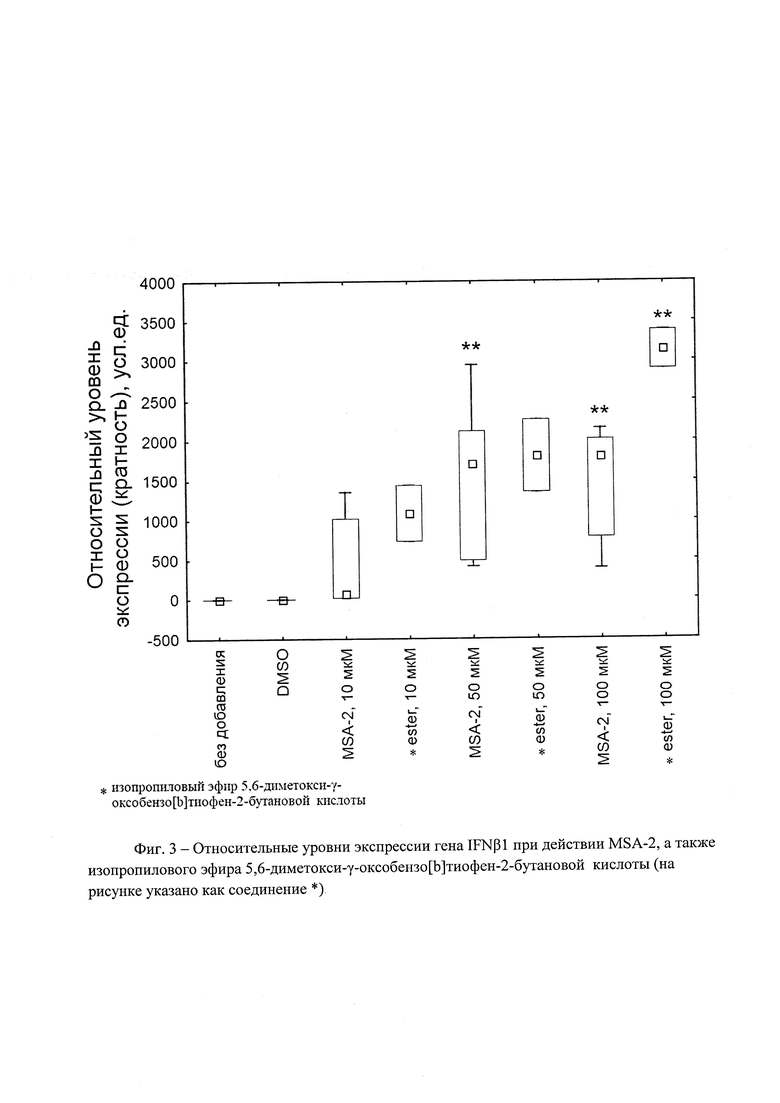
На фиг. 3 - Относительный уровень экспрессии интерферона-бета при стимуляции клеток линии ТНР-1 различными концентрациями MSA-2 и изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты.
Биологическая активность изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты в сравнении с ближайшим аналогом MSA-2.
Пример 1. Антипролиферативная активность изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты на клеточной линии карциномы толстой кишки человека НТ29.
Эксперимент проводили по следующей схеме:
клетки линии НТ29 культивировали в течение 8 суток в среде DMEM с добавлением 3% телячьей сыворотки следующим образом:
- клетки сеяли в 96-луночные планшеты до конечной концентрации 10 тыс.клеток в мл;
- в лунки добавляли мононуклеары периферической крови человека до конечной концентрации либо 0 клеток в мл (без МПК), либо 100 тыс.клеток в мл (+МПК);
- в лунки добавляли серийные разведения MSA-2 либо изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты до конечных концентраций от 0 мкМ до 100 мкМ в трех повторах;
- в качестве контроля добавляли серийные разведения ДМСО до конечных концентраций от 0 до 2‰, что соответствует содержанию ДМСО в лунках с MSA-2 и изопропиловым эфиром 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты.
Пролиферацию оценивали в тесте МТТ, оптическую плотность в лунках измеряли при длине волны 560 нм, находили средние значения в повторах.
Уровень ингибирования пролиферации определяли по методике, описанной в патенте [3].
Строили графики зависимости уровня ингибирования пролиферации в % от концентрации активного вещества. Значение IC50 находили графическим способом.
Результаты приведены на фигурах 1 и 2.
Результат: изопропиловый эфир 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты обладает антипролиферативной активностью в отношении клеток опухолевой линии НТ29 в присутствии мононуклеаров периферической крови человека. Показатель полуингибирующей концентрации изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты IC50 составил 0,1 мкМ, что в 30 раз ниже аналогичного показателя для MSA-2.
IC50 (MSA-2): 3 мкМ;
IC50 (изопропиловый эфир 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты): 0,1 мкМ.
Пример 2. Оценка индукции экспрессии интерферона-бета человека разными концентрациями изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты в сравнении с MSA-2.
Действие соединения на культуру моноцитов острого моноцитарного лейкоза ТНР-1 оценивали по уровню экспрессии интерферона-бета человека с помощью ПЦР-РВ.
Индукцию проводили в чашках Петри диаметром 35 mm;
~1,25*106 кл/чашка;
2 контроля в двух повторах: стандартный и DMSO;
3 рабочие концентрации изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты (50 mM сток) в двух повторах: 10 мкМ, 50 мкМ и 100 мкМ.
Инкубацию с соединением осуществляли в течение 5 часов, после чего проводили выделение суммарной РНК из клеток и, соответственно, ПЦР-РВ. В качестве референсного гена для оценки уровня экспрессии использовали ген «домашнего хозяйства» глицеральдегид-3-фосфатдегидрогеназы (GAPDH). Обработка данных проводилась с использованием критерия Краскела-Уоллиса и программного обеспечения Statistica.
Результаты приведены на фигуре 3.
Приведенные диаграммы демонстрируют значительное увеличение уровня экспрессии интерферона-бета человека (×1000) при воздействии на клетки ТНР-1. При этом наблюдаемый эффект носит дозозависимый характер.
| название | год | авторы | номер документа |
|---|---|---|---|
| Биомедицинский клеточный продукт со специфической противоопухолевой активностью, представленный популяциями лимфокин-активированных киллеров и анти-HER2 CAR-γδΤ-ОИЛ и анти-HER2 CAR-T-NK | 2022 |
|
RU2786210C1 |
| Низкотоксичная фармацевтическая композиция с противоопухолевой активностью в отношении холангиокарциномы | 2023 |
|
RU2825942C1 |
| Фармацевтическая композиция, проявляющая цитотоксичность в отношении клеток карциномы толстой кишки человека | 2020 |
|
RU2747147C1 |
| Комбинированная наноконструкция для терапии рака легкого | 2024 |
|
RU2841547C1 |
| Фармацевтическая композиция, проявляющая цитотоксическое действие в отношении клеток рака мочевого пузыря человека | 2018 |
|
RU2693378C1 |
| Гидроксамовые кислоты, производные 4-аминохиназолина, обладающие противоопухолевой активностью | 2022 |
|
RU2802463C1 |
| Способ получения рекомбинантного белка GAGE1 человека | 2016 |
|
RU2652890C1 |
| АГОНИСТЫ СТИМУЛЯТОРА ГЕНОВ ИНТЕРФЕРОНА STING | 2019 |
|
RU2809022C2 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ РАКА | 2002 |
|
RU2219935C1 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ РАКА | 1999 |
|
RU2159109C1 |
Изобретение относится к области медицины, фармацевтики и онкологии, а именно к изопропиловому эфиру 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты формулы I, стимулирующему продукцию интерферона-бета человека и обладающему антипролиферативной активностью, опосредованной иммунными клетками человека, индукцией активности гена интерферона бета, активацией сигнального пути STING. Также раскрывается способ получения соединения I путем взаимодействия 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты с безводным изопропиловым спиртом и хлористым тионилом, позволяющий получить целевое соединение с выходом 85-94%. 2 н. и 1 з.п. ф-лы, 3 ил., 2 пр.
 I
I
1. Изопропиловый эфир 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты формулы, стимулирующий продукцию интерферона-бета человека формулы
2. Соединение по п. 1, проявляющее антипролиферативную активность в присутствии мононуклеаров периферической крови человека.
3. Способ получения изопропилового эфира 5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановой кислоты:
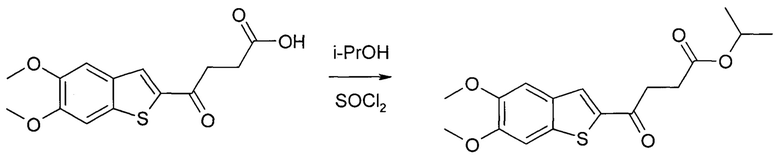
5,6-диметокси-γ-оксобензо[b]тиофен-2-бутановую кислоту перемешивают в безводном изопропиловом спирте и добавляют по каплям хлористый тионил, 1-5 экв., не допуская повышения температуры выше 0°С, затем перемешивают при комнатной температуре в течение 12 часов; после завершения реакции растворитель упаривают и, добавляя насыщенный раствор бикарбоната натрия, рН доводят до 8, экстрагируют хлористым метиленом, органическую фазу собирают и очищают препаративной хроматографией.
| WO 2015077354 A1, 28.05.2015 | |||
| WO 2018067423 A1, 12.04.2018 | |||
| Бензотиофены и родственные соединения в качестве агонистов STING | 2019 |
|
RU2806274C2 |
| Zhang, Han et al | |||
| "Targeting Stimulator of Interferon Genes (STING): A Medicinal Chemistry Perspective." Journal of medicinal chemistry, 2020 vol | |||
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
Авторы
Даты
2024-01-16—Публикация
2023-11-10—Подача