Согласно настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой на выдачу патента США №62/633409, поданной 21 февраля 2018 года, раскрытие которой во всей своей полноте включено в настоящий документ посредством ссылки.
Заявление о государственной поддержке
Настоящее изобретение было разработано при государственной поддержке в рамках гранта №СА200970-02, выданного Национальными институтами здравоохранения. Правительство имеет определенные права на настоящее изобретение.
Область техники, к которой относится настоящее изобретение
Сигнальный путь cGAS-STING играет решающую роль во врожденном иммунном ответе, который клетки организма млекопитающих вырабатывают для уничтожения различных ДНК- и РНК-вирусов. STING (стимулятор генов интерферона) представляет собой резидентный сигнальный белок эндоплазматического ретикулума (ER), частично локализованный на митохондриальных мембранах, который широко экспрессируется как у иммуноцитов, так и отличных от иммуноцитов клеток. В ответ на циклические динуклеотиды (CDN), в том числе 2'-3' cGAMP, вырабатываемый в ответ на цитозольную ДНК с участием циклической GMP-AMP-синтазы (cGAS), STING перемещается в перинуклеарный участок, где быстро индуцирует ТВК1-/IRF3-зависимую выработку интерферона I типа (IFN) и провоспалительных цитокинов. Также было обнаружено, что STING напрямую связывает цитозольную ДНК, хотя физиологическое значение прямой ДНК-распознающей активности еще предстоит полностью охарактеризовать.
В ходе недавних исследований было продемонстрировано, что STING играет важную роль в иммунных ответах на опухолевые клетки. Эффективное инициируемое опухолью примирование Т-клеток в опухолевом микроокружении нуждается в выработке интерферона-бета (IFN-b) резидентными дендритными клетками, и было продемонстрировано, что экспрессия IFN-b зависит от активации пути STING (1). Действительно, было продемонстрировано, что внутриопухолевая доставка нуклеотидных агонистов STING вызывает глубокую регрессию развившихся опухолей у изогенных модельных мышей (1). Кроме того, было продемонстрировано, что активация пути STING в значительной степени способствует развитию противоопухолевого эффекта от облучения посредством развития опосредованного IFN-b иммунного ответа в облученном опухолевом микроокружении.
Краткое раскрытие настоящего изобретения
В соответствии с различными вариантами осуществления, настоящее изобретение относится к агонисту стимулятора генов интерферона (STING), который можно применять при лечении опухолей.
Например, настоящее изобретение может относиться к способу стимуляции экспрессии генов интерферона, предусматривающему введение пациенту эффективной дозы агониста стимулятора генов интерферона (STING), представляющего собой соединение с формулой (I) (ниже), и к способу лечения опухоли у пациента, предусматривающему введение пациенту эффективной дозы агониста стимулятора генов интерферона (STING), представляющего собой соединение с формулой (I):
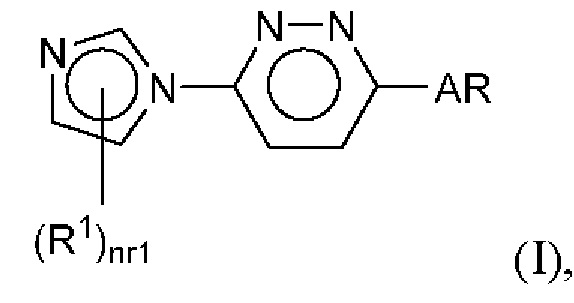
где каждый R1 независимо представляет собой (С1-С4)алкил или CN, nr1 равно 0, 1, 2 или 3, при условии, что каждый R1 связан с атомом углерода; и
AR представляет собой группу с формулой -C(=O)N(R)Ar1;
где Аг1 выбран из группы, состоящей из:
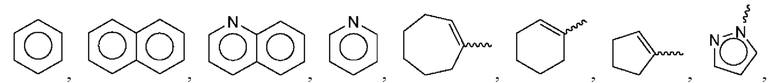
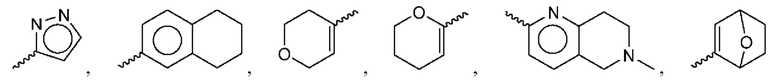 и
и 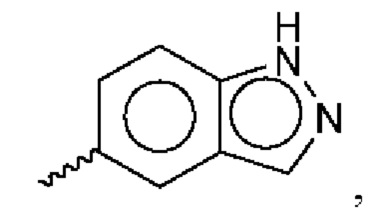 где волнистой линией указано положение связи; где любой Ar1 замещен nr2 раза независимо выбранными группами R2, которые выбраны из группы, состоящей из:
где волнистой линией указано положение связи; где любой Ar1 замещен nr2 раза независимо выбранными группами R2, которые выбраны из группы, состоящей из:
-(С1-С4)-алкила, -(С1-С4)-алкил-O, -(С1-С4)-алкил-ОС(O), -CN, -галогена, -(С3-С7)-циклоалкила, -(С1-С4)-алк-ОС(O), -СООН, (С3-С7)-циклоалкил-ОС(O), -CN, -F, -CI, -SF5, -метилендиокси, -дифторметилендиокси, -этилендиокси, -CF3, -OCF3, -C(O)NH2, -C(O)NH(CH2)2OH, -СН2ОН, -NR2, -С(/)ONH-аргинина, -C(O)O(CH2)2NR2,
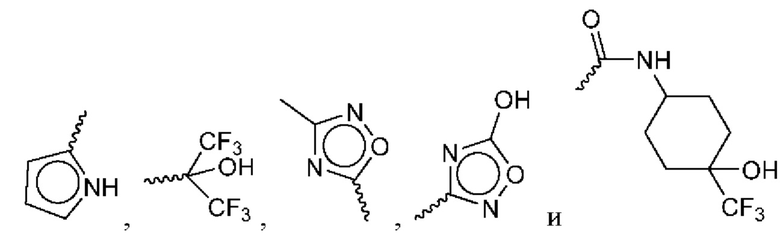 ; где волнистой линией указано положение связи; и пг2 равно 0, 1, 2 или 3; или
; где волнистой линией указано положение связи; и пг2 равно 0, 1, 2 или 3; или
AR представляет собой группу с формулой:
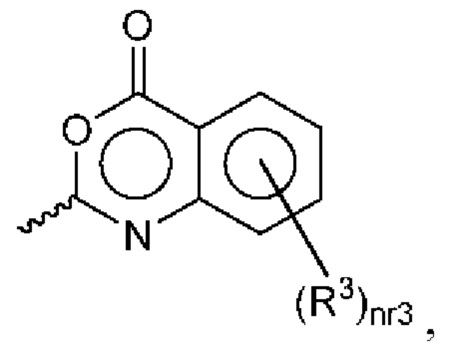
где R3 выбран из группы, состоящей из
(С1-С4)-алкила, (С1-С4)-алкил-0, (С1-С4)-алкил-ОС(O), CN, галогена, (С3-С7)-циклоалкила, (С1-С4)-алк-ОС(O), СООН, (С3-С7)-циклоалкил-ОС(O), CN, F, CI, -SF5, метилендиокси, дифторметилендиокси, этилендиокси, CF3, -OCF3, CONH2, CONH(CH2)2OH, СН2ОН, NR2, CONH-аргинина и C(O)O(CH2)2NR2; и nr3 равно 0, 1, 2 или 3;
или его фармацевтически приемлемую соль.
Более конкретно, способ можно осуществить с применением соединения с формулой (I), где n1 равно 0; или n1 равно 1 или 2, и R1 представляет собой метил.
Более конкретно, способ можно осуществить с применением соединения с формулой (I),
где X представляет собой метиловый, этиловый или изопропиловый эфир карбоновой кислоты. Кроме того, способ можно осуществить с применением соединения с формулой (I), где X представляет собой 1,1,1,3,3,3-гексафторпропан-2-ол-2-ильную группу. Кроме того, способ можно осуществить с применением соединения с формулой (I), где Ar представляет собой фенил. Кроме того, способ можно осуществить с применением соединения с формулой (I). Кроме того, способ можно осуществить с применением соединения с формулой (I), где R2 независимо выбран из фтора, хлора, (С1-С4)-алкила, трифторметила или циано, и n2 равно 1 или 2; или два R2 вместе образуют метилендиоксигруппу.
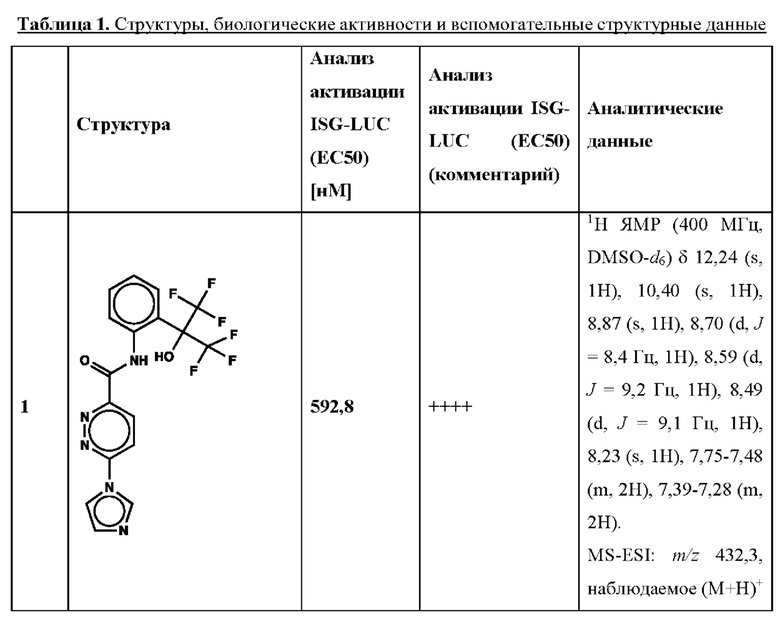
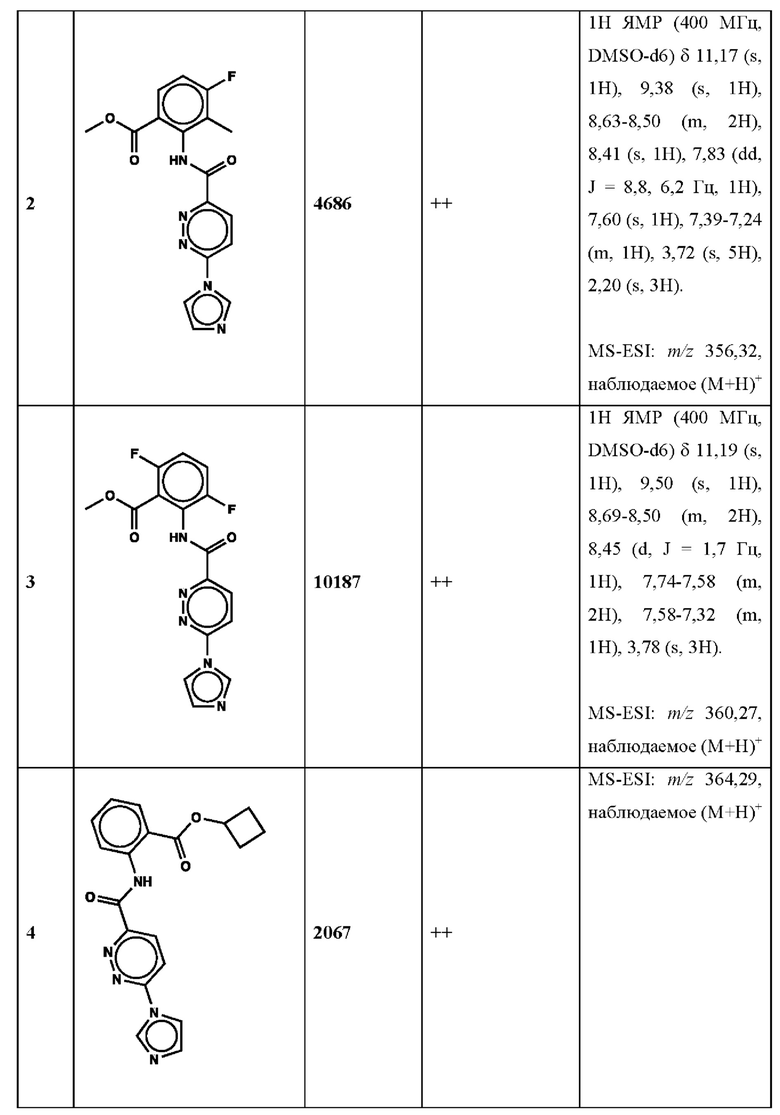
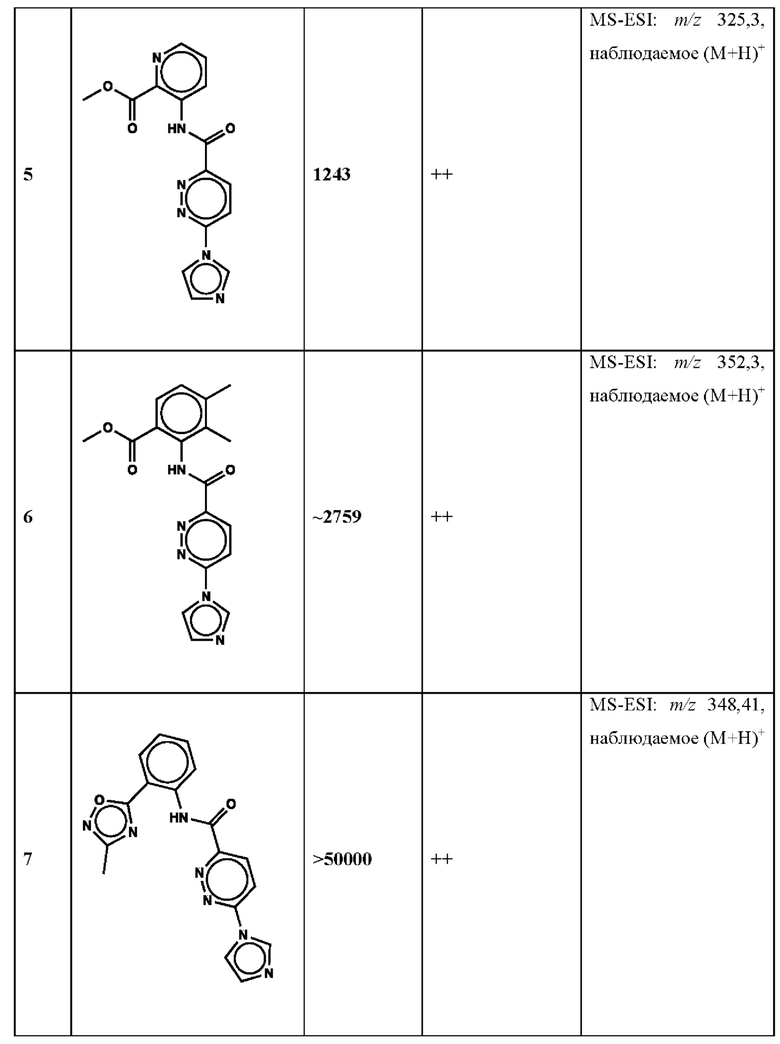
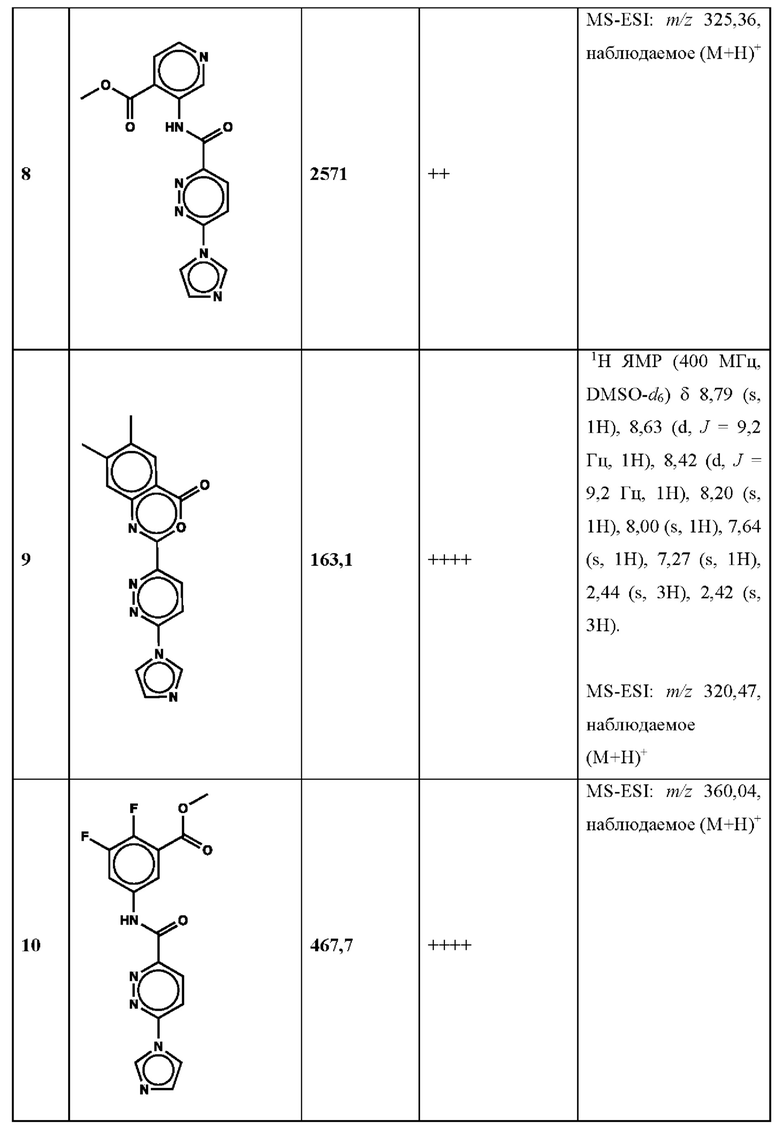
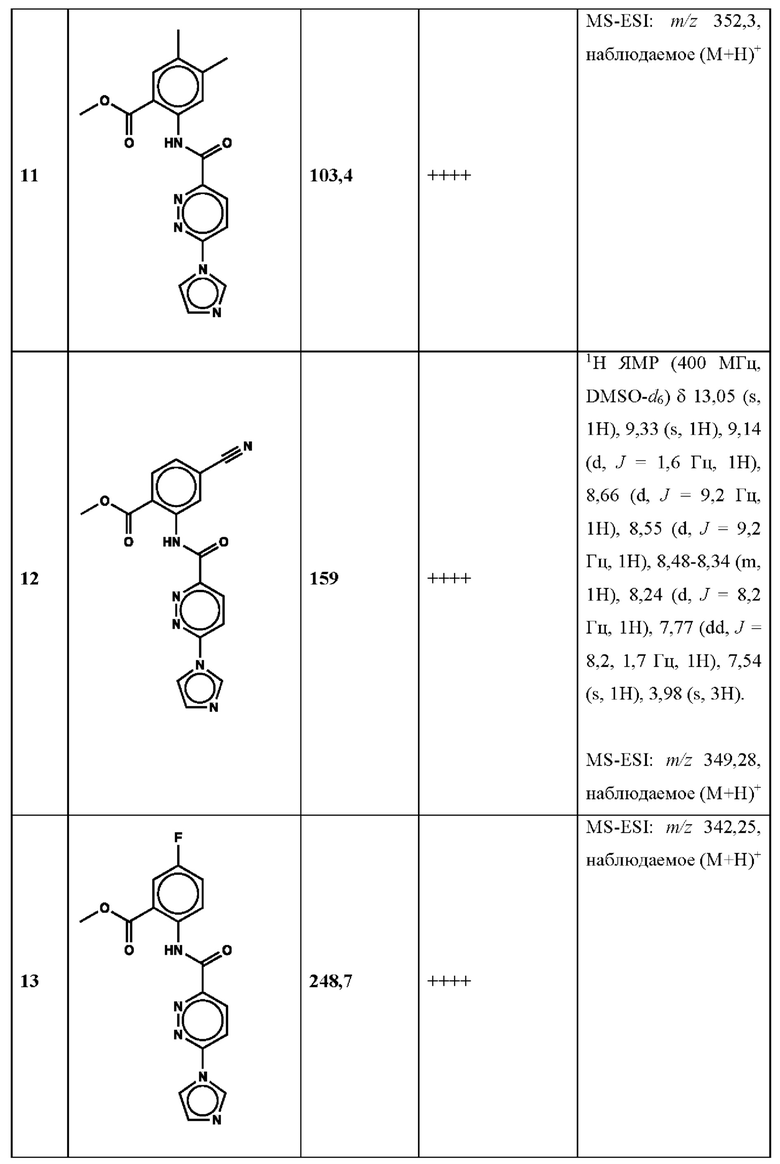
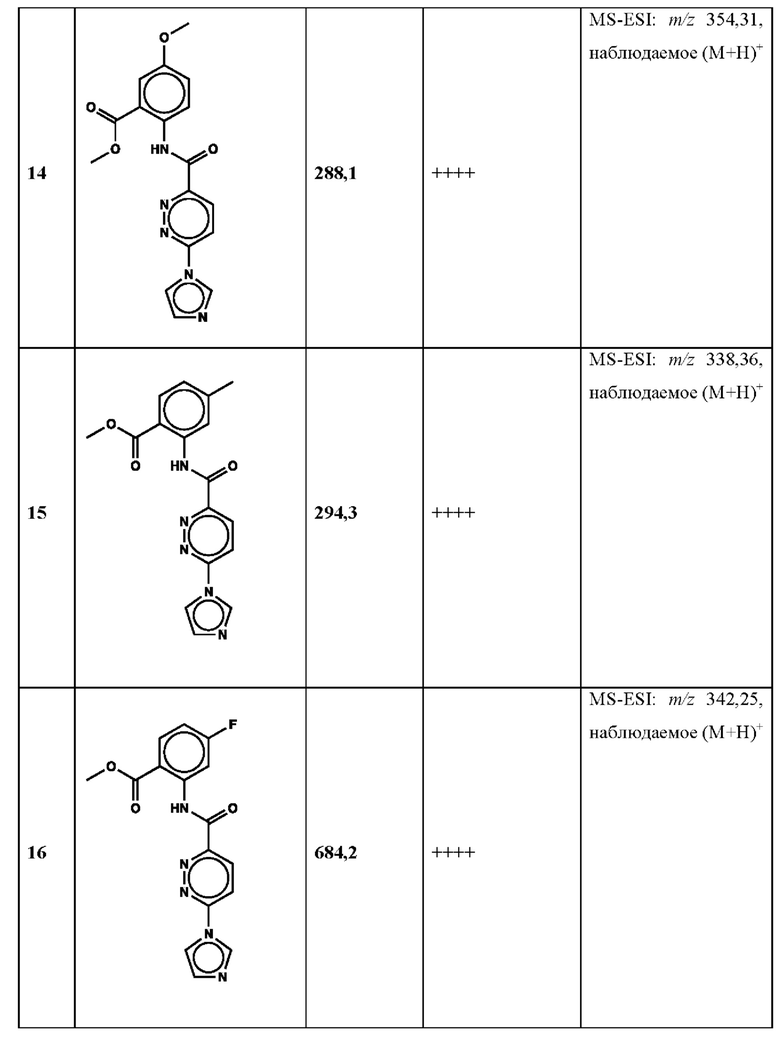
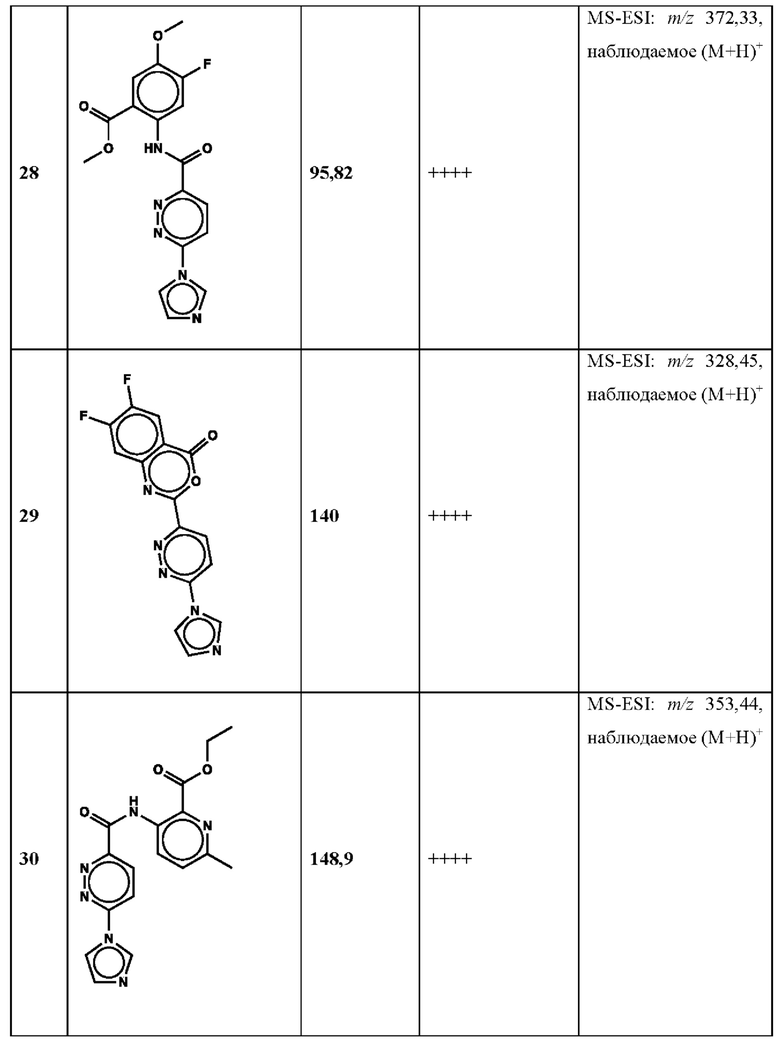
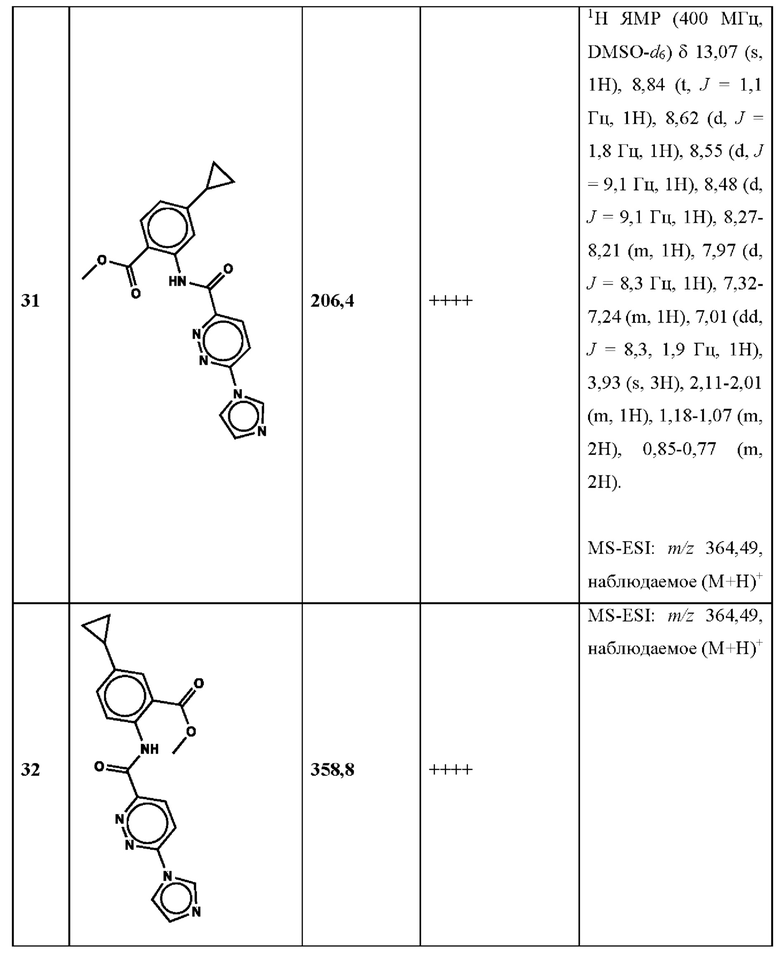
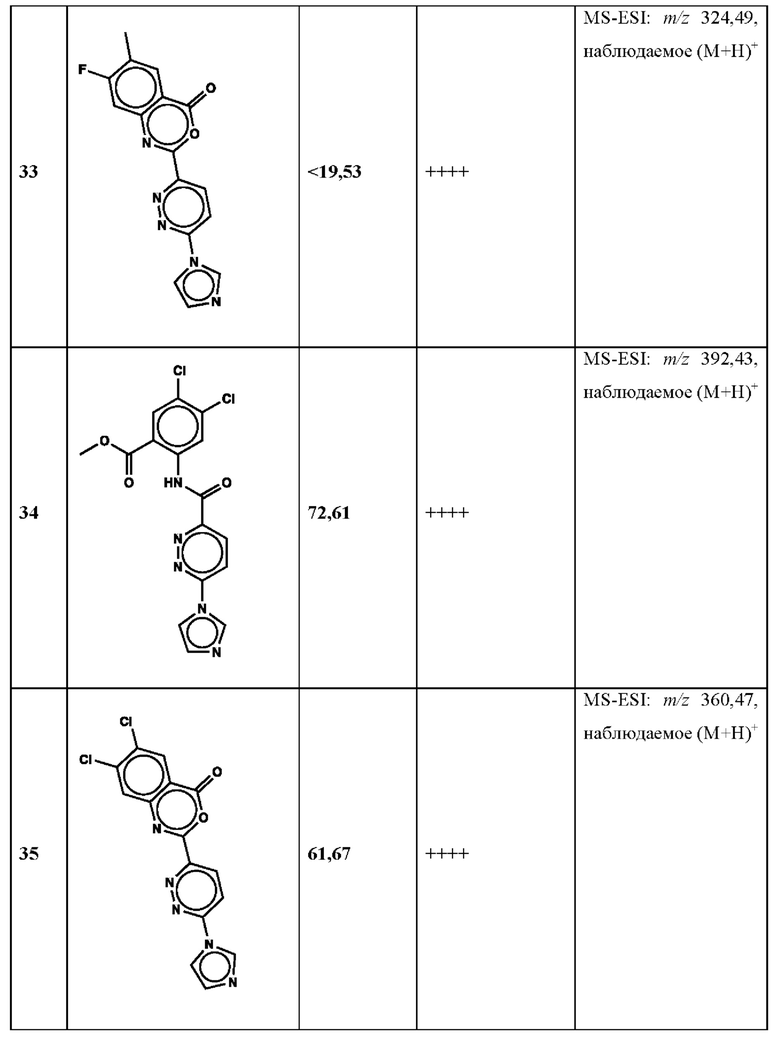
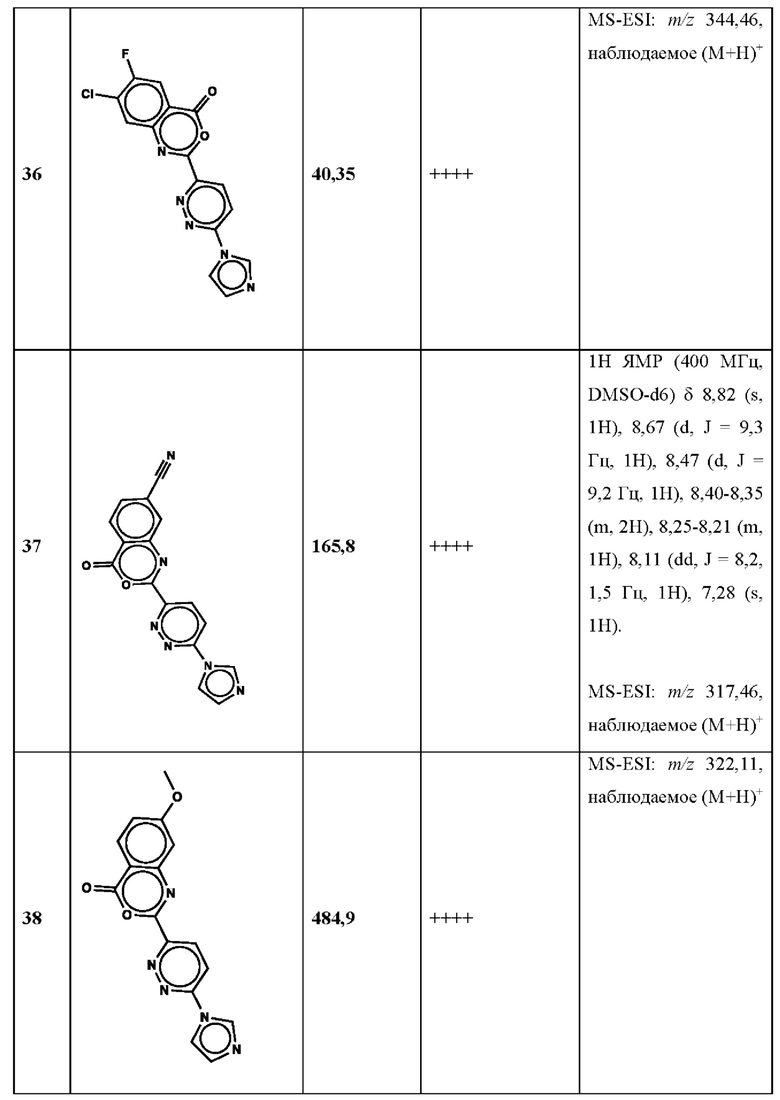
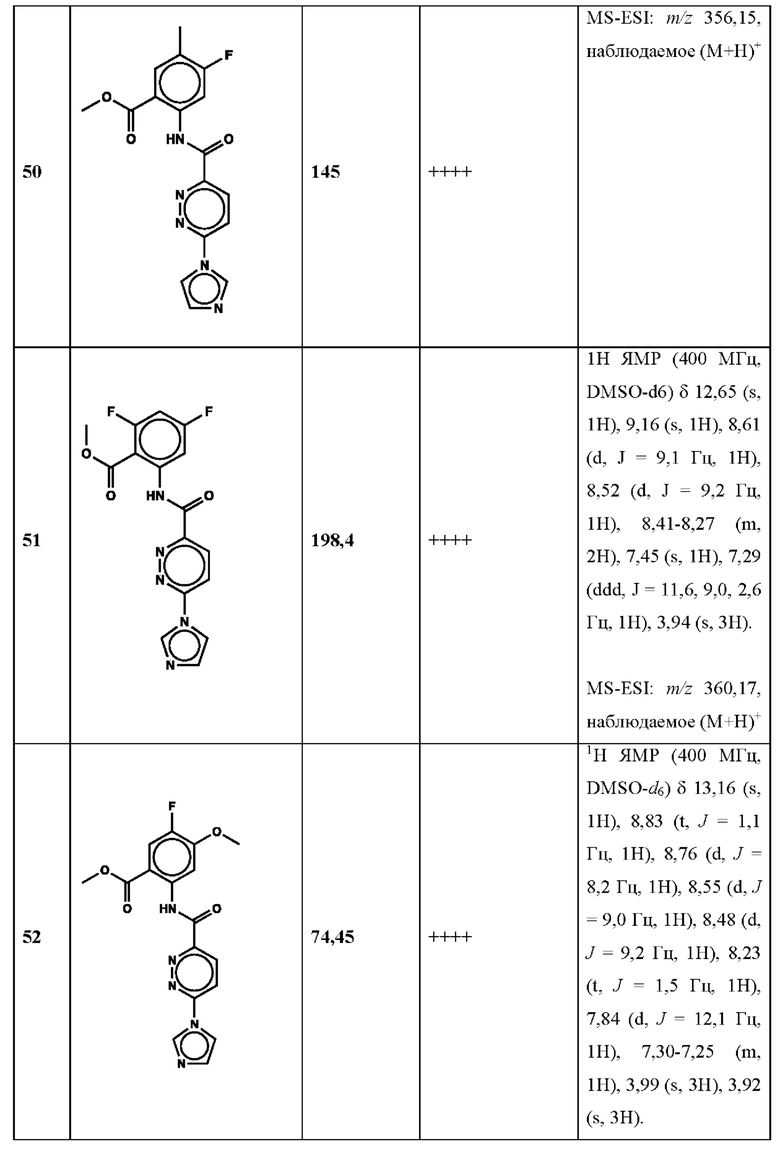
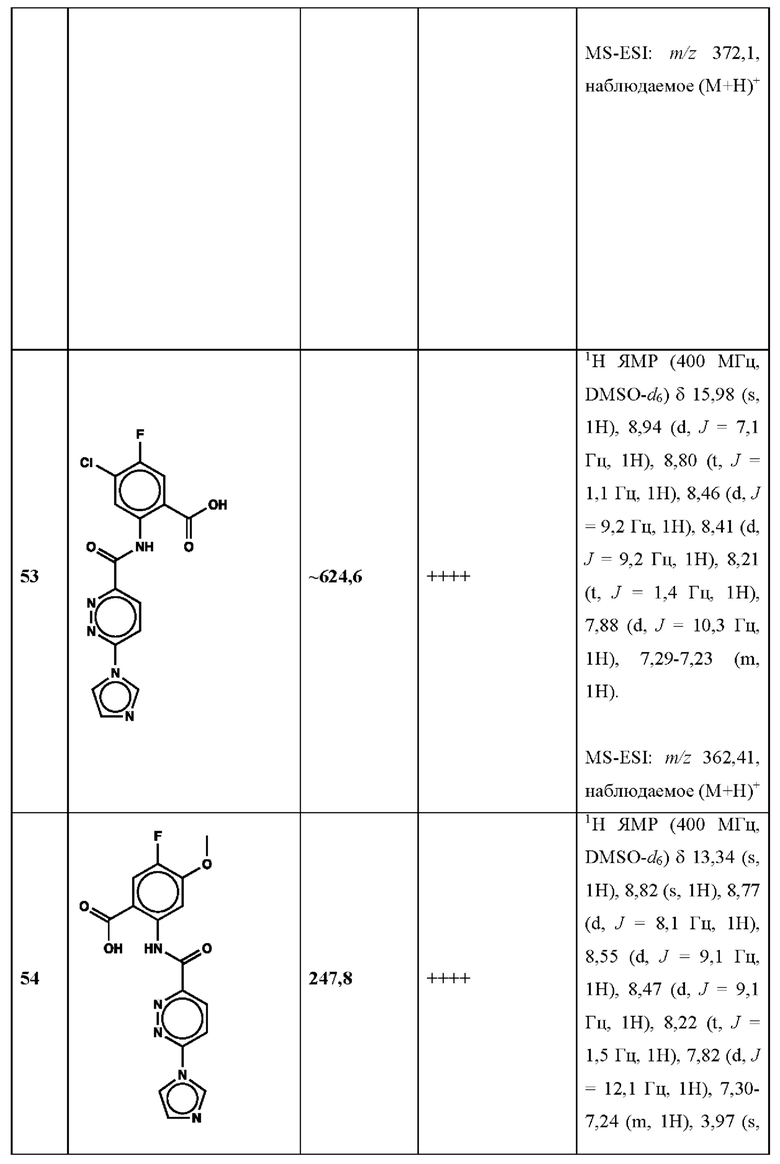
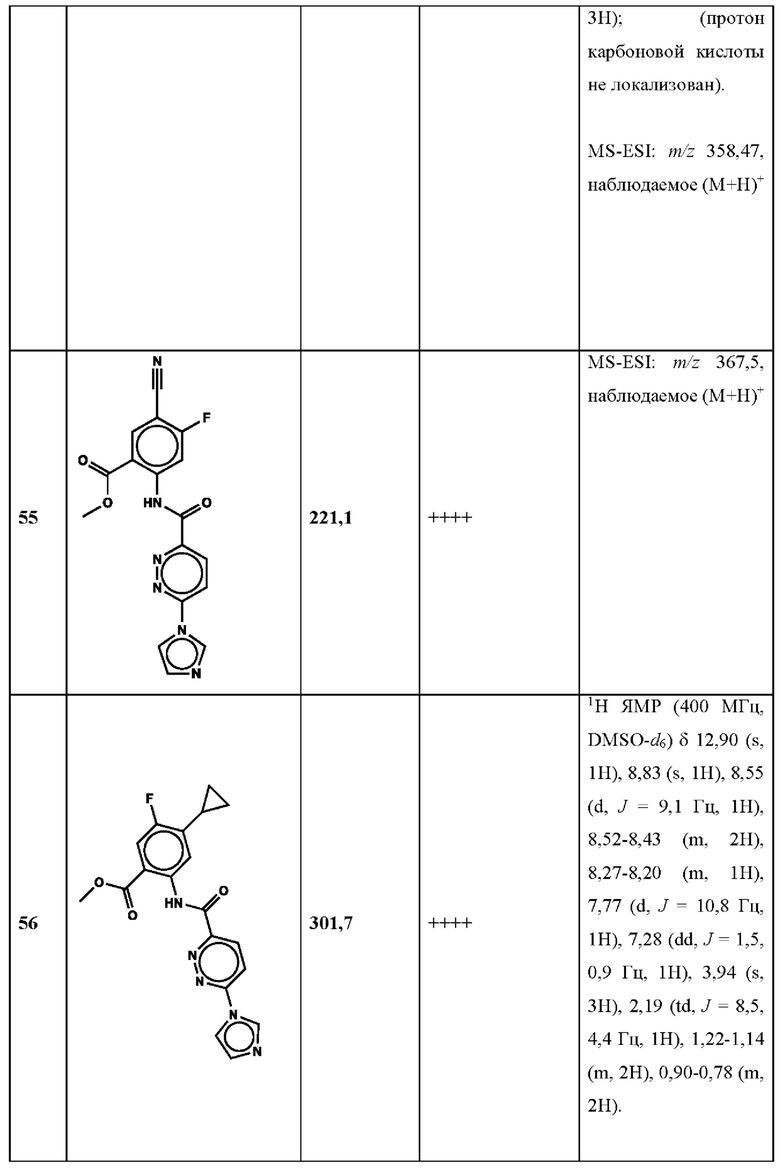
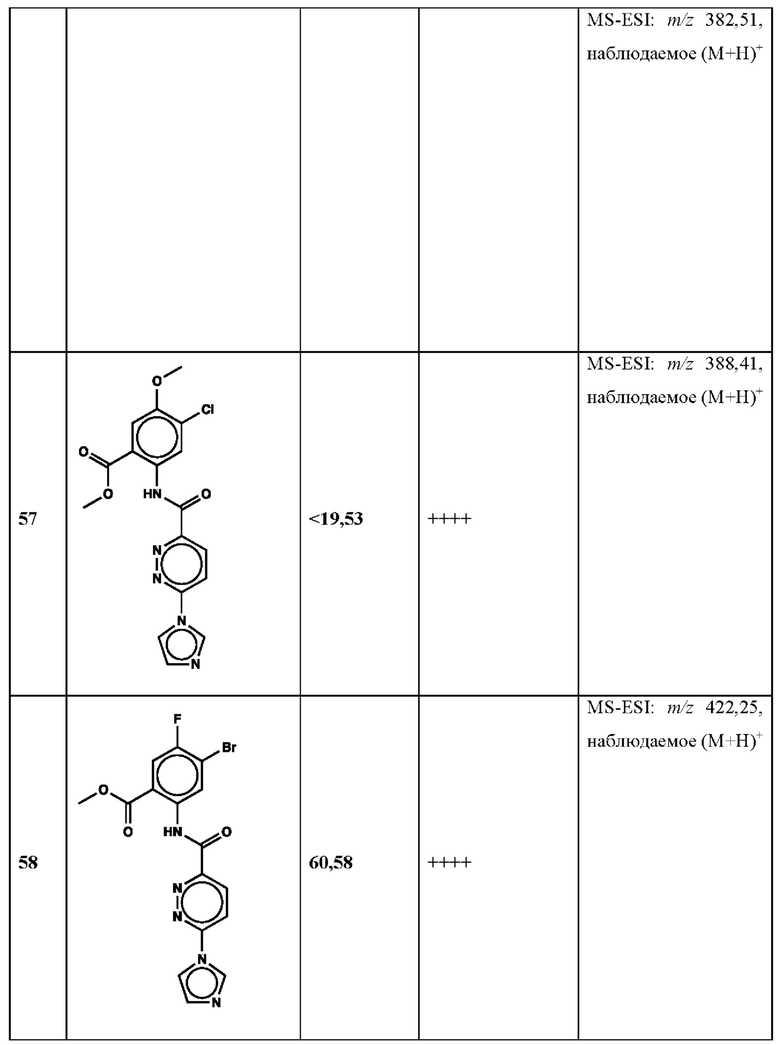
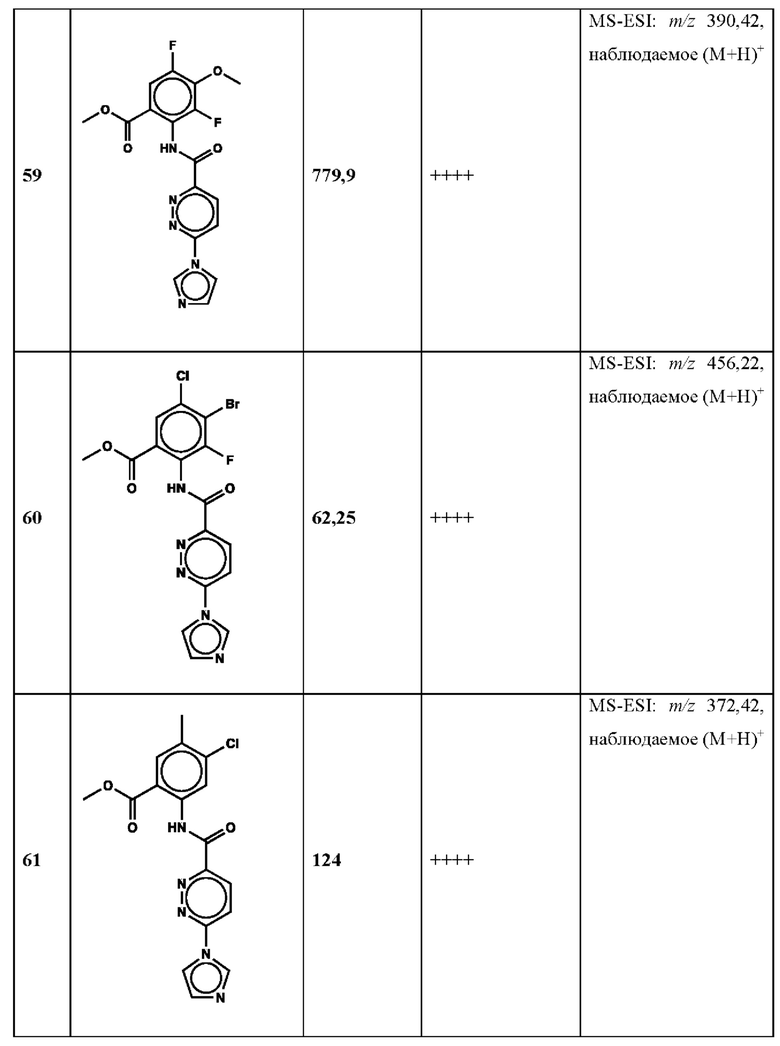
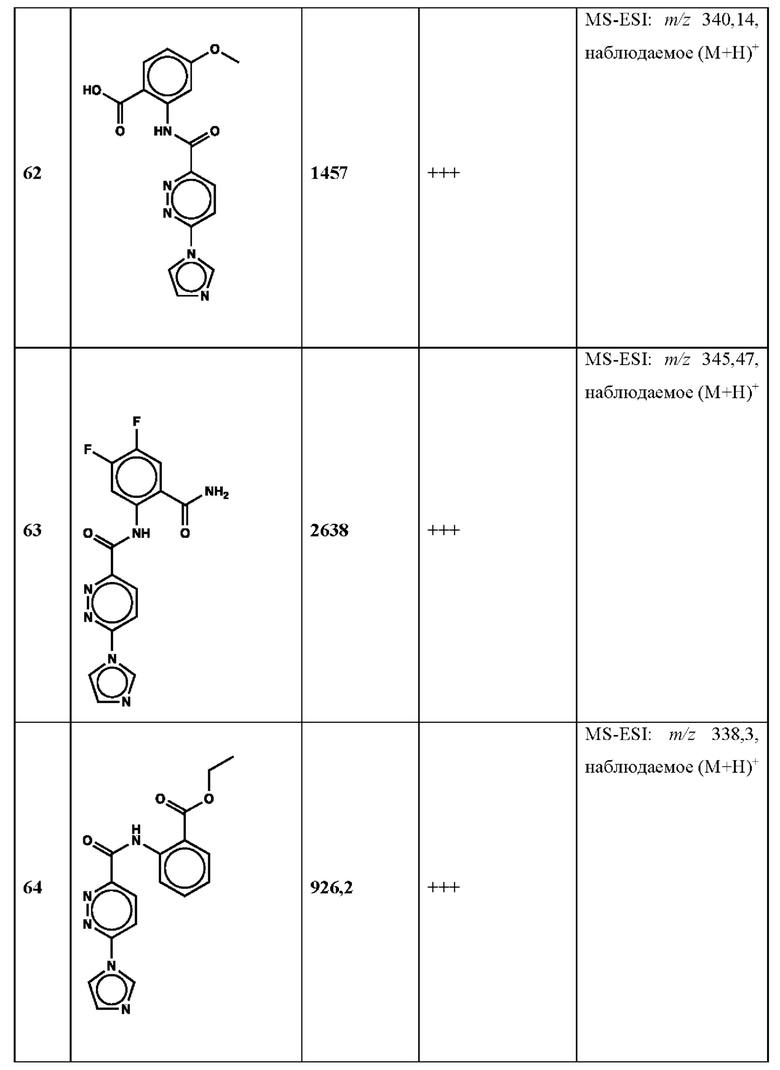
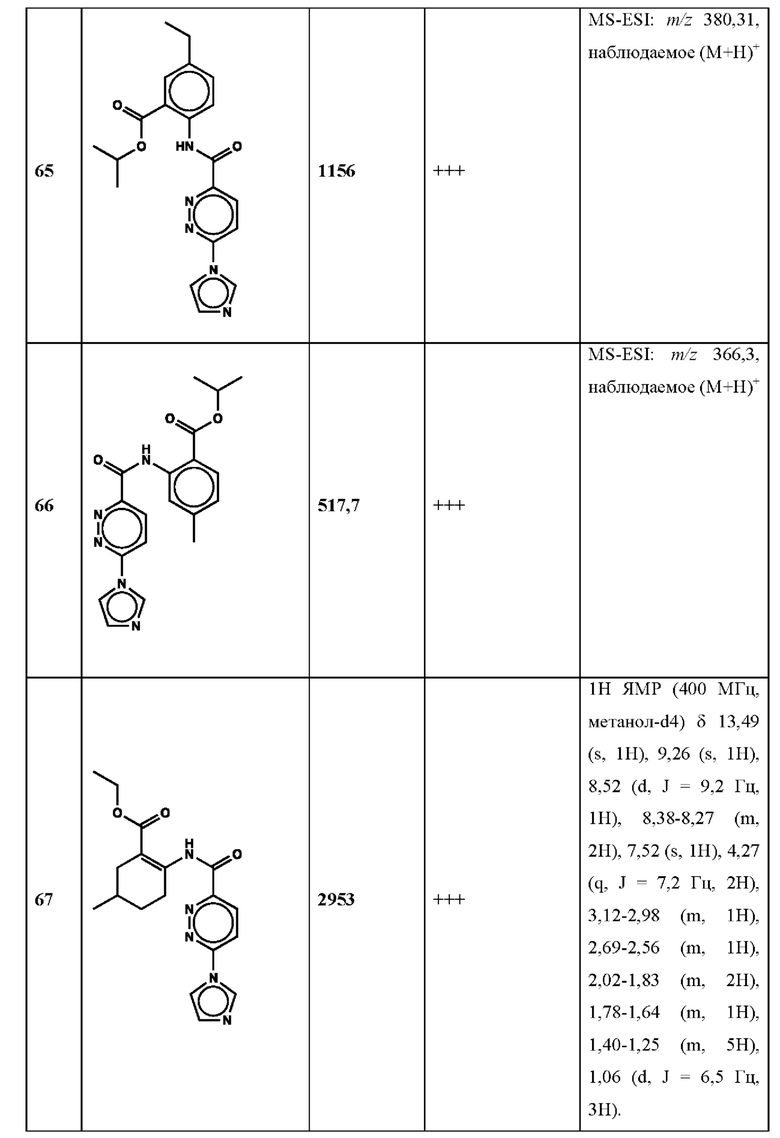
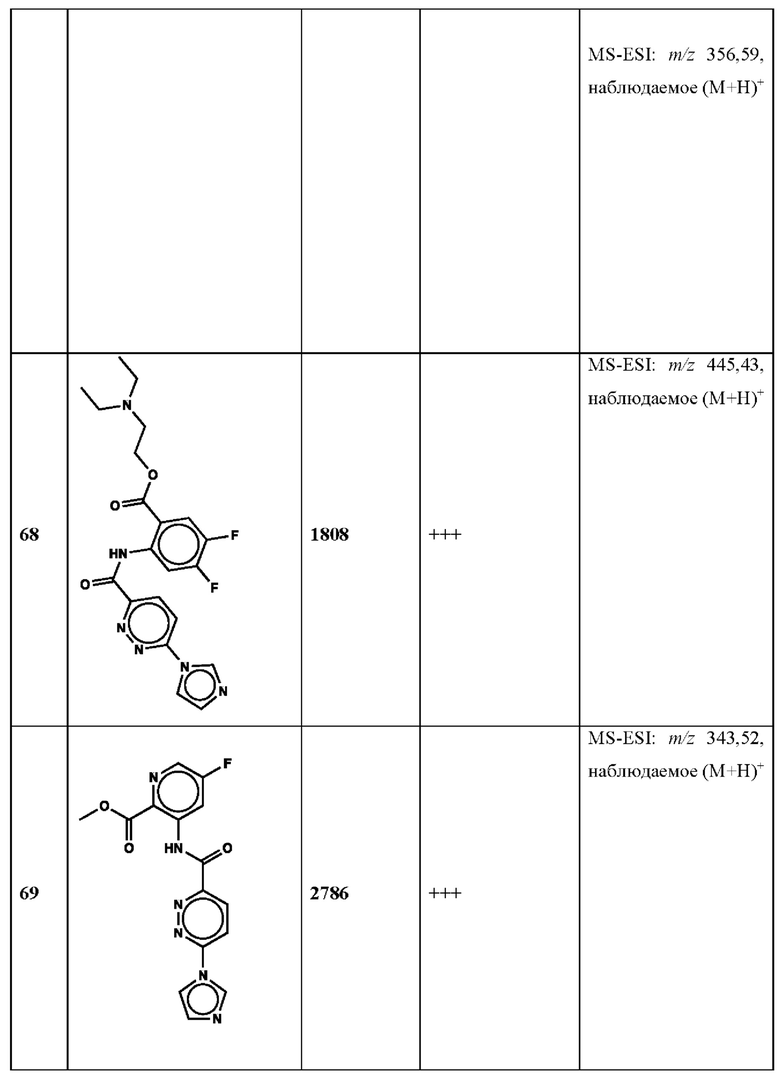
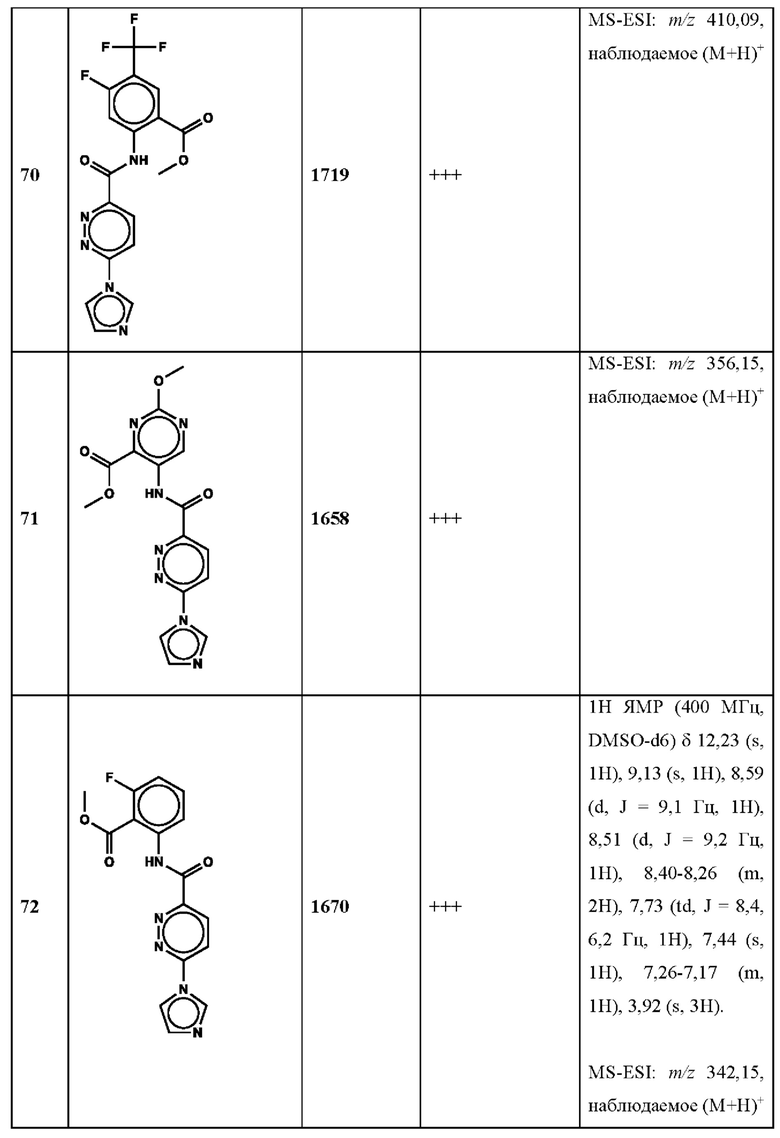
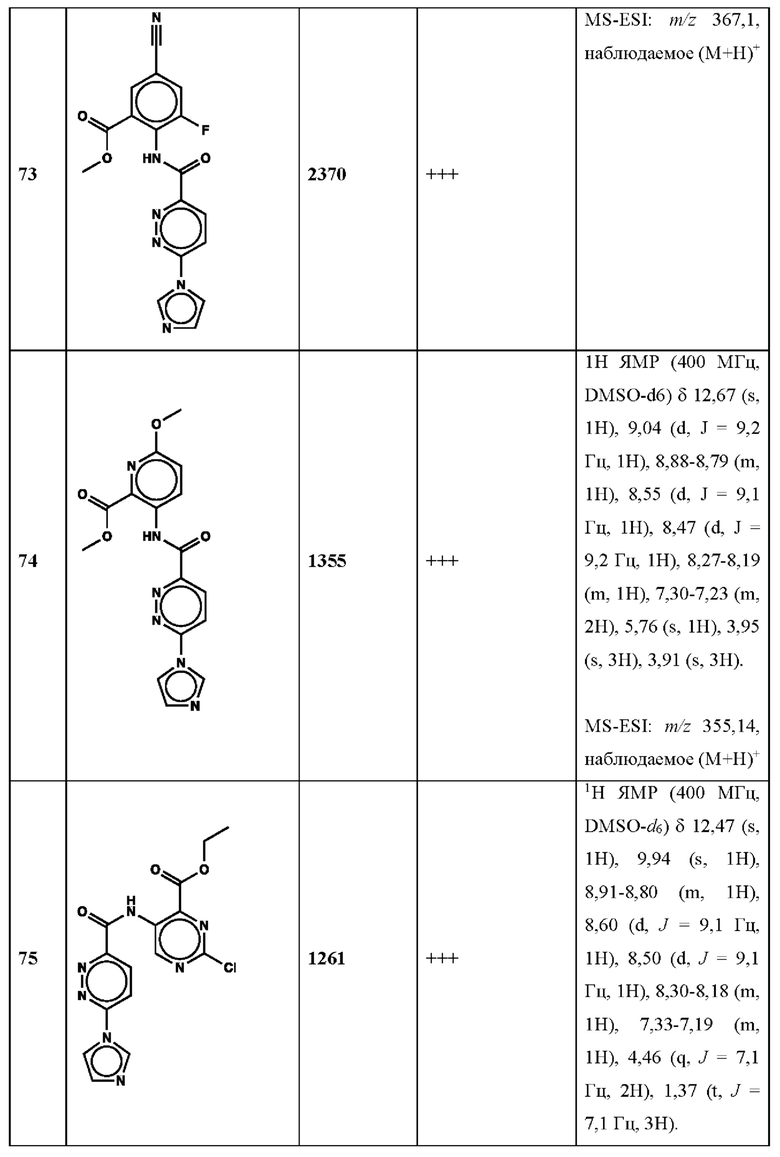
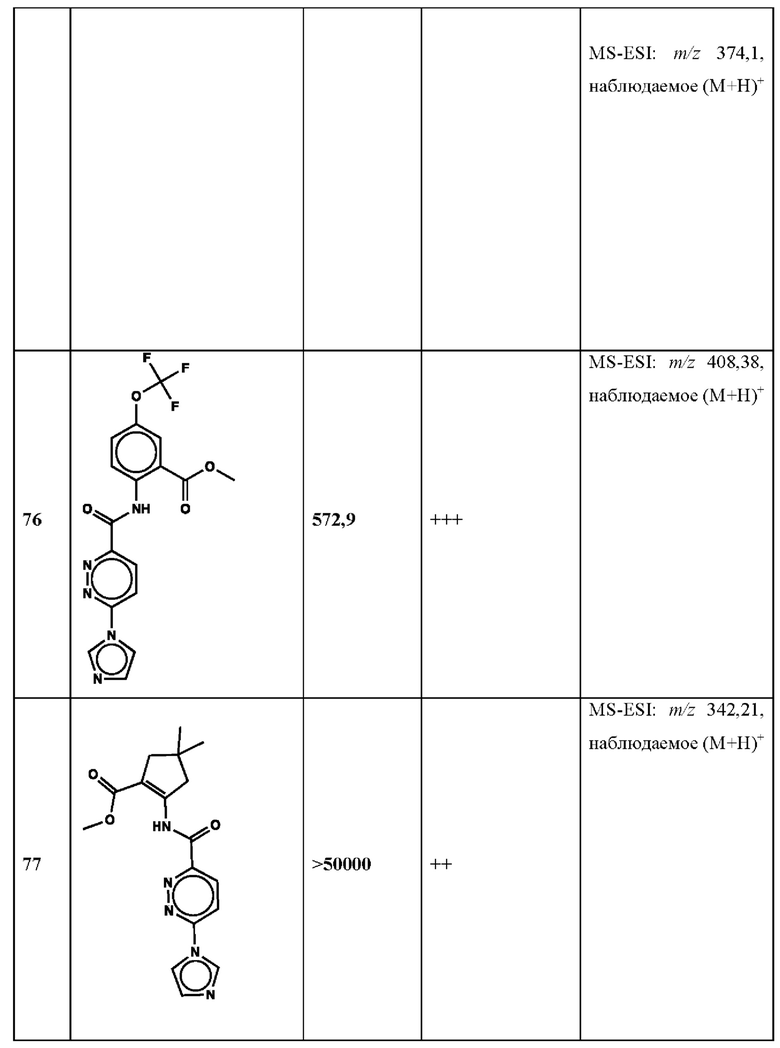
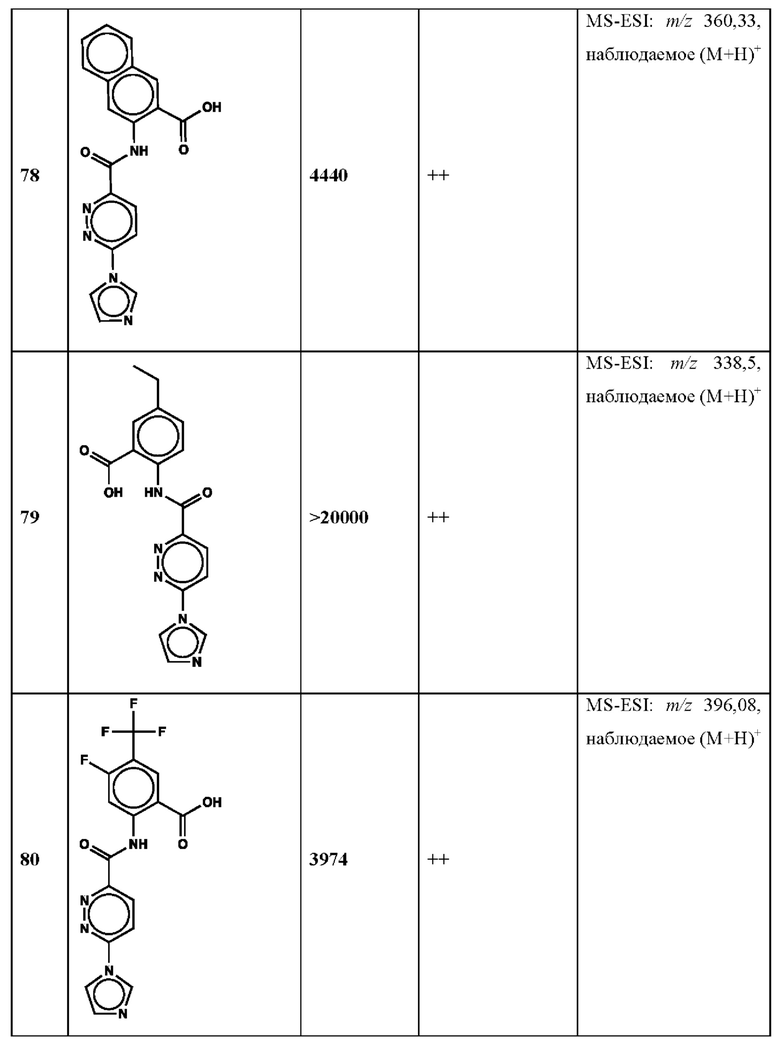
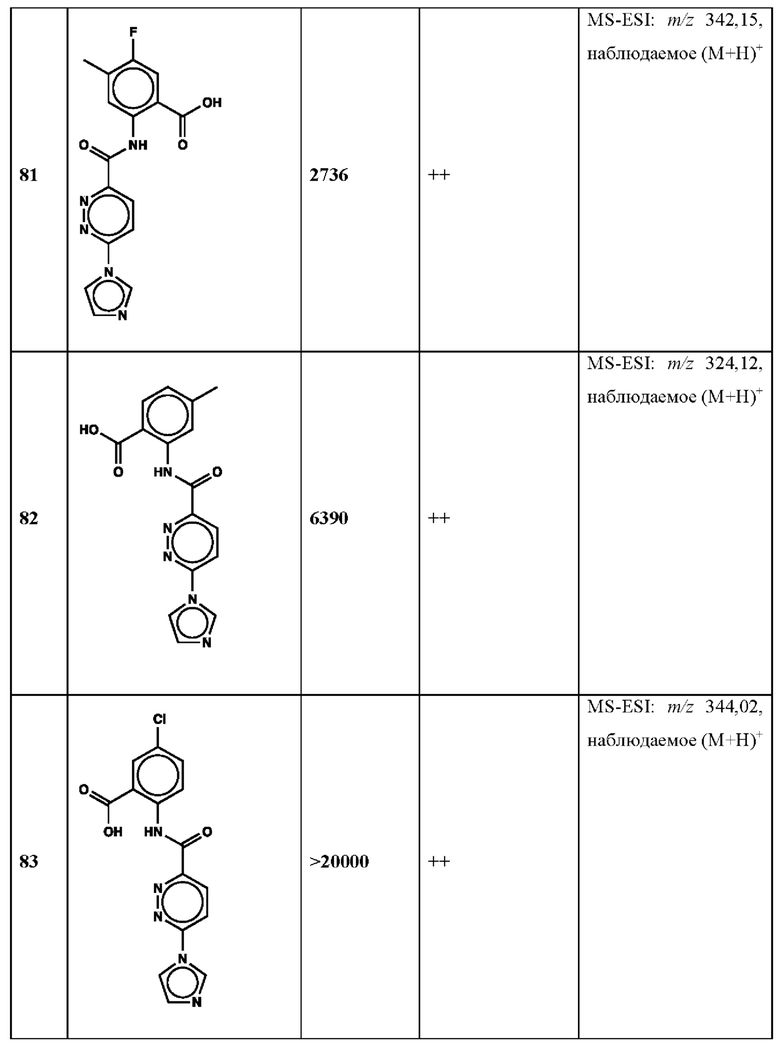
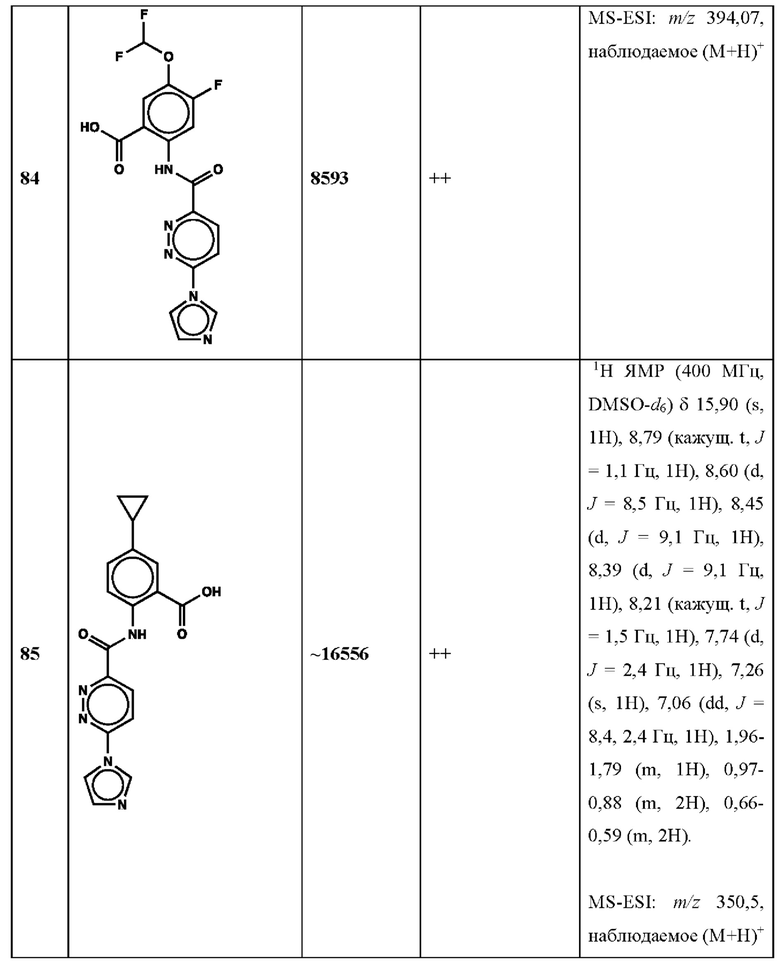
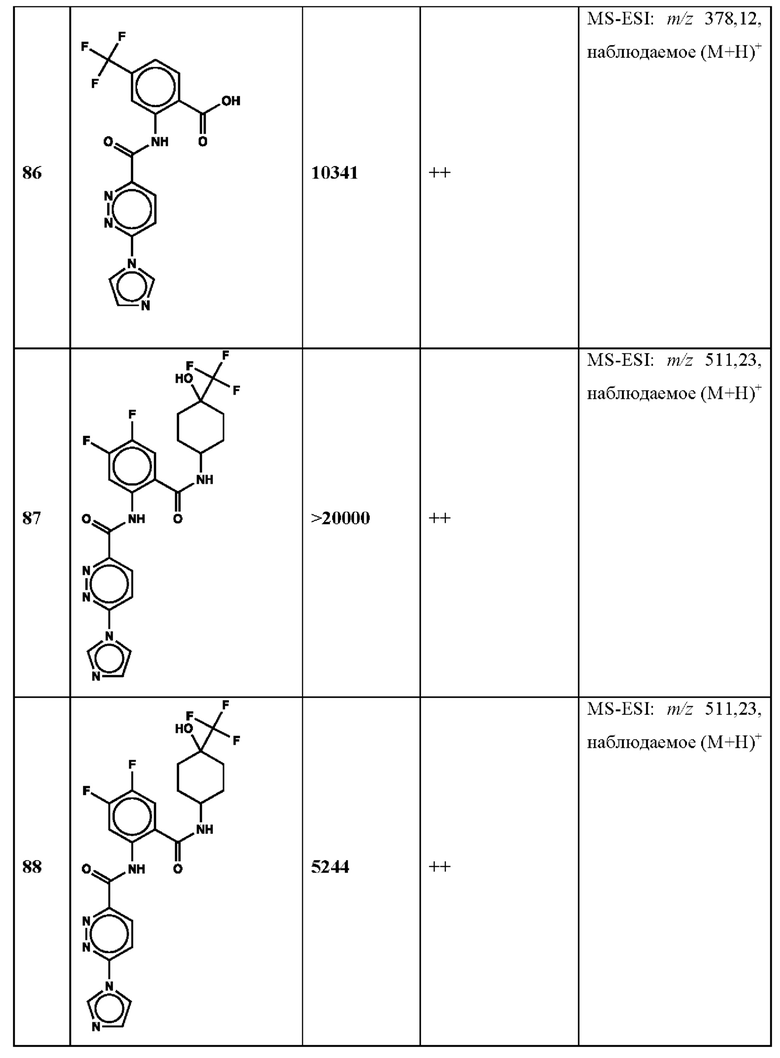
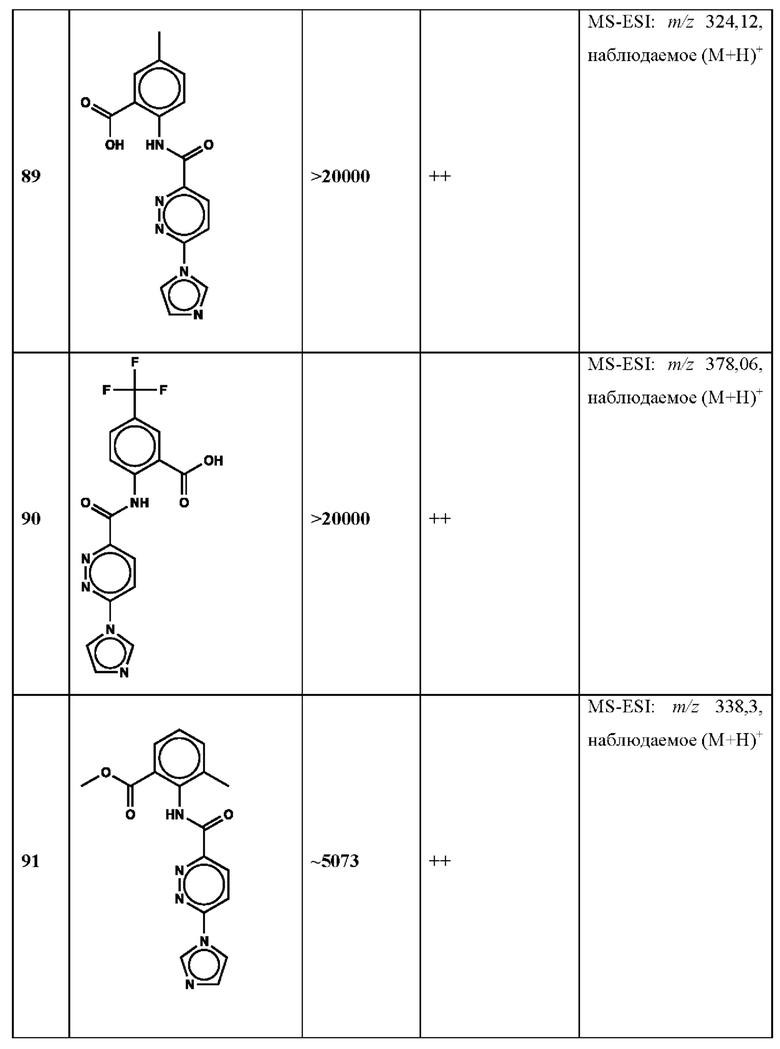
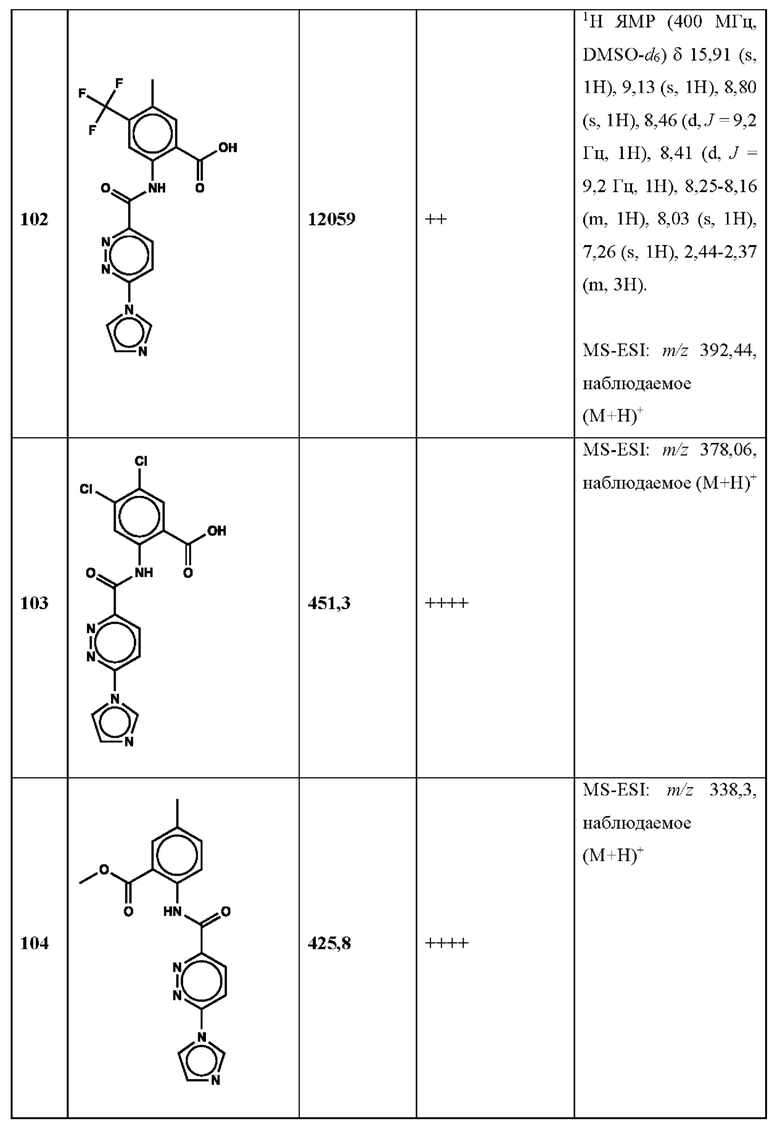
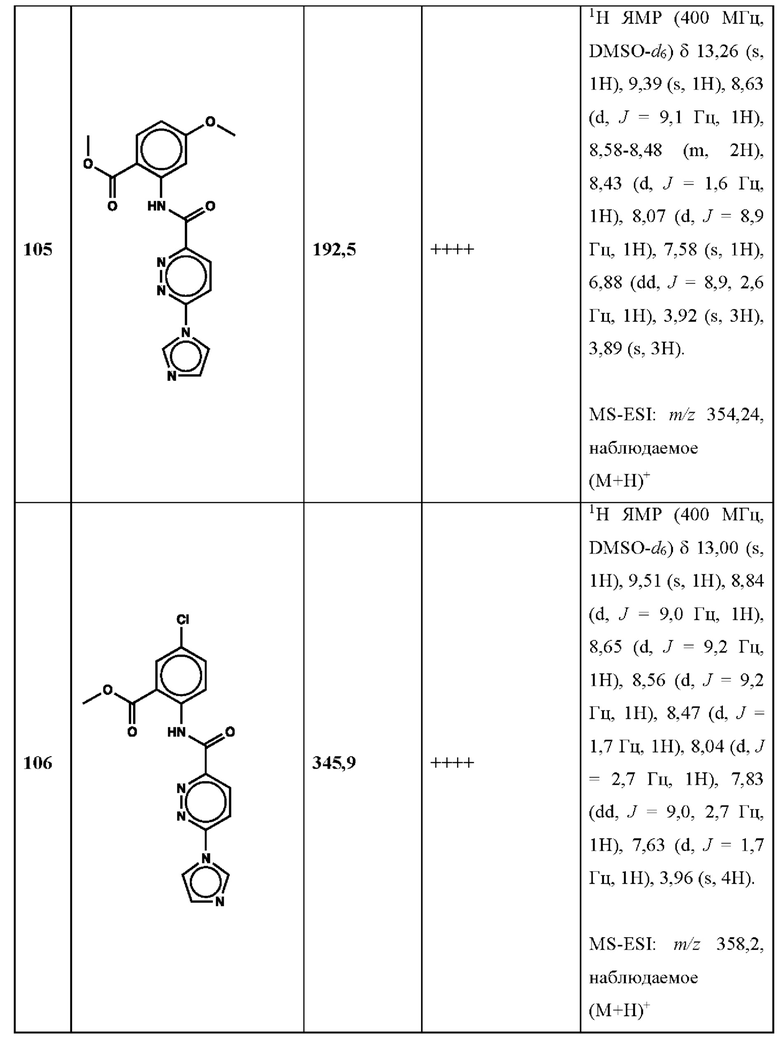
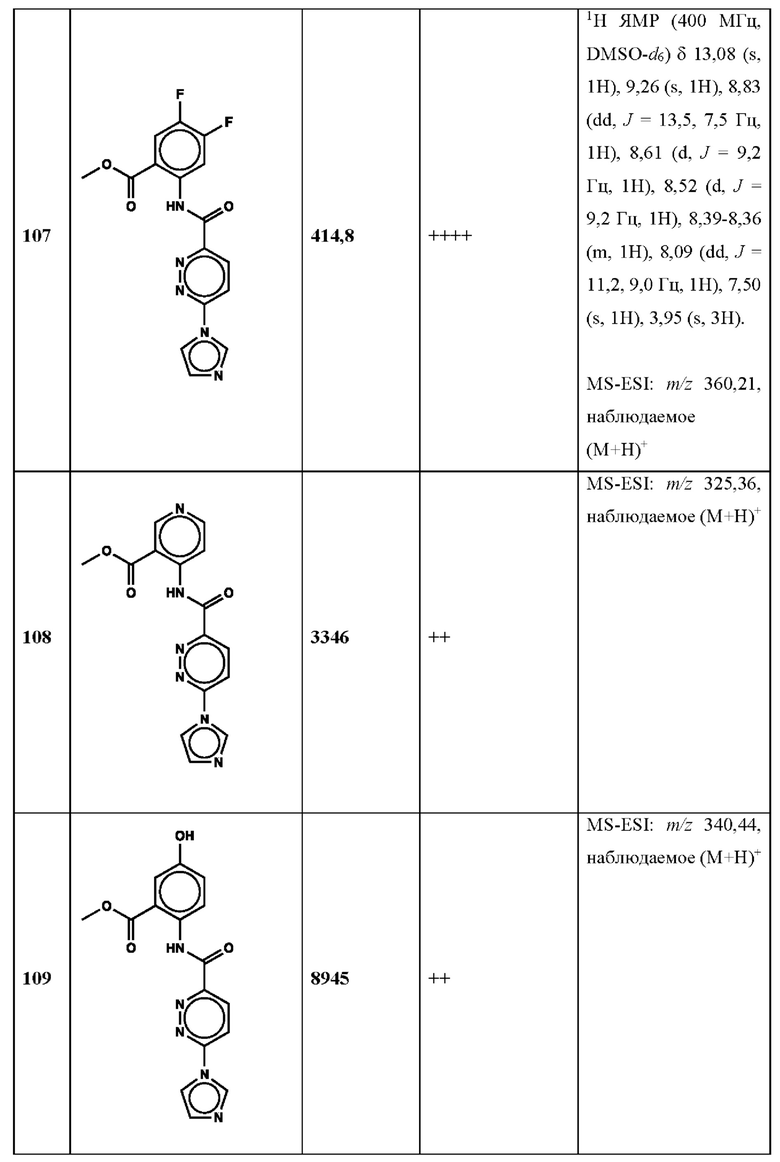
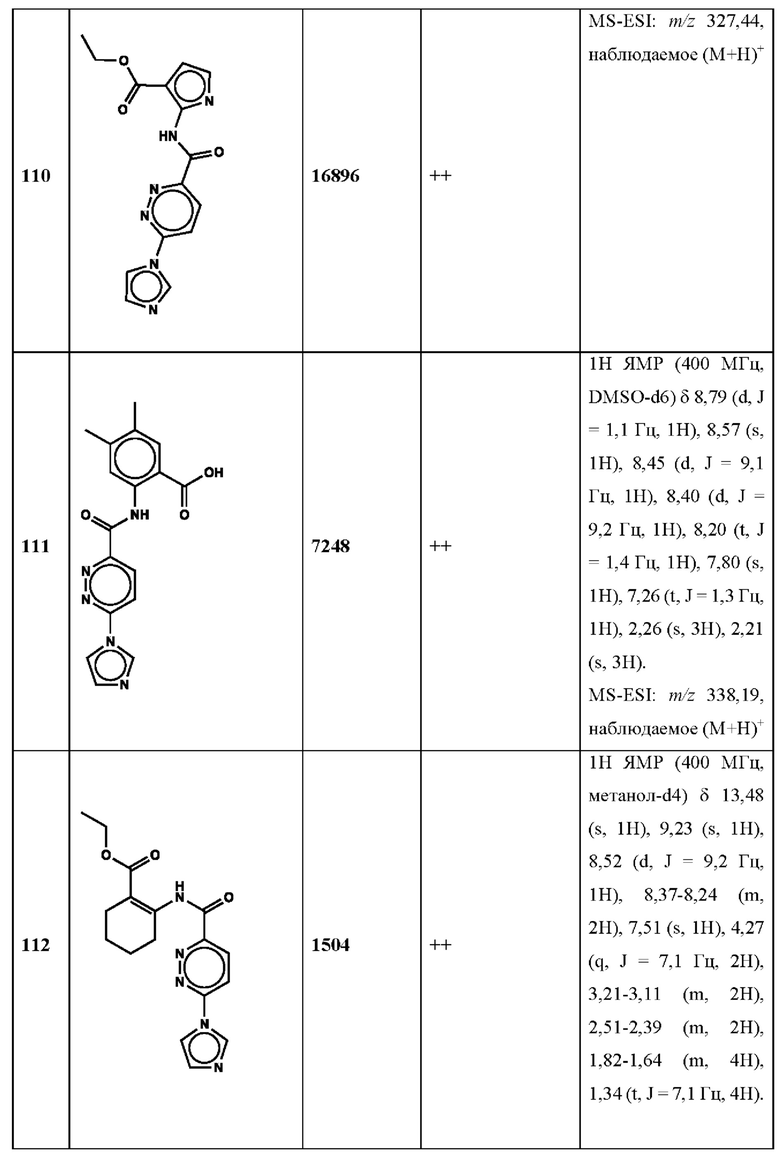
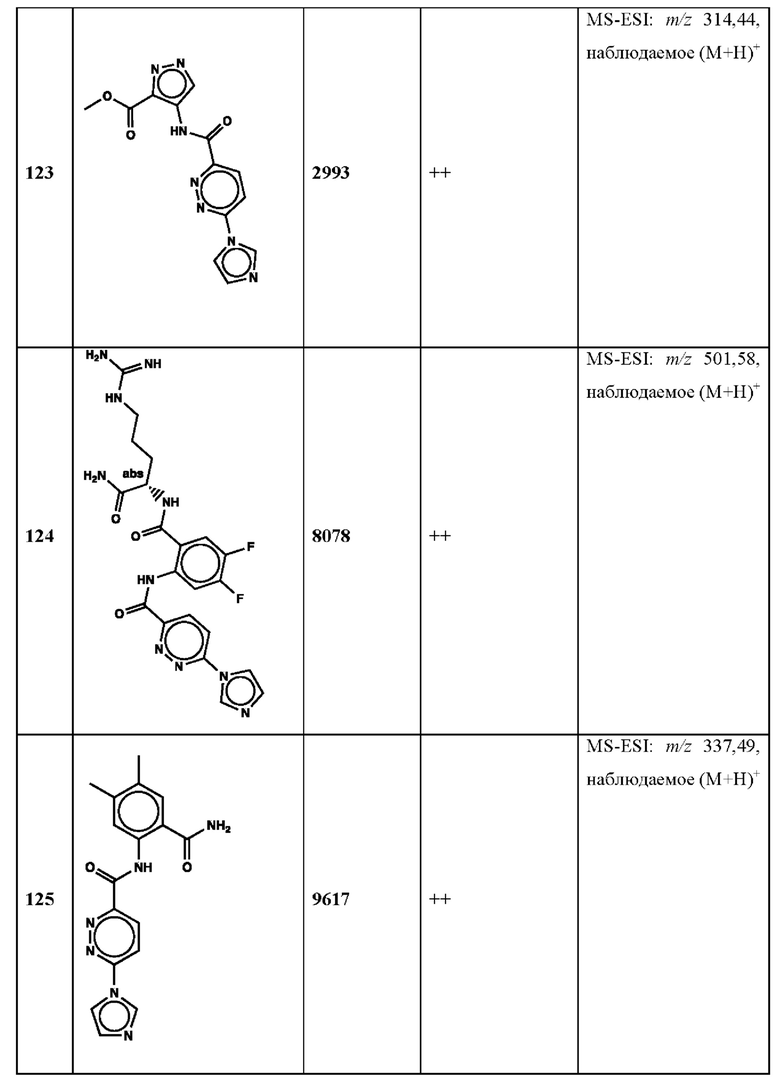
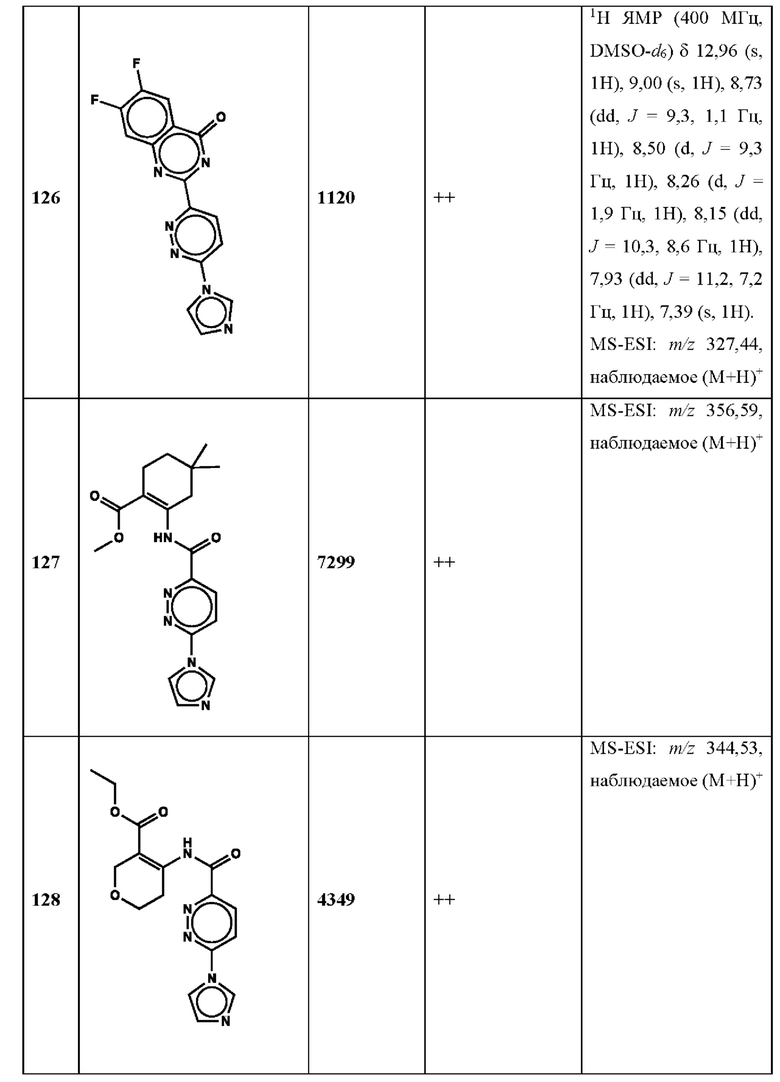
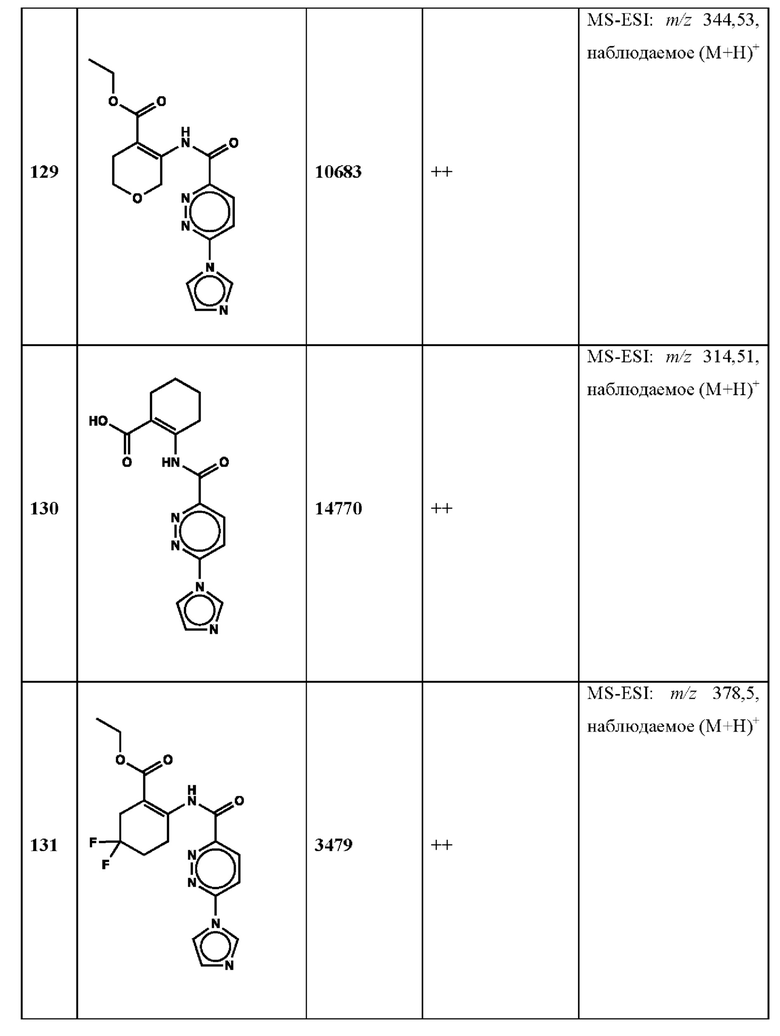
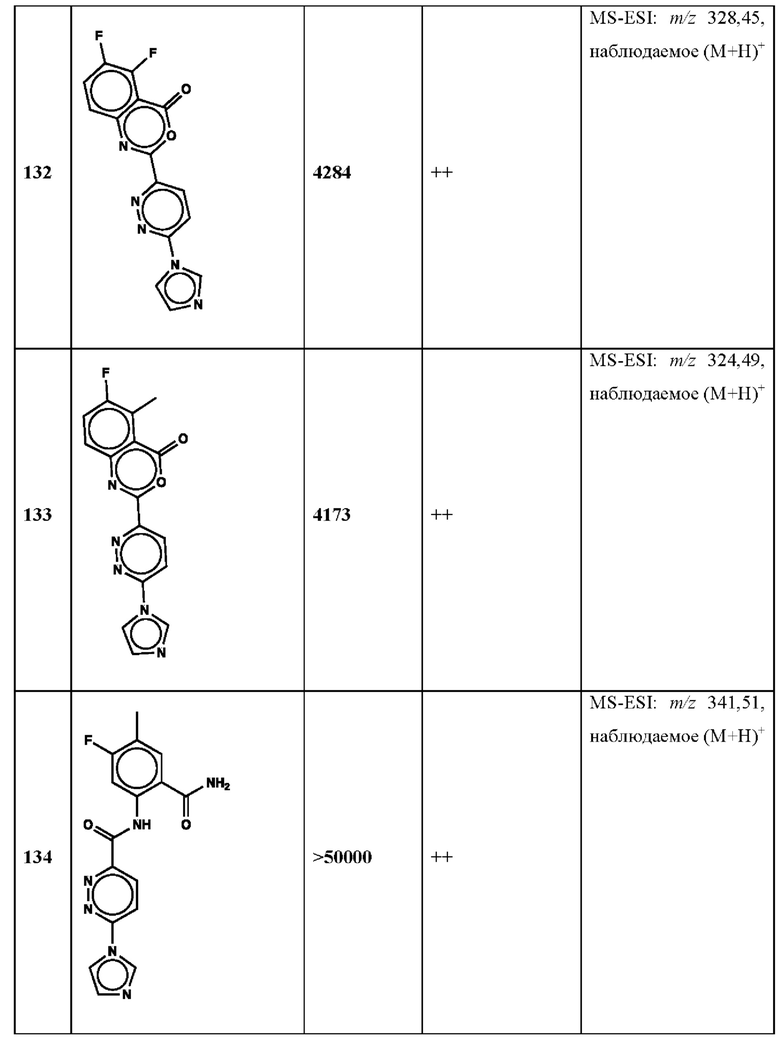
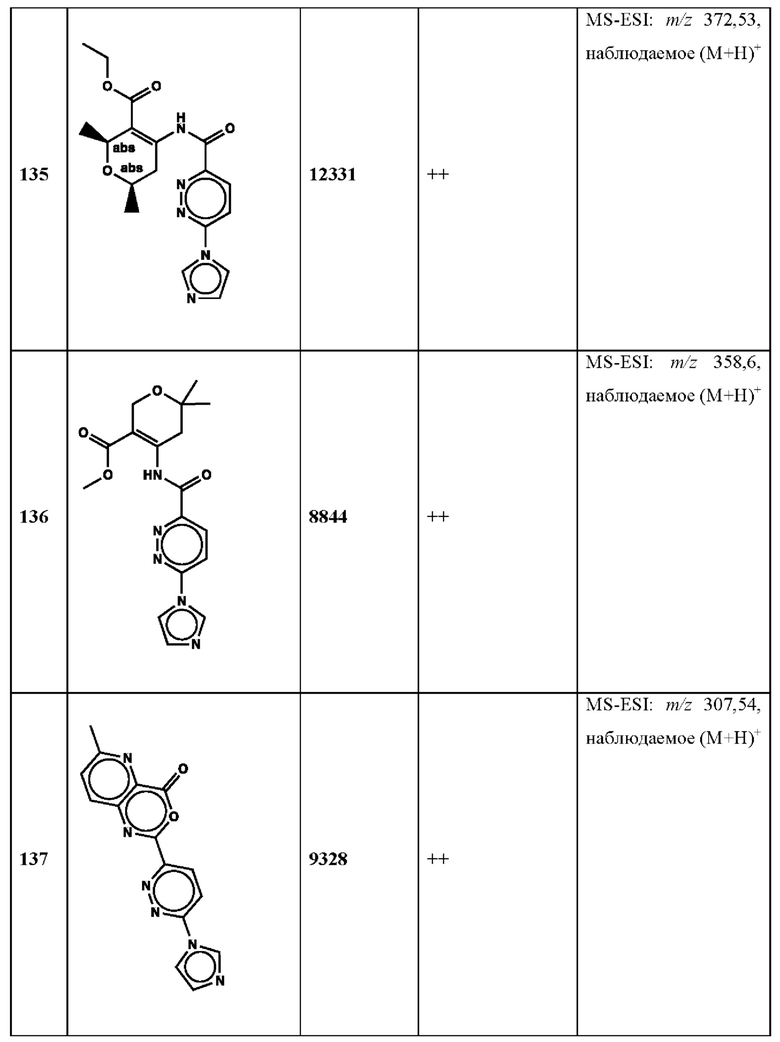
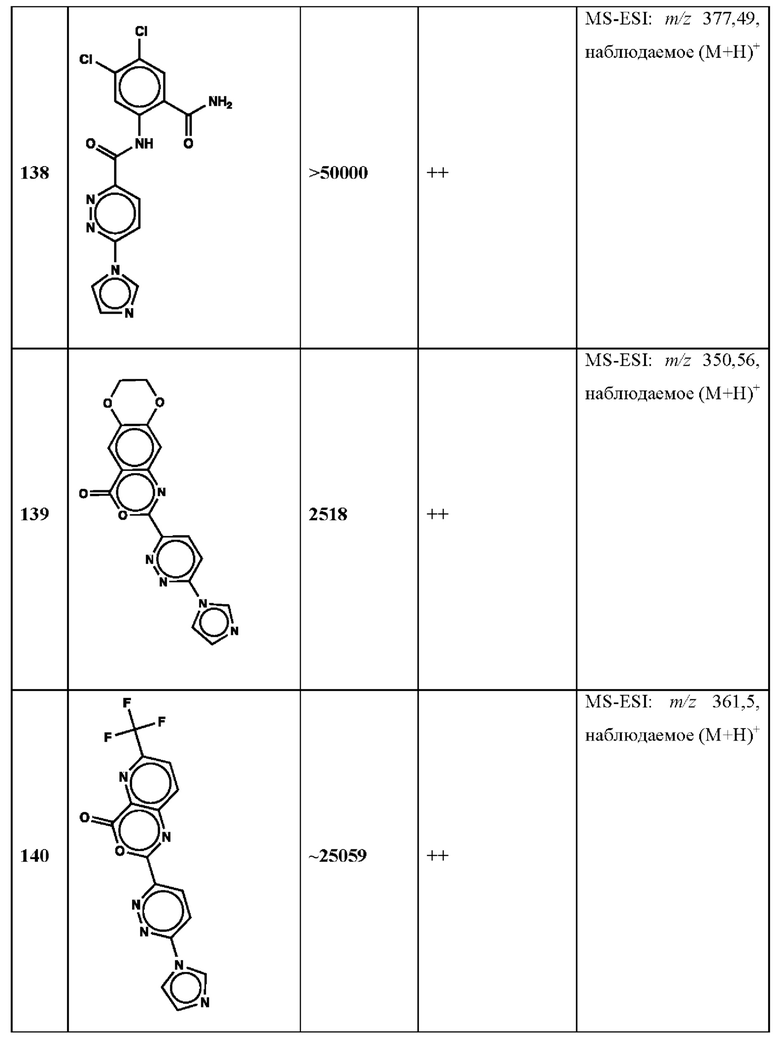
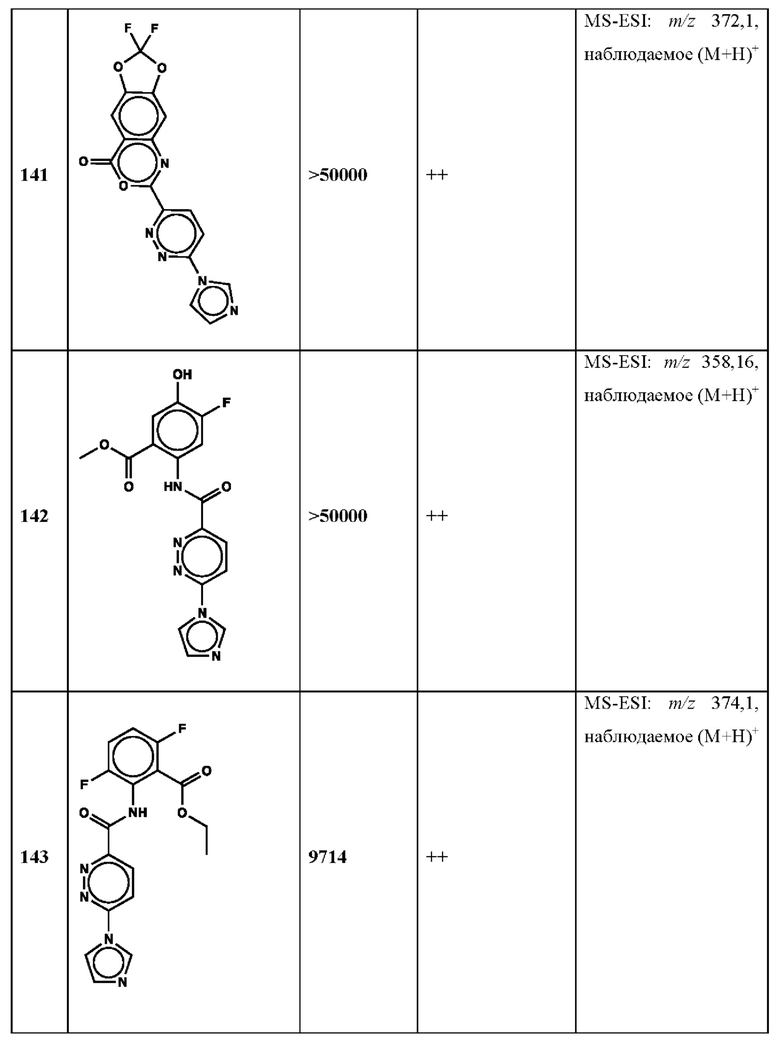
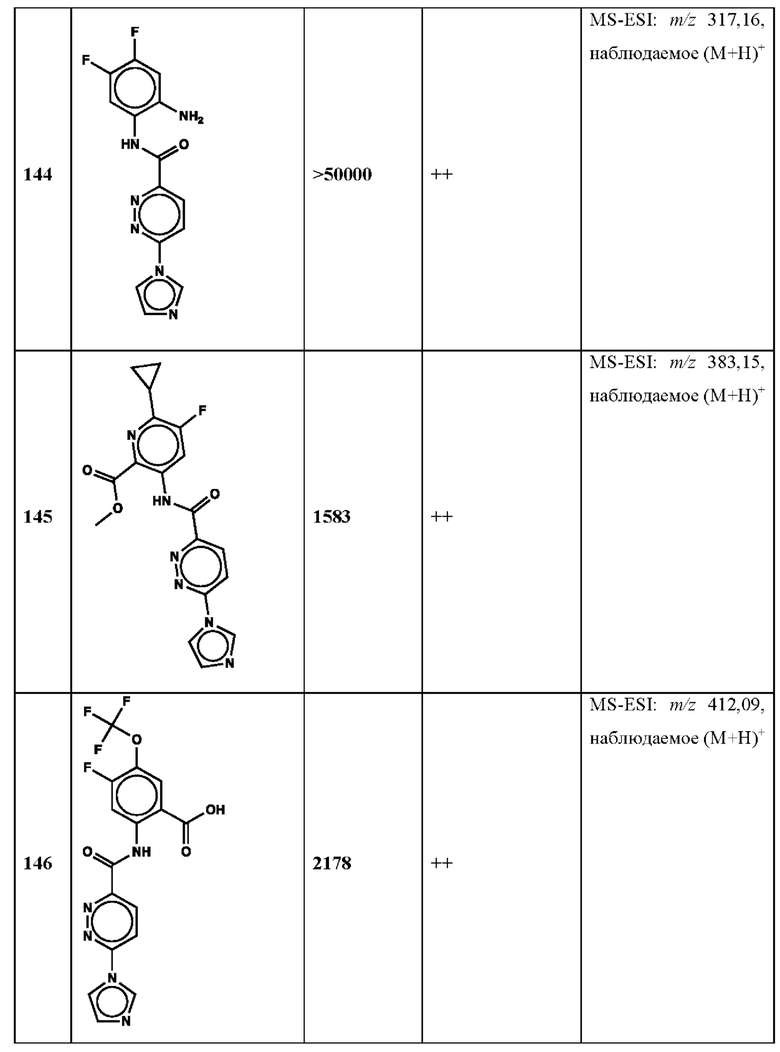
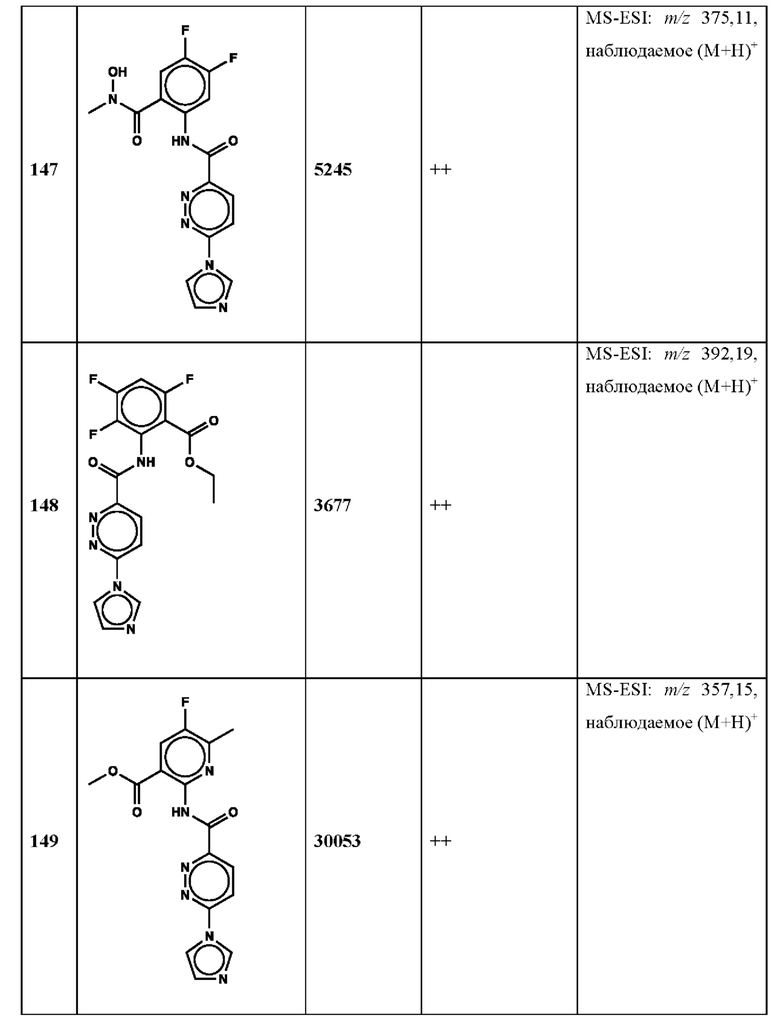
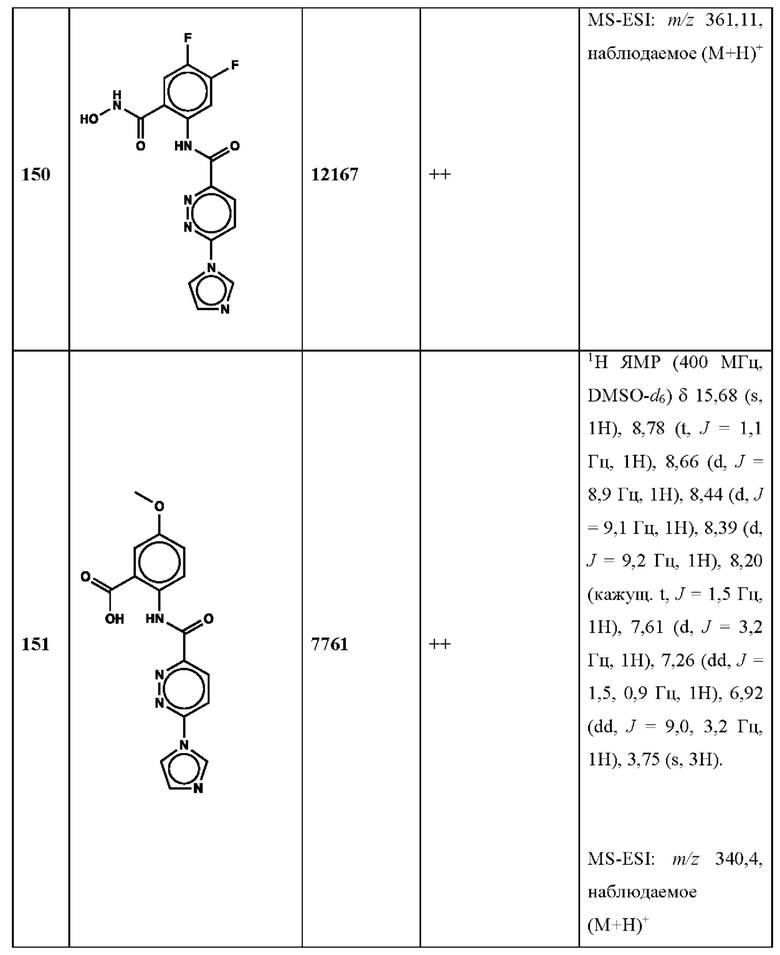
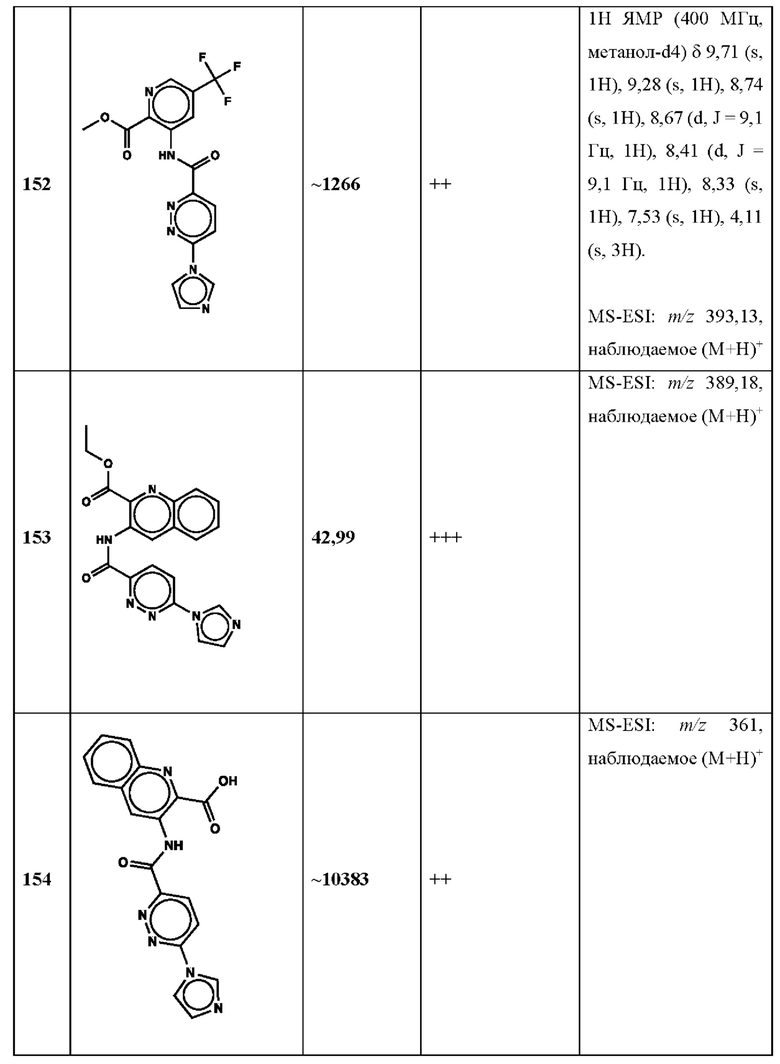
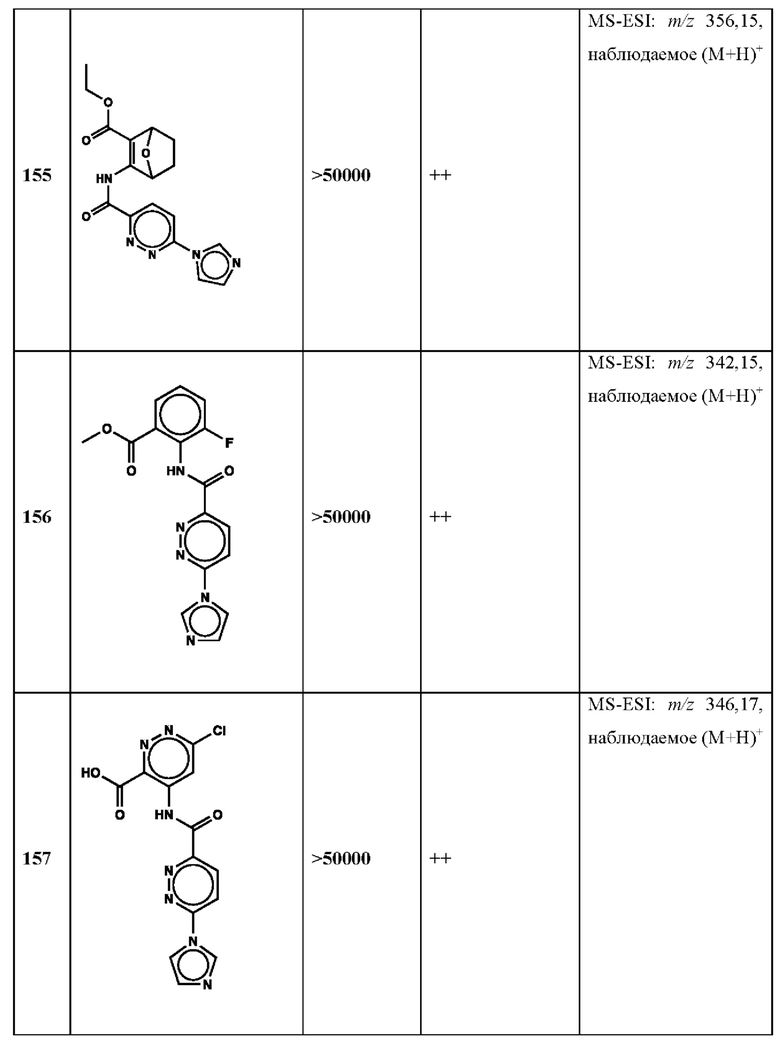
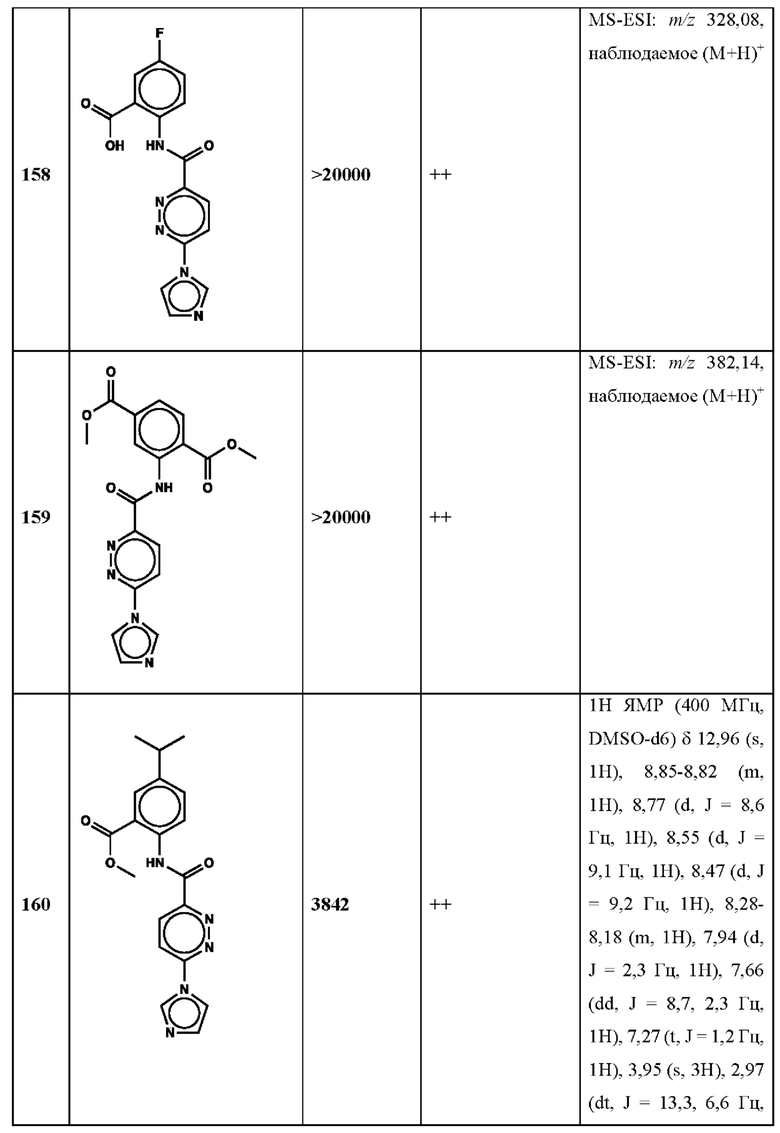
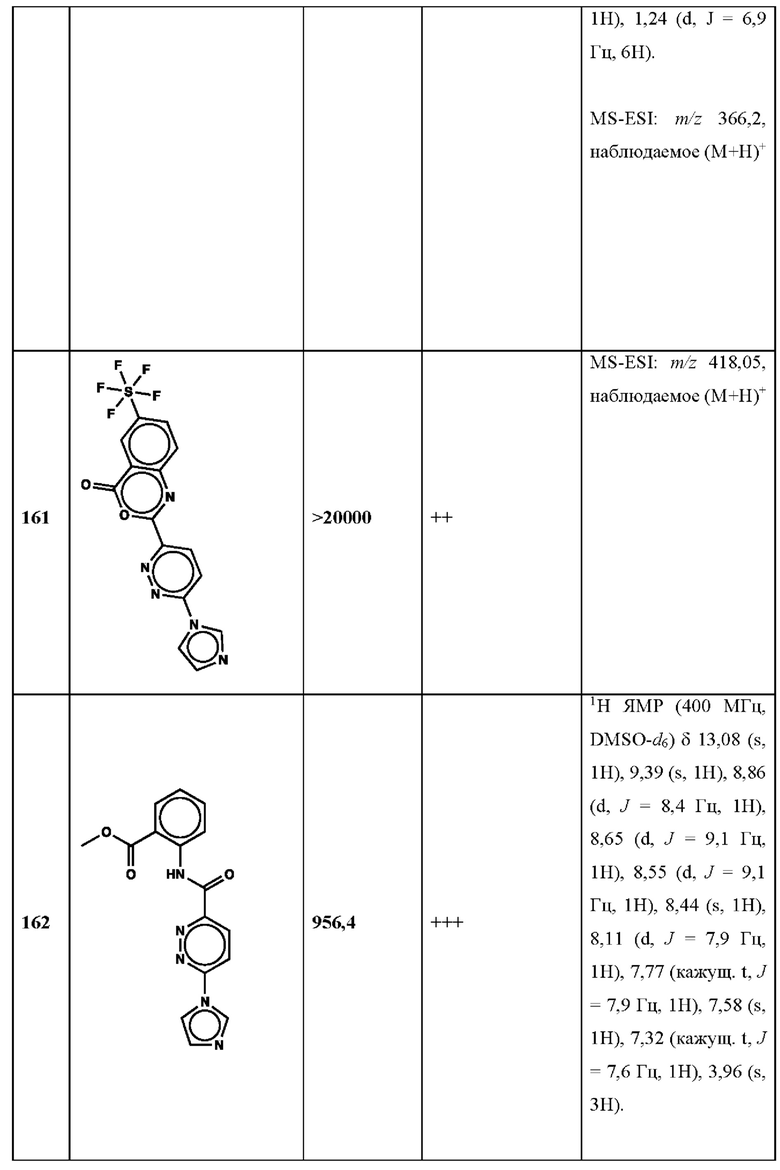
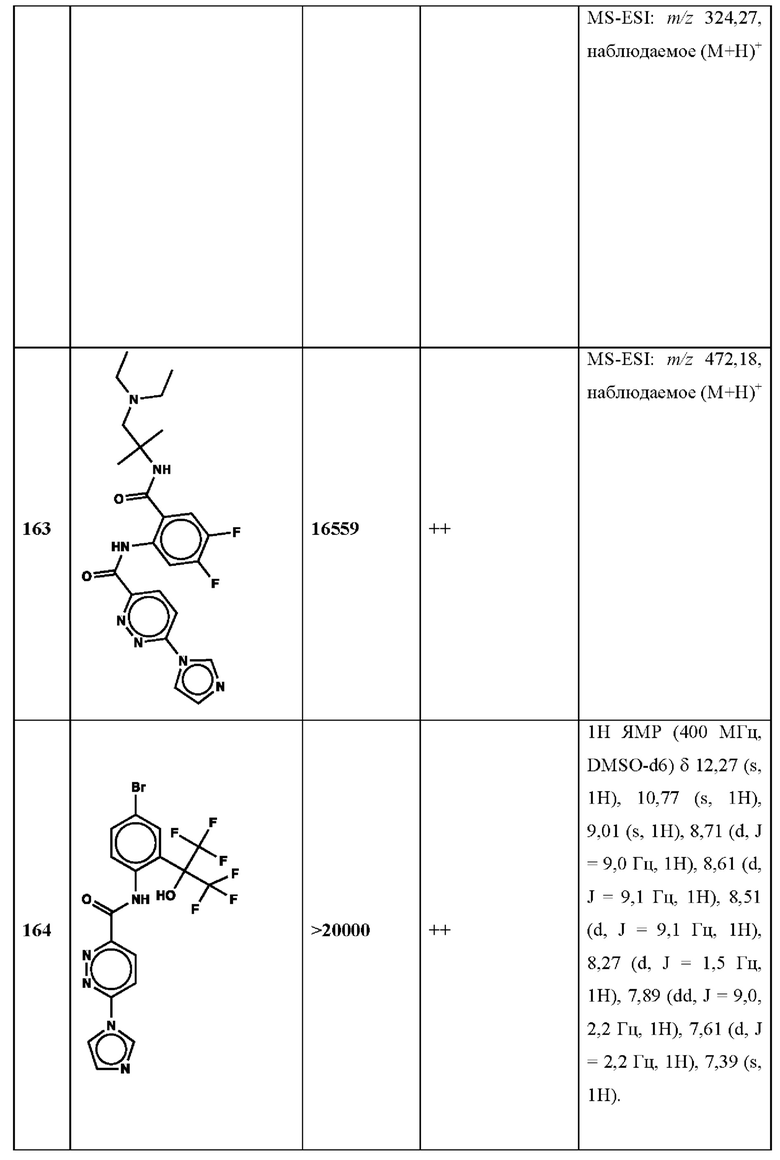
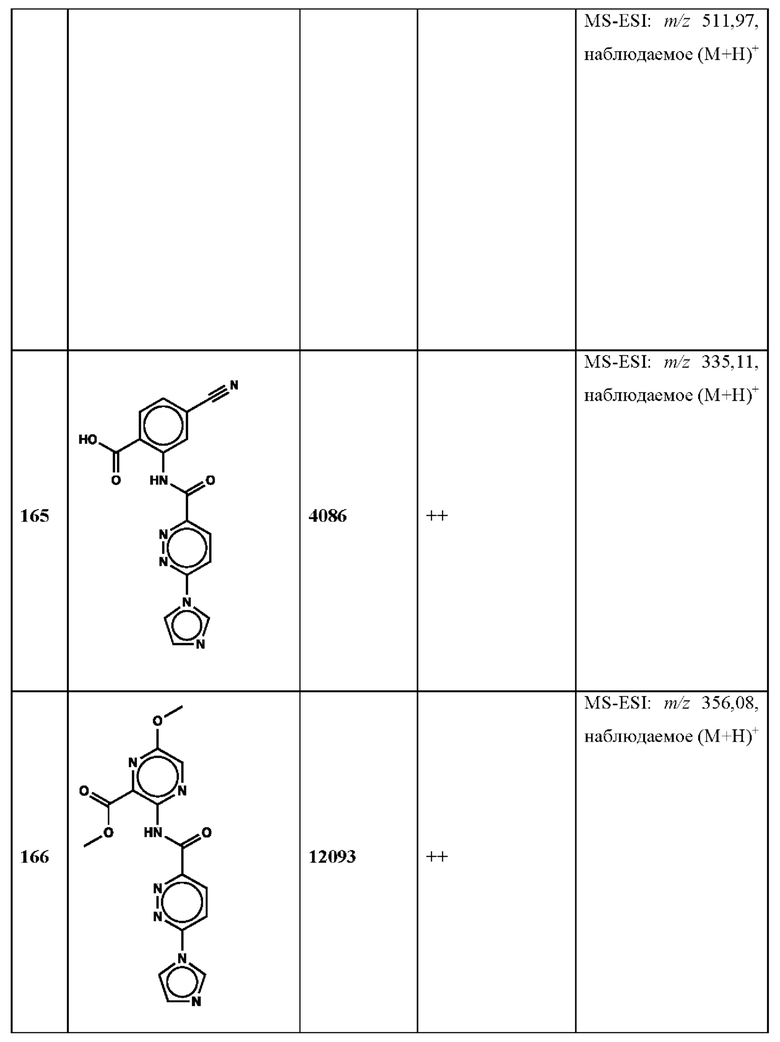
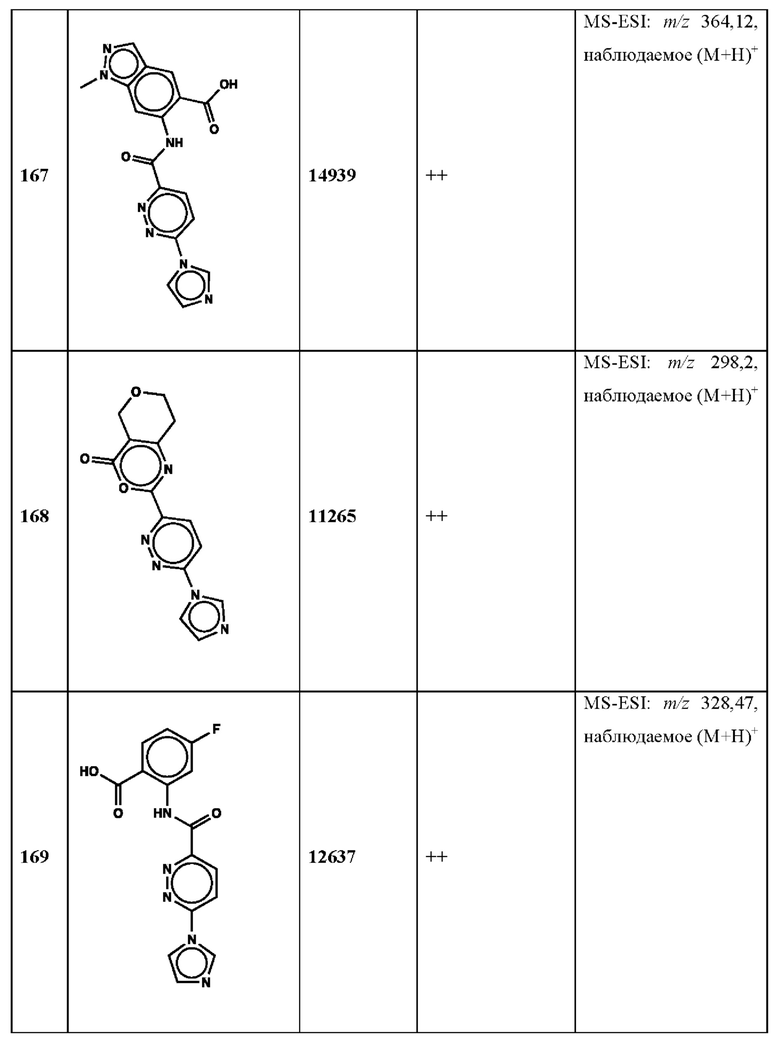
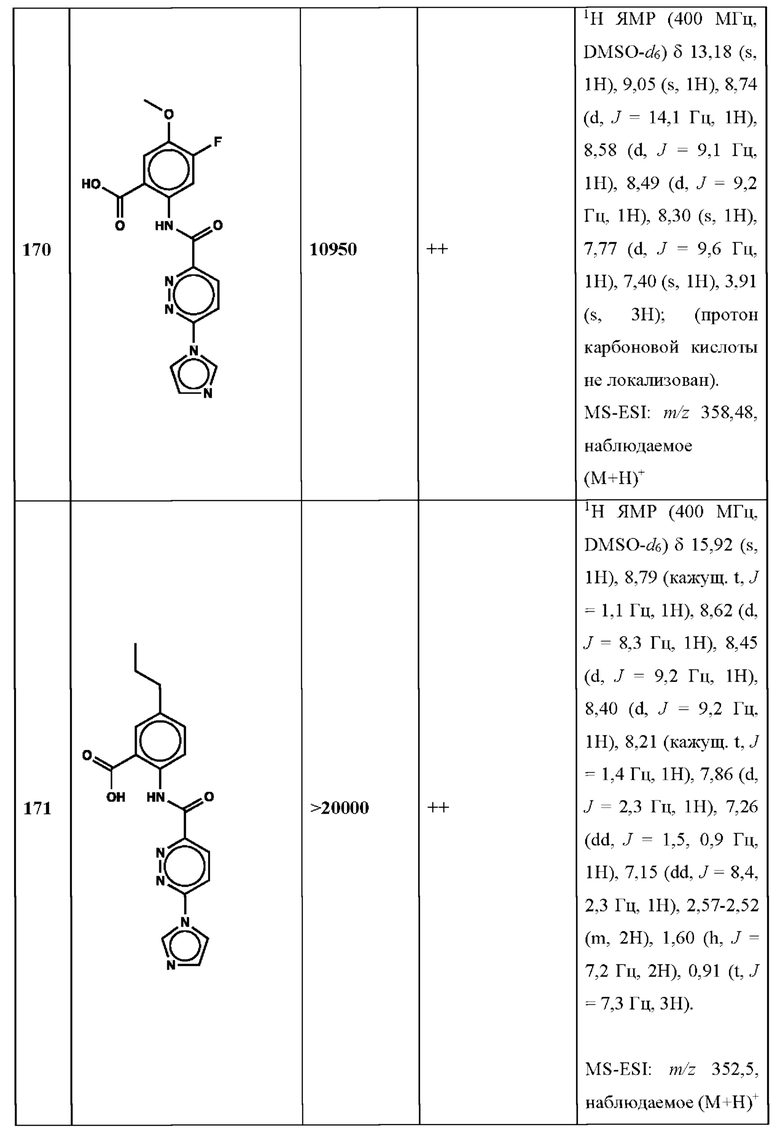
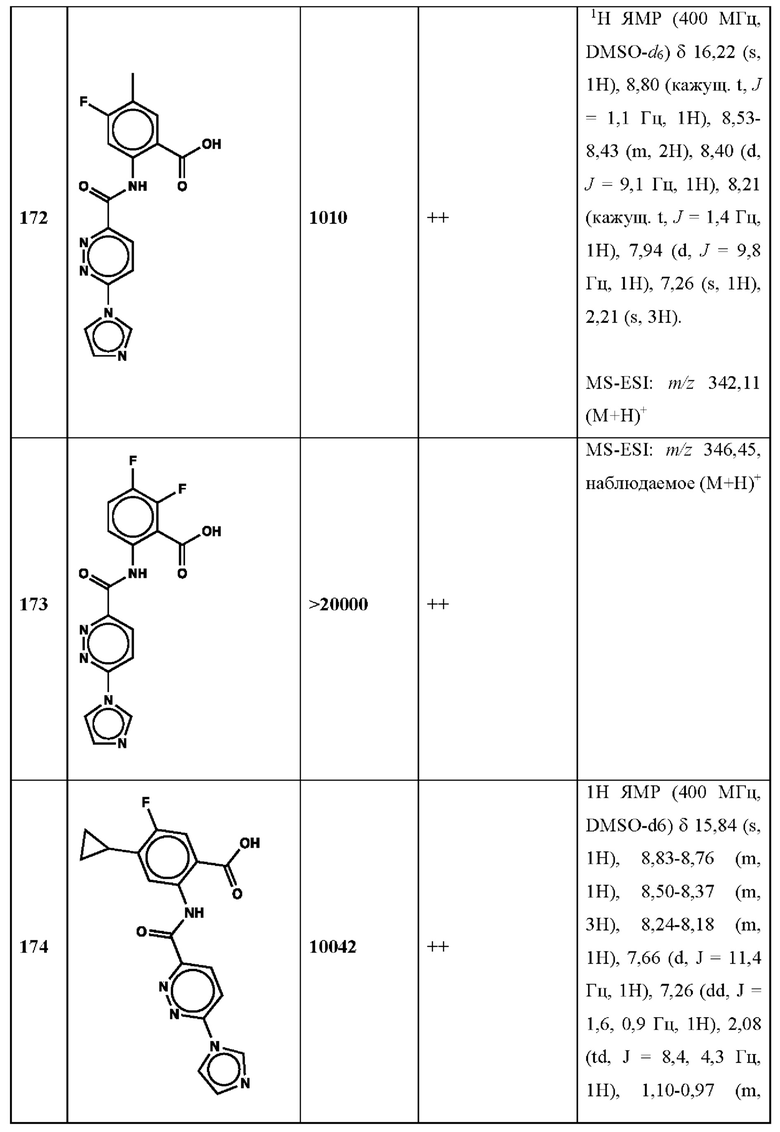
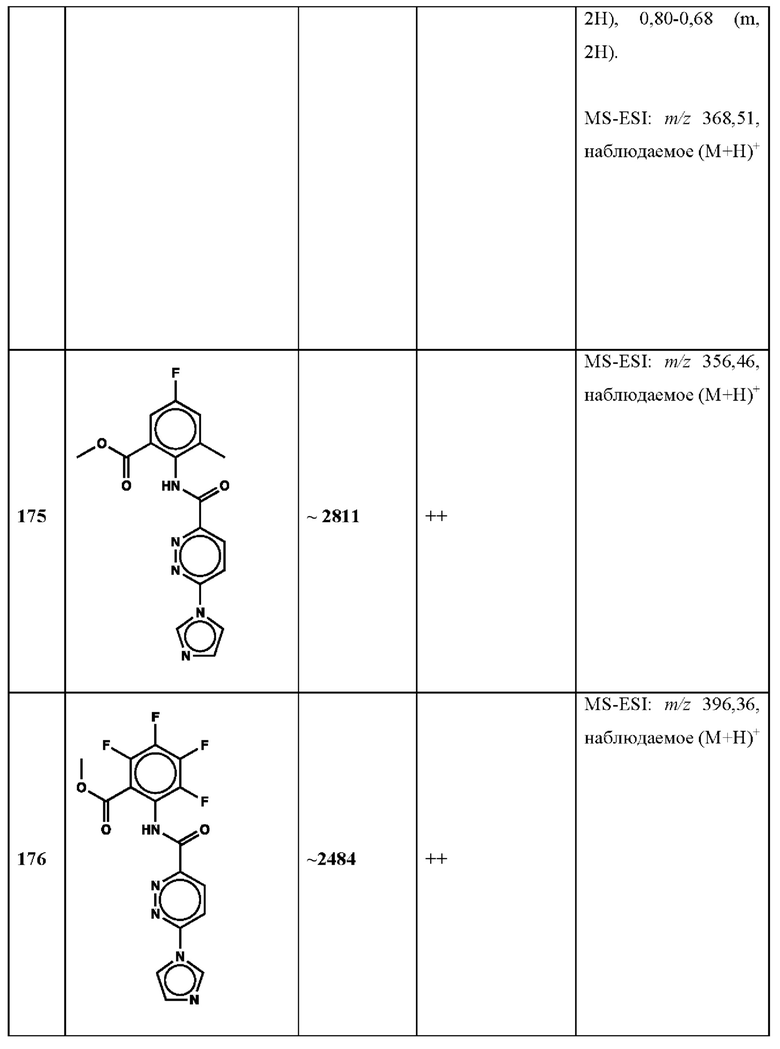
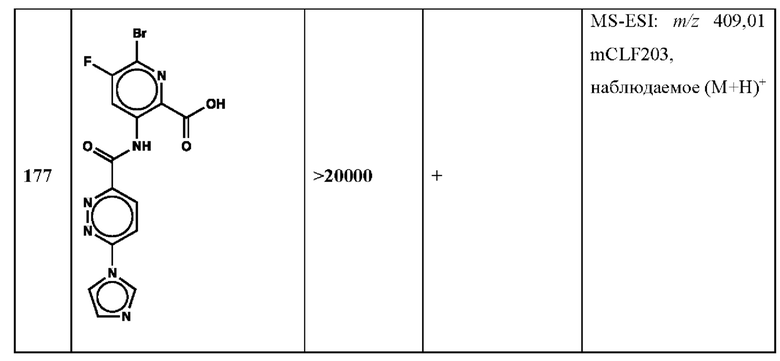
Дополнительно, способ по настоящему изобретению можно осуществить с применением эффективной дозы любого из конкретных раскрываемых в настоящей заявке соединений; см., например, таблицы 1, 2 и 5.
В соответствии с различными вариантами осуществления, способ лечения опухоли может дополнительно предусматривать введение эффективной дозы соединения с формулой (I) или любого из конкретных раскрываемых в настоящем документе соединений путем перорального или внутриопухолевого введения или как первого, так и второго.
В соответствии с различными вариантами осуществления, способ лечения опухоли может дополнительно предусматривать введение эффективной дозы соединения с формулой (I) или любого из конкретных раскрываемых в настоящем документе соединений, причем введение предусматривает введение пациенту соединения в виде конъюгата антитело-лекарственное средство или в составе липосомы.
В соответствии с различными вариантами осуществления, способ лечения опухоли может дополнительно предусматривать введение эффективной дозы соединения с формулой (I) или любого из конкретных раскрываемых в настоящем документе соединений, дополнительно предусматривающий введение эффективной дозы лекарственного средства, целенаправленно воздействующего на контрольные точки иммунного ответа. Например, лекарственное средство, целенаправленно воздействующее на контрольные точки иммунного ответа, может представлять собой антитело к PD-L1, антитело к PD-1, антитело к CTLA-4 или антитело к 4-1 ВВ.
В соответствии с различными вариантами осуществления, способ лечения опухоли может дополнительно предусматривать введение эффективной дозы соединения с формулой (I) или любого из конкретных раскрываемых в настоящем документе соединений, дополнительно предусматривая применение ионизирующего излучения или противораковых лекарственных средств.
Настоящее изобретение также может относиться к новому соединению с формулой (I), которое раскрыто и заявлено в настоящем документе.
Краткое описание чертежей
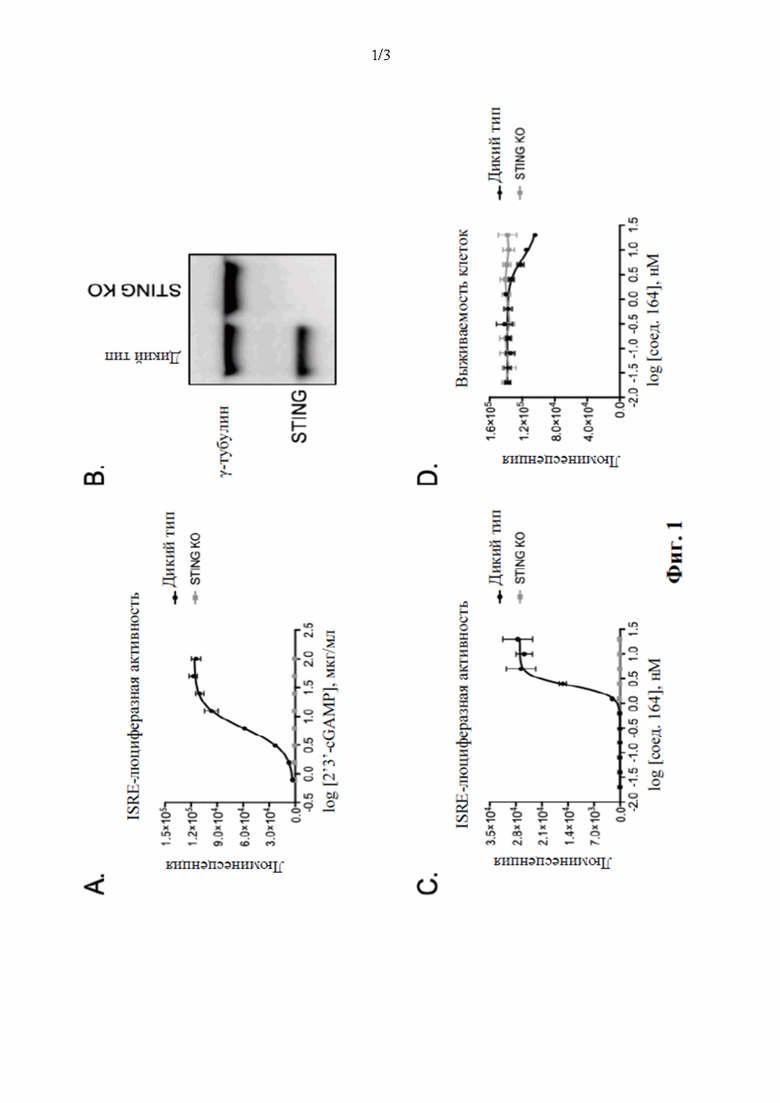
Фигура 1: клетки дикого типа и клетки STING КО ТНР-1 с ISRE-содержащим люциферазным репортером обрабатывали возрастающими дозами 2'3'-cGAMP и через 48 часов после обработки оценивали репортерную активность (люминесценцию) (А). Отсутствие экспрессии белка STING в клетках STING КО ТНР-1 подтверждали с помощью вестерн-блоттинга с применением гамма-тубулина в качестве контрольного белка загрузки (В). Клетки дикого типа и клетки STING КО ТНР-1 с репортером обрабатывали возрастающими дозами соединения 164 (соед. 164) и через 24 часа после обработки оценивали репортерную активность и жизнеспособность клеток (C-D).
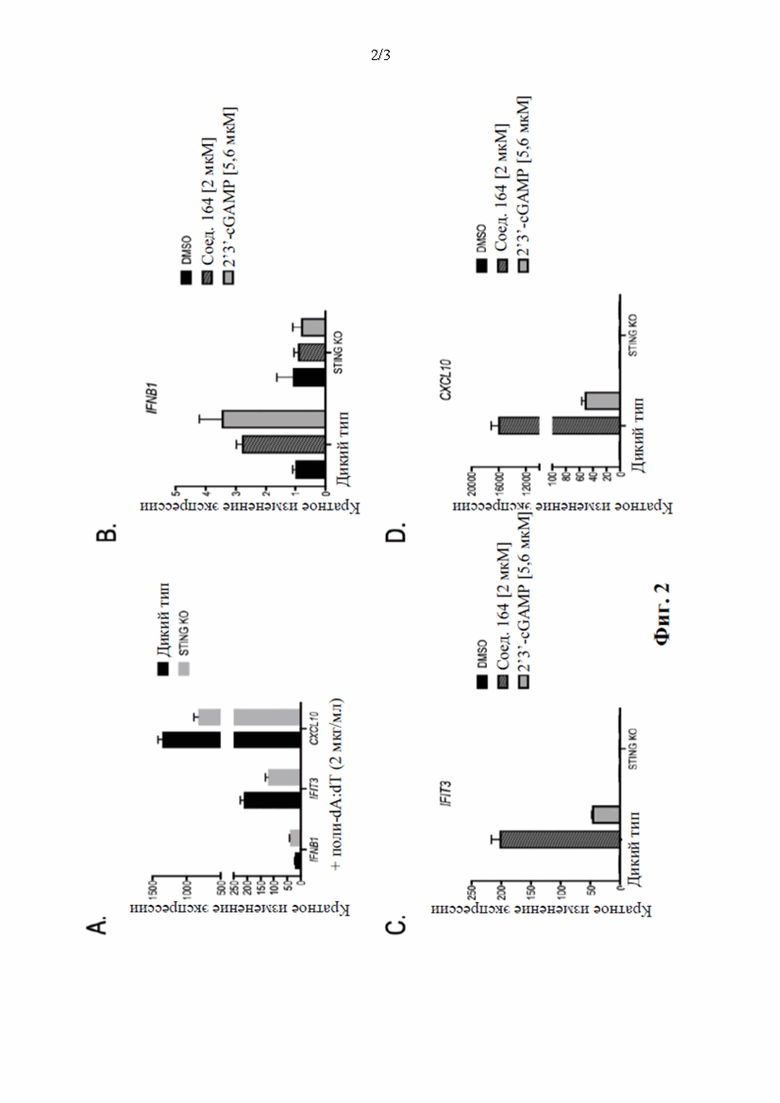
Фигура 2: клетки дикого типа и клетки STING КО ТНР-1 стимулировали поли(dA:dT), известным активатором как RIG-I, так и cGAS-зависимых сигнальных каскадов, и спустя 48 часов с помощью qPCR (А) оценивали экспрессию последующего в каскаде целевого гена. Клетки дикого типа и клетки STING КО ТНР-1 стимулировали 2'3'-cGAMP или соед. 164 в указанных дозах и с помощью анализа экспрессии гена IFNB1 (В) и стимулируемых интерфероном генов IFIT3 (С) и CXCL10 (D) оценивали активацию передачи сигналов с участием интерферона I типа.
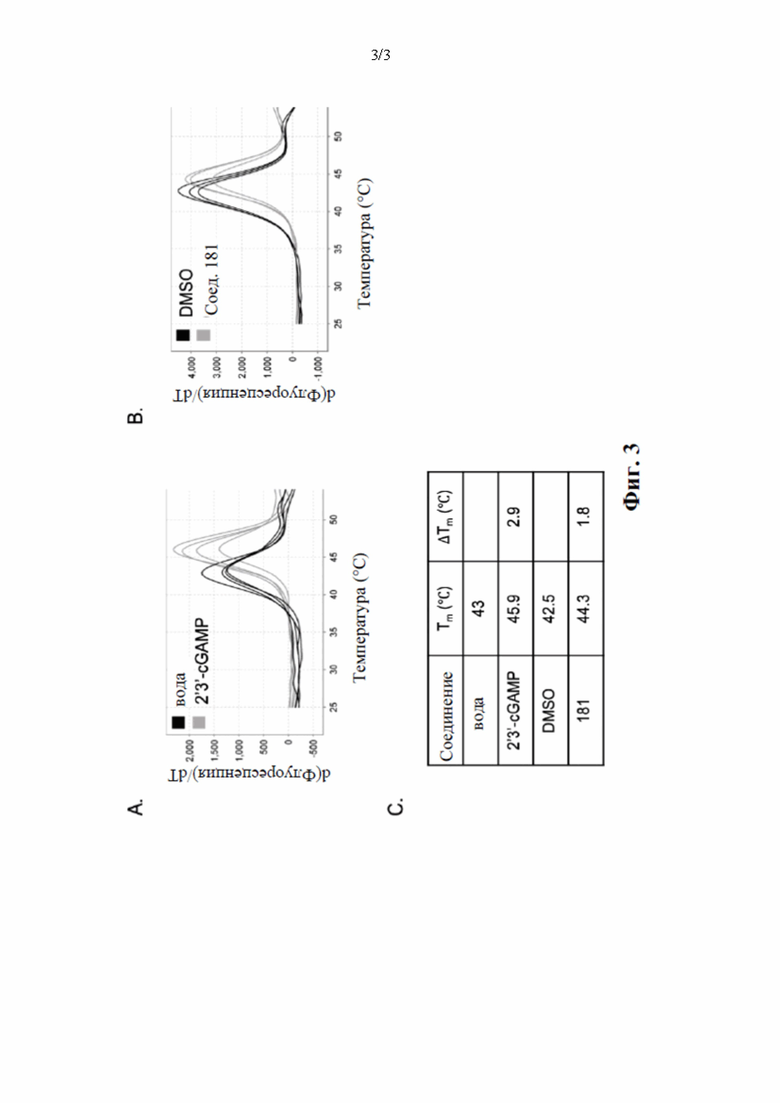
Фигура 3: С-концевой домен человеческого белка STING (аминокислоты 138-379) инкубировали с 2'3'-cGAMP [100 мкМ] (А) или соед. 181 [100 мкМ] (В) и с 1× флуоресцентным красителем с последующим воздействием повышающейся температуры. Температуру плавления (Tm) рассчитывали с помощью способа производных и путем нормализации к соответствующему контрольному наполнителю (С) получали индуцированное связыванием с лигандом изменение температуры плавления (ΔTm).
Подробное раскрытие настоящего изобретения
Существует значительный интерес к разработке агонистов пути STING для различных иммуноонкологических задач. Что особенно важно, агонисты пути STING имеют важное потенциальное применение в качестве части комбинированной терапии с применением лекарственных средств, целенаправленно воздействующих на контрольные точки иммунного ответа, на пациентах, которые не отвечают на одну лишь блокаду контрольных точек.
Нами была создана надежная платформа для выявления ненуклеотидных низкомолекулярных агонистов STING. Это было установлено с помощью первичного анализа с задействованием линии человеческих клеток ТНР-1, несущих IRF-индуцируемый репортер с 5 копиями элемента, отвечающего на передачу сигнала с участием IFN. При скрининговых анализах для изучения избирательности и селективности лекарственных средств с задействованием альтернативных репортерных конструкций используют анализы на клетках грызунов, а также нокаутные по cGAS и STING линии клеток для устранения артефактов с люциферазой и обеспечения межвидовой реактивности между видами человека и грызуна, а также селективности к определенному сигнальному пути. Для выявления конкретной мишени указанных соответствий используют биохимические анализы с задействованием ферментативной активности cGAS и анализы связывания с белком STING. На сегодняшний день по результатам первоначального скрининга ~100000 соединений нами было выявлено по меньшей мере одно новое, хорошо отличимое, стоящее соединение 164 с остовом агониста STING, таблица 1 (ЕС50 ~1 мкМ, таблица 1), которое индуцирует стимулируемую интерфероном экспрессию генного паттерна у клеток соответствующего типа и экспрессию белка IFNI типа у РВМС человека с эффективностью, сравнимой с наблюдаемой для 2'-3' cGAMP. Наблюдаемая активность соединения 164, таблица 1, у клеток дикого типа и у нокаутных по cGAS клеток, а также наблюдаемое отсутствие активности у нокаутных по STING клеток свидетельствует о том, что этот ряд соединений реализует свою функцию путем прямого действия в качестве агонистов STING Дополнительные доказательства представлены данными теплового сдвига у белка STING Предварительная работа в области медицинской химии, предусматривающая разработку, синтез и тестирование ~100 аналогов в серии, позволила выявить ключевые элементы молекулы, которые необходимы для активности, и привела к выявлению производных с ~10-кратным улучшением клеточной эффективности (например, путем изменения схемы замещения в анилиновом кольце) и ~50-кратным повышением стабильности в плазме крови (путем изменения размера заместителя сложноэфирной группы).
«Проведение лечения» или «лечение» в контексте настоящего документа означает облегчение симптомов, связанных с нарушением или заболеванием, или подавление дальнейшего прогрессирования или ухудшения данных симптомов, или предупреждение или профилактику заболевания или нарушения, или излечение заболевания или нарушения. Аналогичным образом, в контексте настоящего документа «эффективное количество» или «терапевтически эффективное количество» соединения по настоящему изобретению означает количество соединения, которое облегчает, полностью или частично, симптомы, связанные с нарушением или патологическим состоянием, или останавливает или замедляет дальнейшее прогрессирование или ухудшение этих симптомов, или предупреждает развитие или обеспечивает профилактику нарушения или патологического состояния. В частности, «терапевтически эффективное количество» обозначает количество, которое является эффективным в дозах и в течение периодов времени, необходимых для достижения требуемого терапевтического результата. Терапевтически эффективное количество также является таким количеством, при котором любые токсические или пагубные эффекты соединений по настоящему изобретению перевешиваются терапевтически благоприятными эффектами.
Выражение «эффективное количество», при его использовании для описания терапевтического лечения страдающего нарушением индивидуума, обозначает количество или концентрацию соединения по настоящему изобретению, которые эффективны для ингибирования или иного действия на STING в тканях индивидуума, при этом STING вовлечен в развитие нарушения, причем такое ингибирование или иное действие представлено в степени, достаточной для достижения благоприятного терапевтического эффекта.
Термин «фармацевтически приемлемые соли» обозначает нетоксичные соли присоединения неорганических или органических кислот и/или оснований, см., например, публикацию Lit et al., Salt Selection for Basic Drugs (1986), Int J. Pharm., 33, 201-217, включенную в настоящий документ посредством ссылки.
Для химических групп использованы стандартные сокращения, такие как хорошо известные в данной области, например: Me=метил, Et=этил, i-Pr=изопропил, Bu=бутил, t-Bu=трет-бутил, Ph=фенил, Bn=бензил, Ас=ацетил, Bz=бензоил и т.д.
Термины «галоген», или «галогенид», или «галоид» сами по себе или как часть другого заместителя означают, если не указано иное, атом фтора, хлора, брома или йода, предпочтительно фтора, хлора или брома.
К «галогеналкильной» группе относятся моногалогеналкильные группы, полигалогеналкильные группы, в которых все атомы галогена могут быть одинаковыми или различаться, и пергалогеналкильные группы, в которых все атомы водорода заменены одинаковыми или различными атомами галогена, такими как атомы фтора и/или хлора. Примеры галогеналкила включают трифторметил, 1,1-дихлорэтил, 1,2-дихлорэтил, 1,3-дибром-3,3-дифторпропил, перфторбутил и др.
Арильные группы представляют собой циклические ароматические углеводороды, которые не содержат гетероатомов в кольце. Ароматическое соединение, как хорошо известно из уровня техники, представляет собой циклическую систему с несколькими ненасыщенными связями, которая содержит 4n+2 π-электронов, где n представляет собой целое число. Таким образом, к арильным группам относятся без ограничения фенильная, азуленильная, гепталенильная, бифенильная, индаценильная, флуоренильная, фенантренильная, трифениленильная, пиренильная, нафтаценильная, хризенильная, бифениленильная, антраценильная и нафтильная группы. В соответствии с некоторыми вариантами осуществления, арильные группы содержат от приблизительно 6 до приблизительно 14 атомов углерода в кольцевых частях групп. Арильные группы могут быть незамещенными или замещенными, как определено выше. Типичные замещенные арильные группы могут быть монозамещенными или замещенными более одного раза, такими как без ограничения 2-, 3-, 4-, 5- или 6-замещенные фенильные или 2-8-замещенные нафтильные группы, которые могут быть замещены углеродными или неуглеродными группами, такими как перечисленные выше группы.
Гетероциклильные группы или термин «гетероциклил» включает ароматические и неароматические кольцевые соединения, содержащие 3 или более кольцевых членов, из которых один или несколько кольцевых атомов являются гетероатомами, такими как без ограничения N, О и S. Таким образом, гетероциклил может представлять собой циклогетероалкил, или гетероарил, или, если гетероциклил является полициклическим, любую их комбинацию. В соответствии с некоторыми вариантами осуществления, гетероциклильные группы включают от 3 до приблизительно 20 кольцевых членов, тогда как другие такие группы содержат от 3 до приблизительно 15 кольцевых членов. Гетероциклильная группа, обозначаемая С2-гетероциклилом, может представлять собой 5-членное кольцо с двумя атомами углерода и тремя гетероатомами, 6-членное кольцо с двумя атомами углерода и четырьмя гетероатомами и так далее. Аналогично, С4-гетероциклил может представлять собой 5-членное кольцо с одним гетероатомом, 6-членное кольцо с двумя гетероатомами и так далее. Количество атомов углерода плюс количество гетероатомов в сумме равняется общему количеству кольцевых атомов. Размеры кольца также можно выразить общим количеством атомов в кольце, например, 3-10-членная гетероциклильная группа, в которой учтены как углеродные, так и неуглеродные кольцевые атомы. Гетероциклильное кольцо также может включать одну или несколько двойных связей. Гетероарильное кольцо представляет собой вариант осуществления гетероциклильной группы. Термин «гетероциклильная группа» включает конденсированные кольцевые системы, в том числе системы, которые содержат конденсированные ароматические и неароматические группы. Например, как диоксоланильное кольцо, так и бенздиоксоланильная кольцевая система (метилендиоксифенильная кольцевая система) в контексте настоящего документа являются гетероциклильными группами. Термин также включает полициклические, например, бициклические и трициклические кольцевые системы, содержащие один или несколько гетероатомов, такие как без ограничения хинуклидил. Гетероциклильные группы могут быть незамещенными или могут быть замещенными.
Гетероарильные группы представляют собой гетероциклические ароматические кольцевые соединения, содержащие 5 или более кольцевых членов, из которых один или несколько представляют собой гетероатом, такой как без ограничения N, О и S; например, гетероарильные кольца могут иметь от 5 до приблизительно 8-12 кольцевых членов. Гетероарильная группа представляет собой разновидность гетероциклильной группы, которая обладает ароматической электронной структурой, представляющей собой циклическую систему с несколькими ненасыщенными связями, которая содержит 4n+2 π-электронов, где n представляет собой целое число. Гетероарильная группа, обозначаемая С2-гетероарилом, может представлять собой 5-членное кольцо (т.е. кольцо с 5 кольцевыми членами) с двумя атомами углерода и тремя гетероатомами, 6-членное кольцо (т.е. кольцо с 6 кольцевыми членами) с двумя атомами углерода и четырьмя гетероатомами и так далее. Аналогично, С4-гетероарил может представлять собой 5-членное кольцо с одним гетероатомом, 6-членное кольцо с двумя гетероатомами и так далее. Количество атомов углерода плюс количество гетероатомов в сумме равняется общему количеству кольцевых атомов.
Примеры описываемых в настоящем документе гетероарильных кольцевых систем включают структурную единицу с формулой 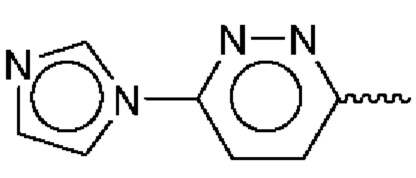 , имидазолил-пиридазин, который, как известно, также можно изобразить в следующем виде:
, имидазолил-пиридазин, который, как известно, также можно изобразить в следующем виде: 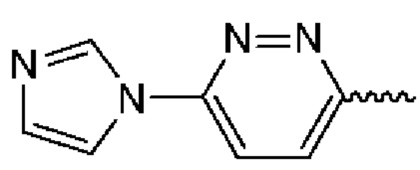 . Другая описываемая в настоящем документе гетероарильная кольцевая система имеет формулу
. Другая описываемая в настоящем документе гетероарильная кольцевая система имеет формулу 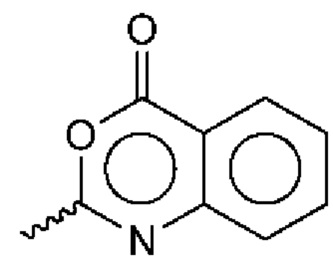 , которую, как известно, также можно изобразить в следующем виде:
, которую, как известно, также можно изобразить в следующем виде: 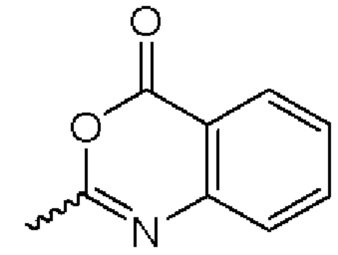 . Аналогичным образом и другие описываемые в настоящем документе арильные (например, фенильные) и гетероарильные (например, пиридильные) кольцевые системы могут быть записаны либо с помощью явных двойных связей, либо с помощью номенклатуры арильного «круга», но они имеют одно и то же значение.
. Аналогичным образом и другие описываемые в настоящем документе арильные (например, фенильные) и гетероарильные (например, пиридильные) кольцевые системы могут быть записаны либо с помощью явных двойных связей, либо с помощью номенклатуры арильного «круга», но они имеют одно и то же значение.
Циклоалкильные группы представляют собой группы, содержащие одно или несколько карбоциклических колец, в том числе без ограничения циклопропильные, циклобутильные, циклопентильные, циклогексильные, циклогептильные и циклооктильные группы. В соответствии с некоторыми вариантами осуществления, циклоалкильная группа может иметь от 3 до приблизительно 8-12 кольцевых членов, тогда как в соответствии с другими вариантами осуществления, количество атомов углерода в кольце варьирует в диапазоне от 3 до 4, 5, 6 или 7. К циклоалкильным группам дополнительно относятся полициклические циклоалкильные группы, такие как без ограничения норборнильные, адамантильные, борнильные, камфенильные, изокамфенильные и каренильные группы, и конденсированные кольца, такие как без ограничения декалинил и др. К циклоалкильным группам также относятся кольца, которые замещены алкильными группами с прямой или разветвленной цепью, определение которым дано выше.
К циклоалкенильным группам относятся циклоалкильные группы, имеющие по меньшей мере одну двойную связь между 2 атомами углерода. Так, например, к циклоалкенильным группам относятся без ограничения циклогексенильные, циклопентенильные и циклогексадиенильные группы. Циклоалкенильные группы могут иметь от 3 до приблизительно 8-12 кольцевых членов, тогда как в соответствии с другими вариантами осуществления, количество атомов углерода в кольце варьирует в диапазоне от 3 до 5, 6 или 7. К циклоалкильным группам дополнительно относятся полициклические циклоалкильные группы, такие как без ограничения норборнильные, адамантильные, борнильные, камфенильные, изокамфенильные и каренильные группы, и конденсированные кольца, такие как без ограничения декалинил и др., при условии, что они содержат по меньшей мере одну двойную связь в кольце. К циклоалкенильным группам также относятся кольца, которые замещены алкильными группами с прямой или разветвленной цепью, определение которым дано выше.
Гетероциклильные группы или термин «гетероциклил» включает ароматические и неароматические кольцевые соединения, содержащие 3 или более кольцевых членов, из которых один или несколько кольцевых атомов являются гетероатомами, такими как без ограничения N, О и S. Таким образом, гетероциклил может представлять собой циклогетероалкил, или гетероарил, или, если гетероциклил является полициклическим, любую их комбинацию. В соответствии с некоторыми вариантами осуществления, гетероциклильные группы включают от 3 до приблизительно 20 кольцевых членов, тогда как другие такие группы содержат от 3 до приблизительно 15 кольцевых членов. Гетероциклильная группа, обозначаемая С2-гетероциклилом, может представлять собой 5-членное кольцо с двумя атомами углерода и тремя гетероатомами, 6-членное кольцо с двумя атомами углерода и четырьмя гетероатомами и так далее. Аналогично, С4-гетероциклил может представлять собой 5-членное кольцо с одним гетероатомом, 6-членное кольцо с двумя гетероатомами и так далее. Количество атомов углерода плюс количество гетероатомов в сумме равняется общему количеству кольцевых атомов. Размеры кольца также можно выразить общим количеством атомов в кольце, например, 3-10-членная гетероциклильная группа, в которой учтены как углеродные, так и неуглеродные кольцевые атомы. Гетероциклильное кольцо также может включать одну или несколько двойных связей. Гетероарильное кольцо представляет собой вариант осуществления гетероциклильной группы. Термин «гетероциклильная группа» включает конденсированные кольцевые системы, в том числе системы, которые содержат конденсированные ароматические и неароматические группы. Например, как диоксоланильное кольцо, так и бенздиоксоланильная кольцевая система (метилендиоксифенильная кольцевая система) в контексте настоящего документа являются гетероциклильными группами. Термин также включает полициклические, например, бициклические и трициклические кольцевые системы, содержащие один или несколько гетероатомов, такие как без ограничения хинуклидил.
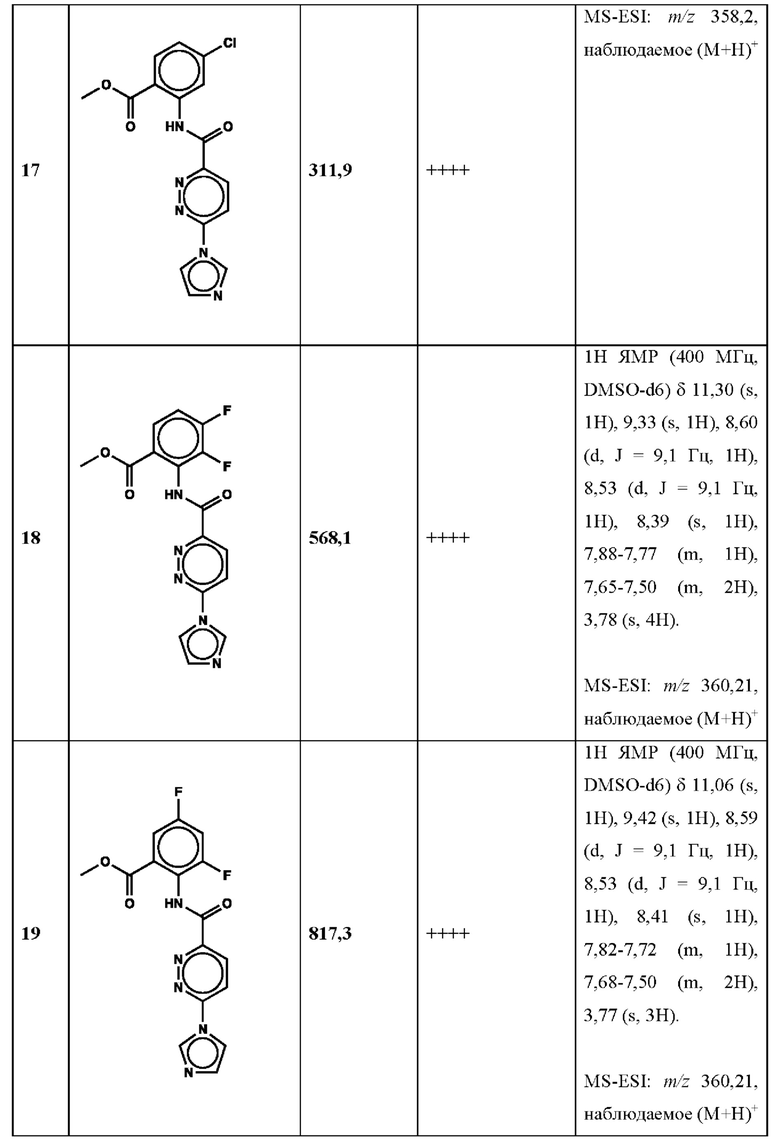
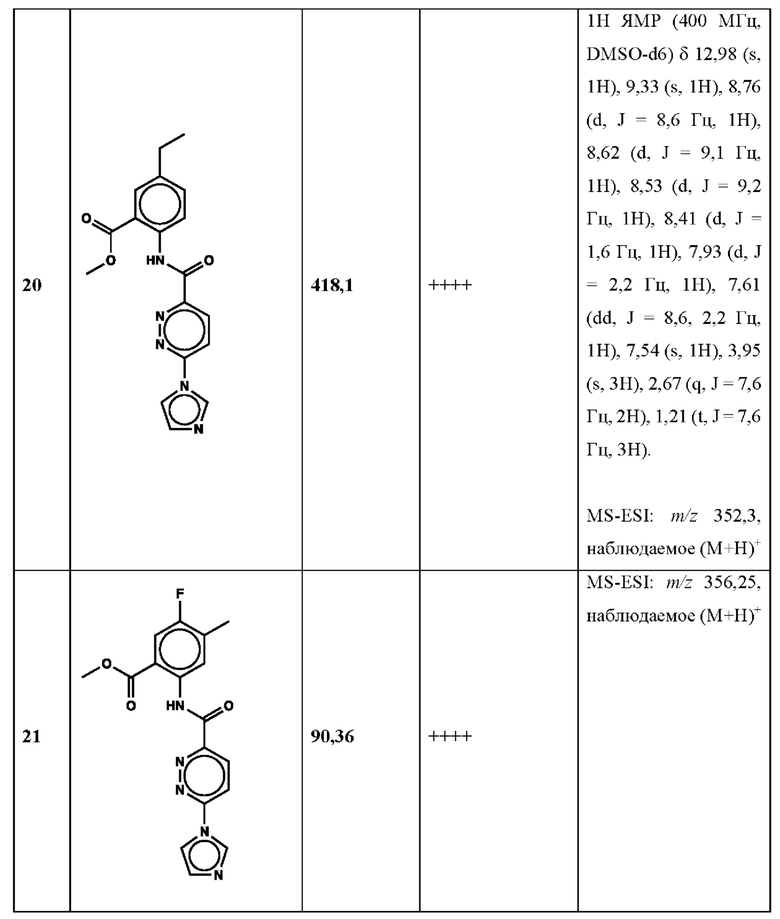
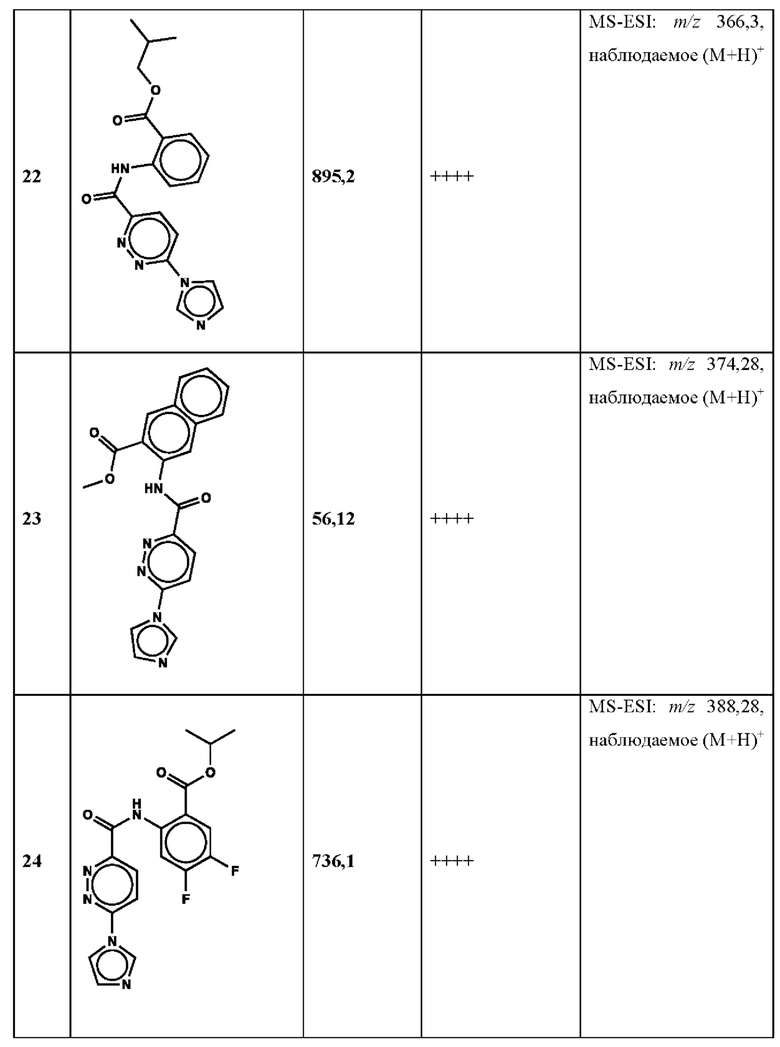
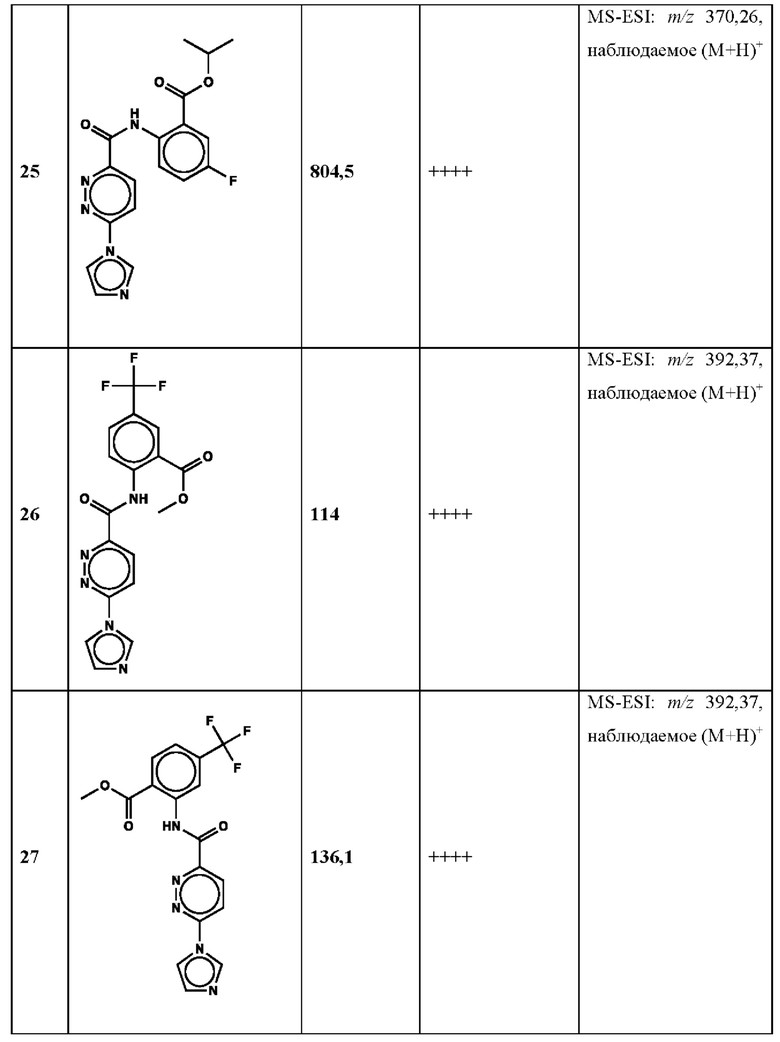
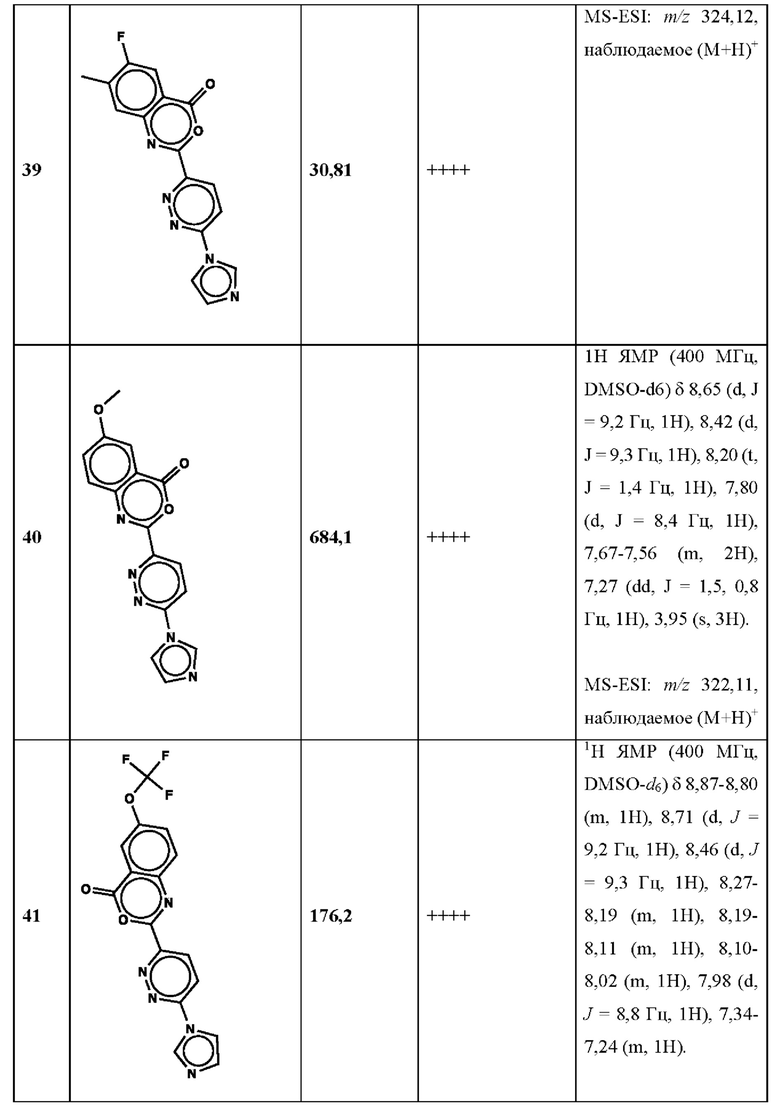
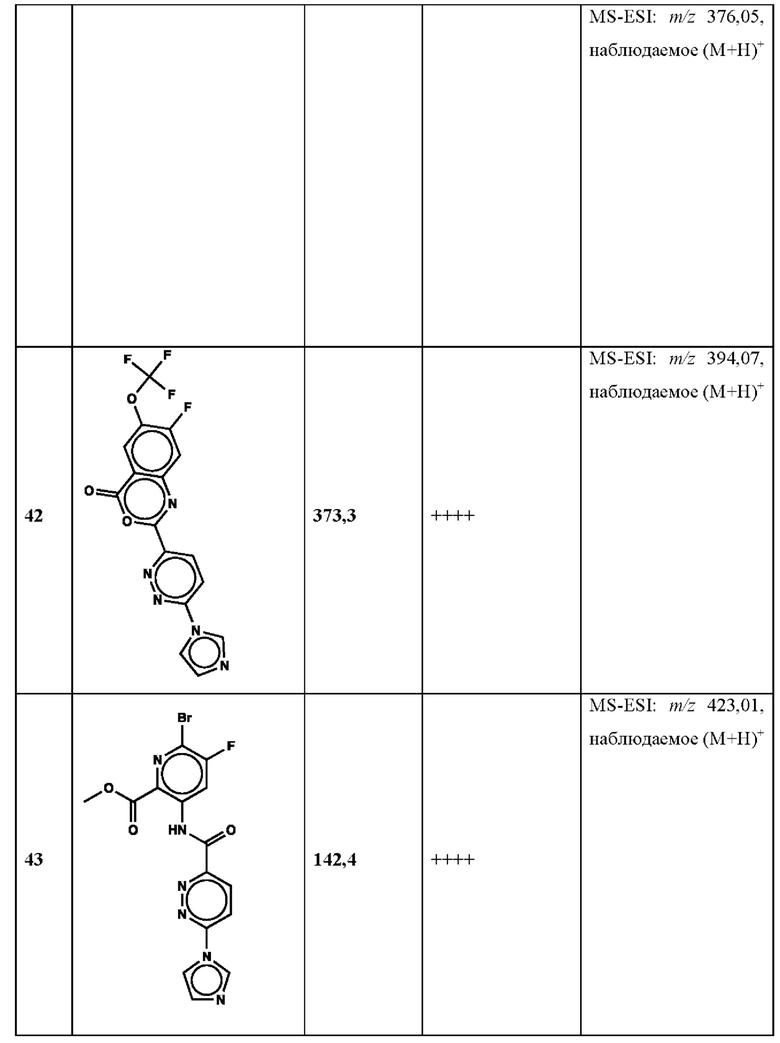
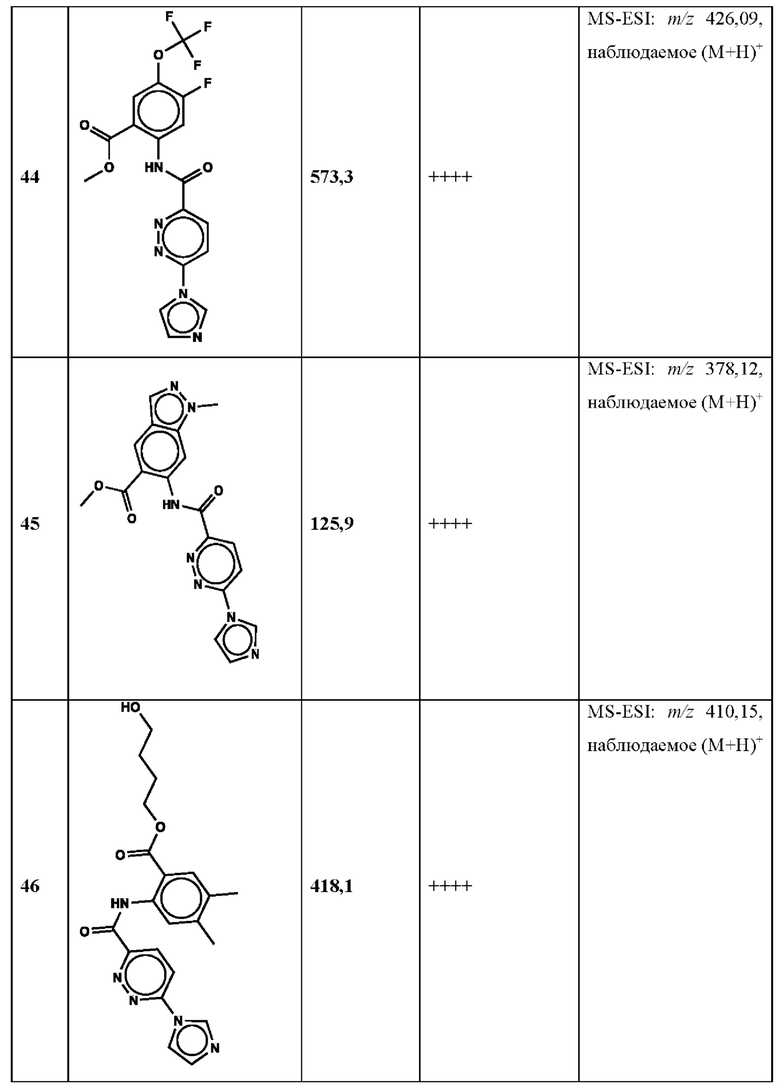
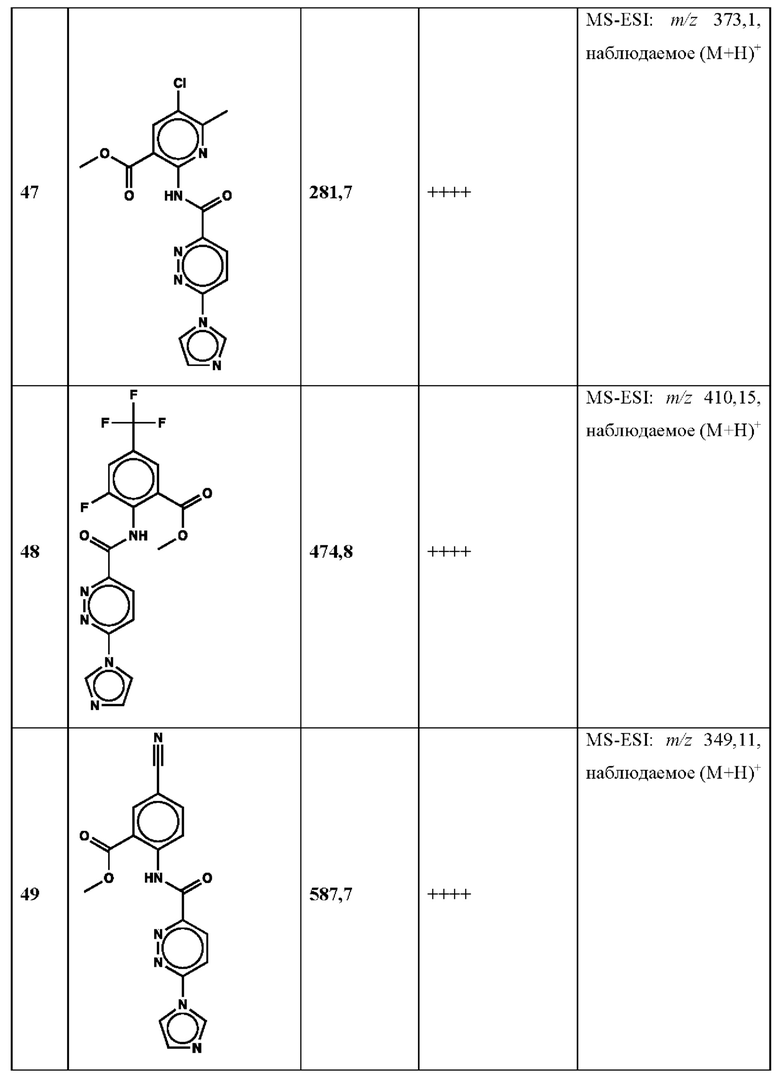
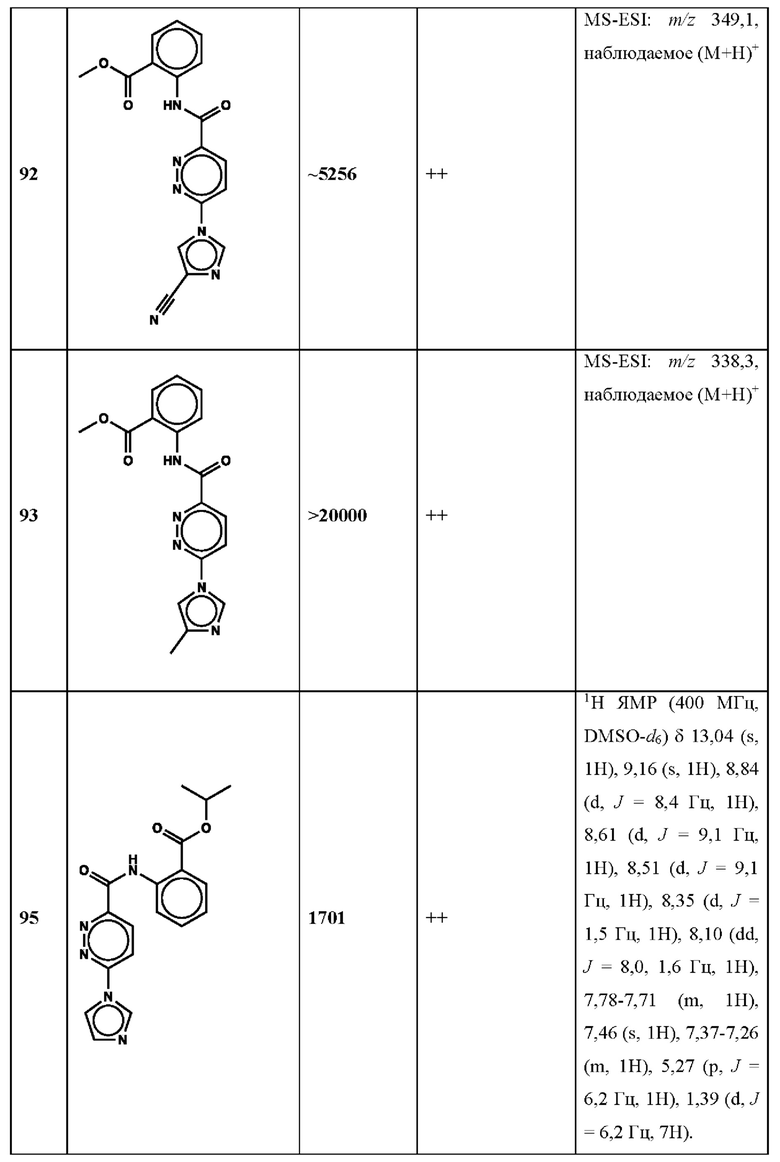
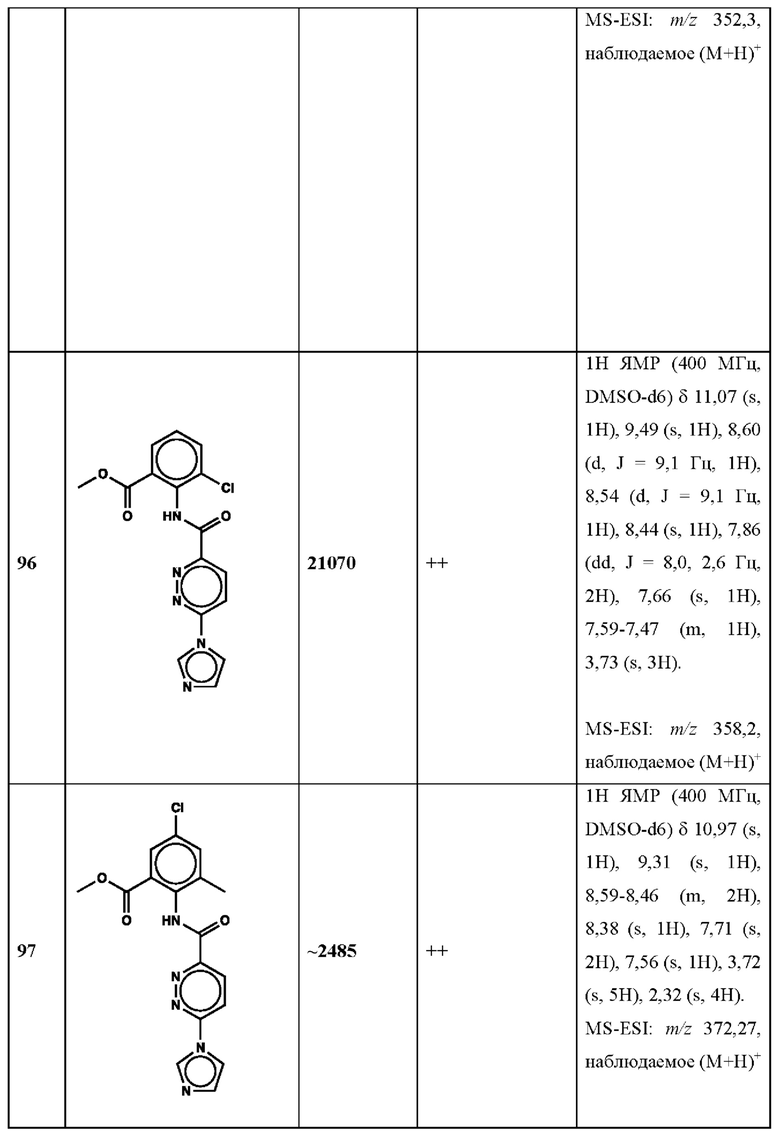
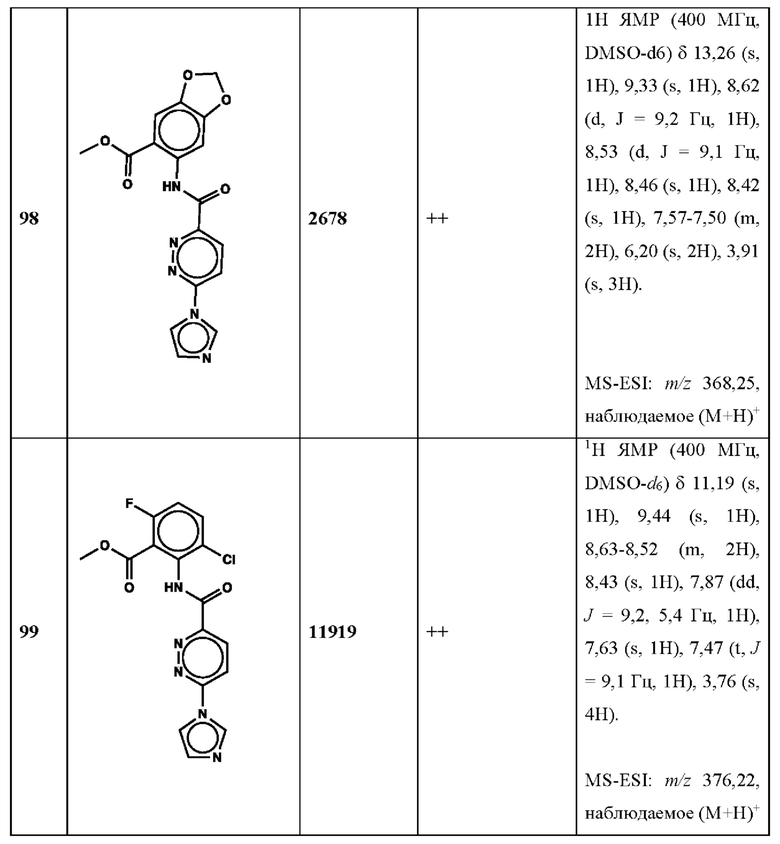
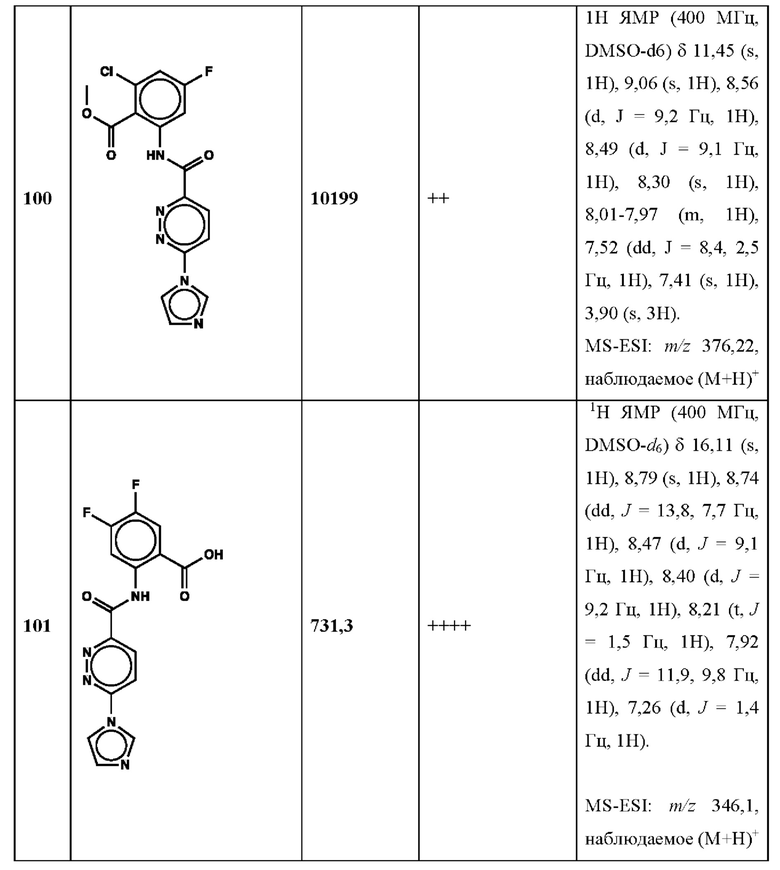
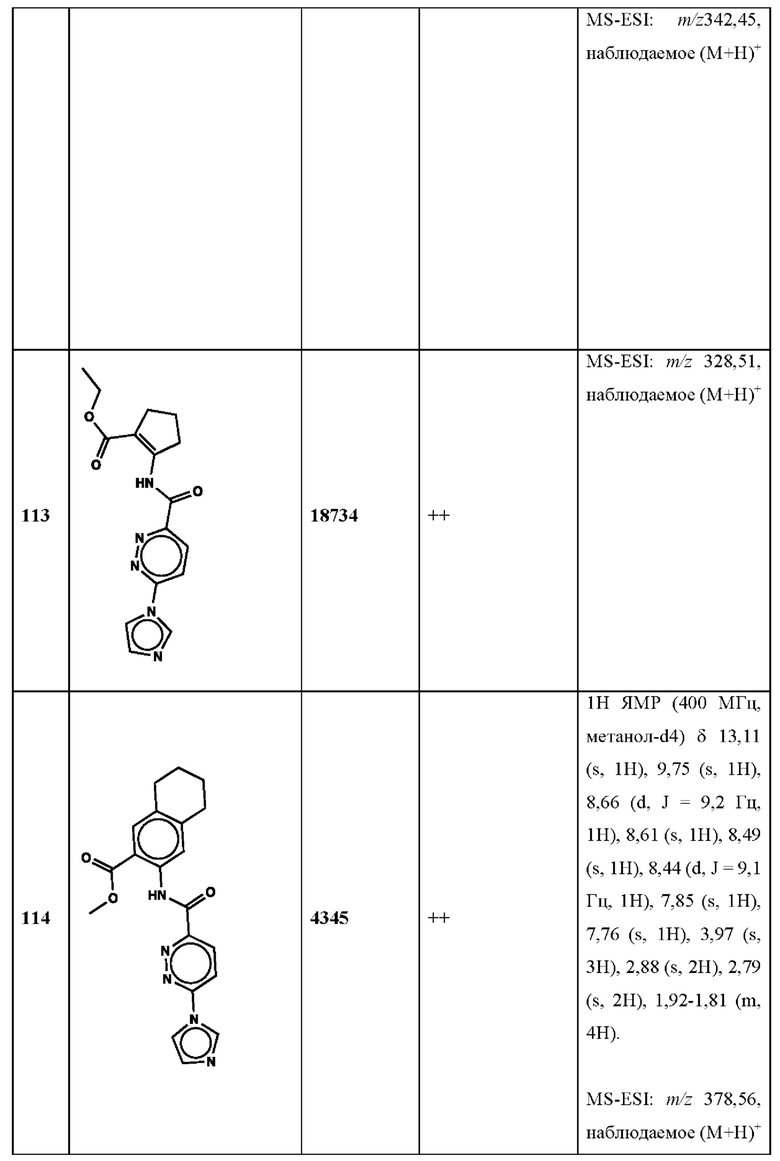
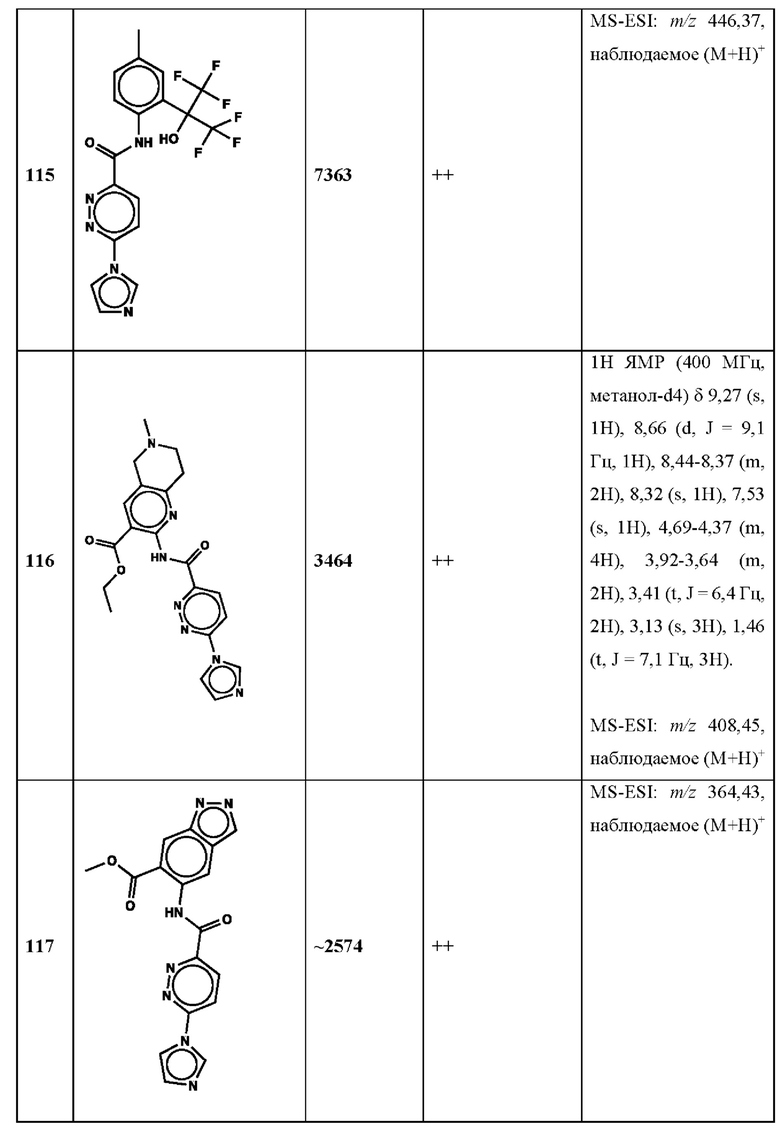
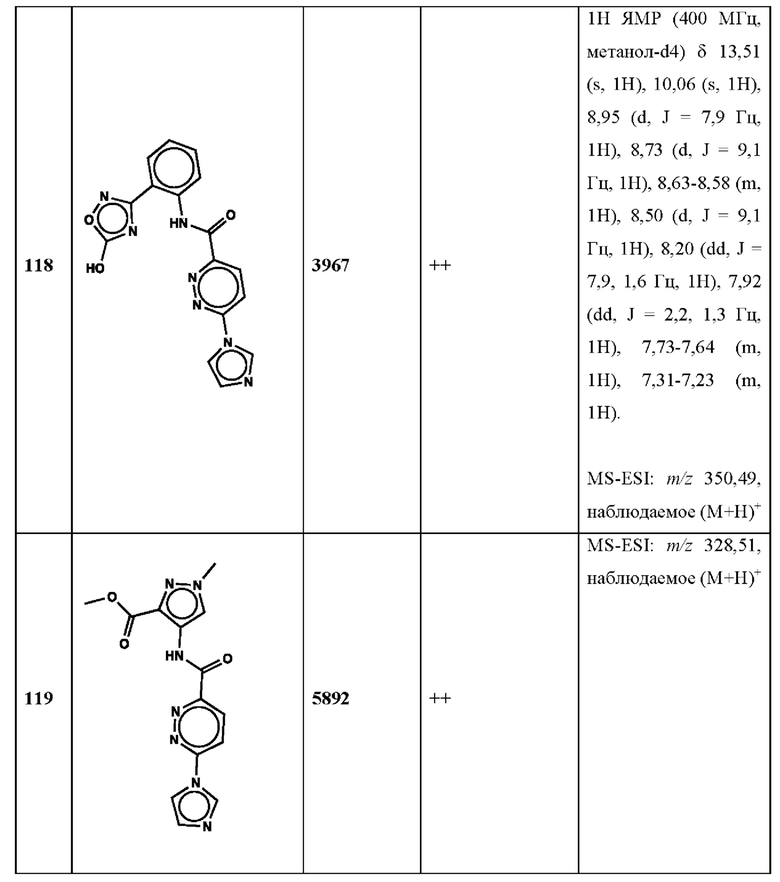
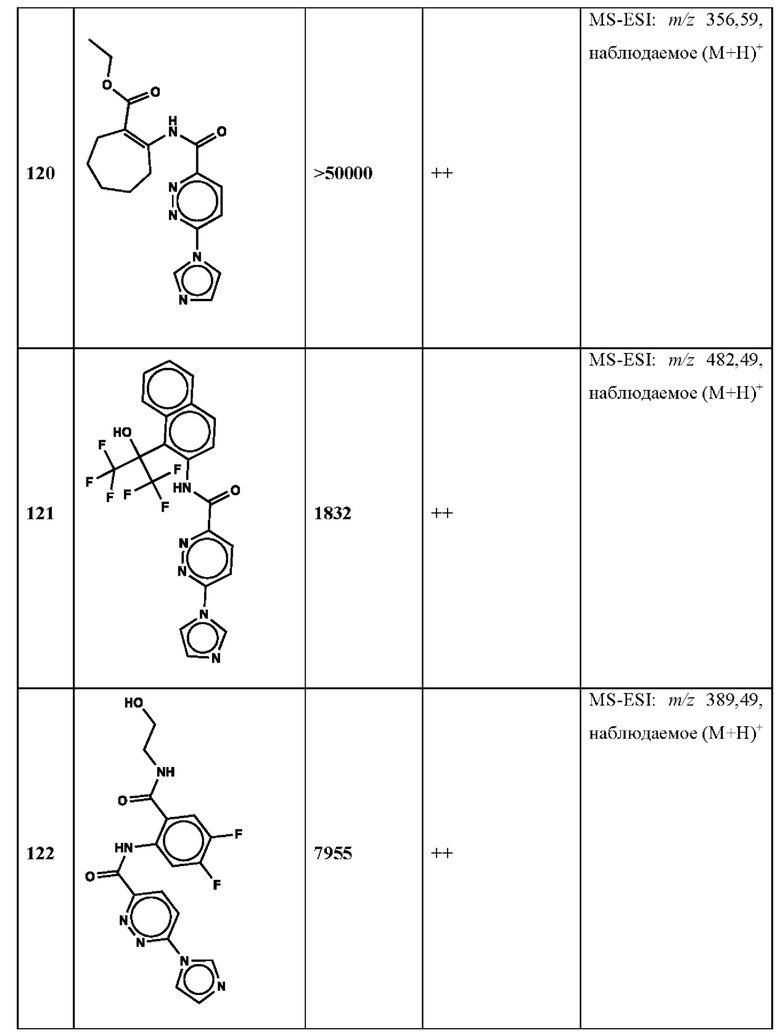

Связанные документы
[1] Corrales L, Glickman LH, McWhirter SM, Kanne DB, Sivick KE, Katibah GE, Woo SR, Lemmens E, Banda T, Leong Д Metchette K, Dubensky TW Jr, Gajewski TF. (2015) Direct Activation of STING in the Tumor Microenvironment Leads to Potent and Systemic Tumor Regression and Immunity. CellRep.11: 1018-30.
[2] Deng, L. et al. (2014) STING-Dependent Cytosolic DNA Sensing Promotes Radiation-Induced Type I Interferon-Dependent Antitumor Immunity in Immunogenic Tumors, Immunity. 41: 843.
[3] Corrales L, Matson V, Flood B, Spranger S, Gajewski TF. (2017) Innate immune signaling and regulation in cancer immunotherapy. Cell Res. 27: 96-108.
[4] Corrales L, McWhirter SM, Dubensky TW Jr, Gajewski TF. (2016) The host STING pathway at the interface of cancer and immunity. J Clin Invest. 126: 2404-11.
Что касается комбинированной терапии, предусматривающей введение соединения по настоящему изобретению и лекарственного средства, целенаправленно воздействующего на контрольные точки иммунного ответа, или что касается комбинированной терапии для усиления воздействия ионизирующего излучения и существующих химиотерапевтических подходов, таких как химиотерапевтические подходы, основанные на повреждении ДНК, полагаем что агонисты STING по настоящему изобретению могут дополнять и усиливать эффекты этих известных терапевтических подходов. Данный вывод основан на недавних статьях, указывающих на критически важную роль STING-зависимого устранения опухоли с участием микронуклеусов при использовании данных подходов, см., например:
[5] Mackenzie, K.F., et all, (2017), cGAS surveillance of micronuclei links genome instability to innate immunity, Nature, 548, 461.
[6] Wang, W. et al., (2016), Effector T Cells Abrogate Stroma-Mediated Chemoresistance in Ovarian Cancer, Cell, 165, 1092 1105.
[7] Charlotte E. Ariyan, et al., January 16, 2018; DOI: 10.1158/2326-6066, Robust antitumor responses result from local chemotherapy and CTLA-4 blockade, cancerimmunolres.aacrjournals.org on January 31, 2018.
[8] Chung Kil Song, et al., www.moleculartherapy.org vol. 15 no. 8 aug. 2007, Chemotherapy Enhances CD8+T Cell-mediated Antitumor Immunity Induced by Vaccination With Vaccinia Virus.
Соединения по настоящему изобретению можно применять в терапевтических комбинациях с введением эффективной дозы лекарственного средства, целенаправленно воздействующего на контрольные точки иммунного ответа. Например, лекарственное средство, целенаправленно воздействующее на контрольные точки иммунного ответа, может представлять собой антитело к PD-L1, антитело к PD-1, антитело к CTLA-4 или антитело к 4-1 ВВ. См., например:
[9] Ager, CR, et al., (2017) Cancer Immunol Res; 5(8), 676.
[10] Fu, J. et al. (2015) Sci Transl Med. 2015 April 15; 7(283): 283ra52. doi: 10.1126/scitranslmed.aaa4306.
[11] Wang, H., et al. (2017) PNAS | February 14, 2017 | vol. 114 | no. 7 | 1637-1642.
Примеры
Тканевая культура
Клетки THP-l-Lucia ISG дикого типа (кат. №thpl-isg) и STING КО (кат. №thpd-kostg) приобретали у Invivogen и поддерживали в питательной среде, состоящей из RPMI 1640, 2 мМ L-глутамина, 25 мМ HEPES, 10% термоинактивированной фетальной бычьей сыворотки (FBS), 1000 единиц/мл пенициллина, 1000 мкг/мл стрептомицина 0,25 мкг/мл амфотерицина В и 100 мкг/мл зеоцина, если не указано иное.
Стимулирование интерфероном 1-го типа
Поли(с1А:с1Т) и 2'3'-cGAMP приобретали у Invivogen и ресуспендировали в соответствии с инструкциями производителя.
ISRE-люциферазньш анализ
Клетки ТНР-1 Lucia ISG ресуспендировали в ростовой среде с низким содержанием сыворотки (2% FBS) плотностью 5×105 клеток/мл и обрабатывали тестируемым продуктом или наполнителем (DMSO). 50 мкл клеток высевали в каждую лунку 384-луночных белых планшетов Greiner и инкубировали в течение 24 часов. Для оценки экспрессии люциферазного репортера в каждую лунку добавляли 30 мкл детектирующего реагента Quanti-luc (Invivogen) и считывали люминесценцию с помощью планшетного ридера Envision (Perkin Elmer) со временем для аккумулирования заряда светодиодом, установленным на 0,1 секунды.
Анализ жизнеспособности
Клетки ресуспендировали в ростовой среде с низким содержанием сыворотки плотностью 5×105 клеток/мл и обрабатывали тестируемым продуктом или наполнителем (DMSO). 50 мкл клеток высевали в каждую лунку 384-луночных белых планшетов Greiner и инкубировали в течение 24 часов. Для оценки экспрессии люциферазного репортера в каждую лунку добавляли 30 мкл детектирующего реагента CellTiter-Glo (Promega) и детектировали люминесценцию с помощью планшетного ридера Envision со временем для аккумулирования заряда светодиодом, установленным на 0,1 секунды.
В естерн-блоттинг
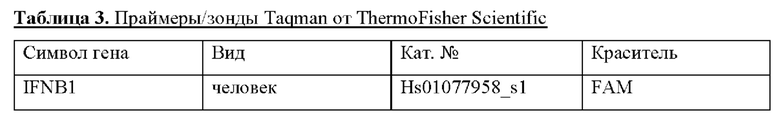
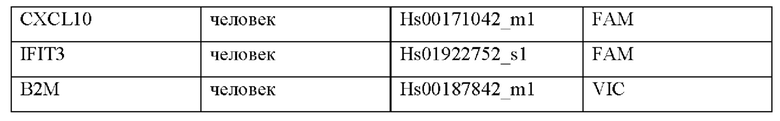
Клетки солюбилизировали в 1× буфере для лизиса белка (25 мМ HEPES, рН 7,4, 300 мМ NaCl, 1,5 мМ MgCl2, 1 мМ EGTA, 1% Р-40, 1% дезоксихолата натрия, 2,5 мМ пирофосфата натрия, 1 мМ глицерофосфата) с недавно добавленными ингибиторами протеаз и фосфатаз (Cell Signaling). Вестерн-блоттинг проводили с применением 4-12% Bis-Tris гелей Bolt™ и мини-системы переноса Bolt™ в соответствии с инструкциями производителя (ThermoFisher Scientific). Антитела к STING и γ-тубулину приобретали у Cell Signaling, разводили в 5% BSA, 1× буфере TBS-T (таблица 3). Антитело с HRP к антителам кролика разводили в 5% обезжиренном сухом молоке, 1× буфере TBS-T, а люминесцентный сигнал регистрировали с помощью визуализатора ChemiDoc Imager (BioRad).
Полуколичественная ПЦР в режиме реального времени (qPCR)
Клетки ТНР-1 ресуспендировали в ростовой среде с низким содержанием сыворотки плотностью 5×105 клеток/мл и обрабатывали тестируемым продуктом или наполнителем (DMSO). 2,5 мл клеток высевали в каждую лунку 6-луночного планшета и инкубировали в течение 24 часов. РНК выделяли с помощью набора RNeasy Plus Mini Kit (Qiagen) и 1 мкг очищенной РНК подвергали обратной транскрипции в кДНК (VILO, кат. №11755050, ThermoFisher Scientific). Экспрессию генов оценивали с применением праймеров и зондов Taqman, перечисленных в таблице 4, со смесью Taqman Universal Mix II (кат. №4440038, ThermoFisher) в соответствии с инструкциями производителя. Экспрессию генов нормализовали с помощью способа двойного дельта Ct и регистрировали как кратное изменение экспрессии.
Анализ теплового сдвига STING (TSA)
С-концевые домены (CTD) человеческого и мышиного STING экспрессировали и очищали так, как подробно описано ранее в (Ouyang et al., 2012). Тестируемый продукт или контрольные наполнители добавляли к разведенному белку STING (0,22 мг/мл) в 1х буфере для измерения теплового сдвига у белка, входящем в набор с красителем для измерения теплового сдвига у белка (кат. №4461146, ThermoFisher Scientific). Добавляли краситель для измерения теплового сдвига и перемешивали перед построением кривой плавления в соответствии с параметрами, указанными для набора красителя. Значения температуры плавления (Tm) рассчитывали с помощью способа с использованием производных с применением программного обеспечения Protein Thermal Shift Software v1.3 (кат.№4466038, ThermoFisher Scientific).

Ouyang, S., Song, X., Wang, Y., Ru, H., Shaw, N., Jiang, Y., Niu, F., Zhu, Y., Qiu, W., Parvatiyar, K., et al. (2012). Structural analysis of the STING adaptor protein reveals a hydrophobic dimer interface and mode of cyclic di-GMP binding. Immunity 36, 1073-1086.
Соединения, пригодные для осуществления способа по настоящему изобретению, можно получить в соответствии с приведенными далее процедурами в сочетании с обычными знаниями и навыками в области органического синтеза путем замены на соответствующие реагенты, как будет очевидно для специалиста-практика.
Экспериментальные процедуры
Сокращения
Использованы следующие сокращения: тетрагидрофуран (THF), дихлорметан (DCM), N,N-диметилформамид (DMF), диметилацетамид (DMA), диметилсульфоксид (DMSO), трифторуксусная кислота (TFA), триэтиламин (TEA), диизопропилэтиламин (DIPEA), (1-циано-2-этокси-2-оксоэтилиденаминоокси)диметиламиноморфолинокарбения гексафторфосфат (COMU), 1-[бис(диметиламино)метилен]-1Н-1,2,3-триазоло [4,5-b]пиридиния 3-оксидгексафторфосфат, N-[(диметиламино)-1Н-1,2,3-триазоло[4,5-b]пиридин-1-илметилен]-N-метилметанаминия гексафторфосфат-N-оксид (HATU).
Общие примеры получения соединений по настоящему изобретению
Исходные материалы и промежуточные продукты для соединений по настоящему изобретению можно получить путем применения или адаптации описанных ниже способов, их очевидных химических эквивалентов или, например, описанных в такой литературе, как The Science of Synthesis, Volumes 1-8. Editors E. M. Carreira et al. Thieme publishers (2001-2008). Подробная информация о реагентах и вариантах реакций также доступна при поиске по структуре и реакциям с использованием коммерческих компьютерных поисковых систем, таких как Scifinder (www.cas.org) или Reaxys (www.reaxys.com).
ЧАСТЬ I: ПОЛУЧЕНИЕ ПРОМЕЖУТОЧНЫХ ПРОДУКТОВ
Схема 1: синтез промежуточного продукта А
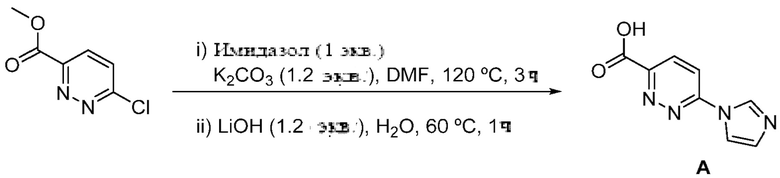
6-(1H-нмндазол-1-шт) пирндазнн-3-карбоновая кислота, А: к суспензии метил-6-хлорггиридазин-3-карбоксилата (1 г, 5,2 ммопя) и имядазопа (400 мг, 5,2 ммоля) в сухом DMF (10 мл) добавляли К2СО2 (950 мг, 6,2 ммопя) и реакционную смесь перемешивали при 120°С в течение 3 часов. Реакцию отслеживали с помощью LCM3. После полного превращения в метип-6-(1 Н-имидазш-1-ил)1 гиридазт-3-карбоксилат в реакционную смесь добавляли 2,5 М водного раствора LiOH (2,2 mi, 6,96 ммоль) и перемешивали при 60°С в течение 1 часа. Реакцию отслеживали с помощью LCMS. После завершения реакции реакционную смесь подкисляли водным раствором 1 М HCl и полученный осадок отфильтровьтапи и промывали водой с получением кислоты А (720 мг) в виде беловатого твердого вещества, которое использовали на следующей стадии без дополнительной очистки. LC-M3 (ESI+): m/z 191,0 [М+Н]+.
ЧАСТЬ II: ПОЛУЧЕНИЕ ПРИМЕРОВ СОЕДИНЕНИЙ
Все соединения получали с испопьзованием приведенных ниже процедур.
Пример 1
Схема 2: синтез соединения 1
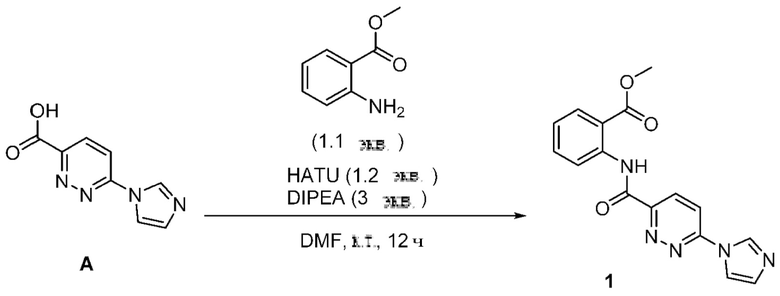
Метнл-2-(6-(1Н-имидазол-1-мл)пиридазин-3-карбоксамидо)бензоат, 1: промежуточный продукт А (190 мг, 1 ммоль), метил-2-аминобензоат (166 мг, 1,1 ммоля), HATU (456 мг, 1,2 ммоля) и DIPEA (0,52 мл, 3 ммоля) растворяли в DMF (5 мл) и перемешивали при комнатной температуре в течение ночи. После завершения реакции растворитель выпаривали при пониженном давлении и полученный неочищенный материал очищали хроматографией на колонке с силикагелем с применением 2-5% МеОН в DCM с получением соединения 1 в виде беловатого твердого вещества (226 мг). LC-MS (ESI+): m/z 32А,21 [М+Н]+.
Схема 3
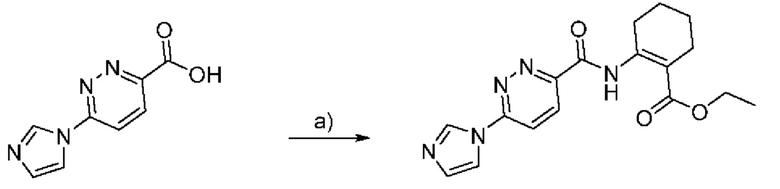
аРеагенты и условия: а) тионилхлорид, кипячение в колбе с обратным холодильником, 3 часа; этил-2-аминоциклогекс-1-ен-1-карбоксилат, DIPEA, ацетонитрил, комнатная температура, 30 минут
Этил-2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)циклогекс-1-ен-1-карбоксилат: 6-(1Н-имидазол-1-ил)пиридазин-3-карбоновую кислоту (19 мг, 0,1 ммоля) растворяли в 0,3 мл тионилхлорида и смесь нагревали в колбе с обратным холодильником в течение 3 часов. Затем избыток тионила удаляли под вакуумом. Твердое вещество растворяли в 0,5 мл безводного ацетонитрила и при комнатной температуре добавляли раствор этил-2-аминоциклогекс-1-ен-1-карбоксилата (16,9 мг, 0,1 ммоля) и DIPEA (26,1 мкл, 0,15 ммоля) в 0,5 мл безводного ацетонитрила. После перемешивания в течение 30 минут неочищенную смесь фильтровали и очищали препаративной ВЭЖХ с получением продукта (6,8 мг, 20% выход).
Схема 4: синтез соединения 8
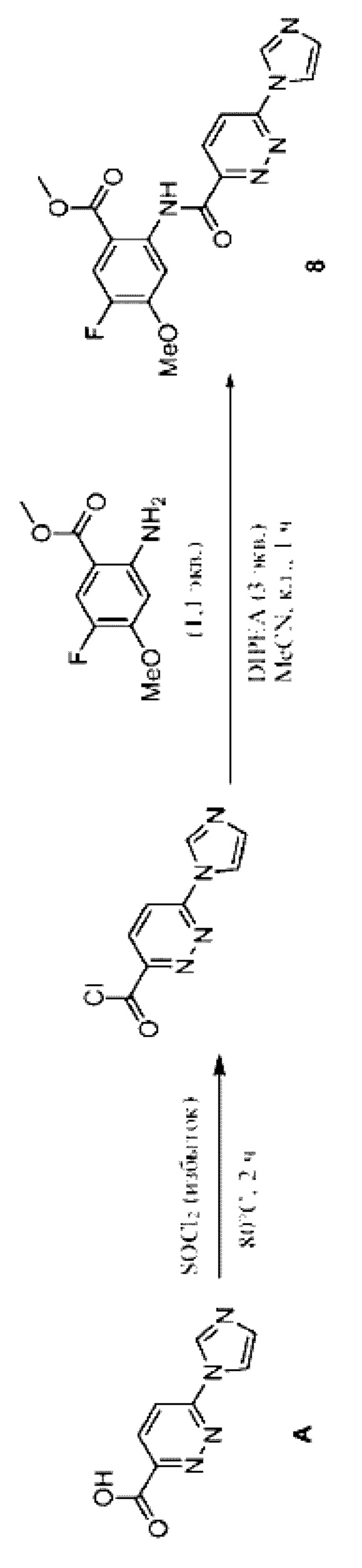
Метил-2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-5-фтор-4-метоксибензоат, 8: промежуточный продукт А (190 мг, 1 ммоль) перемешивали в присутствии SOCl2 (5 мл) при 80°С в течение 2 часов. Затем удаляли летучие вещества с последующим добавлением раствсра метил-2-амино-5-фтор-4-метоксибензоата (219 мг, 1,1 ммоля) и DIPEA (0,52 мл, 3 ммоля) в ацетонитриле (5 мл). Полученную реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакцию отслеживали с помощью LCMS. После завершения реакции растворитель удаляли и полученный неочищенный материал очищали хроматографией на колонке с силикагелем с применением 2-5% МеОН в DCM с получением соединения 8 в виде беловатого твердого вещества (223 мг). LC-MS (ESI+): m/z 372,1 [М+Н]+.
Пример 2-Li
Схема 5: синтез соединения 2-Li
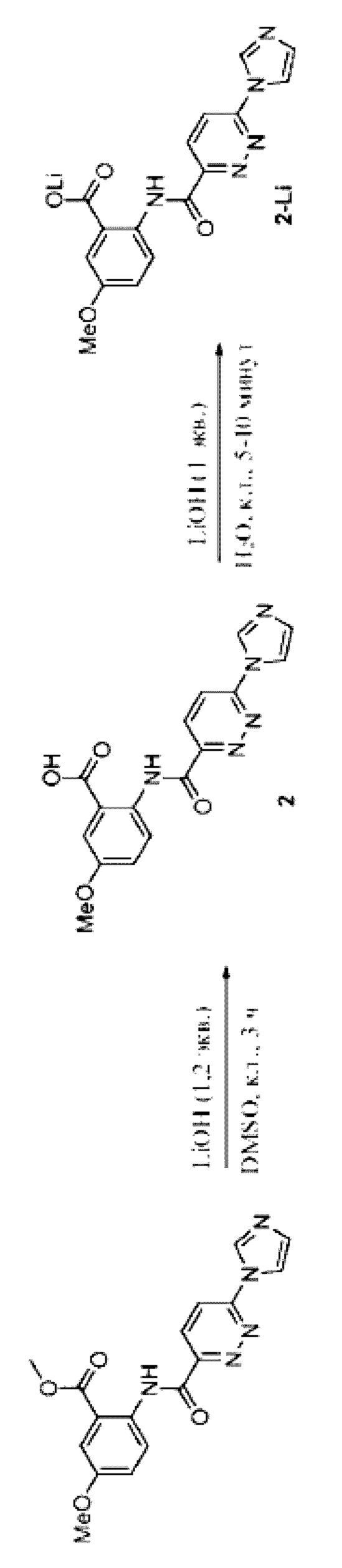
2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-5-метоксибензоат лития, 2-Li: метил- 2-(6-(1Н-имидазол-1-ил)пиридазин-3-кар6оксамидо)-5-метокси6ензоат получали с помощью процедуры, описанной для соединения 1 (схема С). Полученный сложный эфир (20 мг, 0,057 ммоля) растворяли в DMSO (0,8 мл), а затем добавляли водный 0,1 М раствор LiOH (0,68 мл, 1,2 ммоля) с последующим перемешиванием при комнатной температуре до завершения реакции (~3 часа). Реакцию отслеживали с помощью LCMS. Затем реакционную смесь подкисляли путем добавления по каплям 1 М HCl с получением искомой кислоты. Полученный осадок выделяли и промывали водой с получением кислоты 2 в виде беловатого твердого вещества. LC-MS (ESI+): m/z 340,4 [М+Н]+. Кислоту 2 (10,2 мг, 0,03 ммоля) дополнительно суспендировали в 2,5 мл воды (0,25 мл/мг) и обрабатывали ультразвуком в течение 20 минут до получения однородной суспензии. Затем добавляли 1 М LiOH (30 мкл, 0,03 ммоля) с получением прозрачного раствора литиевой соли, который затем фильтровали для удаления каких-либо нерастворимых частиц. Полученный раствор лиофилизировали с получением соответствующей литиевой соли 2-Li. LC-MS (ESI+): m/z 340,4 [М+Н]+.
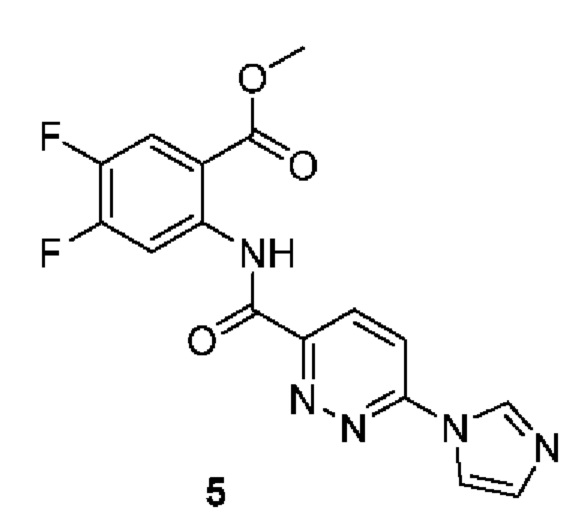
Метил-2-(6-(1Н-имидазол-1-ил)1пиридазин-3-карбоксамидо)-4,5-дифторбензоат, 5: соединение 5 получали с помощью процедуры, аналогичной для соединения 1 (схема С). LC-MS (ESI+): m/z 360,21 [М+Н]+.
Пример 6-Li
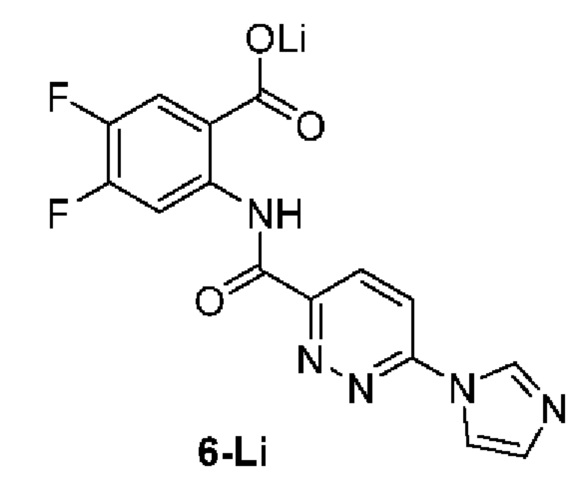
2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-4,5-дифторбензоат лития, 6-Li: соединение 6-Li получали с помощью процедуры, аналогичной для соединения 2-Li (схема D). LC-MS (ESI+): m/z 346,1 [М+Н]+.
Пример 7-Li
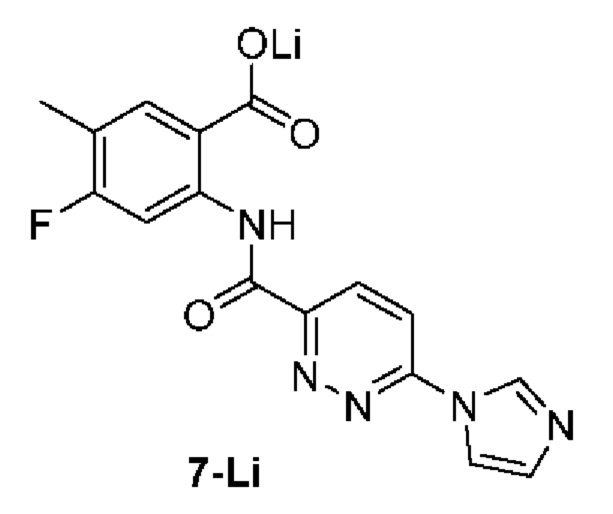
2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-4-фтор-5-метилбензоат лития, 7-Li: соединение 7-Li получали с помощью процедуры, аналогичной для соединения 2-Li (схема D). LC-MS (ESI+): m/z 342,11 [М+Н]+.
Пример 8
Схема F: синтез соединения 8
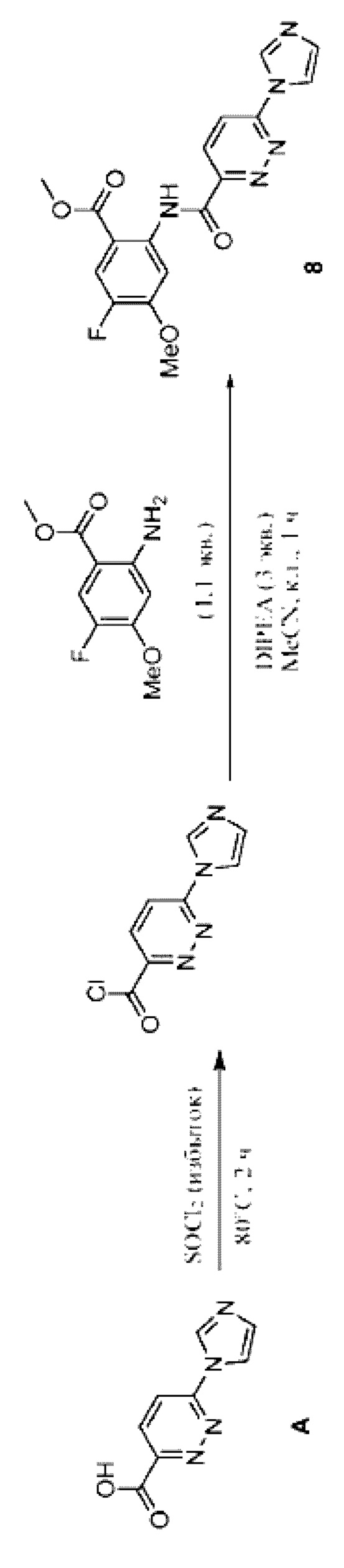
Метил-2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-5-фтор-4-метоксибензоат, 8: промежуточный продукт А (190 мг, 1 ммоль) перемешивали в присутствии SOCl2 (5 мл) при 80°С в течение 2 часов. Затем удаляли летучие вещества с последующим добавлением раствора метил-2-амино-5-фтор-4-метоксибензоат а (219 мг, 1,1 ммоля) и DIPEA (0,52 мл, 3 ммоля) в ацетонитриле (5 мл). Полученную реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакцию отслеживали с помощью LCMS. После завершения реакции растворитель удаляли и полученный неочищенный материал очищали хроматографией на колонке с силикагелем с применением 2-5% МеОН в DCM с получением соединения 8 в виде беловатого твердого вещества (223 мг). LC-MS (ESI+): m/z 372,1 [М+Н]+.
Схема G: синтез диметилоксазинонового соединения
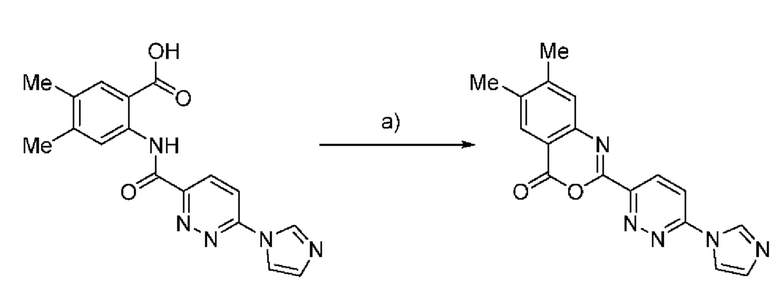
аРеагенты и условия: а) тионилхлорид, кипячение в колбе с обратным холодильником, 3 часа; DIPEA, ацетонитрил, комнатная температура, 30 минут 2 -(6-(1Н-имидазол-1 -и л)пиридазин-3-ил)-6,7 - диметил-4Н-бензо [d] [1,3] оксазин-4-он: 2-(6-(1Н-имидазол-1-ил)пиридазин-3-карбоксамидо)-4,5-диметилбензойную кислоту (33,7 мг, 0,1 ммоля) растворяли в 0,3 мл тионилхлорида и смесь нагревали в колбе с обратным холодильником в течение 3 часов. Затем избыток тионила удаляли под вакуумом. Твердое вещество растворяли в 0,5 мл безводного ацетонитрила и при комнатной температуре добавляли раствор DIPEA (26,1 мкл, 0,15 ммоля) в 0,5 мл безводного ацетонитрила. После перемешивания в течение 30 минут полученный осадок выделяли и промывали ацетонитрилом с получением продукта (26,2 мг, 82% выход).
Схема Н: синтез дифтороксазинонового соединения
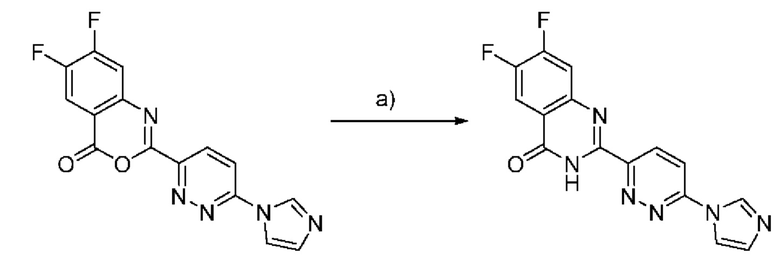
а Реагенты и условия: а) формамид, микроволновая печь, 200°С
2-(6-(1Н-имидазол-1-ил)пиридазин-3-ил)-6,7-дифторхиназолин-4(3Н)-он: раствор 2-(6-(1Н-имидазол-1-ил)пиридазин-3-ил)-6,7-дифтор-4Н-бензо[d][1,3]оксазин-4-она (32,7 мг, 0,1 ммоля) в 2 мл формамида помещали в 10-мл емкость для микроволновой печи, которую герметично закрывали и облучали на уровне температуры 200°С в течение 15 минут. Реакцию отслеживали с помощью LCMS. После завершения реакции добавляли 4 мл метанола и неочищенную смесь фильтровали и очищали препаративной ВЭЖХ с получением продукта (13,0 мг, 40% выход).
Несмотря на то, что настоящее изобретение было достаточно подробно описано и проиллюстрировано для того, чтобы специалисты в настоящей области техники смогли его реализовать и применять, для специалистов в настоящей области техники будут очевидны различные альтернативы, модификации и усовершенствования без отклонения от сути и объема формулы изобретения.
Все упомянутые в настоящем документе патенты и публикации включены в настоящий документ посредством ссылки в той же степени, как если бы каждая отдельная публикация была специально и индивидуально указана как включенная во всей своей полноте посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОЦИКЛИЧЕСКИЕ АГОНИСТЫ СТИМУЛЯТОРА ГЕНОВ ИНТЕРФЕРОНА STING | 2020 |
|
RU2813691C2 |
| БИЦИКЛИЧЕСКИЕ АГОНИСТЫ СТИМУЛЯТОРА ГЕНОВ ИНТЕРФЕРОНА STING | 2020 |
|
RU2800072C1 |
| Ингибиторы ENPP1 и способы модуляции иммунного ответа | 2018 |
|
RU2800798C2 |
| НОВОЕ ПРОИЗВОДНОЕ БЕНЗОТРИАЗОЛА, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ЭКТОНУКЛЕОТИДПИРОФОСФАТАЗЫ-ФОСФОДИЭСТЕРАЗЫ, И ЕГО ПРИМЕНЕНИЕ | 2022 |
|
RU2824598C1 |
| Бензотиофены и родственные соединения в качестве агонистов STING | 2019 |
|
RU2806274C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ АМИДНОЕ СОЕДИНЕНИЕ, ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2020 |
|
RU2823875C1 |
| СЕЛЕКТИВНЫЕ ИНГИБИТОРЫ ЭСТРОГЕНОВЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2734501C2 |
| ИНГИБИТОРЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2019 |
|
RU2806033C2 |
| НОВЫЕ ХИНОЛИНОВЫЕ СОЕДИНЕНИЯ | 2018 |
|
RU2810113C2 |
| ЗАМЕЩЕННОЕ АРОМАТИЧЕСКОЕ ПРОИЗВОДНОЕ С КОНДЕНСИРОВАННЫМИ КОЛЬЦАМИ И КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ ЕГО, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2811484C1 |
Изобретение относится к группе соединений, представленных структурными формулами в п. 1 формулы изобретения, которые обладают агонистической биологической активностью стимулятора генов интерферона (STING) и которые могут найти свое применение в медицине при лечении опухолей у страдающих ими пациентов. 3 н.п. ф-лы, 3 ил., 3 табл., 2 пр.
1. Соединение с любой из следующих формул:
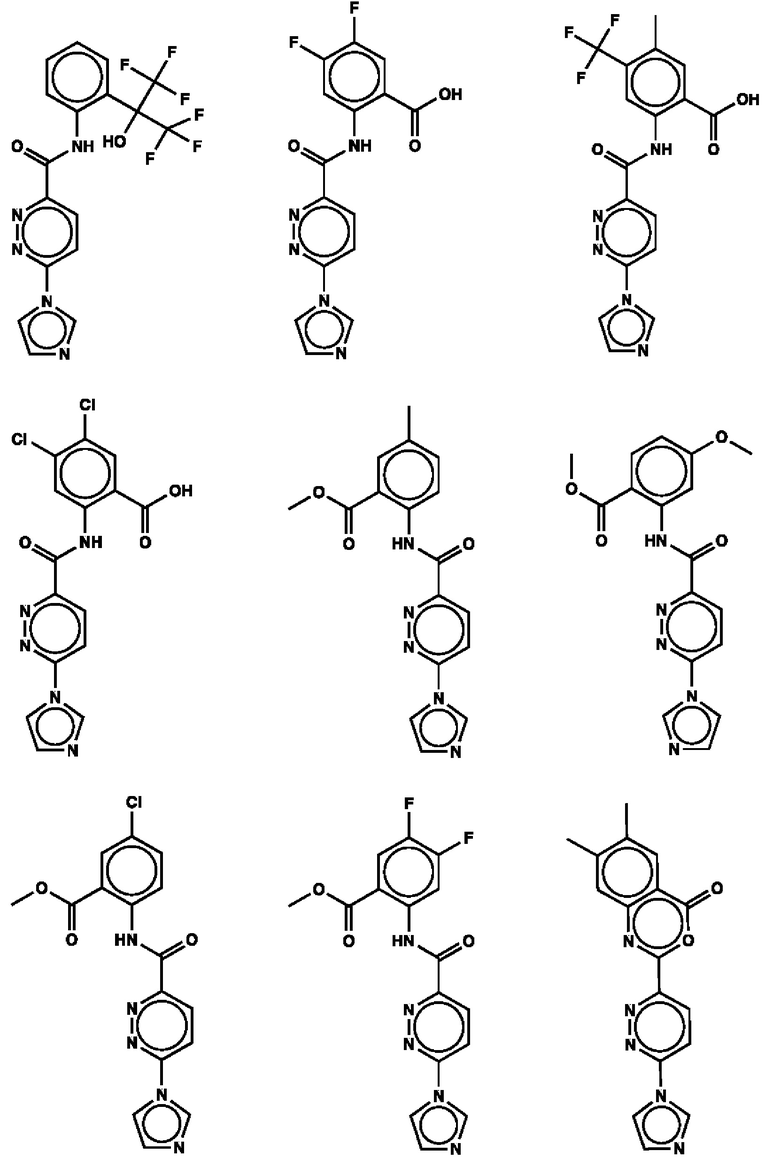
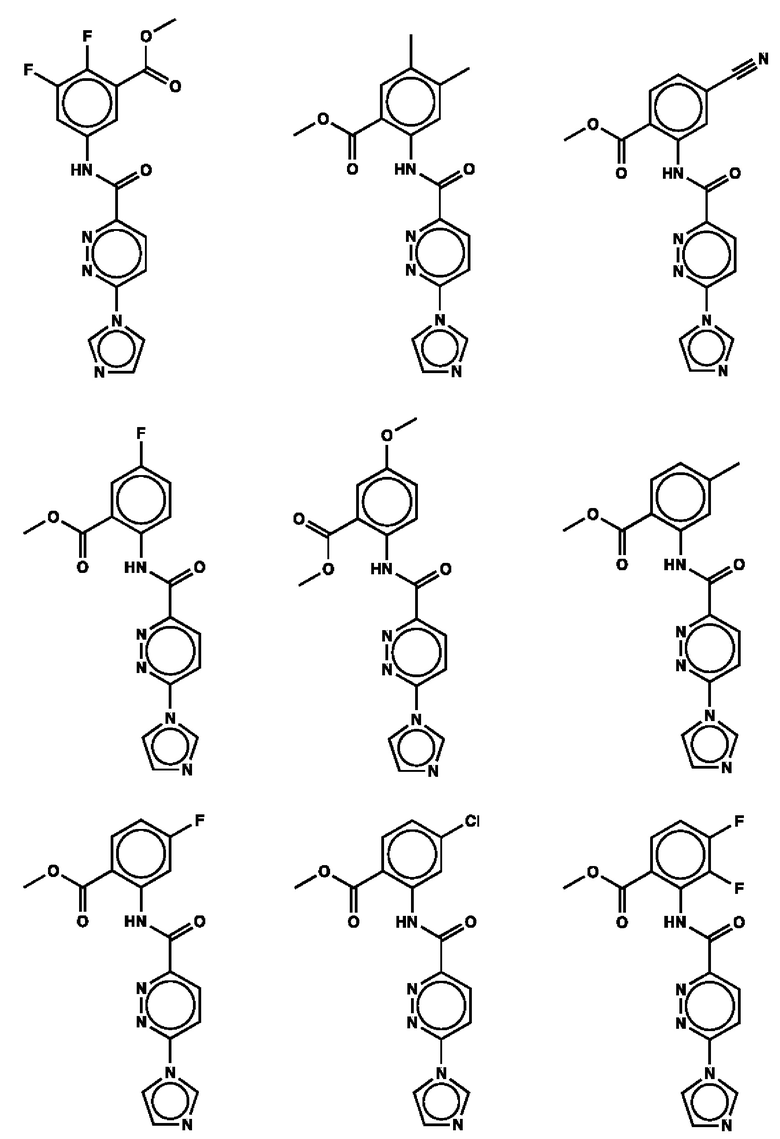
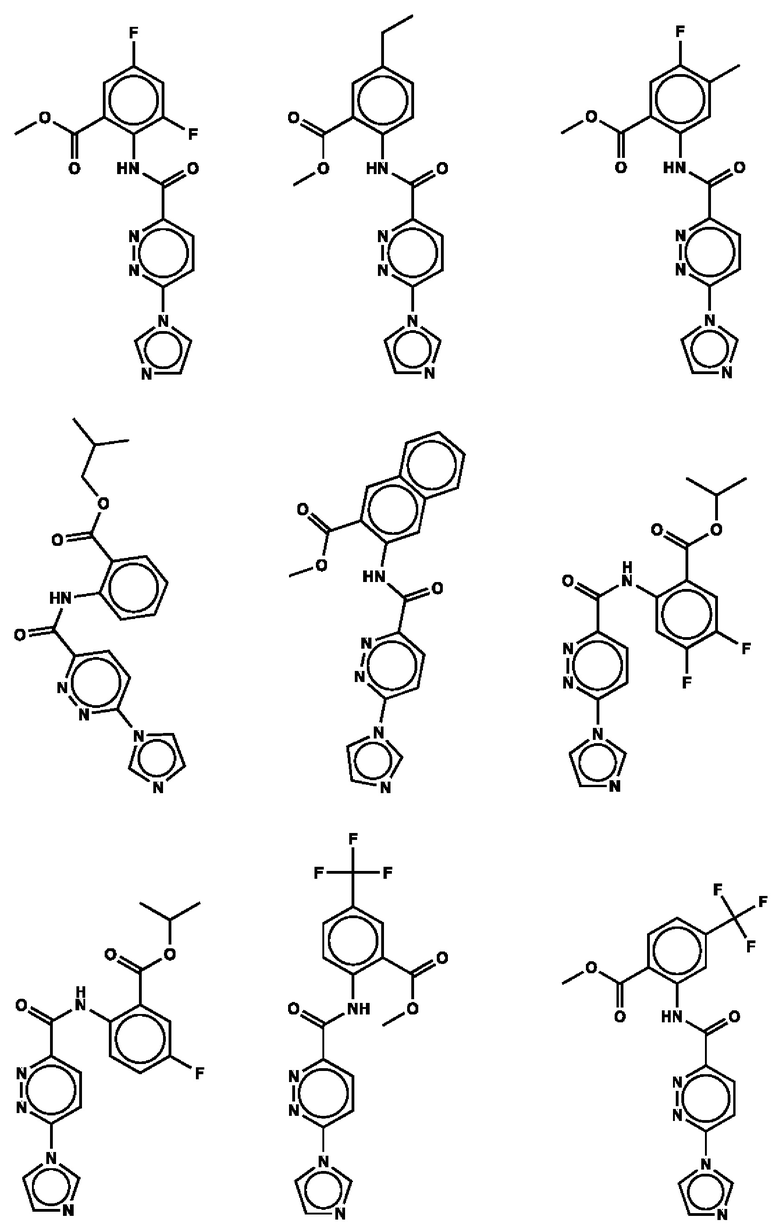
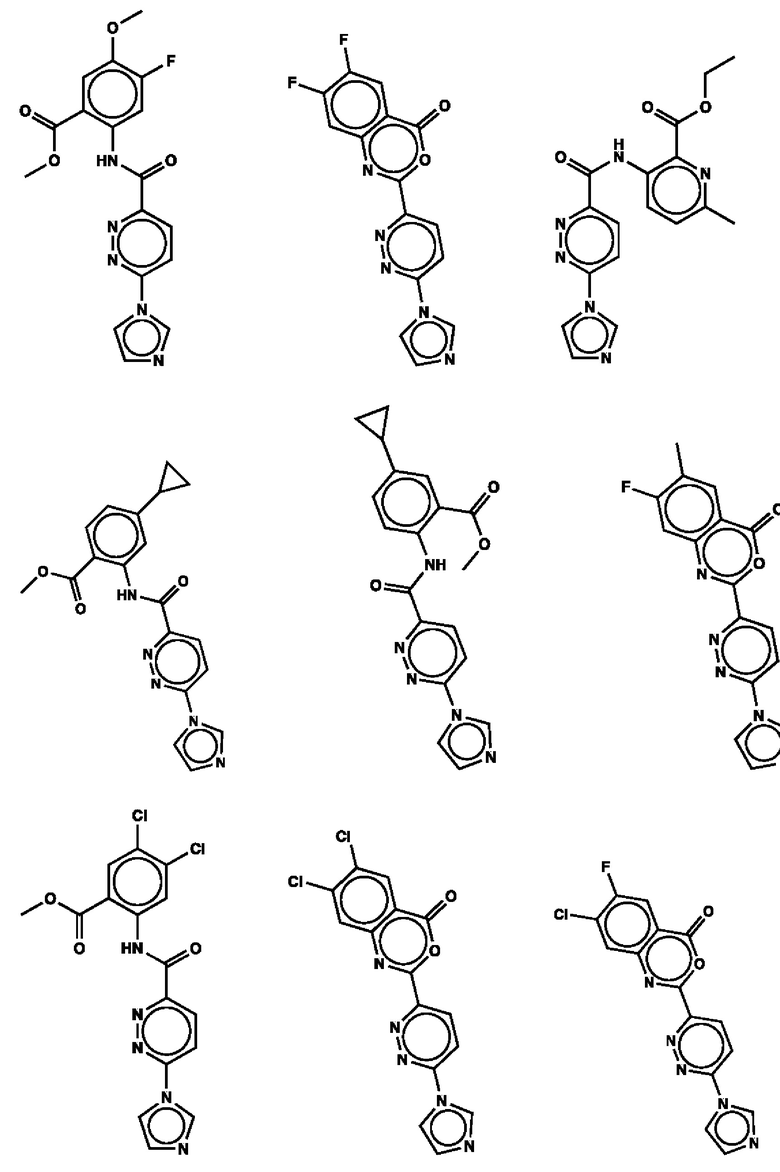
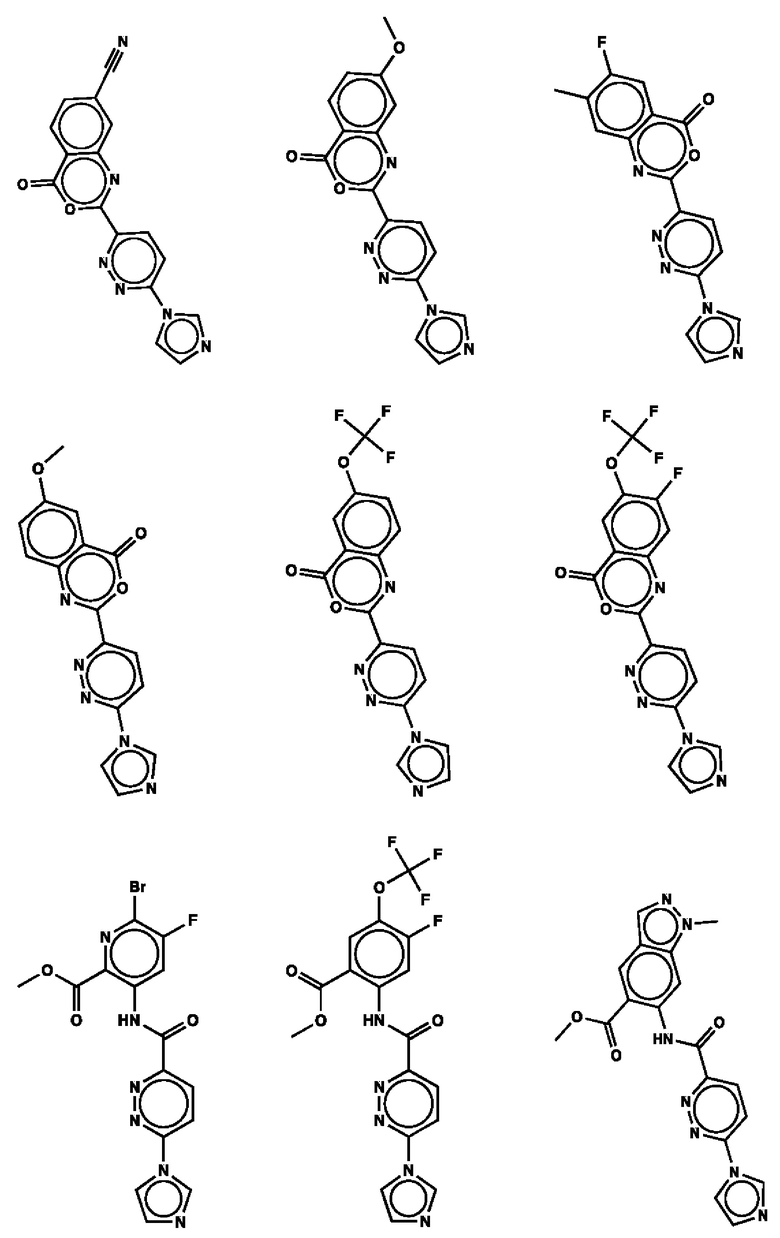
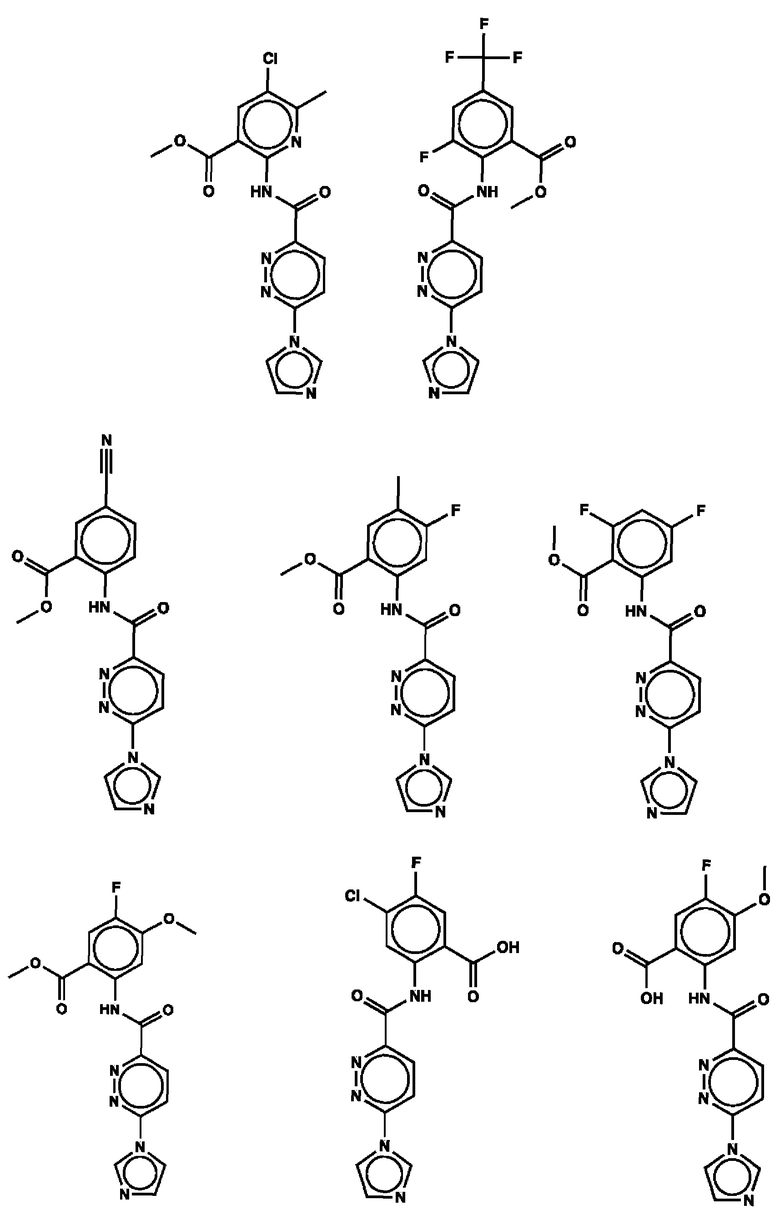
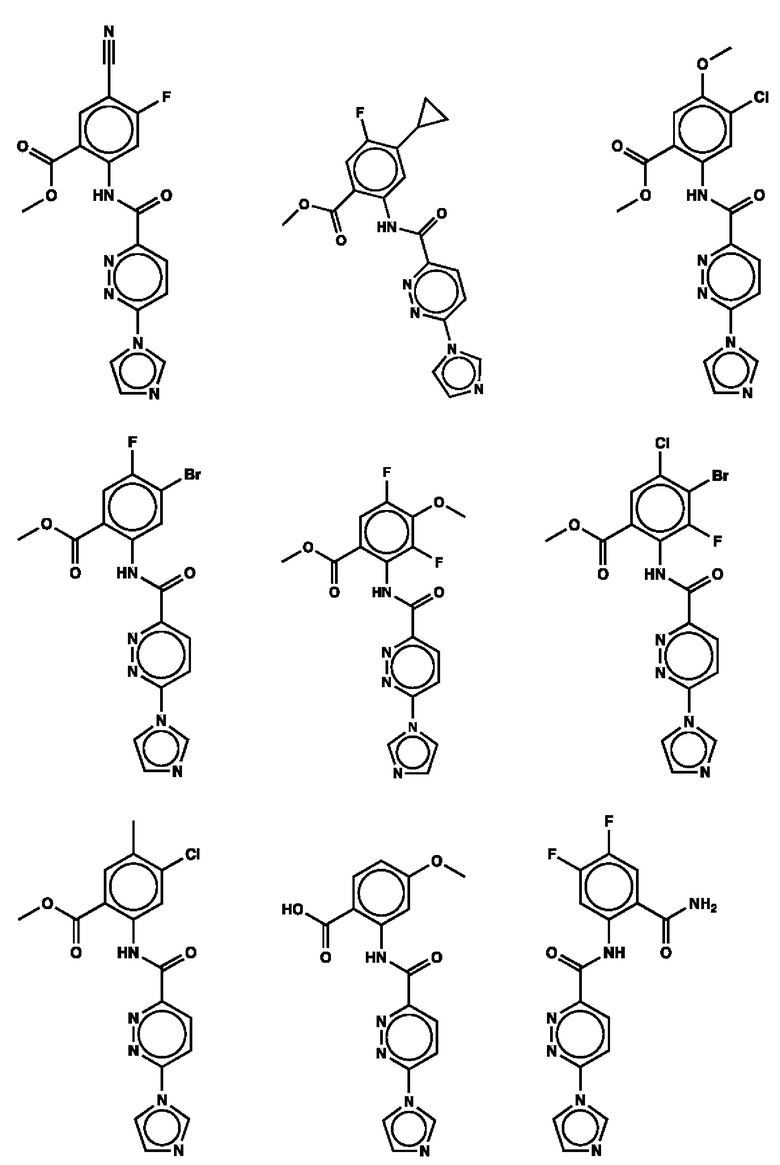
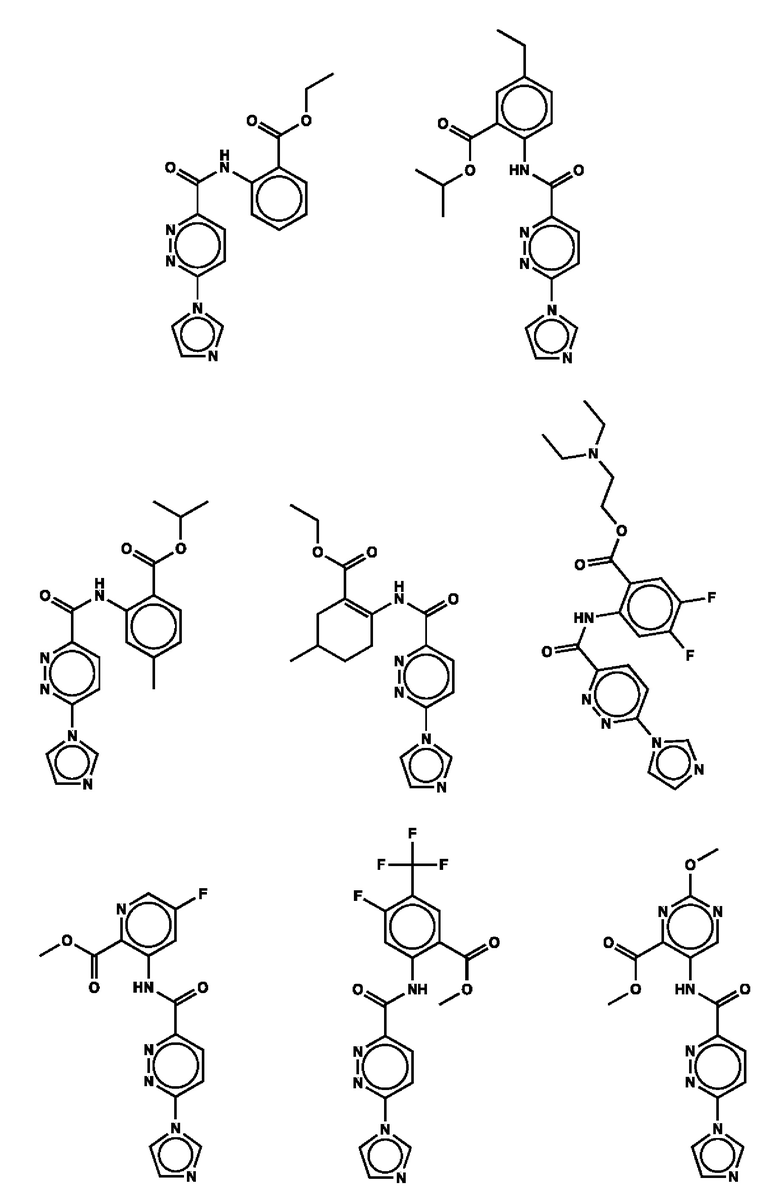
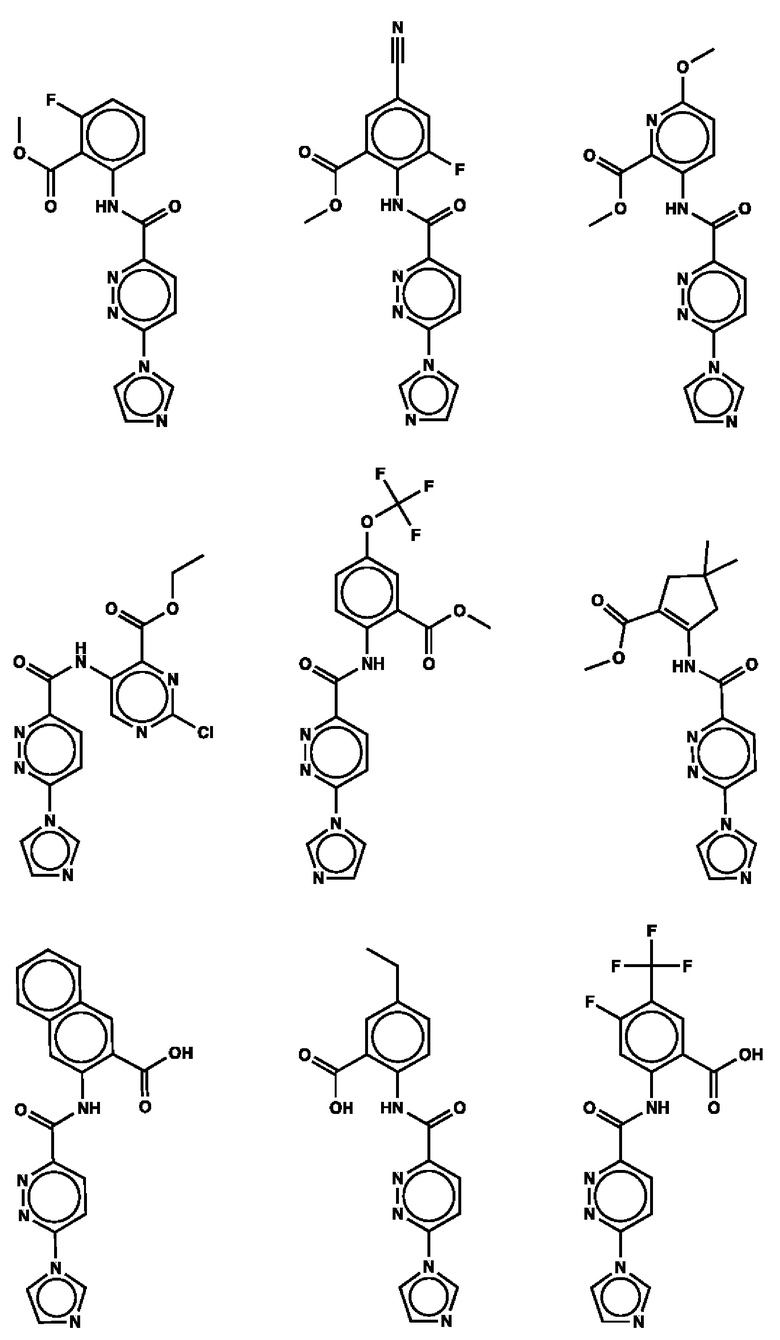
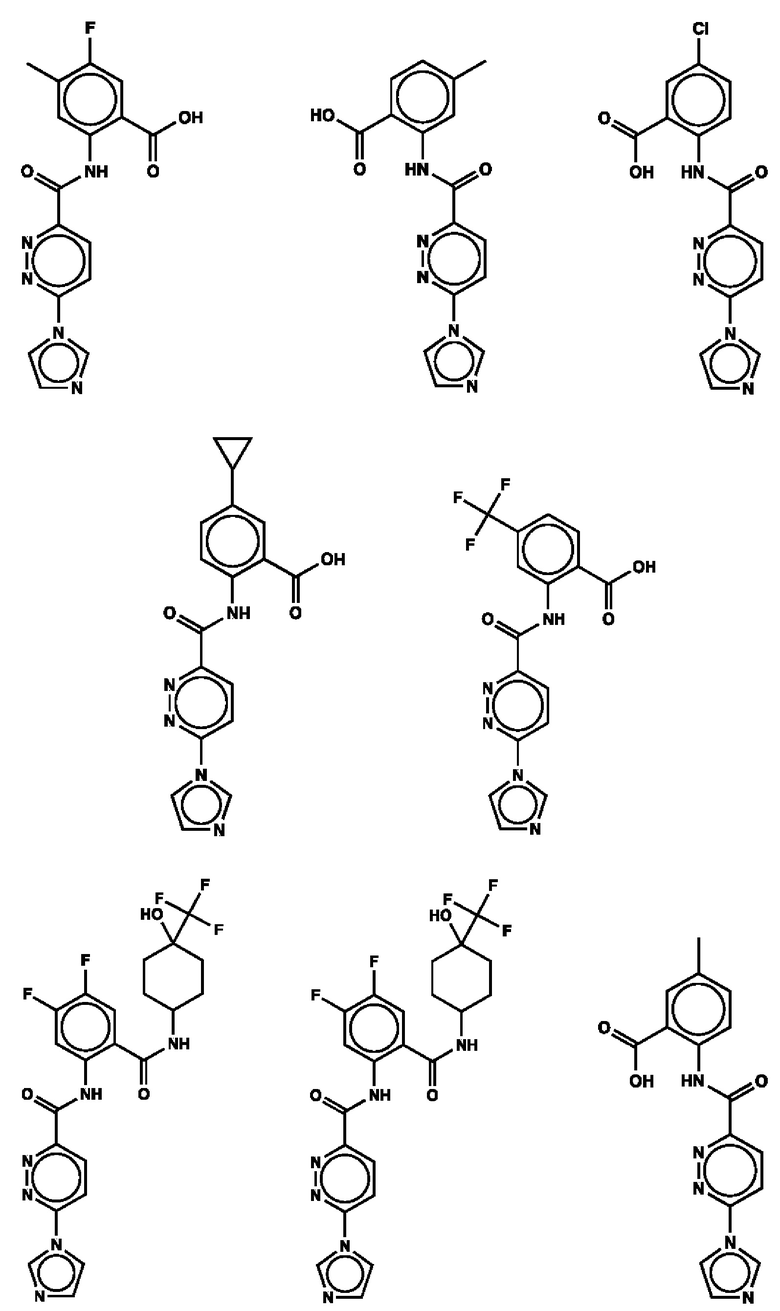
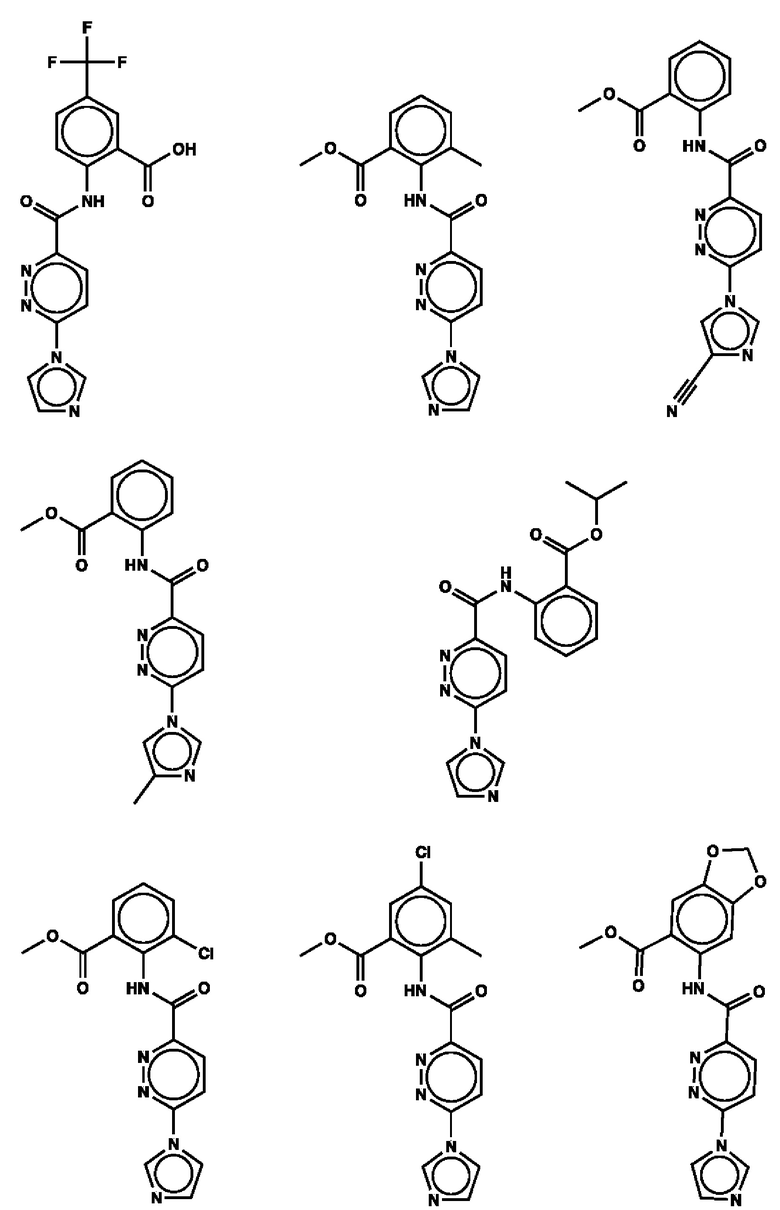
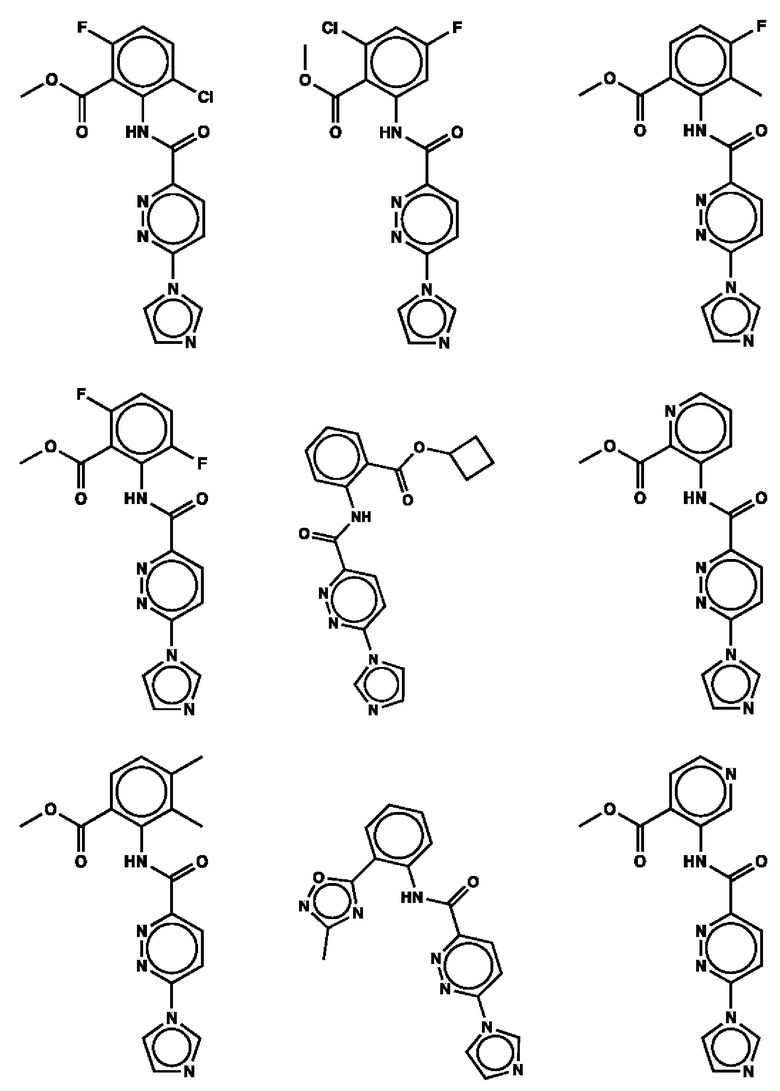
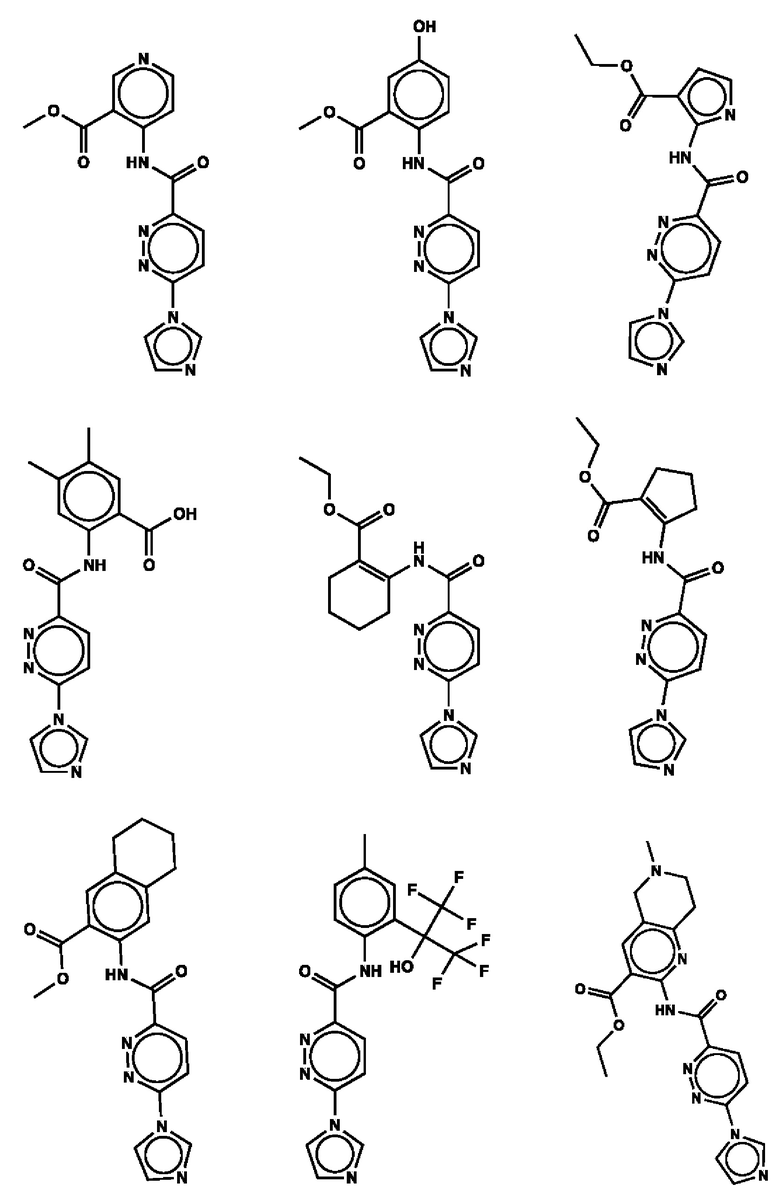
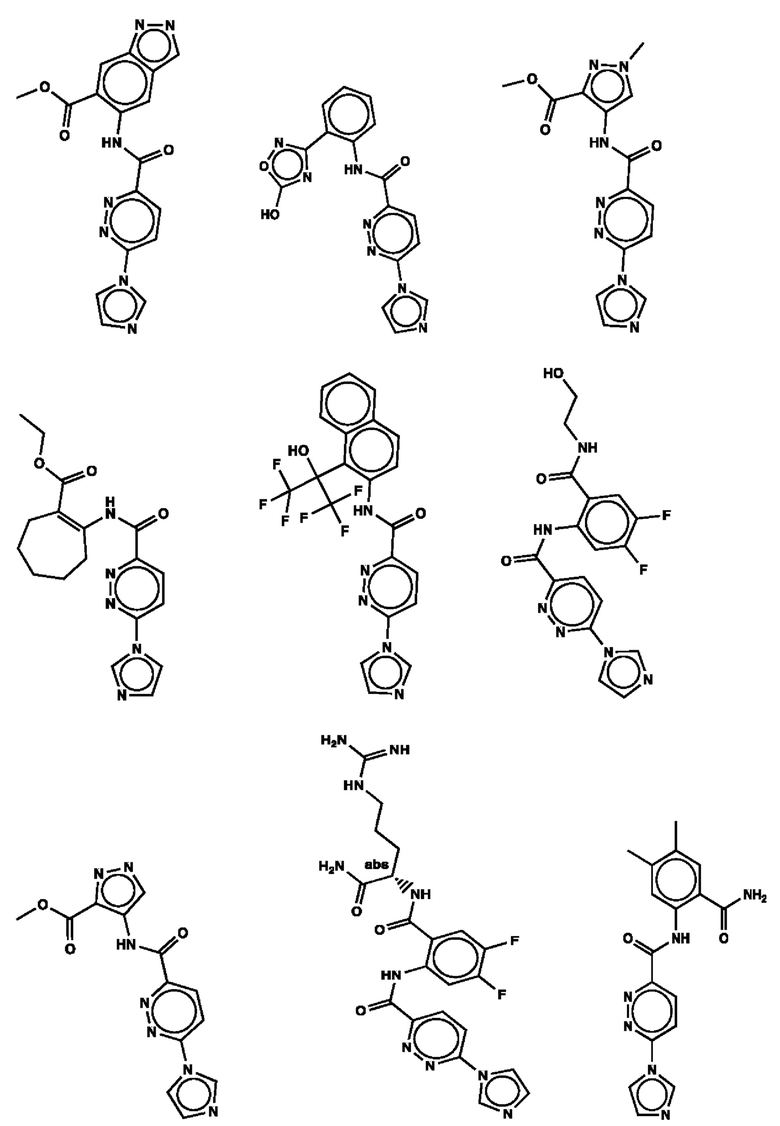
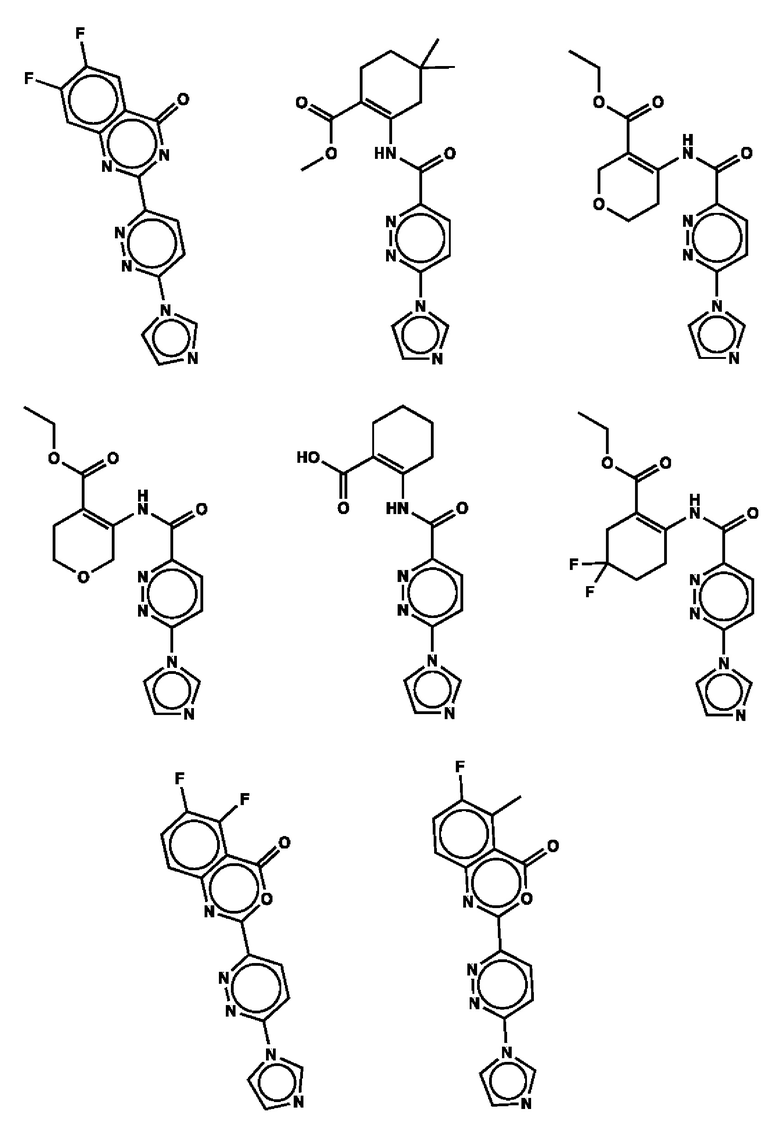
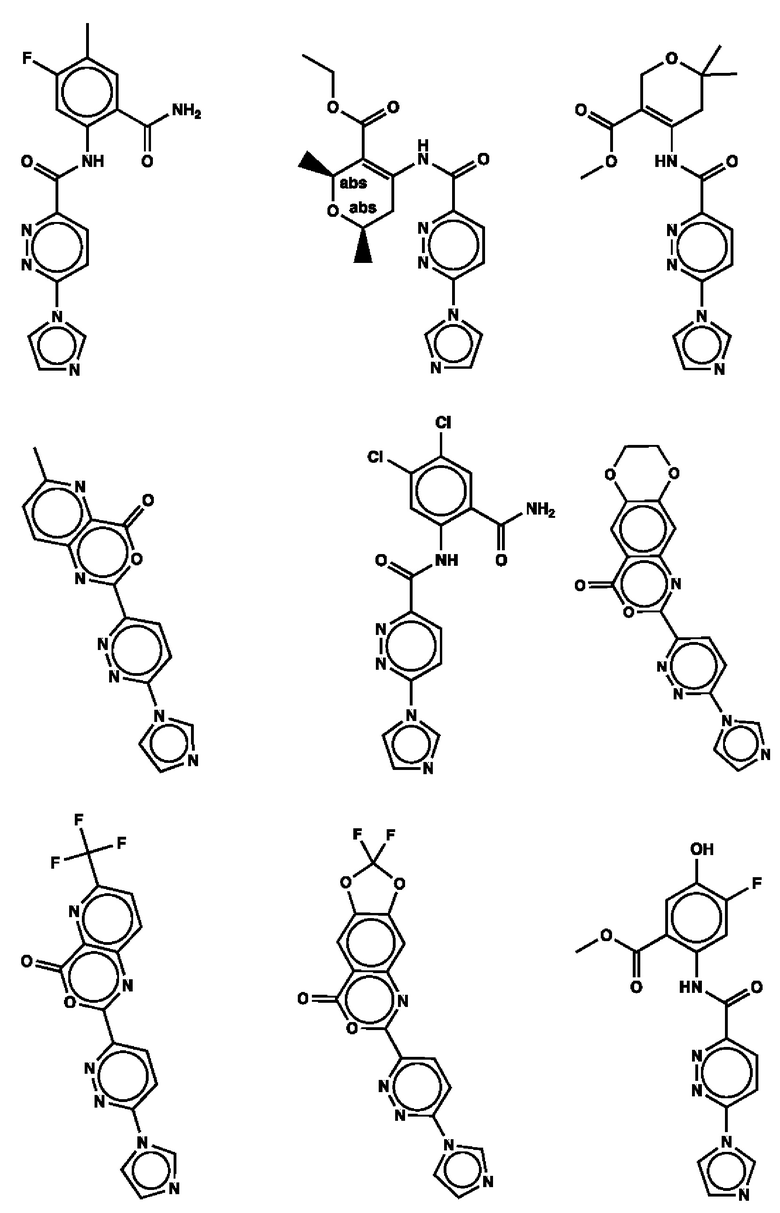
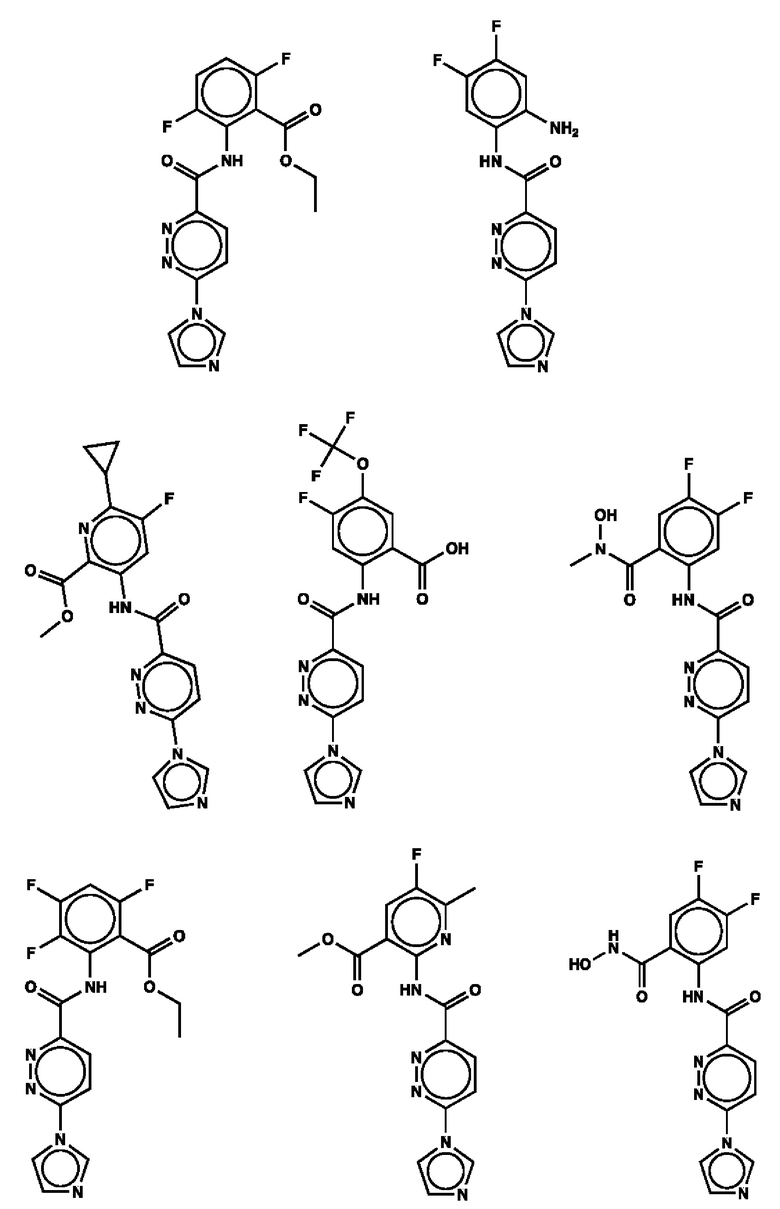
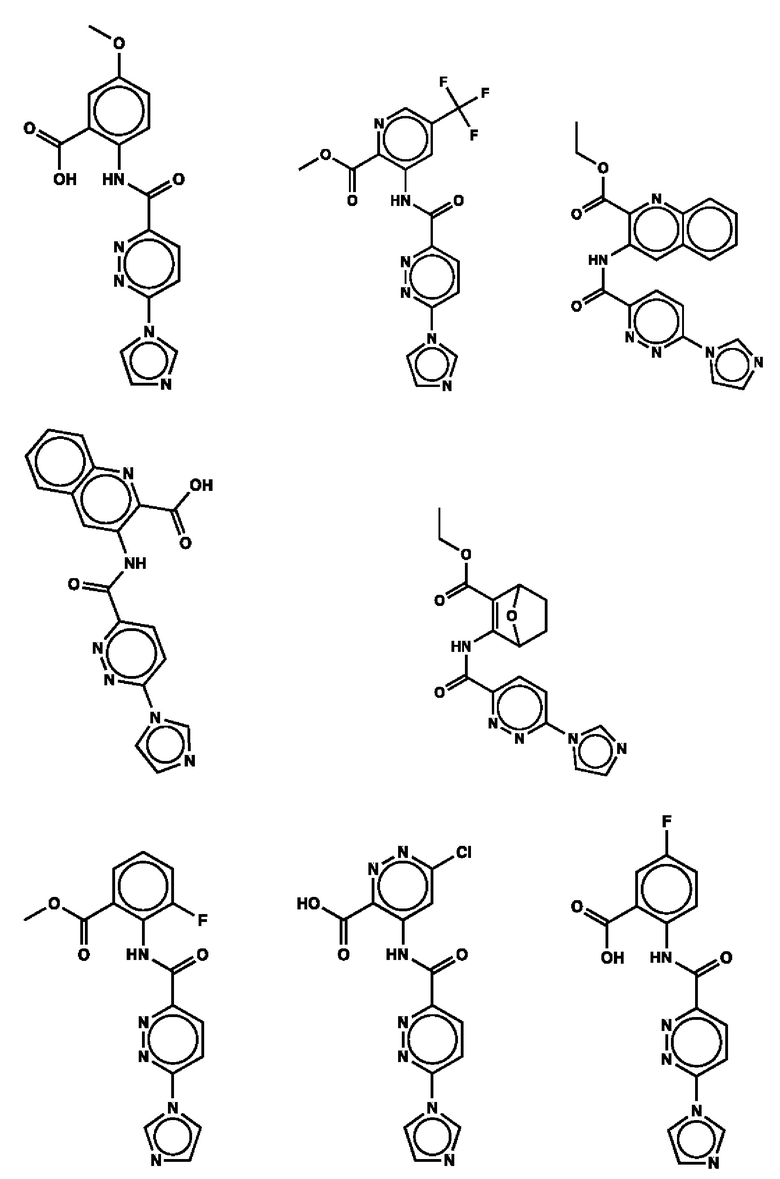
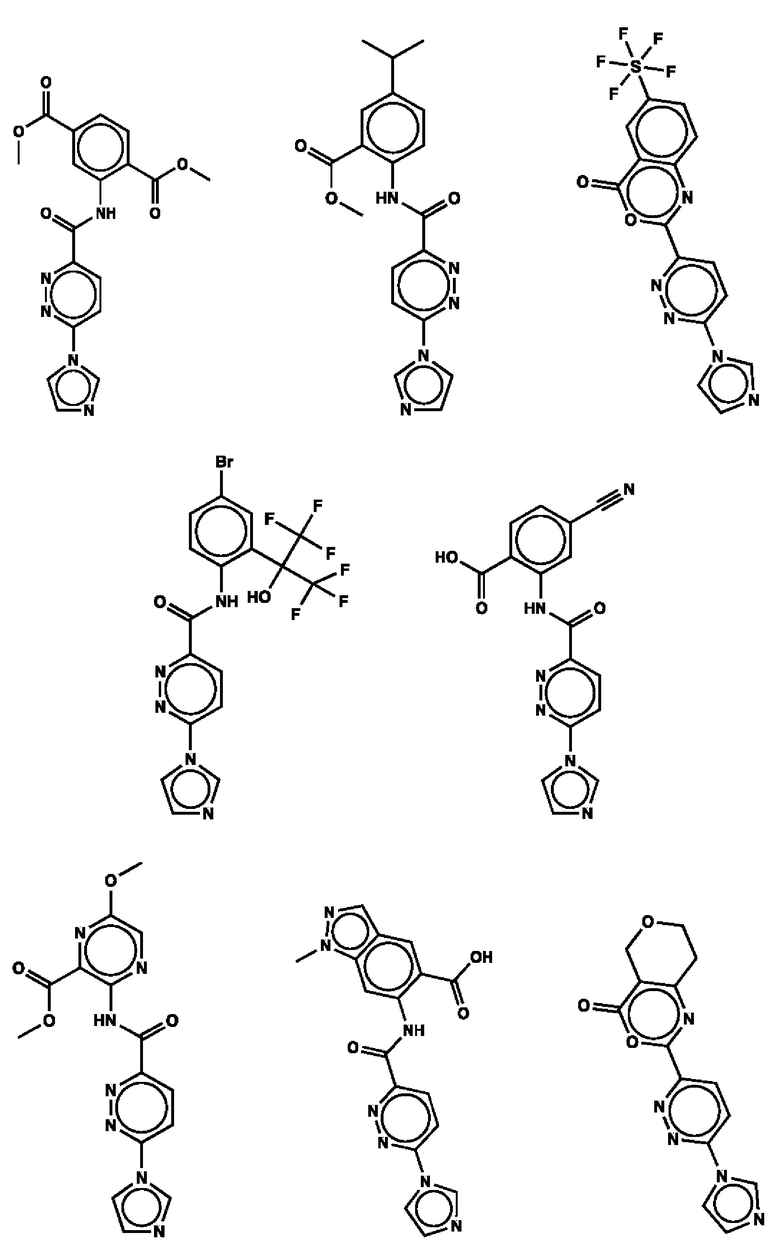
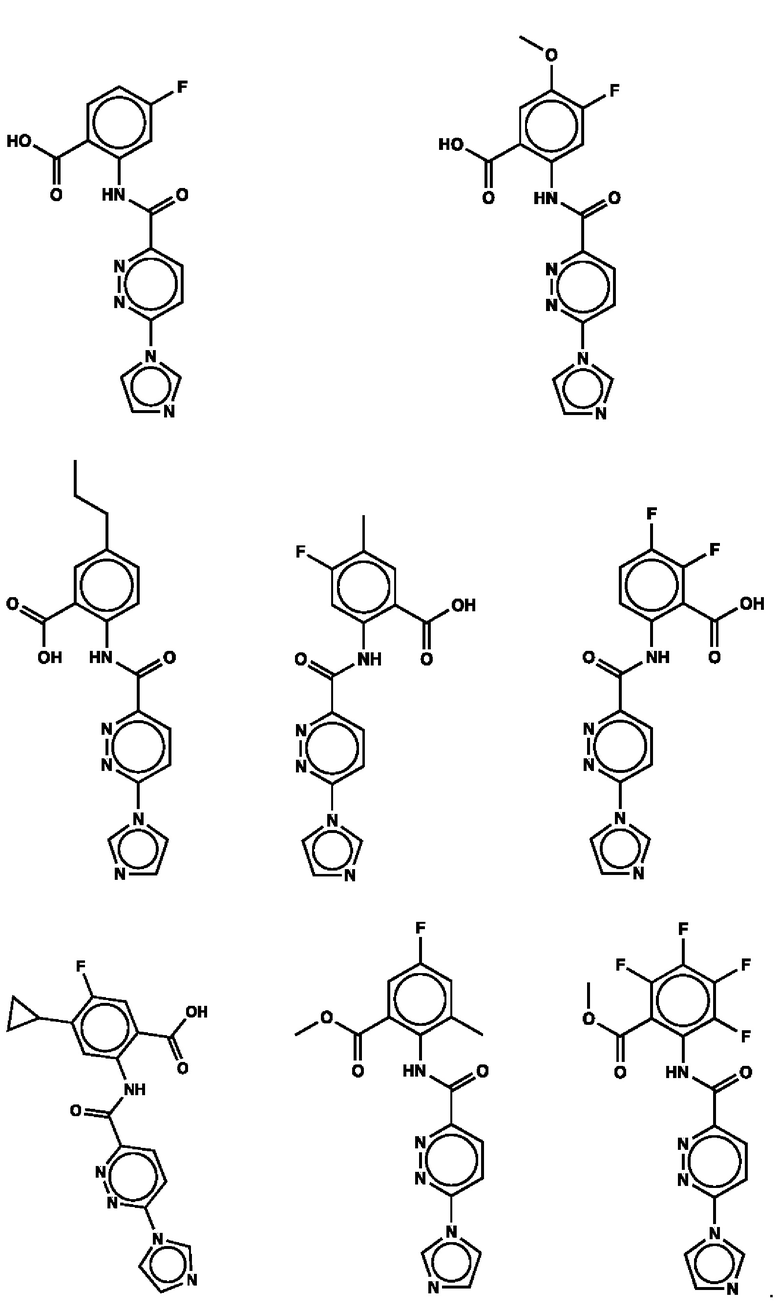
2. Применение соединения по п. 1 для изготовления лекарственного средства для лечения опухоли, связанной со стимулятором генов интерферона (STING).
3. Применение соединения по п. 1 для стимуляции экспрессии генов интерферона.
| WO 2017027646 A1, 16.02.2017 | |||
| US 20170158724 A1, 08.06.2017 | |||
| EA 201692119 А, 13.06.2017 | |||
| WO 2011048525 A1, 28.04.2011. |
Авторы
Даты
2023-12-06—Публикация
2019-02-21—Подача