ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Группа изобретений относится к фармацевтической композиции для предотвращения или лечения пародонтоза или травматического вывиха зуба и к композиции для регенерации пародонта.
УРОВЕНЬ ТЕХНИКИ
Пародонт является общим термином, который относится к тканям, окружающим зубы. Пародонт состоит из альвеолярной кости, которая поддерживает зубы в верхней челюсти (челюстной кости), периодонтальной связки, которая соединяет альвеолярную кость и зубы в пределах верхней челюсти, цементного вещества корня зуба, включающего волокна периодонтальной связки, и десны, которая представляет собой мягкую ткань, покрывающую альвеолярную кость. Фибробласты десны и фибробласты периодонтальной связки являются основными клеточными компонентами соединительной ткани, несущей мягкие ткани десны, и играют роль в формировании и поддержании внеклеточного матрикса. Среди них фибробласты десны в основном участвуют в поддержании соединительной ткани десны, тогда как известно, что фибробласты периодонтальной связки участвуют в восстановлении и регенерации прилегающей альвеолярной кости и цементного вещества корня зуба in vivo, а также формируют периодонтальную связку в качестве их уникальной функции.
Периодонтальная связка относится к фиброзной соединительной ткани, которая соединяет цементное вещество корня зуба (корневую часть) и альвеолярную кость. Оба конца периодонтальной связки заделаны в цементное вещество корня зуба и альвеолярную кость, и пучок волокон периодонтальной связки, заделанный в альвеолярную кость или цементное вещество корня зуба, называют волокном Шарпея. Функция периодонтальной связки заключается не только в фиксации зубов и поддержании структурных свойств твердых тканей, но также и в сопротивлении к воздействию окклюзивного давления и в защите мягких тканей, таких как кровеносные сосуды и нервы, от повреждения. Другой важной функцией является обеспечение питательными веществами и функция в качестве сенсорных рецепторов, и иннервация периодонтальной связки передает проприоцептивные ощущения, тактильные ощущения и болевые ощущения через тройничный нерв для восприятия и регулирования внешнего давления, прикладываемого к отдельным зубам, и играет важную роль в нервно-мышечных механизмах, регулирующих жевательную мускулатуру. Периодонтальная связка содержит много фибробластов, и эти клетки не только формируют периодонтальную связку в качестве своей уникальной функции, но также выполняют функции участия в образовании и резорбции цементного вещества зубов и альвеолярной кости, вызывая физиологическую миграцию зубов и позволяя пародонту адаптироваться к окклюзионному давлению и восстановлению повреждений.
Пародонтоз подразделяют на гингивит, ограничивающийся десной, и пародонтит, при котором воспаление распространяется на альвеолярную кость, окружающую корень зуба, и представляет собой не заболевание, которое повреждает сам зуб, а заболевание, которое вызывает воспаление пародонта, поддерживающего зуб. При возникновении пародонтоза, его клиническое проявление приводит потере зубов вследствие кровоточивости и отека десен, образования периодонтального кармана и разрушения альвеолярной кости, а причины возникновения пародонтоза включают как местные, так и системные факторы. Двумя известными местными причинными факторами являются зубной налет, зубной камень и другие местные причины, а также окклюзионная травма. Механизм патогенеза заключается в том, что при механическом накоплении зубного налета в периодонтальном кармане он становится местом обитания окружающих бактерий, это место обитания постепенно смещается от аэробных грамположительных бактерий к анаэробным грамотрицательным бактериям и пролиферирует вглубь периодонтального кармана, и эти анаэробные грамотрицательные бактерии размножаются и мигрируют вглубь периодонтального кармана. При этом, токсины и все продукты размножения анаэробных грамотрицательных бактерий непосредственно разрушают ткани или стимулируют иммунную систему, вызывая воспаление наряду с разрушением пародонта в результате различных воздействий со стороны стимулированной иммунной системы. В качестве защитного механизма против этого, в роли системных факторов выступают функции и иммунный ответ полиморфноядерных лейкоцитов. Однако известно, что важными факторами профилактики и лечения пародонтоза являются осуществление антибактериального и бактериостатического воздействия на анаэробные грамотрицательные бактерии, которые являются исходными факторами, удаление или разрушение токсических продуктов этих бактерий и восстановление утраченного пародонта.
Основное лечение пародонтоза включает процедуру снятия зубного налета (скейлинга) для удаления зубного налета и зубного камня, вызывающих пародонтоз, и, аналогично, сглаживание корня зуба является процедурой, в процессе которой удаляют зубной налет и камень, а также устраняют факторы, вызывающие воспаление, заложенные в цементном веществе поверхности корня зуба. В случае тяжелой формы воспаления, обусловленного пародонтозом, оно сопровождается повреждением альвеолярной кости, и при сильном рассасывании альвеолярной кости может быть выполнена костная пластика путем регенеративной периодонтальной хирургической операции. В качестве типа трансплантируемой кости может быть использована собственная кость пациента (аллогенная кость), ксеногенная или синтетическая кость.
Поэтому, при лечении пародонтоза считается необходимым не только удаление вызывающих пародонтоз бактерий, но и вместе с этим проведение процесса регенерации пародонта.
В настоящее время, в качестве методов лечения для восстановления разрушенного пародонта применяют костную пластику, направленную тканевую регенерацию и лечение с использованием различных факторов роста. Кроме того, применяют метод реплантации зубов, при котором основное внимание уделяется регенерации клеток периодонтальной связки и формированию нового цементного вещества корня зуба.
В связи с этим, проводятся исследования по разработке метода эффективной регенерации пародонта. Например, в патентном документе Korean Patent Registration No. 1179476 описан ген промиелоцитарного лейкоза с "цинковыми пальцами" (PLZF), который в высокой степени экспрессируется в процессе минерализации клеток периодонтальной связки человека (hPDL), ген Fk506, связывающий белок 5 (FKBP5), ген сывороточного амилоида A1 (ген SAA1), ген белка 4, связывающего жирные кислоты (FABP4), ген семейства A (FAM107A) со сходной последовательностью, ген CORIN, ген связанного с rac субстратом 3 ботулинического токсина C3 (RAC3), или ген полученного из пролактина белка (PIP), экспрессирующиеся в низкой степени гены FNDC1, PTGS2, RSAD2, NPTX1, VCAM1, MX1, IFIT1, CLDN1 или WISP2 в процессе минерализации клеток периодонтальной связки человека (hPDL). Кроме того, в патентном документе Korean Patent Registration No. 101788916 раскрыта фармацевтическая композиция для лечения пародонтоза, включающая раствор культуры амелобластов.
При воздействии на зуб или пародонт травмирующей силы, в зубе и пародонте происходят различные разрушения в зависимости от направления и величины травмирующей силы. Травмы зубов можно разделить, в общих чертах, на переломы и вывихи. Травматический вывих относится к повреждению периодонтальной связки и может быть подразделен на ударный подвывих, орбитальный вывих, латеральный вывих, полный вывих и интрузию, и травматический вывих встречается чаще всего у детей в возрасте от 8 до 12 лет. Успех реплантации полностью вывихнутого зуба зависит от регенерации периодонтальной связки, прикрепленной к полностью вывихнутому зубу, или периодонтальной связки, остающейся в альвеолярной ямке, в которой отсутствует зуб. В случае, когда не происходит регенерации периодонтальной связки, происходит рассасывание цементирующего вещества и твердой ткани корня зуба, и возникает анкилоз, при котором этот участок замещается альвеолярной костью. Поэтому конечной целью пародонтологического лечения является предотвращение прогрессирования пародонтоза и регенерация разрушенного пародонта, в том числе десны, периодонтальной связки, альвеолярной кости и цементирующего вещества, с восстановлением их до исходного состояния, но в литературе еще не сообщалось о способе, который позволяет непосредственно регенерировать или дифференцировать периодонтальную связку.
На основании упомянутых выше фактов, авторы настоящего изобретения провели интенсивные исследования по созданию способа регенерации пародонта (периодонтальной связки, цементирующего вещества и альвеолярной кости), поврежденного вследствие пародонтоза, и благодаря этим исследованиям, используя индуцирование дифференцировки клеток периодонтальной связки, была подтверждена возможность нового применения пептида, которое позволяет не только лечить поврежденную периодонтальную связку при пародонтозе или травматическом вывихе зуба, но и регенерировать поврежденные цементирующую вещество и альвеолярную кость, в результате чего и было создано настоящее изобретение.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая задача
Задачей настоящего изобретения является создание фармацевтической композиции для предотвращения или лечения пародонтоза или травматического вывиха зуба.
Еще одной задачей настоящего изобретения является создание композиции для регенерации пародонта.
Еще одной задачей настоящего изобретения является создание композиции для активирования экспрессии любого одного или более генов BSP, DMP1, CAP, COL3 и периостина.
Еще одной задачей настоящего изобретения является разработка способа лечения пародонтоза или травматического вывиха зуба у индивидуума, где способ включает введение эффективного количества пептида или его фармацевтически приемлемой соли индивидууму, нуждающемуся в лечении пародонтоза или травматического вывиха зуба.
Еще одной задачей настоящего изобретения является разработка применения пептида или его фармацевтически приемлемой соли в производстве лекарственного препарата для предотвращения или лечения пародонтоза или травматического вывиха зуба.
Задачи настоящего изобретения не ограничиваются упомянутыми выше задачами, и для специалистов в данной области, после ознакомления с приведенным далее описанием изобретения, могут быть очевидными дополнительные неупомянутые выше задачи изобретения.
Решение технической задачи
В одном аспекте настоящего изобретения, для решения упомянутой выше технической задачи предлагается фармацевтическая композиция для предотвращения или лечения пародонтоза или травматического вывиха зуба, включающая пептид или его фармацевтически приемлемую соль, содержащий аминокислотную последовательность следующей общей формулы 1:
K-Y-K-Q-X5-X6-X7-X8-Y-K (общая формула 1)
где в общей формуле 1,
от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K);
X8 представляет собой аспарагин (N) или серин (S).
При условии, что пептид может оказывать профилактическое или терапевтическое воздействие на пародонтоз или травматический вывих зуба, альтернативный пептид, имеющий аминокислотную последовательность, из которой состоит пептид, и последовательность, отличающаяся по одному или более аминокислотным остаткам, также включены в объем пептидов, предлагаемых в настоящем изобретении.
В настоящем изобретении, для природных аминокислот, составляющих пептиды, используют традиционные обозначения из одной или трех букв. Кроме того, аминокислоты, которые обозначены в изобретении аббревиатурой, описаны в соответствии с номенклатурой IUPAC-IUB.
Авторы настоящего изобретения создали настоящее изобретение в результате подтверждения того факта, что пептид позволяет лечить пародонтоз или травматический вывих зуба путем активизации регенерации периодонтальной связки или дифференцировки в остеобласты и цементобласты, и регенерации альвеолярной кости и цементного вещества корня зуба.
Было подтверждено, что пептид увеличивает экспрессию BSP, DMP1 и CAP, которые являются маркерными генами для дифференцировки остеобластов и цементобластов, и увеличивает экспрессию периостина и COL3, которые являются маркерными генами для дифференцировки периодонтальной связки в клетках периодонтальной связки человека. Кроме того, было подтверждено, что пептид увеличивает экспрессию BSP и DMP1, маркерных генов дифференцировки остеобластов и цементобластов в мезенхимальных стволовых клетках человека.
Кроме того, в результате повреждения пародонта в экспериментальной модели на животных, было подтверждено, что пептид регенерирует альвеолярную кость, цементное вещество корня зуба и периодонтальную связку. В частности, было подтверждено, что пептид по настоящему изобретению обладает эффектом регенерации альвеолярной кости и формирования новой ткани, подобной ткани цементного вещества корня зуба, и новой ткани, подобной ткани периодонтальной связки, и новая периодонтальная связка, образованная пептидом по настоящему изобретению, встраивается в заново сформированную альвеолярную кость и цементное вещество корня зуба.
В одном варианте осуществления, пептид может представлять собой пептид, в котором была проведена консервативная замена в одной или более аминокислотах.
"Консервативная замена" означает замену аминокислоты на другую аминокислоту, имеющую аналогичные структурные и/или химические свойства. Пептиды могут иметь, например, одну или более консервативных замен, все еще сохраняя при этом ту же самую или аналогичную биологическую активность. Такие аминокислотные замены могут обычно проводиться с учетом сходства полярности, заряда, растворимости, гидрофобности, гидрофильности и/или амфипатической природы остатков. Например, положительно заряженные (с основными свойствами) аминокислоты включают аргинин, лизин и гистидин; отрицательно заряженные (с кислотными свойствами) аминокислоты включают глутаминовую кислоту и аспарагиновую кислоту; ароматические аминокислоты включают фенилаланин, триптофан и тирозин, и гидрофобные аминокислоты включают аланин, валин, изолейцин, лейцин, метионин, фенилаланин, тирозин и триптофан. Кроме того, аминокислоты могут быть подразделены на аминокислоты, имеющие электрически заряженную боковую цепь, и аминокислоты, имеющие электрически незаряженную боковую цепь; и аминокислоты, имеющие электрически заряженную боковую цепь, включают аспарагиновую кислоту, глутаминовую кислоту, лизин, аргинин и гистидин; аминокислоты, имеющие электрически незаряженную боковую цепь, могут быть в свою очередь подразделены на неполярные аминокислоты или полярные аминокислоты; и неполярные аминокислоты включают глицин, аланин, валин, лейцин, изолейцин, метионин и пролин, и полярные аминокислоты включают серин, треонин, цистеин, аспарагин и глутамин. Предполагается, что консервативные замены на аминокислоты, имеющие описанные выше аналогичные свойства, могут проявлять такую же или аналогичную активность.
По сути, даже в случае, когда аминокислоты с кислотными свойствами, аминокислоты с основными свойствами или ароматические аминокислоты, образующие пептид по настоящему изобретению, заменяют на другие аминокислоты с кислотными свойствами, аминокислоты с основными свойствами или ароматические аминокислоты, эффект пептида, предлагаемого в настоящем изобретении, может проявляться сам по себе, и так как эффекты пептида, предлагаемого в настоящем изобретении, могут проявляться сами по себе, то очевидно, что альтернативный пептид, имеющий аминокислотную последовательность, образующую пептид настоящего изобретения, и последовательности, отличающиеся одним или более аминокислотными остатками, также входят в объем пептидов, предлагаемых в настоящем изобретении.
Кроме того, даже в случае, когда пептид по настоящему изобретению имеет форму, в которой любая аминокислота добавлена к его N-концу или C-концу, эффект пептида, предлагаемого в настоящем изобретении, может проявляться сам по себе, и следовательно он входит в объем пептида, предлагаемого в настоящем изобретении. В качестве примера, он может находиться в форме, в которой от 1 до 300 аминокислот добавлены к N-концу или C-концу пептида, в качестве еще одного примера, он может находиться в форме, в которой от 1 до 100 аминокислот добавлены к N-концу или C-концу пептида, и еще в качестве одного примера, он может находиться в форме, в которой от 1 до 24 аминокислот добавлены к N-концу или C-концу пептида.
В одном варианте осуществления, пептид включает аминокислотную последовательность, являющуюся любой одной из последовательностей SEQ ID NOs: 1-16.
В другом варианте осуществления, пептид состоит в основном из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16, или пептид состоит из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16.
Даже в случае, когда пептид описан в изобретении как "пептид, состоящий из конкретной последовательности SEQ ID NO", когда пептид обладает такой же или соответствующей активностью, что и пептид, состоящий из аминокислотной последовательности, соответствующей SEQ ID NO, не исключается добавление бессмысленных последовательностей до и после аминокислотной последовательности, соответствующей SEQ ID NO, или наличие мутаций, которые могут встречаться в природе, или их молчащих мутаций, и даже в случае, когда имеет место такое добавление последовательности или наличие мутации, очевидно, что такой пептид входит в объем настоящего изобретения. То есть, даже в случае наличия различия в некоторых последовательностях, они могут входить в объем настоящего изобретения, если они проявляют гомологичность конкретного или более высокого уровня и проявляют такую же или аналогичную активность. В частности, пептид по настоящему изобретению может включать, не этим не ограничивая, аминокислотную последовательность, имеющую гомологичность или идентичность 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% или выше.
"Гомологичность" или "идентичность" относится к степени, в которой две данных аминокислотных последовательности или нуклеотидных последовательности находятся в родстве друг с другом, и эти характеристики могут быть выражены в процентах. Термины "гомологичность" и "идентичность" часто могут использоваться взаимозаменяемо.
Имеют ли любые две пептидные последовательности гомологичность, сходство или идентичность, может быть определено, например, методом, описанным в публикации Pearson et al, Proc. Natl. Acad. Sci. (1988) USA 85: 2444, используя известный реализуемый на компьютере алгоритм, такой как программа "FASTA". Кроме того, может быть использован, выполняемый в программе Needleman пакета программ EMBOSS (EMBOSS: The European Molecular Biology Open Software Suite, Rice et al., 2000, Trends Genet. 16: 276-277) (version 5.0.0 or later) алгоритм Нидлмана - Вунша (Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443-453). В этот список могут быть включены пакеты программ GCG (Devereux, J., et al, Nucleic Acids Research 12: 387 (1984)), BLASTP, BLASTN, FASTA (Atschul, [S.] [F.,] [ET AL, J MOLEC BIOL 215]: 403 (1990); Guide to Huge Computers, Martin J. Bishop, [ED.,] Academic Press, San Diego,1994, and [CARILLO ETA/.](1988) SIAM J Applied Math 48: 1073). Например, для определения гомологичности, сходства или идентичности могут быть использованы методики BLAST или ClustalW из базы данных Национального центра биотехнологической информации США.
Гомологичность, сходство или идентичность пептидов можно определить путем сравнения информации о последовательности с использованием компьютерной программы GAP, такой как описанной в публикации Needleman et al. (1970), J Mol Biol. 48: 443, например, как описано в публикации Smith and Waterman, Adv. Appl. Math (1981) 2:482. В общих чертах, в программе GAP определяется суммарное число символов в более короткой из двух последовательностей, деленное на число символов со сходным выравниванием (то есть аминокислот). Параметры по умолчанию для программы GAP могут включать: (1) матрицу сравнения с унарной операцией (содержащую значения 1 для идентичности и 0 для неидентичности) и взвешенную матрицу сравнения (или EDNAFULL (EMBOSS version of NCBI NUC4.4) подстановочную матрицу), предложенную в публикации Gribskov et al (1986) Nucl. Acids Res. 14: 6745, описанную в атласе Schwartz and Dayhoff, eds., Atlas Of Protein Sequence And Structure, National Biomedical Research Foundation, pp. 353-358 (1979); (2) штраф 3,0 за каждый пропуск в последовательности и дополнительный штраф 0,10 за каждый символ в каждом пропуске (или штраф на внесение делеции 10 и штраф на продолжение делеции 0,5); и (3) отсутствие штрафа за концевые пропуски. Таким образом, используемый в изобретении термин "гомологичность" или "идентичность" относится к релевантности между последовательностями.
В одном варианте осуществления, пептид может быть использован в форме только единственного пептида или в форме полипептида, в котором пептид повторяется два или более раз и связан.
Поэтому, фармацевтическая композиция по пункту 1, включающая полипептид, представляет собой фармацевтическую композицию, в которой пептид является многократно связанным.
В одном варианте осуществления, пептид, включающий аминокислотную последовательность общей формулы 1, применительно к настоящему изобретению может быть получен комбинацией различных методов получения различных пептидов.
В зависимости от длины пептида по настоящему изобретению, его можно синтезировать с помощью метода, хорошо известного в данной области техники, например, с помощью автоматического синтезатора пептидов, или его можно получить с помощью технологии генной инженерии. В частности, пептиды по настоящему изобретению могут быть получены стандартным синтетическим методом, с помощью рекомбинантной экспрессирующей системы или любым другим методом, известным в данной области. Соответственно, пептиды по настоящему изобретению могут быть синтезированы рядом методов, включающих, но этим не ограничивая, например, приведенные ниже методы:
(a) метод постадийного синтеза пептидов или путем сборки фрагментов при помощи твердофазных или жидкофазных методов, и выделения и очистки готового пептидного продукта; или
(b) метод экспрессирования конструкции нуклеиновой кислоты, кодирующей пептид в клетке-хозяина, и извлечения продукта экспрессирования из культуры клетки-хозяина; или
(c) метод проведения бесклеточного in vitro экспрессирования конструкции нуклеиновой кислоты, кодирующей пептид, и извлечения продукта экспрессирования; или
метод получения фрагмента пептида с помощью любой комбинации методов (a), (b) и (c), и затем лигирования с получением пептида, и извлечения пептида.
Кроме того, получение пептида может включать модификацию с использованием L- или D-формы аминокислоты и/или не встречающихся в природе аминокислот; и/или путем модификации встречающихся в природе последовательностей, например, модификации функциональных групп боковой цепи, внутримолекулярных ковалентных связей, такой как образование кольца между боковыми цепями, метилирование, ацилирование, убиквитинирование, фосфорилирование, аминогексанация, биотинилирование, и так далее. Кроме того, упомянутые выше модификации включают все замены на невстречающиеся в природе соединения.
В качестве замененных или добавленных аминокислот, используемых в упомянутых выше модификациях, могут применяться атипичные или невстречающиеся в природе аминокислоты, а также 20 аминокислот, обычно обнаруживаемых в белках человека. Коммерческие источники атипичных аминокислот могут включать, но этим не ограничивая, фармацевтическую продукцию компаний Sigma-Aldrich, ChemPep и Genzyme. Пептиды, включающие эти аминокислоты и канонические пептидные последовательности, могут быть синтезированы или приобретены у промышленных компаний, специализирующихся на синтезе пептидов, например, American Peptide Company или Bachem в США, или Anygen в Южной Корее, но список производящих пептиды компаний не ограничивается указанными выше.
Производные аминокислот могут быть также получены подобным образом, и в качестве одного из примеров может быть названа 4-имидазоуксусная кислота.
Кроме того, пептид по настоящему изобретению может иметь немодифицированный N-конец и/или С-конец, но для защиты от протеолитических ферментов in vivo и повышения стабильности используют модифицированную форму, в которой его N-конец и/или С-конец химически модифицируют или защищают органической группой, или к пептидному концу добавляют аминокислоту, и такой пептид также входит в объем пептида по настоящему изобретению. В случае, когда С-конец не подвергают модифицированию, конец пептида по настоящему изобретению имеет свободную карбоксильную группу, но эта конкретная группа не является ограничением.
В частности, в случае химически синтезированного пептида, так как N- и С-концы несут на себе заряд, N-конец может быть ацетилирован и/или С-конец может быть амидирован для удаления этих зарядов, но такой подход не является конкретным ограничением.
Пептид может включать пептид, имеющий повышенную структурную стабильность к воздействию нагревания, pH, и других факторов, обусловленную мутацией или модификацией в аминокислотной последовательности; повышенный эффект предотвращения или лечения пародонтоза или травматического вывиха зуба, или повышенную способность к регенерации ткани периодонтальной связки.
Пептид включает как пептид сам по себе, так и его соль (например, фармацевтически приемлемую соль пептида), или его сольват.
На тип соли не накладывают конкретных ограничений. Однако, предпочтительно, когда солевая форма является безопасной и эффективной для индивидуума, такого как млекопитающее, но млекопитающее не является конкретным ограничением.
Кроме того, пептид может находиться в любой фармацевтически приемлемой форме.
"Фармацевтически приемлемое" означает количество, которое является достаточным для проявления терапевтического эффекта и не вызывает побочных эффектов, и это количество может быть легко определено специалистом в данной области с учетом факторов, хорошо известных в медицине, включающих тип заболевания, возраст пациента, массу тела, состояние здоровья или пол, восприимчивость пациента к воздействию препарата, способ применения, способ введения, количество введений, продолжительность лечения и лекарственное средство, используемое в комбинации или параллельно.
В одном варианте осуществления, пептид может быть в форме его фармацевтически приемлемой соли. Соли включают обычные соли присоединения кислоты, используемые в фармацевтике, например, при пародонтозе, например, соли, образованные неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота или азотная кислота, и соли, образованные органическими кислотами, такими как уксусная кислота, пропионовая кислота, янтарная кислота, гликолевая кислота, стеариновая кислота, лимонная кислота, малеиновая кислота, малоновая кислота, метансульфоновая кислота, винная кислота, яблочная кислота, фенилуксусная кислота, глутаминовая кислота, бензойная кислота, салициловая кислота, 2-ацетоксибензойная кислота, фумаровая кислота, толуолсульфоновая кислота, щавелевая кислота или трифторуксусная кислота. Кроме того, соль может представлять собой соль присоединения основания, такого как аммоний, диметиламин, монометиламин, моноэтиламин или диэтиламин. Соли также включают обычные формы солей металлов, например, соли, образованные металлами, такими как литий, натрий, калий, магний или кальций. Соль присоединения кислоты, соль присоединения основания или соль металла могут быть получены обычным способом. Фармацевтически приемлемые соли и общие методики их получения хорошо известны в данной области. Смотрите, например, справочник P. Stahl, et al. Handbook of Pharmaceutical Salts: Properties, Selection, and Use, 2nd Revised Edition (Wiley-VCH, 2011), публикацию S.M. Berge, et al., "Pharmaceutical Salts," Journal of Pharmaceutical Sciences, Vol. 66, No. 1, January 1977.
Для конденсации защищенной аминокислоты или пептида могут быть использованы особенно предпочтительные различные активирующие реагенты, пригодные для синтеза пептида, такие как соль трифосфония, соль тетраметилурония, карбодиимид и другие подобные реагенты. Примеры солей трифосфония включают бензотриазол-1-илокситрис(пирролазино)фосфония гексафторфосфат (PyBOP), бромтрис(пирролазино)фосфония гексафторфосфат (PyBroP) и 7-аза-бензотриазол-1-илокситрис(пирролазино)фосфония гексафторфосфат (PyAOP), примерами солей тетраметилурония являются 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат (HBTU), 2-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат (HATU), 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония тетрафторборат (TBTU), 2-(5-норборнан-2,3-дикарбоксиимид)-1,1,3,3-тетраметилурония тетрафторборат (TNTU) и O-(N-сукцимидил)-1,1,3,3-тетраметилурония тетрафторборат (TSTU), и примеры карбодиимидов включают N, N'-дициклогексилкарбодиимид (DCC), N, N'-диизопропилкарбодиимид (DIPCDI) и N-этил-N'-(3-диметиламинопропил)карбодиимида гидрохлорид (EDCI·HCl). Для использования их в реакции конденсации, могут быть добавлены ингибиторы рацемизации [например, N-гидрокси-5-норборнен-2,3-дикарбоновой кислоты имид (HONB), 1-гидроксибензотриазол (HOBt), 1-гидрокси-7-азабензотриазол (HOAt), 3,4-дигидро-3-гидрокси-4-оксо-1,2,3-бензотриазин (HOOBt) и этил 2-циано-2-(гидроксил амино)ацетат (Oxyma), и другие]. Используемый в реакции конденсации растворитель может быть соответствующим образом выбран из растворителей, по поводу которых известно, что они применяются в реакции конденсации пептида. Например, могут быть использованы амиды кислот, такие как безводные или водосодержащие N, N- диметилформамид, N, N-диметилацетамид и N-метилпирролидон и другие амиды кислот; галогенированные углеводороды, такие как метиленхлорид, хлороформ и другие галогенированные углеводороды; спирты, такие как трифторэтанол, фенол и другие спирты, сульфоксиды, такие как диметилсульфоксид и другие сульфоксиды; третичные амины, такие как пиридин и другие третичные амины; простые эфира, такие как диоксан, тетрагидрофуран и другие простые эфиры; нитрилы, такие как ацетонитрил, пропионитрил и другие нитрилы; сложные эфиры, такие как метилацетат, этил ацетат и другие сложные эфиры, и подходящие их смеси. Температуру проведения реакции соответствующим образом выбирают из известных диапазонов температур, используемых для реакции связывания пептида, и обычно ее выбирают в диапазоне приблизительно от -20°C до 90°C. Активированные производные аминокислот обычно используют в 1,5-6-кратном избытке. При проведении твердофазного синтеза, в случае, когда анализ с использованием нингидриновой реакции показывает, что конденсация является недостаточной, достаточная конденсация может быть достигнута путем повторного проведения реакции конденсации без удаления защитной группы. В случае, когда после повторного проведения реакции конденсации, конденсация все еще остается недостаточной, непрореагировавшая аминокислота может быть подвергнута ацетилированию с помощью ангидрида кислоты, ацетилимидазола и других подобных реагентов, для того чтобы избежать ее влияния на протекание последующей реакции.
Примеры защитных групп для аминогруппы исходной аминокислоты включают бензилоксикарбонил (Z), третбутоксикарбонил (Boc), третпентилоксикарбонил, изоборнилоксикарбонил, 4-метокси-бензилоксикарбонил, 2-хлорбензилоксикарбонил (Cl-Z), 2-бром-бензилоксикарбонил (Br-Z), адамантилоксикарбонил, трифторацетил, фталоил, формил, 2-нитрофенилсульфенил, дифенилфосфинотиоил, 9-флуоренилметилоксикарбонил (Fmoc), тритил и другие подобные защитные группы.
Примеры защитной группы для карбоксильной группы исходной аминокислоты включают, помимо вышеперечисленных групп, C1-6 алкильную группу, C3-10 циклоалкильную группу и C7-14 аралкильную группу, арил, 2-адамантил, 4-нитробензил, 4-метоксибензил, 4-хлорбензил, фенацил, бензилоксикарбонилгидразид, третбутоксикарбонилгидразид, тритилгидразид и другие подобные защитные группы.
Гидроксильная группа серина или треонина может быть защищена, например, путем проведения реакции образования сложного эфира или простого эфира. Примеры групп, подходящих для проведения реакции образования сложных эфиров включают низшие (C2-4) алканоильные группы, такие как ацетильные группы; ароильные группы, такие как бензоильные группы; и группы, образованные из органических кислот, и другие подобные группы. Кроме того, примеры групп, подходящих для проведения реакции образования простых эфиров включают бензил, тетрагидропиранил, третбутил (But), тритил (Trt) и другие подобные группы.
Примеры защитных групп для фенольной гидроксильной группы в тирозине включают Bzl, 2,6-дихлорбензил, 2-нитробензил, Br-Z, третбутил и другие подобные группы.
Примеры защитных групп для имидазола в гистидине включают п-толуолсульфонил (Tos), 4-метокси-2,3,6-триметилбензолсульфонил (Mtr), динитрофенил (DNP), бензилоксиметил (Bom), третбутоксиметил (Bum), Boc, Trt, Fmoc и другие подобные группы.
Примеры защитных групп для гуанидиновой группы в аргинине включают Tos, Z, 4-метокси-2,3,6-триметилбензолсульфонил (Mtr), п-метоксибензолсульфонил (MBS), 2,2,5,7,8-пентаметилхроман-6-сульфонил (Pmc), мезитилен-2-сульфонил (Mts), 2,2,4,6,7-пента-метилдигидробензофуран-5-сульфонил (Pbf), Boc, Z, NO2 и другие подобные группы.
Примеры защитных групп для аминогруппы боковой цепи в лизине включают Z, Cl-Z, трифторацетил, Boc, Fmoc, Trt, Mtr, 4,4-диметил-2,6-диоксоциклогексилиденил (Dde) и другие подобные группы.
Примеры защитных групп для индолила в триптофане включают формил (For), Z, Boc, Mts, Mtr и другие подобные группы.
Примеры защитных групп для аспарагина и глутамина включают Trt, ксантил (Xan), 4,4'-диметоксибензгидрил (Mbh), 2,4,6-триметоксибензил (Tmob) и другие подобные группы.
Примеры активированных карбоксильных групп в исходном веществе включают соответствующий ангидрид кислоты, азид, активные сложные эфиры [эфиры со спиртами (такие как пентахлорфенол, 2,4,5-трихлорфенол, 2,4-динитрофенол, цианометиловый спирт, паранитрофенол, HONB, N-гидроксисукцинимид, 1-гидрокси-бензотриазол (HOBt), 1-гидрокси-7-азабензотриазол (HOAt))] и другие подобные группы. Примеры активированных аминогрупп в исходном веществе включают соответствующие амиды фосфора.
Примеры методов удаления (расщепления) защитных групп включают каталитическое восстановление в токе водорода в присутствии катализатора, такого как Pd-чернь или Pd-уголь; кислотную обработку с помощью безводного фтористого водорода, метансульфоновой кислоты, трифторметансульфоновой кислоты, трифторуксусной кислоты (TFA), триметилсилилбромида (TMSBr), триметилсилилтрифторметансульфоната, тетрафторборной кислоты, трис(трифтор)борной кислоты, трибромида бора или их смешанных растворов; обработку основанием с помощью диизопропилэтиламина, триэтиламина, пиперидина, пиперазина и других подобных оснований; и восстановление натрием в жидком аммиаке и другие подобные методы. Описанную выше реакцию удаления с помощью кислоты обычно проводят при температуре от -20°С до 40°С; и реакцию кислотной обработки эффективно проводят путем добавления анизола, фенола, тиоанизола, метакрезола и паракрезола, и акцептора катионов, такого как диметилсульфид, 1,4-бутандитиол, 1,2-этандитиол, триизопропил-силан и другие подобные акцепторы катионов. Кроме того, 2,4-динитрофенильную группу, используемую в качестве защитной группы имидазола в гистидине, удаляют обработкой тиофенолом; формильную группу, используемая в качестве защитной группы индола в триптофане, удаляют путем снятия защиты не только кислотной обработкой в присутствии 1,2-этандитиола, 1,4-бутандитиола или других подобных соединений, но также щелочной обработкой с помощью разбавленного раствора гидроксида натрия, разбавленного раствора аммиака и других подобных щелочных растворов.
Защита функциональной группы, которая не должна участвовать в реакции исходного вещества, с помощью защитной группы, удаление защитной группы, активация функциональной группы, участвующей в реакции, и другие проводимые подобные операции, могут быть соответствующим образом выбраны из известных защитных групп и известных методов.
В методе получения амида пептида, его получают путем твердофазного синтеза с использованием смолы для синтеза амида или путем амидирования α-карбоксильной группы концевой карбоксильной группы аминокислоты, и цепь пептида удлиняют до требуемой длины в направлении к аминогруппе, после чего получают пептид, в котором удалена защитная группа для N-концевой α-аминогруппы только пептидной цепи, и пептид, содержащий только защитную группу для С-концевой карбоксильной группы, удаленной из пептидной цепи, и эти два пептида конденсируют в описанном выше смешанном растворителе. Более подробное описание реакции конденсации соответствует уже приведенному выше описанию. После очистки защищенного пептида, полученного путем конденсации, все защитные группы могут быть удалены описанным выше методом с получением требуемого неочищенного пептида. Требуемый амид пептида может быть получен путем очистки этого неочищенного пептида с использованием различных общеизвестных методов очистки и лиофилизации основной фракции.
В одном варианте осуществления, пептид может находиться в форме его сольвата. Термин "сольват" означает, что пептид или его соль образуют комплекс с молекулой растворителя.
Термин "пародонтоз" относится к воспалительному заболеванию, которое возникает в тканях, таких как десна, периодонтальная связка, и альвеолярная кость вокруг зуба, которая фиксирует зуб. Пародонтоз относится к заболеванию, при котором бактерии инфицируют карман между десной и зубами и повреждают периодонтальную связку и прилегающие ткани, и по степени тяжести заболевания пародонтоз подразделяют на гингивит и пародонтит. Известно, что по мере прогрессирования воспаления, происходит все в большей степени повреждение ткани, формируется периодонтальный карман, и, в случае тяжелой формы пародонтита, периодонтальный карман углубляется, вследствие чего воспаляется периодонтальная связка и, в результате, происходит потеря костной массы. Поскольку основное лечение такого пародонтоза заключается в восстановлении поврежденной периодонтальной связки соединительной ткани, цементного вещества корня зуба и альвеолярной кости, то для этого необходимо регенерировать не только периодонтальную связку, поддерживающую альвеолярную кость, но и альвеолярную кость и цементное вещество корня зуба, к которым периодонтальная связка может быть присоединена.
Применительно к фармацевтической композиции, пародонтоз может представлять собой воспалительное заболевание пародонта.
Применительно к фармацевтической композиции, пародонтоз может представлять собой гингивит или периодонтит.
В одном варианте осуществления, фармацевтическая композиция может дополнительно включать лекарственное средство для лечения пародонтоза.
Лекарственное средство для лечения пародонтоза может присутствовать отдельно от пептида или может находиться в форме, в которой образуется комплекс с пептидом путем связывания с N-концом или C-концом пептида.
"Травматический вывих" относится к травме, при которой на зуб или пародонт воздействует травмирующая сила, и в зубе и пародонте происходят различные разрушения в зависимости от направления и величины травмирующей силы, и повреждается периодонтальная связка, в том числе разрушения, которые подразделяются на ударный подвывих, орбитальный вывих, латеральный вывих, полный вывих и интрузию. Поэтому основное лечение вывихов требует также регенерации поврежденной периодонтальной связки. В частности, успех реплантации полностью вывихнутого зуба зависит от регенерации периодонтальной связки, прикрепленной к полностью вывихнутому зубу, или периодонтальной связки, остающейся в альвеолярной ямке, в которой отсутствует зуб. В случае, когда не происходит регенерации периодонтальной связки, происходит рассасывание цементирующего вещества и твердой ткани корня зуба, и возникает анкилоз, при котором этот участок замещается альвеолярной костью.
"Реплантация зуба" является методом повторной трансплантации зуба в постэкстракционную лунку после преднамеренного удаления зуба или после проведения или до проведения соответствующего лечения корневых каналов. Преднамеренная реплантация может быть проведена в ситуациях, когда лечение корневых каналов не привело к положительному результату, когда существуют анатомические ограничения, сложность с доступностью, зубы вывихнуты в результате несчастного случая, или когда требуется быстрое преднамеренное ортодонтическое прорезывание зуба.
"Предотвращение" относится к любому действию, которое подавляет или задерживает возникновение пародонтоза или травматического вывиха зуба, путем введения композиции.
"Лечение" относится к любому действию, при котором улучшаются симптомы пародонтоза или травматического вывиха зуба или при котором достигается лечебный эффект, путем введения композиции.
Фармацевтическая композиция может быть приготовлена в форме фармацевтической композиции для лечения пародонтоза, дополнительно включающей соответствующий носитель (носитель природного или неприродного происхождения), вспомогательное вещество или разбавитель, обычно используемый при приготовлении фармацевтических композиций пептида. Фармацевтическая композиция может быть приготовлена и использована в форме стерильного инъекционного раствора, который соответственно может быть введен в пораженную пародонтозом область традиционным методом.
В настоящем изобретении, носители, вспомогательные вещества и разбавители, которые могут быть введены в фармацевтическую композицию, включают лактозу, декстрозу, сахарозу, сорбит, маннит, ксилит, эритрит, мальтит, крахмал, аравийскую камедь, альгинат, желатин, фосфат кальция, силикат кальция, целлюлозу, метилцеллюлозу, микрокристаллическую целлюлозу, поливинил-пирролидон, воду, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния, минеральное масло, коллаген и другие подобные вещества. В случае лекарственной формы, ее можно приготовить с использованием обычно используемых разбавителей или вспомогательных веществ, таких как наполнители, сухие разбавители, связующие вещества, смачивающие вещества, разрыхлители и поверхностно-активные вещества. В частности, лекарственная форма может представлять собой стерильные водные растворы, неводные растворы, суспензии, эмульсии, лиофилизированные препараты, суппозитории и мази (например, мерную тубу и так далее) и другие подобные формы. В качестве неводного растворителя и суспендирующего средства могут быть использованы пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, инъецируемые сложные эфиры, такие как этилолеат, и другие подобные вещества. В качестве основы для суппозиторий могут быть использованы витепсол, макрогол, твин 61, масло какао, лауриновое масло, глицерогератин и другие подобные вещества.
На содержание пептида или его фармацевтически приемлемой соли в фармацевтической композиции по настоящему изобретению не накладывают конкретного ограничения, но его содержание может составлять от 0,0001 до 50 масс.%, или от 0,01 до 20 масс.%, в расчете на суммарную массу готовой композиции.
Фармацевтическая композиция может быть введена в фармацевтически эффективном количестве, и термин "фармацевтически эффективное количество" обозначает количество, которое является достаточным для лечения или предотвращения заболевания при обоснованном соотношении польза/риск, применяемом при терапевтическом лечении или при предотвращении заболевания, и эффективный уровень дозы может быть определен с учетом тяжести заболевания, активности лекарственного средства, возраста, массы тела, состояния здоровья, пола пациента, восприимчивости пациента к воздействию лекарственных средств, времени введения, способа введения и продолжительности лечения, скорости выведения используемой композиции по изобретению, факторов, включающих лекарственные средства, используемые в комбинации или параллельно с используемыми композициями по изобретению, и другие факторов, хорошо известных в области медицины. Фармацевтическая композиция по настоящему изобретению может быть введена отдельно или в комбинации с известными фармацевтическими композициями для лечения пародонтоза. Учитывая все упомянутые выше факторы, важно, чтобы для достижения максимального эффекта без проявления побочных эффектов можно было бы вводить минимальное количество лекарственного средства.
Дозирование фармацевтической композиции может быть определено специалистами в данной области с учетом цели ее применения, тяжести заболевания, возраста, массы тела, пола, анамнеза пациента или типа вещества, используемого в качестве действующего компонента. Например, фармацевтическая композиция по настоящему изобретению может быть введена в дозе от приблизительно 0,1 нг до приблизительно 100 мг/кг, предпочтительно, от 1 нг до 10 мг/кг, в случае введения взрослому человеку, и на частоту дозирования композиции не накладывают конкретных ограничений, но она может быть введена один раз в день или в несколько приемов дробными дозами. Упомянутые выше дозы никоим образом не ограничивают объем изобретения.
В другом аспекте настоящего изобретения, для решения упомянутой выше технической задачи предлагается композиция для регенерации пародонта, включающая пептид, содержащий аминокислотную последовательность следующей общей формулы 1:
K-Y-K-Q-X5-X6-X7-X8-Y-K (общая формула 1)
где в общей формуле 1,
от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K);
X8 представляет собой аспарагин (N) или серин (S).
В одном варианте осуществления, пептид включает аминокислотную последовательность, представляющую собой любую одну из последовательностей SEQ ID NOs: 1-16.
В другом варианте осуществления, пептид состоит в основном из аминокислотной последовательности, представляющей собой любую одну из последовательностей SEQ ID NOs: 1-16, или пептид состоит из аминокислотной последовательности, представляющей собой любую одну из последовательностей SEQ ID NOs: 1-16.
Описание пептида является таким же, как приведенное выше.
"Пародонт" представляет собой сложный орган, состоящий из эпителиальной ткани, соединительной ткани (мягкой ткани) и обызвествленной соединительной ткани, и структурно пародонт состоит из десны, периодонтальной связки (PDL), цементного вещества корня зуба и альвеолярной кости.
"Периодонтальная связка (PDL)", также называемая пародонтом, относится к фиброзной мембране соединительной ткани, которая соединяет цементное вещество корня зуба и стенку альвеолярной кости у млекопитающих. Периодонтальная связка состоит из основного волокна, коллагенового волокна, идущего параллельно или наискосок к длинной оси зуба, и пучка волокон Шарпея, оба конца которых постоянно погружены в твердую ткань, а зуб эластично прикреплен к альвеолярной кости через периодонтальную связку. Периодонтальная связка не только смягчает давление, возникающее при пережевывании пищи, но также имеет большое количество кровеносных сосудов и нервов и, известно, что она принимает участие в процессе приема пищи и восприятия ощущений. Периодонтальная связка содержит различные клетки, такие как фибробласты, недифференцированные мезенхимальные клетки и эпителиальные клетки, среди которых фибробласты периодонтальной связки могут дифференцироваться в остеобласты или цементобласты при соответствующей стимуляции, но механизм дифференцировки фибробластов периодонтальной связки в цементобласты и активирующие дифференцировку белки неизвестны. Сиалопротеин кости (BSP), остеокальцин (OC), CAP (белок адгезии цементного вещества зуба) и другие подобные белки известны как маркеры дифференцировки цементобластов, в частности известно, что CAP играет важную роль в прикреплении волокон периодонтальной связки к цементному веществу зуба.
"Цементное вещество корня зуба" представляет собой обызвествленную ткань, покрывающую корень зубов у млекопитающих. Цементное вещество прикрепляет зуб к альвеолярной кости путем обездвиживания периодонтальной связки. Поэтому, при заражении десны бактериями, цементное вещество, окружающее зуб, дегенерирует, и пучок волокон периодонтальной связки, соединяющий зуб и альвеолярную кость, не может прикрепиться к дегенерированному цементному веществу, что вызывает раскачивания зуба. Для лечения такого дегенерированного цементного вещества необходимо образование нового цементного вещества.
"Альвеолярная кость" является частью верхней и нижней челюсти, которая окружают корень зуба и поддерживает зуб, и которая развивается по мере формирования или прорезывания зубов и постепенно рассасывается при потере зубов. Фиксируя периодонтальную связку вместе с цементным веществом корня зуба, альвеолярная кость играет важную роль в окклюзивном давлении, таком как давление при пережевывании, а также в распределении и поглощении давления на зуб в процессе произношения слов и глотания.
"Фибробласты периодонтальной связки" вместе с фибробластами десны являются основной клеточной составляющей соединительной ткани (мягких тканей) пародонта. Фибробласты периодонтальной связки не только образует периодонтальную связку в качестве своей уникальной функции, но также участвует в репарации и регенерации прилегающей альвеолярной кости и цементирующего вещества in vivo, но не известно вещество, которое могло бы активировать протекание этих процессов, и фибробласты периодонтальной связки отличается от фибробластов десны, которые участвуют в поддержании соединительной ткани десны. Фибробласты периодонтальной связки могут дифференцироваться в остеобласты или цементобласты при соответствующей стимуляции, но механизм дифференцировки фибробластов периодонтальной связки в цементобласты точно неизвестен. Сиалопротеин кости (BSP), остеокальцин (OC) и другие подобные белки известны в качестве маркеров дифференцировки остеобластов и цементобластов, а CAP (белок адгезии цементного вещества корня зуба) известен в качестве гена, играющего важную роль в прикреплении волокон периодонтальной связки к цементному веществу корня зуба. Ген периостина также известен в качестве маркера периодонтальной связки. Согласно ряду недавних исследований, периостин играет важную роль в регенерации периодонтальной связки и альвеолярной кости после хирургического вмешательства на пародонте, стимулируя выработку коллагеновых волокон и миграцию фибробластов и остеобластов, являющихся важными регуляторами формирования пародонта.
"Регенерация" может относиться к любому действию, при котором утраченные или поврежденные клетки или ткани восстанавливаются или восполняются. Регенерация может быть обусловлена дифференцировкой клеток.
Было подтверждено, что пептид обладает эффектом активирования дифференцировки фибробластов периодонтальной связки в цементобласты.
Композиция для регенерации пародонта может активировать регенерацию любой одной или более из тканей десны, периодонтальной связки, цементного вещества корня зуба и альвеолярной кости.
Композиция для регенерации пародонта может представлять собой фармацевтическую композицию.
Фармацевтическая композиция представляет собой фармацевтическую композицию, описанную выше.
Композиция для регенерации пародонта может представлять собой лечебно-профилактическую косметическую композицию. Лечебно-профилактическая косметическая композиция может представлять собой лечебно-профилактическую косметическую композицию для предотвращения или улучшения состояния пародонтоза или травматического вывиха зуба.
Термин "улучшение" относится к любому действию по уменьшению, по меньшей мере, степени показателя, например, симптома, связанного с подвергаемым лечению состоянием.
Улучшение можно интерпретировать как действие, которое активизирует регенерацию пародонта путем введения фармацевтической композиции, содержащей пептид в качестве действующего компонента, индивидууму, нуждающемуся в лечении пародонтоза, вследствие чего улучшаются симптомы пародонтоза или травматического вывиха зуба или достигается положительный эффект.
Термин "лечебно-профилактическое косметическое средство" относится к препаратам, действие которых является более мягким, чем действие лекарственных препаратов, из числа препаратов, применяемых для диагностики, лечения, улучшения, облегчения, лечения или предупреждения заболевания у человека или животного, например, с помощью методов фармацевтики; лечебно-профилактическое косметическое средство представляет собой вещество, не являющееся веществом, используемым в фармацевтике, и включает волокнистое/похожее на каучук вещество, используемое для лечения или профилактики заболеваний людей/животных, вещество, подобное веществу, которое оказывает незначительное или не оказывает прямого действия на организм человека и не является механизмом или устройством и бактерицидным/пестицидным средством для предотвращения инфекционных заболеваний.
На тип или форму лечебно-профилактической косметической композиции, включающей пептид, не накладывают конкретных ограничений, но, в качестве примера, она может представлять собой препарат для дезинфекции полости рта, препарат для очистки полости рта, зубную пасту, нить для чистки промежутков между зубами, мазь для полости рта и другие подобные формы.
Композиция для регенерации пародонта может представлять собой полезную для здоровья функциональную пищевую композицию. Полезная для здоровья функциональная пищевая композиция может представлять собой полезную для здоровья функциональную пищевую композицию для предотвращения или улучшения состояния пародонтоза или травматического вывиха зуба.
"Пища" в соответствии с настоящим изобретением включает молочные продукты, а также мясо, колбасу, хлеб, шоколад, конфеты, легкие закуски, кондитерские изделия, пиццу, рами, другие макаронные изделия, жевательную резинку, мороженое, различные супы, напитки, чаи, алкогольные напитки, угощения, витаминные комплексы, полезные для здоровья функциональные пищевые продукты и продукты для здорового питания и другие подобные продукты, и включает все пищевые продукты в общепринятом смысле.
Упомянутая выше полезная для здоровья функциональная пища определяется одним и тем же термином, что и пища, предназначенная специально для здорового питания (FoSHU), и обозначает пищевой продукт с высоким лечебно-оздоровительным эффектом, который подвергнут обработке таким образом, что помимо снабжения питательными веществами он эффективно проявляет биорегуляторные функции. Используемый в изобретении термин "функция (функциональность)" означает регулирование содержания питательных веществ, необходимых для структуры и функции человеческого организма, или достижение полезного эффекта для здоровья, такого как физиологический эффект.
Пищевой продукт по настоящему изобретению может быть получен способом, обычно используемым в данной области, и при таком способе получения могут быть добавлены сырье и компоненты, обычно добавляемые при промышленном производстве. Пищевой продукт может быть также приготовлен в форме, на которую не накладывают конкретных ограничений, при условии, что эту форму признают пищевым продуктом. Композиция пищевого продукта по настоящему изобретению может быть приготовлена в различных лекарственных формах, которые имеют преимущество, так как, в отличие от обычных лекарственных средств, в качестве сырья используется пищевой продукт, и они не вызывают побочных эффектов и других подобных нежелательных явлений, которые могут возникать при длительном приеме лекарственных средств, и они характеризуются в качестве отличных носителей, и пищевой продукт по данному изобретению может быть также использован для приема внутрь в качестве адъюванта для усиления эффекта предотвращения или улучшения состояния пародонтоза или травматического вывиха зуба.
Термин "полезная для здоровья функциональная пища" относится к пищевому продукту, обладающему эффектом по поддержанию здоровья и укрепляющим действием по сравнению с обычным продуктом, а биологически активная пищевая добавка относится к пищевому продукту, предназначенному для использования в качестве пищевой добавки. В некоторых случаях термины "полезная для здоровья функциональная пища", "продукт лечебного питания" и "биологически активная пищевая добавка" могут использоваться как синонимы.
В частности, упомянутая выше полезная для здоровья функциональная пища обозначает пищевой продукт, приготовленный путем добавления пептида к пищевому материалу, такому как напиток, чай, ароматизатор, жевательная резинка и кондитерское изделие, или путем инкапсулирования, измельчения, суспендирования и другим подобным методом, который оказывает определенное воздействие на здоровье при приеме внутрь, но имеет то преимущество, что не оказывает какого-либо нежелательного воздействия, которое могло бы возникать при длительном введении лекарственного средства, в котором используется пищевой продукт в качестве сырья, в отличие от обычных лекарственных средств.
Так как пищевую композицию по настоящему изобретению можно употреблять ежедневно, то можно ожидать достижения высокого положительного эффекта по предотвращению или улучшению состояния пародонтоза или травматического вывиха зуба, и, в силу этого, эта пищевая композиция может быть использована с очень высокой эффективностью.
Пищевая композиция может дополнительно включать физиологически приемлемый носитель, и на тип носителя не накладывают конкретного ограничения, и может быть использован любой носитель, широко применяемый в данной области.
Кроме того, пищевая композиция может включать дополнительные компоненты, которые обычно используют в пищевых композициях для улучшения запаха, вкуса, внешнего вида и других характеристик. Например, могут быть добавлены витамины A, C, D, E, B1, B2, B6, B12, ниацин, биотин, фолат, пантотеновая кислота и другие подобные компоненты. Пищевая композиция может также включать такие микроэлементы, как цинк (Zn), железо (Fe), кальций (Ca), хром (Cr), магний (Mg), марганец (Mn) и медь (Cu). Она может также содержать аминокислоты, такие, как лизин, триптофан, цистеин, валин и другие подобные аминокислоты.
Кроме того, пищевая композиция может содержать пищевые добавки, такие как антисептики (сорбат калия, бензоат натрия, салициловая кислота, дегидрохолат натрия и другие подобные антисептики), бактерициды (гипохлорит кальция, отбеливатель, гипохлорит натрия и другие подобные бактерициды), антиоксиданты (бутилгидроксианизол (BHA), бутилгидрокситолуол (BHT) и другие подобные антиоксиданты), окрашивающие вещества (окрашивающее вещество на основе смолы и другие подобные окрашивающие вещества), цветообразующие вещества (нитрит натрия, основная уксуснокислая соль натрия и другие подобные цветообразующие вещества), отбеливатели (сульфит натрия), простые вкусовые вещества (глутамат натрия и другие подобные вкусовые вещества), подсластители (дульцин, цикламат, сахарин и другие подобные подсластители), отдушки (ванилин, лактоны и другие подобные отдушки), расширяющие добавки (квасцы, D-тартрат калия и другие подобные вещества), упрочняющие вещества, эмульгаторы, загустители (декстрины), покрывные вещества, экранирующие средства, ингибиторы пенообразования, растворители и кондиционеры. Добавки выбираются в зависимости от типа пищи и могут быть использованы в соответствующем количестве.
Пептид может быть добавлен в чистом виде или использован в сочетании с другими пищевыми продуктами или компонентами пищевых продуктов, и они могут быть соответствующим образом использованы обычным методом. Смешиваемое количество действующего компонента может быть определено соответствующим образом в соответствии с целью его применения (профилактика, поддержание здоровья или терапевтическое лечение). Как правило, при производстве пищевого продукта или напитка, пищевая композиция по настоящему изобретению может быть добавлена в количестве 50 частей по массе или менее, 20 частей по массе или менее, 10 частей по массе или менее, 5 частей по массе или менее, 1 части по массе или менее или 0,1 части по массе или менее. Однако при приеме внутрь в течение длительного периода времени с целью поддержания здоровья и гигиены, содержание может находиться в пределах указанного выше диапазона, и, поскольку нет проблем с точки зрения безопасности, то действующий компонент также может использоваться в количестве, превышающем указанный выше диапазон.
Одним из примеров пищевой композиции может являться композиция напитка для поддержания здоровья, и в этом случае она может содержать в качестве дополнительных компонентов различные ароматизаторы, натуральные углеводы и другие подобные компоненты, такие как в обычных напитках. Упомянутые выше природные углеводы могут представлять собой моносахариды, такие как глюкоза и фруктоза; дисахариды, такие как мальтоза и сахароза; полисахариды, такие как декстрин и циклодекстрин; сахарные спирты, такие как ксилит, сорбит, эритрит, и другие подобные углеводы. В качестве подсластителя могут быть использованы натуральные подсластители, такие как тауматин и экстракт стевии; синтетические подсластители, такие как сахарин, аспартам, и другие подобные подсластители. Доля натуральных углеводов обычно может составлять от около 0,01 до 0,04 г, в частности, от около 0,02 до 0,03 г, на 100 мл композиции напитка для поддержания здоровья по настоящему изобретению
В дополнение к описанному выше, композиция напитка для поддержания здоровья может содержать различные питательные вещества, витамины, электролиты, ароматизаторы, окрашивающие вещества, пектиновую кислоту, соли пектиновой кислоты, альгиновую кислоту, соли альгиновой кислоты, органические кислоты, защитные коллоидные загустители, регуляторы рН, стабилизаторы, антисептики, глицерин, спирты, газирующие вещества и другие подобные вещества. Композиции напитка могут также содержать мякоть для производства натуральных фруктовых соков, напитков из фруктовых соков или напитков из овощей. Эти компоненты могут быть использованы независимо или в комбинации. Доля таких добавок не имеет решающего значения, но обычно ее выбирают в диапазоне от 0,01 до 0,1 части по массе на 100 частей по массе композиции напитка для поддержания здоровья по изобретению.
Пищевая композиция может иметь различные процентные содержания пептида при условии, что при этом проявляется эффект предотвращения или улучшения состояния пародонтоза или травматического вывиха зуба, но конкретно, пищевая композиция может содержать от 0,00001 до 100 масс.% или от 0,01 до 80 масс.% пептида по настоящему изобретению, в расчете на суммарную массу пищевой композиции, но указанные содержания пептида не являются ограничениями.
В другом аспекте настоящего изобретения, для решения упомянутой выше технической задачи предлагается композиция для активизации экспрессии любого одного или более генов сиалопротеина кости (BSP), белка-1 дентинного матрикса (DMP1), белка адгезии цементного вещество корня зуба (CAP), коллагена III (COL3) и периостина, включающая пептид, состоящий из аминокислотной последовательности следующей общей формулы 1:
K-Y-K-Q-X5-X6-X7-X8-Y-K (общая формула 1)
где в общей формуле 1,
от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K);
X8 представляет собой аспарагин (N) или серин (S).
В одном варианте осуществления, пептид включает аминокислотную последовательность, являющуюся любой одной из последовательностей SEQ ID NOs: 1-16.
В другом варианте осуществления, пептид состоит в основном из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16, или пептид состоит из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16.
Описание пептида является таким же, как приведенное выше.
Было подтверждено, что пептид увеличивает экспрессию BSP, DMP1 и CAP, которые являются маркерными генами для дифференцировки остеобластов и цементобластов, и увеличивает экспрессию периостина и COL3, которые являются маркерными генами для дифференцировки периодонтальной связки в клетках периодонтальной связки человека. Кроме того, было подтверждено, что пептид увеличивает экспрессию BSP и DMP1, маркерных генов дифференцировки остеобластов и цементобластов в мезенхимальных стволовых клетках человека
В еще одном аспекте настоящего изобретения, для решения упомянутой выше технической задачи предлагается способ лечения пародонтоза или травматического вывиха зуба у индивидуума, где способ включает введение эффективного количества пептида или его фармацевтически приемлемой соли индивидууму, нуждающемуся в лечение пародонтоза или травматического вывиха зуба.
"Индивидуум" обозначает субъекта, нуждающегося в лечении заболевания, и более конкретно, млекопитающих, таких как человек или низшие приматы, мыши, крысы, собаки, кошки, лошади и крупный рогатый скот.
"Эффективное количество" относится к количеству или дозе пептида или его фармацевтически приемлемой соли, которые при введении пациенту в форме разовой дозы или форме многократных доз обеспечивают требуемый эффект у пациента, которому проводят диагностирование или лечение. Эффективное количество может быть легко определено обычным лечащим врачом с использованием известных методик или путем анализа результатов наблюдения, полученных при аналогичных обстоятельствах. При определении эффективного количества пептида для пациента, лечащий врач учитывает ряд факторов, включая, но этим не ограничивая, вид, размер, возраст и общее состояние здоровья млекопитающего, конкретное заболевание или расстройство, степень развития или тяжести заболевания или расстройства, индивидуальная ответная реакция пациента на проводимое лечение, конкретное вводимое соединение, способ введения, биодоступность вводимого средства, выбранный режим дозирования, использование сопутствующих лекарственных препаратов и другие относящиеся к процессу лечения обстоятельства.
Под "введением" подразумевают введение вещества пациенту любым подходящим способом. Способ введения может представлять собой любой общий способ, который позволяет достигать мишени в организме пациента. Введение включает, но этим не ограничивая, например, интраперитонеальное введение, внутривенное введение, внутримышечное введение, подкожное введение, интрадермальное введение, пероральное введение, местное введение, интраназальное введение и интраректальное введение.
Лечение пародонтоза или травматического вывиха зуба включает, но этим не ограничивая, регенерацию пародонта.
В способе, эффективное количество пептида или его фармацевтически приемлемой соли может быть введено одновременно, раздельно или последовательно с эффективным количеством одного или более других действующих компонентов. Один или более других действующих компонентов включают, но этим не ограничивая, один или более других лекарственных средств для лечения пародонтоза или травматического вывиха зуба.
В еще одном аспекте настоящего изобретения, для решения упомянутой выше технической задачи предлагается применение пептида или его фармацевтически приемлемой соли в производстве лекарственного препарата для предотвращения или лечения пародонтоза или травматического вывиха зуба.
Все приведенные в настоящем изобретении численные значения могут включать в себя смысловую характеристику "приблизительно". "Приблизительно" представляет собой диапазон, включающий ±0,5, ±0,4, ±0,3, ±0,2, ±0,1 и другие подобные значения, и включает, но этим не ограничивая, все значения в диапазоне, эквивалентном или аналогичном значению, которое следует в тексте за термином "приблизительно".
Следует иметь в виду, что каждое описание и вариант осуществления, раскрытые в настоящем изобретении, могут быть также применимы к другим описаниям и вариантам осуществления. То есть все комбинации различных элементов, раскрытых в изобретении, входят в объем настоящего изобретения. Кроме того, следует иметь в виду, что объем настоящего изобретения никоим образом не ограничивается приведенными ниже конкретными описаниями.
Эффекты изобретения
Фармацевтическая композиция для предотвращения или лечения пародонтоза или травматического вывиха зуба по настоящему изобретению активизирует регенерацию пародонта, в том числе периодонтальной связки, альвеолярной кости и цементного вещества корня зуба, и адгезию периодонтальной связки, вследствие чего композиция может быть также использована для восстановления повреждения соединительной ткани, такого как пародонтоз и травматический вывих зуба. Соответственно, пептид может быть использован различными способами в форме фармацевтических композиций, лечебно-профилактических косметических композиций, полезных для здоровья функциональных пищевых композиций и в других подобных формах.
Эффекты настоящего изобретения не ограничиваются теми эффектами, которые были упомянуты выше, и, после ознакомления с приведенным далее описанием, для специалистов в данной области станет очевидным наличие и других не упомянутых выше эффектов.
Описание чертежей
На фигуре 1 в графическом виде представлены данные по воздействию пептидов группы 1 и группы 2, приготовленных в примере 1, на экспрессию сиалопротеина кости (BSP), белка-1 дентинного матрикса (DMP1) и CAP (белка адгезии цементного вещества корня зуба), которые являются маркерными генами для дифференцировки остеобластов и цементобластов в клетках периодонтальной связки человека (hPDL).
На фигуре 2 в графическом виде представлены данные по воздействию пептидов группы 1 и группы 2, приготовленных в примере 1, на экспрессию сиалопротеина кости (BSP) и белка-1 дентинного матрикса (DMP1), которые являются маркерными генами для дифференцировки остеобластов в мезенхимальных стволовых клетках человека (hBMSCs).
На фигуре 3 в графическом виде представлены данные по воздействию пептидов группы 1 и группы 2, приготовленных в примере 1, на экспрессию гена коллагеновых волокон типа 3 (COL3) и гена периостина, которые являются маркерными генами периодонтальной связки, в клетках периодонтальной связки человека.
На фигуре 4 представлены фотографии ткани, окрашенной с помощью красителя гематоксилин/эозин, через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта и приведены результаты подтверждения воздействия пептида на регенерацию альвеолярной кости. A представляет положительный контроль (PC); B представляет отрицательный контроль (NC) без проведения какого-либо лечения после повреждения пародонта; C представляет отрицательный контроль (NC+Plug) с трансплантацией коллагеновой губки только после повреждения пародонта; D представляет экспериментальную группу, подвергаемую лечению с помощью пептида (SEQ ID NO: 16) группы 2; AB обозначает альвеолярную кость; De обозначает дентин зуба.
На фигуре 5 приведены результаты подтверждения воздействия пептида на регенерацию ткани периодонтальной связки путем окрашивания с помощью красителя гематоксилин/эозин через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта. A-D представляют отрицательный контроль (NC) без проведения какого-либо лечения; E-H представляют отрицательный контроль (NC+Plug) только с трансплантацией коллагеновой губки, и I-L представляет экспериментальную группу, подвергаемую лечению с помощью пептида (SEQ ID NO: 16) группы 2. AB обозначает альвеолярную кость; De обозначает дентин зуба; CE обозначает цементное вещество корня зуба; CT обозначает соединительную ткань; NPD относится к вновь образовавшейся ткани, подобной периодонтальной связке; и NCE обозначает вновь образовавшуюся ткань, подобную цементному веществу корня зуба. Размер масштабных полосок, A, E, I, M 500 мкм. B, F, J, N, 200 мкм. C, G, K, O, 100 мкм. D, H, L, P, 50 мкм.
На фигуре 6 приведены результаты подтверждения воздействия пептида на регенерацию ткани периодонтальной связки с помощью метода окрашивания коллагена (окраска трихром по Массону) через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта. A-B представляют отрицательный контроль (NC) без проведения какого-либо лечения; C-D представляют отрицательный контроль (NC+Plug) только с трансплантацией коллагеновой губки; и E-F представляет экспериментальную группу, подвергаемую лечению с помощью пептида (SEQ ID NO: 16) группы 2. AB обозначает альвеолярную кость; De обозначает дентин зуба; CE обозначает цементное вещество корня зуба; CT обозначает соединительную ткань; NPD относится к вновь образовавшейся ткани, подобной периодонтальной связке; NCE обозначает вновь образовавшуюся ткань, подобную цементному веществу корня зуба. Размер масштабных полосок, A, C, E, G 100 мкм. B, D, F, H, 50 мкм.
Варианты осуществления изобретения
Далее настоящее изобретение будет подробно описано с помощью примеров. Однако эти примеры приведены с целью иллюстрации настоящего изобретения, и они никоим образом не ограничивают объем настоящего изобретения.
Пример 1. Синтез пептидов
Было синтезировано 16 пептидов, состоящих из аминокислотных последовательностей, представленных в таблице 1, соответственно. В данном случае, пептид, в котором восьмая аминокислота является аспарагином (N), относили к группе 1, а пептид, в котором восьмая аминокислота является серином (S), относили к группе 2.
Таблица 1
1. Экспериментальный материал и метод. Культивирование клеток
Клетки hBMSCs культивировали в условиях увлажненного воздуха при 37°C при содержании 5% CO2 и использовали их в эксперименте. Мезенхимальные стволовые клетки человека (hBMSCs) приобретали у фирмы Lonza (LONZA, Switzerland) и использовали их в эксперименте. Клетки hBMSCs культивировали в среде α-MEM (Invitrogen), дополненной 10% термоинактивированной бычьей сывороткой.
2. Выделение и культивирование клеток периодонтальной связки человека
Клетки периодонтальной связки человека (клетки hPDL) выделяли из тканей периодонтальной связки из зубов мудрости 10 взрослых людей (в возрасте 18-22 года) в стоматологической больнице Сеульского национального университета. Конкретно, все эксперименты проводили с согласия пациента после получения разрешения от экспертного совета больницы, выделяли ткань периодонтальной связки, присоединенной к корню зуба мудрости, и нарезали ее на двухсторонние кусочки, помещали в чашку диаметром 60 мм и накрывали ее покровным стеклом, и затем проводили культивирование в среде Игла, модифицированной по способу Дульбекко.
3. Анализ методом полимеразной цепной реакции (ПЦР) в режиме реального времени
Выделяли тотальную РНК из клеток периодонтальной связки человека с помощью реагента TRIzol. Синтезировали кДНК, используя 2 мкг тотальной РНК, 1 мкл обратной транскриптазы и 0,5 мкг праймера Oligo (dT). Использовали кДНК синтезированных клеток периодонтальной связки человека для полимеразной цепной реакции в реальном времени с использованием праймеров, приведенных в таблице 2 ниже. Полимеразную цепную реакцию в режиме реального времени проводили в системе определения последовательности ABI PRISM 7500 (Applied Biosystems) с использованием смеси SYBR GREEN PCR Master Mix (Takara, Japan). Полимеразную цепную реакцию в реальном времени проводили при 94°С в течение 1 мин, при 95°С в течение 15 сек - при 60°С в течение 34 сек при условии повторения 40 циклов. Результаты анализировали с использованием сравнительного метода порогового цикла (CT).
Таблица 2
4. Оценка воздействия пептидов на регенерацию пародонта в экспериментальной модели повреждения пародонта на животных
Четырех собак породы бигль (с массой тела 12-16 кг в возрасте 6-8 недель) вводили в состояние общего наркоза путем ингаляции гелорана, внутривенного введения золетила (5 мг/кг) и ксилазина (0,2-0,5 мг/кг), а затем проводили обработку лидокаином (лидокаин 2% с адреналином 1:80000). Из нижней челюсти собаки породы бигль удаляли 4-й премолярный зуб и 2-й молярный зуб, после чего ожидали заживления ранок у собаки в течение 3 месяцев.
После 3 месяцев заживления, формировали трехстеночный дефект пародонта на дистальной и мезиальной поверхностях 1-го молярного зуба. Затем формировали повреждение пародонта размером 4 × 4 × 4 мм с сохранением щечной и дистальной костей вокруг корня зуба, безопасно удаляли корневую альвеолярную кость, выравнивали поверхность корня зуба с помощью кюретки, и затем формировали бороздку на резце с помощью шаровидного бора диаметром 1,2 мм.
Далее в экспериментальной группе проводили трансплантацию коллагеновой губки (раствор пептида, приготовленный растворением пептида в физиологическом растворе, с концентрацией 1 мкг/мкл, добавляли 50 мкл раствора пептида в пробирку Эппендорфа, и затем замачивали в течение 5 минут для приготовления коллагеновой губки), содержащей 50 мкл пептида (SEQ ID NO: 16 группы 2), полученного в примере 1, в области дефекта. После дефекта, только в группе отрицательного контроля (NC) без какой-либо обработки, трансплантировали коллагеновую губку (полученную путем замачивания коллагеновой губки в 50 мкл физиологического раствора в течение 5 минут) путем размещения на внутренней костной стенке костного дефекта, и через 3 месяца умерщвляли животное с трансплантированным отрицательным контролем (NC+Plug) и проводили гистологическую оценку.
Через 3 месяца, собаку породы бигль умерщвляли путем введения избыточного количества (90-120 мг/кг) пентобарбитала. У собаки породы бигль удаляли зуб, фиксировали с помощью 10% формалина, затем удалили кальций путем добавления 5% муравьиной кислоты, формовали и заливали в парафин с получением среза ткани толщиной 5 мкм.
Полученный срез ткани окрашивали гематоксилином и эозином или окрашивали коллаген (окраска трихром по Массону) для подтверждения регенерации периодонтальной связки, и затем проводили анализ с помощью оптического микроскопа, оснащенного цифровой камерой (камера LEICA ICC50, Germany).
Результаты экспериментов
Пример эксперимента 1. Воздействие пептидов на экспрессию маркерных генов для дифференцировки остеобластов и цементобластов в клетках периодонтальной связки человека
Гены сиалопротеина кости (BSP) и белка-1 дентинного матрикса (DMP1) используют в качестве маркеров для дифференцировки остеобластов и цементобластов, и известно, что они являются важными генами для процесса кальцификации кости и цементного вещества корня зуба. Кроме того, ген CAP (белок адгезии цементного вещества корня зуба) экспрессируется в дифференцированных цементобластах, и известно, что он является геном, принимающим участие в прикреплении пучка волокон периодонтальной связки к цементному веществу корня зуба.
На фигуре 1 в графическом виде представлены данные по воздействию пептидов группы 1 и группы 2, полученных в примере 1, на экспрессию маркерных генов BSP, DMP1 и CAP для дифференцировки остеобластов и цементобластов в клетках периодонтальной связки человека (hPDL).
Как показано на фигуре 1, в случае экспериментальной группе, подвергавшейся обработке пептидами группы 1 и группы 2, было доказано, что экспрессия генов BSP, DMP1 и CAP увеличивалась приблизительно в два раза или более по сравнению с контрольной группой.
В таблице 3 приведены результаты ПЦР в режиме реального времени, подтверждающие воздействие пептидов группы 1 и группы 2 на определяемую с помощью ПЦР экспрессию мРНК, и приведены данные по относительному уровню экспрессии мРНК по сравнению с контролем.
В таблице 4 приведены результаты ПЦР в режиме реального времени, подтверждающие воздействие пептидов группы 1 и группы 2 на экспрессию CAP мРНК, и приведены данные по относительному уровню экспрессии мРНК по сравнению с контролем. Приведенные в таблицах 3 и 4 результаты представляют собой средние значения и их стандартные отклонения (SD), полученные путем проведения трех параллельных экспериментов.
Таблица 3
Таблица 4
Пример эксперимента 2. Воздействие пептидов на экспрессию маркерных генов для дифференцировки остеобластов и цементобластов в мезенхимальных стволовых клетках человека
На фигуре 2 представлены результаты, демонстрирующие воздействие пептидов группы 1 и группы 2, полученных в примере 1, на экспрессию маркерных генов для дифференцировки остеобластов и цементобластов в мезенхимальных стволовых клетках человека.
Как показано на фигуре 2, было доказано, что при обработке мезенхимальных стволовых клеток человека с помощью пептида группы 1 и группы 2, экспрессия генов BSP и DMP1, которые являются маркерными генами для дифференцировки остеобластов и цементобластов, была приблизительно от 2 до 4 раз выше, чем экспрессия в контрольной группе.
Пример эксперимента 3. Воздействие пептидов на экспрессию маркерных генов для периодонтальной связки в клетках периодонтальной связки человека
Периостин представляет собой белок, впервые обнаруженный в периодонтальной связке и периосте кости, и периостин экспрессируется в периодонтальной связке и мезенхиме развивающегося зуба и, известно, что он участвует в клеточной адгезии. Согласно нескольким недавним исследованиям, периостин является важным регулятором формирования пародонта, активизирует выработку коллагеновых волокон и миграцию фибробластов и остеобластов, и известно, что он играет ключевую роль в регенерации периодонтальной связки и альвеолярной кости после пародонтологического хирургического вмешательства с целью лечения пародонтоза. Поэтому, было подтверждено воздействие пептида примера 1 на экспрессию периостина, который является маркерным геном дифференцировки клеток периодонтальной связки и геном коллагеновых волокон типа 3 (COL3).
На фигуре 3 представлены результаты, демонстрирующие воздействие пептидов группы 1 и группы 2, полученных в примере 1, на экспрессию гена коллагеновых волокон типа 3 (COL3) и гена периостина, которые являются маркерные гены периодонтальной связки, в клетках периодонтальной связки человека.
Как показано на фигуре 3, было подтверждено, что экспрессия гена коллагеновых волокон типа 3 (COL 3) и гена периостина увеличивается более чем в два раза в клетках периодонтальной связки человека при обработке с помощью пептида группы 1 и группы 2.
В таблице 5 приведены результаты ПЦР в режиме реального времени, подтверждающие воздействие пептидов группы 1 и группы 2 на экспрессию периостина мРНК и приведены данные по относительному уровню экспрессии мРНК по сравнению с контролем. Приведенные в таблице 5 результаты представляют собой средние значения и их стандартные отклонения (SD), полученные путем проведения трех параллельных экспериментов.
Таблица 5
Пример эксперимента 4. Верификация воздействия пептидов на регенерацию пародонта в экспериментальной модели повреждения пародонта на животных
После удаления 4-го премолярного зуба и 2-го молярного зуба из нижней челюсти 4 собак породы бигль, ожидали заживления ранок у собак в течение 3 месяцев. После 3 месяцев заживления, формировали трехстеночный дефект пародонта на дистальной и мезиальной поверхностях 1-го молярного зуба. Затем формировали повреждение пародонта размером 4 × 4 × 4 мм с сохранением щечной и дистальной костей вокруг корня зуба, безопасно удаляли корневую альвеолярную кость, выравнивали поверхность корня зуба с помощью кюретки, и затем формировали бороздку на резце. Далее в экспериментальной группе проводили трансплантацию коллагеновой губки, содержащей 50 мкг пептида (SEQ ID NO: 16) из Примера 1, в области дефекта, и после дефекта, отрицательный контроль (НК) без какой-либо обработки и контроля (НК+Plug) трансплантировали путем размещения только коллагеновой губки на внутренней костной стенке костного дефекта, и через 3 месяца умерщвляли животное с трансплантированным отрицательным контролем (NC+Plug) и проводили гистологическую оценку.
На фигуре 4 приведена фотография ткани, окрашенной с помощью красителя гематоксилин/эозин, через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта и приведены результаты подтверждения воздействия пептида на регенерацию альвеолярной кости.
Как показано на фигуре 4, было подтверждено, что регенерация альвеолярной кости происходила в большей области поврежденного пародонта в экспериментальной группе по сравнению с отрицательным контролем.
На фигуре 5 приведены результаты подтверждения воздействия пептида на регенерацию ткани периодонтальной связки путем окрашивания с помощью красителя гематоксилин/эозин через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта.
Как показано на фигуре 5, в случае отрицательного контроля без какого-либо лечения (фигуры 5A-D) или в случае отрицательного контроля с трансплантированной только коллагеновой губкой (фигуры 5E-H), вдоль поверхности корня зуба не наблюдалось формирования новой ткани, подобной ткани периодонтальной связки (NPD), но наблюдалось формирование соединительной ткани (CT). Кроме того, наблюдалась резорбция дентина в альвеолярной области. Однако, в экспериментальной группе, подвергнутой обработке пептидом (SEQ ID NO: 16) группы 2 (фигуры 5I-L), вдоль поверхности корня зуба наблюдалось не только формирование новой ткани, подобной ткани цементному веществу корня зуба, но также наблюдалось и формирование новой ткани, подобной ткани периодонтальной связки. Новая периодонтальная связка была встроена во вновь сформированную альвеолярную кость и цементное вещество корня зуба.
На фигуре 6 приведены результаты подтверждения воздействия пептида на регенерацию ткани периодонтальной связки с помощью метода окрашивания коллагена (окраска трихром по Массону) через 3 месяца после лечения пептидом (SEQ ID NO: 16) примера 1 в области пораженного пародонта.
Как показано на фигуре 6, в случае отрицательного контроля без какого-либо лечения (фигуры 6A-B) или в случае отрицательного контроля с трансплантированной только коллагеновой губкой (фигуры 6C-D), вдоль поверхности корня зуба формировалась большая часть соединительной ткани (CT), и в некоторых случаях наблюдалось формирование новой ткани, подобной ткани периодонтальной связки (NPD), но пучок волокон периодонтальной связки был распложен неупорядоченно. Кроме того, в случае отрицательного контроля, было обнаружено вдоль поверхности корня зуба формирование нового цементного вещества корня зуба. Однако в случае экспериментальной группы, подвергавшейся обработке с помощью пептида (SEQ ID NO: 16) группы 2 (фигуры 6E-F), наблюдалось формирование вдоль поверхности корня зуба не только новой ткани, подобной ткани цементному веществу корня зуба, но также наблюдалось и формирование новой ткани, подобной ткани периодонтальной связки. Новый пучок волокон периодонтальной связки был вертикально встроен во вновь сформировавшиеся альвеолярную кость и цементное вещество корня зуба.
Таким образом, было подтверждено, что пептид по настоящему изобретению обладает эффектом по регенерации альвеолярной кости и формированию новой ткани, подобной ткани цементного вещества корня зуба, и новой ткани, подобной ткани периодонтальной связки, и новая периодонтальная связка, сформированная пептидом по настоящему изобретению, встроена в заново образованную альвеолярную кость и цементное вещество корня зуба. В связи с этим, было обнаружено, что пептид по настоящему изобретению может быть использован для регенерации пародонта, для предотвращения или лечения пародонтоза и для предотвращения или лечения травматического вывиха зуба.
В описании настоящего изобретения и в чертежах были раскрыты предпочтительные варианты осуществления настоящего изобретения, и хотя в изобретении используются конкретные термины, тем не менее, они используются в самом широком смысле и только для того, чтобы в более легкой форме разъяснить техническое содержание настоящего изобретения и помочь понять настоящее изобретение. Предполагается, что эти термины не ограничивают объем настоящего изобретения. Специалистам в данной области является очевидным, что на основе технической концепции настоящего изобретения могут быть предложены и осуществлены и другие модификации в дополнение к раскрытым в изобретении вариантам осуществления.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ ПЕПТИД | 2018 |
|
RU2764770C1 |
| НОВЫЙ ПЕПТИД | 2017 |
|
RU2719434C1 |
| ВАКЦИНА, НАБОР И СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ПАРОДОНТОЗА У ЖИВОТНЫХ-КОМПАНЬОНОВ | 2005 |
|
RU2364417C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ СПОСОБНОСТЬЮ СТИМУЛИРОВАТЬ РЕПАРАТИВНЫЕ ПРОЦЕССЫ ТКАНЕЙ ПАРОДОНТА, А ТАКЖЕ АНТИОКСИДАНТНЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЯ-2-(3-БЕНЗОИЛФЕНИЛ)-ПРОПАНОАТ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2022 |
|
RU2793537C1 |
| НОВЫЙ ПЕПТИД И ЕГО ПРИМЕНЕНИЕ | 2011 |
|
RU2525913C1 |
| КОМПОЗИЦИИ МАТРИКСНЫХ ПРОТЕИНОВ ДЛЯ ЗАЛЕЧИВАНИЯ РАН | 1999 |
|
RU2241489C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ТКАНЕЙ ПАРОДОНТА | 2008 |
|
RU2368338C1 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭДТК ДЛЯ ПОДГОТОВИТЕЛЬНОЙ ОБРАБОТКИ БИОЛОГИЧЕСКОЙ ПОВЕРХНОСТИ, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И СПОСОБ ОБРАБОТКИ БИОЛОГИЧЕСКОЙ ПОВЕРХНОСТИ | 1995 |
|
RU2155575C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОСТИ АЛЬВЕОЛЯРНОГО ГРЕБНЯ ЧЕЛЮСТИ И ТКАНЕЙ ПАРОДОНТА С РЕДУЦИРОВАННЫМ РЕГЕНЕРАТОРНЫМ ПОТЕНЦИАЛОМ | 2006 |
|
RU2320285C2 |
| Биокомплекс для стимуляции регенерации и ремоделирования тканей | 2021 |
|
RU2794464C1 |
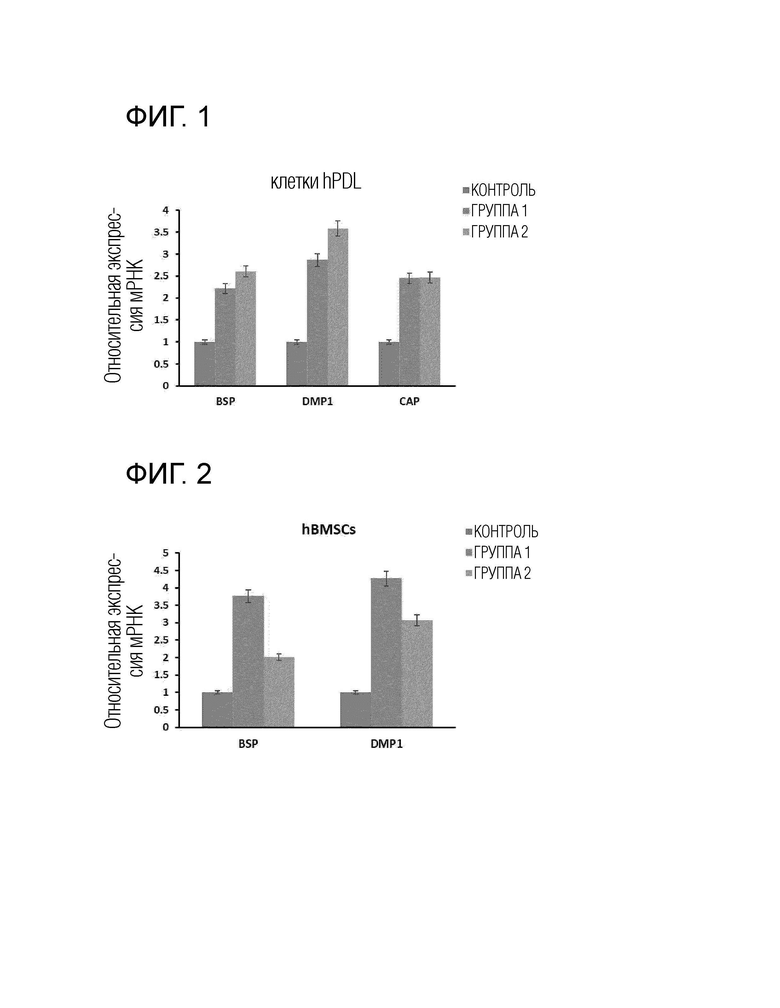
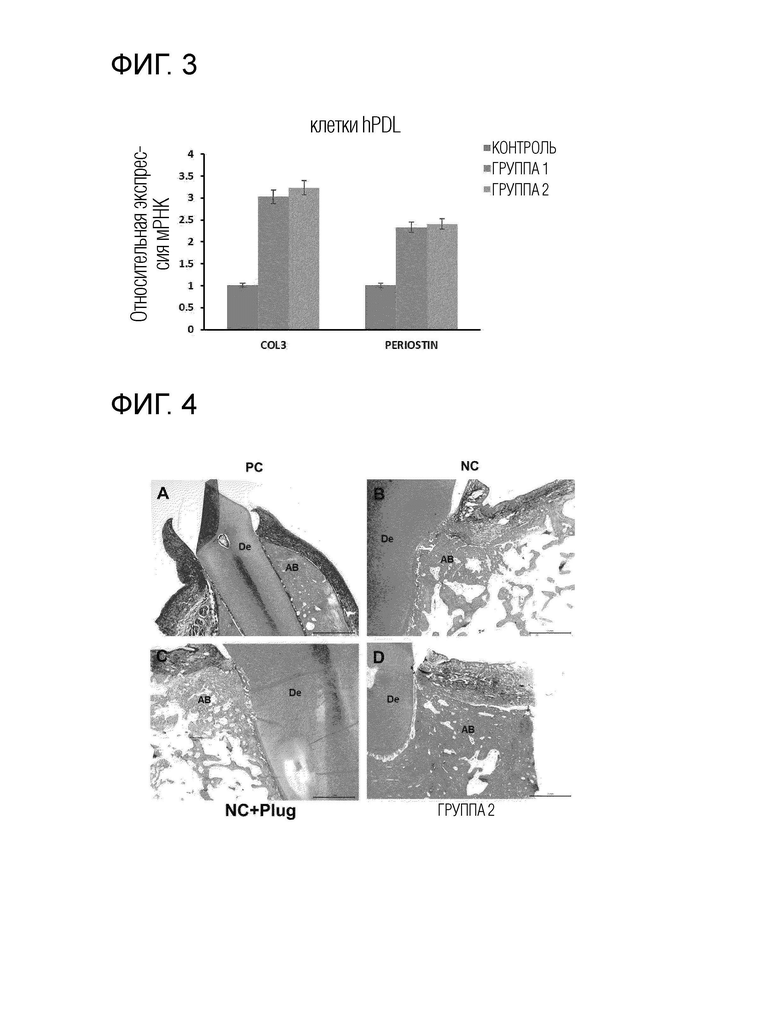
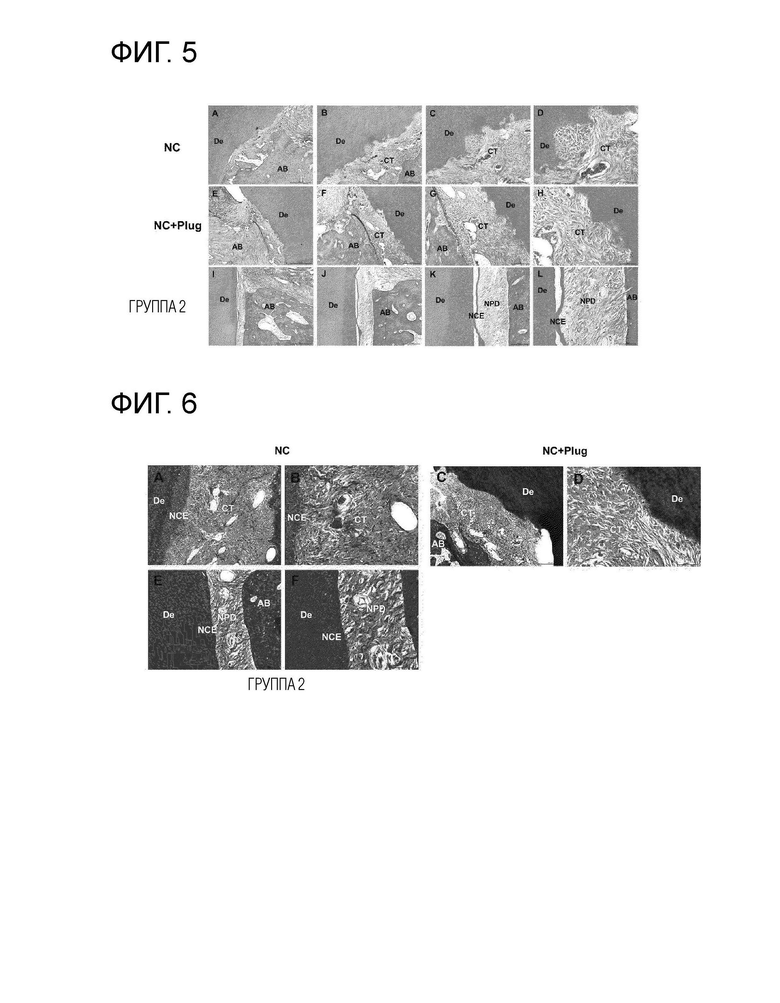
Группа изобретений относится к области стоматологии и касается различных применений композиции, содержащей пептид или его фармацевтически приемлемую соль, где пептид содержит аминокислотную последовательность следующей общей формулы 1: K-Y-K-Q-X5-X6-X7-X8-Y-K (общая формула 1), где в общей формуле 1 от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K); X8 представляет собой аспарагин (N) или серин (S). Предлагается применение фармацевтической композиции, содержащей указанный выше пептид или его фармацевтически приемлемую соль для предотвращения или лечения травматического вывиха зуба. Также предлагается применение композиции, содержащей указанный выше пептид, для регенерации периодонтальной связки. Указанный выше пептид обладает эффектом по регенерации альвеолярной кости и формированию новой ткани, подобной ткани цементного вещества корня зуба, и новой ткани, подобной ткани периодонтальной связки, и новая периодонтальная связка, сформированная пептидом по настоящему изобретению, встроена в заново образованную альвеолярную кость и цементное вещество корня зуба. В связи с чем изобретения могут быть использованы как для регенерации периодонтальной связки, так и для предотвращения или лечения травматического вывиха зуба. 2 н. и 10 з.п. ф-лы, 5 табл., 5 пр., 6 ил.
1. Применение фармацевтической композиции для предотвращения или лечения травматического вывиха зуба, где указанная композиция содержит пептид или его фармацевтически приемлемую соль, содержащий аминокислотную последовательность следующей общей формулы 1:
K-Y-K-Q-X5-X6-X7-X8-Y-K (общая формула 1)
где в общей формуле 1,
от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K);
X8 представляет собой аспарагин (N) или серин (S).
2. Применение по п. 1, где пептид состоит из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16.
3. Применение по п. 1, где пептид находится в форме полипептида, в котором пептид повторяется два или более раз.
4. Применение по п. 1, которое активирует экспрессию генов коллагеновых волокон типа III (COL3) или периостина.
5. Применение по п. 1, где травматический вывих зуба представляет собой ударный подвывих, орбитальный вывих, латеральный вывих или полный вывих, или интрузию вследствие повреждения периодонтальной связки.
6. Применение по п. 1, которое активирует экспрессию любого одного или нескольких генов костного сиалопротеина (BSP), белка-1 дентинного матрикса (DMP1), белка адгезии цементного вещества корня зуба (CAP), коллагена типа III (COL3) и периостина в клетках периодонтальной связки человека.
7. Применение композиции для регенерации периодонтальной связки, где указанная композиция содержит пептид, содержащий аминокислотную последовательность следующей общей формулы 1:
K-Y-K-Q-X5-X6-X7-X8-Y-K (Общая формула 1)
где в общей формуле 1,
от X5 до X7 каждый независимо представляет собой аргинин (R) или лизин (K);
X8 представляет собой аспарагин (N) или серин (S).
8. Применение по п. 7, где пептид состоит из аминокислотной последовательности, являющейся любой одной из последовательностей SEQ ID NOs: 1-16.
9. Применение по п. 7, которое активирует регенерацию цементного вещества корня зуба или альвеолярной кости.
10. Применение по п. 7, где композиция представляет собой фармацевтическую композицию.
11. Применение по п. 7, где композиция представляет собой лечебно-профилактическую косметическую композицию.
12. Применение по п. 7, где композиция представляет собой композицию полезной для здоровья функциональной пищи.
| НОВЫЙ ПЕПТИД | 2017 |
|
RU2719434C1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Терапевтическая стоматология | |||
| Учебник | |||
| Под ред | |||
| Е.В.Боровского, М., ООО "Медицинское информационное агентство", 2004, с | |||
| Саморазгружающаяся платформа | 1922 |
|
SU385A1 |
Авторы
Даты
2024-01-18—Публикация
2021-06-01—Подача