Изобретение относится к медицине, а именно к сосудистой нейрохирургии, целью которого является улучшение результатов хирургического восстановления мозгового кровообращения с использованием шунтирующих операций. Данные операции направлены на создание путей обходного (коллатерального) кровообращения дистальнее области закупорки магистральной артерии головного мозга у пациентов с острой и хронической церебральной ишемией, последствиями ишемического инсульта, в хирургии церебральных аневризм и распространенных опухолей основания черепа. Отсутствие своевременной и адекватной коррекции перфузионного дефицита в подобных случаях может приводить к развитию ишемического инсульта, а также затруднять реабилитационный прогноз у пациентов с его последствиями.
Наиболее распространенной шунтирующей операцией при лечении окклюзий артерий каротидного бассейна в настоящее время является создание экстра-интракраниального микрососудистого анастомоза (ЭИКМА) между лобной или теменной ветвью поверхностной височной артерии (ПВисА) и корковой ветвью средней мозговой артерии (СМА). Техника подобных операций хорошо изучена - они отличаются относительной технической простотой, малой инвазивностью и небольшой продолжительностью хирургического вмешательства. В тоже время для восполнения дефицита мозгового кровотока в ряде случаев одного анастомоза бывает недостаточно, даже при ангиографическом подтверждении хорошего функционирования ЭИКМА.
Эффективность шунтирующих операций напрямую зависит от степени восстановления мозгового кровообращения в бассейне окклюзированной артерии. Поэтому сохраняющийся перфузионный дефицит может нивелировать значение выполненной операции [1]. В подобных случаях целесообразным является использование альтернативных реваскуляризирующих операций: наложения двух анастомозов между лобной и теменной ветвями ПВисА и корковыми артериями бассейна СМА, а также применение широкопросветных анастомозов с использованием аутоартериальных и венозных шунтов.
Обладая способностью обеспечить больший объемный кровоток через анастомозы, данные варианты реваскуляризации способны эффективно компенсировать даже полушарный перфузионный дефицит. В тоже время они являются значительно более инвазивными и продолжительными, а также несут в себе дополнительные риски периоперационных осложнений - ишемических, гиперперфузионных, геморрагических и инфекционно-трофических. Переизбыток кровотока через двойные или широкопрофильные анастомозы может приводить к необоснованным перестройкам системы мозгового кровообращения с замещением естественных путей коллатерального кровообращения и развитием гемодинамической конкуренции между ними, повышая в свою очередь риски развития тромбозов.
Во избежание неоправданных и рискованных оперативных вмешательств актуальным является разработка способа динамического интраоперационного определения необходимого объема реваскуляризации головного мозга. Под объемом реваскуляризации головного мозга понимается совокупность экстра-интракраниальных анастомозов с учетом их объемного кровотока и реваскуляризируемых ими областей, необходимых для компенсации имеющегося перфузионного дефицита.
В настоящее время решение об объеме реваскуляризации принимается на основании предоперационных исследований перфузионного дефицита, состояния коллатерального кровотока и функциональных проб и носит зачастую эмпирический, экспертный характер. Такой подход не учитывает динамические изменения церебральной перфузии после наложения ЭИКМА, не позволяет своевременно локализовать области сохраняющегося перфузионного дефицита и участки локальной гиперперфузии.
В настоящее время известные способы интраоперационного контроля мозгового кровотока ограничиваются использованием флуоресцентной видеоангиографии с интравенозным введением раствора индацианинового зеленого (ICG), ультразвуковой флоуметрии и допплерографии. Они эффективны в оценке проходимости анастомоза и исследовании локальной гемодинамики, однако не позволяют судить о степени компенсации мозгового кровотока.
Принципиально новым подходом является динамическое исследование мозгового кровотока, при котором можно получить наиболее раннюю информацию о степени реперфузии головного мозга в ходе самого оперативного вмешательства. Для этих целей известно использование интраоперационной МРТ (иоМРТ), что разработано и ранее использовано в первую очередь для оценки степени радикальности резекции опухолей головного мозга [3]. В литературе существует лишь две публикации, посвященные исследованию мозгового кровотока с помощью иоМРТ - работа 2015 года D. Wang, в которой у 14 пациентов с болезнью Мойя-мойя после создания ЭИКМА проводилась МРТ в режиме PWI для ранней диагностики синдрома гиперперфузии [3]. Интраоперационную МРТ удалось успешно провести всем пациентам, у 5 из которых интраоперационно были диагностированы признаки гиперперфузии. Это позволило вовремя адаптировать периоперационное ведение больных для предотвращения геморрагических осложнений в послеоперационном периоде. В другом исследовании G. Muscas от 2019 года использовалась методика исследования изменения содержания кислорода в крови (BOLD-эффект) у 5 пациентов после создания ЭИКМА - при этом была подтверждена безопасность и эффективность данной методики во время операции [4]. Однако во всех представленных случаях авторы применяли иоМРТ лишь для раннего послеоперационного контроля и не подразумевали ее использование для коррекции тактики оперативного вмешательства.
На сегодняшний момент в литературе нет работ, в которых был бы предложен способ определения тактики хирургической реваскуляризации головного мозга на основании интраоперационного исследования изменений мозгового кровотока.
Технической задачей заявляемого изобретения является разработка способа определения тактики хирургической реваскуляризации головного мозга на основании результатов динамического исследования мозгового кровотока с помощью иоМРТ.
Технический результат разработанного нами способа заключается в интраоперационном определении наличия показаний или противопоказаний к дополнительной реваскуляризации головного мозга второй донорской ветвью, определении локализации зон остаточной гипоперфузии, выявлении признаков локальной гиперперфузии с целью максимальной компенсации недостаточного мозгового кровоснабжения головного мозга.
Предлагаемый способ позволяет достигнуть значительного, качественного улучшения результатов хирургической реваскуляризации головного мозга, способствует наиболее рациональному восполнению недостаточного мозгового кровотока, необходимого в каждом конкретном случае и минимизировать возможные осложнения.
Его применение целесообразно при окклюзиях артерий каротидного бассейна с обширной областью перфузионного дефицита при условии наличия обеих ветвей поверхностной височной артерии, а также при выполнении нейрохирургических вмешательств, связанных с возможностью выключения из кровотока крупной артерии бассейна СМА.
Решение поставленной технической задачи достигается тем, что у больных непосредственно во время хирургической реваскуляризации выполняется исследование перфузии головного мозга с помощью МРТ в режиме безконтрастного метода псевдонепрерывной маркировки спинов артериальной крови (pCASL). Применение контрастных методов исследования церебральной перфузии не рекомендуется в связи с накоплением контрастного вещества в сосудистом русле, способствующем искажению результатов повторных измерений мозгового кровотока.
В предоперационном периоде пациенту необходимо выполнить исходное перфузионное исследование, которое будет в дальнейшем использоваться для интраоперационной оценки изменений мозгового кровотока после первого этапа реваскуляризации.
Оперативное вмешательство выполняется в специализированной операционной, оборудованной MP-томографом. Техника выполнения операции имеет ряд особенностей:
1. Выбор разреза кожи должен учитывать возможность выделения обеих ветвей поверхностной височной артерии - как правило, это дугообразный разрез в лобно-височной области на стороне реваскуляризации.
2. Производится диссекция обеих ветвей поверхностной височной артерии. При отсутствии признаков функционирующего каротидно-офтальмического анастомоза (окклюзии средней мозговой артерии, болезнь Мойя-Мойя) выбирается в качестве донорской наиболее крупная артерия, в противном случае - теменная ветвь поверхностной височной артерии. Она пересекается и проводится в планируемую область анастомоза. Вторая выделенная ветвь не пересекается.
3. Выполняется костно-пластическая трепанация черепа в проекции сильвиевой щели - не менее 4 см в диаметре, что необходимо для поиска адекватных акцепторных артерий.
4. Первым этапом выполняется реваскуляризация лобных ветвей с целью достижения наибольшей компенсации перфузионого дефицита в конвекситальных функционально значимых областях лобных долей.
5. После наложения анастомоза по стандартной методике проводится контроль его проходимости с помощью контактной допплерографии, флоуметрии или флуоресцентной ангиографии. Сомнительные или низкие параметры кровотока по донорской артерии являются показанием для проведения ревизии анастомоза.
6. После подтверждения функционирования анастомоза субдурально вводится подключичный катетер диаметром 1,5-2 мм (Fr5-6), который фиксируется к твердой мозговой оболочке (ТМО). ТМО, височная мышца с апоневрозом фиксируются наводящими швами. Костный лоскут не устанавливается. Через катетер субдурально вводится физиологический раствор до его истечения через швы мягких тканей с целью выведения остатков воздуха, который может приводить к ухудшению визуализационной картины MP-изображений. Накладываются наводящие временные узловые швы на кожу, рана накрывается асептической повязкой.
7. Пациент перемещается в помещение с интраоперационным МР-томографом. Проводится калибровка и обзорное сканирование головного мозга с последующей безконтрастной MP-ангиографией - лишь при визуализации анастомоза имеет смысл выполнять более продолжительные перфузионные исследования.
8. Основной этап способа - интраоперационное исследование церебральной перфузии в режиме pCASL. Цель исследования - определить степень реперфузии головного мозга, локализовать области остаточного перфузионного дефицита, исключить признаки локальной гиперперфузии. В зависимости от степени восстановления мозгового кровотока можно выделить:
a. Удовлетворительную компенсацию мозгового кровотока, при которой отмечается увеличение кровотока как области реваскуляризации, так и отдаленных областей бассейна средней мозговой артерии. В данном случае принимается решение о завершении операции. Выявление признаков локальной гиперперфузии является показанием для мониторинга АД и ЭЭГ в послеоперационном периоде с решением вопроса о назначении антиконвульсантной терапии.
b. Частичная локальная реперфузия в области реваскуляризации с крупными сохраняющимся без динамики областями перфузионного дефицита в лобно-полярной, теменной или височной областях. Принимается решение о наложении дополнительного анастомоза с акцепторной артерий, кровоснабжающей область перфузионного дефицита, избегая реваскуляризации артериального бассейна с признаками локальной гиперперфузии.
c. Отсутствие признаков реперфузии, обширная область перфузионного дефицита. Принимается решение о повторной ревизии области анастомоза и наложении дополнительного анастомоза. Возможно повторное интраоперационное исследование перфузии. При острых окклюзиях ставится вопрос о широкопросветном шунтировании.
9. Пациент переводится в операционный зал, проводится его повторная укладка, обработка раны, драпировка. Наводящие швы снимаются, восстанавливается доступ к области реваскуляризации. Рана промывается физиологическим раствором. Временный катетер удаляется. В зависимости от результатов перфузионного исследования выполняется наложение дополнительного анастомоза с учетом выбранного типа с выделенной заранее второй ветвью ПВисА, которая коагулируется дистально и пересекается. При определении показаний возможно выполнение высокопотокового шунтирования (пункт 8с). При отсутствии показаний для дополнительной реваскуляризации ТМО ушивается наглухо с герметизацией тахокомбом. Устанавливается и фиксируется костный лоскут, накладываются послойные швы на мягкие ткани и кожу.
Разработанный способ и достигнутые результаты проиллюстрированы на чертежах:
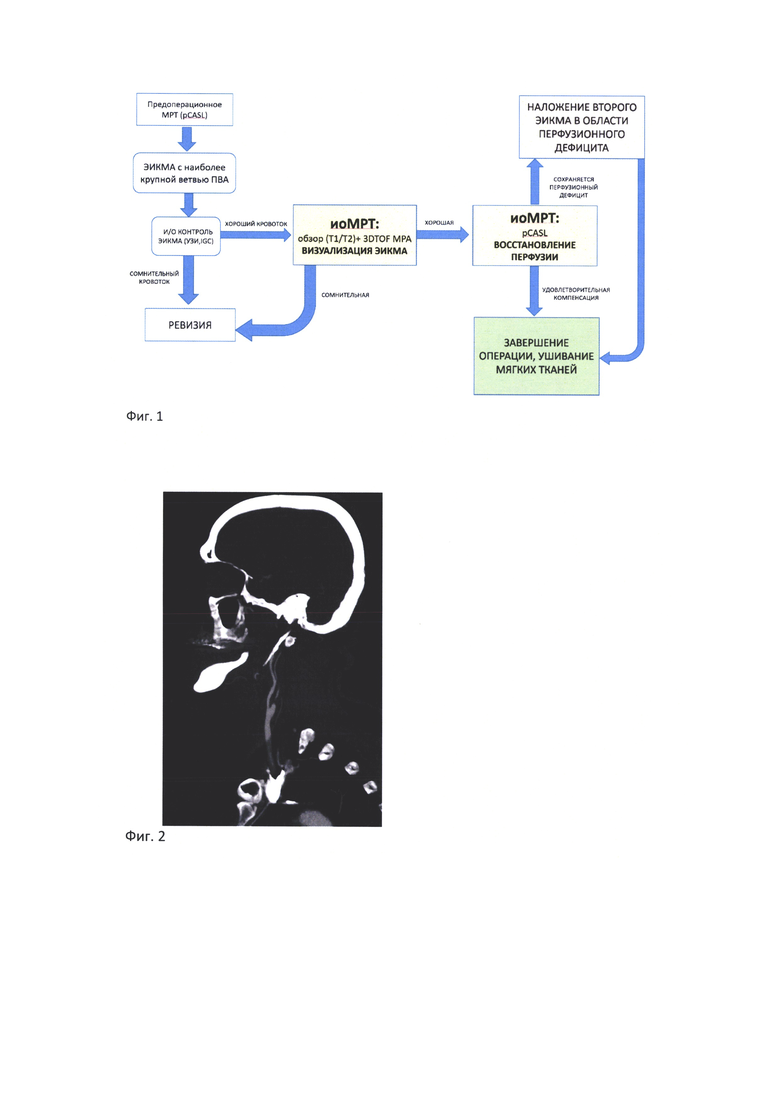
- на Фиг. 1 представлен алгоритм изобретенного способа динамического определения объема реваскуляризации с помощью иоМРТ (белым фоном обозначены известные в настоящее время этапы данного способа, цветным фоном обозначены новые этапы, отражающие суть изобретения).
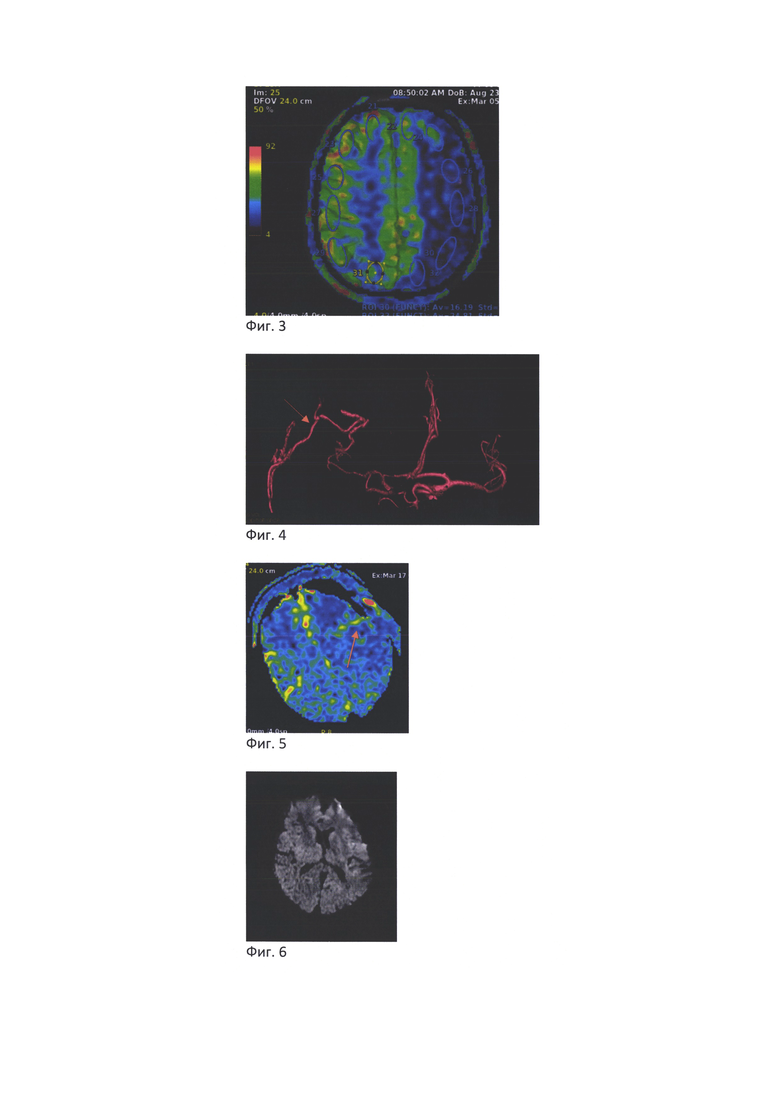
- на Фиг. 2 представлены данные КТ-ангиографии, демонстрирующие окклюзию левой ВСА от устья.
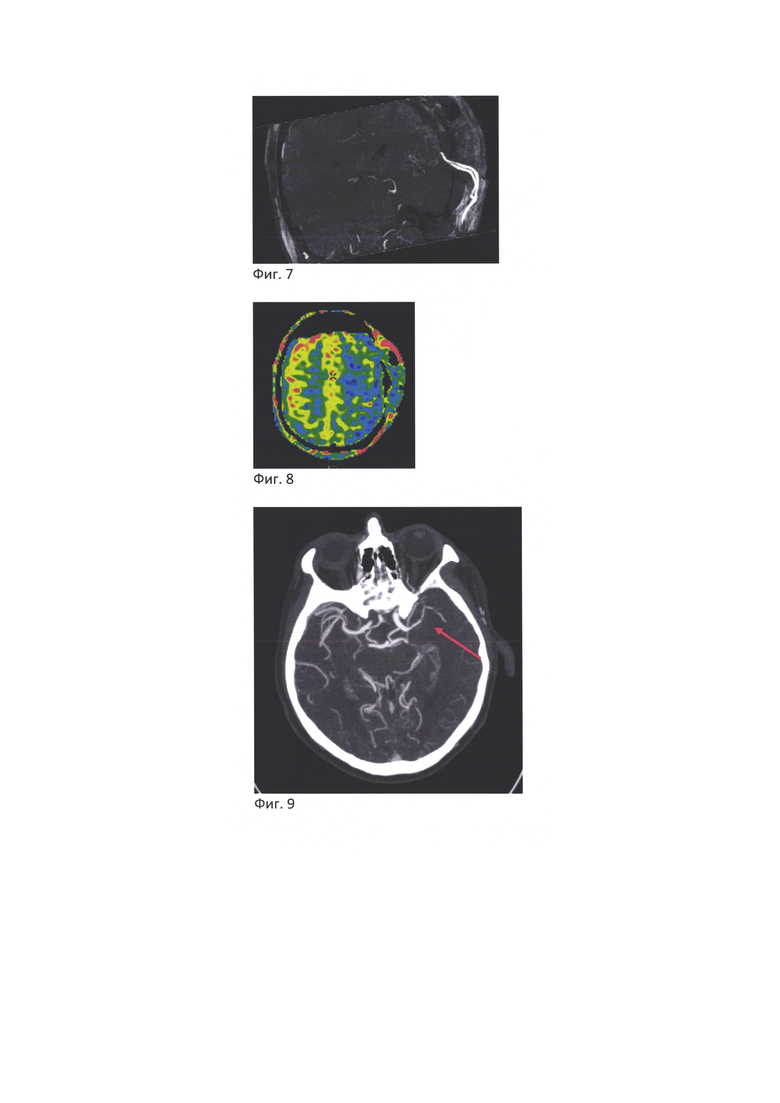
- на Фиг. 3 представлены дооперационные совмещенные изображения МРТ в режиме Т2-FLAIR и ASL у пациента с окклюзией левой ВСА с наличием выраженного перфузионого дефицита всего левого полушария головного мозга.
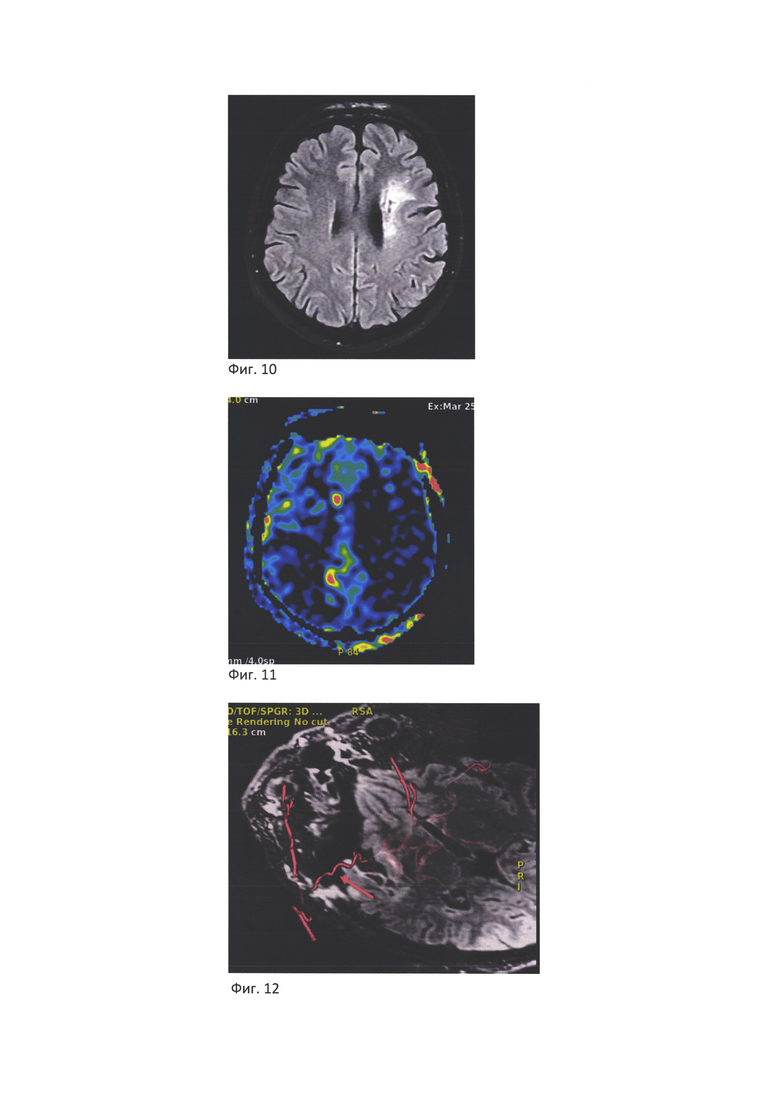
- на Фиг. 4 представлены результаты иоМРТ в режиме ангиографии 3D TOF после наложения первого ЭИКМА, на которых визуализирован хорошо функционирующий анастомоз (стрелка).
- на Фиг. 5 представлены результаты иоМРТ в режиме перфузии ASL, где определяется локальная область реперфузии в зоне анастомоза (стрелка) с сохраняющимися областями гипоперфузии в лобной и теменной областях.
- на Фиг. 6 представлены результаты иоМРТ в диффузионно-взвешенном режиме (DWI), демонстрирующие отсутствие признаков острой ишемии.
- на Фиг. 7 представлены результаты контрольной МРТ пациента после наложения второго анастомоза в режиме ангиографии 3D TOF, демонстрирующие хорошее функционирование обоих стволов ЭИКМА.
- на Фиг. 8 представлены результаты контрольной МРТ пациента после наложения второго анастомоза в режиме перфузии ASL, показывающие полное восстановление мозгового кровотока в левом полушарии.
- на Фиг. 9 представлены данные дооперационной КТ-ангиографии артерий головного мозга, демонстрирующие окклюзию лобной ветви левой СМА (стрелка).
- на Фиг. 10 представлены дооперационные данные МРТ головного мозга в режиме Т2-FLAIR, на которых определяется постишемический очаг в левом полушарии головного мозга.
- на Фиг. 11 представлены данные предоперационной МРТ в режиме ASL, демонстрирующие тяжелый полушарный перфузионный дефицит - выраженное снижение мозгового кровотока ниже 20 мл/100 г/мин всего левого полушария головного мозга.
- на Фиг. 12 представлены интраоперационные совмещенные изображения МРТ в режимах 3DTOF ангиографии и T2-FLAIR, на которых визуализирован функционирующий ЭИКМА.
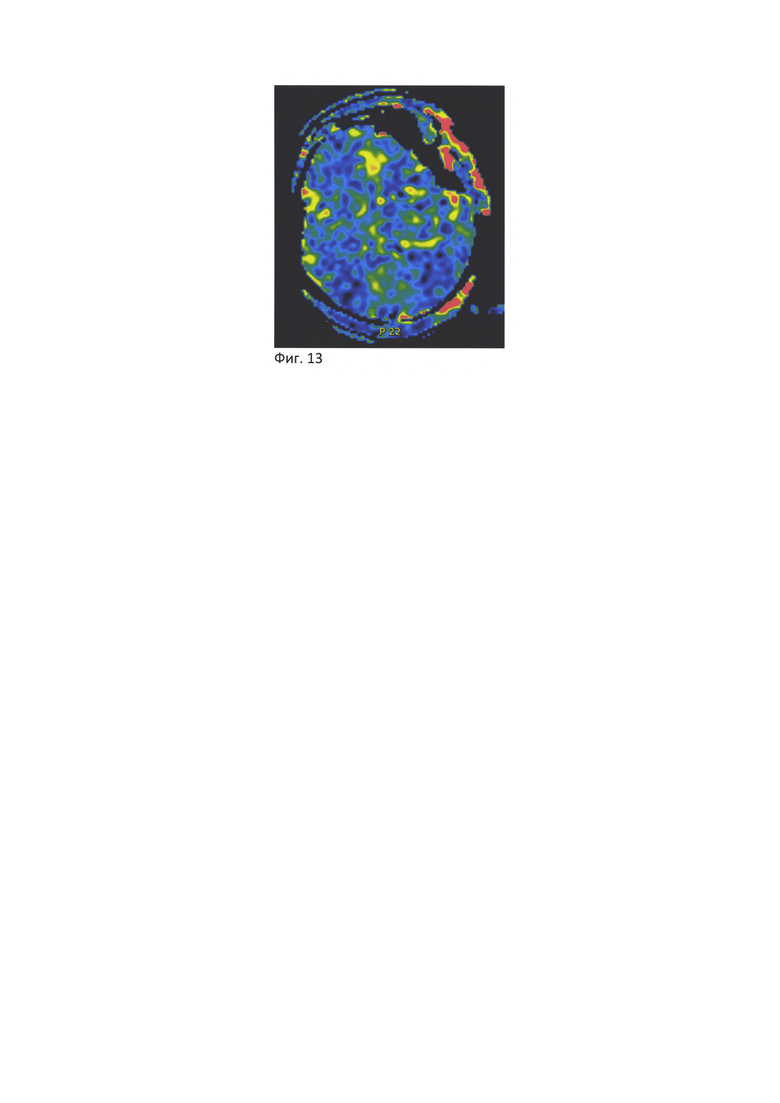
- на Фиг. 13 представлены интраоперационные изображения МРТ в режиме перфузии ASL, демонстрирующие значительное восстановление кровотока в бассейне кровоснабжения лобных ветвей левой СМА.
Заявляемый способ был разработан во ФГАУ «НМИЦН им. ак. Н.Н. Бурденко» Минздрава России и прошел клинические испытания на 24 больных - у 10 пациентов с болезнью Мойя-мойя и у 14 - с посттромботической окклюзией внутренней сонной артерии. Во всех случаях использование данного способа позволило вовремя определить тактику реваскуляризации головного мозга с использованием одной или двух донорских ветвей. Все пациенты перенесли вмешательства удовлетворительно, послеоперационных осложнений ни у одного больного не отмечалось.
Клинические примеры
Клинический пример №1. Показания к дополнительной реваскуляризации второй донорской ветвью. История болезни №1790/22
Пациент С., 68 лет, 2 месяца назад перенес ишемический инсульт в бассейне левой ВСА с развитием нарушения речи и слабости в правых конечностях, сохранявшиеся на момент поступления, несмотря на проведенное реабилитационное лечение.
При обследовании была диагностирована окклюзия левой ВСА (Фиг. 2) и выраженный полушарный дефицит мозгового кровотока (Фиг. 3), зона которого значительно превосходила объем ишемического очага, что говорило о повышенных рисках повторных нарушений мозгового кровообращения и сниженного потенциала для реабилитации пациента. Это обусловило наличие показаний к хирургическому лечению - хирургической реваскуляризации левого полушария головного мозга.
В подобных случаях при реваскуляризации головного мозга важно добиться максимального восполнения имеющегося перфузионного дефицита, поэтому было принято решение динамически определить объем реваскуляризации с помощью иоМРТ. Первым этапом был наложен один анастомоз между теменной ветвью поверхностной височной артерии и лобной прецентральной корковой ветвью М4 бассейна СМА. Контактная допплерография выявила хорошее функционирование анастомоза с величиной линейной скорости кровотока в донорской артерии 50 см/сек.
Для определения показаний к наложению второго анастомоза в соответствии с предложенным в изобретении способом после первого этапа операции выполнена интраоперационная МРТ. В режиме ангиографии 3D TOF визуализирован широкий хорошо функционирующий ствол созданного анастомоза (Фиг. 4), однако по данным pCASL перфузии отмечено лишь локальное улучшение кровотока в области анастомоза, значимого восполнения мозгового кровотока, особенно в передней и задней областях смежного кровообращения, не наблюдалось, а значительная часть полушария демонстрировала низкие значения кровотока (Фиг. 5).
Учитывая данный факт, отсутствие признаков гиперперфузии и участков острой ишемии по данным иоМРТ в режиме DWI, было принято решение о дополнительной реваскуляризации области гипоперфузии левого полушария второй ветвью поверхностной височной артерии.
Пациент вновь был транспортирован в операционную, где проведен второй этап операции. В качестве акцепторной артерии была выбрана ангулярная ветвь СМА, кровоснабжающая зону остаточного дефицита кровотока - к ней была подшита вторая донорская лобная ветвь ПВА. После этого была проведена контрольная МРТ, которая продемонстрировала восстановление кровотока всего бассейна СМА слева (Фиг. 7, 8).
После операции наблюдалась значительная положительная динамика в неврологическом статусе пациента в виде появления и расширения речевой продукции. Пациент был отправлен на дальнейшее реабилитационное лечение.
Клинический пример №2. Отсутствие показаний к дополнительной реваскуляризации второй донорской ветвью. История болезни №2675/22
Пациент Р., 52 лет. перенес ишемический инсульт в бассейне левой СМА с развитием правосторонней гемиплегии и речевых нарушений с последующим частичным восстановлением. На момент поступления у пациента сохранялся умеренный правосторонний гемипарез и моторная афазия. При обследовании по данным СКТ-ангиографии выявлена окклюзия лобной ветви М2 сегмента левой СМА (Фиг. 9).
На МРТ головного мозга визуализировался постишемический очаг левой подкорковой области и передних отделов левой лобной доли (Фиг. 10), по данным pCASL-перфузии диагностировано выраженное снижение мозгового кровотока ниже 20 мл/100 г/мин всего левого полушария головного мозга, значительно превышающее зону постишемических изменений (Фиг. 11). Ввиду высокого риска повторных нарушений мозгового кровообращения в условиях окклюзии СМА и тяжелого дефицита кровоснабжения, было рекомендовано хирургическое лечение - реваскуляризация левого полушария головного мозга. По данным предоперационного обследования спрогнозировать необходимость наложения одного или двух анастомозов являлось невозможным, ввиду чего принято решение о выполнении интраоперационной МРТ. Во время операции после вскрытия ТМО выявлены постишемические изменения и признаки атрофии лобной доли ближе к полюсу - в данном месте лобные корковые ветви были гипоплазированы и не подходили в качестве акцепторных ветвей. В качестве акцепторной ветви была выбрана лобная центральная ветвь бассейна СМА с низким кровотоком, к которой была подшита теменная ветвь ПВисА. После этого с целью оценки степени восстановления кровотока и определения показаний к дополнительной реваскуляризации была выполнена интраоперационная МРТ.
Интраоперационная МРТ визуализировала хорошее функционирование анастомоза (Фиг. 12) с полным восстановлением бассейна кровоснабжения левой СМА, за исключением зоны постишемических изменений передних отделов лобной доли (Фиг. 13). Учитывая обширную зону восстановления кровотока, за исключением области ишемического очага с гипоплазированными корковыми артериями, от наложения второго анастомоза принято решение воздержаться.
Операцию пациент перенес без осложнений, в раннем послеоперационном периоде отмечена положительная динамика в виде улучшения речи и увеличения силы и объема движений в правых конечностях.
Использованная тактика с применением интраоперационного контроля степени и объема восстановления кровотока позволяет своевременно скорректировать тактику хирургического лечения и определить показания или противопоказания к наложению второго анастомоза, а также исключить ранние ишемические осложнения.
Источники информации, принятые во внимание:
1. Lukshin, V.A., et al., Criteria of the efficacy of surgical brain revascularization in patients with chronic cerebral ischemia. Zh Vopr Neirokhir Im N N Burdenko, 2016. 80(2): p. 53-62.
2. Burkhardt, J.K., et al., Single-Barrel Versus Double-Barrel Superficial Temporal Artery to Middle Cerebral Artery Bypass: A Comparative Analysis. World Neurosurg, 2019.125: p. e408-e415.
3. Lindner, Т., et al., Intraoperative resection control using arterial spin labeling - Proof of concept, reproducibility of data and initial results. Neuroimage Clin, 2017.15: p. 136-142.
4. Усачев Д.Ю., Л.В.А., Шевченко E.B., Шульгина A.A., Ахмедов А.Д., Способ выбора акцепторной артерии при хирургической реваскуляризации головного мозга у пациентов с хронической церебральной ишемией. Патент РФ №2019142988. 2019.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выбора акцепторной артерии при хирургической реваскуляризации головного мозга у пациентов с хронической церебральной ишемией | 2019 |
|
RU2742191C1 |
| СПОСОБ РЕВАСКУЛЯРИЗАЦИИ ГОЛОВНОГО МОЗГА ПРИ ОСТРОМ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ | 2019 |
|
RU2707258C1 |
| СПОСОБ ВЫПОЛНЕНИЯ СЕЛЕКТИВНОГО ЭИКМА В РЕГИОНЕ ГИПОПЕРФУЗИИ С ИСПОЛЬЗОВАНИЕМ НЕЙРОНАВИГАЦИИ | 2017 |
|
RU2648001C1 |
| СПОСОБ ЛЕЧЕНИЯ ЦЕРЕБРАЛЬНОЙ ИШЕМИИ | 2008 |
|
RU2408300C2 |
| СПОСОБ ОТБОРА ПАЦИЕНТОВ ДЛЯ ОПЕРАЦИИ ЭКСТРА-ИНТРАКРАНИАЛЬНОГО МИКРОАНАСТОМОЗА ПРИ АТЕРОСКЛЕРОТИЧЕСКОЙ ОККЛЮЗИИ ВНУТРЕННЕЙ СОННОЙ АРТЕРИИ | 2018 |
|
RU2695275C1 |
| СПОСОБ АУТОВЕНОЗНОГО ШУНТИРОВАНИЯ ПРИ ОККЛЮЗИРУЮЩИХ ПОРАЖЕНИЯХ АРТЕРИЙ ГОЛОВНОГО МОЗГА | 2014 |
|
RU2554210C1 |
| СПОСОБ ВЫБОРА ТИПА ЭКСТРА-ИНТРАКРАНИАЛЬНОГО ШУНТА ПО ПРОПУСКНОЙ СПОСОБНОСТИ ПРИ ОСТРЫХ И ХРОНИЧЕСКИХ ЦЕРЕБРОВАСКУЛЯРНЫХ ПАТОЛОГИЯХ, ТРЕБУЮЩИХ РЕВАСКУЛЯРИЗИРУЮЩЕГО ВМЕШАТЕЛЬСТВА | 2021 |
|
RU2784442C1 |
| Способ планирования мини-доступа для создания экстра-интракраниального микроанастомоза с использованием МСКТ-ангиографии головного мозга в 3D реконструкции. | 2016 |
|
RU2637826C1 |
| СПОСОБ КОМБИНИРОВАННОЙ РЕВАСКУЛЯРИЗАЦИИ ГОЛОВНОГО МОЗГА ПРИ БОЛЕЗНИ МОЙАМОЙА | 2013 |
|
RU2522917C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ОБХОДНОГО ШУНТИРОВАНИЯ ГОЛОВНОГО МОЗГА С ИСПОЛЬЗОВАНИЕМ УСТЬЯ ВЕРХНЕЧЕЛЮСТНОЙ АРТЕРИИ (анастомоз по типу конец-в-конец) | 2021 |
|
RU2781443C1 |
Изобретение относится к медицине, а именно к сосудистой нейрохирургии, и может быть использовано для определения тактики хирургической реваскуляризации головного мозга при создании экстра-интракраниального микрососудистого анастомоза (ЭИКМА). После подшивания одной ветви ЭИКМА оценивают реперфузию головного мозга при помощи интраоперационной магнитно-резонансной томографии в режиме ASL. Если определяют увеличение кровотока области реваскуляризации и отдаленных областей бассейна средней мозговой артерии, принимают решение о завершении операции. Если определяют локальную реперфузию в области реваскуляризации с крупными сохраняющимся без динамики областями перфузионного дефицита в лобно-полярной, теменной или височной областях, принимают решение о наложении дополнительного анастомоза с акцепторной артерией, кровоснабжающей область перфузионного дефицита, избегая реваскуляризации артериального бассейна с признаками локальной гиперперфузии. Если определяют отсутствие признаков реперфузии или обширную область перфузионного дефицита, принимают решение о повторной ревизии области анастомоза и наложении дополнительного анастомоза. Способ обеспечивает улучшение результатов хирургического восстановления мозгового кровообращения с использованием шунтирующих операций за счет определения наличия показаний или противопоказаний к дополнительной реваскуляризации головного мозга второй донорской ветвью, определения локализации зон остаточной гипоперфузии и признаков локальной гиперперфузии. 13 ил., 2 пр.
Способ определения тактики хирургической реваскуляризации головного мозга при создании экстра-интракраниального микрососудистого анастомоза (ЭИКМА), заключающийся в том, что после подшивания одной ветви ЭИКМА оценивают реперфузию головного мозга при помощи интраоперационной магнитно-резонансной томографии в режиме ASL и,
если определяют увеличение кровотока области реваскуляризации и отдаленных областей бассейна средней мозговой артерии, принимают решение о завершении операции;
если определяют локальную реперфузию в области реваскуляризации с крупными сохраняющимся без динамики областями перфузионного дефицита в лобно-полярной, теменной или височной областях, принимают решение о наложении дополнительного анастомоза с акцепторной артерией, кровоснабжающей область перфузионного дефицита, избегая реваскуляризации артериального бассейна с признаками локальной гиперперфузии;
если определяют отсутствие признаков реперфузии или обширную область перфузионного дефицита, принимают решение о повторной ревизии области анастомоза и наложении дополнительного анастомоза.
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ПРОФИЛАКТИКИ ГИПОКСИИ ГОЛОВНОГО МОЗГА ВО ВРЕМЯ ПРОВЕДЕНИЯ КАРОТИДНОЙ ЭНДАРТЕРЭКТОМИИ | 2020 |
|
RU2759654C1 |
| Способ выбора акцепторной артерии при хирургической реваскуляризации головного мозга у пациентов с хронической церебральной ишемией | 2019 |
|
RU2742191C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНОЙ СТРАТЕГИИ РЕВАСКУЛЯРИЗАЦИИ У ПАЦИЕНТОВ С СИМУЛЬТАННЫМ АТЕРОСКЛЕРОТИЧЕСКИМ ПОРАЖЕНИЕМ БРАХИОЦЕФАЛЬНЫХ И КОРОНАРНЫХ АРТЕРИЙ | 2017 |
|
RU2681581C1 |
| ЛУКШИН В.А | |||
| и др | |||
| Локальная гемодинамика после создания ЭИКМА у пациентов с симптоматическими окклюзиями сонных артерий | |||
| Журнал "Вопросы нейрохирургии" имени Н.Н | |||
| Бурденко | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Солесос | 1922 |
|
SU29A1 |
| ВИШНЯКОВА М.В | |||
| и др | |||
| Информативность перфузионной | |||
Авторы
Даты
2024-01-19—Публикация
2023-03-30—Подача