Настоящее изобретение относится к протезу камеры сердца, выбранной из группы, состоящей из левого желудочка, левого предсердия, правого желудочка и правого предсердия, который позволяет простым, регулируемым, эффективным и надежным способом обеспечивать физиологическую морфологию и функционирование в соответствии с управлением, наилучшим образом соответствующими его физиологическим характеристикам. Настоящее изобретение также относится к системе протезов камер сердца с двумя или более такими протезами камер сердца и к кардиологической вспомогательной системе, содержащей такой протез камеры сердца или такую систему протезов камер сердца. Кроме того, протез камеры сердца согласно настоящему изобретению обладает уменьшенным размером и массой, что позволяет упростить его имплантацию и управление кардиологической вспомогательной системы, что требует сниженного энергопотребления, значительно расширяя терапевтические возможности для пациентов с тяжелой сердечной недостаточностью, обеспечивая улучшенные терапевтические результаты. Кроме того, протез камеры сердца и соответствующая кардиологическая вспомогательная система согласно настоящему изобретению просты и недороги при изготовлении.
Как известно, сердце представляет собой мышцу, которая прокачивает кровь через весь организм: правая сторона сердца принимает лишенную кислорода кровь из организма и перекачивает ее в легкие, где кровь обогащается кислородом и из нее устраняется двуокись углерода, в то время как левая сторона сердца принимает богатую кислородом кровь и возвращает из легких и прокачивает через организм, где она снабжает клетки кислородом и питательными веществами.
На фиг. 1 показано сердце, имеющее четыре камеры, т.е. два верхних предсердия и два нижних желудочка, а именно: правое предсердие 10, левое предсердие 20, правый желудочек 30 и левый желудочек 40. Предсердия 10 и 30 являются принимающими камерами сердца, а желудочки 30 и 40 являются перекачивающими камерами сердца.
Кроме того, сердце имеет четыре клапана, а именно: трикуспидальный клапан 50, расположенный между правым предсердием 10 и правым желудочком 30; легочный клапан 60, расположенный между правым желудочком 30 и легочной артерией 110; митральный клапан 70, расположенный между левым предсердием 20 и левым желудочком 40; и аортальный клапан 80, расположенный между левым желудочком 40 и аортой 100. Функция клапанов сердца состоит в том, чтобы обеспечивать кровоток в правильном направлении через сердце (указано пунктирными стрелками). В частности, лишенная кислорода кровь перекачивается из правого желудочка 30 в легочную артерию 110, а из нее в легкие. Аналогичным образом, обогащенная кислородом кровь перекачивается из левого желудочка 40 в аорту 100, а из нее через все тело. Кроме того, верхняя полая вена 120 и нижняя полая вена 125 переносят лишенную кислорода кровь из верхней половины и нижней половины тела, соответственно, в правое предсердие 10, в то время как легочные вены 130 переносят обогащенную кислородом кровь из легких к левому предсердию 20.
Более конкретно, во время систолической фазы камеры сердца происходит сокращение мышц сердца, при котором рассматриваемая камера сердца сжимается и кровь перекачивается. Во время систолы предсердий (показана на фиг. 1b) сокращаются только предсердия 10 и 20, а трикуспидальный клапан 50 и митральный клапан 70 открыты, в то время как легочный клапан 60 и аортальный клапан 80 закрыты, при этом кровь переносится из предсердий 10 и 20 к желудочкам 30 и 40 соответственно; во время систолы желудочков (показана на фиг. 1a) сокращаются только желудочки 30 и 40, трикуспидальный клапан 50 и митральный клапан 70 закрыты, а легочный клапан 60 и аортальный клапан 80 открыты, при этом кровь переносится из желудочков 30 и 40 в легочную артерию 110 и аорту 100 соответственно.
Аналогичным образом, во время диастолической фазы камеры сердца происходит релаксация мышц сердца, при которой рассматриваемая камера сердца расширяется и заполняется кровью. При диастоле предсердий (показана на фиг. 1a) предсердия 10 и 20 расширяются (раньше, чем при систоле предсердий), трикуспидальный клапан 50 и митральный клапан 70 закрыты, при этом кровь из верхней и нижней полых вен 120 и 125 и из легочных вен 130 заполняет предсердия 10 и 20 соответственно; при диастоле желудочков (показана на фиг. 1b) желудочки 30 и 40 расширяются (раньше, чем при систоле желудочков), пока они не достигнут максимального объема, также называемого теледиастолическим объемом желудочков, легочный клапан 60 и аортальный клапан 80 закрыты, при этом кровь из предсердий 10 и 20 заполняет желудочки 30 и 40 соответственно. В частности, систола предсердий происходит в соответствии с диастолой желудочков, а диастола предсердий происходит в соответствии с систолой желудочков.
Другими словами, систолы предсердий и желудочков и диастолы предсердий и желудочков в синусовом ритме (т.е. при физиологии здорового человека) точно синхронизированы по времени, что позволяет сердцу повторно обогащать кислородом лишенную кислорода кровь, поступающую из организма, путем ее перекачивания к легким и, соответственно, через весь организм.
Некоторые заболевания могут снижать способность сердца перекачивать кровь. Когда сердце не перекачивает кровь соответствующим образом, жидкость может скапливаться в легких и других частях организма. Симптомы сердечной недостаточности обычно возникают из-за неспособности сердца подавать достаточный кровоток к жизненно важным органам тела. В этом случае могут потребоваться кардиологические вспомогательные системы, когда лекарственные средства и другие хирургические возможности недостаточны для решения проблемы сердечной недостаточности.
Среди кардиологических вспомогательных систем предшествующего уровня техники широко распространенным решением является устройство для помощи желудочкам с аксиальным кровотоком (VAD), которое включает в себя механический насос, обладающий значительно улучшенными терапевтическими возможностями для пациентов с тяжелой сердечной недостаточностью. Такие VAD-устройства, как, например, устройство Jarvik, предлагаемое американской компанией Jarvik Heart, Inc. и устройство DeBakey, предлагаемое американской компанией MicroMed Technology, Inc., описаны в патентных публикациях WO 89/07427 A1, WO 99/49912 A1, US 2018/0303991 A1 и WO 2018/078370 A1 и Ootaki Y. et al. в публикации ʺPhasic coronary blood flow pattern during a continuous flow left ventricular assist supportʺ (Паттерн фазного коронарного кровотока при непрерывном поддержании кровотока левого желудочка), Eur. J. of Cardio-thorac. Surg. 28 (2005) 711-16, Radovancevic B. et al. в публикации ʺEnd-organ Function in Patients on Long-term Circulatory Support With Continuous- or Pulsatile-flow Assist Devicesʺ (Функция концевого органа у пациентов с долговременным поддержанием вспомогательного кровообращения поддерживающими непрерывный или пульсирующий кровоток устройствами), J. of Heart and Lung Transp. 2007, 815-18, Frazier O.H. et al. в публикации ʺMulticenter clinical evaluation of the HeartMate vented electric left ventricular assist system in patients awaiting heart transplantationʺ (Мультицентровая клиническая оценка электрически вентилируемой системы поддержания функции левого желудочка HeartMate у пациентов, ожидающих пересадки сердца), J. Thorac. Cardiovasc. Surg. 2001, 122:1186-95, Letsou G.V. et al. в публикации ʺContinuous axial-flow left ventricular assist device (Jarvik 2000) maintains kidney and liver perfusion for up to 6 monthsʺ (Устройство поддержания непрерывного аксиального кровотока левого желудочка), Ann. Thorac. Surg. 2003; 76:1167-70, Thalmann M. et al. в публикации ʺPhysiology of continuous blood flow in recipients of rotary cardiac assist devicesʺ (Физиология непрерывного кровотока у пациентов с роторными устройствами поддержания функции сердца), J. Heart Lung Transplant 2005; 24:237-45, Thohan V. et al. в публикации ʺCellular and hemodynamics responses of failing myocardium to continuous flow mechanical circulatory support using the DeBakey – Noon left ventricular assist device: a comparative analysis with pulsatile-type devicesʺ (Клеточный и гемодинамический отклик при нарушении функции миокарда для механического поддержания непрерывного кровотока сердца с использованием устройства DeBakey – Noon поддержания функции левого желудочка: сравнительный анализ с устройствами поддержания пульсирующего кровотока), J. Heart Lung Transplant 2005; 24:566-75, и Hetzer R. et al. в публикации ʺFirst experiences with a novel magnetically suspended axial flow left ventricular assist deviceʺ (Первый опыт использования нового устройства поддержания функции левого желудочка с аксиальным кровотоком, свободно плавающего за счет магнитного воздействия), Eur. J. Cardiothorac. Surg. 2004; 25:964-70.
VAD-устройства основаны на роторных насосах, разработанных для решения некоторых проблем устройств пульсирующего кровотока предшествующего уровня техники, таких как размер и сложность, трудности при имплантации и неблагоприятные события (например, интраоперационное кровотечение, инфекция, тромбоз и неисправность устройства). Миниатюрные имплантируемые насосы VAD-устройств обеспечивают непрерывный кровоток вместо пульсирующего кровотока за счет использования электромагнитного устройства, состоящего из ротора с лопастями. Современные насосы непульсирующего аксиального кровотока имеют тенденцию к компактной конструкции с использованием одиночной подвижной части и обладают низкими требованиями в отношении энергопотребления. Например, устройство Jarvik предназначено для имплантации в основную часть левого желудочка и, следовательно, канюля для поступающей жидкости не нужна. Долговременные имплантаты роторных VAD-устройств для левого желудочка все шире используются для терапии пациентов с терминальной стадией сердечной недостаточности.
Однако имеющиеся в настоящее время VAD-устройства также обладают некоторыми недостатками.
Прежде всего, роторные насосы, которыми они снабжены, функционируют на скорости, которая должна быть тщательно отрегулирована во избежание как обратного потока, так и чрезмерного всасывания. Действительно, может возникать обратный поток (регургитация), когда скорость насоса (об/мин) установлена на слишком низкое значение, вызывая возврат крови из аорты 100 в левый желудочек 40 через насос, в то время как чрезмерное всасывание может возникать, когда насос пытается втягивать больше крови, чем имеется в левом желудочке 40, за счет высокой скорости насоса. Всасывание может привести к коллапсу левого желудочка 40, что может вызвать боль в груди и повреждение тканей сердца. Следовательно, подача насоса, которая зависит, главным образом, от скорости, которая связана с частотой сердечных сокращений, и которая не регулируется в пульсирующем режиме, не способна физиологически соответствовать синусовому ритму и изменениям периферического кровотока, что приводит к отсутствию адаптации объемной скорости кровотока при использовании. Кроме того, имплантация такого устройства чрезвычайно инвазивна и требует необратимого повреждения камеры сердца, в которую оно имплантируется, а также создает дополнительные перегрузки других камер сердца, на которые воздействует неестественный сердечный кровоток.
Линия оттока из насоса присоединена к нисходящему отделу аорты. При высокой скорости насоса аортальный клапан 80 остается закрытым, и VAD-устройство позволяет полностью восстановить функцию желудочков сердца. Чтобы ограничить возможное образование тромбов в аортальном клапане 80, в современных VAD-системах скорость снижена до 10 секунд в минуту, и во время этого интервала аортальный клапан 80 открывается повторно, а пульсирующий кровоток является значительным. По мере повторного повышения числа оборотов роторного насоса пульсация аортального кровотока уменьшается, но полностью исчезнуть не может из-за минимального давления, достаточного, чтобы продолжать открывать аортальный клапан 80. Когда аортальный клапан 80 вновь остается закрытым, градиент давления между левым желудочком 40 и аортой 100 фактически меняется на протяжении сердечного цикла, поскольку изменения давления, вызванного открытием и закрытием митрального клапана 70 (и в гораздо меньшей степени остаточной систолой желудочков), передаются в аорту 100 через насос. Изучение профиля артериальных пульсаций позволяет оценить дикротическую выемку в нисходящей части кривой давления, которая коррелирует с закрытием митрального клапана 70 (аортальный клапан 60 постоянно закрыт в этот период 50 секунд). Другими словами, движения миокарда, при которых имплантируется VAD-устройство, создают непрерывный поток, что дает вклад в остаточное слабое пульсовое давление результирующего кровотока системы кровообращения.
Подводя итоги, VAD-устройства создают не пульсирующий и, следовательно, нефизиологичный поток (т.е. не соответствующий синусовому ритму) и их гемодинамические характеристики отличаются от устройств с пульсирующим кровотоком.
Как указано выше, при заданной скорости вращения поток через роторный насос является непрерывным, а не пульсирующим, как в физиологическом кровотоке.
Кроме того, если скорость насоса слишком велика, изменения, типичные для морфологии формы кривой собственного артериального давления имеют тенденцию исчезать, а дикротическая выемка отсутствует (указывая, что аортальный клапан 60 закрыт).
Наконец, при наличии VAD-устройства с роторным насосом, флуктуации давления в левом желудочке передаются в артерии через VAD-устройство, даже когда скорость насоса достаточно высока для удержания аортального клапана 60 закрытым. Это может иметь важные клинические последствия (например, срастание створки аортального клапана 60 и тромбоз нисходящей аорты), и данное исследование направлено на оптимизацию их использования для предотвращения таких осложнений.
Для преодоления этих недостатков были разработаны другие устройства, которые охватывают весь орган, например, описанные в патентных документах США 2016/0317729 A1 и 2016/0346085 A1. Внутрижелудочковый ортотопический насос, используемый в сочетании с обычным сердцем, предложен в патентной публикации США 5139517 A.
Однако последние устройства являются в равной степени высоко инвазивными и неселективными для камер сердца, которые впоследствии могут изнашиваться и ухудшаться со временем, и эти устройства не способны соответствовать физиологической морфологии и могут порождать проблемы электрофизиологического характера.
Следовательно, задачей настоящего изобретения является селективная помощь в функционировании какой-либо камеры сердца, а не только левого желудочка, простым, совместимым, эффективным и надежным способом, чтобы гарантировать, что камера сердца обладает физиологичной морфологией и функциональностью, которые в наибольшей степени соответствуют ее физиологическим характеристикам.
Объектом настоящего изобретения является протез камеры сердца, предназначенный для имплантации в камеру сердца пациента, выбранную из группы, состоящей из левого желудочка, левого предсердия, правого желудочка и правого предсердия,
причем камера сердца содержит собственный выпускной клапан и по меньшей мере одно впускное отверстие, выбранное из группы, состоящей из собственного впускного клапана и одного или более выпускных устий полых вен или легочных вен,
при этом протез содержит:
- внутреннюю упругую мембрану, поверхность которой ограничивает упруго изменяемый объем и которая имеет первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем,
- базовую опорную упругую мембранную структуру, содержащую или состоящую из наружной упругой мембраны, имеющей первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, причем наружная упругая мембрана дополнительно содержит множество фиксаторов, выполненных с возможностью зацепления за внутреннюю стенку камеры сердца,
при этом края первых отверстий внутренней и наружной упругих мембран неразъемно соединены друг с другом для формирования наружного края, предназначенного для того, чтобы он окружал собственный выпускной клапан и был пришит к нему,
причем края второго отверстия внутренней и наружной упругих мембран неразъемно соединены друг с другом для формирования по меньшей мере одного впускного края, предназначенного для того, чтобы он окружал по меньшей мере одно впускное отверстия и был пришит к нему,
при этом внутренняя упругая мембрана и базовая опорная упругая мембранная структура присоединены друг к другу посредством множества первичных различных соединительных элементов,
причем внутренняя упругая мембрана и базовая опорная упругая мембранная структура ограничивают первичный промежуток между ними, который предназначен для приема текучей среды с разным количеством и/или давлением для динамического изменения объема первичного промежутка и указанного упруго изменяющегося объема, ограниченного внутренней поверхностью внутренней упругой мембраны.
Согласно другому аспекту настоящего изобретения наружная упругая мембрана может обладать коэффициентом упругости, который не больше, необязательно меньше, чем коэффициент упругости внутренней упругой мембраны.
Согласно другому аспекту настоящего изобретения каждая из внутренней и наружной упругих мембран может обладать изменяющимся коэффициентом упругости, причем каждая из внутренней и наружной упругих мембран, необязательно, содержит две или более областей с соответствующими коэффициентами упругости.
Согласно другому аспекту настоящего изобретения текучая среда может представлять собой жидкость, необязательно гемосовместимый раствор, более необязательно стерильный физиологический раствор, или газ, необязательно гелий.
Согласно другому аспекту настоящего изобретения протез камеры сердца может дополнительно содержать по меньшей мере один искусственный клапан, неразъемно присоединенный к наружному краю или по меньшей мере одному впускному краю.
Согласно другому аспекту настоящего изобретения первичные изменяемые соединительные элементы могут представлять собой первичные упругие связи, каждая из которых обладает коэффициентом упругости, который больше, чем коэффициент упругости наружной упругой мембраны и чем коэффициент упругости внутренней упругой мембраны, причем указанные первичные упругие связи обладают коэффициентами упругости, необязательно, меняющимися в зависимости от области внутренней упругой мембраны, к которой они присоединены.
Согласно другому аспекту настоящего изобретения протез камеры сердца выполнен с возможностью помещения внутрь катетера.
Согласно другому аспекту настоящего изобретения наружная упругая мембрана и/или внутренняя упругая мембрана могут содержать рентгеноконтрастные участки.
Согласно другому аспекту настоящего изобретения первичный промежуток может быть сообщен по текучей среде по меньшей мере с одним упругим пакетом переменного объема, которым снабжен протез, или с внешним насосом.
Согласно дополнительному аспекту настоящего изобретения по меньшей мере одна из внутренней упругой мембраны и наружной упругой мембраны может обладать прерывистой структурой, необязательно выбранной из группы, содержащей:
- ячеистую прерывистую структуру, образованную множество упругих пластинок, необязательно шестигранной формы, соединенных друг с другом вдоль линий упругого соединения, причем, необязательно, линии упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих пластинок, и
- прерывистую структуру, образованную множеством упругих многоугольных пластинок, необязательно пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения, причем, необязательно, линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости упругих многоугольных пластин.
Согласно другому аспекту настоящего изобретения каждая из внутренней упругой мембраны и наружной упругой мембраны могут содержать множество электродов, предназначенных для электрической и/или электромагнитной поляризации внутренней упругой мембраны и наружной упругой мембраны соответственно под управлением электронного блока обработки данных, присоединенного к указанным электродам посредством соответствующих кабелей управления.
Согласно другому аспекту настоящего изобретения базовая опорная упругая мембранная структура может дополнительно содержать промежуточную упругую мембрану, которая расположена между наружной упругой мембраной и внутренней упругой мембраной, причем промежуточная упругая мембрана, необязательно, обладает коэффициентом упругости, который не больше, необязательно меньше, чем коэффициент упругости наружной упругой мембраны и чем коэффициент упругости внутренней упругой мембраны,
причем промежуточная упругая мембрана имеет первое отверстие, ограниченное первым краем, неразъемно соединенным с краями первых отверстий внутренней и наружной упругих мембран, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, неразъемно соединенным с краями указанных вторых отверстий внутренней и наружной упругих мембран,
причем промежуточная упругая мембрана и наружная упругая мембрана соединены друг с другом посредством множества вторичных изменяемых соединительных элементов, необязательно, состоящих из вторичных упругих связей, каждая из которых, необязательно, обладает коэффициентом упругости, который больше коэффициента упругости наружной упругой мембраны и коэффициента упругости промежуточной упругой мембраны, причем вторичные упругие связи обладают коэффициентом упругости, изменяющимся в зависимости от области промежуточной упругой мембраны, к которой они присоединены,
при этом множество первичных изменяемых соединительных элементов присоединяют внутреннюю упругую мембрану и промежуточную упругую мембрану друг к другу,
причем наружная упругая мембрана и промежуточная упругая мембрана ограничивают вторичный промежуток между ними, который предназначен для приема текучей среды, необязательно, состоящей из жидкости, необязательно из гемосовместимого раствора, более необязательно из стерильного физиологического раствора, или из газа, необязательно гелия.
Согласно дополнительному аспекту настоящего изобретения вторичный промежуток может быть предназначен для приема текучей среды с переменным количеством и/или давлением для динамического изменения объема вторичного промежутка, причем вторичный промежуток, необязательно, сообщен по текучей среде по меньшей мере с одним изменяемым объемом упругого пакета, которым снабжен протез, или с внешним насосом.
Согласно другому аспекту настоящего изобретения промежуточная упругая мембрана может обладать прерывистой структурой, необязательно выбранной из группы, содержащей:
- ячеистую прерывистую структуру, образованную множеством упругих пластинок, необязательно шестигранной формы, соединенных друг с другом вдоль линий упругого соединения, причем, необязательно, линии упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих пластинок, и
- прерывистую структуру, образованную множеством упругих многоугольных пластинок, необязательно пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения, причем, необязательно, линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости упругих многоугольных пластин.
Согласно другому аспекту настоящего изобретения промежуточная упругая мембрана может содержать множество электродов, предназначенных для электрической и/или электромагнитной поляризации промежуточной упругой мембраны под управлением электронного блока обработки данных, присоединенного к указанным электродам посредством соответствующих кабелей управления.
Согласно дополнительному аспекту настоящего изобретения протез камеры сердца может быть выполнен с возможностью имплантации:
- в левый желудочек, при этом наружный край является аортальным краем, который предназначен для того, чтобы он окружал собственный аортальный клапан и был пришит к нему, а по меньшей мере один впускной край состоит из митрального края, который предназначен для того, чтобы он окружал собственный митральный клапан и был пришит к нему, или
- в левое предсердие, при этом выпускной край является митральным краем, предназначенным для окружения собственного митрального клапана и пришивания к нему, а по меньшей мере один впускной край состоит из одного или более краев легочных вен, предназначенных для того, чтобы они окружали одно или более соответствующих выпускных устьев легочных вен и были пришиты к ним с, или
- в правый желудочек, при этом выпускной край является краем легочного клапана, предназначенным для того, чтобы он окружал собственный легочный клапан и был пришит к нему, а по меньшей мере один впускной край состоит из края трикуспидального клапана, предназначенного для того, чтобы он окружал собственный трикуспидальный клапан и был пришит к нему, или
- в правое предсердие, при этом наружный край является краем трикуспидального клапана, который предназначен для того, чтобы окружать собственный трикуспидальный клапан и быть пришитым к нему, а по меньшей мере один впускной край состоит из одного или более краев полых вен, которые предназначены для того, чтобы они окружали одно или более соответствующих выпускных устьев полых вен и были пришиты к ним.
Также объектом настоящего изобретения является система протезов камер сердца, содержащая от двух до четырех протезов камер сердца, как указано выше, причем указанные протезы камер сердца предназначены для имплантации в соответствующие две или более камер сердца пациента.
Согласно другому аспекту настоящего изобретения протезы камер сердца могут содержать или состоять из двух протезов камер сердца, связанных друг с другом, которые предназначены для имплантации в левый желудочек и в левое предсердие или в правый желудочек и в правое предсердие, причем первичные промежутки связанных протезов камер сердца сообщаются по текучей среде друг с другом через передающий канал, при этом объем первичного промежутка одного из двух связанных протезов камер сердца выполнен с возможностью увеличения, когда объем первичного промежутка другого из двух связанных протезов камер сердца уменьшается, и наоборот, посредством перемещения текучей среды между первичными промежутками двух связанных протезов камер сердца.
Еще одним объектом настоящего изобретения является кардиологическая вспомогательная система, содержащая:
- протез камеры сердца или систему протезов камер сердца, описанную выше,
- по меньшей мере один насос и/или электронный блок обработки данных, предназначенный для управления количеством и/или давлением указанной текучей среды, поступающей в первичный промежуток протеза камеры сердца или протезов камер сердца системы протезов камер сердца для динамического изменения объема первичного промежутка протеза камеры сердца или протезов камер сердца системы протезов камер сердца.
Протез камеры сердца согласно настоящему изобретению, а также соответствующая система позволяют способствовать функционированию какой-либо камеры сердца (или двум или более камерам сердца) физиологичным образом, также адаптируемым для различных обстоятельств, благодаря электрическому и/или электромагнитному и/или пневматическому управлению.
В частности, протез камеры сердца, соответствующая система и соответствующая кардиологическая вспомогательная система согласно настоящему изобретению значительно повышают терапевтические возможности для пациентов с тяжелой сердечной недостаточностью. Действительно, система поддержания функции сердца согласно настоящему изобретению способна создавать пульсирующий и физиологический кровоток, гемодинамические характеристики которого отличаются от характеристик непрерывного кровотока, полученных с VAD-устройством на основе роторного насоса. При заданной скорости активации протез камеры сердца согласно настоящему изобретению, а также соответствующая система используются изменяемым и адаптивным образом, при этом они чувствительны к градиенту давления кровотока, который проходит через них (например, в случае применения для левого желудочка 40, этот градиент представляет собой перепад давления между давлением в аорте 100 и давлением в левом желудочке 40 во время систолы желудочков, в то время как он представляет собой перепад давления между давлением в левом предсердии 20 и давлением в левом желудочке 40 во время систолы предсердий). Кроме того, кривая полученного артериального давления соответствует физиологической кривой сердца человека, на которой присутствует дикротическая выемка (т.е. аортальный клапан 80 закрывается).
Кроме того, протез камеры сердца, соответствующая система и соответствующая кардиологическая вспомогательная система согласно настоящему изобретению обладают уменьшенным размером и весом, что позволяет проще осуществлять имплантацию и управление, причем они имеют сниженное энергопотребление.
Наконец, протез камеры сердца, соответствующая система и соответствующая кардиологическая вспомогательная система согласно настоящему изобретению просты и дешевы при изготовлении.
Далее настоящее изобретение описано посредством иллюстрации, причем это описание не подразумевает ограничения им, согласно предпочтительным вариантам осуществления, со ссылкой на приложенные чертежи.
На фиг. 1 схематично показан вид сердца в разрезе;
на фиг. 2 – вид в перспективе первого варианта выполнения протеза согласно настоящему изобретению, из которого удалена часть;
на фиг. 3 – вид сердца в разрезе, в которое имплантирован протез, показанный на фиг. 2;
на фиг. 4 – вид спереди сердца пациента, показанного на фиг. 3;
на фиг. 5 – вид в перспективе второго варианта выполнения протеза согласно настоящему изобретению, из которого удалена часть (фиг. 5a), и вид в перспективе его увеличенного участка (фиг. 5b);
на фиг. 6 – вид в разрезе сердца, в которое имплантирован третий вариант выполнения протеза согласно настоящему изобретению;
на фиг. 7 – вид спереди сердца пациента, показанного на фиг. 6;
на фиг. 8 – вид в разрезе сердца, в которое имплантирован четвертый вариант выполнения протеза согласно настоящему изобретению;
на фиг. 9 – вид в разрезе сердца, в которое имплантирован первый вариант выполнения системы протезов камер сердца согласно настоящему изобретению;
на фиг. 10 – вид в разрезе сердца, в которое имплантирован второй вариант выполнения системы протезов камер сердца согласно настоящему изобретению;
на фиг. 11 – вид в разрезе сердца, в которое имплантирован третий вариант выполнения системы протезов камер сердца согласно настоящему изобретению; и
на фиг. 12 – вид в разрезе сердца, в которое имплантирован четвертый вариант выполнения системы протезов камер сердца согласно настоящему изобретению.
На чертежах идентичные номера позиций будут использоваться для аналогичных элементов.
На фиг. 2 и 3 показан первый вариант выполнения протеза согласно настоящему изобретению, который предназначен для левого желудочка, т.е. он является протезом левого желудочка. Протез левого желудочка содержит наружную упругую мембрану 200 и внутреннюю упругую мембрану 250, каждая из которых имеет первое отверстие и второе отверстие. Края первых отверстий наружной и внутренней упругих мембран 200 и 250 неразъемно соединены друг с другом для формирования аортального края 285, ограничивающего аортальное отверстие 280; края вторых отверстий наружной и внутренней упругих мембран 200 и 250 неразъемно соединены друг с другом для формирования митрального края 275, ограничивающего митральное отверстие 270. Предпочтительно, края первых отверстий наружной и внутренней упругих мембран 200 и 250 соединены друг с другом электросваркой для формирования аортального края 285; аналогичным образом, края вторых отверстий наружной и внутренней упругих мембран 200 и 250 соединены друг с другом электросваркой для формирования митрального края 275.
Наружная упругая мембрана 200 и внутренняя упругая мембрана 250 упруго соединены друг с другом посредством нескольких упругих связей 290, каждая из которых имеет два конца, неразъемно присоединенных к внутренней поверхности 204 наружной упругой мембраны 200 и к наружной поверхности 252 внутренней упругой мембраны 250 соответственно. Каждая из упругих связей 290 выполнена с возможностью упругого удлинения, когда она подвергается нагрузке, которая вызывает расхождение концов друг от друга, начиная из состояния покоя. Наружная поверхность 202 наружной упругой мембраны 200 содержит множество обычных крючков 210 (также называемых фиксаторами), аналогичными используемым для прикрепления уменьшающих объем левого желудочка протезов к внутренней стенке 45 левого желудочка, которые выполнены с возможностью зацепления за внутреннюю стенку 45 левого желудочка, когда они втыкаются в ткань левого желудочка, и обеспечивают надежную имплантацию наружной упругой мембраны 200 в ней, как показано на фиг. 3.
Как наружная упругая мембрана 200, так и внутренняя упругая мембрана 250 обладают морфологией, которая соответствует морфологии внутренней стенки 45 левого желудочка (для имплантации в который предназначен), поэтому они по существу содержат три области: основание, у которого расположены первое и второе отверстия, верхушку желудочка и промежуточную стенку, которая соединяет основание и верхушку желудочка, таким образом, промежуточная стенка расположена в промежуточном положении между основанием и верхушкой желудочка. Это позволяет наружной упругой мембране 200 прилегать к внутренней стенке желудочка подобно внутренней перчатке, при этом она удерживается фиксаторами 210.
В связи с этим протез левого желудочка, а именно наружная упругая мембрана 200 и внутренняя упругая мембрана 250, могут быть изготовлены разного размера, чтобы применять их для конкретных объемов левого желудочка разных пациентов, которые связаны с площадью поверхности тел пациентов (ППТ – площадь поверхности тела).
Благодаря такой форме наружной и внутренней упругих мембран 200 и 250, протезы могут быть имплантированы внутрь левого желудочка путем адаптации к его ткани, при этом они зацепляются за его внутреннюю стенку 45 фиксаторами 210. Необязательно, форма боковой поверхности двух наружной и внутренней упругих мембран 200 и 250 может включать в себя два выреза (не показаны на чертежах), без фиксаторов, предназначенных для приема передней и задней папиллярных мышц и сухожильных хорд левого желудочка (также не показаны на чертежах), присоединенных к митральному клапану 70, чтобы протезы не создавали помех функционированию самих папиллярных мышц и сухожильных корд.
В любом случае, как наружная, так и внутренняя упругие мембраны 200 и 250, необязательно, должны обладать морфологически точным соответствием одной из внутренних стенок 45 левого желудочка (в которую предполагается имплантировать протезы), поскольку их упругость позволяет компенсировать любые морфологические различия; в частности, упругость наружной упругой мембраны 200 позволяет ей повторять морфологию внутренней стенки 45 левого желудочка, за которую зацепляются фиксаторы 210.
Митральный край 275 выполнен с возможностью окружения собственного митрального клапана 70 и пришивания к нему, а аортальный край 285 выполнен с возможностью окружения собственного аортального клапана 80 и пришивания к нему. В частности, митральный край 275 действует как впускной край, собственный митральный клапан 70 действует как собственный впускной клапан, из которого состоит по меньшей мере одно впускное отверстие камеры сердца, аортальный край 285 действует как наружный край, а собственный аортальный клапан 80 действует как собственный выпускной клапан.
Наружная и внутренняя упругие мембраны 200 и 250 и связи 290 изготовлены из биологически совместимых упругих материалов, необязательно биологически совместимых упругих полимерных материалов, более необязательно из политетрафторэтилена (также известного, как пористый ПТФЭ).
Фиксаторы 210 изготовлены из биологически совместимого металлического материала, необязательно сплава с памятью формы, более необязательно из сплава никеля-титана с памятью формы (также известного, как нитинол).
Наружная и внутренняя упругие мембраны 200 и 250, упруго присоединенные друг к другу посредством нескольких упругих связей 290, ограничивают замкнутый промежуток 230 между ними с объемом, который может упруго изменяться, как будет подробно указано далее. В частности, базовая опорная упругая мембранная структура состоит из наружной упругой мембраны 200, при этом промежуток 230 действует как первичный промежуток, а множество упругих связей 290 используются как несколько первичных изменяемых соединительных элементов.
Предпочтительно, наружная упругая мембрана 200 обладает коэффициентом упругости, который не больше (т.е. меньше или равен), необязательно меньше (т.е. она менее упругая), коэффициента упругости внутренней упругой мембраны 250. Кроме того, для улучшения моделирования физиологически упругого поведения левого желудочка коэффициент упругости внутренней упругой мембраны 250, необязательно, меняется в зависимости от ее области, как будет подробно описано далее.
Предпочтительно, упругие связи 290 обладают коэффициентом упругости, превышающим коэффициент упругости наружной и внутренней упругих мембран 200 и 250. Также для улучшения моделирования физиологического упругого поведения левого желудочка коэффициент упругости упругих связей 290, необязательно, меняется в зависимости от области внутренней упругой мембраны 250, к которой они присоединены одним концом, как будет подробно описано далее.
Протез левого желудочка, показанный на фиг. 2 и 3, может быть имплантирован в левый желудочек посредством минимально инвазивного чрескожного имплантата, путем его введения через аортальный клапан 80 с помощью катетера, необязательно, с диаметром в диапазоне от 18 до 24 французских единиц, более необязательно в диапазоне от 18 до 21 французской единицы (где французская единица – это единица измерения диаметров катетеров по так называемой французской шкале, также известной как шкала Шарьера, где 1 французская единица = 0,33 мм), который, по сути, будет содержать протез в сжатом состоянии. Это введение аналогично обычно выполняемым в настоящее время введениям других устройств, таких как искусственные аортальные клапаны, митральные фиксаторы и периферические стенты.
После введения в левый желудочек протезы расширяются, а фиксаторы 210, которые содержит наружная поверхность 202 наружной упругой мембраны 200, зацепляются за внутреннюю стенку 45 левого желудочка, чтобы стабилизировать положение протезов в левом желудочке. Митральный край 275, который располагается так, чтобы он окружал митральный клапан 70, пришивается в непосредственной близости от митрального клапана 70; аналогичным образом, аортальный край 285, который располагается так, чтобы он окружал аортальный клапан 80, пришивается в непосредственной близости от аортального клапана 80.
В качестве альтернативы протез левого желудочка, показанный на фиг. 2 и 3, может быть имплантирован в левый желудочек посредством не очень инвазивной хирургической операции на сердце (например, трансапикальной или с подключичным доступом) или посредством инвазивной хирургической операции на сердце. В этом случае после позиционирования протеза путем введения фиксаторов 210 в ткань левого желудочка, протезы также могут быть стабилизированы хирургом за счет пришивания к внутренней стенке 45 левого желудочка. Также в этом случае митральный край 275 и аортальный край 285 пришиваются в непосредственной близости от митрального клапана 70 и аортального клапана 80 соответственно.
Предпочтительно, протез левого желудочка согласно настоящему изобретению содержит участки, например, в наружной упругой мембране 200 и/или внутренней упругой мембране 250, которые являются рентгеноконтрастными, чтобы они были видны при рентгеноскопии, что помогает хирургу во время размещения протеза в левом желудочке (например, митральный край 275 и аортальный край 285 могут быть рентгеноконтрастными).
Промежуток 230, ограниченный наружной упругой мембраной 200 и внутренней упругой мембраной 250, предназначен для приема текучей среды, в частности жидкости, такой как гемосовместимый раствор, например стерильный физиологический раствор, или газа, например гелия, с изменяющимся количеством и/или давлением для динамического изменения объема промежутка 230 и, таким образом, для изменения упруго изменяемого объема, ограниченного внутренней поверхностью 254 внутренней упругой мембраны 250.
Для этого доступ к промежутку 230 осуществляется через (по меньшей мере) одно отверстие для доступа, выполненное в наружной упругой мембране 200, причем после имплантации протеза в левый желудочек к этому отверстию пришивается канал 330, причем канал 330 присоединяет промежуток 230 к внешнему (гидравлическому или пневматическому) насосу 340A. Необязательно, края этого (по меньшей мере одного) отверстия для доступа изготовлены из рентгеноконтрастного материала, что позволяет их легко идентифицировать для позиционирования канала 330; во время введения протеза в левый желудочек эти (по меньшей мере одно) отверстия для доступа закрыты для предотвращения попадания биологического материала в промежуток 230. Указанное (по меньшей мере одно) отверстие может быть расположено в любом месте наружной упругой мембраны 200, а следовательно, канал 330 может пересекать соответствующую область миокарда (может также проходить через аорту 100). Предпочтительно, протезы могут иметь несколько уплотненных отверстий для доступа (или просто края, ограничивающие область наружной упругой мембраны 200, которая может быть удалена для получения отверстия для доступа, к краям которого может быть пришит канал 330), при этом несколько уплотненных отверстий для доступа могут быть распределены по наружной упругой мембране 200: хирург может выбрать отверстие для доступа, к которому следует пришить канал 330 на основе места наружной упругой мембраны 200, которое соответствует надлежащей области миокарда, и может открыть выбранное отверстие для доступа (или удалить область наружной упругой мембраны 200, ограниченную выбранным краем, чтобы получить отверстие для доступа), а затем пришить канал 330 к его краю. В альтернативном варианте хирург может создать отверстие для доступа в любом месте на наружной упругой мембране 200 (которое соответствует определенной области миокарда), удалив область наружной упругой мембраны 200, а затем пришив канал 330 к краю созданного таким образом отверстия.
Для лучшего понимания настоящего изобретения далее описаны основные режимы работы протеза левого желудочка, показанного на фиг. 2 и 3. В конце систолы предсердий внутренняя упругая мембрана 250 расширяется до теледиастолического объема желудочка и содержит обогащенную кислородом кровь, поступающую из левого предсердия 20. На фиг. 3a можно видеть, что для того, чтобы вызвать эффективную систолу желудочков, насос 340A подает текучую среду в промежуток 230, например, путем введения жидкости (например, гемосовместимого раствора) или путем вдувания газа (например, гелия). Это вызывает увеличение объема промежутка 230 и перемещение внутренней упругой мембраны 250 от наружной упругой мембраны 200, т.е. внутренняя упругая мембрана 250 перемещается внутрь левого желудочка. Как следствие, это вызывает повышение давления во внутренней упругой мембране 250 (т.е. повышение давления крови, заключенной во внутренней упругой мембране 250) и, следовательно, закрывание митрального клапана 70, открытие аортального клапана 80 и выброс систолического толчка, также известный, как УО (ударный объем), через аортальное отверстие 280. В частности, общее изменение внутреннего объема, ограниченного внутренней упругой мембраной 250, составляет в диапазоне, например, от примерно 80 до примерно 120 миллилитров для взрослого среднего телосложения, что равно объему выброса УО; предпочтительно, насос 340A предназначен для вытеснения объема примерно 200 миллилитров жидкости или газа.
На фиг. 3b показано, что в конце систолы желудочков аортальный клапан 80 закрывается, и начинается систола предсердий, при которой митральный клапан 70 открывается и внутреннее пространство внутренней упругой мембраны 250 начинает заполняться кровью, поступающей из левого предсердия 20 и проходящей через митральное отверстие 270. Для получения эффективной диастолы желудочков насос 340A удаляет текучую среду из промежутка 230, например, путем всасывания жидкости (например, гемосовместимого раствора) или газа (например, гелия). Это вызывает сжатие объема промежутка 230, и внутренняя упругая мембрана 250 прижимается ближе к наружной упругой мембране 200, т.е. внутренняя упругая мембрана 250 перемещается к внутренней стенке 45 левого желудочка. Это сохраняет давление во внутренней упругой мембране 250 (т.е., давление крови, заключенной во внутренней упругой мембране 250) при более низких значениях, чем кровяное давление в аорте 100 и кровяное давление в левом предсердии 20, удерживая аортальный клапан 80 закрытым, а митральный клапан 70 открытым, а также обеспечивая кровоток из левого предсердия 20 во внутреннюю упругую мембрану 250. Предпочтительно, внутренняя упругая мембрана 250 по существу соприкасается с наружной упругой мембраной 200, при этом внутренняя и наружная упругие мембраны 250 и 200 могут продолжать расширяться с увеличением общего объема левого желудочка, пока не будет достигнут соответствующий теледиастолический объем; в альтернативном варианте, например в случае миокарда с незначительно нарушенной дилатацией желудочков, внутренняя упругая мембрана 250 может расширяться, достигая теледиастолического объема желудочков, также не вызывая расширения наружной упругой мембраны 200.
В конце систолы предсердий кровь перестает перетекать из левого предсердия 20 во внутреннюю упругую мембрану 250, митральный клапан 70 закрывается, а аортальный клапан 80 открывается, таким образом, начинается новый сердечный цикл.
Протезы позволяют добиться эффективного опорожнения внутренней части внутренней упругой мембраны 250 во время систолы желудочков за счет введения текучей среды в промежуток 230, а также улучшения опорожнения левого предсердия 20 и эффективного наполнения внутренней части внутренней упругой мембраны 250 во время систолы предсердий за счет удаления текучей среды из промежутка 230.
Другими словами, наружная упругая мембрана 200, жестко соединенная с внутренней стенкой 45 левого желудочка, действует как опора для внутренней упругой мембраны 250, помогая ей сместиться к центру левого желудочка и в противоположном направлении к внутренней стенке 45 левого желудочка, обеспечивая надежное, быстрое и эффективное изменение объема промежутка 230. Поэтому наружная упругая мембрана 200, предпочтительно, обладает меньшим коэффициентом упругости, чем внутренняя упругая мембрана 250, чтобы она была более жесткой и обладала ограниченной возможностью расширения.
Как указано, для улучшения моделирования физиологически упругого поведения левого желудочка, коэффициент упругости внутренней упругой мембраны 250, необязательно, является различным в зависимости от области. Действительно, верхушка желудочка обладает большим смещением, чем промежуточные области, и даже в большей степени относительно областей митрального клапана 70 и аортального клапана 80, которые являются более жесткими, поскольку линии кровотока от первого ко второму достаточно короткие. Следовательно, необязательно, основание внутренней упругой мембраны 250 обладает меньшим коэффициентом упругости, чем промежуточная стенка внутренней упругой мембраны 250, а коэффициент упругости промежуточной стенки внутренней упругой мембраны 250 меньше, чем у верхушки желудочка внутренней упругой мембраны 250 (которая обладает максимальным коэффициентом упругости). Это позволяет избежать потенциального появления турбулентности кровотока и потерь энергии. Возможно, коэффициент упругости внутренней упругой мембраны 250 также может меняться непрерывным образом (постепенно возрастая), начиная от основания к верхушке желудочка внутренней упругой мембраны 250.
При этом для улучшения моделирования физиологического упругого поведения левого желудочка коэффициент упругости упругих связей 290, необязательно, меняется в зависимости от области внутренней упругой мембраны 250, к которой они присоединены одним концом, а именно: упругие связи 290, присоединенные к основанию внутренней упругой мембраны 250, обладают меньшим коэффициентом упругости, чем упругие связи 290, присоединенные к промежуточной стенке внутренней упругой мембраны 250, а коэффициент упругости упругих связей 290, присоединенных к промежуточной стенке внутренней упругой мембраны 250, меньше, чем у упругих связей 290, присоединенных к верхушке желудочка внутренней упругой мембраны 250 (которые обладают максимальным коэффициентом упругости). Возможно, коэффициент упругости упругих связей 290 также может меняться непрерывным образом (постепенно возрастая) от основания к верхушке желудочка внутренней упругой мембраны 250.
Как показано на фиг. 4, насос 340A заключен, вместе с, возможно, перезаряжаемыми батареями или аккумуляторами, предназначенными для его электропитания, в корпус (или даже рюкзак) 430, носимый пациентом 440, который, например, присоединен к ремню 435. Канал 330 соединяет насос 340A, заключенный в корпус 430, с протезом левого желудочка, имплантированным в сердце 445 пациента 440. Насос 340A содержит электронный блок обработки данных, который управляет работой насоса, чтобы регулировать расширение и сжатие внутренней упругой мембраны 250 с амплитудой и скоростью, адаптированными для конкретной ППТ пациента 440, которому имплантирован протез согласно настоящему изобретению. При этом работой насоса 340A, и, следовательно, изменением объема промежутка 230 можно управлять аналогично работе кардиостимулятора.
Кардиологическая вспомогательная система, содержащая протез левого желудочка и насос 340A (управляемый электронным блоком обработки данных), может быть использована в качестве полупостоянной меры, т.е. в качестве временной системы поддержания функции, пока новый сердечный орган не будет доступен для трансплантации, или в качестве системы постоянного протеза, как альтернатива замене всего сердечного органа.
Значительным преимуществом, предлагаемым протезами согласно настоящему изобретению, перед решениями предшествующего уровня техники, является то, что пациент продолжает обладать собственным сердечным органом, несмотря на его сниженную и условную функциональность. Также за счет менее инвазивной природы протеза согласно настоящему изобретению это позволяет поддерживать или восстанавливать правильную функциональность других камер сердца, у которых может начать проявляться дисфункция, вызванная дисфункцией левого желудочка. Например, дисфункция левого желудочка со временем может привести к дегенерации и, следовательно, также к патологии левого предсердия; даже корректируя только один левый желудочек можно восстановить соответствующую работу левого предсердия, а также правого желудочка и, следовательно, правого предсердия. Таким образом, протезы согласно настоящему изобретению позволяют восстановить оставшийся орган, работа которого еще не полностью нарушена.
На фиг. 5 показан второй вариант выполнения протеза согласно настоящему изобретению, который также предназначен для левого желудочка, т.е. он является протезом левого желудочка, который отличается от первого варианта осуществления изобретения, показанного на фиг. 2 и 3, конфигурацией внутренней упругой мембраны. В частности, в то время как внутренняя упругая мембрана 250 согласно первому варианту осуществления изобретения обладает непрерывной структурой, внутренняя упругая мембрана 260 согласно второму варианту осуществления изобретения, показанному на фиг. 5, обладает прерывистой ячеистой структурой, образованной множеством упругих пластинок 265, необязательно шестиугольной формы, присоединенных друг к другу вдоль линий 267 упругого соединения.
Другие варианты выполнения протеза согласно настоящему изобретению могут содержать внутреннюю упругую мембрану, которая имеет прерывистую структуру, отличающуюся от показанной на фиг. 5, например, образованную множеством упругих многоугольных пластинок, таких как пятиугольники и/или шестиугольники, соединенных друг с другом вдоль линий упругого соединения.
Предпочтительно, упругие связи 290, присоединяющие внутреннюю поверхность 204 наружной упругой мембраны 200 к наружной поверхности внутренней упругой мембраны 260, зафиксированы на вершинах упругих пластинок 265 (совпадающих с концами линий 267 упругого соединения), образующих ячеистую прерывистую структуру (или, в общем виде, с вершинами упругих многоугольных пластинок, образующих прерывистую структуру).
Необязательно, коэффициент упругости линий 267 упругого соединения больше, чем у упругих пластинок 265; в этом случае минимальный объем, ограниченный внутренней упругой мембраной 260, обязательно больше нуля, что повышает надежность и эффективность использования протезов.
Другие варианты выполнения протеза согласно настоящему изобретению могут содержать наружную упругую мембрану, которая имеет прерывистую структуру, образованную множеством упругих пластинок, соединенных друг с другом, причем такая прерывистая структура может обладать ячеистой конфигурацией, например, с шестигранными пластинками или многоугольными пластинками, такими как пятиугольники и/или шестиугольники. Предпочтительно, упругие связи, присоединяющие внутреннюю поверхность наружной упругой мембраны к наружной поверхности внутренней упругой мембраны, зафиксированы на вершинах упругих пластинок (совпадающих с концами линий упругого соединения), образующих прерывистую структуру наружной упругой мембраны. Кроме того, наружная упругая мембрана может быть перфорирована. Варианты осуществления изобретения с наружной упругой мембраной, обладающей прерывистой структурой, могут содержать внутреннюю упругую мембрану, обладающую непрерывной или прерывистой структурой.
На фиг. 6 показан третий вариант выполнения протеза согласно настоящему изобретению, также предназначенного для левого желудочка, т.е. он является протезом левого желудочка. Вместо гидравлического или пневматического управления объемом, ограниченным промежутком 230 (посредством насоса 340A, который вводит или всасывает текучую среду в него или из него), такой третий вариант выполнения протеза согласно настоящему изобретению содержит наружную упругую мембрану 205 и внутреннюю упругую мембрану 255, каждая из которых содержит множество, необязательно электрически изолированных, электродов, предназначенных для электрической и/или электромагнитной поляризации наружной и внутренней упругих мембран 205 и 255 под управлением электронного блока 345A обработки данных, соединенного с электродами наружной и внутренней упругих мембран 205 и 255 посредством соответствующих кабелей 206 и 256 управления.
Изменением объема промежутка 230 управляет электрическая и/или электромагнитная полярность наружной и внутренней упругих мембран 205 и 255. Во время систолы желудочков (показанной на фиг. 6a) электронный блок 345A обработки данных управляет электродами так, чтобы наружная и внутренняя упругие мембраны 205 и 255 обладали одной и той же электрической и/или электромагнитной полярностью, поэтому они отталкиваются друг от друга и увеличивают объем промежутка 230, вызывая выброс систолического ударного объема в аорту 100, аналогично тому, как это описано со ссылкой на фиг. 3a. При систоле предсердий (показана на фиг. 6b), электронный блок 345A обработки данных управляет электродами так, чтобы наружная и внутренняя упругие мембраны 205 и 255 обладали противоположной электрической и/или электромагнитной полярностью, поэтому они притягиваются друг к другу и уменьшают объем промежутка 230 (возможно, до нуля), способствуя кровотоку из левого предсердия 20 внутрь внутренней упругой мембраны 255, аналогично тому, как это описано со ссылкой на фиг. 3b.
При этом промежуток 230 может быть заполнен жидкостью (например, гемосовместимым раствором) и сообщен по текучей среде по меньшей мере с одним упругим пакетом переменного объема (не показан на чертежах), действующим как емкость для жидкости, которая может быть расположена внутри миокарда (например, вблизи аортального клапана 80 и/или вблизи митрального клапана 70) или вне миокарда; во время систолы предсердий жидкость вытесняется из промежутка 230 в упругий пакет (который увеличивается в объеме), а во время систолы желудочков жидкость вытесняется из упругого пакета (который уменьшается в объеме) в промежуток 230. В качестве альтернативы или дополнительно к жидкости промежуток 230 может быть заполнен газом (например, гелием), который, поскольку он сжимается, позволяет изменять давление от высокого значения во время систолы предсердий до низкого во время систолы желудочков без необходимости того, чтобы промежуток 230 сообщался по текучей среде с упругим пакетом переменного объема (который в этом случае является необязательным).
Электронный блок 345A обработки данных может управлять электрической и/или электромагнитной полярностью каждой из наружной и внутренней упругих мембран 205 и 255 так, чтобы она менялась во времени и по амплитуде в зависимости от конкретной области рассматриваемой (наружной или внутренней) упругой мембраны (205 или 255). В частности, электронный блок 345A обработки данных позволяет управлять электродами наружной упругой мембраны 205 одним и тем же управляющим сигналом (также меняющимся во времени), или, если электроды разделены на разные группы (например, основная группа, состоящая из одного или более электродов, расположенных в основании наружной упругой мембраны 205, группа промежуточной стенки, содержащая один или более электродов, расположенных в промежуточной стенке наружной упругой мембраны 205, и группа верхушки желудочка, содержащая один или более электродов, расположенных в верхушке желудочка наружной упругой мембраны 205), каждая из них управляется соответствующим управляющим сигналом (также меняющимся по времени), или путем передачи соответствующего управляющего сигнала (также меняющегося по времени) на каждый из электродов (причем, возможно, два или более электродов могут принимать соответствующие управляющие сигналы, идентичные друг другу). Аналогичным образом, электронный блок 345A обработки данных также может управлять электродами внутренней упругой мембраны 255 в аналогичных режимах, т.е. с одним и тем же управляющим сигналом (также меняющимся во времени) или с соответствующими управляющими сигналами (также меняющимися во времени) для различных групп, на которые поделены электроды, или с соответствующими сигналами управления (также меняющимся во времени) для каждого из электродов. При этом режим управления электродами наружной упругой мембраны 205 может быть тем же самым или может отличаться от режима управления электродами внутренней упругой мембраны 255.
Подача питания электронного блока 345A обработки данных, который управляет функционированием протеза, осуществляется посредством, необязательно, перезаряжаемых батарей (или аккумуляторов), причем они могут быть заключены во внешний корпус (или даже рюкзак), носимый пациентом (аналогично показанному на фиг. 4). В альтернативном варианте, показанном на фиг. 7, электронный блок 345A обработки данных вместе с батареями для электропитания может быть имплантирован подкожно в тело пациента 440, в сердце 445 которого имплантирован протез левого желудочка, аналогично обычному кардиостимулятору. При этом электродами и, следовательно, полярностью, наружной и внутренней упругих мембран 205 и 255, а также изменением полученного объема промежутка 230 можно управлять аналогично тому, как это происходит для кардиостимулятора. Также, электронный блок 345A обработки данных управляет функционированием протеза, чтобы регулировать расширение и сжатие внутренней упругой мембраны 255 с амплитудой и скоростью, адаптированными для конкретной ППТ пациента 440, которому имплантированы протезы согласно настоящему изобретению, например, путем регулировки интенсивности электрической и/или электромагнитной полярности, чтобы вызывать переменное притяжение и отталкивание между наружной и внутренней упругими мембранами 205 и 255.
Кардиологическая вспомогательная система, включающая в себя протез левого желудочка, показанный на фиг. 6, и электронный блок 345A обработки данных, управляющий его работой, также может быть использована в качестве полупостоянной меры или в качестве системы постоянного протеза.
Протез левого желудочка, показанный на фиг. 6, дополнительно содержит искусственный аортальный клапан 530, неразъемно соединенный с аортальным краем 285, ограничивающим аортальное отверстие 280 протеза. Такой искусственный аортальный клапан 530 позволяет преодолеть проблемы, вызванные непригодным или патологическим собственным аортальным клапаном. В этом случае протезы, предпочтительно, имплантируются посредством хирургической операции на сердце, путем открытия собственного аортального клапана или, в альтернативном варианте, путем минимально инвазивного чрескожного пути или не чрезмерно инвазивного трансапикального или чресключичного пути. После имплантации искусственный аортальный клапан 530 толкает собственный клапан, удерживая его открытым, тем самым, открытие и закрытие аортального отверстия 280 протеза зависит от открытия (как показано на фиг. 6a, где открытие искусственного аортального клапана 530 схематично представлено поднятыми краями 535) или закрытия (показано на фиг. 6b) искусственного аортального клапана 530.
В частности, искусственный аортальный клапан 530, неразъемно присоединенный к аортальному краю 285, ограничивающему аортальное отверстие 280 протеза согласно настоящему изобретению, обладает улучшенным позиционированием и большей стабильностью по сравнению с искусственными аортальными клапанами предшествующего уровня техники. В частности, работой искусственного аортального клапана 530 также можно управлять с помощью особых электродов, распределенных на компонентах самого клапана, которые предназначены для того, чтобы открывать и закрывать клапан посредством электрической и/или электромагнитной поляризации таких компонентов, причем этими электродами, в свою очередь, управляет электронный блок 345A обработки данных. Кроме того, искусственный аортальный клапан 530 позволяет избежать проблем остаточной регургитации после имплантации, которая возникает с обычным чрескожным имплантатом искусственного аортального клапана, также известной, как способ TAVI (чрескатетерная имплантация аортального клапана).
Альтернативно или в сочетании с искусственным аортальным клапаном 530 могут быть предусмотрены другие варианты выполнения протеза согласно настоящему изобретению с искусственным митральным клапаном. Также могут быть предусмотрены варианты выполнения протеза согласно настоящему изобретению с искусственными клапанами, в которых объемом, ограниченным промежутком 230, управляет насос, вводящий или перекачивающий текучую среду в него или из него.
Следует отметить, что в других вариантах выполнения протеза согласно настоящему изобретению может использоваться как гидравлическое или пневматическое управление, как показано на фиг. 3 и 4, так и электрическое и/или электромагнитное управление, как показано на фиг. 6 и 7, в которых два типа управления используются совместно при изменении объема, ограниченного промежутком 230; в частности, в случае, когда при гидравлическом управлении используется жидкость (например, гемосовместимый раствор), насос 340A, предпочтительно, может заменять по меньшей мере один упругий пакет переменного объема (расположенный внутри или снаружи относительно миокарда) с электрическим и/или электромагнитным управлением. Кроме того, может использоваться одиночный электронный блок обработки данных, управляющий как насосом 340A, так и электродами наружной и внутренней упругих мембран 205 и 255.
На фиг. 8 показан четвертый вариант выполнения протеза согласно настоящему изобретению, также предназначенный для левого желудочка, т.е. он является протезом левого желудочка, который предназначен для пациентов, миокард которых обладает патологическими характеристиками, не позволяющими использовать внутреннюю стенку 45 левого желудочка достаточно эффективным и надежным образом, тем самым, наружная упругая мембрана 200, жестко соединенная с внутренней стенкой 45 левого желудочка, не способна функционировать достаточно эффективно и надежно в качестве опоры для внутренней упругой мембраны 250. В качестве примера, и не подразумевая ограничений этим примером, это случай пациентов с дилатационной кардиомиопатией.
Протез левого желудочка, показанный на фиг. 8, отличается от протезов, показанных на фиг. 6–7, тем, что он дополнительно содержит промежуточную упругую мембрану 225, которая расположена между наружной упругой мембраной 205 и внутренней упругой мембраной 255. Промежуточная упругая мембрана 225 обладает формой, аналогичной форме наружной упругой мембраны 205 и внутренней упругой мембраны 255, таким образом, она имеет первое отверстие и второе отверстие, края которых неразъемно присоединены к краям первых отверстий и вторых отверстий соответственно наружной и внутренней упругих мембран 205 и 255, чтобы сформировать аортальный край (выполненный с возможностью окружения собственного аортального клапана 80 и пришивания к нему), ограничивающий аортальное отверстие протеза левого желудочка, и митральный край (выполненный с возможностью окружения собственного митрального клапана 70 и пришивания к нему), ограничивающий митральное отверстие протеза левого желудочка. Также в этом случае, предпочтительно, края первых отверстий наружной, промежуточной и внутренней упругих мембран 205, 225 и 255 соединены электросваркой друг с другом для формирования аортального края; аналогичным образом, края вторых отверстий наружной, промежуточной и внутренней упругих мембран 205, 225 и 255 соединены электросваркой друг с другом для формирования митрального края.
Аналогично наружной и внутренней упругим мембранам 205 и 255, сходная промежуточная упругая мембрана 225 содержит множество, необязательно электрически изолированных, электродов, предназначенных для электрической и/или электромагнитной поляризации промежуточной упругой мембраны 225 под управлением электронного блока 345B обработки данных, также управляющего электрической и/или электромагнитной поляризацией наружной и внутренней упругих мембран 205 и 255, при этом указанный блок соединен с электродами наружной, промежуточной и внутренней упругих мембран 205, 225 и 255 посредством соответствующих кабелей 206, 226 и 256 управления.
Промежуточная упругая мембрана 225 упруго присоединена к наружной упругой мембране 205 и к внутренней упругой мембране 255 посредством множества наружных упругих связей 290A и множества внутренних упругих связей 290B соответственно. Каждая из наружных упругих связей 290A имеет два конца, неразъемно присоединенных к внутренней поверхности наружной упругой мембраны 205 и к наружной поверхности (т.е. поверхности, обращенной к наружной упругой мембране 205) промежуточной упругой мембраны 225 соответственно; аналогичным образом, каждая из внутренних упругих связей 290B имеет два конца, неразъемно присоединенных к наружной поверхности внутренней упругой мембраны 255 и к внутренней поверхности (т.е. поверхности, обращенной к внутренней упругой мембране 205) промежуточной упругой мембраны 225 соответственно. Каждая из внутренних упругих связей 290B выполнена с возможностью упругого удлинения, когда она подвергается натяжению, вызывающему перемещение ее концов друг от друга, начиная из состояния без нагрузки; предпочтительно, также каждая из наружных упругих связей 290A выполнена с возможностью упругого удлинения, когда она подвергается напряжению, которое вызывает перемещение ее концов друг от друга, начиная из состояния без нагрузки. Необязательно, коэффициент упругости наружных упругих связей 290A больше коэффициента упругости промежуточной упругой мембраны 225 и коэффициента упругости наружной упругой мембраны 205; необязательно, коэффициент упругости наружных упругих связей 290A изменяется в зависимости от области промежуточной упругой мембраны 225, к которой они присоединены.
Как указано, наружная и внутренняя упругие мембраны 205 и 255 аналогичны мембранам варианта осуществления изобретения, показанного на фиг. 6–7, поэтому наружная поверхность наружной упругой мембраны 205 содержит множество обычных фиксаторов 210, которые выполнены с возможностью зацепления за внутреннюю стенку 45 левого желудочка за счет прокалывания ткани левого желудочка, что позволяет надежно имплантировать наружную упругую мембрану 205.
Также промежуточная упругая мембрана 225, как и наружная и внутренняя упругие мембраны 205 и 255, предпочтительно, обладает морфологией, которая приблизительно соответствует морфологии внутренней стенки 45 левого желудочка (в которую предполагается имплантировать протезы), необязательно, включающей два выреза, предназначенных для приема передней и задней папиллярных мышц и сухожильных хорд левого желудочка, присоединенных к митральному клапану 70, и может быть изготовлена разного размера, адаптированного к конкретным объемам левого желудочка разных пациентов, связанным с ППТ пациентов. В любом случае аналогично двум наружной и внутренней упругим мембранам 205 и 255, сходная промежуточная упругая мембрана 225, необязательно, должна обладать морфологией, точно соответствующей морфологии внутренней стенки 45 левого желудочка (в которую предполагается имплантировать протезы), поскольку ее упругость позволяет компенсировать любые морфологические различия.
Кроме того, промежуточная упругая мембрана 225, наружная и внутренняя упругие мембраны 205 и 255, а также наружные упругие связи 290A и внутренние упругие связи 290B изготовлены из биологически совместимых упругих материалов, необязательно биологически совместимых упругих полимерных материалов, более необязательно политетрафторэтилена (также известного, как пористый ПТФЭ).
Наружная и промежуточная упругие мембраны 205 и 225, упруго соединенные друг с другом посредством множества наружных упругих связей 290A, ограничивают замкнутый наружный промежуток 230A между ними, обладающий объемом, выполненным с возможностью упругого изменения (даже если это несущественная особенность изобретения). Промежуточная и внутренняя упругие мембраны 225 и 255, упруго присоединенные друг к другу посредством множества внутренних упругих связей 290B, ограничивают замкнутый внутренний промежуток 230B между ними с объемом, который может упруго изменяться, как подробно описано далее.
В частности, базовая опорная структура упругой мембраны состоит из наружной упругой мембраны 205, промежуточной упругой мембраны 225 и нескольких наружных упругих связей 290A. Кроме того, внутренний промежуток 230B функционирует как первичный промежуток, наружный промежуток 230A функционирует как вторичный промежуток, множество внутренних упругих связей 290B функционируют как множество первичных изменяемых соединительных элементов, а множество наружных упругих связей 290A функционируют как множество вторичных изменяемых соединительных элементов.
Промежуточная упругая мембрана 225 может обладать как сплошной, так и прерывистой структурой, образованной множеством упругих пластинок, соединенных друг с другом, причем такая прерывистая структура может обладать ячеистой формой, например, с шестиугольными пластинками, или формой многоугольной пластинки, такой как пятиугольники и/или шестиугольники. Предпочтительно, упругие связи, присоединяющие внутреннюю поверхность наружной упругой мембраны к наружной поверхности промежуточной упругой мембраны, и упругие связи, присоединяющие наружную поверхность внутренней упругой мембраны к внутренней поверхности промежуточной упругой мембраны, зафиксированы на вершинах упругих пластинок (совпадающих с концами линий упругого соединения), образующих прерывистую структуру промежуточной упругой мембраны. Варианты осуществления изобретения с промежуточной упругой мембраной, обладающей прерывистой структурой, могут содержать внутреннюю упругую мембрану, обладающую либо непрерывной, либо прерывистой структурой, и наружную упругую мембрану либо с непрерывной, либо с прерывистой структурой.
Также в четвертом варианте выполнения протеза, показанном на фиг. 8, аналогично варианту, показанному на фиг. 6, электронный блок 345B обработки данных управляет электрической и/или электромагнитной поляризацией всеми и каждой из наружной, промежуточной и внутренней упругих мембран 205, 225 и 255, чтобы изменять объем внутреннего промежутка 230B. В частности, промежуточная упругая мембрана 225 обладает коэффициентом упругости, который не больше (т.е. меньше или равен), необязательно меньше (т.е. является менее упругой), коэффициента упругости наружной упругой мембраны 205. Это позволяет использовать промежуточную упругую мембрану 225 в качестве опоры для внутренней упругой мембраны 255, способствуя ее смещению к центру левого желудочка и в противоположном направлении к внутренней стенке 45 левого желудочка, обеспечивая надежное, быстрое и эффективное общее изменение внутреннего объема, ограниченного внутренней упругой мембраной 255. В частности, в отношении компоновки (необязательно, в состоянии покоя), которая предполагается по существу в качестве статического (т.е. постоянного) базового положения, промежуточная упругая мембрана 225, необязательно, выполнена с возможностью только незначительного расширения относительно амплитуды расширения наружной и внутренней упругих мембран 205 и 255 и по существу не сжимается вообще.
При этом электронный блок 345B обработки данных управляет электрической и/или электромагнитной поляризацией всех и каждой из наружной, промежуточной и внутренней упругих мембран 205, 225 и 255 так, что промежуточная упругая мембрана 225 остается по существу в статичном (т.е. постоянном) положении, которое, по сути, образует физиологический теледиастолический объем желудочка пациента, так что внутренняя упругая мембрана 255 перемещается относительно промежуточной упругой мембраны 225, циклически изменяя объем внутреннего промежутка 230B. В частности, при систоле предсердий (показана на фиг. 8b), электронный блок 345B обработки данных управляет электрической и/или электромагнитной поляризацией всех и каждой из наружной, промежуточной и внутренней упругих мембран 205, 225 и 255, чтобы внутренняя и промежуточная упругие мембраны 255 и 225 притягивались друг к другу и уменьшали объем внутреннего промежутка 230B (необязательно) до нуля, способствуя кровотоку из левого предсердия 20 во внутреннюю упругую мембрану 255 аналогично тому, как это описано со ссылкой на фиг. 3b. При систоле желудочков (показана на фиг. 8a) электронный блок 345B обработки данных управляет электрической и/или электромагнитной поляризацией всех и каждой из наружной, промежуточной и внутренней упругих мембран 205, 225 и 255, чтобы промежуточная и внутренняя упругие мембраны 225 и 255 отталкивались друг от друга и увеличивали объем внутреннего промежутка 230B, вызывая выброс систолического объема в аорту 100 аналогично тому, как это описано со ссылкой на фиг. 3a.
В первом режиме работы электронный блок 345B обработки данных сохраняет поляризацию промежуточной упругой мембраны 225 постоянной и динамически меняет поляризацию наружной упругой мембраны 205 и внутренней упругой мембраны 255. В частности, во время сердечного цикла электронный блок 345B обработки данных также динамически меняет поляризацию наружной упругой мембраны 205 для предотвращения изменения полярности внутренней упругой мембраны 255, чтобы не вызывать смещения промежуточной упругой мембраны 225 относительно по существу статического (т.е. постоянного) базового положения, которое, по сути, определяет физиологический теледиастолический объем желудочка пациента. Другими словами, в таком первом режиме работы объем наружного промежутка 230A остается по существу постоянным.
В других режимах работы протеза, показанного на фиг. 8, электронный блок 345B обработки данных может также динамически меняет поляризацию промежуточной упругой мембраны 225, вместо ее сохранения постоянной. Даже в этих других режимах работы объем наружного промежутка 230A может оставаться по существу постоянным.
Кроме того, в других режимах работы протеза, показанного на фиг. 8, электронный блок 345B обработки данных может управлять электрической и/или электромагнитной поляризацией всех и каждой из наружной, промежуточной и внутренней упругих мембран 205, 225 и 255, чтобы также менять объем наружного промежутка 230A, помимо объема внутреннего промежутка 230B.
Аналогично промежутку 230 протеза, показанного на фиг. 6, внутренний промежуток 230B может быть заполнен жидкостью (например, гемосовместимым раствором) и сообщаться по текучей среде по меньшей мере с одним упругим пакетом переменного объема (не показан на чертежах), функционирующего в качестве емкости для жидкости, которая может быть расположена внутри миокарда (например, вблизи аортального клапана 80 и/или около митрального клапана 70) или вне миокарда; при систоле предсердий жидкость перемещается из внутреннего промежутка 230B в упругий пакет (который увеличивается в объеме), а во время систолы желудочков жидкость перемещается из упругого пакета (который уменьшается в объеме) во внутренний промежуток 230B. Альтернативно или в сочетании с жидкостью, внутренний промежуток 230B может быть заполнен газом (например, гелием), у которого, поскольку он является сжимаемым, может меняться давление от высокого значения во время систолы предсердий до низкого значения во время систолы желудочков, без необходимости сообщения внутреннего промежутка 230B по текучей среде с упругим пакетом переменного объема (который в этом случае является необязательным).
В режимах работы, при которых объем наружного промежутка 230A остается по существу постоянным, он может быть заполнен заранее определенным количеством жидкости (например, гемосовместимым раствором) или газом (например, гелием).
В других режимах работы протеза, показанного на фиг. 8, в которых объем наружного промежутка 230A также меняется, он может быть заполнен жидкостью (например, гемосовместимым раствором) и сообщаться по текучей среде по меньшей мере с одним упругим пакетом переменного объема (не показан на чертежах), расположенным внутри миокарда (например, около аортального клапана 80 и/или около митрального клапана 70) или вне миокарда, возможно, совпадая по меньшей мере с одним упругим пакетом переменного объема, с которым внутренний промежуток 230B сообщается по текучей среде. Альтернативно или в сочетании с жидкостью, наружный промежуток 230A может быть заполнен газом (например, гелием), который, поскольку он является сжимаемым, может меняться в объеме без необходимости сообщения наружного промежутка 230A по текучей среде с упругим пакетом переменного объема (который в этом случае является необязательным).
Пятый вариант выполнения протеза согласно настоящему изобретению, также предназначенный для левого желудочка, отличается от показанного на фиг. 8 тем, что вместо электрического и/или электромагнитного управления объемом внутреннего промежутка 230B (и, возможно, объемом наружного промежутка 230A) посредством поляризации наружной, промежуточной и внутренней упругих мембран 205, 225 и 255, объем внутреннего промежутка 230B (и, возможно, объем наружного промежутка 230A) меняется с помощью гидравлического или пневматического управления посредством насоса (или двух насосов), который вводит или перекачивает текучую среду в или из внутреннего промежутка 230B (и, возможно, в наружный промежуток 230A), аналогично тому, как это описано для протезов, показанных на фиг. 2–5. В этом случае протезы могут быть снабжены уже перед имплантацией (по меньшей мере) одним участком канала для доступа к внутреннему промежутку 230B, который соединяет (по меньшей мере) одно соответствующее отверстие для доступа, имеющееся на наружной упругой мембране 205, с внутренним промежутком 230B; на этапе имплантации хирург пришивает к (необязательно, рентгеноконтрастному) краю такого отверстия для доступа соответствующий канал, который вместе с участком канала соединяет внешний насос с внутренним промежутком 230B, изменениями объема которого управляет насос.
Следует отметить, что в других вариантах выполнения протезов согласно настоящему изобретению, предназначенных для левого желудочка и содержащих наружную, промежуточную и внутреннюю упругие мембраны 205, 225 и 255, могут использоваться и гидравлическое или пневматическое управление, и электрическое и/или электромагнитное управление, причем два типа управления используются совместно при изменении объема, ограниченного внутренним промежутком 230B (и, возможно, объема, образованного наружным промежутком 230A).
Другие варианты выполнения протеза согласно настоящему изобретению предназначены для одной из трех других камер сердца, т.е. левого предсердия 20, правого желудочка 30 и правого предсердия 10, и аналогичны протезам, показанным на фиг. 2–8; а именно:
- протезы, предназначенные для одного из левого желудочка 40 и правого желудочка 30, имеют первое отверстие и второе отверстие, предназначенные для того, чтобы они окружали два собственных клапана камеры сердца, для которых они предназначены, и были пришиты к ним; необязательно, форма боковой поверхности упругих мембран протеза может включать в себя три выреза, без фиксаторов, предназначенных для приема папиллярных мышц правого желудочка, присоединенных к трикуспидальному клапану 50, чтобы протезы не соприкасались с папиллярными мышцами;
- протезы, предназначенные для левого предсердия 20, имеют первое отверстие, предназначенное для того, чтобы оно окружало собственный митральный клапан 70 и было пришито к нему, и по меньшей мере одно второе отверстие, предназначенное для пришивания к устью по меньшей мере одной соответствующей легочной вены 130;
- протезы, предназначенные для правого предсердия 10, имеют первое отверстие, предназначенное для того, чтобы оно окружало собственный трикуспидальный клапан 50 и было пришито к нему, и одно или более вторых отверстий, предназначенных для пришивания к верхней полой вене 120 и/или нижней полой вене 125;
- протезы содержат две или три мембраны, упруго присоединенные друг к другу посредством упругих связей, таким образом, они содержат наружную упругую мембрану и внутреннюю упругую мембрану, которые ограничивают замкнутый промежуток между ними с объемом, который может упруго изменяться, или промежуточную упругую мембрану между наружной упругой мембраной и внутренней упругой мембраной, которые ограничивают с промежуточной упругой мембраной замкнутый наружный промежуток и замкнутый внутренний промежуток с объемом, который может упруго изменяться, при этом наружная упругая мембрана выполнена с возможностью зацепления за внутреннюю стенку камеры сердца посредством фиксаторов;
- протезы содержат по меньшей мере один насос, предназначенный для осуществления гидравлического или пневматического управления, и/или электронный блок обработки данных, предназначенный для управления электрической и/или электромагнитной поляризацией упругих мембран, которые содержат электроды, чтобы управлять изменением объема промежутков переменного объема в соответствующих сердечных циклах и фазах сердечного цикла;
- протезы могут содержать по меньшей мере один искусственный клапан, аналогично протезу левого желудочка, показанному на фиг. 6.
В частности, коэффициент упругости упругих мембран протезов также может быть различен в зависимости от конкретной камеры сердца, для которой предназначен каждый протез.
Аналогично протезам для левого желудочка, показанным на фиг. 2–8, протезы согласно настоящему изобретению, которые предназначены для одной из трех других камер сердца, т.е. левого предсердия 20, правого желудочка 30 и правого предсердия 10, также могут быть имплантированы посредством хирургической операции на сердце или, в альтернативном варианте, через минимально инвазивный чрескожный путь или малоинвазивный трансапикальный или чресключичный путь, посредством конкретного доступа для конкретной камеры сердца. В качестве примера, и не подразумевая ограничений им, протез согласно настоящему изобретению, предназначенный для правого желудочка, т.е. являющийся протезом правого желудочка, может быть имплантирован при хирургической операции на сердце путем открытия трикуспидального клапана или легочного клапана.
Система протезов камер сердца согласно настоящему изобретению также может быть предназначена для более чем одной камеры сердца.
В качестве примера на фиг. 9 показан первый вариант выполнения системы протезов камер сердца для левого желудочка 40 и левого предсердия 20. В частности, система содержит протез левого желудочка, аналогичный показанному на фиг. 3, предназначенный для имплантации в левый желудочек 40, и протез левого предсердия, также аналогичный протезу, показанному на фиг. 3, предназначенный для имплантации в левое предсердие 20. В частности, протез левого предсердия системы, показанной на фиг. 9, содержит наружную упругую мембрану 600 и внутреннюю упругую мембрану 650, упруго соединенные друг с другом посредством нескольких упругих связей 290, которые ограничивают замкнутый промежуток 630 между ними с объемом, который может упруго изменяться, при этом наружная упругая мембрана 650 выполнена с возможностью зацепления за внутреннюю стенку 25 левого предсердия 20 посредством множества фиксаторов 210. Наружная упругая мембрана 600 и внутренняя упругая мембрана 650 протеза левого предсердия имеют первое отверстие и второе отверстие, края которых неразъемно соединены друг с другом для формирования, соответственно, митрального края 675, ограничивающего митральное отверстие, который предназначен для того, чтобы он окружал собственный митральный клапан 70 и был пришит к нему, и край 685 легочных вен, ограничивающий отверстие выпускного устья легочных вен 130, который предназначен для того, чтобы он окружал выпускные устья легочных вен 130 и был пришит к ним. В других вариантах выполнения протеза левого предсердия может быть два или более отверстий, края которых неразъемно соединены друг с другом для формирования двух или более краев легочных вен, ограничивающих одно или более соответствующих отверстий для выпускных устий легочных вен 130, при этом каждый из них предназначен для того, чтобы он окружал выпускное устье соответствующей легочной вены 130 и был пришит к нему.
Аналогично протезу левого желудочка (фиг. 3), промежуток 630 предназначен для приема текучей среды, а именно жидкости, такой как гемосовместимый раствор, например стерильный физиологический раствор, или газа, например гелия, в изменяемом количестве для динамического изменения объема промежутка 630 и, следовательно, изменения упруго изменяемого объема, ограниченного внутренней поверхностью 654 внутренней упругой мембраны 650. Для этого обеспечивается доступ к промежутку 630 (по меньшей мере) через одно отверстие для доступа, выполненное в наружной упругой мембране 600, причем после имплантации протеза в левое предсердие к этому отверстию пришивается канал 360, при этом канал 360 присоединяет промежуток 630 к внешнему (гидравлическому или пневматическому) насосу 340B, который дополнительно присоединен к промежутку 230 протеза левого желудочка посредством канала 330; в альтернативном варианте промежуток 630 может быть присоединен к внешнему насосу, отдельному от насоса, к которому присоединен промежуток 230 протеза левого желудочка. Необязательно, края этого (по меньшей мере одного) отверстия для доступа могут быть изготовлены из рентгеноконтрастного материала, и/или хирург может выполнить отверстие для доступа в любом месте наружной упругой мембраны 600, аналогично тому, как это показано на фиг. 3 для протеза левого желудочка.
В частности, для протеза левого предсердия, показанного на фиг. 9, базовая опорная упругая мембранная структура состоит из наружной упругой мембраны 600, при этом митральный край 675 функционирует в качестве выпускного края, собственный митральный клапан 70 функционирует как собственный выпускной клапан, край 685 легочных вен функционирует как впускной край, выпускные устья легочных вен 130 функционируют как впускное отверстие камеры сердца, промежуток 630 функционирует как первичный промежуток, а множество упругих связей 290 функционируют как множество первичных изменяемых соединительных элементов.
Другие варианты выполнения системы протезов камер сердца, предназначенных для левого желудочка 40 и левого предсердия 20, в альтернативном или дополнительном варианте могут обладать гидравлическим или пневматическим управлением посредством (по меньшей мере) одного насоса 340B, электрическим и/или электромагнитным управлением, осуществляемым электронным блоком обработки данных, предназначенным для управления электрической и/или электромагнитной поляризацией упругих мембран, которые содержат электроды, протезов левого желудочка 40 и левого предсердия 20 аналогично тому, как это показано для протезов на фиг. 6. В этом случае промежутки 230 и 630 могут быть заполнены жидкостью (например, гемосовместимым раствором) и могут сообщаться по текучей среде друг с другом (вместо или совместно по меньшей мере с одним упругим пакетом переменного объема) через передающий канал: во время систолы предсердий электрическое и/или электромагнитное управление вызывает увеличение объема промежутка 630 и уменьшение объема промежутка 230, перемещая жидкость из последнего в первый; во время систолы желудочков электрическое и/или электромагнитное управление вызывает уменьшение объема промежутка 630 и увеличение объема промежутка 230, перемещая жидкость из первого во второй. Необязательно, такой передающий канал между промежутками 230 и 630 может быть пришит хирургом во время имплантации к протезам левого желудочка 40 и левого предсердия 20 в соответствии с промежутками 230 и 630 после заполнения по меньшей мере одного из них жидкостью.
Другие варианты выполнения системы протезов камер сердца также могут включать в себя один или более искусственных клапанов сердца. В качестве примера, и не подразумевая ограничения им, на фиг. 10 показан второй вариант выполнения системы протезов камер сердца, предназначенных для левого желудочка 40 и левого предсердия 20, который отличается от показанного на фиг. 9 тем, что протез левого предсердия содержит искусственный митральный клапан 540, неразъемно присоединенный к митральному краю 675, ограничивающему митральное отверстие протеза. Такой искусственный митральный клапан 540 позволяет преодолеть проблемы, вызванные нарушенным или паталогическим собственным митральным клапаном, тем самым, открытие или закрытие митрального отверстия протеза зависит от открытия (как показано на фиг. 10b, на которой открытие искусственного митрального клапана 540 схематично представлено приподнятыми краями 545) или закрытия (как показано на фиг. 10a) искусственного митрального клапана 540. Следует отметить, что два протеза, предназначенные для левого желудочка 40 и левого предсердия 20, могут быть присоединены друг к другу согласно соответствующим митральным краям 275 и 675 и что в этом случае система протезов камер сердца также может быть имплантирована без пришивания митрального края 275 и/или митрального края 675 к собственному митральному клапану 70.
На фиг. 11 показан третий вариант выполнения системы протезов камер сердца, предназначенных для левого желудочка 40, правого желудочка 30 и правого предсердия 10. В частности, система содержит протез левого желудочка и протез левого предсердия, аналогичные показанным на фиг. 9, и протез правого желудочка, аналогичный протезам, показанным на фиг. 3, предназначенным для имплантации в правый желудочек 30. В частности, протез правого желудочка системы, показанной на фиг. 11, включает в себя наружную упругую мембрану 700 и внутреннюю упругую мембрану 750, упруго присоединенные друг к другу посредством множества упругих связей 290, которые ограничивают замкнутый промежуток 730 между ними с объемом, выполненным с возможностью упругого изменения, при этом наружная упругая мембрана 700 предназначена для зацепления за внутреннюю стенку 35 правого желудочка 30 посредством множества фиксаторов 210. Наружная упругая мембрана 700 и внутренняя упругая мембрана 750 протеза правого желудочка имеют первое отверстие и второе отверстие, края которых неразъемно соединены друг с другом для формирования, соответственно, края 785 легочного клапана, который ограничивает отверстие легочного клапана и который предназначен для того, чтобы он окружал собственный легочный клапан 60 и был пришит к нему, и края 775 трикуспидального клапана, который ограничивает отверстие трикуспидального клапана и который предназначен для того, чтобы он окружал собственный трикуспидальный клапан 50 и был пришит к нему.
В частности, для протеза правого желудочка, показанного на фиг. 11, базовая опорная упругая мембранная структура состоит из наружной упругой мембраны 700, при этом край 785 легочного клапана функционирует как выпускной край, собственный легочный клапан 60 функционирует как собственный выпускной клапан, край 775 трикуспидального клапана функционирует как впускной край, трикуспидальный клапан функционирует как собственный впускной клапан, из которого состоит по меньшей мере одно впускное отверстие камеры сердца, промежуток 730 функционирует как первичный промежуток, а множество упругих связей 290 функционируют как множество первичных изменяемых соединительных элементов.
Аналогично показанному для протеза левого желудочка (фиг. 3), промежуток 730 предназначен для приема текучей среды, а именно жидкости, такой как гемосовместимый раствор, например стерильный физиологический раствор, или газа, например гелия, в переменном количестве для динамического изменения объема промежутка 730 и, таким образом, изменения упруго изменяемого объема, ограниченного внутренней поверхностью 754 внутренней упругой мембраны 750. Для этого доступ к промежутку 730 осуществляется через (по меньшей мере) одно отверстие для доступа, выполненное в наружной упругой мембране 700, причем после имплантации протеза в правое предсердие к этому отверстию пришивается канал 370, при этом канал 370 присоединяет промежуток 730 к внешнему (гидравлическому или пневматическому) насосу 340C. Необязательно, края этого (по меньшей мере одного) отверстия для доступа могут быть изготовлены из рентгеноконтрастного материала, и/или хирург может выполнить отверстие для доступа в любом месте наружной упругой мембраны 700 аналогично тому, как это описано выше для протеза левого желудочка, показанного на фиг. 3.
Также в этом случае, в альтернативном варианте или в сочетании с гидравлическим или пневматическим управлением, система протезов, показанная на фиг. 11, может обладать электрическим и/или электромагнитным управлением, осуществляемым электронным блоком обработки данных, предназначенным для управления электрической и/или электромагнитной поляризацией внутренней и наружной упругих мембран 750 и 700, которые содержат электроды. В этом случае промежуток 730 может быть заполнен жидкостью (например, гемосовместимым раствором) и может сообщаться по текучей среде (по меньшей мере) с одним упругим пакетом изменяемого объема: во время систолы желудочков электрическое и/или электромагнитное управление увеличивает объема промежутка 730, перемещая жидкость из упругого пакета в этот промежуток 730; во время систолы предсердий электрическое и/или электромагнитное управление уменьшает объем промежутка 730, перемещая жидкость из последнего в упругий пакет.
Кроме того, система протезов, показанная на фиг. 11, также может содержать один или более искусственных клапанов сердца.
На фиг. 12 показан четвертый вариант выполнения системы протезов камер сердца, предназначенных для левого желудочка 40, левого предсердия 20, правого желудочка 30 и правого предсердия 10. В частности, система содержит протез правого предсердия и протез левого предсердия, аналогичные показанным на фиг. 9, а также протез правого желудочка, аналогичный протезам, показанным на фиг. 11, и протез правого предсердия, предназначенный для имплантации в правое предсердие 10. В частности, протез правого предсердия системы, показанной на фиг. 12, содержит наружную упругую мембрану 800 и внутреннюю упругую мембрану 850, упруго присоединенные друг к другу посредством множества упругих связей 290, которые ограничивают замкнутый промежуток 830 между ними с объемом, выполненным с возможностью упругого изменения, при этом наружная упругая мембрана 800 выполнена с возможностью зацепления за внутреннюю стенку 15 предсердия 10 посредством множества фиксаторов 210. Наружная упругая мембрана 800 и внутренняя упругая мембрана 850 протеза правого предсердия имеют первое отверстие и два вторых отверстия, края которых неразъемно присоединены друг к другу для формирования, соответственно, края 885 трикуспидального клапана, который ограничивает отверстие трикуспидального клапана и который предназначен для того, чтобы он окружал собственный трикуспидальный клапан 50 и был пришит к нему, края 875A верхней полой вены, который ограничивает отверстие верхней полой вены и который предназначен для того, чтобы он окружал выпускное устье верхней полой вены 120 и был пришит к нему, и края 875B нижней полой вены, который ограничивает отверстие нижней полой вены и который предназначен для того, чтобы он окружал выпускное устье нижней полой вены 125 и был пришит к нему.
В частности, для протеза правого предсердия, показанного на фиг. 12, базовая опорная упругая структура состоит из наружной упругой мембраны 800, при этом край 885 трикуспидального клапана функционирует как выпускной край, собственный трикуспидальный клапан 50 функционирует как собственный выпускной клапан, край 875A верхней полой вены и край 875B нижней полой вены функционируют как впускные края, выпускные устья верхней и нижней полых вен 120 и 125 функционируют как впускные отверстия камеры сердца, промежуток 830 функционирует как первичный промежуток, а множество упругих связей 290 функционируют как множество первичных изменяемых соединительных элементов.
Аналогично показанному для протеза левого желудочка (фиг. 3), промежуток 830 предназначен для приема текучей среды, в частности жидкости, такой как гемосовместимый раствор, например стерильный физиологический раствор, или газа, например гелия, в переменном количестве для динамического изменения объема промежутка 830 и, таким образом, изменения упруго изменяемого объема, ограниченного внутренней поверхностью 854 внутренней упругой мембраны 850. Для этого доступ к промежутку 830 осуществляется через (по меньшей мере) одно отверстие для доступа, выполненное в наружной упругой мембране 800, причем после имплантации протеза в правое предсердие к этому отверстию пришивается канал 380, при этом канал 380 присоединяет промежуток 830 к внешнему (гидравлическому или пневматическому) насосу 340D, который также присоединен к промежутку 730 протеза правого желудочка через канал 370; в альтернативном варианте промежуток 830 может быть присоединен к внешнему насосу, отдельному от насоса, к которому присоединен промежуток 730 протеза правого желудочка. Необязательно, края этого (по меньшей мере одного) отверстия для доступа могут быть изготовлены из рентгеноконтрастного материала, и/или хирург может выполнить отверстие для доступа в любом месте наружной упругой мембраны 800 аналогично тому, как это описано выше для протеза левого желудочка, показанного на фиг. 3.
Также в этом случае, альтернативно или в сочетании с гидравлическим или пневматическим управлением, система протезов, показанная на фиг. 12, может обладать электрическим и/или электромагнитным управлением, осуществляемым посредством электронного блока обработки данных, предназначенного для управления электрической и/или электромагнитной поляризацией внутренней и наружной упругих мембран 850 и 800, которые содержат электроды. В этом случае промежутки 730 и 830 могут быть заполнены жидкостью (например, гемосовместимым раствором) и могут сообщаться по текучей среде друг с другом (вместо или совместно по меньшей мере с одним упругим пакетом переменного объема) через соединительный канал: во время систолы предсердий электрическое и/или электромагнитное управление вызывает увеличение объема промежутка 830 и уменьшение объема промежутка 730, перемещая жидкость из второго в первый; во время систолы желудочков электрическое и/или электромагнитное управление вызывает уменьшение объема промежутка 830 и увеличение объема промежутка 730, перемещая жидкость из первого в второй.
Кроме того, система протезов, показанная на фиг. 12, также может содержать один или более искусственных клапанов сердца. При этом следует отметить, что в случае, когда система протезов содержит искусственный трикуспидальный клапан, два протеза, предназначенные для правого желудочка 30 и правого предсердия 10, могут быть присоединены друг к другу по краям 775 и 885 их соответствующих трикуспидальных клапанов, при этом система протезов клапанов сердца также может быть имплантирована без пришивания края 775 трикуспидального клапана и/или края 885 трикуспидального клапана к собственному трикуспидальному клапану 50.
Хотя варианты выполнения системы протезов камер сердца, показанные на фиг. 9–12, содержат протезы только с внутренней упругой мембраной и наружной упругой мембраной, следует отметить, что другие варианты выполнения системы протезов камер сердца согласно настоящему изобретению могут содержать, альтернативно или в сочетании с двухмембранными протезами, сходные протезы камер сердца также с промежуточной упругой мембраной, расположенной между внутренней упругой мембраной и наружной упругой мембраной, аналогично тому, как это описано для протезов, показанных на фиг. 8, причем изменением объема промежутков управляют посредством гидравлического или пневматического управления и/или электрического и/или электромагнитного управления. Например, у пациентов с гипертрофической патологией с дилатированным предсердием может быть имплантирована система протезов, содержащая протез левого желудочка с двумя мембранами и протез левого предсердия с тремя мембранами.
Следует отметить, что другие варианты выполнения протеза камеры сердца согласно настоящему изобретению могут содержать первичные (и вторичные) изменяемые соединительные элементы, необязательно упругие, которые присоединяют две мембраны друг к другу, такие как, например, нанотехнологичные структуры, предназначенные в предположении компоновки, заключенной между ними в сжатом состоянии, при котором соединенные мембраны расположены на первом предельном расстоянии, и расширенным состоянием, при котором соединенные мембраны находятся на втором предельном расстоянии, которое больше первого предельного расстояния. В качестве примера, такие нанотехнологичные структуры могут содержать две связи, каждая из которых имеет собственные концы, присоединенные к соответствующей мембране, которые шарнирно соединены друг с другом (необязательно, в центральной области связей).
Протез камеры сердца и соответствующая система согласно настоящему изобретению могут быть снабжены датчиками (например, механическими, пьезоэлектрическими или электрическими датчиками) на соответствующих упругих мембранах, предназначенными для регистрации изменения давления и электрокардиограммы во время разных фаз сердечного цикла. Таким образом, регулировка управления изменением объема промежутков переменного объема может быть осуществлена для улучшения общих физиологических характеристик. Например, внутри левого желудочка датчик давления может обеспечивать обработку управляющего сигнала способом, известным, как PRAM (предложен в патентном документе WO 00/64339). Эта обработка может быть использована для определения времени и амплитуд изменения объемов, ограниченных внутренними мембранами в конкретных камерах сердца, в которые имплантированы соответствующие протезы.
Как указано, протезом камеры сердца и соответствующей системой согласно настоящему изобретению, предпочтительно, управляют посредством гидравлического или пневматического управления и/или электрического и/или электромагнитного управления, предпочтительно посредством вспомогательной памяти EPROM, имплантированной в качестве кардиостимулятора. Она позволяет управлять одним или несколькими протезами, имплантированными в соответствующие одну или более из четырех камер сердца.
Описаны предпочтительные варианты осуществления настоящего изобретения, и предложено большое число их вариантов, но следует понимать, что для специалистов очевидны другие варианты и изменения, вносимые без отступления от защищаемого объема настоящего изобретения, определенного приложенной формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МИТРАЛЬНОГО И АОРТАЛЬНОГО ПРОТЕЗИРОВАНИЯ КЛАПАНОВ СЕРДЦА ПРИ ДЕСТРУКЦИИ МИТРАЛЬНО-АОРТАЛЬНОГО СОЕДИНЕНИЯ | 1999 |
|
RU2196527C2 |
| ПРОТЕЗ КЛАПАНА, УСТАНАВЛИВАЕМЫЙ ПОСРЕДСТВОМ КАТЕТЕРА, И СООТВЕТСТВУЮЩИЙ СПОСОБ | 2014 |
|
RU2666591C2 |
| Способ задней пластики корня аорты и выводного тракта левого желудочка для имплантации в аортальную позицию большего размера протеза | 2021 |
|
RU2774779C1 |
| ПЕРСОНИФИЦИРОВАННАЯ 3D МОДЕЛЬ КАРДИО-АОРТАЛЬНОГО КОМПЛЕКСА, СИСТЕМА ДЛЯ ПЛАНИРОВАНИЯ И ПРОВЕДЕНИЯ ОПЕРАЦИЙ ПРИ СТРУКТУРНЫХ ПОРАЖЕНИЯХ СЕРДЦА НА ОСНОВЕ МОДЕЛИ И СПОСОБ ИЗГОТОВЛЕНИЯ ТАКОЙ СИСТЕМЫ | 2023 |
|
RU2825771C1 |
| УСТРОЙСТВО ДЛЯ СОЕДИНЕНИЯ ИМПЛАНТИРУЕМОГО ПРОТЕЗА СЕРДЦА С СОСУДИСТОЙ СИСТЕМОЙ ПАЦИЕНТА И ПРОТЕЗ СЕРДЦА, СНАБЖЕННЫЙ ТАКИМ СОЕДИНИТЕЛЬНЫМ УСТРОЙСТВОМ | 2022 |
|
RU2821745C2 |
| СПОСОБ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ КОМБИНИРОВАННЫХ ПОРОКОВ МИТРАЛЬНОГО И АОРТАЛЬНОГО КЛАПАНОВ НА ФОНЕ АКТИВНОГО ИНФЕКЦИОННОГО ЭНДОКАРДИТА | 2006 |
|
RU2355327C2 |
| СПОСОБ АМПУТАЦИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАЦИЕНТОВ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ | 2024 |
|
RU2833936C1 |
| СПОСОБ ИМПЛАНТАЦИИ КАРКАСНЫХ ПРОТЕЗОВ КЛАПАНОВ СЕРДЦА В АОРТАЛЬНУЮ ПОЗИЦИЮ ПРИ ОДНОМОМЕНТНОМ ПРОТЕЗИРОВАНИИ МИТРАЛЬНОГО И АОРТАЛЬНОГО КЛАПАНОВ | 2016 |
|
RU2626318C1 |
| Способ хирургического лечения гипертрофической обструктивной кардиомиопатии | 2015 |
|
RU2608705C1 |
| ПРОТЕЗ ТРИКУСПИДАЛЬНОГО КЛАПАНА СЕРДЦА | 2013 |
|
RU2541043C2 |
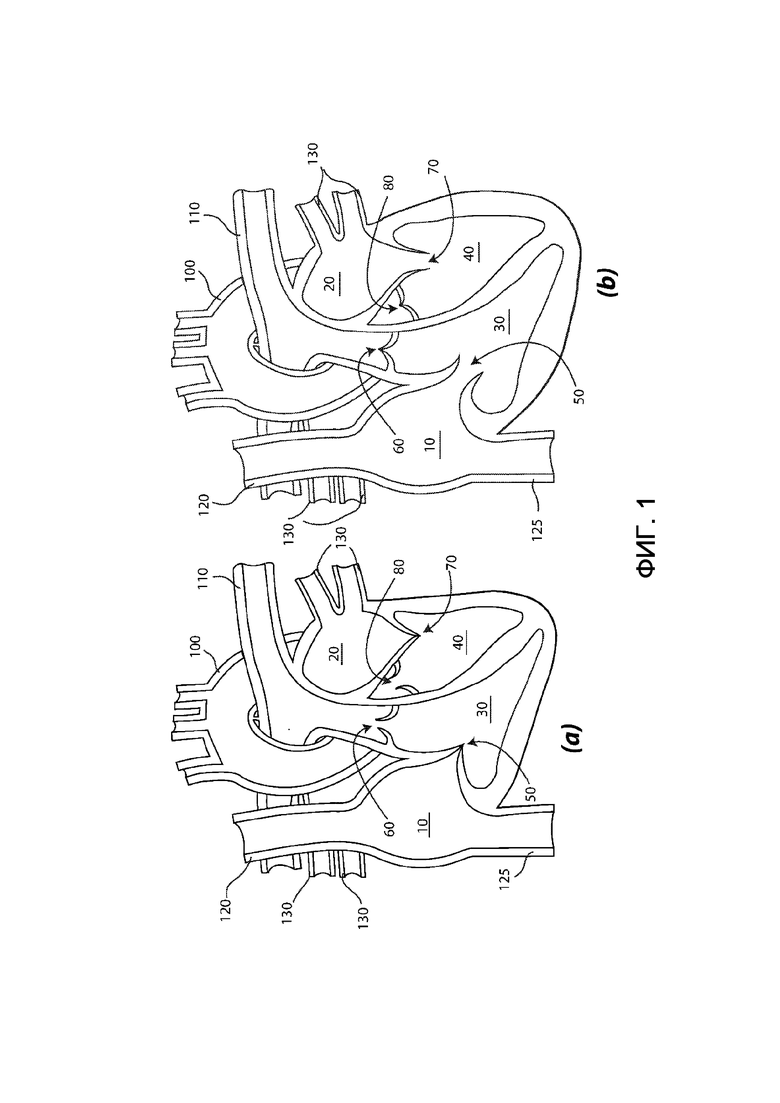
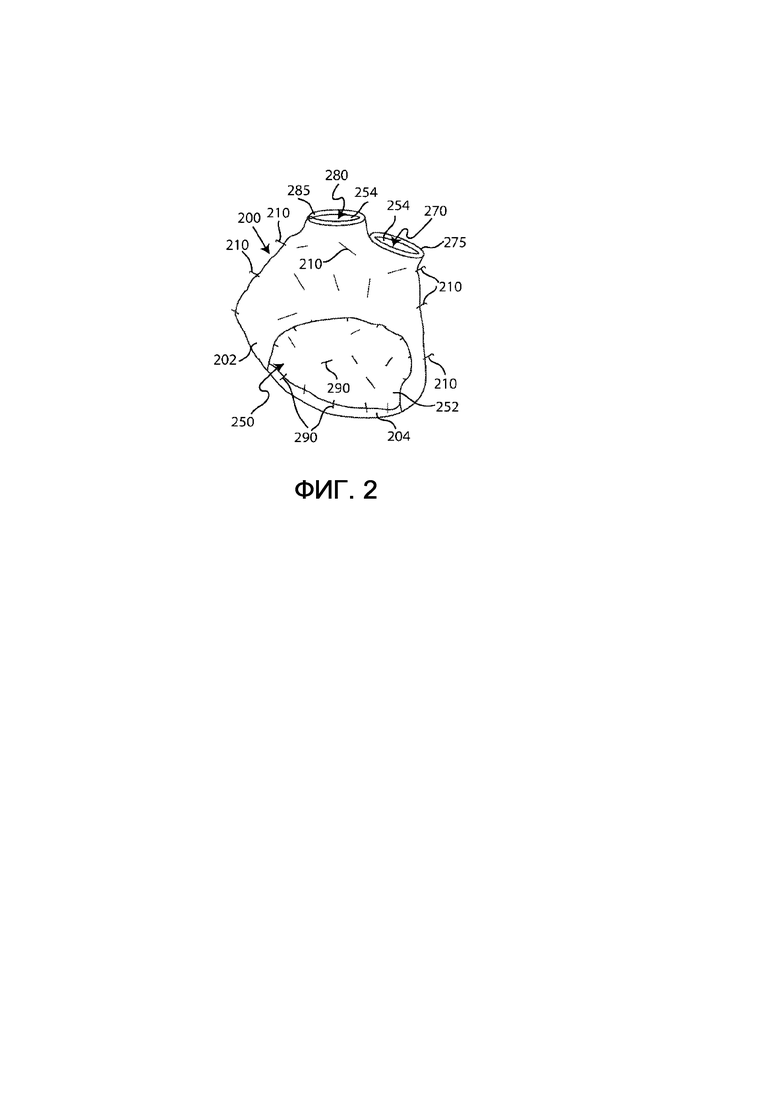
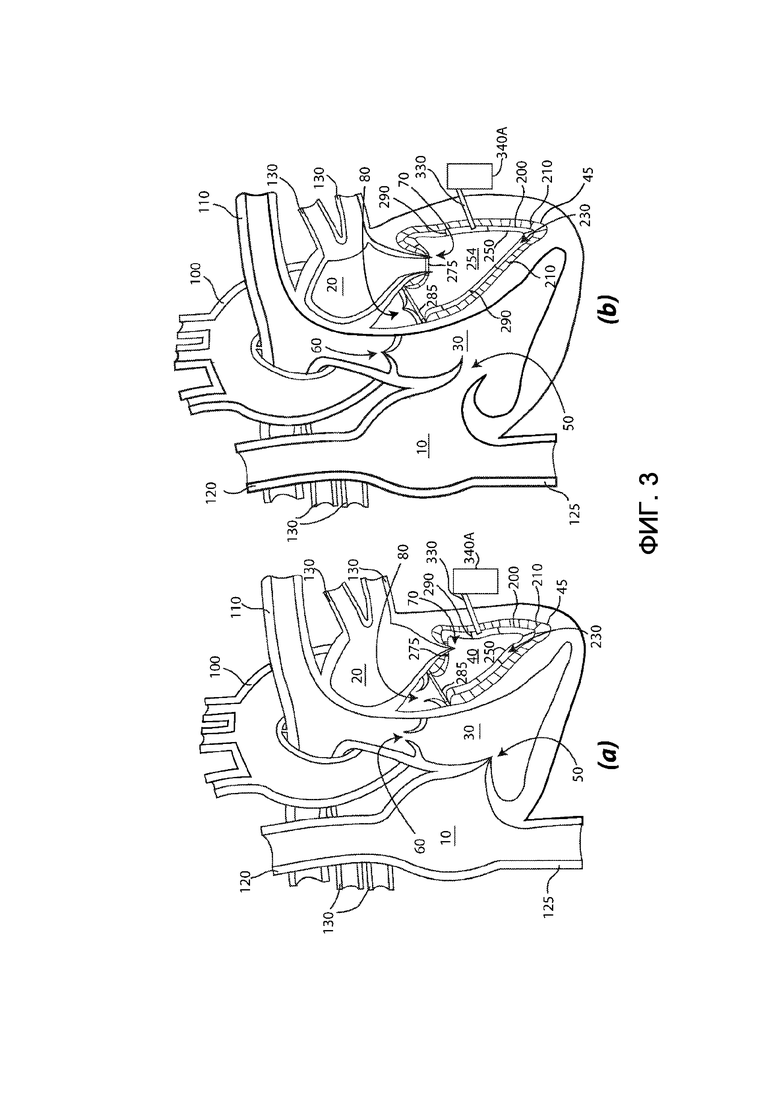
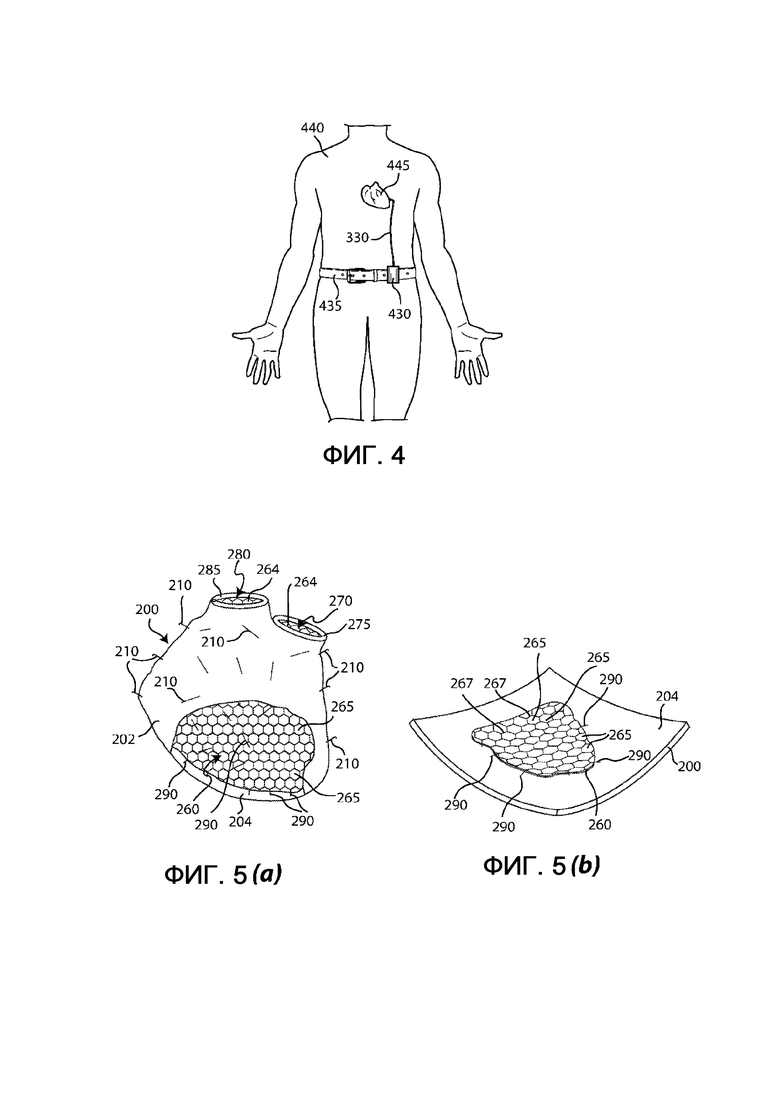
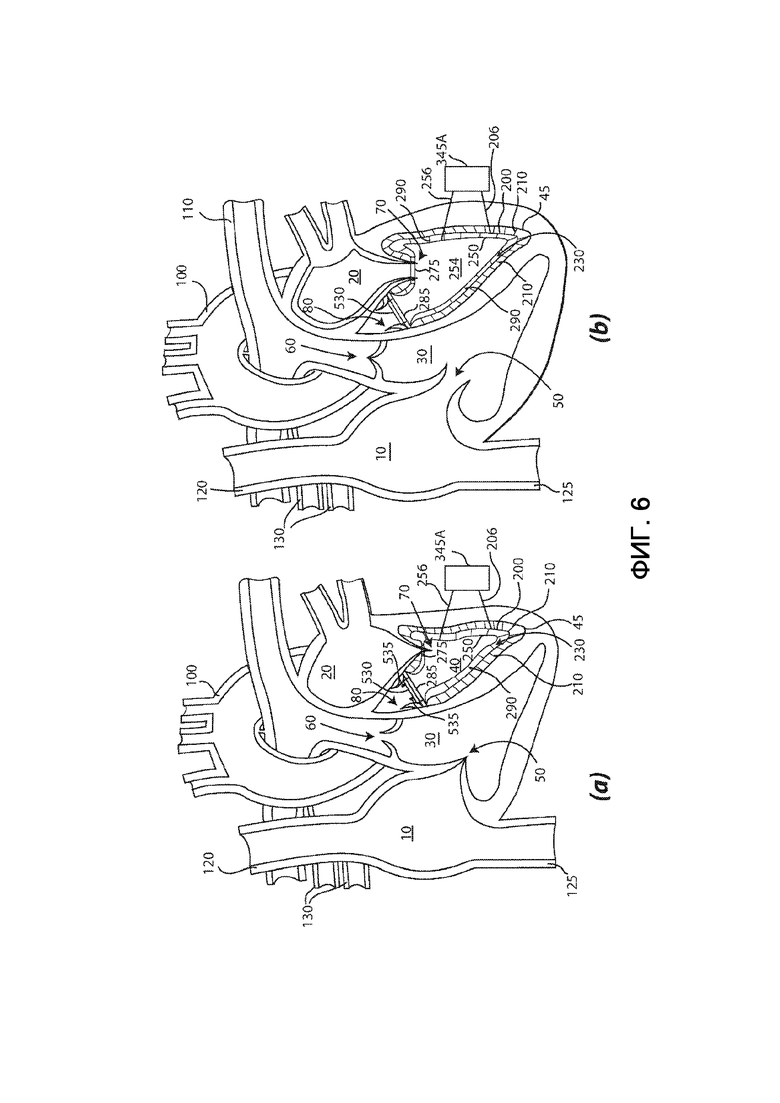
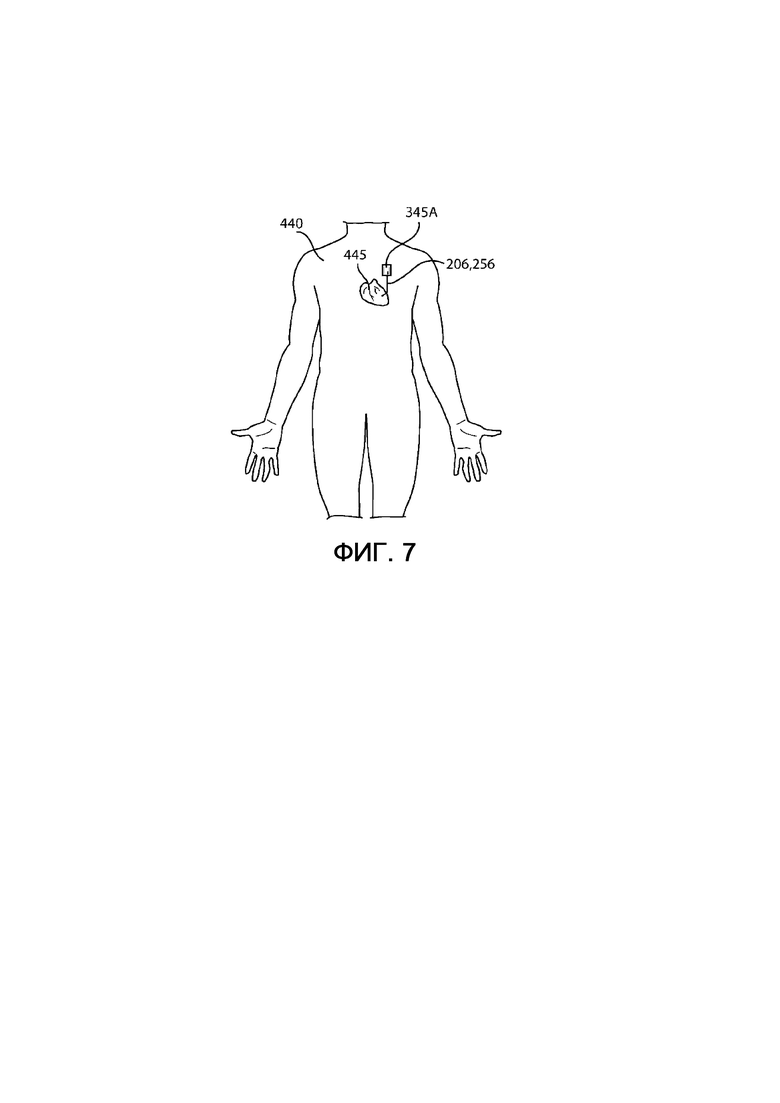
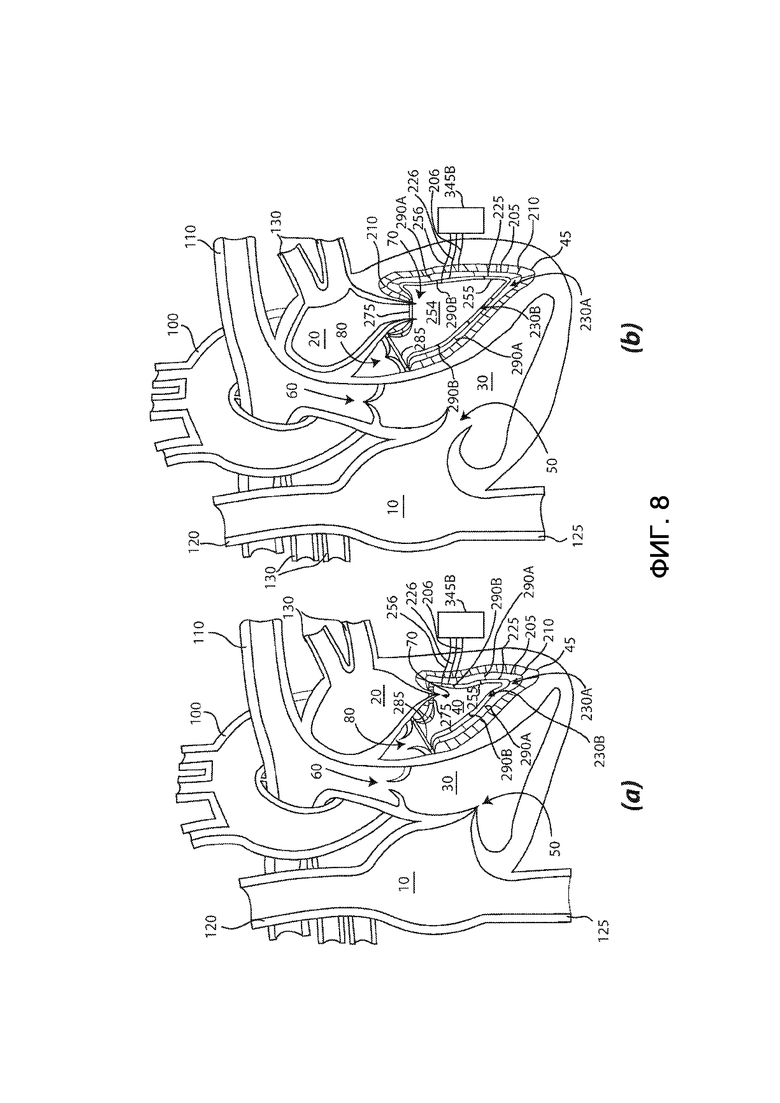
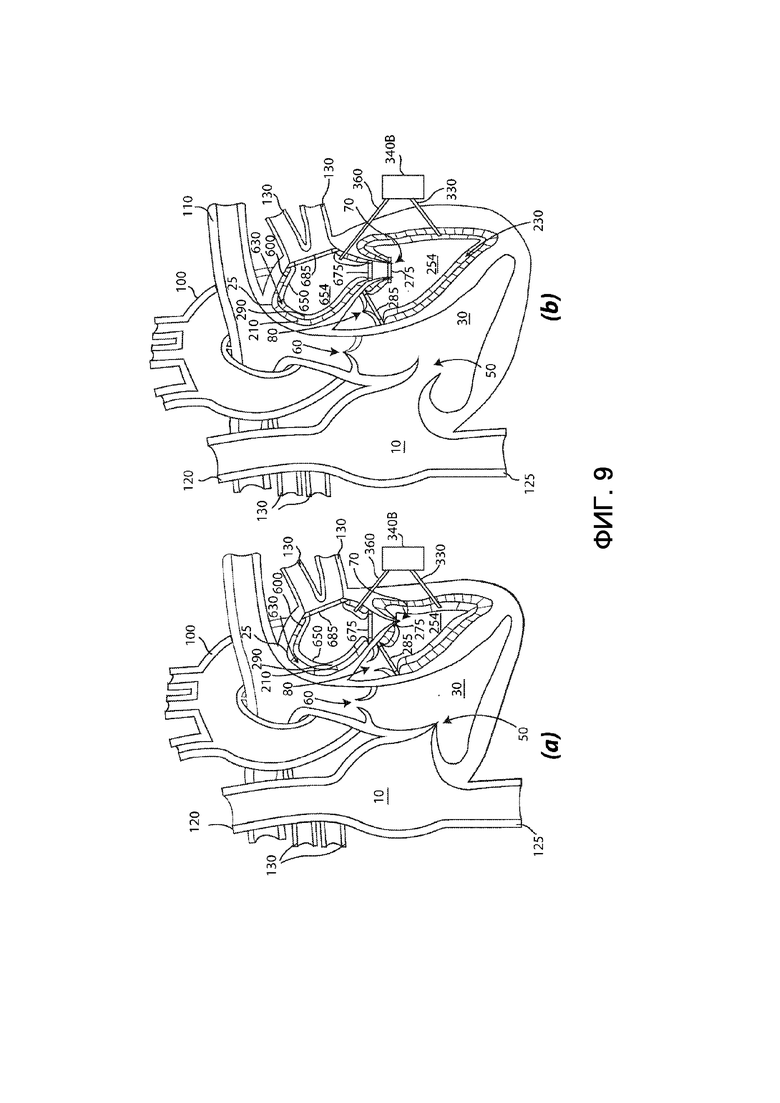
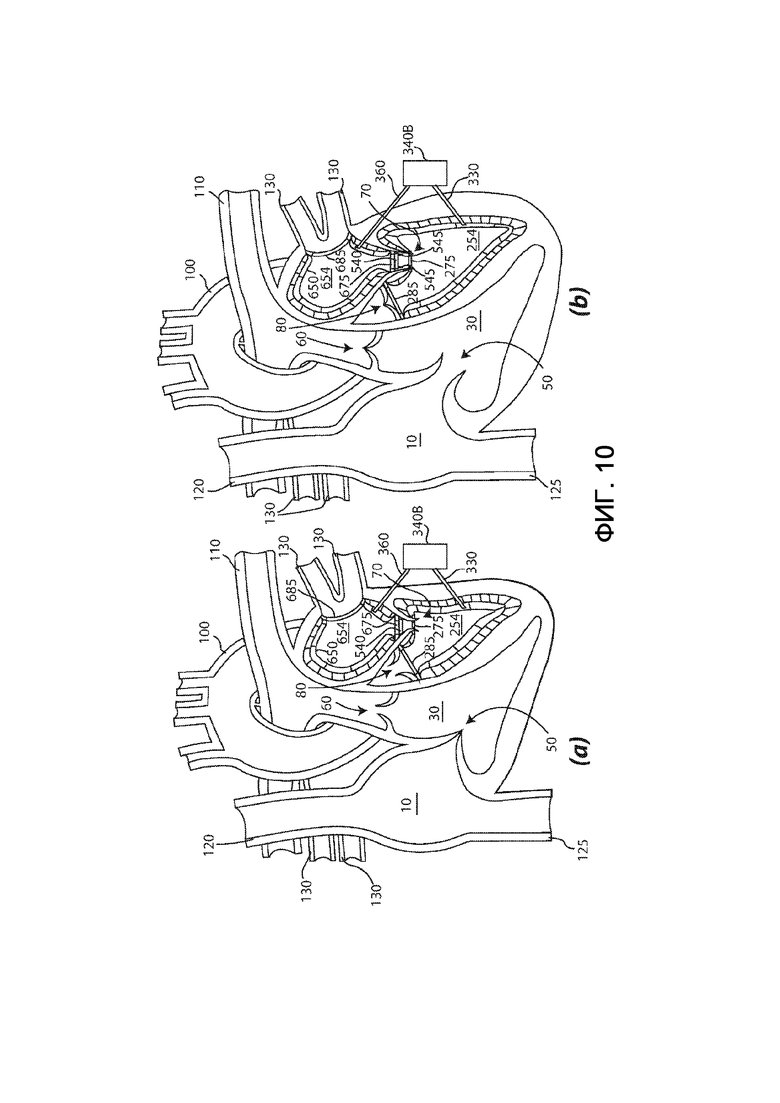
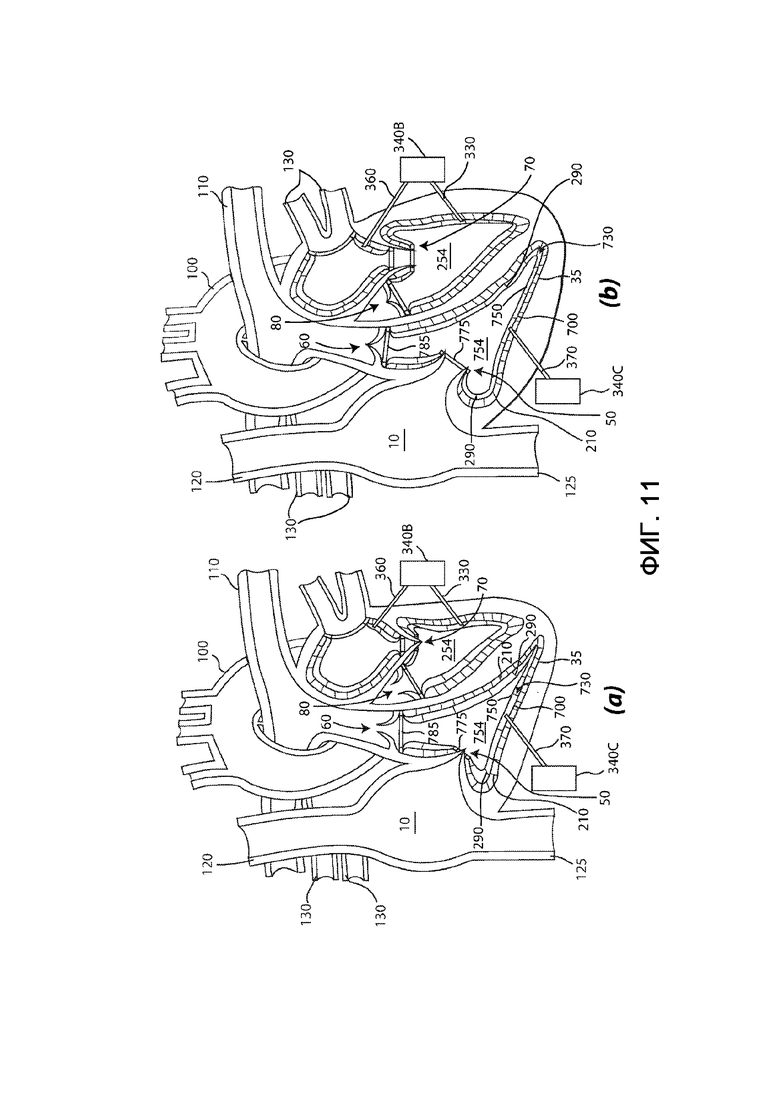
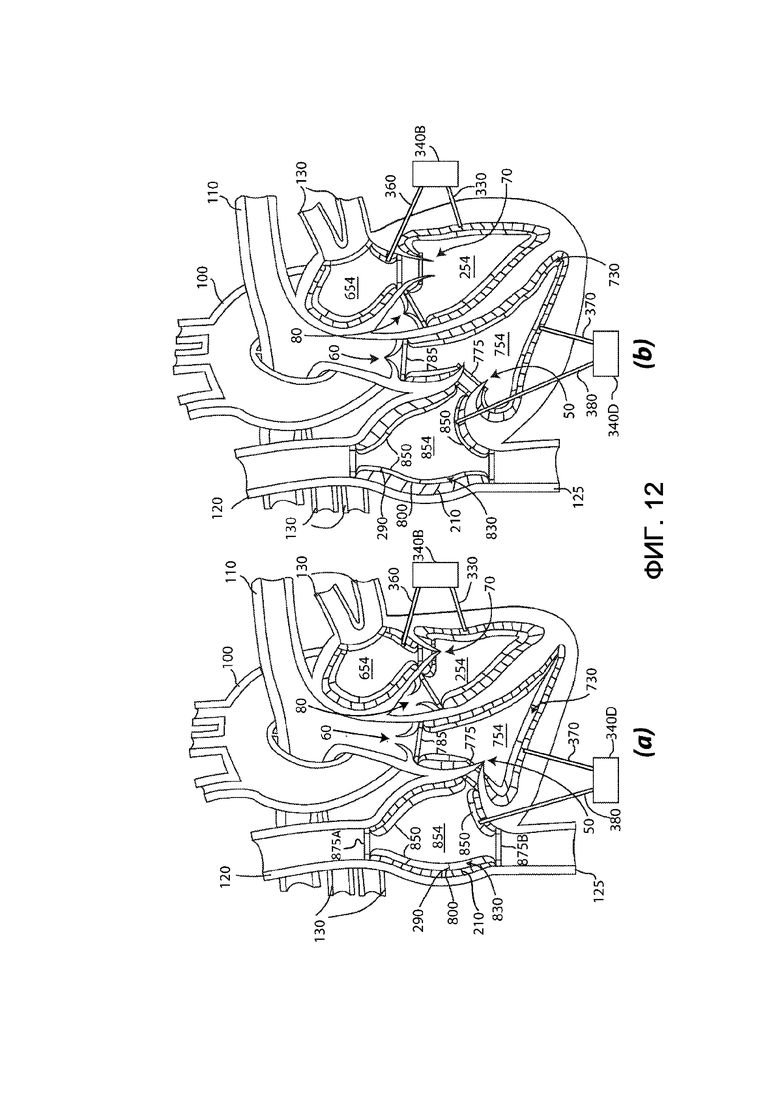
Группа изобретений относится к медицинской технике. Протез камеры сердца, предназначенный для имплантации в камеру сердца, содержит внутреннюю упругую мембрану, имеющую внутреннюю поверхность, ограничивающую упруго изменяемый объем, и имеющую первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, и базовую опорную упругую мембранную структуру, содержащую или состоящую из наружной упругой мембраны, имеющей первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, причем наружная упругая мембрана дополнительно содержит множество фиксаторов, выполненных с возможностью зацепления за внутреннюю стенку сердца. Края первых отверстий внутренней и наружной упругих мембран неразъемно соединены друг с другом для формирования внешнего края, предназначенного для окружения собственного выпускного клапана и пришивания к нему. Края указанного второго отверстия внутренней и наружной упругих мембран неразъемно соединены друг с другом для формирования по меньшей мере одного впускного края, предназначенного для окружения по меньшей мере одного впускного отверстия и пришивания к нему. Внутренняя упругая мембрана и базовая опорная упругая мембранная структура присоединены друг к другу посредством множества первичных изменяемых соединительных элементов. Внутренняя упругая мембрана и базовая опорная упругая мембранная структура ограничивают первичный промежуток между ними, предназначенный для приема текучей среды с изменяемым количеством и/или давлением для динамического изменения объема первичного промежутка и указанного упруго изменяемого объема, ограниченного внутренней поверхностью внутренней упругой мембраны. Раскрыты система протезов камер сердца и кардиологическая вспомогательная система. Технический результат состоит в обеспечении селективной помощи в функционировании камеры простым, совместимым, эффективным и надежным способом. 3 н. и 41 з.п. ф-лы, 12 ил.
1. Протез камеры сердца, предназначенный для имплантации в камеру (10; 20; 30; 40) сердца пациента (440), выбранную из группы, состоящей из левого желудочка (40), левого предсердия (20), правого желудочка (30) и правого предсердия (10),
причем камера (10; 20; 30; 40) сердца содержит собственный выпускной клапан (50; 60; 70; 80) и по меньшей мере одно впускное отверстие (50; 70), выбранное из группы, содержащей собственный впускной клапан (50; 70) и одно или более выпускных устий полых вен или легочных вен (120; 125; 130),
при этом протез содержит:
- внутреннюю упругую мембрану (250; 255; 260; 650; 750; 850), имеющую внутреннюю поверхность (254; 654; 754; 854), ограничивающую упруго изменяемый объем, и имеющую первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем,
- базовую опорную упругую мембранную структуру (200; 205, 225, 290A; 600; 700; 800), содержащую или состоящую из наружной упругой мембраны (200; 205; 600; 700; 800), имеющей первое отверстие, ограниченное соответствующим первым краем, и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, причем наружная упругая мембрана (200; 205; 600; 700; 800) дополнительно содержит множество фиксаторов (210), выполненных с возможностью зацепления за внутреннюю стенку (45) камеры (10; 20; 30; 40) сердца,
причем края первых отверстий внутренней и наружной упругих мембран (250, 200; 255, 205; 260, 200; 650, 600; 750, 700; 850, 800) неразъемно соединены друг с другом для формирования внешнего края (285; 675; 785; 885), предназначенного для окружения собственного выпускного клапана (50; 60; 70; 80) и пришивания к нему,
при этом края указанного второго отверстия внутренней и наружной упругих мембран (250, 200; 255, 205; 260, 200; 650, 600; 750, 700; 850, 800) неразъемно соединены друг с другом для формирования по меньшей мере одного впускного края (275; 685; 775; 875A, 875B), предназначенного для окружения по меньшей мере одного впускного отверстия (50; 70) и пришивания к нему,
причем внутренняя упругая мембрана (250; 255; 260; 650; 750; 850) и базовая опорная упругая мембранная структура (200; 205, 225, 290A; 600; 700; 800) присоединены друг к другу посредством множества первичных изменяемых соединительных элементов (290; 290B),
при этом внутренняя упругая мембрана (250; 255; 260; 650; 750; 850) и базовая опорная упругая мембранная структура (200; 205, 225, 290A; 600; 700; 800) ограничивают первичный промежуток (230; 230B; 630; 730; 830) между ними, предназначенный для приема текучей среды с изменяемым количеством и/или давлением для динамического изменения объема первичного промежутка (230; 230B; 630; 730; 830) и указанного упруго изменяемого объема, ограниченного внутренней поверхностью (254; 654; 754; 854) внутренней упругой мембраны (250; 255; 260; 650; 750; 850).
2. Протез камеры сердца по п. 1, в котором наружная упругая мембрана (200; 205; 600; 700; 800) обладает коэффициентом упругости, который не больше коэффициента упругости внутренней упругой мембраны (250; 255; 260; 650; 750; 850).
3. Протез камеры сердца по п. 2, в котором наружная упругая мембрана (200; 205; 600; 700; 800) обладает коэффициентом упругости, который меньше коэффициента упругости внутренней упругой мембраны (250; 255; 260; 650; 750; 850).
4. Протез камеры сердца по любому из пп. 1–3, в котором каждая из внутренней и наружной упругих мембран (250, 200; 255, 205; 260, 200; 650, 600; 750, 700; 850, 800) обладает изменяющимся коэффициентом упругости.
5. Протез камеры сердца по п. 4, в котором каждая из внутренней и наружной упругих мембран (250, 200; 255, 205; 260, 200; 650, 600; 750, 700; 850, 800) содержит две или более областей, имеющих соответствующие коэффициенты упругости.
6. Протез камеры сердца по любому из пп. 1–5, в котором указанной текучей средой является жидкость или газ.
7. Протез камеры сердца по любому из пп. 1–5, в котором указанной текучей средой является гемосовместимый раствор, или стерильный физиологический раствор, или гелий.
8. Протез камеры сердца по любому из пп. 1–7, который дополнительно содержит по меньшей мере один искусственный клапан (530, 540), неразъемно соединенный с выпускным краем (285; 675; 785; 885) или указанным по меньшей мере одним впускным краем (275; 685; 775; 875A, 875B).
9. Протез камеры сердца по любому из пп. 1–8, в котором указанными первичными изменяемыми соединительными элементами являются первичные упругие связи (290; 290B), каждая из которых обладает коэффициентом упругости, который больше, чем коэффициент упругости наружной упругой мембраны (200; 205; 600; 700; 800) и чем коэффициент упругости внутренней упругой мембраны (250; 255; 260; 650; 750; 850).
10. Протез камеры сердца по п. 9, в котором указанные первичные упругие связи (290; 290B) обладают различными коэффициентами упругости в зависимости от области внутренней упругой мембраны (250; 255; 260; 650; 750; 850), к которой они присоединены.
11. Протез камеры сердца по любому из пп. 1–10, который выполнен с возможностью помещения внутрь катетера.
12. Протез камеры сердца по любому из пп. 1–11, в котором наружная упругая мембрана (200; 205; 600; 700; 800) и/или внутренняя упругая мембрана (250; 255; 260; 650; 750; 850) содержат рентгеноконтрастные участки.
13. Протез камеры сердца по любому из пп. 1–12, в котором первичный промежуток (230; 230B; 630; 730; 830) выполнен с возможностью сообщения по текучей среде по меньшей мере с одним упругим пакетом переменного объема, которым снабжен протез, или с внешним насосом (340A; 340B; 340C; 340D).
14. Протез камеры сердца по любому из пп. 1–13, в котором по меньшей мере одна из внутренней упругой мембраны (260) и наружной упругой мембраны обладает прерывистой структурой.
15. Протез камеры сердца по п. 14, в котором указанная прерывистая структура выбрана из группы, содержащей:
- ячеистую прерывистую структуру, образованную множеством упругих пластинок (265), присоединенных друг к другу вдоль линий (267) упругого соединения,
- прерывистую структуру, образованную множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения,
- ячеистую прерывистую структуру, образованную множеством шестиугольных упругих пластинок (265), присоединенных друг к другу вдоль линий (267) упругого соединения,
- прерывистую структуру, образованную множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения,
- ячеистую прерывистую структуру, образованную множеством упругих пластинок (265), присоединенных друг к другу вдоль линий (267) упругого соединения, причем линии (267) упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих пластинок (265),
- прерывистую структуру, образованную множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих многоугольных пластинок,
- ячеистую прерывистую структуру, образованную множеством шестиугольных упругих пластинок (265), присоединенных друг к другу вдоль линий (267) упругого соединения, причем линии (267) упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих пластинок (265), и
- прерывистую структуру, образованную множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше коэффициента упругости упругих многоугольных пластинок.
16. Протез камеры сердца по любому из пп. 1–15, в котором каждая из внутренней упругой мембраны (250; 255; 260; 650; 750; 850) и наружной упругой мембраны (200; 205; 600; 700; 800) содержит множество электродов, предназначенных для электрической и/или электромагнитной поляризации внутренней упругой мембраны (250; 255; 260; 650; 750; 850) и наружной упругой мембраны (200; 205; 600; 700; 800) соответственно под управлением электронного блока (345A; 345B) обработки данных, соединенного с указанными электродами посредством соответствующих кабелей (206, 256) управления.
17. Протез камеры сердца по любому из пп. 1–15, в котором базовая опорная упругая мембранная структура (205, 225, 290A) дополнительно содержит промежуточную упругую мембрану (225), которая расположена между наружной упругой мембраной (205) и внутренней упругой мембраной (255),
при этом промежуточная упругая мембрана (225) имеет первое отверстие, ограниченное соответствующим первым краем, неразъемно соединенным с краями первых отверстий внутренней и наружной упругих мембран (255, 205), и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, неразъемно соединенным с краями указанных вторых отверстий внутренней и наружной упругих мембран (255, 205),
причем промежуточная упругая мембрана (225) и наружная упругая мембрана (205) присоединены друг к другу посредством множества вторичных изменяемых соединительных элементов (290A), при этом указанные вторичные упругие связи (290A) обладают различными коэффициентами упругости в зависимости от области промежуточной упругой мембраны (225), к которой они присоединены,
причем указанное множество первичных изменяемых соединительных элементов (290B) соединяют внутреннюю упругую мембрану (255) и промежуточную упругую мембрану (225) друг с другом,
при этом наружная упругая мембрана (205) и промежуточная упругая мембрана (225) ограничивают вторичный промежуток (230A) между ними, который предназначен для приема текучей среды.
18. Протез камеры сердца по п. 17, в котором промежуточная упругая мембрана (225) обладает коэффициентом упругости, который не больше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости внутренней упругой мембраны (255).
19. Протез камеры сердца по п. 18, в котором промежуточная упругая мембрана (225) обладает коэффициентом упругости, который меньше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости внутренней упругой мембраны (255).
20. Протез камеры сердца по любому из пп. 17–19, в котором указанное множество вторичных изменяемых соединительных элементов (290A) состоит из вторичных упругих связей (290A), при этом указанные вторичные упругие связи (290A) обладают различными коэффициентами упругости в зависимости от области промежуточной упругой мембраны (225), к которой они присоединены.
21. Протез камеры сердца по п. 20, в котором каждая из указанных вторичных упругих связей (290A) обладает коэффициентом упругости, который больше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости промежуточной упругой мембраны (225).
22. Протез камеры сердца по любому из пп. 17–21, в котором текучая среда, для приема которой предназначен указанный вторичный промежуток (230A), состоит из жидкости или газа.
23. Протез камеры сердца по любому из пп. 17–21, в котором текучая среда, для приема которой предназначен указанный вторичный промежуток (230A), является гемосовместимым раствором, или стерильным физиологическим раствором, или гелием.
24. Протез камеры сердца по п. 16, в котором базовая опорная упругая мембранная структура (205, 225, 290A) дополнительно содержит промежуточную упругую мембрану (225), которая расположена между наружной упругой мембраной (205) и внутренней упругой мембраной (255),
при этом промежуточная упругая мембрана (225) имеет первое отверстие, ограниченное соответствующим первым краем, неразъемно соединенным с краями первых отверстий внутренней и наружной упругих мембран (255, 205), и по меньшей мере одно второе отверстие, ограниченное соответствующим вторым краем, неразъемно соединенным с краями указанных вторых отверстий внутренней и наружной упругих мембран (255, 205),
причем промежуточная упругая мембрана (225) и наружная упругая мембрана (205) присоединены друг к другу посредством множества вторичных изменяемых соединительных элементов (290A), при этом указанные вторичные упругие связи (290A) обладают различными коэффициентами упругости в зависимости от области промежуточной упругой мембраны (225), к которой они присоединены,
причем указанное множество первичных изменяемых соединительных элементов (290B) соединяют внутреннюю упругую мембрану (255) и промежуточную упругую мембрану (225) друг с другом,
при этом наружная упругая мембрана (205) и промежуточная упругая мембрана (225) ограничивают вторичный промежуток (230A) между ними, который предназначен для приема текучей среды.
25. Протез камеры сердца по п. 24, в котором промежуточная упругая мембрана (225) обладает коэффициентом упругости, который не больше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости внутренней упругой мембраны (255).
26. Протез камеры сердца по п. 25, в котором промежуточная упругая мембрана (225) обладает коэффициентом упругости, который меньше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости внутренней упругой мембраны (255).
27. Протез камеры сердца по любому из пп. 24–26, в котором указанное множество вторичных изменяемых соединительных элементов (290A) состоит из вторичных упругих связей (290A), при этом указанные вторичные упругие связи (290A) обладают различными коэффициентами упругости в зависимости от области промежуточной упругой мембраны (225), к которой они присоединены.
28. Протез камеры сердца по п. 27, в котором каждая из указанных вторичных упругих связей (290A) обладает коэффициентом упругости, который больше, чем коэффициент упругости наружной упругой мембраны (205) и чем коэффициент упругости промежуточной упругой мембраны (225).
29. Протез камеры сердца по любому из пп. 24–28, в котором текучая среда, для приема которой предназначен указанный вторичный промежуток (230A), состоит из жидкости или газа.
30. Протез камеры сердца по любому из пп. 24–28, в котором текучая среда, для приема которой предназначен указанный вторичный промежуток (230A), является гемосовместимым раствором, или стерильным физиологическим раствором, или гелием.
31. Протез камеры сердца по любому из пп. 17–23, в котором вторичный промежуток (230A) предназначен для приема текучей среды с переменным количеством и/или давлением для динамического изменения объема вторичного промежутка (230A).
32. Протез камеры сердца по п. 31, в котором вторичный промежуток (230A) выполнен с возможностью сообщения по текучей среде по меньшей мере с одним упругим пакетом переменного объема, которым снабжен протез, или с внешним насосом (340A; 340B; 340C; 340D).
33. Протез камеры сердца по любому из пп. 24–30, в котором вторичный промежуток (230A) предназначен для приема текучей среды с переменным количеством и/или давлением для динамического изменения объема вторичного промежутка (230A).
34. Протез камеры сердца по п. 33, в котором вторичный промежуток (230A) выполнен с возможностью сообщения по текучей среде по меньшей мере с одним упругим пакетом переменного объема, которым снабжен протез, или с внешним насосом (340A; 340B; 340C; 340D).
35. Протез камеры сердца по любому из пп. 17–23, 31, 32, в котором промежуточная упругая мембрана (225) обладает прерывистой структурой.
36. Протез камеры сердца по п. 35, в котором указанная прерывистая структура выбрана из группы, состоящей из:
- ячеистой прерывистой структуры, образованной множеством упругих пластинок, соединенных друг с другом вдоль линий упругого соединения,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения,
- ячеистой прерывистой структуры, образованной множеством шестиугольных упругих пластинок, соединенных друг с другом вдоль линий упругого соединения,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения,
- ячеистой прерывистой структуры, образованной множеством упругих пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих пластинок,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих многоугольных пластинок,
- ячеистой прерывистой структуры, образованной множеством шестиугольных упругих пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих пластинок, и
- прерывистой структуры, образованной множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих многоугольных пластинок.
37. Протез камеры сердца по любому из пп. 24–30, 33, 34, в котором промежуточная упругая мембрана (225) обладает прерывистой структурой.
38. Протез камеры сердца по п. 37, в котором указанная прерывистая структура выбрана из группы, состоящей из:
- ячеистой прерывистой структуры, образованной множеством упругих пластинок, соединенных друг с другом вдоль линий упругого соединения,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения,
- ячеистой прерывистой структуры, образованной множеством шестиугольных упругих пластинок, соединенных друг с другом вдоль линий упругого соединения,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения,
- ячеистой прерывистой структуры, образованной множеством упругих пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих пластинок,
- прерывистой структуры, образованной множеством упругих многоугольных пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих многоугольных пластинок,
- ячеистой прерывистой структуры, образованной множеством шестиугольных упругих пластинок, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих пластинок, и
- прерывистой структуры, образованной множеством упругих многоугольных пластинок пятиугольной и/или шестиугольной формы, соединенных друг с другом вдоль линий упругого соединения, причем указанные линии упругого соединения обладают коэффициентом упругости, который больше, чем коэффициент упругости указанных упругих многоугольных пластинок.
39. Протез камеры сердца по любому из пп. 24–30, 33, 34, 37, 38, в котором промежуточная упругая мембрана (225) содержит множество электродов, предназначенных для электрической и/или электромагнитной поляризации промежуточной упругой мембраны (225) под управлением указанного электронного блока (345B) обработки данных, соединенного с указанными электродами посредством соответствующего одного или более кабелей (226) управления.
40. Протез камеры сердца по любому из пп. 1–15, 17–23, 31, 32, 35, 36, который предназначен для имплантации:
- в левый желудочек (40), при этом наружный край является аортальным краем (285), предназначенным для окружения собственного аортального клапана (80) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из митрального края (275), предназначенного для окружения собственного митрального клапана (70) и пришивания к нему, или
- в левое предсердие (20), при этом наружный край является митральным краем (675), предназначенным для окружения собственного митрального клапана (70) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из одного или более краев (685) легочных вен, предназначенных для окружения соответствующего одного или более выпускных устий легочных вен (130) и пришивания к ним, или
- в правый желудочек (30), при этом выпускной край является краем (785) легочного клапана, предназначенным для окружения собственного легочного клапана (60) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из края (775) трикуспидального клапана, предназначенного для окружения собственного трикуспидального клапана (50) и пришивания к нему, или
- в правое предсердие (10), при этом выпускной край является краем (775) трикуспидального клапана, предназначенным для окружения собственного трикуспидального клапана (50) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из одного или более краев (875A, 875B) полых вен, предназначенных для окружения соответствующего одного или более выпускных устьев полых вен (120, 125) и пришивания к ним.
41. Протез камеры сердца по любому из пп. 16, 24–30, 33, 34, 37, 38, 39, который предназначен для имплантации:
- в левый желудочек (40), при этом наружный край является аортальным краем (285), предназначенным для окружения собственного аортального клапана (80) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из митрального края (275), предназначенного для окружения собственного митрального клапана (70) и пришивания к нему, или
- в левое предсердие (20), при этом наружный край является митральным краем (675), предназначенным для окружения собственного митрального клапана (70) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из одного или более краев (685) легочных вен, предназначенных для окружения соответствующего одного или более выпускных устий легочных вен (130) и пришивания к ним, или
- в правый желудочек (30), при этом выпускной край является краем (785) легочного клапана, предназначенным для окружения собственного легочного клапана (60) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из края (775) трикуспидального клапана, предназначенного для окружения собственного трикуспидального клапана (50) и пришивания к нему, или
- в правое предсердие (10), при этом выпускной край является краем (775) трикуспидального клапана, предназначенным для окружения собственного трикуспидального клапана (50) и пришивания к нему, а указанный по меньшей мере один впускной край состоит из одного или более краев (875A, 875B) полых вен, предназначенных для окружения соответствующего одного или более выпускных устьев полых вен (120, 125) и пришивания к ним.
42. Система протезов камер сердца, содержащая от двух до четырех протезов камер сердца по любому из пп. 1–41, причем протезы камер сердца предназначены для имплантации в соответствующие две или более камер (10; 20; 30; 40) сердца пациента (440).
43. Система протезов камер сердца по п. 42, в которой указанные протезы камер сердца содержат или состоят из двух протезов камер сердца по п. 16 или по любому из пп. 24–30, 33, 34, 37, 38, 39, 41, которые связаны друг с другом и предназначены для имплантации в левый желудочек (40) и в левое предсердие (20) или в правый желудочек (30) и в правое предсердие (10), при этом первичные промежутки (230, 630; 730, 830) связанных двух протезов камер сердца сообщены по текучей среде друг с другом через передающий канал, причем объем первичного промежутка (230; 730) одного из двух связанных протезов камер сердца выполнен с возможностью увеличения, когда объем первичного промежутка (630; 830) другого из двух связанных протезов камер сердца уменьшается, и наоборот, посредством перемещения текучей среды между первичными промежутками (230, 630; 730, 830) двух связанных протезов камер сердца.
44. Кардиологическая вспомогательная система, содержащая:
- протез камеры сердца по любому из пп. 1–41 или систему протезов камер сердца по п. 42 или 43,
- по меньшей мере один насос (340A; 340B; 340C; 340D) и/или электронный блок (345A; 345B) обработки данных, выполненный с возможностью управления количеством и/или давлением указанной текучей среды, поступающей в первичный промежуток (230; 230B; 630; 730; 830) протеза камеры сердца или протезов камер сердца указанной системы протезов камер сердца для динамического изменения объема первичного промежутка (230; 230B; 630; 730; 830) указанного протеза камеры сердца или протезов камер сердца указанной системы протезов камер сердца.
| US 5139517 A1, 18.08.1992 | |||
| US 20170136162 A1, 18.05.2017 | |||
| US 7341584 B1, 11.03.2008 | |||
| US 20050246013 A1, 03.11.2005 | |||
| US 20110153010 A1, 23.06.2011 | |||
| ИСКУССТВЕННЫЙ ЖЕЛУДОЧЕК СЕРДЦА И СПОСОБ ЕГО РАБОТЫ | 2007 |
|
RU2360704C1 |
| Протез сердца с гидравлическим приводом | 1983 |
|
SU1438599A3 |
Авторы
Даты
2024-01-24—Публикация
2020-07-13—Подача