Изобретение относится к области биотехнологии и может быть использовано в медицине и ветеринарии.
Эволюция и повсеместное распространение резистентных патогенов является одной из ключевых проблем медицины в XXI веке. Во всем мире инфекционные заболевания являются основной причиной смерти для людей младше 60 лет, причем около 17 млн человек ежегодно умирают в результате заражения бактериальными инфекциями. Внутрибольничные бактериальные инфекции (ВБИ) все чаще становятся причиной смерти пациентов, подвергающихся инвазивным процедурам при лечении в стационарах. Статистика по США, Великобритании и странам ЕС свидетельствует о том, что в 5% случаев стационарного лечения у пациентов возникает внутрибольничная бактериальная инфекция. Таким образом, в этих странах ежегодно около 4 млн. пациентов приобретают ВБИ, что приводит к 100 тыс. смертельных исходов, причем около 70% штаммов обладают резистентностью хотя бы к одному из классов антибиотиков. Подобная ситуация значительно усложняет борьбу с типичными бактериальными инфекциями и ставит под угрозу здоровье пациентов после применения многих жизненно необходимых медицинских процедур. В структуре ВБИ наибольшее распространение имеют пневмония, инфекции мочевыводящих путей, а также инфекции кожи и мягких тканей. Ключевыми возбудителями ВБИ являются так называемые «ESKAPE» патогены (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumanii, Pseudomonas aeruginosa, Enterobacter sp.). Важно также отметить, что в условиях глобальной пандемии (например, COVID-19) критически возрастает нагрузка на систему здравоохранения, что, в конечном счете, может привести к резкому росту смертности от вторичных ВБИ.
Среди кандидатов на роль антибактериальных и противоопухолевых средств нового поколения рассматриваются белки и пептиды системы врожденного иммунитета человека и животных, относящиеся к числу наиболее значимых компонентов иммунной системы. Система врожденного иммунитета обеспечивает первую линию противостояния различным инфекционных агентам, а также участвует в реализации механизмов противоопухолевой защиты организма. Одними из ключевых эффекторных молекул системы врожденного иммунитета являются защитные пептиды, содержащиеся преимущественно в лизосомоподобных гранулах нейтрофилов. Эти пептиды обладают широким спектром антибиотической активности - они подавляют рост и развитие грамотрицательных, грамположительных бактерий, грибов, паразитов (включая планарий и нематод) и ряда вирусов, например, таких как ВИЧ и вирус герпеса. Поскольку эти молекулы, как правило, обладают положительным зарядом при нейтральных значениях pH среды и проявляют ингибирующую активность в отношении микроорганизмов, их обычно называют катионными антимикробными пептидами (АМП) (Emelianova et al., 2018; Panteleev et al., 2018).
Наиболее близким аналогом заявляемого изобретения являются открытый нами ранее антимикробный пептид ChMAP (SEQ ID NO 1) из лейкоцитов козы Capra hircus, относящийся к семейству α-спиральных кателицидинов [Panteleev, P.V., Bolosov, I.A., Kalashnikov, A.A., Kokryakov, V.N., Shamova, O.V., Emelianova, A.A., Balandin, S.V., and Ovchinnikova, T.V. Combined Antibacterial Effects of Goat Cathelicidins With Different Mechanisms of Action // Front. Microbiol. 2018, Vol.9, 2983; Emelianova, A.A., Kuzmin, D.V., Panteleev, P.V., Sorokin, M., Buzdin, A.A., and Ovchinnikova, T.V. Anticancer Activity of the Goat Antimicrobial Peptide ChMAP-28 // Front. Pharmacol. 2018, Vol.9, 1501]. ChMAP проявляет высокую антибактериальную и противоопухолевую активность в микромолярном диапазоне концентраций. Ключевым недостатком пептида ChMAP является сравнительно высокая цитотоксичность в отношении клеток млекопитающих, что не позволяет отнести его к числу агентов с высокой селективностью антибактериального действия. В частности, гемолитическая и цитотоксическая активность данного пептида в отношении клеток человека начинает проявляться при концентрациях лишь на порядок превышающих значения минимальных ингибирующих концентраций (МИК) в отношении бактерий в тестах in vitro. Изобретение решает техническую проблему расширения ассортимента пептидов, проявляющих выраженным антибактериальный эффект и широкий спектр активности и обладающих низкой цитотоксичностью, которые могут найти применение для наружного применения, в частности - для лечения инфицированных ран со сложной бактериальной этиологией. Технический результат - это снижение цитотоксичности пептидов при сохранении высокой антибактериальной активности на уровне родоначального пептида.
Для решения указанной технической проблемы, и достижения заявленного технического результата предлагается пептид, обладающий антимикробной активностью в отношении грамположительных и грамотрицательных бактерий и имеющий аминокислотную последовательность SEQ ID NO 2, SEQ ID NO 3.
Заявляемые катионные пептиды были отобраны путем модификации структуры пептида ChMAP путем введения единичных аминокислотных замен. Для выбора заменяемых остатков в структуре кателицидина ChMAP с использованием биоинформатических методов и геномных баз данных нами была составлена библиотека его природных изоформ из других видов млекопитающих и обнаружены наиболее вариабельные остатки в структуре гомологичных пептидов (данные не приведены). С целью снижения цитотоксичности аминокислотные остатки в данных положениях у пептида ChMAP-28 были заменены на менее гидрофобные, в частности, остатки аланина, в то время как наиболее консервативные элементы структуры не подвергались изменениям. Заявляемое изобретение включает в себя аналоги пептида ChMAP, для которых удалось сохранить высокую антибактериальную активность пептида дикого типа и, вместе с тем, снизить цитотоксические свойства в отношении нормальных клеток человека.
Заявляемые соединения проявляют высокую активность в отношении широкого спектра бактериальных возбудителей инфекционных заболеваний: значения минимальных ингибирующих концентраций от 0,03 до 8 мкМ в отношении широкой панели грамотрицательных и грамположительных бактерий из группы «ESKAPE»-патогенов в тестах in vitro, сопоставимую с активностью липопептидного антибиотика полимиксина В и значительно превосходящую активность известного катионного АМП пексиганана («Pexiganan», «MSI-78», «Locilex»), который проходил за рубежом клинические испытания (3 фаза) в качестве антибиотика для наружного применения с широким спектром активности [Lamb, H.M., and Wiseman, L.R. Pexiganan Acetate // Drugs. 1998. Vol.56, 1047-1052].
Заявляемые пептиды характеризуется низкой гемолитической активностью (менее 10% при 128 мкМ) в диапазоне концентрации, при которых проявляется антибактериальный эффект. Техническим результатом изобретения является выраженная антибактериальная активность заявляемых соединений. Заявляемые пептиды состоят из 27 аминокислотных остатков, имеют линейную структуру и заряд+8 при нейтральных значениях pH, а также не несут дополнительных структурных модификаций. Заявляемые пептиды могут быть получены путем гетерологической экспрессии в бактериальной системе на основе Escherichia coli, а также с помощью химического синтеза.
Изобретение иллюстрируют графические материалы:
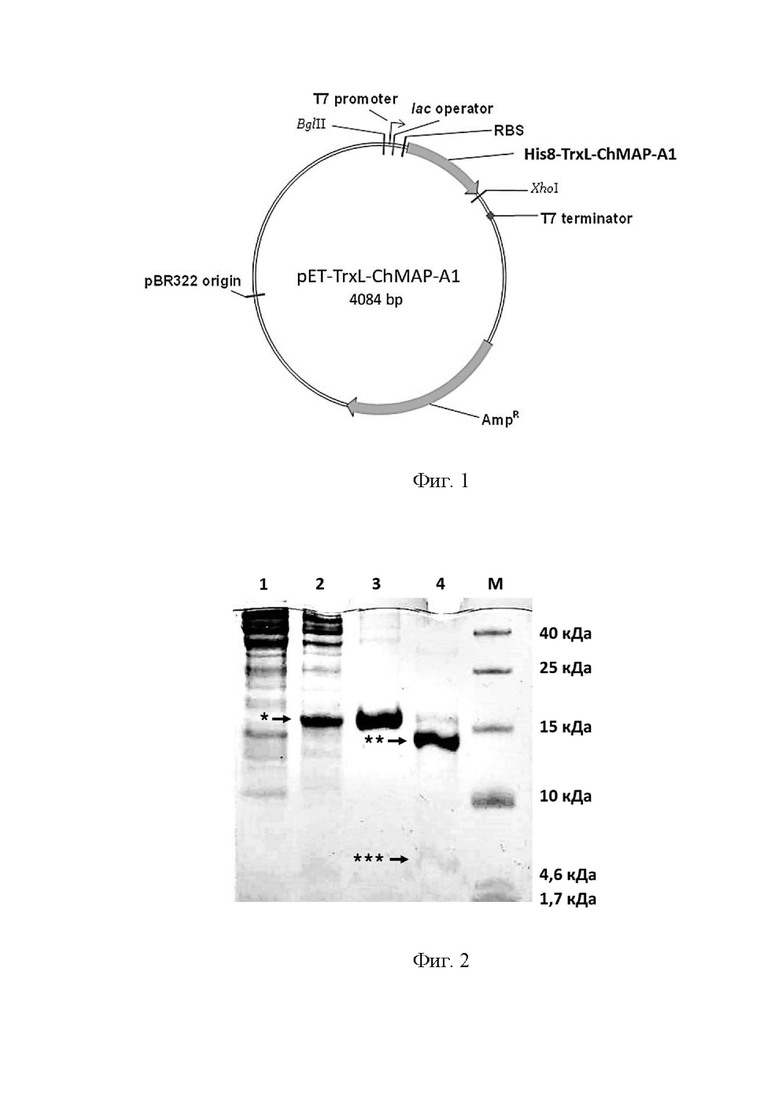
Фиг.1. Физическая карта плазмидного вектора для экспрессии пептида ChMAP-A1: pBR322 origin - участок инициации репликации плазмиды; AmpR - ген устойчивости к β-лактамным антибиотикам; T7 promoter - промотор транскрипции; T7 terminator - терминатор транскрипции; lac operator - сайт связывания lac-репрессора; RBS - сайт связывания рибосомы; His8-TrxL-ChMAP-A1 - последовательность, кодирующая гибридный белок, содержащий целевой пептид.
Фиг.2. Электрофоретический анализ биосинтеза, очистки и расщепления гибридного белка His8-TrxL-ChMAP-А1 (SEQ ID No. 7). 1 - суммарный клеточный лизат перед добавлением индуктора IPTG; 2 - суммарный клеточный лизат после индукции биосинтеза; 3 - элюат металлохелатной хроматографии; 4 - продукты расщепления гибридного белка бромцианом; М - стандарт М.М. (значения указаны в кДа). Стрелкой указаны: * - нерасщепленный гибридный белок, ** - белок-носитель после расщепления, *** - целевой пептид после расщепления.
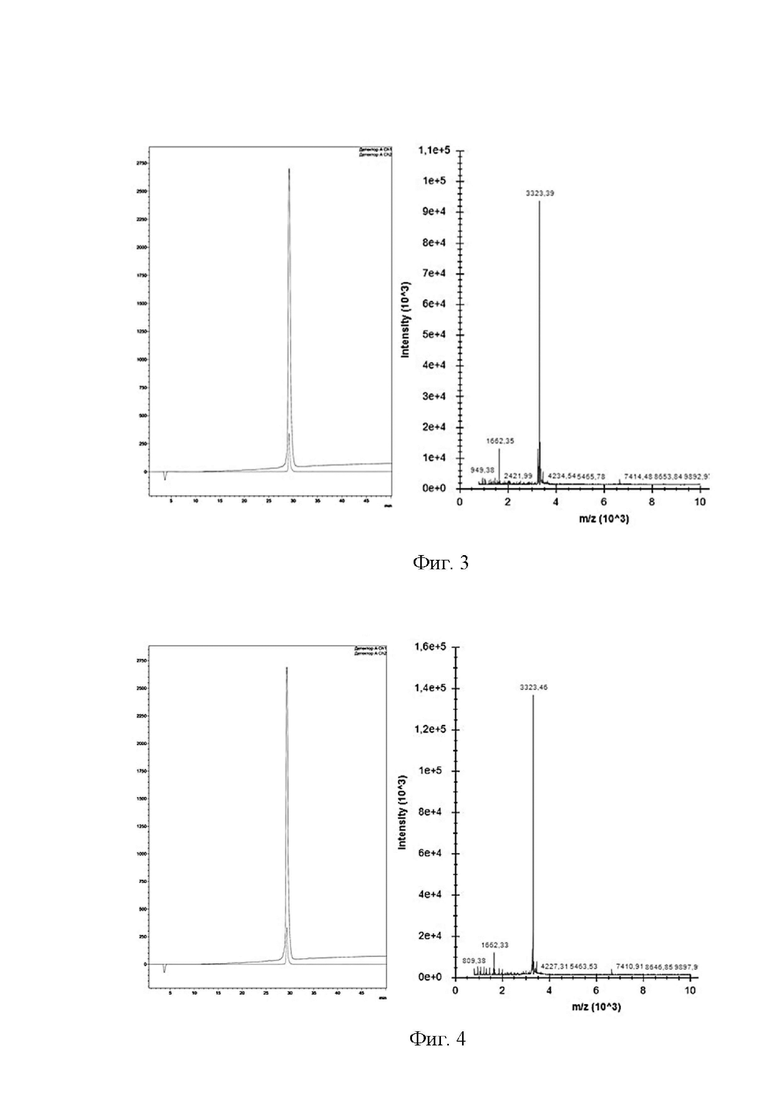
Фиг.3. ОФ-ВЭЖХ (слева) и MALDI-TOF (справа) анализ рекомбинантного пептида ChMAP-A1 (SEQ ID No. 2).
Фиг.4. ОФ-ВЭЖХ (слева) и MALDI-TOF (справа) анализ рекомбинантного пептида ChMAP-A2 (SEQ ID No. 3).
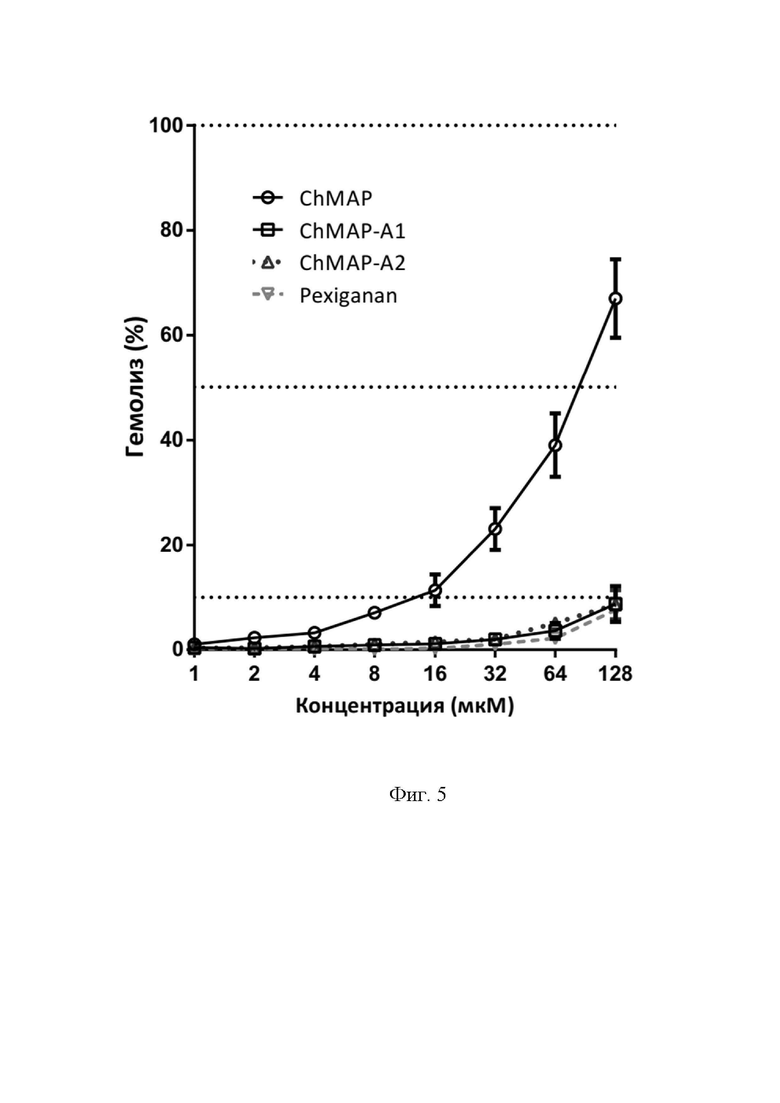
Фиг.5. Гемолитическая активность пептидов (SEQ ID No. 1-3) и пептида Pexiganan (SEQ ID No. 4) в отношении человеческих эритроцитов.
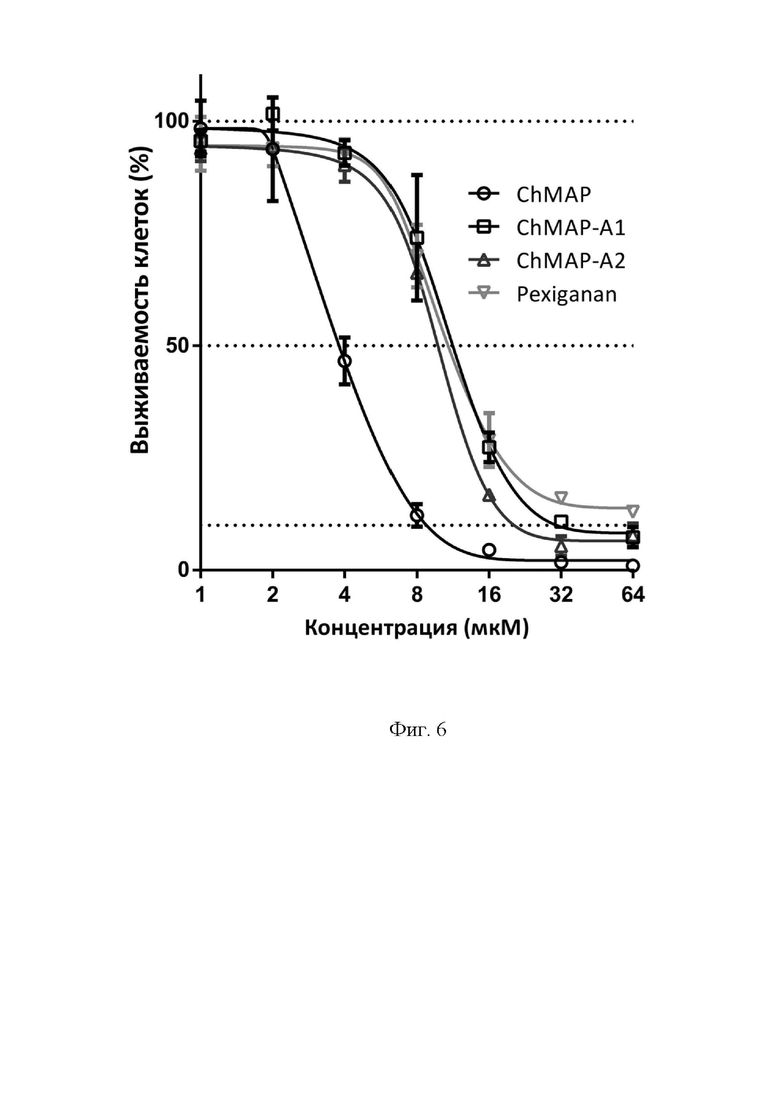
Фиг.6. Цитотоксичность пептидов (SEQ ID No. 1-3) и пептида Pexiganan (SEQ ID No. 4) в отношении клеточной линии эмбриональных фибробластов человека.
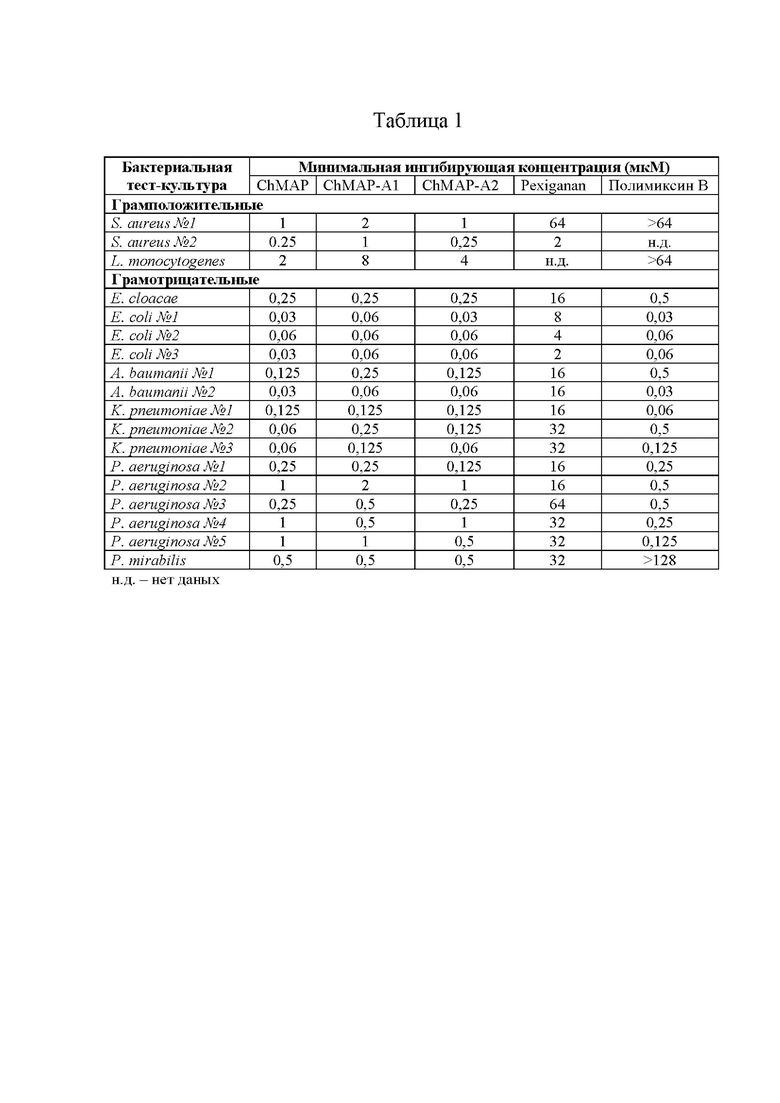
Таблица 1. Антибактериальная активность пептидов (SEQ ID No. 1-3), пептида Pexiganan (SEQ ID No. 4) и полимиксина В.
Изобретение иллюстрируют примеры.
Пример 1
Конструирование плазмид pET-TrxL-ChMAP-A1 и pET-TrxL-ChMAP-A2
Нуклеотидные последовательности SEQ ID No. 5-6, содержащие промотор транскрипции Т7 РНК-полимеразы, lac оператор, участок связывания рибосомы и участок, кодирующий гибридный белок (последовательно связанные гистидиновый октамер, тиоредоксин с заменой M37L, сайт расщепления бромцианом и целевой пептид), получают химико-ферментативным синтезом с помощью ПЦР. Олигонуклеотиды, используемые в ПЦР, синтезируют твердофазным фосфорамидитным методом с наращиванием олигонуклеотидной цепи в направлении от 3’-конца к 5’-концу с помощью защищенных фосфорамидитов - 5’-диметокситритил-N-ацил-2’-дезоксинуклеозид-3’-O-(β-цианэтилдиизопропиламино)-фосфитов, активированных тетразолом. Фрагмент ДНК, кодирующий белок-носитель тиоредоксин (M37L), получают методом ПЦР-амплификации и направленного мутагенеза с помощью ген-специфических праймеров, используя в качестве исходной матрицы плазмиду pET32a(+), содержащую ген тиоредоксина. Фрагменты ДНК, кодирующие целевые пептиды, получают с помощью ПЦР с использованием двух перекрывающихся праймеров. В ходе дизайна праймеров используют кодоны, предпочтительные для экспрессии в E.coli. Остальные участки последовательности, кодирующей гибридный белок, получают путем последовательного отжига и элонгации взаимно перекрывающихся олигонуклеотидов. На завершающей стадии синтеза последовательность амплифицируют с помощью праймеров, несущих на 5’-концах сайты узнавания рестриктаз BglII и XhoI. Продукт амплификации гидролизуют указанными рестриктазами, очищают электрофорезом в 1% агарозном геле, целевую полосу ДНК выделяют из геля с помощью колонки с силикагелем и лигируют с фрагментом ДНК размером 3,5 тыс.п.н., полученным в результате обработки плазмиды pET-20b(+) рестриктазами BglII и XhoI. В результате лигазной реакции получают кольцевые ковалентно замкнутые ДНК размером 4084 п.н. (Фиг.1). Продуктами лигазной реакции трансформируют компетентные клетки E.coli DH10B, приготовленные с помощью 0,1 М хлорида кальция. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 45 мин при 37°C и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина.
Первичный отбор клонов, содержащих нужные плазмиды, осуществляют методом «ПЦР с клонов». Отобранные клоны подращивают в жидкой питательной среде и выделяют плазмидную ДНК, которую анализируют на наличие вставки с помощью секвенирования по Сэнгеру. По данным секвенирования отбирают плазмиды с требуемой вставкой, нуклеотидные последовательности которых полностью соответствуют запланированным (SEQ ID No. 5,6).
Пример 2
Получение рекомбинантных пептидов
Проводят трансформацию компетентных клеток E.coli BL21(DE3), приготовленных с помощью 0,1 М хлорида кальция, плазмидными векторами, сборка которых описана в примере 1. После трансформации суспензию бактерий смешивают с питательной средой LB, растят 1 ч при 37°C и высевают на чашки Петри с LB-агаром, содержащим 100 мкг/мл ампициллина и 0,02 М глюкозы. Чашки инкубируют при 37°C в течение 18 ч.
Бактериологической петлей переносят выросшие колонии в 10 мл жидкой среды LB, содержащей 100 мкг/мл ампициллина, растят в течение 18 ч на термостатируемой качалке со скоростью вращения 220 об*мин-1 при температуре 37°C. Полученную культуру засевают в жидкую питательную среду LB, содержащую 0,02 М глюкозы, 100 мкг/мл ампициллина, 1 мМ MgSO4 и 0,1 мМ CaCl2 при этом начальная OD600 составляет 0,05. Индукцию биосинтеза гибридного белка осуществляют путем добавления изопропилтио-β-D-галактопиранозида (IPTG) к культуре клеток с оптической плотностью 0,8 до конечной концентрации 0,2 мМ. Культуру растят в течение 4-6 ч при температуре 30°С на термостатируемой качалке со скоростью вращения 220 об*мин-1.
После экспрессии клетки осаждают центрифугированием, ресуспендируют в фосфатном буфере (pH 7.8) с добавлением 6М гуанидин гидрохлорида и 20 мМ имидазола при помощи стеклянного гомогенизатора и разрушают путем ультразвуковой обработки. Лизат клеток центрифугируют при 25 000 g в течение 40 мин. Все работы по получению осветленного лизата проводят при температуре 4°С. Очистку гибридного белка, содержащего в качестве аффинной метки октагистидиновую последовательность, осуществляют с помощью металлохелатной хроматографии на препаративной колонке с Ni-NTA агарозой в денатурирующих условиях. Элюцию проводят повышением концентрации имидазола в буфере до 0,5 М. Собранную после очистки с помощью металлохелатной хроматографии фракцию, содержащую гибридный белок, титруют концентрированной соляной кислотой до значения pH 1,0, после чего добавляют равную массу бромциана (1 г бромциана на 1 г белка) и выдерживают при температуре 25°С в защищенном от света месте в течение 20 ч. Реакцию останавливают добавлением пятикратного объема деионизированной воды, после чего упаривают образцы на вакуумной центрифуге до исходного объема раствора и титруют до нейтрального значения pH.
Контроль уровня экспрессии, очистки и расщепления гибридного белка осуществляют методом денатурирующего трис-трицинового SDS-электрофореза в полиакриламидном геле. Расчетная молекулярная масса нефрагментированных гибридных белков (SEQ ID No. 7,8) составляет 16,8 кДа (Фиг.2). Финальную стадию очистки пептида проводят методом обращенно-фазовой ВЭЖХ (ОФ-ВЭЖХ) на колонке Reprosil-Pur C18-AQ в системе водных буферов, содержащих ацетонитрил и 0,1% ТФУ. Разделение происходит в линейном градиенте ацетонитрила от 5% до 80% за 60 мин. Выход пептидов детектируют по изменению оптического поглощения при двух длинах волн: 214 и 280 нм. Концентрацию водного раствора очищенного пептида ChMAP определяют методом спектрофотометрии по поглощению при 280 нм и расчета на основе коэффициентов экстинкции.
Далее проводили проверку чистоты и гомогенности образцов рекомбинантных антимикробных пептидов с помощью методов аналитической ОФ-ВЭЖХ и MALDI-TOF масс-спектрометрии (Фиг.3, Фиг.4). Хроматографическое разделение проводили с использованием аналитической колонки Symmetry 300 C18 (4,6 × 250 мм, 5 мкм, размер пор 300 Å; Waters) при объемной скорости потока 1 мл/мин в линейном градиенте концентрации ацетонитрила от 5 до 80% за 35 мин. Детектирование элюции целевых пептидов проводили при двух длинах волн: 214 и 280 нм. Анализ чистоты целевого пептида проводили путем автоматического сопоставления площадей пиков на хроматограмме. Масс-спектрометрический анализ проводился на MALDI-времяпролетном масс-спектрометре Ultraflex II (Bruker Daltonics). В качестве матрицы использовали 2,5-дигидроксибензойную кислоту в 20% ацетонитриле, 0,1% ТФУ в концентрации 10 мг/мл. Образцы готовили стандартным способом. При анализе всех фракций использовали режим рефлектрона.
Хроматографическая подвижность анализируемых пептидов находилась в диапазоне от 29 до 30 мин, что указывает на схожесть их физико-химических свойств, в первую очередь, доле гидрофобных аминокислотных остатков в структуре. Согласно результатам сопоставления площадей пиков на хроматограмме чистота анализируемых пептидов составляет не менее 95%. Экспериментальные значения m/z пиков для анализируемых пептидов соответствовали расчетным значениям средних молекулярных масс с учетом их протонирования в ходе масс-спектрометрического анализа (средняя молекулярная масса 3323,01 Да для пептидов ChMAP-A1 и ChMAP-A2). Полученные данные указывают на гомогенность препаратов и их высокую чистоту.
Пример 5
Тестирование антибактериальной активности пептида
Антибактериальную активность пептидов определяют методом двукратных серийных разведений в 96-луночных планшетах в жидкой питательной среде Мюллера-Хинтона (MHB) в присутствии 0,9% NaCl и инкубации с грамположительными (S. aureus, Listeria monocytogenes) и грамотрицательными (E.coli, P. aeruginosa, Proteus mirabilis, A. baumanii, Enterobacter cloacae, K. pneumoniae) тест-культурами бактерий, для некоторых из которых было проанализировано несколько штаммов. В качестве антибактериальных соединений сравнения используют антибиотик «последней линии» полимиксин В и известный пептидный антибиотик, разработанный на основе природного АМП магейнина линейный α-спиральный пептид Pexiganan, права на который в настоящий момент принадлежат компании Dipexium Pharmaceuticals, Inc. Тест-культуры высевают из консерва в 10 мл жидкой среды МНВ без антибиотика и растят в течение 18 ч при 37°С и 220 об*мин-1. После этого аликвоту культуры объемом 300 мкл добавляют к 6 мл среды MHB и инкубируют в термостатируемой качалке при 37°С до достижения культурой оптической плотности OD600 1,0. Аликвоты тест-культуры объемом 50 мкл, содержащие по 2*105 КОЕ, добавляют к 50 мкл растворов пептидов, предварительно разведенных от 64 до 0,031 мкМ в пересчете на конечную концентрацию в лунке c помощью стерильного 0,1% раствора бычьего сывороточного альбумина. После добавления культуры, планшет инкубируют в течение 24 часов при 37°С и интенсивном перемешивании (1000 об*мин-1). Значения минимальных ингибирующих концентраций (МИК) определяются визуально и спектрофотометрически, как минимальная концентрация пептида, при которой отсутствует рост культуры. Эксперименты проводят в течение трех раз в трехкратной повторности, причем итоговую МИК рассчитывают как медиану девяти полученных значений. Полученные данные представлены в Таблице 1. В отличие от полимиксина В и пептида Pexiganan аналоги ChMAP-A1 (SEQ ID No. 2) и ChMAP-A2 (SEQ ID No. 3) проявляют высокую активность в отношении всех протестированных бактерий и сопоставимую с таковой для пептида дикого типа ChMAP. Примечательно, что значения МИК для пептида ChMAP и его аналогов как минимум на порядок ниже по сравнению с таковыми для пептида Pexiganan, разработанного на основе α-спирального магейнина.
Пример 6
Тестирование гемолитической активности пептида
Для тестирования гемолитической активности пептида используют свежевыделенные человеческие эритроциты. Для предотвращения свертывания к цельной крови добавляют цитратный буфер. Кровь центрифугируют в растворе фиколла и урографина плотностью 1,077 г/мл в течение 15 мин при 1500 об*мин-1. Фракцию эритроцитов отбирают со дна и трижды промывают двадцатью объемами изотонического натрий-фосфатного буфера (pH 7,4), последовательно осаждая эритроциты путем центрифугирования при 2000 об*мин-1 в течение 10 мин. После отмывки готовят 8% суспензию эритроцитов в изотоническом натрий-фосфатном буфере.
Для теста в 96-луночном планшете готовят серии двойных разведений исследуемого пептида от 128 до 1 мкМ (в пересчете на конечную концентрацию) объемом 50 мкл. После этого к раствору пептида добавляют по 50 мкл 8% суспензии эритроцитов. Планшет инкубируют в течение 1,5 ч при 37°С и перемешивании 1000 об*мин-1. После инкубации планшеты центрифугируют в течение 15 мин при 3000 об*мин-1 для осаждения интактных эритроцитов. Далее аликвоты супернатанта переносят в другой планшет для измерения количества свободного гемоглобина. Определение количества гемоглобина в растворе осуществляют по поглощению раствора при 405 нм. В качестве отрицательного контроля (K-) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в растворе натрий-фосфатного буфера без добавления пептидов. В качестве положительного контроля (K+) используют супернатант, полученный после центрифугирования эритроцитов, инкубировавшихся в 0,1% водном растворе неионогенного детергента Triton X-100, вызывающего их полный лизис. Эксперименты проводят дважды с кровью одного и того же человека в трехкратной повторности. Процент гемолиза рассчитывают по формуле:
гемолиз (%)=(OD405 пробы - OD405 «K-»)×100%/(OD405 «K+» - OD405 «K-»)
Результаты тестирования свидетельствуют о том, что в отличие от родоначального пептида ChMAP (SEQ ID No. 1), который является умеренным цитолитиком (более 50% лизис при 128 мкМ), пептиды ChMAP-A1 (SEQ ID No. 2) и ChMAP-A2 (SEQ ID No. 3) обладают слабо выраженными гемолитическими свойствами (менее 10% лизис при 128 мкМ), сопоставимыми с таковыми для пептида сравнения Pexiganan (SEQ ID No. 4).
Пример 7
Тестирование цитотоксического действия пептида
Тестирование цитотоксического действия АМП в отношении нормальных клеток млекопитающих проводили с помощью МТТ-теста. Методика основана на способности дегидрогеназ живых клеток, восстанавливать 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-2H-тетразолий бромид (МТТ-реагент) до нерастворимого в воде фиолетового кристаллического фармазана. Клеточные линии человеческих эмбриональных фибробластов (HEF) высаживали в 96-луночные планшеты (по 104 клеток в каждую лунку) и растили в среде DMEM/F-12 в присутствии 10% эмбриональной телячьей сыворотки (ЭТС) в течение 24 ч при 37°С в CO2-инкубаторе (5% CO2 в воздухе). Далее культуральную жидкость заменяли свежей средой, в которой предварительно растворяли тестируемый пептид. После инкубации в течение 24 ч в вышеописанных условиях в каждую лунку добавляли по 20 мкл МТТ (5 г/л), после чего продолжали инкубацию еще 4 ч. Аккуратно удаляли среду, добавляли в лунки по 100 мкл смеси диметилсульфоксида (ДМСО) и этилового спирта (1:1) для растворения кристаллов формазана и измеряли оптическую плотность растворов при 570 нм в планшетном спектрофотометре. Долю живых клеток определяли по формуле:
Выживаемость клеток (%)=[(OD570 пробы - OD570 «K-»)/(OD570 клетки без пептида - OD570 «K-»)]×100%,
где «K-» фоновое поглощение лунки с растворителем. Эксперименты проводились дважды в трехкратной повторности. С помощью математической модели нелинейной регрессии строят графики сглаживающих кривых для экспериментальных значений выживаемости клеток. Показано, что аналоги ChMAP-A1 (SEQ ID No. 2) и ChMAP-A2 (SEQ ID No. 3) обладают пониженной цитотоксичностью в отношении фибробластов (концентрация полуингибирования около 10 мкМ) по сравнению с родоначальным пептидом ChMAP (SEQ ID No. 1). Важно отметить, что модифицированные аналоги имеют профиль цитотоксичности сопоставимый с пептидом Pexiganan (SEQ ID No. 4), который, ранее достиг 3 фазы КИ как препарат наружного применения, однако, в значительной степени превосходят его по уровню антибактериальной активности in vitro.
Перечень аминокислотных и нуклеотидных последовательностей
SEQ ID No. 1 Аминокислотная последовательность пептида ChMAP
SEQ ID No. 2 Аминокислотная последовательность модифицированного аналога ChMAP-A1
SEQ ID No. 3 Аминокислотная последовательность модифицированного аналога ChMAP-A2
SEQ ID No. 4 Аминокислотная последовательность антимикробного пептида пексиганана
SEQ ID No. 5 Нуклеотидная последовательность вставки (экспрессионной кассеты для получения ChMAP-A1)
SEQ ID No. 6 Нуклеотидная последовательность вставки (экспрессионной кассеты для получения ChMAP-A2)
SEQ ID No. 7 Аминокислотная последовательность гибридного белка His8-TrxL-ChMAP-А1
SEQ ID No. 8 Аминокислотная последовательность гибридного белка His8-TrxL-ChMAP-А2
--->
Перечень последовательностей
<110> IBCH RAS
Panteleev, Pavel
Bolosov, Ilia
Ovchinnikova, Tatiana
<120> Катионный пептид, обладающий антибактериальными свойствами
<130> (Reference Number)
<160> 8
<170> PatentIn version 3.5
<210> 1
<211> 27
<212> PRT
<213> Capra hircus
<220> Аминокислотная последовательность пептида ChMAP
<223> Capra hircus
<400> 1
Gly Arg Phe Lys Arg Phe Arg Lys Lys Leu Lys Arg Leu Trp His Lys
1 5 10 15
Val Gly Pro Phe Val Gly Pro Ile Leu His Tyr
20 25
<210> 2
<211> 27
<212> PRT
<213> Artificial Sequence
<220> Аминокислотная последовательность модифицированного аналога ChMAP-A1
<223> Artificial Sequence
<400> 2
Gly Arg Phe Lys Arg Phe Arg Lys Lys Ala Lys Arg Leu Trp His Lys
1 5 10 15
Val Gly Pro Phe Val Gly Pro Ile Leu His Tyr
20 25
<210> 3
<211> 27
<212> PRT
<213> Artificial Sequence
<220> Аминокислотная последовательность модифицированного аналога ChMAP-A2
<223> Artificial Sequence
<400> 3
Gly Arg Phe Lys Arg Phe Arg Lys Lys Leu Lys Arg Ala Trp His Lys
1 5 10 15
Val Gly Pro Phe Val Gly Pro Ile Leu His Tyr
20 25
<210> 4
<211> 26
<212> PRT
<213> Artificial Sequence
<220> Аминокислотная последовательность антимикробного пептида пексиганана
<223> Artificial Sequence
<400> 4
Gly Ile Gly Lys Phe Leu Lys Lys Ala Lys Lys Phe Gly Lys Ala Phe
1 5 10 15
Val Lys Ile Leu Lys Lys
20
<210> 5
<211> 585
<212> DNA
<213> Artificial Sequence
<220> Нуклеотидная последовательность вставки (экспрессионной кассеты для
получения ChMAP-A1)
<223> Artificial sequence
<400> 5
agatctgcgg gatctcgatc ccgcgaaatt aatacgactc actatagggg aattgtgagc 60
ggataacaat tcccctctag agtcgacgga tcttacttta agaaggagat atacatatga 120
gccatcacca ccaccatcac catcacggat ctagcgataa aattattcac ctgactgacg 180
acagttttga cacggatgta ctcaaagcgg acggggcgat cctcgtcgat ttctgggcag 240
agtggtgcgg tccgtgcaaa ctgatcgccc cgattctgga tgaaatcgct gacgaatatc 300
agggcaaact gaccgttgca aaactgaaca tcgatcaaaa ccctggcact gcgccgaaat 360
atggcatccg tggtatcccg actctgctgc tgttcaaaaa cggtgaagtg gcggcaacca 420
aagtgggtgc actgtctaaa ggtcagttga aagagttcct cgacgctaac ctggccggat 480
ctcatatggg tcgcttcaaa cgctttcgca aaaaggcgaa acgtctttgg cataaggttg 540
gcccgttcgt gggtccaatt ttacactact aagaattctc tcgag 585
<210> 6
<211> 585
<212> DNA
<213> Artificial Sequence
<220> Нуклеотидная последовательность вставки (экспрессионной кассеты для
получения ChMAP-A2)
<223> Artificial sequence
<400> 6
agatctgcgg gatctcgatc ccgcgaaatt aatacgactc actatagggg aattgtgagc 60
ggataacaat tcccctctag agtcgacgga tcttacttta agaaggagat atacatatga 120
gccatcacca ccaccatcac catcacggat ctagcgataa aattattcac ctgactgacg 180
acagttttga cacggatgta ctcaaagcgg acggggcgat cctcgtcgat ttctgggcag 240
agtggtgcgg tccgtgcaaa ctgatcgccc cgattctgga tgaaatcgct gacgaatatc 300
agggcaaact gaccgttgca aaactgaaca tcgatcaaaa ccctggcact gcgccgaaat 360
atggcatccg tggtatcccg actctgctgc tgttcaaaaa cggtgaagtg gcggcaacca 420
aagtgggtgc actgtctaaa ggtcagttga aagagttcct cgacgctaac ctggccggat 480
ctcatatggg tcgcttcaaa cgctttcgca aaaagctgaa acgtgcttgg cataaggttg 540
gcccgttcgt gggtccaatt ttacactact aagaattctc tcgag 585
<210> 7
<211> 151
<212> PRT
<213> Artificial Sequence
<220> Аминокислотная последовательность гибридного белка His8-TrxL-ChMAP-А1
<223> Artificial Sequence
<400> 7
Met Ser His His His His His His His His Gly Ser Ser Asp Lys Ile
1 5 10 15
Ile His Leu Thr Asp Asp Ser Phe Asp Thr Asp Val Leu Lys Ala Asp
20 25 30
Gly Ala Ile Leu Val Asp Phe Trp Ala Glu Trp Cys Gly Pro Cys Lys
35 40 45
Leu Ile Ala Pro Ile Leu Asp Glu Ile Ala Asp Glu Tyr Gln Gly Lys
50 55 60
Leu Thr Val Ala Lys Leu Asn Ile Asp Gln Asn Pro Gly Thr Ala Pro
65 70 75 80
Lys Tyr Gly Ile Arg Gly Ile Pro Thr Leu Leu Leu Phe Lys Asn Gly
85 90 95
Glu Val Ala Ala Thr Lys Val Gly Ala Leu Ser Lys Gly Gln Leu Lys
100 105 110
Glu Phe Leu Asp Ala Asn Leu Ala Gly Ser His Met Gly Arg Phe Lys
115 120 125
Arg Phe Arg Lys Lys Ala Lys Arg Leu Trp His Lys Val Gly Pro Phe
130 135 140
Val Gly Pro Ile Leu His Tyr
145 150
<210> 8
<211> 151
<212> PRT
<213> Artificial Sequence
<220> Аминокислотная последовательность гибридного белка His8-TrxL-ChMAP-А2
<223> Artificial Sequence
<400> 8
Met Ser His His His His His His His His Gly Ser Ser Asp Lys Ile
1 5 10 15
Ile His Leu Thr Asp Asp Ser Phe Asp Thr Asp Val Leu Lys Ala Asp
20 25 30
Gly Ala Ile Leu Val Asp Phe Trp Ala Glu Trp Cys Gly Pro Cys Lys
35 40 45
Leu Ile Ala Pro Ile Leu Asp Glu Ile Ala Asp Glu Tyr Gln Gly Lys
50 55 60
Leu Thr Val Ala Lys Leu Asn Ile Asp Gln Asn Pro Gly Thr Ala Pro
65 70 75 80
Lys Tyr Gly Ile Arg Gly Ile Pro Thr Leu Leu Leu Phe Lys Asn Gly
85 90 95
Glu Val Ala Ala Thr Lys Val Gly Ala Leu Ser Lys Gly Gln Leu Lys
100 105 110
Glu Phe Leu Asp Ala Asn Leu Ala Gly Ser His Met Gly Arg Phe Lys
115 120 125
Arg Phe Arg Lys Lys Leu Lys Arg Ala Trp His Lys Val Gly Pro Phe
130 135 140
Val Gly Pro Ile Leu His Tyr
145 150
<---
Изобретение относится к области биотехнологии, конкретно к модифицированным вариантам пептида кателицидина, и может быть использовано в медицине и ветеринарии как антимикробное средство. Предложены модифицированные пептиды, обладающие антимикробной активностью в отношении грамположительных и грамотрицательных бактерий. Изобретение позволяет сохранить высокую антибактериальную активность пептида кателицидина дикого типа и, вместе с тем, снизить цитотоксические свойства в отношении нормальных клеток человека. 2 н.п. ф-лы, 1 табл., 7 пр., 6 ил.
1. Пептид, обладающий антимикробной активностью в отношении грамположительных и грамотрицательных бактерий и имеющий аминокислотную последовательность SEQ ID NO: 2.
2. Пептид, обладающий антимикробной активностью в отношении грамположительных и грамотрицательных бактерий и имеющий аминокислотную последовательность SEQ ID NO: 3.
| Пептид, проявляющий антибактериальные и противоопухолевые свойства | 2019 |
|
RU2702661C1 |
| PANTELEEV P.V | |||
| et al., Combined Antibacterial Effects of Goat Cathelicidins With Different Mechanisms of Action, Front | |||
| Microbiol., 2018, v.9, art.2983 | |||
| KOPEIKIN P.M | |||
| et al., Caprine Bactenecins as Promising Tools for Developing New Antimicrobial and Antitumor Drugs, Front Cell Infect Microbiol., 2020, v.10, art.552905. | |||
Авторы
Даты
2022-08-26—Публикация
2021-10-20—Подача