Изобретение относится к медицине, а именно к иммунологии, кардиологии и эндокринологии, и может быть использовано для диагностики метавоспаления у пациентов с ишемической болезнью сердца (ИБС) и сахарным диабетом (СД) 2 типа.
В последнее время концепция патогенеза сахарного диабета 2 типа неразрывно связана с понятием метавоспаления. Этот термин был впервые введен Геканом Хотэмислигилом, и подразумевает развитие иммунологической дисфункции на фоне нарушения метаболического гомеостаза [1]. Инсулинорезистентность является отличительной чертой, как классического воспаления, так и метавоспаления. Однако, в отличие от классического воспаления, которое условно назвали «горячее воспаление», при метавоспалении, или «холодном воспалении», отсутствует патоген и его эрадикация, а индуктором является дисфункция метаболически активных тканей, которая сохраняется на протяжении длительного времени и способствует поддержанию провоспалительного фона, и, как следствие, системных метаболических нарушений [2].
Т-регуляторные лимфоциты представляют собой субпопуляцию CD4+ Т-лимфоцитов с противовоспалительной активностью [3]. По результатам проведенного ранее мета-анализа для пациентов с СД 2 типа характерно снижение содержания CD4+CD25+Foxp3+T-регуляторных лимфоцитов, и их ключевого цитокина IL-10 [3]. С другой стороны, в некоторых крупных исследованиях, содержание T-регуляторных лимфоцитов у пациентов с СД 2 типа не отличалось от такового у пациентов без СД 2 типа [4, 5]. Объяснением может служить увеличение продукции T-регуляторных лимфоцитов при СД 2 типа, наблюдаемое на начальном этапе заболевания, которое затем сменяется истощением иммунорегуляторного резерва и развитием дефицита T-регуляторных клеток. При этом образуются клетки с фенотипом CD4+CD25lowFoxP3+ [6], определение содержания которых у пациентов с СД 2 типа в настоящее время не проводится.
Известен способ неинвазивной диагностики метавоспаления, заключающийся в определении содержания С-реактивного белка (СРБ) [7]. У пациентов с СД 2 типа содержание СРБ варьирует в пределах 4,49 – 16,48 мг/л [8].
Недостатком способа является то, что увеличение содержания СРБ является неспецифичным для метавоспаления [9]. Поэтому актуальным является поиск новых диагностических биомаркеров воспаления у пациентов с СД 2 типа в периферической крови.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задачей изобретения является разработка способа диагностики метавоспаления у пациентов с сочетанием ИБС и СД 2 типа.
Поставленная задача решается путем определения относительного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов от всех CD4+ лимфоцитов в периферической крови, затем по данным абсолютного содержания лимфоцитов, полученным в ходе общего анализа крови на автоматическом гематологическом анализаторе, рассчитывают абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови, и при суммарном абсолютном содержании CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови равном 1,39×107 клеток/л и более диагностируют метавоспаление.
Новым в предлагаемом способе является то, что для диагностики метавоспаления проводят оценку относительного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов от всех CD4+ лимфоцитов в периферической крови, и по данным общего анализа крови рассчитывают суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови. При содержании CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови равном 1,39×107 клеток/л крови и более диагностируют метавоспаление у пациентов с ишемической болезнью сердца и сахарным диабетом 2 типа.
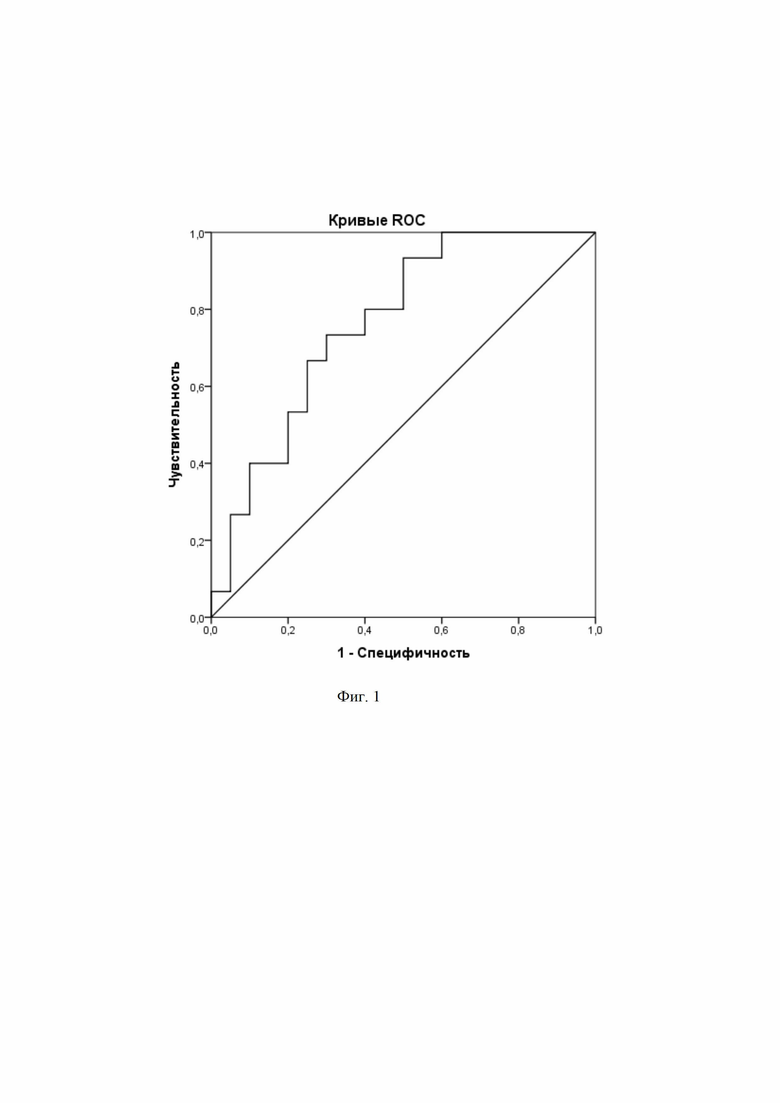
Изобретение будет понятно из следующего описания и приложенных к нему фигур. На фиг. 1 представлена ROC-кривая для оценки предсказательной мощности пограничных значений суммарного абсолютного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови у пациентов с сочетанием ишемической болезни сердца и сахарного диабета 2 типа.
Способ осуществляют следующим образом.
В исследование были включены 20 пациентов с ишемической болезнью сердца и 15 пациентов с сочетанием ишемической болезни сердца и СД 2 типа, госпитализированных в клиники Научно-исследовательского института кардиологии. Критериями включения являлись диагноз ИБС и СД 2 типа, соответственно, которые были выставлены в предыдущую госпитализацию на основании данных анамнеза, объективного обследования, инструментальных и лабораторных методов. Критерии исключения: наличие воспалительных процессов любой локализации. Пациенты не имели существенных различий по основным клиническим данным, все находились на регулярной кардиоактивной терапии. Все пациенты подписали информированное согласие на участие в исследовании после беседы и ответов на вопросы. Протокол исследования был одобрен комитетом по биомедицинской этике НИИ кардиологии (протокол №210 от 18.02.2021).
В утренние часы натощак осуществляли взятие крови из кубитальной вены в объеме 4 мл в пробирку с гепарином для получения фракции мононуклеарных лейкоцитов и в объеме 2 мл в пробирку с этилендиаминтетрауксусной кислотой (ЭДТА) для проведения общего анализа крови. Полученные образцы крови при комнатной температуре доставляли в клинико-диагностическую лабораторию. Путем центрифугирования на градиенте плотности Histopaque 1077 (Sigma Aldrich, США) получали фракцию мононуклеарных лейкоцитов периферической крови. Клетки окрашивали моноклональными антителами к поверхностным антигенам, конъюгированными с флуорохромами: анти-CD4 FITC, анти-CD25 PE (BD Pharmingen, США), остаточные эритроциты лизировали, фиксировали клетки и пермеабилизировали с помощью специального набора буферов для окрашивания FoxP3+ Т-регуляторных лимфоцитов в течение 30 минут (BD Pharmingen, США), а затем проводили окрашивание с помощью моноклональных антител к FoxP3, конъюгированных с флуорохромом AF647 (BD Pharmingen, США) в течение 40 минут, затем клетки отмывали от несвязавшегося флуорохрома двукратно отмывочным буфером (BD Pharmingen, США) и фиксировали с помощью буфера CellFix (BD Pharmingen, США). Клетки собирали на проточном цитометре FACSCalibur (Becton Dickinson, США) с помощью программного обеспечения CellQuestPro (BD Biosciences, США). С помощью последовательного гейтирования выделяли регион лимфоцитов на гистограмме с параметрами «Прямое светорассеяние (FSC)» и «Боковое светорассеяние (SSC)», затем выделяли CD4+ Т-лимфоциты на гистограмме с параметрами «Боковое светорассеяние (SSC)» и «Интенсивность флуоресценции CD4», среди которых выделяли CD25lowFoxP3+ клетки на гистограмме с параметрами «Интенсивность флуоресценции CD25» и «Интенсивность флуоресценции FoxP3». Результаты выражали в виде относительного содержания CD4+CD25lowFoxP3+ клеток от всех CD4+ лимфоцитов. Используя результаты общего анализа крови (абсолютное содержание лимфоцитов), рассчитывали суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови.
При анализе данных определили, что пациенты с ИБС и с сочетанием ИБС и СД 2 типа статистически значимо различаются по суммарному абсолютному содержанию CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови (р=0,025). Для выявления пороговой величины суммарного абсолютного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови, свойственной для пациентов с сочетанием ИБС и СД 2 типа, построили ROC (Receiver Operating Characteristics)-кривую (фиг. 1). По данным ROC-анализа для пациентов с СД 2 типа оказалось свойственным увеличение суммарного абсолютного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови 1,39×107 клеток/л и более (площадь под кривой: 0,763; чувствительность: 73,3%; специфичность: 70%) (Таблица 1). В связи с тем, что площадь под кривой была приближена к 80%, суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови можно рассматривать в качестве хорошего классификатора наличия метавоспаления у пациентов с сочетанием ИБС и СД 2 типа [10].
Таблица 1.
Координаты ROC-кривой для оценки предсказательной мощности пограничных значений суммарного абсолютного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови
если больше или равноa
Ниже приводятся 3 клинических примера использования разработанного способа.
Пример 1.
Пациентка Ф., 57 лет, поступила в плановом порядке в отделение атеросклероза и хронической ИБС для проведения аорто-коронарного шунтирования по поводу многососудистого стенозирующего атеросклероза коронарных артерий.
Основное заболевание: ИБС: стенокардия напряжения, ФК III. Атеросклероз коронарных артерий: стеноз передней нисходящей артерии 75% в дистальной трети, стеноз ветви тупого края 75%
Фоновое заболевание: Гипертоническая болезнь III стадии, достигнутая степень артериальной гипертонии 2, риск 4. Гипертрофия левого желудочка. Дислипидемия. Сахарный диабет 2 типа с потребностью в инсулине, целевой гликированный гемоглобин менее 7,5%, достигнутый гликированный гемоглобин 12,4%. Диабетическая непролиферативная ретинопатия. Ожирение I ст.
Жалобы: ангинозные боли соответствуют III ФК.
Из анамнеза: давящие боли за грудиной при небольшой физической нагрузке.
Сахарный диабет 2 типа поставлен 12 лет назад. Отмечает увеличение гликемии до 17-20 ммоль/л постоянно натощак.
Объективно: общее состояние удовлетворительное, ИМТ 34,6 кг/м2. Содержание глюкозы натощак 12,8 ммоль/л; содержание глюкозы через 2 часа после стандартной пищевой нагрузки 14,1 ммоль/л; содержание гликированного гемоглобина 11,26%; содержание общего холестерола 3,26 ммоль/л; содержание триглицеридов 1,26 ммоль/л; содержание холестерола липопротеинов высокой плотности 1,04 ммоль/л; содержание холестерола липопротеинов низкой плотности 1,66 ммоль/л; содержание высокочувствительного С-реактивного белка составило 6,95 мг/л.
Проведено исследование согласно предлагаемому способу:
Суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови составило 3,09×107 клеток/л крови.
Таким образом, у пациентки выявлено наличие метавоспаления.
Пример 2.
Пациентка Л., 78 лет, поступила в плановом порядке в отделение атеросклероза и хронической ИБС для проведения аорто-коронарного шунтирования по поводу многососудистого стенозирующего атеросклероза коронарных артерий.
Основное заболевание: ИБС, стенокардия напряжения III ФК. Атеросклероз коронарных артерий (стеноз задне-боковой артерии 70%, проксимальный сегмент огибающей артерии 40%, изгиб ствола левой коронарной артерии 50%). Критический стеноз аортального клапана с трансклапанным градиентом 160/60 мм рт. ст.
Фоновое заболевание: Гипертоническая болезнь III стадия, достигнутый целевой уровень АД, риск 4. Гипертрофия левого желудочка. Атеросклероз сонных (слева в бифуркации общей сонной артерии 40%, в устье внутренней сонной артерии до 40%, в устье внутренней сонной артерии до 45%), бедренных артерий (справа по ходу подколенной артерии до 50%, слева по ходу общей бедренной артерии 20%, по ходу поверхностной бедренной артерии 20-23%). Хроническая ишемия головного мозга II ст. Дислипидемия. Сахарный диабет 2 типа, впервые выявленный.
Жалобы: увеличение артериального давления до 170-180/… мм рт. ст. (подташнивание, жар), больше в ночное время и под утро; одышка при ходьбе по ровному месту >100 м, >1 пролета лестницы; тупая ноющая боль в левой половине грудной клетки, появляется в покое, при физической нагрузке уменьшается и исчезает.
Из анамнеза: в 2015 году выявлен сложный аортальный порок (сейчас на УЗИ сердца критический аортальный стеноз с градиентом 150/86 мм рт. ст., аортальная регургитация 1 ст.). Не обследовалась, не наблюдалась. Сейчас при появлении болей в грудной клетке вновь обратилась к кардиологу, сделали УЗИ, направили на госпитализацию. В предыдущую госпитализацию проведено обследование. Консультирована кардиохирургом – показано оперативное лечение: протезирование аорты+аорто-коронарное шунтирование.
Объективно: общее состояние удовлетворительное. ИМТ 27,57 кг/м2. Содержание глюкозы натощак 19,8 ммоль/л, содержание глюкозы через 2 часа после стандартной пищевой нагрузки 23,00 ммоль/л, содержание гликированного гемоглобина 8,4%, содержание общего холестерола 4,35 ммоль/л, содержание триглицеридов 1,04 ммоль/л, содержание холестерола липопротеинов высокой плотности 1,74 ммоль/л, содержание холестерола липопротеинов низкой плотности 2,13 ммоль/л; содержание высокочувствительного С-реактивного белка составило 0,54 мг/л.
Проведено исследование согласно предлагаемому способу:
Суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови составило 1,39×107 клеток/л крови.
Таким образом, у пациентки выявлено наличие метавоспаления.
Пример 3.
Пациент К., 59 лет, поступил в плановом порядке в кардиохирургическое отделение №1 для обследования и определения тактики лечения.
Основное заболевание: ИБС: атеросклероз коронарных артерий (стеноз первой ветив диагональной артерии 80%). Гипертрофическая кардиомиопатия с обструкцией выводного отдела с градиентом 85 мм. рт. ст.
Фоновое заболевание: Гипертоническая болезнь III стадия, достигнута 1 степень, дислипидемия. Атеросклероз сонных артерий: стеноз внутренней сонной артерии с обеих сторон менее 25%. Атеросклероз сосудов нижних конечностей: стеноз общей бедренной артерии с обеих сторон до 30%, стеноз поверхностной бедренной артерии с обеих сторон до 50%. Риск 4.
Объективно: общее состояние удовлетворительное. ИМТ 20,3 кг/м2. Содержание глюкозы натощак 5,15 ммоль/л; содержание глюкозы через 2 часа после стандартной пищевой нагрузки 5,7 ммоль/л; содержание гликированного гемоглобина 5,65%; содержание общего холестерола 3,28 ммоль/л; содержание триглицеридов 0,77 ммоль/л; содержание холестерола липопротеинов высокой плотности 1,18 ммоль/л; содержание холестерола липопротеинов низкой плотности 1,75 ммоль/л; содержание высокочувствительного С-реактивного белка составило 2,28 мг/л.
Проведено исследование согласно предлагаемому способу:
Суммарное абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови составило 0,44×107 клеток/л крови.
Таким образом, у пациента метавоспаление отсутствует.
Предлагаемый в качестве изобретения способ апробирован на 35 больных, может быть использован в практическом здравоохранении для выявления наличия метавоспаления и повышает качество диагностики у пациентов с ишемической болезнью сердца и сахарным диабетом 2 типа.
Источники информации:
1. Hotamisligil G.S. Inflammation, metaflammation and immunometabolic disorders // Nature. 2017; 542(7640):177-185.
doi: 10.1038/nature21363
2. Calay E., Hotamisligil G. Turning off the inflammatory, but not the metabolic, flames // Nat Med. 2013; 19: 265–267
doi: 10.1038/nm.3114
3. Qiao Y.C., Shen J., He L., et al. Changes of Regulatory T Cells and of Proinflammatory and Immunosuppressive Cytokines in Patients with Type 2 Diabetes Mellitus: A Systematic Review and Meta-Analysis // J Diabetes Res. 2016; 2016: 3694957.
doi: 10.1155/2016/3694957
4. Afzal N., Zaman S., Shahzad F., et al. Immune mechanisms in type-2 diabetic retinopathy // J Pak Med Assoc. 2015; 65(2): 159-63.
5. Rattik S., Engelbertsen D., Wigren M., et al. Elevated circulating effector memory T cells but similar levels of regulatory T cells in patients with type 2 diabetes mellitus and cardiovascular disease // Diab Vasc Dis Res. 2019;16(3): 270-280.
doi: 10.1177/1479164118817942
6. Ferreira R.C., Simons H.Z., Thompson W.S., et al. Cells with Treg-specific FOXP3 demethylation but low CD25 are prevalent in autoimmunity // J Autoimmun. 2017; 84: 75-86.
doi: 10.1016/j.jaut.2017.07.009
7. Tabassum R., Mia A.R., Reza-Ul-Haq K.M., et al. C-reactive Protein Level in Type-2 Diabetic Patients Attending Mymensingh Medical College Hospital, Mymensingh // Mymensingh Med J. 2017; 26(1): 56-60.
8. Stanimirovic J., Radovanovic J., Banjac K., et al. Role of C-Reactive Protein in Diabetic Inflammation // Mediators Inflamm. 2022; 2022: 3706508.
doi: 10.1155/2022/3706508
9. Lee C.C., Adler A.I., Sandhu M.S. et al. Association of C-reactive protein with type 2 diabetes: prospective analysis and meta-analysis // Diabetologia. 2009; 52: 1040–1047.
doi: 10.1007/s00125-009-1338-3
10. Carter J.V., Pan J., Rai S.N., Galandiuk S. ROC-ing along: Evaluation and interpretation of receiver operating characteristic curves // Surgery. 2016; 159(6): 1638-1645.
doi: 10.1016/j.surg.2015.12.029
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ПРЕДРАСПОЛОЖЕННОСТИ К ПРОГРЕССИРОВАНИЮ АТЕРОСКЛЕРОЗА У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА ПО СОДЕРЖАНИЮ ИНТЕРЛЕЙКИН-10-ПРОДУЦИРУЮЩИХ Т-ЛИМФОЦИТОВ В ПЕРИФЕРИЧЕСКОЙ КРОВИ | 2014 |
|
RU2575791C1 |
| Способ диагностики предрасположенности к прогрессированию атеросклероза сонных артерий у лиц с нормолипидемией по содержанию CD4+ Т-лимфоцитов в периферической крови | 2016 |
|
RU2636238C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ РАЗВИТИЯ АТЕРОСКЛЕРОЗА У ШАХТЕРОВ С АНТРАКОСИЛИКОЗОМ | 2015 |
|
RU2595086C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ АТЕРОСКЛЕРОЗА КОРОНАРНЫХ АРТЕРИЙ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ С СЕРДЕЧНО-СОСУДИСТЫМИ НАРУШЕНИЯМИ | 2013 |
|
RU2532521C1 |
| Способ определения риска быстропрогрессирующего атеросклероза у больных ишемической болезнью сердца | 2022 |
|
RU2789003C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ В ТЕЧЕНИЕ 12 МЕСЯЦЕВ ПОСЛЕ КОРОНАРНОГО ШУНТИРОВАНИЯ | 2024 |
|
RU2830502C1 |
| Способ прогнозирования риска развития кардиоваскулярных осложнений у пациентов со стабильной ишемической болезнью сердца, перенесших плановую эндоваскулярную реваскуляризацию миокарда | 2021 |
|
RU2770273C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ НЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА С САХАРНЫМ ДИАБЕТОМ 2 ТИПА, ПЕРЕНЕСШИХ СТЕНТИРОВАНИЕ КОРОНАРНЫХ АРТЕРИЙ | 2015 |
|
RU2582291C1 |
| Способ прогнозирования риска развития ишемического инсульта у пациентов с инфарктом миокарда. | 2020 |
|
RU2760854C1 |
| Способ прогнозирования неблагоприятных сердечно-сосудистых событий в течение года после операции коронарного шунтирования | 2020 |
|
RU2731305C1 |
Изобретение относится к медицине, а именно к иммунологии, кардиологии и эндокринологии, и может быть использовано для диагностики метавоспаления у пациентов с ишемической болезнью сердца и сахарным диабетом 2 типа. Проводят определение относительного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов от всех CD4+ лимфоцитов периферической крови. По данным абсолютного содержания лимфоцитов, полученным в ходе общего анализа крови, рассчитывают абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови. При суммарном абсолютном содержании CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови 1,39×107 клеток/л и более диагностируют метавоспаление. Способ обеспечивает диагностику метавоспаления у пациентов с ишемической болезнью сердца и сахарным диабетом 2 типа за счет определения суммарного абсолютного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов 1,39×107 клеток/л и более в периферической крови. 1 ил., 1 табл., 3 пр.
Способ диагностики метавоспаления у пациентов с ишемической болезнью сердца и сахарным диабетом 2 типа, характеризующийся тем, что у пациента проводят определение относительного содержания CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов от всех CD4+ лимфоцитов периферической крови, затем по данным абсолютного содержания лимфоцитов, полученным в ходе общего анализа крови, рассчитывают абсолютное содержание CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови, и при суммарном абсолютном содержании CD4+CD25lowFoxP3+ Т-регуляторных лимфоцитов в периферической крови, равном 1,39×107 клеток/л и более, диагностируют метавоспаление.
| US 20200147118 A1, 14.05.2020 | |||
| КОЛОГРИВОВА И.В | |||
| и др | |||
| Взаимосвязь факторов воспаления и метаболических параметров при ожирении у пациентов с артериальной гипертонией высокого и очень высокого риска | |||
| РКЖ | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| LLAGUNO M | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2024-02-15—Публикация
2023-06-09—Подача