Изобретение относится к медицинским токсикологическим исследованиям, в частности, к санитарной токсикологии, и может быть использовано для количественного определения фурана и метилфурана в крови.
Фуран и метилфуран - это ароматические гетероциклические соединения, которые отличаются высокой летучестью.
В окружающей среде присутствуют сотни различных химических соединений, для которых характерны высокая токсичность, способность к накоплению в трофических цепях, устойчивость в окружающей среде. К их числу следует отнести фуран и его производные, которые являются опасными загрязнителями объектов окружающей среды. Международное агентство по исследованию рака классифицирует фуран как «возможный канцероген для человека (группа 2B)». Известно, что фуран может вызывать раздражение глаз, кожи и слизистых оболочек, ощущение жжения и в тяжелых случаях коррозию. При вдыхании фуран может вызвать отек легких и некроз бронхов. При всасывании фуран происходит угнетение центральной нервной системы вплоть до наркоза и тонических судорог.
Для оценки уровня неблагоприятных экологических воздействий, решения современных гигиенических проблем, формирования интегральных оценок состояния окружающей среды и здоровья населения, основанных на показателях риска поступления химических соединений в организм человека в условиях многокомпонентной комплексной нагрузки, необходимо располагать высокочувствительными, селективными, информативными и метрологически аттестованными методиками определения содержания химических соединений в биологических средах человека. Установлено, что в РФ контроль содержания фурана и его производных не проводится, так как в РФ не существует действующей системы биомониторинга человека ни на федеральном, ни на региональном уровне. Обзор отечественных и зарубежных научно-методических документов по физико-химическим методам контроля определения фурана и метилфурана в биологических жидкостях показал, что задача оценки токсичных гетероциклов остается весьма актуальной в РФ.
Из уровня техники известен способ определения фурадана и его метаболитов в биосредах методом хроматографии в тонком слое (статья В.Н.Оськина «Определение фурадана и его метаболитов в биосредах методом хроматографии в тонком слое», Киевский НИИ гигиена труда и профзаболеваний, 1981, https://cyberleninka.ru/article/n/opredelenie-furadana-i-ego-metabolitov-v-biosredah-metodom-hromatografii-v-tonkom-sloe), согласно которому пробу крови помещают в пробирку, смоченную раствором лимоннокислого натрия. Далее к 1 мл этой крови приливают 2 мл дистиллированной воды. Смесь экстрагируют дважды смесью хлороформа и диэтилового эфира в течение 15 мин. Полученный экстрак пропускают через слой безводного сернокислого натрия и производят отгонку растворителя. Количественное опроеделение проводили путем сопоставления окраски и размеров пятен проб и стандартных растворов. Чувствительность метода для крови составляла 0,5 мкг.
Также известен метод анализа пробы крови на наличие фурана SPME-GC/MS [IARC Classifies Radiofrequency Electromagnetic Fields as Possibly Carcinogenic to Humans [Электронный ресурс]. – URL: https://www.iarc.who.int/wpcontent/uploads/2018/07/pr208_E.pdf (дата обращения: 15.02.2023)]. Согласно известному методу образцы крови объемом 10 мл собирали в пробирки с этилендиаминтетраминовой кислотой (ЭДТА) и немедленно помещали в морозильную камеру, чтобы предотвратить потерю фурана при испарении. Плазму выделяли центрифугированием (630×g, 10 мин, 4 ºC). Клинические образцы хранились при температуре −80 ºC до тех пор, пока не было проведено измерение содержания фурана. Подготовка образцов крови к химическому анализу проводилась с использованием волокна карбоксен/полидиметилсилоксан (CAR/PDMS) толщиной 75 мкм. Волокно выдерживали при 60 ºC в течение 20 мин при постоянном перемешивании (200 об/мин) во флаконе для образца объемом 20 мл. Перед использованием волокно выдерживали в инжекционном отверстии газового хроматографа при 250 ºC в течение 1 ч. Инъекцию осуществляли путем десорбции волокна в течение 5 мин при 250 ºC. Волокно высушивали в течение 5 мин при 250 ºC перед следующей экстракцией, чтобы удалить остатки анализируемого вещества. Для анализа GC/MS использовали газовую систему GC Agilent 6890N, с массселективным детектором Agilent 5975. Хроматографическое разделение проводили на колонке HP-PLOT Q (15 м×0,32 мм, пленка 20 мкм. В качестве газа-носителя использовали гелий со скоростью потока 44 см/с. Масс-спектрометр работал в режиме селективного ионного мониторинга (SIM) путем регистрации токов следующих ионов: m/z 68 и 39 для фурана и m/z 72 и 42 для d4-фурана. Соответствующие соотношения ионов для фурана и d4-фурана определяли для каждого измерения. В режиме SIM данные полной сканирующей электронной ионизации (EI) были получены одновременно для определения подходящих масс для режима SIM.
Авторами M.I. Churchwell, R.C. Scheri, L.S. et al. [Evaluation of serum and liver toxicokinetics for furan and liver DNA adduct formation in male Fischer 344 rats / M.I. Churchwell, R.C. Scheri, L.S. Von Tungeln [et al.] // Food and Chemical Toxicology. – 2015. – Vol. 86. – P. 1–8. DOI: 10.1016/j.fct.2015.08.029] предложена методика определения фурана в крови. В данном методе цельную кровь собирали путем пункции сердца в вакуумные пробирки с ЭДТА объемом 3 мл. Пробирки были заполнены полностью, хорошо перемешаны и немедленно охлаждены. Образцы крови были проанализированы в тот же день, когда осуществлен забор крови. Аликвоту цельной крови объемом 1 мл добавляли во флакон объемом 10 мл и добавляли 100 п/моль внутреннего стандарта d4 фурана. Внутренний стандарт хранился на льду во время подготовки образца. Затем флакон закрывали обжимной крышкой с тефлоновой подкладкой и анализировали образец методом анализа равновесной паровой фазы (headspace GC/MS). Пределы обнаружения варьировались в диапазоне 0,4–1,5 пмоль/мл.
Из источника информации: Quantification of seven microbial volatile organic compounds in human serum by solid-phase microextraction gas chromatography-tandem mass spectrometry / I.J. Wazeerud-Din, L.K. Silva, M.M. Smith [et al.] // Chemosphere – 2021. – Vol. 266. DOI: 10.1016/j.chemosphere.2020.128970, известен высокопроизводительный автоматизированный метод количественного определения семи МЛОС (3-метилфуран, 2-гексанон, 2-гептанон, 3-октанон, 1-октен-3-ол, 2-этил1-гексанол и геосмин) в сыворотке крови человека. Методика пробоподготовки образцов крови заключается в том, что взятый биоматериал центрифугировали при 3000 об/мин в течение 10 мин, тем cамым отделяя эритроциты от сыворотки. Образцы крови до анализа хранятся при температуре минус 70 °C. Перед анализом образцы сыворотки размораживали и смешивали на гематологическом смесителе. Аликвота 0,5 мл была удалена из крови и перенесена во флакон SPME объемом 10 мл. Впоследствии образец сыворотки добавляли 40 мкл стандартного раствора, закрывали и смешивали в течение 5 мин. После пробоподготовки флаконы помещали в лоток для образцов кулера Пельтье (15 °C) на автопробоотборнике PAL. Для анализа образцов использовался газовый хроматограф Agilent Technologies 7000C в сочетании с трехквадрупольным масс-спектрометром (GC-MS/MS). Автопробоотборник Leap Technologies Inc. установлен на системе GC-MS/MS; эта двухрельсовая система выполняла автоматический нагрев образцов, извлечение и вкол. Целевые аналиты разделяли на капиллярной колонке Restek Rxi-5Sil MS (30 м; 0,25 мм; пленка 0,25 мкм). Метод позволяет количественно определить целевые аналиты с использованием твердофазной микроэкстракционной газовой хроматографии и тандемной масс-спектрометрии при низких уровнях содержания частиц на миллиард. Пределы обнаружения варьировались от 0,076 до 2,77 мкг/л.
Недостатками указанных известных способов является сложность исполнения, необходимость в применении нестандартного оборудования, а также сложность подготовки биологических образцов (кровь) к химическому анализу фурана и метилфурана.
При этом из уровня техники не были выявлены известные способы количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием, поэтому сделать выбор ближайшего аналога к заявляемому изобретению не представляется возможным.
Технический результат, достигаемый предлагаемым способом, заключается в разработке достоверного и селективного способа количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием.
Указанный технический результат достигается предлагаемым способом количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием, характеризующийся тем, что производят отбор пробы крови, выполняют подготовку ее к анализу путем подщелачивания 10%-ным водным раствором гидроокиси натрия до рН 8-9, далее осуществляют экстракцию гептаном, объем которого соотносится с объемом пробы крови как 1:2,5 соответственно, причем экстракцию ведут в течение 5 минут до установления межфазного равновесия, затем выполняют центрифугирование экстракта при 5000 об/мин в течение 10 мин, далее осуществляют отбор шприцем 1 мм3 образующегося экстракта и вводят его в инжектор испарителя газового хроматографа, снимают при этом хроматограмму, определяя площадь пика, причем время удерживания для фурана составляет 4,1 мин, а для метилфурана – 5,7 мин, а концентрацию фурана и метилфурана определяют с использованием градуировочного графика, характеризующего зависимость площади пика от содержания исследуемого компонента на хроматограмме, при этом газохроматографический анализ проводят на капиллярной колонке DB-5MS- 60м*0,25 мм*0,25мкм при температурном режиме: колонка - 40-200 °С; испаритель – 230°С; температура источника ионов – детектора, – 200 °С; расход газа-носителя азота – 20 см3/мин.
Подщелачивание пробы 10%-ным водным раствором гидроокиси натрия производят в объемном соотношении как 2,5:1 соответственно.
Поставленный технический результат достигается за счет следующего.
Измерение массовой концентраций фурана и метилфурана в биосреде (кровь) в предлагаемом способе основана на экстракционном концентрировании из крови объемом 2,5 см3 органическим растворителем (гептан) объемом 1 см3 (время контакта фаз 5 мин) с добавлением 1 см3 10 % NaOH, центрифугировании при 5000 об/мин в течении 10 мин для денатурации белка крови, газохроматографическом разделении на капиллярной колонке, идентификации веществ по масс-спектрам и количественному определению по извлеченным ионам методом ГХ/МС.
Экспериментальным путем обнаружено, что указанный технический результат обеспечивается именно совокупностью предложенных признаков, при реализации которых и достигается высокая чувствительность определения фурана и метилфурана в пробе крови, а также упрощается способ по сравнению с известными методами.
Высокая эффективность предлагаемого способа определения фурана и метилфурана в крови достигнута путем подбора оптимальных условий газохроматографического анализа: капиллярной колонки серии DB-5MS- 60м*0,25 мм*0,25мкм длиной 60 метров, внутренним диаметром 0,250 мм и толщиной пленки неподвижной фазы 0,250 мкм при оптимальном температурном режиме: колонка – 40-200 °С; испаритель –230°С; температура источника ионов (детектор) –200 °С; расход газа-носителя (азот) – 20 см3/мин.
Кроме того, полнота извлечения предлагаемым способом фурана из крови составляет 98 % и метилфурана 98,5 %.
В процессе валидации заявляемого способа установлены пределы обнаружения (LOD) изучаемых соединений в крови, которые составили: для фурана до 0,00011 мкг/см3 и до 0,000021 мкг/см3 для метилфурана.
Благодаря совокупности существенных признаков предлагаемого способа обеспечено снижение пределов количественного определения (LOQ) до 0,0011 мкг/см3 для фурана и до 0,00021 мкг/см3 для метилфурана. Предел количественного определения LOQ для фурана в крови составил 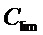 = 0,0011 мкг/см3 и установлен больше предела обнаружения
= 0,0011 мкг/см3 и установлен больше предела обнаружения 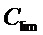 >
>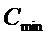 . Для метилфурана предел количественного определения LOQ в крови составил
. Для метилфурана предел количественного определения LOQ в крови составил 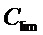 = 0,00021 мкг/см3.
= 0,00021 мкг/см3.
Предлагаемый способ реализуется следующим образом.
- производят отбор пробы крови в объеме 2,5 мл;
- выполняют подготовку ее к анализу путем подщелачивания ее 10%-ным водным раствором гидроокиси натрия до рН 8-9, ориентировочно, используют 1 мл указанного раствора;
- далее осуществляют экстракцию гептаном объемом 1 мл, объем которого соотносится с объемом пробы крови как 1:2,5 соответственно,
- причем экстракцию ведут в течение 5 минут до установления межфазного равновесия,
- выполняют центрифугирование экстракта при 5000 об/мин в течение 10 мин,
- далее осуществляют отбор шприцем 1 мм3 образующегося экстракта и введение его в инжектор испарителя газового хроматографа, снимают при этом хроматограмму, определяя площадь пика, причем время удерживания для фурана составляет 4,1 мин, для метилфурана – 5,7 мин,
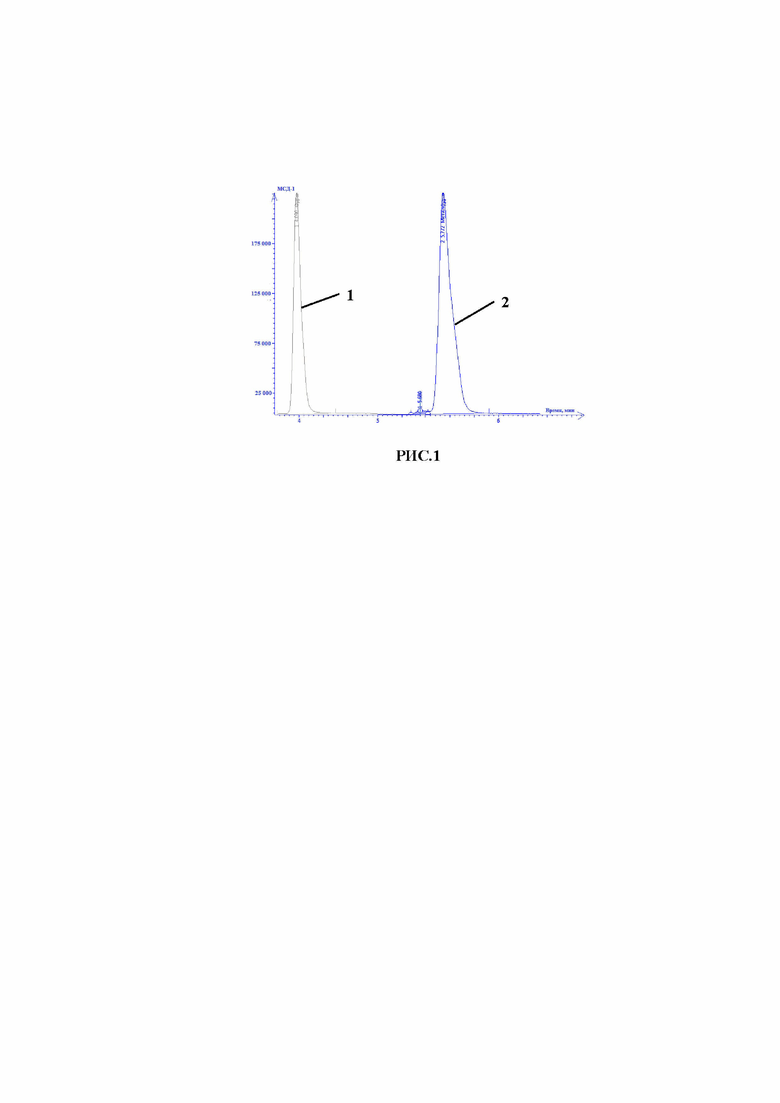
- а концентрацию фурана и метилфурана определяют с использованием градуировочного графика (Рис.1), характеризующего зависимость площади пика от содержания исследуемого компонента на хроматограмме, при этом газохроматографический анализ проводят на капиллярной колонке DB-5MS- 60м*0,25 мм*0,25мкм при температурном режиме: колонка– 40-200 °С; испаритель – 230°С; температура источника ионов – детектора, – 200 °С; расход газа-носителя (азот)– 20 см3/мин.
Чувствительность и точность способа лимитируется, прежде всего, процессом газовой экстракции. Константа распределения вещества между конденсированной и газовой фазами очень чувствительна к температуре. Это накладывает довольно жесткие ограничения на стабильность температуры в процессе распределения вещества между фазами при количественных измерениях, что значительно влияет на точность анализа.
При разработке газохроматографических методик определения органических соединений в биологических средах важным этапом является отработка параметров газохроматографического определения. Для установления высокой степени селективности и высокой чувствительности определения используются специфические детекторы (детектор электронного захвата, термоионный детектор, масс-селективный детектор и т.д.), капиллярные колонки различной длины (от 20 до 100 м) заполненные неподвижными жидкими фазами различной полярности.
Отработка оптимальных хромато-масс-спектрометрических параметров определения фурана и метилфурана при использовании стандартного образца осуществлялась с использованием газовой хроматографии и масс-спектрометрии (ГХ/МС): газовый хроматограф (Хроматэк-Кристалл) и при анализе биологических образцов для того, чтобы свести к минимуму влияние основного компонента пробы крови,
использовали масс-селективный детектор (Хроматэк-Кристалл) и квадрупольный масс-анализатор. Режим ионизации электронным ударом при 70 эВ.
Одним из основных факторов, определяющих эффективность хроматографического разделения, является правильный выбор неподвижной жидкой фазы (НЖФ), которая должна быть наиболее селективной по отношению к разделяемым соединениям. Используя капиллярные колонки с различными по полярности НЖФ, можно варьировать селективность и достигать высокой эффективности разделения. Поэтому были изучены условия разделения на капиллярных колонках с различными характеристиками неподвижных жидких фаз: DB-624-25m⋅0,32mm⋅5,0µm (полярная цианопропильная фаза; температурный предел от 60°С до 260/300°С), HP-FFAP-50m•0,32mm•0,5µm (полярная фаза с покрытием нитротерефталевой кислотой; температурный предел от 60°С до 240/250°С) и DB-5MS- 60м*0,25 мм*0,25мкм длиной 60 метров, внутренним диаметром 0,250 мм и толщиной пленки неподвижной фазы 0,250 мкм. Качественное разделение в пробе крови фурана и метилфурана с близкими физико-химическими свойствами было достигнуто на капиллярной колонке серии DB-5MS- 60м*0,25 мм*0,25мкм.
В процессе исследования определяли влияние температуры на параметры процесса разделения фурана и метилфурана. Под эффективностью хроматографической системы понимается ее способность препятствовать размыванию хроматографических пиков хроматограмм. На селективность оказывает влияние температура, а на эффективность влияет скорость потока газа-носителя. В процессе разделения фурана и метилфурана во времени применяли нелинейный закон, т.е. температуру капиллярной колонки повышали от 40 ºС до 200 ºС со скоростью 40 ºС/мин, что позволило разделить и выделить все компоненты биологического образца. В условиях эксперимента были отработаны расходы газа-носителя, деление потока азот : воздух и без деления потока азот : воздух. Температуру источника ионов установили на 200 ºС. Сканирование масс анализируемых соединений образца крови выполняли в диапазоне от 37 до 150 а.е.м. Оптимальные газохроматографические параметры представлены в таблице 1.
Таблица 1 - Оптимальные условия хроматографирования образца крови предлагаемым способом
ºС
азот: воздух/ без деления потока азот: воздух
(коэффициент деления)
В режимах 1 и 3 не наблюдалось достаточно эффективного разделения фурана и метилфурана. Эффективное разделение следовых количеств легколетучих органических соединений (фуран и метилфуран) основано на экспериментально отработанных оптимальных газохроматографических параметрах и вводе пробы в поток газа-носителя с делением потока с коэффициентом деления 12,5 (режим 2 таблица 1).
Хроматограмма стандартного раствора фурана и метилфурана при оптимально отработанных условиях хромато-масс-спектрометрического анализа, зарегистрированная по полному ионному току, представлена на рисунке 1.
При этом на хроматограмме пик 1 относится к фурану, пик 2 – к метилфурану.
Температурные режимы, использованные при выборе оптимальных условий разделения фурана и метилфурана, в предлагаемом способе, представлены в таблице 2.
Таблица 2 - Температурные режимы, использованные при выборе оптимальных условий разделения фурана и метилфурана в пробе крови
Данные, приведенные в таблице 2, показывают, что оптимальные условия хроматографирования фурана и метилфурана из пробы крови предлагаемым способом достигнуты в режиме 2 при температурном режиме: колонка – 40-200 °С; испаритель – 230°С; температура источника ионов (детектор) – 200 °С; расход газа-носителя (азот) – 20 см3/мин.
Для обнаружения гетероциклов в биологических средах (кровь) использовали высокочувствительный масс-селективный детектор (МСД). Характеристики газохроматографического анализа гетероциклов (фурана и метилфурана) представлены в таблице 3.
Таблица 3 - Характеристики газохроматографического анализа гетероцикла (фуран) и сильвана (метилфуран) в крови
мм3
В современном химико-токсикологическом анализе одним из перспективных методов разделения и концентрирования органических соединений является гетерогенная жидкостная экстракция. Задача экстракции состоит в том, чтобы полно и селективно перевести аналит из биологической среды в органическую фазу.
Для обеспечения полноты извлечения фурана и метилфурана из биосреды (кровь) были подобраны условия экстракции: выбор органического растворителя, объем экстрагента, рН среды, число экстракций и время достижения равновесия.
В ходе экспериментальных работ по выбору экстрагента и для эффективного извлечения фурана и метилфурана из крови применена жидкостная экстракция различными органическими растворителями, изучены экстракционные характеристики. Данные приведены в таблице 4.
Таблица 4 - Зависимость полноты экстракции фурана и метилфурана из крови от полярности органических растворителей (n=5, р=0,95)
н/о – не определялся; р – вероятность.
Данные, приведенные в таблице 4, показывают, что с учетом максимальной степени экстракции фурана и метилфурана (62-86 %) из крови и оптимальных условий разделения в качестве растворителя-экстрагента был выбран гептан.
В таблице 5 приведена зависимость степени экстракции фурана и метилфурана из крови от объема растворителя.
Таблица 5 - Зависимость степени экстракции фурана и метилфурана из крови от объема органического растворителя
гептана
Данные, приведенные в таблице 5, показывают, что при использовании органического растворителя гептана в объеме 1,0 мл для экстракции (соотношение объема гептана к объему пробы крови составляет 1:2,5 соответственно) степень извлечения из крови составила для фурана 62,8 % и для метилфурана 86,7 %.
Далее осуществляли изучение зависимости степени экстракции фурана и метилфурана из цельной крови и плазмы от объема биоматериала и органических растворителей. Изолирование токсичных соединений методом экстракции может
проводится из цельной крови, плазмы или сыворотки. Прецизионность анализа и эффективность извлечения фурана и метилфурана из крови и из плазмы крови устанавливали экспериментально способом «введено–найдено» с применением стандартных растворов. Данные приведены в таблице 6.
Таблица 6 - Зависимость степени экстракции фурана и метилфурана из крови и из плазмы крови от объема органического растворителя и объема крови для анализа
(мкг/мл)
Анализ полученных результатов (таблица 6) показал, что при использовании 1 см3 экстрагента (гептан) и 2,5 см3 крови, экстракции в течение 5 минут и центрифугирования экстракта в течение 10 минут при 5000 об/мин позволило достичь степени экстракции для фурана 77 % и метилфурана 91 %.
Кроме того, было установлено, что предлагаемый способ не подходит для исследования плазмы крови, т.к. полнота извлечения фурана и метилфурана из плазмы составила для фурана 15 % и для метилфурана 16 %.
Было проведено изучение зависимости степени экстракции фурана и метилфурана из крови от рН. Экстракция органических соединений из биосреды зависит от ряда факторов, в том числе и от рН среды. С целью максимального извлечения фурана и метилфурана из крови и установления параметров экстракции в экспериментальных исследованиях применяли и подкисление неорганической кислотой, и подщелачивание щелочью щелочноземельных металлов биопробы, т.к. фуран и его производные находятся в виде комплексов с белками. Результаты представлены в таблице 7.
Таблица 7 - Зависимость степени экстракции фурана и метилфурана из крови от рН среды (n=2, р=0,95)
Полученные результаты (таблица 7) позволили заключить, что фуран и метилфуран с высокой степенью извлечения 98 и 98,5 % из пробы крови изолируются именно из щелочной среды.
Экспериментальным путем установлено, что применение в качестве экстрагента гептана объемом 1 см3 позволяет более полно извлечь фуран и метилфуран из крови, и только при использовании 10%-ного р-ра NaOH (подщелачивание до рН 8-9) обеспечивается повышение степени экстракции до 98 % и 98,5 % соответственно.
Это, по-видимому, объясняется тем, что при подкислении происходит денатурация молекул белка и разрушение водородных связей, солевых и иных мостиков, поддерживающих вторичную и третичную структуру молекулы белка. Вследствие этого молекула белка теряет специфическую пространственную форму, утрачивает свое биологическое действие и происходит ее разложение с выделением летучих продуктов. Вместе с тем, при взаимодействии фурана и его производных с сильными кислотами уменьшается стабильность кольца – фурановое кольцо расщепляется и полимеризуется. Неустойчивость фурана в кислой среде сопровождается сильным осмолением и промежуточным образованием диеновых соединений.
Вместе с тем, фуран устойчив к действию щелочей щелочноземельных металлов и поэтому фурановое кольцо не разрушается, а потому повышается полнота извлечения фурана и метилфурана из пробы крови.
Исходя из вышеизложенного, оптимальные условия процесса определения фурана и метилфурана в пробе крови предлагаемым способом следующие:
- максимальная полнота извлечения фурана и метилфурана из крови – 98% и 98,5% соответственно, достигнута при подобранных оптимальных условиях подготовки пробы для газохроматографического анализа путем подщелачивания пробы крови до рН 8-9 10%-ным водным раствором гидроокиси натрия, концентрирования из крови (время контакта 5 мин) органическим растворителем-экстрагентом - гептан, (соотношение его объема к объему крови 1:2,5 соответственно), денатурации белка центрифугированием биосреды при 5000 об/мин в течение 10 мин, и последующем определении на газовом хроматографе с детектором электронного захвата (ДЭЗ).
Опыты показали, что полнота разделения фурана и метилфурана в пробе крови достигнута на капиллярной колонке DB-5MS- 60м*0,25 мм*0,25мкм при температурном режиме: колонка– 40-200 °С; испаритель – 230°С; температура источника ионов – детектора, – 200 °С; расход газа-носителя (азот)– 20 см3/мин.
Для обнаружения фурана и метилфурана в пробе крови в биологической среде (кровь) использовали высокоспецифичный электронно-захватный детектор (ДЭЗ). Ниже в таблице 8 приведены параметры и условия режима работы хромато-масс-спектрометра при реализации предлагаемого способа.
Таблица 8 - Параметры и условия режима работы хромато-масс-спектрометра
режим сканирования:
Благодаря тому что образующийся при пробоподготовке экстракт анализируют методом газовой хроматографии с детектором электронного захвата, обеспечивает максимально возможное по чувствительности газохроматографическое определение. Определение количества фурана и метилфурана в крови методом газохроматографического анализа проводят с использованием градуировочного графика. Для его построения выполняют традиционные действия.
Предлагаемый способ устанавливает порядок применения метода капиллярной газовой хроматографии для измерения массовых концентраций фурана и метилфурана в пробах крови в диапазоне концентраций от 0,0019 до 0,09 мг/дм3 при стандартном отклонении не более 10 % и погрешности не более 20 %.
Длительность анализа, включая экстракцию биопробы, составляет не более 60 мин.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения фурана и метилфурана в детских кашах на основе зерна газохроматографическим методом с использованием парофазного анализа | 2022 |
|
RU2798667C1 |
| Способ определения фурана и метилфурана в атмосферном воздухе методом капиллярной газовой хроматографии с масс-селективным детектором при использовании метода низкотемпературного концентрирования | 2022 |
|
RU2789634C1 |
| Способ количественного определения акрилонитрила в воде газохроматографическим методом с использованием парофазного анализа | 2024 |
|
RU2831530C1 |
| Способ количественного определения фурана и метилфурана в детских кашах | 2022 |
|
RU2782424C1 |
| Способ количественного определения гексахлорбензола в крови методом газохроматографического анализа | 2016 |
|
RU2613306C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АКРИЛОНИТРИЛА В КРОВИ МЕТОДОМ ГАЗОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА | 2011 |
|
RU2452961C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 2,4-ДИХЛОРФЕНОЛА В КРОВИ МЕТОДОМ ГАЗОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА | 2013 |
|
RU2521277C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ N-НИТРОЗОДИМЕТИЛАМИНА И N-НИТРОЗОДИЭТИЛАМИНА В МОЧЕ МЕТОДОМ ГАЗОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА | 2013 |
|
RU2521711C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ПЕНТАХЛОРФЕНОЛА В КРОВИ МЕТОДОМ ГАЗОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА | 2014 |
|
RU2546527C1 |
| Способ количественного определения N-нитрозаминов в детских кашах | 2015 |
|
RU2613303C1 |
Изобретение относится к области токсикологии. Описан способ количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием. Концентрацию фурана и метилфурана, согласно способу, определяют с использованием градуировочного графика, характеризующего зависимость площади пика от содержания исследуемого компонента на хроматограмме. Технический результат, достигаемый предлагаемым способом, заключается в разработке достоверного и селективного способа количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием. 1 з.п. ф-лы, 1 ил., 8 табл., 1 пр.
1. Способ количественного определения фурана и метилфурана в крови методом газохроматографического анализа с масс-селективным детектированием, характеризующийся тем, что производят отбор пробы крови, выполняют подготовку ее к анализу путем подщелачивания 10%-ным водным раствором гидроокиси натрия до рН 8-9, далее осуществляют экстракцию гептаном, объем которого соотносится с объемом пробы крови как 1:2,5 соответственно, причем экстракцию ведут в течение 5 минут до установления межфазного равновесия, затем выполняют центрифугирование экстракта при 5000 об/мин в течение 10 мин, далее осуществляют отбор шприцем 1 мм3 образующегося экстракта и вводят его в инжектор испарителя газового хроматографа, снимают при этом хроматограмму, определяя площадь пика, причем время удерживания для фурана составляет 4,1 мин, а для метилфурана - 5,7 мин, а концентрацию фурана и метилфурана определяют с использованием градуировочного графика, характеризующего зависимость площади пика от содержания исследуемого компонента на хроматограмме, при этом газохроматографический анализ проводят на капиллярной колонке DB-5MS-60 м*0,25 мм*0,25 мкм при температурном режиме: колонка - 40-200°С; испаритель - 230°С; температура источника ионов - детектора, - 200°С; расход газа-носителя азота - 20 см3/мин.
2. Способ по п.1, характеризующийся тем, что подщелачивание пробы 10%-ным водным раствором гидроокиси натрия производят в объемном соотношении 2,5:1 соответственно.
| WO 2016126923 A1, 11.08.2016 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ O-(2,3-ДИГИДРО-2,2-ДИМЕТИЛ-7-БЕНЗОФУРАНИЛ)-N-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269780C1 |
| Субботина Д | |||
| Ю | |||
| Экспериментальные исследования по выбору метода пробоподготовки к химическому анализу фурана и метилфурана в пищевых продуктах на примере детских каш методом хромато-масс-спектрометрии / Д | |||
| Ю | |||
| Субботина, Т | |||
| В | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Фундаментальные и | |||
Авторы
Даты
2024-02-19—Публикация
2023-06-13—Подача