Изобретение относится к химико-фармацевтической промышленности и может быть использовано в центрах контроля качества лекарственных средств и контрольно-аналитических лабораториях при проведении количественного определения суммы флавоноидов в листьях тополя белого (Populus alba L.).
Виды растения рода Тополь (Populus L.) широко произрастают на территории Российской Федерации (1). Тополь белый (Populus alba L.) не является фармакопейным представителем рода Populus, но имеет схожий химический состав с тополем черным и может выступать в качестве перспективного источника сырья, содержащего фенольные соединения, в частности, флавоноиды (2, 4).
Почки, листья, побеги и кора тополя белого содержат флавоноиды (пиностробин, пиноцембрин, рутин, кверцетин) и другие фенольные соединения, в том числе салицин (3, 7, 8). Одним из основных флавоноидов листьев тополя белого является рутин (7). Известно, что рутин проявляет капилляроукрепляющую активность. Этот флавоноид обладает способностью связывать металлы в прочные комплексы с образованием каталитически неактивных комплексов. Рутин (3-О-рутинозид кверцетина) в дозе 25 мг/кг оказывает антиоксидантное действие, проявляющееся в снижении содержания МДА (малонового диальдегида) в гомогенате (в 1,3 раза), повышает активность каталазы (в 1,2 раза), проявляет тенденцию к повышению активности ферментов супероксиддисмутазы и глутатионпероксидазы (5).
Ранее была разработана методика определения суммы флавоноидов в листьях тополя черного (6). Данная методика выбрана нами в качестве прототипа.
Следовательно, является актуальным исследование в плане разработки методики количественного определения суммы флавоноидов в сырье данного растения.
Таким образом, целью изобретения является разработка способа количественного определения суммы флавоноидов в листьях тополя белого, обладающего высокой специфичностью и точностью.
Техническим результатом является создание способа количественного определения суммы флавоноидов в листьях тополя белого в пересчете на рутин.
Технический результат достигается тем, что экстракцию сырья осуществляют однократно, в качестве экстрагента используют этиловый спирт в концентрации 80% в соотношении «сырье-экстрагент» - 1:30, время экстракции - извлечение на кипящей водяной бане в течение 90 мин, степень измельчения сырья - 2 мм, реакция комплексообразования с хлоридом алюминия в течение 30 мин. Количественное определение суммы флавоноидов в листьях тополя белого проводят при длине волны 410 нм в пересчете на рутин; содержание суммы флавоноидов (X в процентах) в пересчете на рутин и абсолютно сухое сырье вычисляют по формуле:
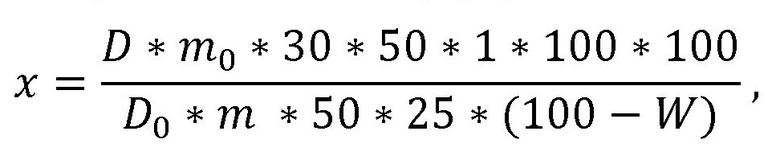
где D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора стандартного образца рутина;
m - масса сырья, г;
mо - масса стандартного образца рутина, г;
W - потеря в массе при высушивании, %.
В случае отсутствия стандартного образца рутина для расчета целесообразно использовать теоретическое значение удельного показателя поглощения при 410 нм - 220:
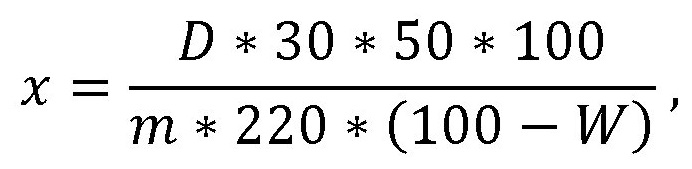
где D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
mо - масса СО рутина, г;
220 - удельный показатель поглощения (E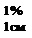 ) СО рутина при 410 нм;
) СО рутина при 410 нм;
W - потеря в массе при высушивании в процентах.
При изучении спектральных характеристик было выявлено, что именно
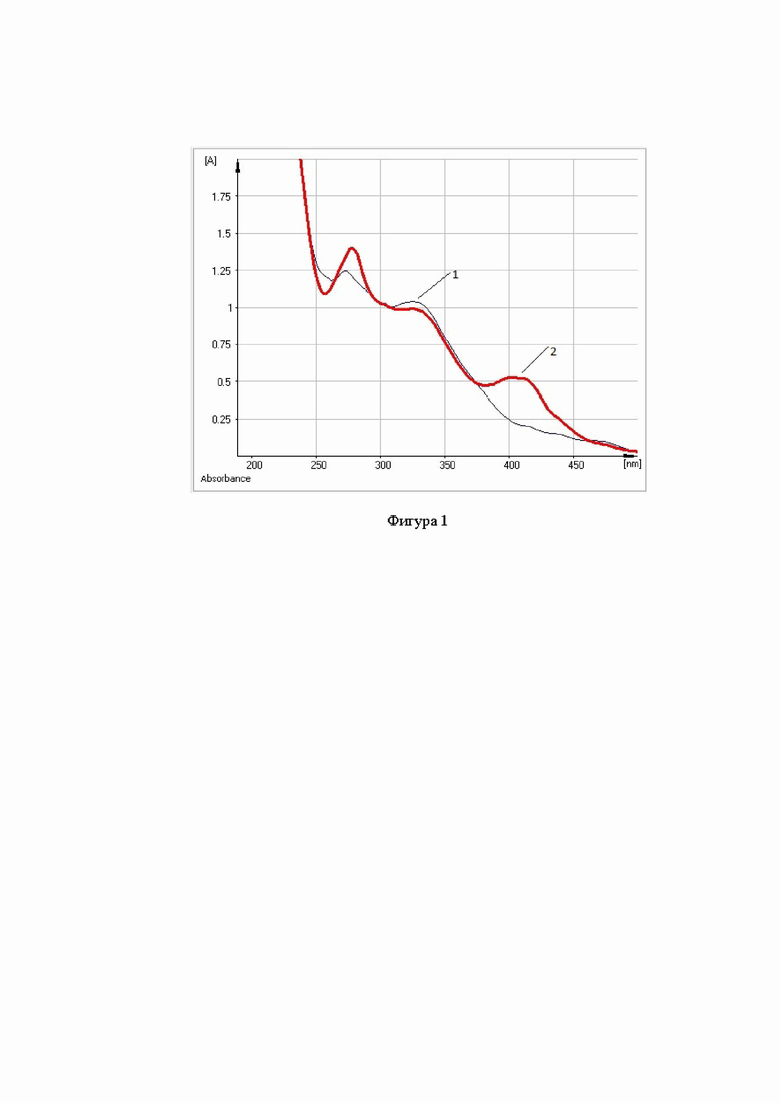
рутин определяет характер кривой поглощения водно-спиртового извлечения из листьев тополя белого. Определено, что в УФ-спектре водно-спиртового извлечения тополя белого наблюдается батохромный сдвиг длинноволновой полосы флавоноидов - Фигура 1, как и в случае рутина - Фигура 2, где кривая 1 на фигуре 1 и фигуре 2 демонстрирует исходный раствор водно-спиртового извлечения из листьев тополя белого или исходный раствор рутина соответственно, а кривая 2 - раствор водно-спиртового извлечения из листьев тополя белого в присутствии алюминия хлорида или раствор рутина в присутствии алюминия хлорида соответственно.
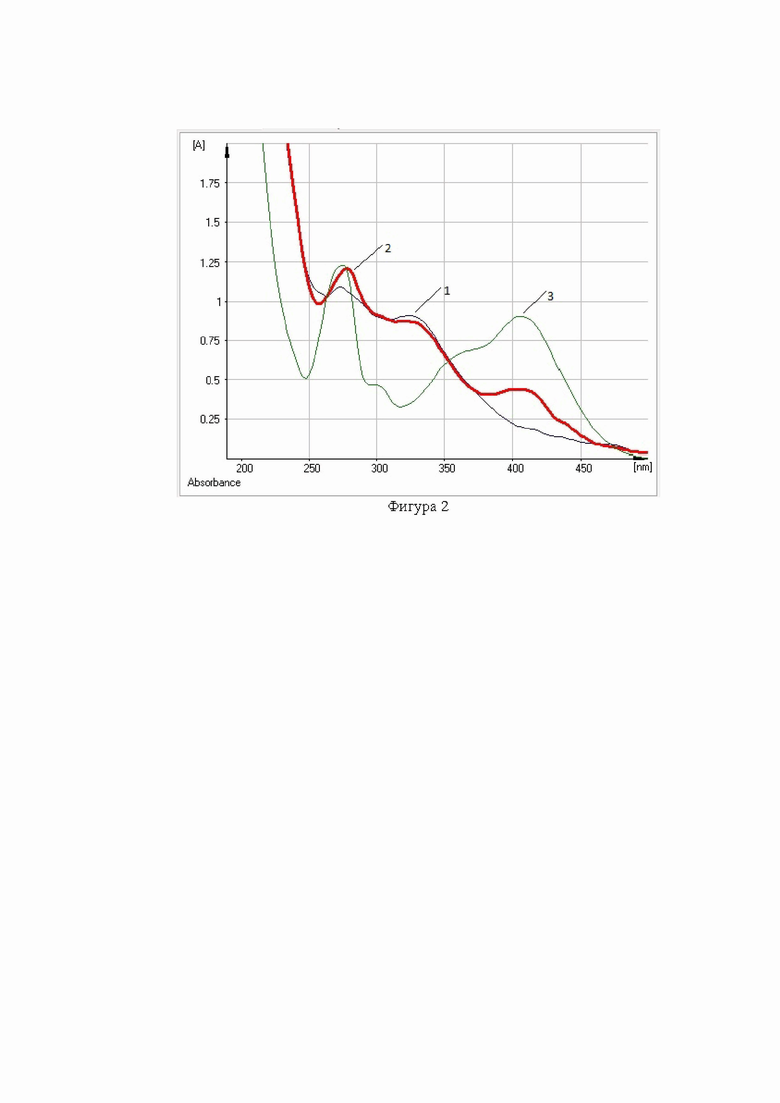
Изучение УФ-спектров фигуры 2 (где кривая 1 - раствор рутина, а кривая 2 - раствор рутина с добавлением алюминия хлорида) показало, что раствор СО рутина в присутствии алюминия хлорида имеет максимум поглощения при длине волны 410 нм. В УФ-спектре водно-спиртового извлечения из листьев тополя белого в дифференциальном варианте на фигуре 3 обнаруживается при длине волны 410 нм максимум поглощения, который соответствует максимуму поглощения спиртового раствора рутина.
Данный факт позволяет проводить спектрофотометрическое определение суммы флавоноидов в листьях тополя белого при аналитической длине волны 410 нм.
Также нами было изучено влияние экстрагента на процесс экстракции. В таблице 1 представлена зависимость выхода флавоноидов листьев тополя белого от концентрации экстрагента. В результате эксперимента в качестве оптимального экстрагента нами был выбран 80% этиловый спирт, так как выход действующих веществ из сырья при его использовании максимален.
Далее нами был изучен вопрос относительно продолжительности экстракции на кипящей водяной бане, в таблице 2 представлена зависимость выхода флавоноидов листьев тополя белого от времени экстракции на кипящей водяной бане, при этом было выбрано время экстракции 90 минут.
В таблице 3 представлена зависимость выхода флавоноидов листьев тополя белого от соотношения «сырье-экстрагент». Из таблицы видно, что максимальный выход действующих веществ наблюдается при соотношении «сырье-экстрагент» 1:30, по этой причине данное соотношение было выбрано нами в качестве оптимального.
Учитывая, что увеличение числа операций на стадии пробоподготовки ведет к возрастанию ошибки, выбор сделан в пользу одностадийного процесса экстракции с подтверждением требуемой точности количественного определения.
Таким образом, было определено, что оптимальными параметрами экстракции являются: однократное извлечение 80% этиловым спиртом на кипящей водяной бане в течение 90 минут в соотношении «сырье-экстрагент» - 1:30.
Принимая по внимание тот факт, что специфическим для листьев тополя белого является рутин, а максимумы поглощения раствора рутина и водно-спиртового извлечения листьев тополя белого находятся в области 410 нм, целесообразным является определение содержания суммы флавоноидов в пересчете на рутин при длине волны 410 нм.
Способ реализуется следующим образом.
Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 1 г измельченного сырья (точная навеска) помещают в колбу со шлифом вместимостью 100 мл, прибавляют 30 мл 80 % этилового спирта. Колбу закрывают пробкой и взвешивают на тарированных весах с точностью до ±0,01. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 90 мин. Затем ее охлаждают в течение 30 мин, закрывают той же пробкой, снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение фильтруют через бумажный фильтр (красная полоса) (испытуемый раствор А).
1 мл полученного извлечения помещают в мерную колбу вместимостью 50 мл, прибавляют 2 мл 3% спиртового раствора алюминия хлорида и доводят объем раствора до метки спиртом этиловым 96 % концентрации (испытуемый раствор Б).
Оптическую плотность испытуемого раствора Б измеряют через 30 мин на спектрофотометре при длине волны 410 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют раствор, состоящий из 1 мл раствора А, доведенный спиртом 96 % до метки в мерной колбе вместимостью 50 мл.
Примечание: Приготовление раствора стандартного образца рутина. Около 0,025 г (точная навеска) рутина помещают в мерную колбу вместимостью 50 мл, растворяют в 30 мл спирта 70% концентрации при нагревании на водяной бане. После охлаждения содержимого колбы до комнатной температуры доводят объем раствора спиртом этиловым 70% концентрации до метки (раствор А рутина). 1 мл раствора А рутина помещают в мерную колбу на 25 мл, прибавляют 2 мл 3% спиртового раствора алюминия (III) хлорида и доводят объем раствора до метки спиртом 96 % концентрации (испытуемый раствор Б рутина). Измеряют оптическую плотность раствора Б на спектрофотометре при длине волны 410 нм. В качестве раствора сравнения используют раствор, который готовят следующим образом: 1 мл раствора А рутина помещают в мерную колбу на 25 мл и доводят объем раствора до метки спиртом 96 % концентрации (раствор сравнения Б рутина).
Измерение оптической плотности проводят при длине волны 410 нм через 30 минут после приготовления всех растворов.
Содержание суммы флавоноидов в пересчете на рутин и абсолютно сухое сырье в процентах (X) вычисляют по формуле:
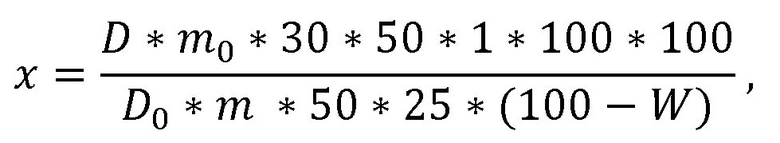
где D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора СО рутина;
m - масса сырья, г;
mо - масса СО рутина, г;
W - потеря в массе при высушивании, %.
При условиях, когда отсутствует стандартный образец рутина, целесообразно использовать теоретическое значение удельного показателя поглощения, равное 220.
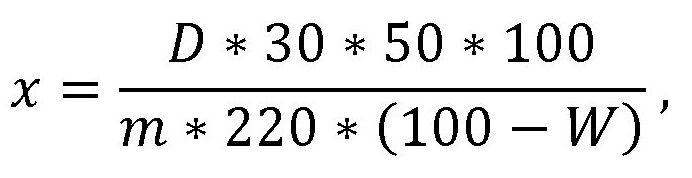
где D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
mо - масса СО рутина, г;
220 - удельный показатель поглощения (E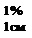 ) СО рутина при 410 нм;
) СО рутина при 410 нм;
W - потеря в массе при высушивании, %.
Предлагаемый способ поясняется следующими примерами.
Пример 1.
Аналитическую пробу листьев тополя белого измельчают до размера частиц 2 мм (заготовлено в Самарской области, июнь 2022 г.). 1,0020 г измельченного сырья помещают в колбу со шлифом вместимостью 100 мл, прибавляют 30 мл 80% этилового спирта. Колбу закрывают пробкой и взвешивают на тарирных весах с точностью до ±0,01. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 90 минут. Затем колбу охлаждают в течение 30 мин, закрывают той же пробкой, снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение фильтруют через бумажный фильтр (красная полоса).
Испытуемый раствор для анализа суммы флавоноидов готовят следующим образом: 1 мл полученного извлечения помещают в мерную колбу вместимостью 50 мл, прибавляют 2 мл 3% спиртового раствора алюминия хлорида и доводят объем раствора до метки спиртом этиловым 96% (испытуемый раствор).
Раствор сравнения готовят следующим образом: 1 мл полученного извлечения помещают в мерную колбу на 50 мл, доводят объем раствора до метки спиртом этиловым 96% (раствор сравнения).
Для расчета содержания суммы флавоноидов готовят раствор стандартного образца рутина, добавляют к нему 3% спиртовой раствор хлорида алюминия, измеряют оптическую плотность окрашенного комплекса при длине волны 410 нм и определенное значение оптической плотности используют в формуле расчета.
Приготовление раствора стандартного образца рутина.
0,0208 г рутина помещают в мерную колбу вместимостью 50 мл, растворяют в 30 мл 70% этилового спирта при нагревании на водяной бане. После охлаждения содержимого колбы до комнатной температуры доводят объем раствора 70% этиловым спиртом до метки (раствор А рутина). 1 мл раствора А рутина помещают в мерную колбу на 25 мл, прибавляют 2 мл 3% спиртового раствора алюминия (III) хлорида и доводят объем раствора до метки спиртом 96 % концентрации (испытуемый раствор Б рутина). Измеряют оптическую плотность раствора Б на спектрофотометре при длине волны 410 нм. В качестве раствора сравнения используют раствор, который готовят следующим образом: 1 мл раствора А рутина помещают в мерную колбу на 25 мл и доводят объем раствора до метки спиртом 96 % концентрации (раствор сравнения Б рутина).
Измерение оптической плотности проводят при длине волны 410 нм через 30 минут после приготовления всех растворов.
Содержание суммы флавоноидов (X в процентах) в пересчете на рутин и абсолютно сухое сырье вычисляют по формуле:
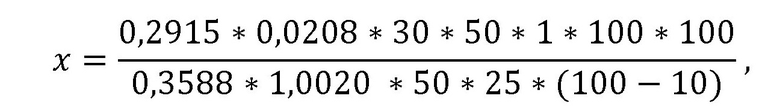
где:
0,2915 - оптическая плотность испытуемого раствора;
0,3588 - оптическая плотность раствора стандартного образца
рутина;
1,0020 - масса сырья, г;
0,0208 - масса стандартного образца рутина, г.
10 - потеря в массе при высушивании, %.
Содержание суммы флавоноидов в пересчете на рутин = 2,23 %.
Пример 2.
При необходимости определения суммы флавоноидов в листьях тополя белого при отсутствии стандартного образца рутина, необходимо провести все действия из примера 1 до приготовления раствора стандартного образца рутина.
После измерения оптической плотности извлечения из листьев тополя белого при длине волны 410 нм, содержание суммы флавоноидов (X в процентах) в пересчете на рутин и абсолютно сухое сырье вычисляют по формуле, используя теоретическое значение удельного показателя поглощения при 410 нм - 220.
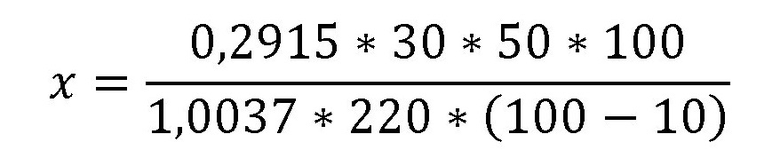
где:
0,2915 - оптическая плотность испытуемого раствора;
1,0037 - масса сырья, г;
220 - удельный показатель поглощения (E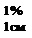 - оптическая плотность раствора вещества с концентрацией 1 г/100 мл в кювете с толщиной слоя 1 см) стандартного образца рутина при 410 нм;
- оптическая плотность раствора вещества с концентрацией 1 г/100 мл в кювете с толщиной слоя 1 см) стандартного образца рутина при 410 нм;
10 - потеря в массе при высушивании, %.
Содержание суммы флавоноидов в пересчете на рутин = 2,21 %, что сравнимо со значением, полученном в примере 1.
Все результаты были статистически обработаны. Ошибка единичного количественного определения составила ±5,22%.
Таким образом, предлагаемый способ количественного определения суммы флавоноидов в пересчете на рутин в листьях тополя белого с использованием дифференциальной спектрофотометрии разработан впервые для данного вида сырья и обладает следующими преимуществами:
1. Разработанный метод является специфичным и селективным, а также позволяет эффективно проводить экстракцию сырья однократно, поскольку в качестве экстрагента используется 80% этиловый спирт, позволяющий исчерпывающе извлекать целевые вещества (флавоноиды) в течение 90 минут.
2. Пересчет суммы флавоноидов идет на специфическое для листьев тополя белого вещество - рутин, содержащийся в сырье данного растения.
Этот способ можно применять в центрах контроля качества лекарственных средств, на фармацевтических предприятиях и контрольно-аналитических лабораториях для количественного определения суммы флавоноидов в листьях тополя белого (Populus alba L.).
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. Браславский В.Б. Ива, тополь и прополис в медицине и фармации: монография. Самара, 2012. 116 с.
2. Государственная фармакопея Российской Федерации / МЗ РФ. - XIV изд. - Т. I-IV. М., 2018. [Электронный ресурс] URL: http://femb.ru/femb/pharmacopea.php .
3. Куркин В.А., Куприянова Е.А. Сравнительное исследование флавоноидного состава листьев фармакопейных видов рода Populus / Куркин В.А. // Химия растительного сырья. - 2020. - № 1. - С. 117-124. DOI: 10.14258/jcprm.2020015818.
4. Куркин В.А. Фармакогнозия: учебник для студентов фармацевтических вузов. 5-е изд., перераб. и доп. ООО «Полиграфическое объединение «Стандарт», Самара (2020). С. 372-377.
5. Куркина А.В. Флавоноиды фармакопейных растений: монография. Самара: ООО «Офорт», ГБОУ ВПО «СамГМУ Росздрава», 2012. 290 с.
6. Куприянова Е.А., Куркин В.А. Разработка подходов к стандартизации листьев тополя черного // Аспирантский вестник Поволжья. - 2018. - № 5-6. - С. 17-22.
7. Куприянова Е.А. Сравнительное фармакогностическое исследование представителей рода Тополь (Populus L.): Дис. …канд. фарм. наук. - Самара, 2020. Доступно по: https://samsmu.ru/files/referats/2020/kupriyanova/dissertation.pdf.
В ЛИСТЬЯХ ТОПОЛЯ БЕЛОГО
Таблица 1
1.
В ЛИСТЬЯХ ТОПОЛЯ БЕЛОГО
Таблица 2
2.
В ЛИСТЬЯХ ТОПОЛЯ БЕЛОГО
Таблица 3
«сырье-экстрагент»
рутин
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ ТОПОЛЯ ЧЕРНОГО | 2018 |
|
RU2701726C1 |
| Способ количественного определения суммы флавоноидов в почках дуба черешчатого | 2021 |
|
RU2782618C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ ЧЕРНУШКИ ПОСЕВНОЙ | 2022 |
|
RU2786440C1 |
| Способ количественного определения суммы флавоноидов в траве лабазника вязолистного | 2023 |
|
RU2811264C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ ТЫСЯЧЕЛИСТНИКА ОБЫКНОВЕННОГО | 2022 |
|
RU2806035C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ СОЛОДКИ ГОЛОЙ | 2022 |
|
RU2806047C1 |
| Способ количественного определения суммы флавоноидов в листьях цефалярии гигантской | 2023 |
|
RU2807831C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ ДУБА ЧЕРЕШЧАТОГО | 2020 |
|
RU2751189C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ СИРЕНИ ОБЫКНОВЕННОЙ | 2020 |
|
RU2752316C1 |
| Способ количественного определения суммы антраценпроизводных в свежих листьях алоэ древовидного | 2021 |
|
RU2792011C2 |
Изобретение относится к химико-фармацевтической промышленности. Раскрыт способ количественного определения суммы флавоноидов в листьях тополя белого путем экстракции сырья органическими растворителями с последующей пробоподготовкой и определения оптической плотности методом дифференциальной спектрофотометрии, при этом экстракцию сырья осуществляют в соотношении 1 г сырья на 30 мл этилового спирта в концентрации 80%, время экстракции - извлечение на кипящей водяной бане в течение 90 мин, степень измельчения сырья - 2 мм, реакция комплексообразования с хлоридом алюминия в течение 30 мин; количественное определение суммы флавоноидов в листьях тополя белого проводят при длине волны 410 нм в пересчете на рутин; рассчитывают содержание суммы флавоноидов X в процентах в пересчете на рутин. Изобретение обеспечивает создание способа количественного определения суммы флавоноидов в листьях тополя белого в пересчете на рутин. 3 ил., 3 табл., 2 пр.
Способ количественного определения суммы флавоноидов в листьях тополя белого путем экстракции сырья органическими растворителями с последующей пробоподготовкой и определения оптической плотности методом дифференциальной спектрофотометрии, отличающийся тем, что экстракцию сырья осуществляют в соотношении 1 г сырья на 30 мл этилового спирта в концентрации 80%, время экстракции - извлечение на кипящей водяной бане в течение 90 мин, степень измельчения сырья - 2 мм, реакция комплексообразования с хлоридом алюминия в течение 30 мин; количественное определение суммы флавоноидов в листьях тополя белого проводят при длине волны 410 нм в пересчете на рутин; содержание суммы флавоноидов X в процентах в пересчете на рутин вычисляют по формуле:
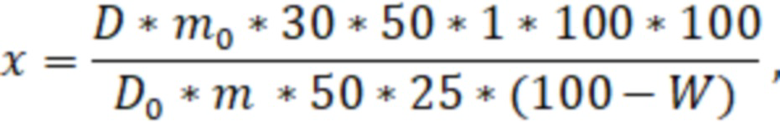
где D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора стандартного образца рутина;
m - масса сырья, г;
mо - масса стандартного образца рутина, г;
W - потеря в массе при высушивании, %;
или по формуле
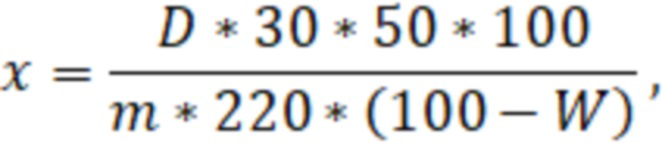
где D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
mо - масса СО рутина, г;
220 - удельный показатель поглощения (E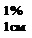 ) СО рутина при 410 нм;
) СО рутина при 410 нм;
W - потеря в массе при высушивании в процентах.
| DANISE T | |||
| et al | |||
| White poplar (Populus alba L.) leaf waste recovery and intercropping outcome on its polyphenols // Industrial Crops & Products, 2021, V | |||
| Аппарат для передачи изображений на расстояние | 1920 |
|
SU171A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ ОРЕХА ГРЕЦКОГО | 2020 |
|
RU2747482C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ В РАСТИТЕЛЬНОМ СЫРЬЕ ФЛУОРИМЕТРИЧЕСКИМ МЕТОДОМ | 2011 |
|
RU2475724C2 |
| CN 106511577B, 20.12.2019 | |||
| ЗОЛОТОВ Ю | |||
| А | |||
| Основы аналитической химии // Издательский центр "Академия", Москва, 2012, Т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-03-04—Публикация
2023-07-03—Подача