Область техники, к которой относится изобретение
Изобретение относится к области фармации, а именно фармацевтической химии, а также нутрициологии, а именно к химии пищевых фитонугриентов. Может быть использовано для количественного определения содержания индивидуальных компонентов бинарных композиционных смесей или природных составов.
Уровень техники
Комбинированное использование лекарственных средств является одним из перспективных направлений совершенствования фармакотерапии. Композиции, особенно на основе природных соединений, как правило, характеризуются более широким спектром фармакологического действия, более высокой эффективностью и безопасностью применения как в профилактических целях, так и в лечении заболеваний. Фитонутриенты, применяемые в качестве биологически активных добавок к пище, также часто применяются в виде композиций. Возникает необходимость проведения количественного анализа компонентов комбинированных лекарственных средств. Решение этой проблемы часто осложнено схожестью физико-химических свойств индивидуальных соединений, входящих в состав композиций, кроме того определенные ограничения связаны с дороговизной лабораторного оборудования, комплектующих и расходных материалов.
Из уровня техники известны запатентованные способы определения содержания полифенольных соединений спектрофотометрическим методом с использованием реактива Фолина-Чокалтеу (патент RU 2700787 С1, опубл. 23.09.2017; патент RU 2519767 С1, опубл. 20.06.2014). Основным недостатком этих способов является невозможность количественного определения содержания индивидуальных компонентов анализируемой смеси в виду того, что реактив Фолина-Чокалтеу неизбирательно вступает в реакцию как с восстанавливающими веществами фенольной, так и нефенольной природы с образованием хромогенов.
Другим широкоизвестным способом количественного анализа композиций полифенолов является дифференциальная спектрофотометрия с использованием алюминия хлорида (патент RU 2266544 С2, опубл. 20.12.2005). Основными его недостатками являются узкий спектр определяемых соединений, ограниченный только флавоноидами, и невозможность количественного определения отдельных компонентов композиций.
Известен способ-прототип количественного определения полифенольных соединений на примере флавоноида кверцетина (Ирискина Л.Б, Суюнбаева А.Т. Кинетический анализ кверцетина // Агропромышленный комплекс и пищевая промышленность, №1, 2020, с. 25-29.), в основе которого лежит реакция взаимодействия окрашенного стабильного радикала 1,1-дифенил-2-пикрилгидразила с фенольными соединениями. В органических растворителях 1,1-дифенил-2-пикрилгидразил имеет полосу поглощения в видимой части спектра с максимумом при 517 нм, при взаимодействии радикала с веществами способными выступать в качестве доноров атомов водорода, которыми могут являться полифенольные соединения происходит падение поглощения при указанной длине волны.
Прототип имеет следующие недостатки:
- Невозможность количественного анализа индивидуальных компонентов композиций полифенолов в виду того, что предложенный радикал также неизбирательно вступает в реакцию как с восстанавливающими веществами фенольной, так и нефенольной природы и дифференцировать вклад компонентов композиций данным способом не представляется возможным. Важно отметить, что в отсутствие такой возможности предложенный способ решает проблему анализа только монокомпонентных составов на основе индивидуального полифенола, которая, в свою очередь, может быть решена значительно проще, путем непосредственного измерения интенсивности поглощения характерных полос спектрофотометрически или фотоэлектроколориметрически.
- Используемый стабильный радикал 1,1-дифенил-2-пикрилгидразила практически нерастворим в воде, что ограничивает применение данного способа растворами в органических растворителях и является негативным с точки зрения принципов зеленой химии.
- Инкубирование проводится при повышенной температуре (термостатирование при 60°С), что в случае анализа термолабильных веществ может приводить к неверным результатам.
- Спектрофотометрическое проведение регистрации в видимой области в максимуме при 517 нм может интерферировать с самими полифенольными соединениями и/или их интермедиатами, образующимися в процессе взаимодействия с радикалом 1,1-дифенил-2-пикрилгидразила, внося ошибку в получаемые результаты
Раскрытие изобретения
Проблема, на решение которой направлено изобретение, является невозможность спектрофотометрического количественного определения содержания индивидуальных компонентов в композиционных смесях полифенольной природы с близкими физико-химическими свойствами.
Техническим результатом, на достижение которого направлено заявленное изобретение, является возможность одновременного спектрофотометрического количественного определения содержания индивидуальных полифенольных компонентов в бинарных композициях
Технический результат достигается за счет того, что для осуществления изобретения берут раствор 2,2'-азинобис(3-этилбензотиазолин-6-сульфоновой кислоты) диаммониевой соли (далее - ABTS) в воде, водном буфере, водно-метанольной или водно-этанольной смеси к которому добавляют раствор включающий в себя исследуемую смесь, после чего добавляют раствор пероксодисульфата калия в воде или водном буфере, до мольного соотношения ABTS:PP от 2:1 до 3:1, полученный раствор встряхивают и снимают кинетическую кривую в максимуме поглощения при 730-750 нм, которую регистрируют на спектрофотометре до появления устойчивого роста поглощения; на кинетической кривой наблюдаются несколько периодов плато, отделенных друг от друга короткими периодами роста поглощения, каждый из которых соответствует одному из компонентов композиционного состава, сопоставляя кинетические кривые композиций с кинетическими кривыми индивидуальных компонентов-стандартов, выясняют, каким из компонентов соответствуют какие из периодов плато, далее осуществляют расчет количественного содержания компонентов смеси путем соотнесения продолжительностей периодов плато индивидуально взятых референсных образцов с соответствующими им периодами плато на кинетической кривой композиции по формуле:
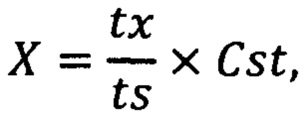
где Х - содержание компонента в исследуемой композиции, %;
tx - продолжительность периода плато исследуемой композиции, мин;
tst - продолжительность периода плато стандартного образца, мин;
Cst - содержание исследуемого компонента в стандартном образце.
Краткое описание чертежей
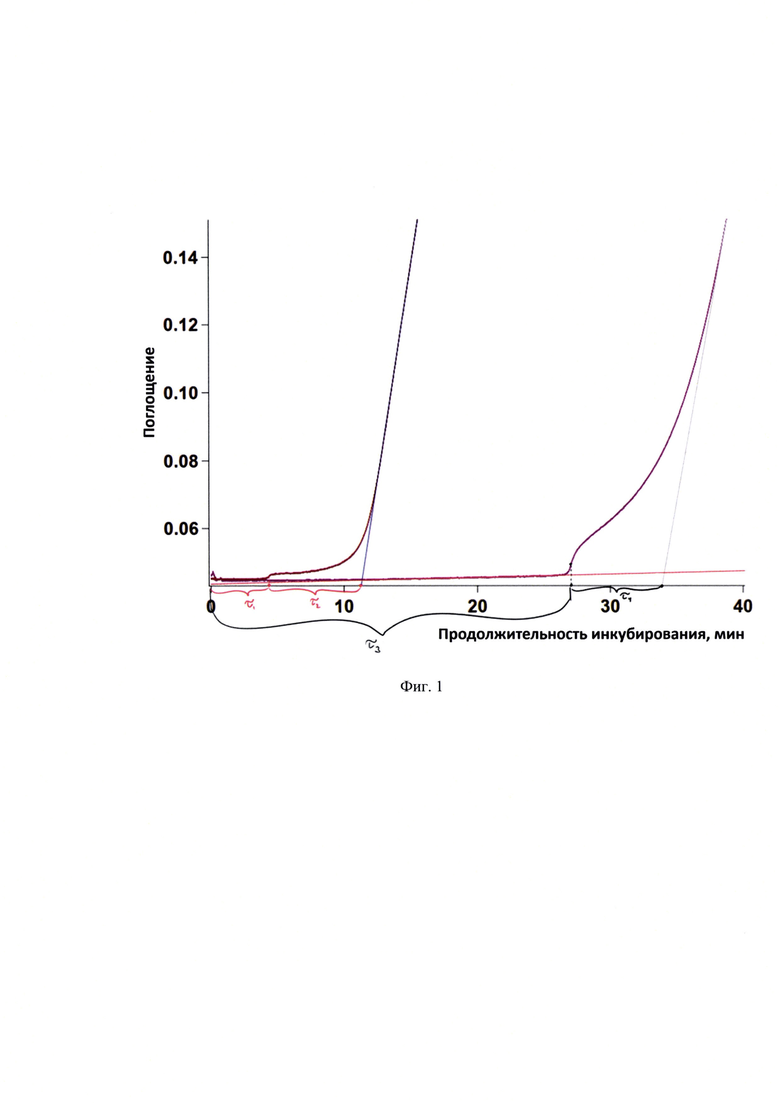
Изобретение поясняется чертежами, где фиг. 1 представлены кинетические кривые развития 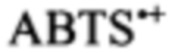 в присутствии композиции α-токоферол-дигидрокверцетин при соотношении компонентов 6:1 (36 мкмоль/л и 6 мкмоль/л альфа-токоферола и дигидрокверцетина, соответственно). Ось абсцисс - время после введения K2S2O8, мин. Ось ординат - оптическая плотность раствора при 750 нм, на фиг. 2 - кинетические кривые развития
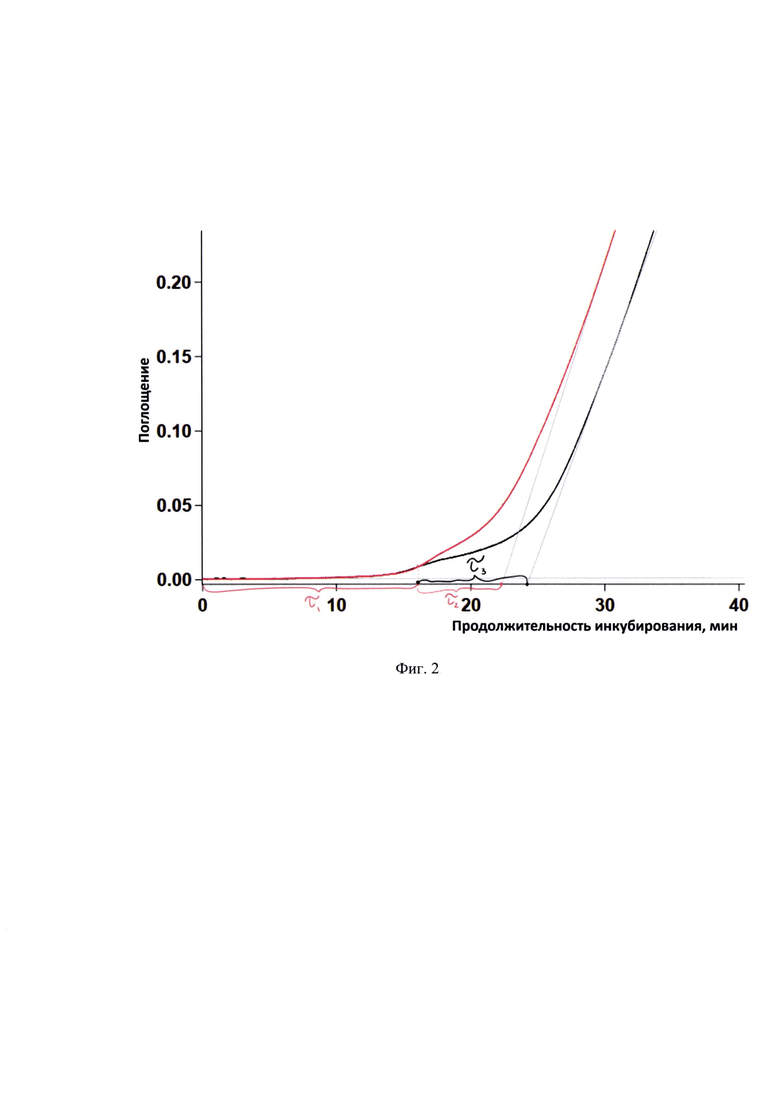
в присутствии композиции α-токоферол-дигидрокверцетин при соотношении компонентов 6:1 (36 мкмоль/л и 6 мкмоль/л альфа-токоферола и дигидрокверцетина, соответственно). Ось абсцисс - время после введения K2S2O8, мин. Ось ординат - оптическая плотность раствора при 750 нм, на фиг. 2 - кинетические кривые развития 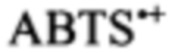 в присутствии сухих экстрактов сучковой зоны древесины лиственницы даурской с разным содержанием доминирующих компонентов: дигидрокверцетина и секоизоларицирезинола. Ось абсцисс - время после введения K2S2O8, мин. Ось ординат - оптическая плотность раствора при 730 нм. Кроме того, заявляемое решение поясняется таблицей, в которой приведены результаты анализа сухих экстрактов сучковой зоны древесины лиственницы даурской.
в присутствии сухих экстрактов сучковой зоны древесины лиственницы даурской с разным содержанием доминирующих компонентов: дигидрокверцетина и секоизоларицирезинола. Ось абсцисс - время после введения K2S2O8, мин. Ось ординат - оптическая плотность раствора при 730 нм. Кроме того, заявляемое решение поясняется таблицей, в которой приведены результаты анализа сухих экстрактов сучковой зоны древесины лиственницы даурской.
Осуществление изобретения
Для осуществления изобретения берут раствор 2,2'-азинобис(3-этилбензотиазолин-6-сульфоновой кислоты) диаммониевой соли (далее - ABTS) в воде, водном буфере, водно-метанольной или водно-этанольной смеси к которому добавляют раствор включающий в себя исследуемую смесь, после чего добавляют раствор пероксодисульфата калия в воде или водном буфере. Мольное соотношение ABTS:PP в полученном растворе должно составлять от 2:1 до 3:1. Полученный раствор встряхивают и снимают кинетическую кривую в максимуме поглощения при 730-750 нм. Полученную кинетическую кривую регистрируют на спектрофотометре до появления устойчивого роста поглощения. На кинетической кривой наблюдаются несколько периодов плато, отделенных друг от друга короткими периодами роста поглощения, каждый из которых соответствует одному из компонентов композиционного состава. Сопоставляя кинетические кривые композиций с кинетическими кривыми индивидуальных компонентов-стандартов, выясняют, каким из компонентов соответствуют какие из периодов плато. Путем соотнесения продолжительностей периодов плато индивидуально взятых референсных образцов с соответствующими им периодами плато на кинетической кривой композиции осуществляют расчет количественного содержания компонентов смеси.
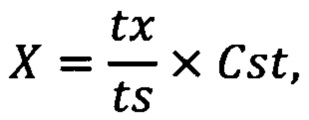
где Х - содержание компонента в исследуемой композиции, %;
tx - продолжительность периода плато исследуемой композиции, мин;
tst - продолжительность периода плато стандартного образца, мин;
Cst - содержание исследуемого компонента в стандартном образце.
Изобретение поясняется примерами
Пример 1. Анализировали композицию альфа-токоферола с дигидрокверцетином. Для анализа брали точные навески стандартов дигидрокверцетина и α-токоферола, которые затем растворяли в этаноле. Получали такие концентрации, которые при добавлении в количестве 10-50 мкл в инкубационную смесь содержащую 3,5 мл раствора ABTS в смеси метанол-вода 95:5 с концентрацией 2,6 мг/мл вызывали задержку в появлении поглощения при 750 нм после добавления 0,5 мл раствора пероксодисульфата калия с концентрацией 3,2 мг/мл (температура инкубирования 24°С) длительностью 5-50 мин. Комбинируя разные концентрации компонентов и сопоставляя кинетические кривые композиций с кинетическими кривыми индивидуальных компонентов, выяснили, что на кинетической кривой композиции наблюдаются два периода плато, первый из которых соответствует α-токоферолу, а второй дигидрокверцетину.
Например, добавление раствора дигидрокверцетина в конечной концентрации 6 мкмоль/л вызывало появление периода плато продолжительностью 6,77±0,24 мин; добавление альфа-токоферола в количестве 6 мкмоль/л и 36 мкмоль/л вызывало появление периода плато продолжительностью 4,88±0,45 мин и 29,03±1,14 мин, соответственно. На кинетических кривых композиций альфа-токоферол-дигидрокверцетин 1:1 (по 6 мкмоль/л) и 6:1 (36 мкмоль/л и 6 мкмоль/л альфа-токоферола и дигидрокверцетина, соответственно) наблюдались первые периоды плато продолжительностью 4,54 мин и 28,18 мин (фиг. 1, период плато τ1 и период плато τ3), в то время как вторые периоды плато составили 6,98 мин и 6,43 мин (фиг. 1, период плато τ2 и период плато τ4), сопоставляя кривые индивидуальных соединений и композиций, можно сделать вывод о том, что первый период плато соответствует альфа-токоферолу, а второй дигидрокверцетину.
Далее брали для анализа модельную композицию дигидрокверцетина и α-токоферола, по полученным кинетическим кривым выяснили, что первый период плато длительностью 43,13±2,14 мин соответствует концентрации α-токоферола 52,2 мкмоль/л (n=3), а второй, длительностью 10,9±0,4 мин минут концентрации дигидрокверцетина 9,7 мкмоль/л (n=3). Реально взятые количества смоделированной смеси соответствовали концентрациям 50,0 мкмоль/л и 10,0 мкмоль/л, таким образом ошибка определения составила в первом случае 4,4%, а во втором 3,0%.
Пример 2.
Анализировали сухие экстракты сучковой зоны древесины лиственницы даурской с разным содержанием доминирующих компонентов: дигидрокверцетина и секоизоларицирезинола.
К 2,6 мл фосфатного буферного раствора (рН=7,4) прибавляли 0,7 мл 3,84 мг/мл раствора ABTS, а также 20 мкл исследуемого раствора (этанольный раствор точной навески экстракта, стандартного образца, или их смеси). К полученной смеси добавляли 0,7 мл раствора 0,66 мг/мл пероксодисульфата калия, встряхивали в течение 15 секунд, после чего спектрофотометрически регистрировали оптическую плотность полосы поглощения в максимуме при 730 нм в течение 45 мин (температура инкубирования 24°С) для получения кинетической кривой. Предварительно получали кинетические кривые этанольных (этанол-вода 95:5) растворов аутентичных образцов 2 мг/мл дигидрокверцетина, 2 мг/мл секоизоларицирезинола и растворов модельных смесей, одновременно содержащих 2 мг/мл дигидрокверцетина и 2 мг/мл секоизоларицирезинола (смесь 1) и 2 мг/мл дигидрокверцетина и 3 мг/мл секоизоларицирезинола (смесь 2).
На кинетических кривых модельных смесей можно выделить несколько стадий: период плато 1 (фиг. 2, τ1), период плато 2 (фиг. 2, τ2 или τ3) с последующим периодом роста кривой. Период плато 1 был одинаков для обеих модельных смесей (соответствует дигидрокверцетину, так как его концентрацию не меняли). Периоды плато 2 на кинетических кривых модельных смесей отличаются (соответствуют секоизоларицирезинолу в разных концентрациях), последний короче для смеси с меньшим содержанием секоизоларицирезинола пропорционально содержанию. Затем брали навески экстракта 1 и экстракта 2 в количестве по 0,05 г (точная навеска) и растворяли в 25 мл этанола. Полученные растворы исследовали в условиях аналогичных таковым растворов стандартных образцов (фиг. 1). Содержание компонентов в экстрактах определяли по формуле:
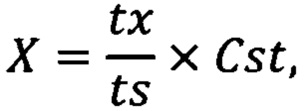
где Х - содержание компонента в исследуемой композиции, %;
tx - продолжительность периода плато исследуемой композиции, мин;
tst - продолжительность периода плато стандартного образца, мин;
Cst - содержание исследуемого компонента в стандартном образце.
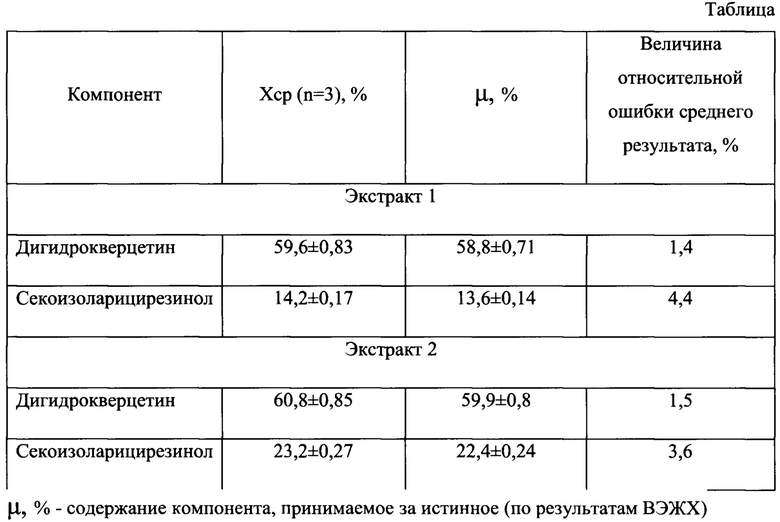
Сопоставление полученных данных с результатами, полученными методом ВЭЖХ (таблица) показывает, что ошибка определения составила не более 1,5% и 4,4 в отношении дигидрокверцетина и секоизоларицирезинола, соответственно.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭКСПРЕСС ТЕСТ-СИСТЕМА ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ ЁМКОСТИ ИНДИВИДУАЛЬНЫХ СОЕДИНЕНИЙ И КОМПОЗИЦИОННЫХ СОСТАВОВ | 2023 |
|
RU2814285C1 |
| Способ получения липидного комплекса из жома плодов граната | 2015 |
|
RU2606844C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ МИКОЗА НОГТЕЙ | 2019 |
|
RU2699653C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КАЛЬЦИЯ И МАГНИЯ В ЛЕКАРСТВЕННОМ РАСТИТЕЛЬНОМ СЫРЬЕ | 2011 |
|
RU2466387C1 |
| СРЕДСТВО ДЛЯ ПРОПИТКИ ГИГИЕНИЧЕСКОГО ТАМПОНА, ОБЛАДАЮЩЕЕ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ, И СПОСОБ ПОЛУЧЕНИЯ ФИТОТАМПОНА, ОБЛАДАЮЩЕГО АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2740284C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДУБИЛЬНЫХ ВЕЩЕСТВ В РАСТИТЕЛЬНОМ СЫРЬЕ | 2010 |
|
RU2439568C1 |
| Фармацевтическая субстанция для лечения инфицированных ран различного генеза | 2018 |
|
RU2687102C1 |
| СПОСОБ ХРАНЕНИЯ СЫВОРОТОК КРОВИ С АНТИТЕЛАМИ К ВОЗБУДИТЕЛЯМ ПАРАЗИТАРНЫХ БОЛЕЗНЕЙ | 2019 |
|
RU2704134C1 |
| СПОСОБ ДИНАМИЧЕСКОЙ МАГНИТНО-РЕЗОНАНСНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЯИЧНИКОВ | 2015 |
|
RU2578184C1 |
| СОСТАВ И СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННЫХ ПЛЕНОК, ОБЛАДАЮЩИХ АНТИМИКРОБНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2762154C1 |
Изобретение относится к области спектрофотометрического анализа и касается способа спектрофотометрического анализа количественного содержания полифенольных компонентов в бинарных композициях. При осуществлении способа к раствору 2,2'-азинобис(3-этилбензотиазолин-6-сульфоновой кислоты) диаммониевой соли (ABTS) добавляют раствор исследуемой смеси и раствор пероксодисульфата калия. Раствор встряхивают и снимают кинетическую кривую в максимуме поглощения при 730-750 нм, которую регистрируют до появления устойчивого роста поглощения. На кинетической кривой наблюдают несколько периодов плато, отделенных друг от друга короткими периодами роста поглощения. Сопоставляя кинетические кривые композиций с кинетическими кривыми индивидуальных компонентов-стандартов, определяют, какие из периодов плато соответствуют отдельным компонентам. Расчет количественного содержания компонентов смеси осуществляют путем соотнесения продолжительностей периодов плато референсных образцов с соответствующими им периодами плато на кинетической кривой композиции. Технический результат заключается в обеспечении возможности количественного анализа компонентов композиции, упрощении способа анализа и повышении точности измерений. 2 ил., 1 табл.
Способ спектрофотометрического анализа количественного содержания полифенольных компонентов в бинарных композициях, включающий регистрацию оптической плотности продуктов взаимодействия компонентов композиции со свободными радикалами, отличающийся тем, что берут раствор 2,2'-азинобис (3-этилбензотиазолин-6-сульфоновой кислоты) диаммониевой соли (далее - ABTS) в воде, водном буфере, водно-метанольной или водно-этанольной смеси, к которому добавляют раствор, включающий в себя исследуемую смесь, после чего добавляют раствор пероксодисульфата калия в воде или водном буфере, до мольного соотношения ABTS:PP от 2:1 до 3:1, полученный раствор встряхивают и снимают кинетическую кривую в максимуме поглощения при 730-750 нм, которую регистрируют на спектрофотометре до появления устойчивого роста поглощения; на кинетической кривой наблюдаются несколько периодов плато, отделенных друг от друга короткими периодами роста поглощения, каждый из которых соответствует одному из компонентов композиционного состава, сопоставляя кинетические кривые композиций с кинетическими кривыми индивидуальных компонентов-стандартов, выясняют, каким из компонентов соответствуют какие из периодов плато, далее осуществляют расчет количественного содержания компонентов смеси путем соотнесения продолжительностей периодов плато индивидуально взятых референсных образцов с соответствующими им периодами плато на кинетической кривой композиции по формуле:
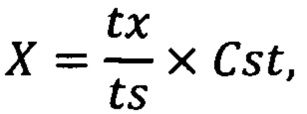
где Х - содержание компонента в исследуемой композиции, %;
tx - продолжительность периода плато исследуемой композиции, мин;
tst - продолжительность периода плато стандартного образца, мин;
Cst - содержание исследуемого компонента в стандартном образце.
| Ирискина Л.Б, Суюнбаева А.Т | |||
| "Кинетический анализ кверцетина", АГРОПРОМЫШЛЕННЫЙ КОМПЛЕКС И ПИЩЕВАЯ ПРОМЫШЛЕННОСТЬ, No 1, 2020 г., стр | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Способ определения суммарного содержания фенольных соединений в растительных объектах | 2019 |
|
RU2700787C1 |
| CN 108593577, 28.09.2018 | |||
| CN 106226431 A, 14.12.2016. | |||
Авторы
Даты
2024-03-06—Публикация
2023-10-02—Подача