Область применения
Изобретение относится к области физиологии и биохимии растений и может быть использовано при проведении фундаментальных исследований по физиологии, биохимии, селекции и биотехнологии растений, а также найти применение в химико-фармацевтической промышленности при оценке качества растительного сырья.
Уровень техники
Фенольные соединения (ФС) представляют собой уникальные вещества вторичного метаболизма, обладающие антирадикальными свойствами и антиоксидантной активностью, образование которых характерно именно для растений (Меньшикова Е.Б., Ланкин В.З., Кандалинцева Н.В. «Фенольные антиоксиданты в биологии и медицине. Строение, свойства, механизмы действия». Berlin, Academic Publishing, 2012, 488).
Характерной особенностью ФС является способность к взаимодействию с активными формами кислорода (АФК), тем самым способствуя их инактивации во всех живых организмах (растения, животные, человек). Избыточные количества АФК образуются в клетках при действии различных стрессоров, включая тяжелые металлы, токсические отходы химических производств и пр., а также при повышенном уровне озона и ультрафиолетового излучения в атмосфере (Тараховский Ю.С., Ким Ю.А., Абдрасилов Б.С., Музафаров Е.Н. «Флавоноиды: биохимия, биофизика, медицина» М., Пущино, 2013, 380). АФК взаимодействуют с белками, липидами и ДНК, повреждая их и даже вызывая гибель клеток (Тюкавкина Н.А. «Биофлавоноиды», М., Русский врач, 2002, 56). В этом аспекте присутствие ФС в растительных объектах, включая их количество, является важным показателем устойчивости растений к стрессовым воздействиям, а также критерием целесообразности использования растительного сырья в качестве продукта с антиоксидантной активностью в пищевом рационе человека (Куркин В.А. "Актуальные вопросы совершенствования стандартизации лекарственного растительного сырья и лекарственных растительных препаратов, содержащих фенольные соединения" // Современные наукоемкие технологии. 2016. №8-2. С. 247-250).
Известен способ определения суммарного содержания ФС колориметрическим методом с использованием реактива Фолина-Чокальтеу, содержащего фосфовольфрамовые и фосфомолибденовые кислоты, которые при восстановлении фенольными соединениями (ФС) в щелочной среде образуют комплекс синего цвета (вольфрамовая синь), интенсивность окраски которого пропорциональна количеству ФС (Singleton, V.L., Orthofer, R., Lamuela-Raventos, R.M. "Analysis of total phenols and other oxidation substrates and antioxidants by means of Folin-Ciocalteu reagent ", in Methods in Enzymology, Academic Press Inc., San-Diego, 1999, Vol. 299, P. 152-178).
Еще известен способ определения суммарного содержания ФС в водно-метанольных экстрактах из 24-х экзотических фруктов методом Фолина-Чокальтеу (J. Contreras-Calderon, L. Calderon-Jaimes, E. Guerra-Hernandez, В. Garcia-Villanova "Antioxidant capacity, phenolic content and vitamin С in pulp, peel and seed from 24 exotic fruits from Colombia" Food Research International. 2011. Vol. 44. P. 2047-2053).
Кроме того, известен способ определения суммарного содержания ФС в метанольных экстрактах из листьев айвы и чая методом Фолина-Чокальтеу (R.М. Costa, A.S. Magalhes, J.A. Pereira, Р.В. Andrade, P. Valentro "Evaluation of free radical-scavenging and antihemolytic activities of quince (Cydonia oblonga) leaf: A comparative study with green tea (Camellia sinensis) Food and Chemical Toxicology. 2009. Vol. 47. P. 860-865).
Недостатками этих методов является большой расход реактивов, длительность процедуры определения суммарного содержания ФС, а также использование токсичного растворителя - метанола.
Также известен способ определения суммарного содержания ФС методом Фолина-Чокальтеу с использованием микропланшетов в метанольных экстрактах из клубники, киви и моркови ("The Folin- Ciocalteu assay revisited: improvement of its specificity for total phenolic content determination", Analytical Methods. 2013.Vol. 5. P. 5990-5999). В этом способе в ячейку микропланшета помещают 0,015 см3 экстракта, содержащего ФС, добавляют 0,240 см3 дистиллированной воды, 0,015 см3 реактива Фолина-Чокальтеу, 0,030 см3 5,3% водного раствора натрия углекислого. С помощью специального спектрофотометра, позволяющего измерять оптическую плотность растворов на микропланшетах, плотность образовавшей окраски измеряют при 765 нм.
Недостатком этого метода, несмотря на минимальный расход реактива Фолина-Чокальтеу, является необходимость использования специального оборудования: микропланшетов и спектрофотометра, позволяющего измерять оптическую плотность растворов на микропланшетах, а также использование токсичного растворителя - метанола.
Ближайшим способом к предлагаемому является способ определения суммарного содержания ФС в чае (ГОСТ Р ИСО 14502-1-2010. Чай. Метод определения общего содержания полифенолов) - прототип.
Способ предусматривает 2-хкратное экстрагирование ФС из измельченной пробы чая (массой 0,2 г) 70% водным раствором метанола при температуре 70°С при периодическом перемешивании с последующим центрифугированием и промыванием осадка. Экстракты объединяют, доводят их объем до 10,0 см3 холодным 70% водным раствором метанола и перемешивают. Приготовленный таким образом экстракт разбавляют дистиллированной водой в 100 раз, помещают по 1,0 см3 разбавленного экстракта в отдельные градуированные пробирки. В каждую пробирку добавляют по 5,0 см3 реактива Фолина-Чокальтеу, разбавленного в 10 раз, и перемешивают. Через 3 мин в каждую пробирку добавляют по 4,0 см3 7,5%-ного водного раствора натрия углекислого, пробирки закрывают пробками, перемешивают и оставляют при комнатной температуре. Через 1 ч суммарное содержание ФС в экстрактах определяют колориметрическим методом с применением реактива Фолина-Чокальтеу. Оптическую плотность раствора измеряют относительно воды при длине волны 765 нм. Длина оптического пути - 1 см. Суммарное содержание ФС выражают мг-эквивалентах (мг-экв.) галловой кислоты на г сухой массы чая.
Недостатком этого способа является большой расход реактивов, продолжительность времени экстракции ФС и использование токсичного растворителя метанола, а также высокая температура экстракции, что может приводить к окислению части ФС и, как следствие, неправильной оценке результатов определения.
Задача изобретения
Задачей нашего изобретения является разработка безопасного, экономически выгодного способа определения суммарного содержания ФС в растительных объектах с использованием стандартного оборудования для лабораторных исследований, без применения метанола, при сокращении времени экстракции.
Решение задачи
Данная задача решается созданием нового способа определения суммарного содержания ФС в растительных объектах (гречиха, пшеница, каллусная культура ткани чайного растения) заключающийся в их измельчении, экстрагировании в спирте при перемешивании, последующим центрифугированием, добавлением к экстракту реактива Фолина-Чокальтеу и натрия углекислого, причем пробу растительного сырья массой 0,05 г измельчают, растирают с 1,5 см3 96% этанола в пробирках, настаивают в течение 45 мин при температуре 45°С при периодическом перемешивании с последующим центрифугированием в течение 2-х минут при частоте вращения 16000 об/мин, из полученного экстракта, содержащего ФС, отбирают пробы, объемом 0,075 см3, добавляют к ним по 0,075 см3 реактива Фолина-Чокальтеу, разбавленного в 5 раз, перемешивают, через 3 мин добавляют по 0,15 см3 20% раствора натрия углекислого и по 1,2 см3 дистиллированной воды, закрывают крышкой, перемешивают и оставляют при комнатной температуре, через 1 ч измеряют оптическую плотность образовавшейся вольфрамовой сини при длине волны 725 нм, длина оптического пути - 1 см.
Суммарное содержание ФС выражают мг-экв. галловой кислоты на г сырой массы сырья
Существенное отличие предлагаемого способа от прототипа состоит в том, что экстракцию ФС из растертого сырья проводят в одну стадию при более низкой температуре с использованием нетоксичного растворителя, а также изменяют соотношение реактивов при определении суммарного содержания ФС.
Новизна изобретения.
Новизной настоящего изобретения является создание нового способа определения суммарного содержания ФС в растительных объектах, позволяющего получать достоверные результаты при значительной экономии реактивов и сырья и без использования токсичного растворителя.
Сущность изобретения.
По мнению авторов, предлагаемое изобретение состоит в том, что замена токсичного растворителя метанола на этанол повышает безопасность работы, а снижение температуры экстракции уменьшает вероятность окисления ФС. Изменения в соотношениях сырья и реактивов, а также уменьшение их количеств позволяет сократить расход реактивов и растительного сырья при высокой чувствительности способа и достоверности получаемых данных о содержании ФС в растительных объектах.
Изобретение иллюстрируется следующими примерами.
Пример 1 (по прототипу)
В пробирки для экстрагирования помещают по 0,700 г каллусной культуры ткани чайного растения, свежих измельченных листьев пшеницы (сорт Амир) или гречихи (сорт Дарья), соответственно. Пробирки помещают на водяную баню с температурой 70°С, вносят 5,0 см3 нагретого до 70°С 70% водного раствора метанола, закрывают пробкой и перемешивают. Экстрагирование проводят на водяной бане в течение 10 мин., перемешивая через 5 и 10 мин. Извлекают пробирки из водяной бани, охлаждают до комнатной температуры и центрифугируют в течение 10 мин при частоте вращения 3500 об/мин. Надосадочную жидкость (экстракт) переносят в градуированную пробирку. Повторную экстракцию осадка проводят при тех же условиях. Экстракты объединяют, доводят их объем до 10,0 см3 холодным 70% водным раствором метанола и перемешивают. По 1,0 см3 приготовленных таким образом экстрактов из каллусной культуры ткани чая, листьев пшеницы и гречихи помещают в отдельные градуированные пробирки. В отдельные градуированные пробирки вместо экстракта, содержащего ФС, помещают по 1,0 см3 дистиллированной воды для холостых проб. В каждую пробирку добавляют по 5,0 см3 реактива Фолина-Чокальтеу, разбавленного в 10 раз, и перемешивают. Через 3 мин в каждую пробирку добавляют по 4,0 см3 7,5%-ного водного раствора натрия углекислого, пробирки закрывают пробками, перемешивают и оставляют при комнатной температуре. Через 1 ч измеряют оптическую плотность раствора относительно воды при длине волны 765 нм. Длина оптического пути - 1 см.
Суммарное количество ФС, содержащееся в 1 г сырья рассчитывают по формуле:
С=(Dоп-Dк)⋅V/K⋅М⋅1000, где
С - суммарное количество ФС в мг-экв галловой кислоты/г сырой массы сырья
Dоп - оптическая плотность образца при 765 нм
Dк - оптическая плотность холостого опыта при 765 нм
K - тангенс угла наклона калибровочной кривой (0,0037)
V - объем экстракта (10 см3)
m - масса сырья (0,7 г), г
1000 - пересчет мкг в мг
Анализ проводят в трех биологических и двух аналитических повторностях. Время, затраченное на проведение эксперимента, составляет 215 мин. Все результаты статистически обрабатываются в программе Excel. В таблице 1 представлены средние значения и их стандартные ошибки.
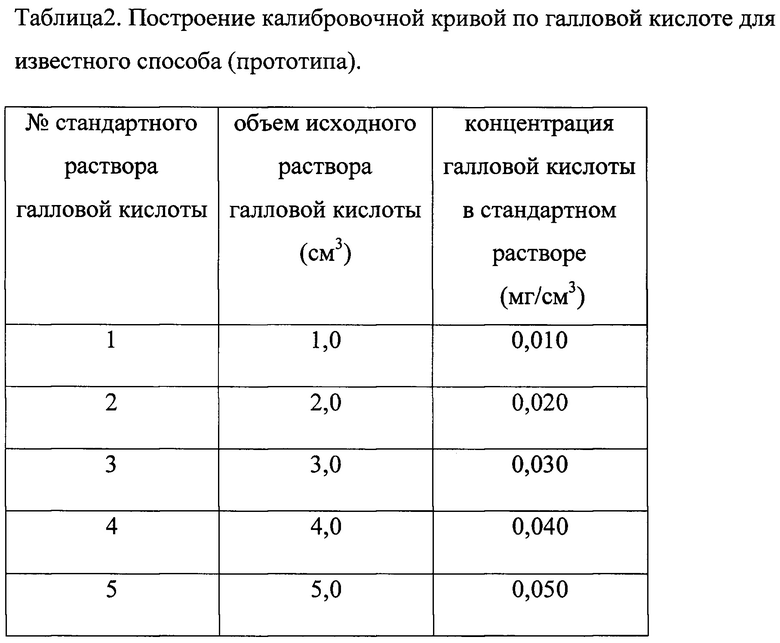
Для построения калибровочной кривой в мерной колбе, объемом 100 см3, готовят исходный стандартный водный раствор галловой кислоты с массовой концентрацией 1 мг/см3. Переносят исходный стандартный раствор галловой кислоты в объемах, указанных в таблице 2, в мерные колбы на 100 см3 и доводят до метки дистиллированной водой. Затем помещают по 1,0 см3 стандартных растворов галловой кислоты, согласно табл. 2 в отдельные градуированные пробирки. В отдельные градуированные пробирки вместо растворов галловой кислоты помещают по 1,0 см3 дистиллированной воды для холостых опытов. В каждую пробирку добавляют по 5,0 см3 реактива Фолина-Чокальтеу, разбавленного в 10 раз, и перемешивают. Через 3 мин в каждую пробирку добавляют по 4,0 см3 7,5%-ного водного раствора натрия углекислого, пробирки закрывают пробками, перемешивают и оставляют при комнатной температуре. Через 1 ч измеряют оптическую плотность растворов относительно воды при длине волны 765 нм. Длина оптического пути - 1 см.
Анализ проводят в двух повторностях. Строят калибровочную кривую зависимости оптической плотности раствора галловой кислоты от массовой концентрации галловой кислоты в растворе. Определяют коэффициент линейной зависимости К (тангенс угла наклона калибровочной кривой).
Пример 2 (предлагаемый способ)
Измельченные пробы сырья (каллусной культуры ткани чая, свежих листьев пшеницы (сорт Амир) или гречихи (сорт Дарья), массой 0,05 г растирают с 1,5 см3 96% этанола в пробирках «Эппендорф», закрывают крышкой, настаивают в течение 45 мин при температуре 45°C с периодическим перемешиванием (каждые 15 мин) и центрифугируют в течение 2-х минут при частоте вращения 16000 об/мин. Из полученных экстрактов отбирают образцы по 0,075 см3, к каждому образцу добавляют по 0,075 см3 реактива Фолина-Чокальтеу, разбавленного в 5 раз, перемешивают, через 3 мин добавляют по 0,15 см3 20% раствора натрия углекислого и по 1,2 см3 дистиллированной воды, перемешивают и оставляют при комнатной температуре. Через 1 ч измеряют оптическую плотность раствора при длине волны 725 нм против холостого опыта. Длина оптического пути - 1 см.
Суммарное содержание ФС выражают в мг-экв. галловой кислоты на г сырой массы сырья.
Суммарное количество ФС, содержащееся в 1 г сырья рассчитывают по формуле:
C=D⋅V/K⋅М⋅1000, где
С - суммарное количество ФС в мг-экв галловой кислоты/г сырой массы сырья
D - оптическая плотность раствора при 725 нм
K - тангенс угла наклона калибровочной кривой (0,0040)
V - объем экстракта (1,5 см3), см3
m - масса сырья (0,05 г), г
1000 - пересчет мкг в мг
Анализ проводят в трех биологических и двух аналитических повторностях. Время, затраченное на проведение эксперимента, составляет 120 мин. Все результаты статистически обрабатываются в программе Excel. В таблице 1 представлены средние значения и их стандартные ошибки.
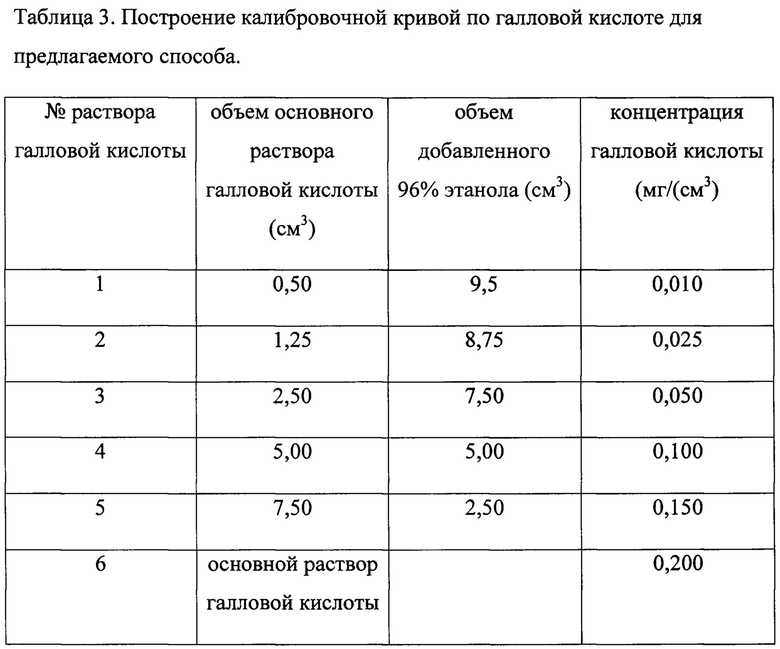
Для построения калибровочной кривой в мерной колбе, объемом 50 см3, готовят исходный стандартный раствор галловой кислоты в 96% этаноле с массовой концентрацией 0,200 мг/см3. Разбавляя исходный раствор галловой кислоты 96% этанолом в пропорциях, указанных в таблице 3, получают растворы меньшей концентрации. Затем помещают по 0,075 см3 стандартных растворов галловой кислоты, согласно табл. 2 в отдельные градуированные пробирки. В отдельные градуированные пробирки вместо растворов галловой кислоты помещают по 0,075 см3 96% этанола для холостых опытов, в каждую пробирку добавляют по 0,075 см3 реактива Фолина-Чокальтеу, разбавленного в 5 раз, перемешивают, через 3 мин. добавляют по 0,150 см3 20% раствора натрия углекислого и по 1,2 см3 дистиллированной воды, перемешивают. Реакция протекает при комнатной температуре. Через 1 ч измеряют оптическую плотность раствора против холостого опыта при длине волны 725 нм. Длина оптического пути - 1 см.
Анализ проводят в двух повторностях. Строят калибровочную кривую зависимости оптической плотности раствора галловой кислоты от массовой концентрации галловой кислоты в растворе. Определяют коэффициент линейной зависимости К (тангенс угла наклона калибровочной кривой).
Перечень графических материалов
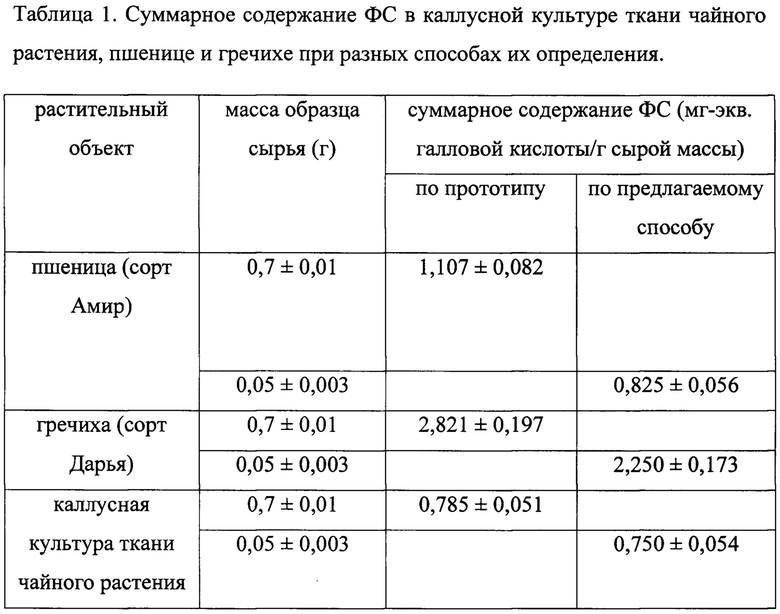
Таблица 1. Суммарное содержание ФС в каллусной культуре ткани чайного растения, пшенице и гречихе при разных способах их определения.
Таблица 2. Построение калибровочной кривой по галловой кислоте для известного способа (прототипа).
Таблица 3. Построение калибровочной кривой по галловой кислоте для предлагаемого способа.
Результаты изобретения
Как следует из анализа данных (таблица 1) при определении суммарного содержания ФС в растительных объектах по прототипу требуется увеличить массу пробы сырья (0,7 г) по сравнению с чаем (0,2 г). Это объясняется тем, что чай относится к так называемым «растениям-фенолонакопителям» и суммарное содержание ФС в нем превышает 60 мг/г сухой массы (Запрометов М.Н. «Биохимия катехинов», М., «Наука», 1964). Количество таких растений в природе очень невелико.
Уменьшение количества ФС в примере 2 (по предлагаемому способу) по сравнению с примером 1 (по прототипу) обусловлено разными условиями экстракции. При использовании водно-спиртовых экстрагентов при высокой температуре в экстракт переходят не только ФС, но и сахара и часть аминокислот, которые также взаимодействуют с реактивом Фолина-Чокальтеу, что приводит к завышению результатов определения.
Основной целью нашей разработки является создание нового чувствительного способа определения суммарного содержания ФС в растительных объектах, позволяющего получать достоверные данные при значительном сокращении расхода сырья и реактивов, а также повысить безопасность работы при сокращении времени экстракции.
В отличие от прототипа в предлагаемом способе новое соотношение реагентов: объема экстракта, раствора натрия углекислого и реактива Фолина-Чокальтеу, полученное в ходе лабораторных испытаний, обеспечивает значительное сокращение расхода реактивов при высокой чувствительности способа (от 0,010 мг/см3 экстракта). Расход сырья также сокращается. Замена токсичного экстрагента метанола на этанол повышает безопасность работы.
Таким образом, достигнута поставленная цель настоящего изобретения -создание нового чувствительного способа определения суммарного содержания ФС в растительных объектах.
Предлагаемый способ определения суммарного содержания ФС в растительных объектах позволяет сократить расход сырья, продолжительность экстракции ФС при более низкой температуре, что предотвращает переход в экстракт веществ нефенольной природы, взаимодействующих с реактивом Фолина-Чокальтеу, расход реактива Фолина-Чокальтеу в 20 раз, повысить безопасность работы заменой токсичного растворителя метанола на этанол, получить достоверные данные о содержании ФС в растительных объектах.
Отличие предлагаемого способа от прототипа состоит в том, что экстракцию ФС из сырья проводят в одну стадию при более низкой температуре с использованием нетоксичного растворителя, а также изменяют соотношение реактивов при определении суммарного содержания фенольных соединений.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ повышения ингибирующей активности цефтазидима комплексом фенольных соединений | 2024 |
|
RU2839893C1 |
| Способ выделения полифенолов из корневищ имбиря | 2019 |
|
RU2740997C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИФЕНОЛОВ ЧАЯ | 2013 |
|
RU2519767C1 |
| Способ установления подлинности и качества зверобоя продырявленного (Hypericum perforatum L.) | 2015 |
|
RU2614200C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ ОКСИДА ЦЕРИЯ | 2019 |
|
RU2698679C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДУБИЛЬНЫХ ВЕЩЕСТВ В РАСТИТЕЛЬНОМ СЫРЬЕ | 2010 |
|
RU2439568C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ СТЕПЕНИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ ОРГАНИЗМА У БОЛЬНЫХ РАСПРОСТРАНЕННЫМИ ХРОНИЧЕСКИМИ ДЕРМАТОЗАМИ | 2006 |
|
RU2333496C1 |
| Способ идентификации и раздельного количественного определения танина и галловой кислоты при совместном присутствии в растительном сырье и фитопрепаратах без предварительного разделения | 2015 |
|
RU2613878C2 |
| Противовирусное средство на основе экстракта культуры "бородатых корней" ("hairy roots") селитрянки Шобера (Nitraria schoberi L.) | 2016 |
|
RU2615376C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ОБЩЕГО СОСТОЯНИЯ БОЛЬНОГО С ОСТРЫМ ДЕСТРУКТИВНЫМ ПАНКРЕАТИТОМ И ПРОГНОЗИРОВАНИЯ ИСХОДА ЗАБОЛЕВАНИЯ | 2013 |
|
RU2568601C2 |
Изобретение относится к области физиологии и биохимии растений и может быть использовано при определении содержания фенольных соединений (ФС) в растительных объектах. Способ включает измельчение растительного сырья, экстрагирование в спирте при перемешивании, последующее центрифугирование, добавление к экстракту реактива Фолина-Чокальтеу и натрия углекислого. Измельчение пробы сырья массой 0,05 г производят с растиранием с 1,5 см3 96% этанола, экстрагирование фенольных соединений проводят в течение 45 мин при температуре 45°C с периодическим перемешиванием (каждые 15 мин) и последующим центрифугированием в течение 2-х минут при частоте вращения 16000 об/мин, из полученного экстракта отбирают пробы, объемом 0,075 см3, добавляют к ним по 0,075 см3 реактива Фолина-Чокальтеу, разбавленного в 5 раз, перемешивают, через 3 мин добавляют по 0,15 см3 20% раствора натрия углекислого и по 1,2 см3 дистиллированной воды, закрывают крышкой, перемешивают и оставляют при комнатной температуре и через 1 ч измеряют оптическую плотность образовавшейся вольфрамовой сини при длине волны 725 нм, длина оптического пути - 1 см. Суммарное содержание ФС выражают в мг-эквивалентах галловой кислоты на г сырой массы сырья. Использование изобретения позволяет разработать безопасный, экономически выгодный способ определения суммарного содержания ФС в растительных объектах с использованием стандартного оборудования для лабораторных исследований, без применения метанола, при сокращении времени экстракции. 3 табл., 2 пр.
Способ определения суммарного содержания фенольных соединений в растительных объектах, заключающийся в их измельчении, экстрагировании в спирте при перемешивании, последующим центрифугированием, добавлением к экстракту реактива Фолина-Чокальтеу и натрия углекислого, отличающийся тем, что измельчение пробы сырья массой 0,05 г производят с растиранием с 1,5 см3 96% этанола, экстрагирование фенольных соединений проводят в течение 45 мин при температуре 45°C с периодическим перемешиванием (каждые 15 мин) и последующим центрифугированием в течение 2-х минут при частоте вращения 16000 об/мин, из полученного экстракта отбирают пробы, объемом 0,075 см3, добавляют к ним по 0,075 см3 реактива Фолина-Чокальтеу, разбавленного в 5 раз, перемешивают, через 3 мин добавляют по 0,15 см3 20% раствора натрия углекислого и по 1,2 см3 дистиллированной воды, закрывают крышкой, перемешивают и оставляют при комнатной температуре и через 1 ч измеряют оптическую плотность образовавшейся вольфрамовой сини при длине волны 725 нм, длина оптического пути - 1 см, суммарное содержание фенольных соединений выражают в мг-эквивалентах галловой кислоты на г сырой массы сырья.
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИФЕНОЛОВ ЧАЯ | 2013 |
|
RU2519767C1 |
| УНИФИЦИРОВАННЫЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ В ТРАВЕ И ЭКСТРАКЦИОННЫХ ПРЕПАРАТАХ ОЧАНКИ | 2003 |
|
RU2266544C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| КАЗБЕКОВА А.Т | |||
| и др | |||
| Взаимосвязь между уровнем полифенолов и антиоксидантной активностью эфирных масел тимьяна, распространенного на территории Казахстана/ Фенольные соединения: фундаментальные и прикладные аспекты | |||
| Материалы Докладов VIII Международного Симпозиума, Москва, 2-5 октября 2012 года | |||
| ОЛЕЙНИЦ Е.Ю | |||
| и др | |||
| Фенольные соединения растительных чаев, их роль в определении антиоксидантной активности/ Фенольные соединения: свойства, активность, инновации | |||
| Cборник научных статей по материалам X Международного симпозиума "Фенольные соединения: фундаментальные и прикладные аспекты", М.: 2018, С | |||
| Ручной ткацкий станок | 1922 |
|
SU339A1 |
Авторы
Даты
2019-09-23—Публикация
2019-04-05—Подача