Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно, к флуоресцентной диагностике и фотодинамической терапии опухолевых тканей, и может применяться для определения индивидуальных энергетических параметров лазерного излучения при фотодинамической терапии тканей шейки матки.
Уровень техники
Несмотря на широкое применение фотодинамической терапии (ФДТ) в клинической практике, в настоящее время отсутствуют точные персонализированные методы оценки достаточности фотодинамического воздействия в зависимости от индивидуальных особенностей опухоли у каждого пациента. Оптимальные энергетические параметры лазерного излучения, такие как плотность энергии, плотность мощности и диаметр светового пятна варьируются от пациента к пациенту, поэтому стандартизированные протоколы лечения методами ФДТ могут вызывать недостаточный терапевтический эффект и ограничивать эффективность проводимой терапии [Wilson, В. С. (2002). Photodynamic therapy for cancer: principles. Canadian journal of gastroenterology, 76(6), 393-396.]. приводя в дальнейшем к рецидивам заболевания или вызывать поверхностные термические повреждения как опухолевой, так и нормальной ткани вследствие избыточной дозы энергии. Основной проблемой при оценке достаточности фотодинамического воздействия на опухолевую ткань является неравномерное фотообесцвечивание фотосенсибилизатора (ФС) по глубине в ткани. Динамика фотообесцвечивания зависит от длины волны, плотности энергии, плотности мощности, диаметра, пятна лазерного излучения: разновидности, размера и оптических параметров опухолевой ткани: типа и концентрации ФС, вводимого в организм пациента. Контроль фотообесцвечивания ФС по изменению интенсивности флуоресценции ФС в процессе лазерного облучения опухолевой ткани является хорошо изученным и легкодоступным дозиметрическим методом, позволяющим определять оптимальные энергетические параметры лазерного излучения, необходимые для обеспечения терапевтического эффекта по всей глубине инвазии опухолевой ткани [Jarvi, М. Т., М. S. Patterson and В. С. Wilson (2012) Insights into photodynamic therapy dosimetry: Simultaneous singlet oxygen luminescence and photosensitizer photobleaching measurements. Biophys. J. 102. 661-671.; Kim, M. M., J. C. Finlay and Т. C. Zhu (2015) Macroscopic singlet oxygen model incorporating photobleaching as an input parameter. Proc. SP1E Int. Soc. Opt. Eng. 9308, 93080v.: Finlay, J. C, S. Mitra and T. 11. Foster (2002) In vivo mTHPC photobleaching in normal rat skin exhibits unique irradiance-dependent features. Photochem. Photobiol. 75, 282- 288.; Finlay, J. C, S. Mitra, M. S. Patterson and T. 11. Foster (2004) Photobleaching kinetics of Photo frin in vivo and in multicell tumour spheroids indicate two simultaneous bleaching mechanisms. Phys. Med. Biol. 49. 4837- 4860.]. Наличие остаточных очагов накопления ФС, обусловленное недостаточной глубиной фотодинамического воздействия на опухолевую ткань, является наиболее существенной причиной рецидивов заболевания после лечения.
При планировании ФДТ важно также учитывать влияние диаметра пятна на плотность потока лазерного излучения в приповерхностном слое ткани на глубине 500 мкм относительно плотности потока падающего излучения [Marijnissen, J., & Star, W. M. (1987). Quantitative light dosimetry in vitro and in vivo. Lasers in Medical Science, 2(4), 235-242.; Star W. M. Light dosimetry in vivo //Physics in Medicine & Biology. - 1997. - T. 42. - №. 5. - C. 763.: Star, W. M. (1990). Light delivery and light dosimetry for photodynamic therapy. Lasers in Medical Science, 5(2), 107-113.; Star W. M., Wilson В. C, Patterson M. S. Light Delivery and Optical Dosimetry in //Photodynamic Therapy: Basic Principles and Clinical Applications. - 2020. - C. 335.]. Высокий коэффициент рассеяния биологической ткани является причиной распространения значительной доли излучения в обратном направлении и диффузного отражения от границы биоткань-воздух обратно в ткань, если угол падения света па границу биоткань-воздух больше критического угла, определяемого как arcsin(l/n) = 45° [Marijnissen, J.. & Star. W. M. (1987). Quantitative light dosimetry in vitro and in vivo. Lasers in Medical Science. 2(4), 235-242.]. Таким образом, фотоны в приповерхностном слое биологических тканей с высоким коэффициентом рассеяния задерживаются на более длительное время, чем в приповерхностном слое среды без рассеяния. При этом поток обратно рассеянного и диффузно отраженного в ткани излучения перекрывается с падающим потоком фотонов. При увеличении диаметра пятна увеличивается объем приповерхностного слоя ткани, подверженный облучению, и, соответственно, больше фотонов рассеивается от неоднородностей среды. Таким образом, энергия излучения, сосредоточенная в приповерхностном слое среды с высоким коэффициентом рассеяния, существенно увеличится с увеличением диаметра пятна падающего лазерного излучения, и большая часть этой энергии либо поглотится с выделением тепла, что может привести к поверхностному термическому повреждению биологической ткани, либо будет направлена на фотодинамический эффект. Способ определения оптимальных энергетических параметров лазерно-индуцированной фотодинамической терапии опухолевых тканей шейки матки посредством мониторинга фотообесцвечивания ФС и численного моделирования распространения лазерного излучения с различным диаметром пятна в биологической среде позволяет повысить эффективность фотодинамического воздействия за счет обеспечения терапевтического эффекта по всей глубине поражения без поверхностных термических повреждений.
Имеются методы определения оптимальных параметров фотодинамического воздействия на биологические ткани, аналогичные предлагаемому изобретению.
Авторы патента RU 672806 C1 предложили способ ФДТ с контролем эффективности в режиме реального времени. Для этого осуществляют доставку тетрапиррольного красителя тетра(арил)тетрацианопорфиразинового ряда к опухолевым клеткам. Далее проводят флуоресцентную визуализацию опухоли и определяют время жизни возбужденного состояния ФС по достижении максимального накопления в опухоли. Выполняют фотодинамическую деструкцию опухоли путем поэтапного облучения. Процедуру повторяют до увеличения времени жизни возбужденного состояния ФС в 1,5-2 раза относительно исходного уровня.
В патенте RU 2382660 C1 представлен способ флуоресцентной диагностики и ФДТ заболеваний кожи с использованием ФС группы порфиринов, с применением на участках, не обладающих интенсивной собственной флуоресценцией аппликатора, содержащего 5-аминолевулиновую кислоту для индуцирования накопления протопорфирина IX. Способ включает облучение пораженного участка кожи и прекращение облучения при уменьшении концентрации ФС. При этом облучение и диагностику осуществляют одновременно путем облучения импульсным световым излучением и непрерывной регистрации флуоресцентных изображений.
В патенте RU 2576823 C1 описан способ ФДТ центрального рака легкого с применением ФС хлоринового ряда и контроля ее эффективности. Бронхоскопически выявляют участки, обладающие интенсивной флуоресценцией, при их освещении светом в диапазоне 398-410 нм. Осуществляют фотодинамическую деструкцию выявленных участков излучением диодного лазера с длиной волны 660-665 нм и плотностью мощности около 100-200 мВт/см2. Оценивают уровень интенсивности флуоресцентного свечения красного цвета в промежутках между импульсами. При падении интенсивности флуоресценции в два раза относительно исходного уровня приостанавливают облучение обоими видами излучения на 3-5 минут до восстановления исходного уровня флуоресценции в красном диапазоне спектра, определяемого при освещении фиолетовым светом.
В патенте RU 2539367 C1 предложен способ ФДТ онкологических заболеваний, включающий введение ФС в зону опухолевой ткани и воздействие на нее лазерным излучением одновременно на двух длинах волн, обеспечивающих воздействие на ФС и оксигемоглобин, отличающийся тем, что дополнительно облучают ткань широкополосным излучением видимого и ближнего ИК диапазонов спектр и измеряют спектр диффузного отражения ткани, по которому определяются ее структурно-морфологические параметры, в том числе концентрация кровеносных сосудов и ФС в ткани, а также относительное содержание оксигемоглобина и метгемоглобина в крови.
В патенте CN 101522261 A предложен способ контроля и регулирования параметров внутритканевой ФДТ. Представлены вычислительные методы, которые используются для мониторинга и регулировки параметров облучения опухолевой ткани во время ФДТ. Также приводится описание метода, который используется для контроля процесса ФДТ, при котором общее время лечения определяется в соответствии с концентрацией ФС, интенсивностью излучения и степенью оксигенации ткани. Предложены способы дозиметрии при ФДТ опухолей в режиме реального времени.
Авторы патента WO 2008I37737 A3 предложили способ ФДТ с одновременным мониторингом дозы облучения. Спектроскопические измерения флуоресценции и отражения проводят через определенные промежутки времени во время ФДТ опухолевой ткани. Далее анализируются полученные спектры для определения дозиметрических показателей, таких как флуоресцентное фотообесцвечивание ФС, содержание кислорода в крови и оптические свойства обрабатываемой области.
В вышеперечисленных способах проведения ФДТ не учитывается влияние диаметра пятна излучения на плотность потока излучения в приповерхностном слое ткани относительно плотности потока падающего излучения, что может приводить к поверхностным термическим повреждениям биологической ткани. Кроме того, методы флуоресцентной диагностики, включенные в данные способы для контроля процесса фотодинамического воздействия, не учитывают эффективность фотообесцвечивания ФС по глубине с учетом плотности энергии и диаметра пятна облучения, что может приводить к недостаточному облучению опухолевой ткани по глубине и, в дальнейшем, к рецидивам заболевания. Поэтому для определения индивидуальных энергетических параметров при проведении фотодинамической терапии опухолевых тканей необходим предварительный мониторинг фотообесцвечивания ФС по глубине в опухолевой ткани и проведение численного моделирования распространения лазерного излучения с различным диаметром пятна в биологической среде с оптическими параметрами, характерными тканям шейки матки.
Ближайшим аналогом к предлагаемому изобретению (прототипом) является патент RU 2552032 C1, в котором описан способ ФДТ опухолей, заключающийся во введении ФС и воздействии низкоинтенсивным лазерным излучением. После проведения ФДТ проводят спектрально-флуоресцентную диагностику и определяют степень выгорания препарата. Если отношение опухоль/норма выше 1,0, диагностируют отсутствие выгорания. При соотношении опухоль/норма 0,8-1,0 диагностируют частичное выгорание. При соотношении опухоль/норма ниже 0,8 диагностируют полное выгорание. При регистрации полного выгорания процедура ФДТ завершается.
Метод спектрально-флуоресцентной диагностики не позволяет оценить фотообесцвечивание ФС по глубине в опухолевой ткани. Отношение опухоль/норма может варьироваться с увеличением глубины. Данный способ также не учитывает влияние диаметра пятна на фотообесцвечивание ФС по глубине и плотность потока излучения в приповерхностном слое ткани относительно плотности потока падающего излучения. При фотодинамическом воздействии на опухолевую ткань кроме исследования фотообесцвечивания ФС также необходимо мониторить степень оксигенации гемоглобина. Степень оксигенации гемоглобина имеет большое значение при проведении ФДТ, так как недостаток молекулярного кислорода в ткани может снизить ее эффективность. Молекула ФС при поглощении фотона вступает во взаимодействие с кислородом, присутствующим в ткани, с образованием высокоактивного синглетного кислорода [Agostinis P. et al. Photodynamic therapy of cancer: an update //CA: a cancer journal for clinicians. - 2011. - T. 61. - №. 4. - C. 250-281.].
Раскрытие сущности изобретения
Задачей предлагаемого изобретения является разработка неинвазивного способа определения оптимальных энергетических параметров лазерно-индуцированной фотодинамической терапии опухолевых тканей шейки матки, который позволит повысить эффективность фотодинамического воздействия за счет обеспечения терапевтического эффекта по всей глубине поражения без возникновения поверхностных термических повреждений.
Поставленная задача решается посредством мониторинга фотообесцвечивания ФС и степени оксигенации гемоглобина.
Задача также решается посредством проведения численного моделирования распространения лазерного излучения с различным диаметром пятна в среде с оптическими параметрами, характерными опухолевой ткани.
Осуществление метода
Определение оптимальных энергетических параметров лазерно-индуцированной фотодинамической терапии опухолевых тканей шейки матки осуществляется в два этапа. На первом этапе выполняется мониторинг фотообесцвечивания ФС и степени оксигенации гемоглобина на фантомах (оптических моделях), имитирующих оптические свойства опухолевых тканей шейки матки. Осуществляется подготовка фантомов на основе агарозы, жировой эмульсии 0,8% и цельной крови человека, содержащих равномерно распределенный ФС Фотодитазин. активным веществом которого является три натриевая соль Се6, в концентрации 1 мг/кг. Концентрация Се6 в фантоме определяется, исходя из средней концентрации ФС, наблюдаемой в биологических тканях пациентов с новообразованиями шейки матки в клинических условиях. Жировая эмульсия (Lipofundin MCT/LCT 10%™, В. Braun Melsungen AG. 36 Германия), содержащаяся в фантоме, используется для моделирования рассеивающих свойств тканей шейки матки [Di Ninni P. et al. Effect of dependent scattering on the optical properties of Intralipid tissue phantoms // Biomedical optics express. - 2011. - T. 2. - №. 8. - C. 2265-2278; Assadi H. et al. Optical scattering properties of intralipid phantom in presence of encapsulated microbubbles // International Journal of Photoenergy. - 2014. - T. 2014]. Для определения процентного содержание жировой эмульсии в фантоме, рассчитывается приведенный коэффициент рассеяния жировой эмульсин 10% на исследуемой длине волны 660 нм по формуле [Michels. R.. Foschum, F., & Kienle, A. (2008). Optical properties of fat emulsions. Optics express, 16(8), 5907-5925].

где 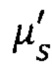 - приведенный коэффициент рассеяния; λ - длина волны лазерного излучения; у0 = 49,57; а = -0,09; b = 0,00005.
- приведенный коэффициент рассеяния; λ - длина волны лазерного излучения; у0 = 49,57; а = -0,09; b = 0,00005.
На длине волны 660 нм приведенный коэффициент рассеяния интралипида 10% составляет 100 см-1. Для расчета процентного содержания интралипида в фантоме используется приведенный коэффициент рассеяния тканей шейки матки  на длине волны 660 нм [Liu Q., Ramanujam N. Sequential estimation of optical properties of a two-layered epithelial tissue model from depth-resolved ultraviolet-visible diffuse reflectance spectra //Applied optics. - 2006. -T. 45. - №. 19. - C. 4776-4790]. По расчетам, доля интралипида в фантоме, исходя из общей доли интралипида составляет 0,8%.
на длине волны 660 нм [Liu Q., Ramanujam N. Sequential estimation of optical properties of a two-layered epithelial tissue model from depth-resolved ultraviolet-visible diffuse reflectance spectra //Applied optics. - 2006. -T. 45. - №. 19. - C. 4776-4790]. По расчетам, доля интралипида в фантоме, исходя из общей доли интралипида составляет 0,8%.
Цельная кровь человека вводится в фантом с целью имитации поглощающих свойств биологической ткани, так как в ней основным поглотителем света в видимом диапазоне спектра является гемоглобин [Zonios, G., Bykowski, J., & Kollias, N. (2001). Skin melanin, hemoglobin, and light scattering properties can be quantitatively assessed in vivo using diffuse reflectance spectroscopy. Journal of Investigative Dermatology, 117(6), 1452-1457]. Доля цельной крови в фантоме рассчитывается, исходя из коэффициента поглощения оксигенированного гемоглобина в цельной крови [Prahl, S. (1999). Optical absorption of hemoglobin. http://omlc.ogi.edu/spectra/hemoglobin] и коэффициента поглощения ткани шейки матки μа= 2,24 см-1 на длине волны 660 нм. По расчетам, доля цельной крови в фантоме составляет 7%. Агароза фиксирует компоненты раствора в неподвижном состоянии.
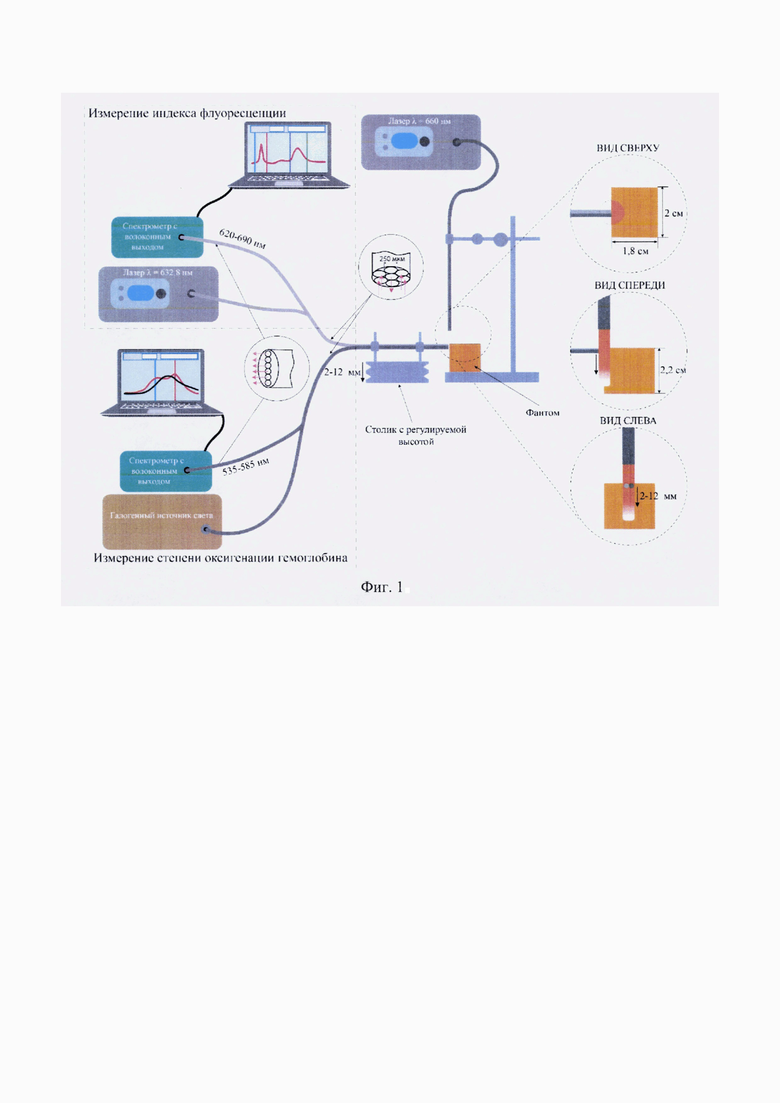
Подготовленный фантом размещается на лабораторном столике, оснащенном системой регулировки высоты подъема, который позволяет преобразовать вращение приводного винта в вертикальное перемещение плоскости столика (Фиг. 1).
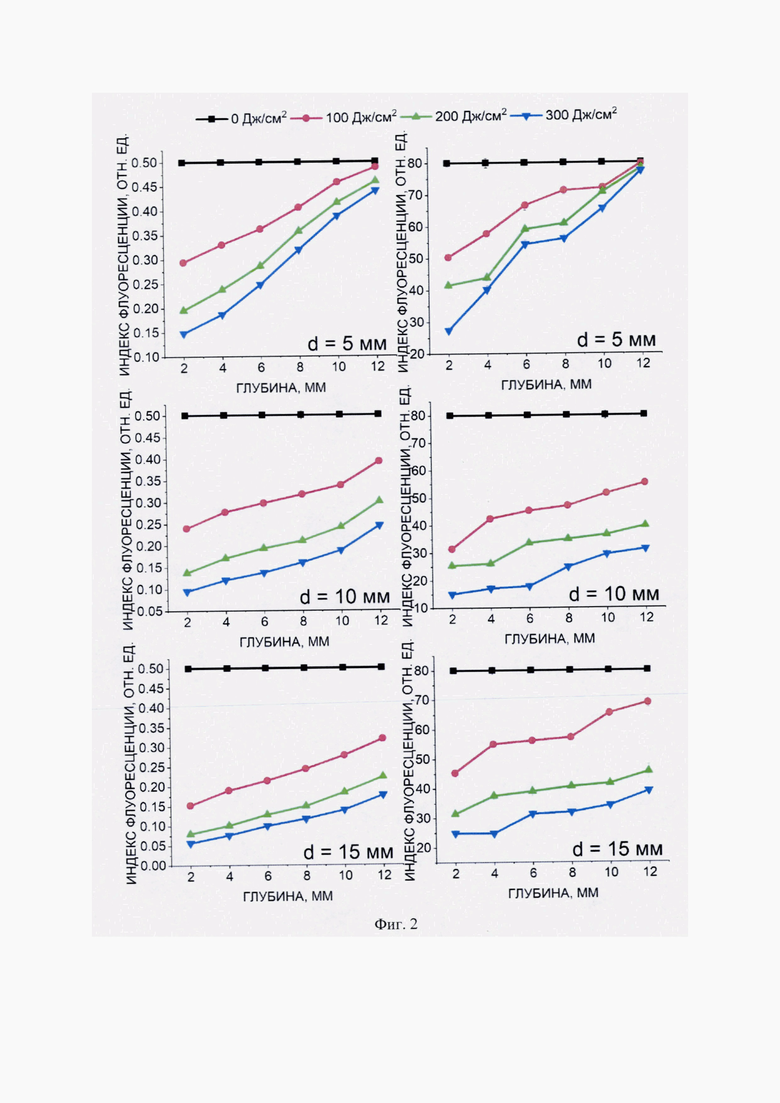
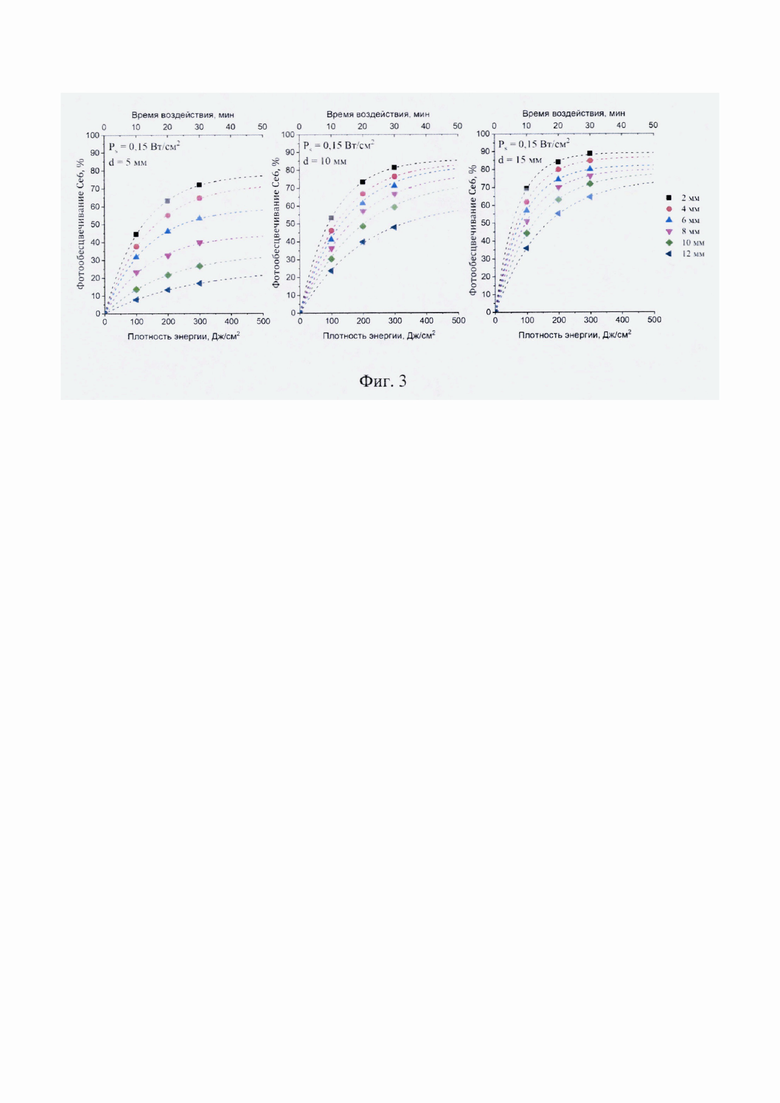
Столик с фантомом в процессе экспериментального исследования опускается вниз с шагом 2 мм на глубину 12 мм. К верхней поверхности фантома подводится оптическое волокно, обеспечивающее доставку излучения от терапевтического лазера с длиной волны 660 нм и мощностью лазерного излучения 0,03; 0,12 и 0.3 Вт при диаметре пятна 5 мм; 10 мм и 15 мм (Ps = 0,15 Вт/см2). Оптическое волокно закрепляется с помощью держателя на лабораторном штативе с возможностью регулировки размера пятна лазерного излучения. К боковой поверхности фантома подводится два дистальных конца диагностических Y-образных оптических волокон, состоящих из одного центрального волокна для доставки излучения к поверхности фантома и шести приемных с диаметром каждого волокна в оболочке 200 мкм и числовой апертурой 0,22, закрепленных посредством специального держателя, расположенного на дополнительном лабораторном подъемном столике. Один из дистальных концов оптических волокон применяется для доставки излучения от гелий-неонового лазера с длиной волны 632,8 нм для возбуждения флуоресценции ФС и регистрации обратно рассеянного лазерного излучения и флуоресценции ФС, второе - от вольфрамового галогенного источника излучения для доставки света к поверхности образца и измерения спектров диффузного отражения с целью определения оксигенации гемоглобина в образце. Измерение спектров обратно рассеянного лазерного излучения и флуоресценции Се6, а также спектров диффузного отражения в образце осуществляется до и после ФДТ с помощью двух спектрометров в каждой позиции оптического волокна вдоль фантома по глубине от 2 до 12 мм. Регистрация спектров обратно рассеянного лазерного излучения до и после ФДТ осуществляют с экспозицией 100 мс в диапазоне длин волн 625-641 нм, спектров флуоресценции - в диапазоне 665-690 нм. Индекс флуоресценции ФС рассчитывают как отношение площади под спектром флуоресценции к площади под спектром обратно рассеянного лазерного излучения. Спектры диффузного отражения регистрируют в диапазоне 500-600 нм, что позволяет количественно оценить оксигенацию гемоглобина в образце. Спектры диффузного отражения регистрируют относительно стандартного образца (BaSO4) с коэффициентом диффузного отражения, близким к единице. По спектрам диффузного отражения программно рассчитывают степень оксигенации гемоглобина в образце. Во время всех измерений торцы оптоволоконных зондов находятся в мягком контакте с образцом. В результате исследования оценивают распределения индексов флуоресценции ФС и степени оксигенации гемоглобина по глубине в модели ткани шейки матки до и после ФДТ при различной плотности энергии и диаметре пятна лазерного излучения (Фиг. 2). Исходя из полученных индексов флуоресценции ФС рассчитывают значения фотообесцвечивания Се6 (Фиг. 3). Данные результаты позволяют с достаточной точностью определять параметры лазерного излучения для облучения ткани шейки матки по всей глубине поражения, которая при дисплазиях и раке шейки матки, исходя из гистологической оценки, варьируется от 1 до 2 мм [Протасова А. Э. и др. Дисплазия шейки матки -этиопатогенез, диагностика, оптимальная тактика лечения // Учебное пособие. СПб.: МЗ РФ ФГБУ «ФМИЦ им. В. А. Алмазова» кафедра акушерства и гинекологии, СЗГМУ им. И. И. Мечникова кафедра онкологии. - 2014].
На втором этапе проводят численное моделирование распространения лазерного излучения с различной плотностью энергии и диаметром пятна в ткани шейки матки. В качестве начальных условий задают оптические параметры ткани шейки матки μа = 0,22 мм-1, μ's = 0,78 мм-1, g = 0,80, n = 1,40 [Liu Q., Ramanujam N. Sequential estimation of optical properties of a two-layered epithelial tissue model from depth-resolved ultraviolet-visible diffuse reflectance spectra //Applied optics. - 2006. - T. 45. - №. 19. - C. 4776-4790].
Пакеты фотонов распространяются через среду толщиной 12 мм. Диаметр пятна составляет 0.2; 1; 2,5: 5; 10 и 15 мм. В среду запускается 109 пакетов по 1000 фотонов в пакете. Чтобы учесть постоянство плотности мощности все полученные значения пропускания, поглощения и отражения, как и числа входящих фотонов, масштабируют. Полученные количественные распределения поглощенных фотонов по глубине для каждого диаметра пятна приводятся к величине относительной плотности потока энергии излучения по следующей формуле:

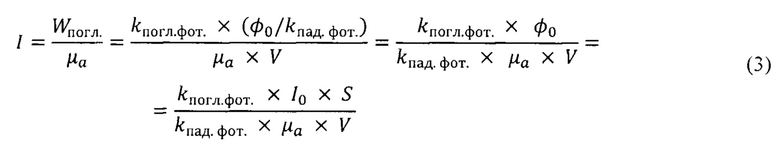
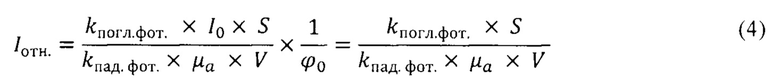
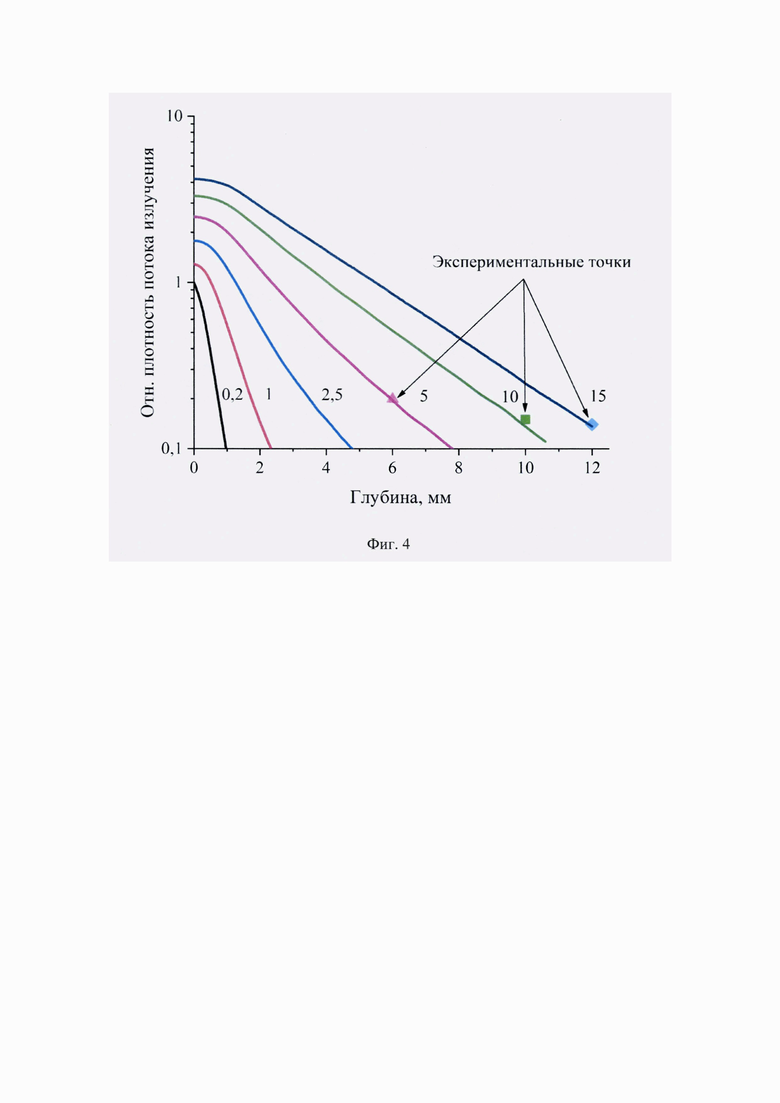
где Iотн - относительная плотность потока излучения; I - плотность потока излучения в среде [Вт/см2]; I0 - плотность потока падающего излучения [Вт/см2]; Wпогл. - объемная плотность поглощенного потока энергии [Вт/см3]; V - единичный объем; kпогл.фот. - количество поглощенных фотонов в единичном объеме, определяемом расчетной сеткой; φ0 - поток энергии падающего излучения [Вт]; kпад.фот - количество падающих фотонов; S - площадь лазерного пятна. Зависимость относительной плотности потока лазерного излучения от глубины проникновения в модели ткани шейки матки при различном диаметре пятна (Фиг. 4) позволяет прогнозировать процесс фотодинамического воздействия без возникновения поверхностных термических повреждений тканей.
Исходя из совокупности полученных результатов и учитывая глубину поражения ткани шейки матки, установленную посредством гистологического исследования, формулируются оптимальные энергетические параметры лазерного излучения (диаметр пятна и плотность энергии) для фотодинамической терапии дисплазии и рака шейки матки, при которых фотообесцвечивание ФС достигает 70% от первоначального значения [Jarvi М. Т. et al. Insights into photodynamic therapy dosimetry: simultaneous singlet oxygen luminescence and photosensitizer photobleaching measurements //Biophysical journal. - 2012. -T. 102. №. 3. C. 661-671]. До начала ФДТ с установленными энергетическими параметрами пациенту внутривенно капельно вводится фотосенсибилизатор Фотодитазин в концентрации 1 мг/кг в течении 30 мин в затемненном помещении. Пациент проходит инструктаж о необходимости строгого соблюдения светового режима (исключение воздействия прямого солнечного света и т.д.). Время экспозиции фотосенсибилизатора составляет 3 часа. Непосредственно перед проведением ФДТ шейку матки пациента разбивают на несколько небольших исследуемых зон. В каждой зоне проводят видеофлуоресцентную диагностику для визуализации очагов поражения шейки матки и спектрально-флуоресцентную диагностика для уточнения их границ. Оценивают индексы флуоресценции ФС в каждой зоне. Далее каждую зону облучают лазерным излучением с установленными энергетическими параметрами. После ФДТ повторно проводят видео- и спектрально-флуоресцентную диагностику исследуемых зон шейки матки для оценки степени фотообесцвечивания ФС. Через 3 месяца после ФДТ проводят гистологическую оценку тканей шейки матки.
Краткое описание чертежей
Изобретение иллюстрируется следующими рисунками.
Па Фиг. 1 приведена схема экспериментальной установки для исследования глубины фотодинамического воздействия на опухолевые ткани шейки матки
На Фиг. 2 представлены распределения индексов флуоресценции ФС (средняя ошибка-0.03%) и степени оксигенации гемоглобина (средняя ошибка - 0.90%) по глубине в модели ткани шейки матки при фотодинамическом воздействии с различной плотностью энергии и диаметром пятна.
На Фиг. 3 приведена зависимость фотообесцвечивания Се6 на различной глубине в моделях биологических тканей от плотности энергии и времени воздействия лазерного излучения с различным диаметром пятна.
На Фиг. 4 приведена зависимость относительной плотности потока излучения от глубины проникновения в модели ткани шейки матки при различном диаметре пятна.
Полученные оптимальные энергетические параметры лазерно-индуцированиого фотодинамического воздействия были апробированы на пациентах с дисплазией и раком шейки матки. Предлагаемое изобретение иллюстрируется нижеприведенными примерами. Пример 1
Пациент А., 22 года с дисплазией шейки матки тяжелой степени. Обнаружен вирус папилломы человека 16 и 6 типа по результатам ПЦР-диагностики. Исследование было проведено в Университетской клинической больнице №1 Первого МГМУ им. И.М. Сеченова. Институте кластерной онкологии им. Л.Л. Левшина. Пациенту был внутривенно введен Фотодитазин в концентрации 1 мг/кг. Глубина поражения по данным гистологического исследования составляла 2 мм. Посредством предложенного способа были определены оптимальные параметры ФДТ. Шейка матки пациента разбивалась на четыре исследуемые зоны, каждая из которых облучалась лазерным излучением с диаметром пятна 10 мм. Плотность энергии при ФДТ составляла 200 Дж/см2, плотность мощности - 0.15 Вт/см2 (Фиг. 3). Эффективность ФДТ оценивалась посредством проведения видео- и спектрально-флуоресцентной диагностики. По результатам видео-флуоресцентной диагностики до ФДТ индекс флуоресценции в области опухолевой ткани составил 34 отн.ед., а нормальной ткани - 9 отн.ед. После ФДТ индекс снизился до 10 отн.ед. Фотообеецвечивание ФС по результатам видео-флуоресцентной диагностики составило 74%. В результате спектральной диагностики с возбуждением флуоресценции ФС гелий-неоновым лазером с длиной волны 632,8 нм получены спектры флуоресценции и обратно рассеянного лазерного излучения. Индекс флуоресценции опухолевой ткани шейки матки до ФДТ составлял 9.1 отн.ед.. а нормальной ткани - 2,5 отн.ед. После ФДТ, вследствие фотообесцвечивания ФС, индекс флуоресценции ФС составил 2.5 отн.ед. Фотообесцвечивание ФС по результатам спектрально-флуоресцентной диагностики составило 72%. По результатам морфологического исследования материала биопсии шейки матки, взятого у пациента через 3 месяца после ФДТ. не наблюдалось признаков дисплазии шейки матки тяжелой степени и ранее выявленных типов вируса папилломы человека. Пример 2
Пациент Б.. 54 года с преинвазивным раком шейки матки. Обнаружены вирусы папилломы человека 16 типа по результатам ПЦР-диагностики. Исследование было проведено в Университетской клинической больнице №1 Первого МГМУ им. И.М. Сеченова. Институте кластерной онкологии им. Л.Л. Левшина. Пациенту был внутривенно введен Фотодитазин в концентрации 1 мг/кг. Глубина поражения по данным гистологического исследования составляла 4 мм. Посредством предложенного способа были определены оптимальные параметры ФДТ. Шейка матки пациента разбивалась на четыре исследуемые зоны, каждая из которых облучалась лазерным излучением с диаметром пятна 10 мм. Плотность энергии при ФДТ' составляла 250 Дж/см2, плотность мощности - 0.15 Вт/см2 (Фиг. 3). Эффективность ФДТ оценивалась посредством проведения видео- и спектрально-флуоресцентной диагностики. По результатам видеофлуоресцентной диагностики до ФДТ индекс флуоресценции в области опухолевой ткани составил 39 отн.ед., а нормальной ткани - 10 отн.ед. После ФДТ индекс снизился до 10 отн.ед. Фотообесцвечивание ФС по результатам видео-флуоресцентной диагностики составило 74%. В результате спектральной диаг ностики с возбуждением флуоресценции ФС гелий-неоновым лазером с длиной волны 632,8 нм полу чены спектры флуоресценции и обратно рассеянного лазерного излучения. Индекс флуоресценции ФС в опухолевой ткани шейки матки до ФДТ составлял 9,4 отн.ед., а нормальной ткани - 2.5 отн.ед. После ФДТ, вследствие фотообесцвечивания ФС, индекс флуоресценции ФС составил 2.4 отн.ед. Фотообесцвечивание ФС по результатам спектрально-флуоресцентной диагностики составило 74%. По результатам морфологического исследования материала биопсии шейки матки, взятого у пациента через 3 месяца после ФДТ, не наблюдалось признаков преинвазивного рака шейки матки и ранее выявленных типов вируса папилломы человека.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ НОВООБРАЗОВАНИЙ ШЕЙКИ МАТКИ И ВУЛЬВЫ ПОД КОНТРОЛЕМ СОВМЕСТНОЙ ВИДЕО- И СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ ХЛОРИНОВОГО РЯДА | 2021 |
|
RU2782643C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОПУХОЛЕЙ | 2012 |
|
RU2519936C2 |
| УСТРОЙСТВО ДЛЯ СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ СОСТОЯНИЯ БИОЛОГИЧЕСКИХ ТКАНЕЙ В ПРОЦЕССЕ ФОТОДИНАМИЧЕСКОГО ВОЗДЕЙСТВИЯ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРОВ НА ОСНОВЕ ХЛОРИНА E6 | 2022 |
|
RU2807133C1 |
| УСТРОЙСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РЕЗИДУАЛЬНЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА С ФЛУОРЕСЦЕНТНЫМ КОНТРОЛЕМ ФОТООБЕСЦВЕЧИВАНИЯ ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2801893C2 |
| Способ лечения фоновых и предраковых заболеваний шейки матки | 2023 |
|
RU2813949C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБИННЫХ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА, РАСПОЛОЖЕННЫХ ВБЛИЗИ КОРТИКОСПИНАЛЬНОГО И КОРТИКОБУЛЬБАРНОГО ТРАКТОВ, С ПРИМЕНЕНИЕМ СТЕРЕОТАКСИЧЕСКОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПОД СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНЫМ И НЕЙРОФИЗИОЛОГИЧЕСКИМ МОНИТОРИНГОМ | 2023 |
|
RU2830942C1 |
| Способ фотодинамической диагностики и терапии центрального рака легкого и устройство его осуществления | 2019 |
|
RU2736909C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА И ТКАНЕЙ ПАРОДОНТА МЕТОДОМ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ПРИМЕНЕНИЕМ ФОТОСЕНСИБИЛИЗАТОРА НА ОСНОВЕ ЛИПОСОМ С КУРКУМИНОМ | 2023 |
|
RU2827761C1 |
| УСТРОЙСТВО ДЛЯ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ВОЗМОЖНОСТЬЮ ОДНОВРЕМЕННОГО СПЕКТРАЛЬНО-ФЛУОРЕСЦЕНТНОГО КОНТРОЛЯ ФОТОБЛИЧИНГА ФОТОСЕНСИБИЛИЗАТОРА | 2021 |
|
RU2777486C1 |
| ПРЕПАРАТ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ РАКА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2012 |
|
RU2521327C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано при лазерно-индуцированной фотодинамической терапии дисплазии и рака шейки матки. Осуществляют внутривенное введение фотосенсибилизатора на основе хлорина е6 в концентрации 1 мг/кг, затем воздействуют на зону поражения лазерным излучением с длиной волны 660 нм, диаметром пятна 10-15 мм, плотностью мощности 0,15 Вт/см2, плотностью энергии 200-250 Дж/см2. Облучение проводят до фотообесцвечивания фотосенсебилизатора более 70% по всей глубине поражения. Способ позволяет повысить эффективность фотодинамической терапии опухолевых тканей шейки матки, минимизировать побочные эффекты и предотвратить рецидивы заболевания за счет обеспечения терапевтического эффекта по всей глубине поражения без поверхностных термических повреждений. 4 ил., 2 пр.
Способ фотодинамической терапии дисплазии и рака шейки матки, включающий введение фотосенсебилизатора и воздействие лазерным излучением, отличающийся тем, что осуществляют внутривенное введение фотосенсибилизатора на основе хлорина е6 в концентрации 1 мг/кг, воздействуют на зону поражения лазерным излучением с длиной волны 660 нм, диаметром пятна 10-15 мм, плотностью мощности 0,15 Вт/см2, плотностью энергии 200-250 Дж/см2, облучение проводят до фотообесцвечивания фотосенсебилизатора более 70% по всей глубине поражения.
| СПОСОБ ОПРЕДЕЛЕНИЯ ОПТИМАЛЬНЫХ РЕЖИМОВ ФЛУОРЕСЦЕНТНОЙ ДИАГНОСТИКИ И ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2008 |
|
RU2376044C1 |
| МОДЕЛИРОВАНИЕ ДЕЙСТВИЯ ОПТИЧЕСКОГО ВОЛОКНА ПРИ ЛЕЧЕНИИ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИЕЙ И СОДЕЙСТВИЕ ПЛАНИРОВАНИЮ ТАКОГО ЛЕЧЕНИЯ | 2011 |
|
RU2632512C2 |
| АМИНОДОВА И.П | |||
| и др | |||
| Оптимизация параметров лечения при фотодинамичекой терапии предрака и рака шейки матки | |||
| Фотодинамическая терапия и фотодиагностика | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| ХАЧАТУРЯН А.Р | |||
| и др | |||
| Флуоресцентный контроль фотодинамической терапии доброкачественных вирус-ассоциированных | |||
Авторы
Даты
2024-03-12—Публикация
2023-02-22—Подача