Изобретение относится к ветеринарной травматологии и ортопедии, применяемое для прагматизации репаративного остеогенеза у животных при дегенеративно-дистрофических нарушениях костной системы, псевдоартрозах, замедленной консолидации, бактериальной инфекции, а также при нарушении анатомической целостности костей.
Предложенный способ характеризует использование биокомпозиционного покрытия на накостных и внутрикостных (интрамедуллярных) имплантатах, в частности, зону нарушения анатомической целостности костей или дегенеративно-дистрофических нарушений.
Изобретение сокращает время на консолидацию и стабилизацию репаративного остеогенеза при осложнениях благодаря наличию остеокондуктивного, остеоиндуктивного потенциала, биосовместимости, полной биоинтеграции и антибактериального действия покрытия.
В гуманной медицине известен способ активации репаративного остеогенеза (RU 2601858 C1, МПК А61В 17/56, опубл. 10.11.2016). Предложенный способ осуществляется за счет установки аппарата внешней фиксации, имеющий полый стержень-шуруп, фиксирующийся в кронштейне. Упомянутый полый стержень-шуруп вводят на расстоянии 20-40 мм от места перелома в проксимальный и дистальный отломки. Вводят через полость стержня ультразвуковой волновод-инструмент так, чтобы он выступал за внутренний край упомянутого полого стержня-шурупа на 3-15 мм. Осуществляют озвучивание области повреждения низкочастотными ультразвуковыми колебаниями с одновременной подачей в область воздействия лекарственного раствора. Осуществляется озвучивание области повреждения низкочастотными ультразвуковыми колебаниями с параметрами 26-42 кГц и амплитудой от 15 мкм до 30 мкм продолжительностью воздействия от 2 до 15 мин с одновременной подачей в область воздействия лечебного лекарственного раствора (Лавасепт). Данный способ имеет следующие недостатки:
1) Дополнительная ятрогенная травматизация мягких тканей при установке дополнительного стержня - шурупа
2) Отсутствие антибактериального действия.
3) Необходимо использование специализированного оборудования - аппарат Ярус-М, для которого был разработан специализированный излучатель и специальный волновод-инструмент.
Также известен способ сочетанной стимуляции репаративного остеогенеза у животных (RU 2469679 C1, МПК A61D 99/00, опубл. 20.12.2012). Данный способ определен чрескостным остеосинтезом и лазерной остеоперфорацией. Однократную остеоперфорацию выполняют в течение 3-10 сек в очаге перелома в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома. Используют инфракрасный оптоволоконный лазер в импульсно-периодическом режиме 100x50, с длиной волны 1560 нм, развивающий мощность 25-40 Вт. При этом доставку энергии осуществляют чрескожно, контактным путем, через кварцевый световод диаметром 0,4 мм. При этом формируют сквозные перфорационные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях.
Данный способ имеет следующие недостатки:
1) Использование инфракрасного излучения создает перегрев мягких тканей оперируемой зоны.
2) Дополнительная травматизация костной ткани в пяти дополнительных точках с повышенным риском развития хирургической инфекции.
В гуманной медицине известен способ оптимизации репаративного остеогенеза (RU 2738406 C1, МПК А61К 31/10, А61К 31/728, А61Р 19/00 опубл. 11.12.2016). Способ осуществляется следующим образом. Готовят стерильный биоантиоксидантный раствор тиофана путем разведения 10 мг тиофана в предварительно подогретом до 38°С 2% растворе гиалуроновой кислоты, иммобилизованной на Полисорбе МП из расчета 10 мг тиофана на 20 мл 2% гиалуроновой кислоты и 10 мг Полисорба МП. Полученный раствор в дозе 0,05 мг/кг веса шприцем вводят однократно в верхнечелюстной синус во время операции субантральной аугментации после размещения на дне синуса биоматериала (ауто- аллогенная кость, препараты на основе гидроксида кальция, пористый титан).
Данный способ имеет следующие недостатки:
1) Используется только при конкретизированном хирургическом случае, в частности стоматологии и челюстно-лицевой хирургии, с отсутствием возможности применения при хирургических вмешательствах на трубчатых костях.
2) Отсутствие антибактериального действия.
Технической задачей является разработка способа прагматизации репаративного остеогенеза трубчатых костей животных с помощью биокомпозиционного покрытия на известные накостные и внутрикостные имплантаты.
Техническая задача решается тем, что для прагматизации репаративного остеогенеза, необходимо применение остеокондуктивного и остеоиндуктивного покрытия на основе гидроксиапатита, метилурацила, амоксициллина, полилактида на применяемые накостные или внутрикостные имплантаты. При этом данное покрытие получаем растворением в 50 мл хлороформа, при температуре окружающей среды в 22°С при непрерывном перемешивании, например, на магнитной мешалке, 1 гр. полилактида до образования густой суспензии прозрачного цвета. После полного растворения полилактида добавляют последовательно при непрерывном перемешивании метилурацил, гидроксиапатит и амоксициллин по 400 мг каждого компонента каждые 20 минут 5 раз. На выходе получаем молочного цвета суспензию. Стерильные хирургические импланты (спицы, штифты, винты, остеофиксаторы, накостные пластины) опускаем в полученный раствор 5 раз, по 10 секунд каждый, с интервалом в 2 минуты. Образуется тонкая пленка 1-1,5 мм, после, устанавливаем импланты с нанесенным слоем в штатив и проводим однократно лиофильную сушку при температуре 3-5°С при давлении 5⋅10-1Па в течение 30 минут. Последующая предоперационная стерилизация имплантов автоклавированием или в сухожаровом шкафу согласно инструкции.
Техническим результатом заявленного изобретения является разработка способа прагматизации репаративного остеогенеза у животных, обеспечивающего эффект при однократном применении, который можно использовать для уменьшения времени консолидирования вяло срастающихся переломов, хирургического лечения ложных суставов, профилактирование бактериальной обсемененности, благодаря высвобождению действующих компонентов непосредственно в местах приложения.
Заявленное изобретение иллюстрируется следующими фигурами.
На фиг.1 представлен общий вид (фотография) биокомпозитного остеопластического покрытия, нанесенного на имплантат (спица).
На фиг.2 представлена рентгенограмма посттравматического псевдоартроза средней трети диафиза лучевой кости с обширной остеодеструкцией дорзо-вентральной (прямая) проекции (пример 1).
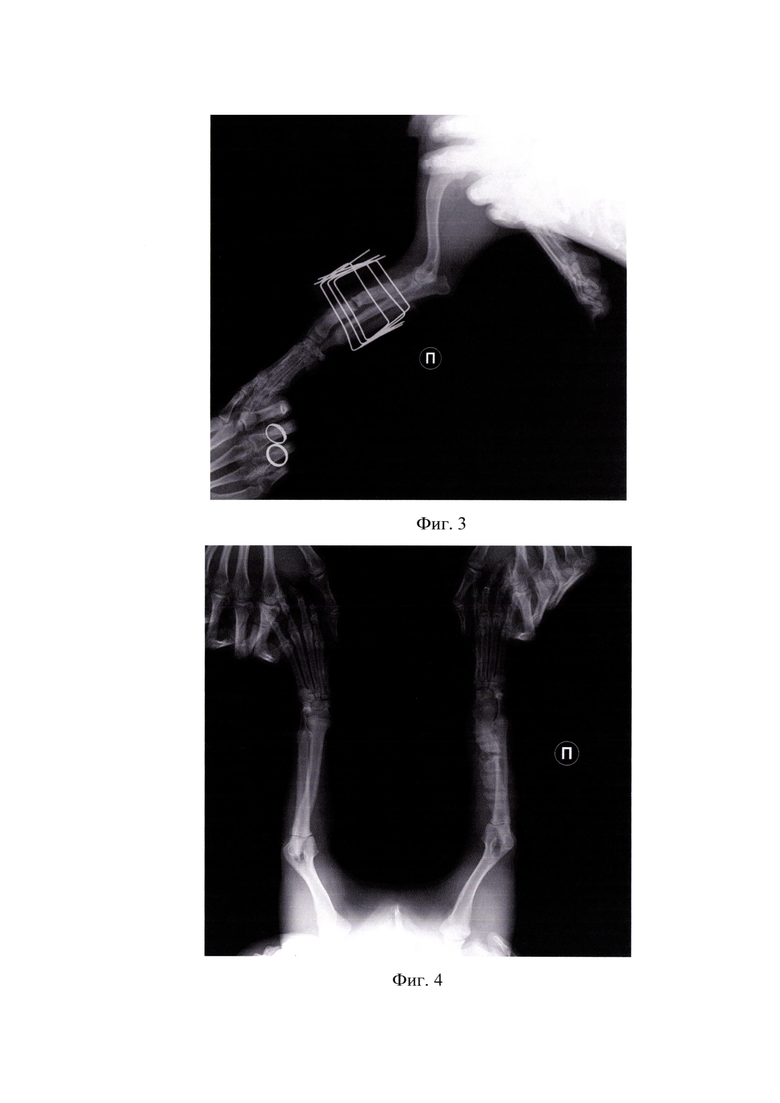
На фиг.3 представлена рентгенограмма посттравматического псевдоартроза средней трети диафиза лучевой кости с обширной остеодеструкцией в латеро-медиальной (боковая) проекции (пример 1).
На фиг.4 представлена рентгенограмма псевдоартроза сразу после снятия внеочагового аппарата в дорзо-вентральной проекции (пример 1).
На фиг.5 представлена рентгенограмма псевдоартроза сразу после снятия внеочагового аппарата в латеро-медиальной проекции (пример 1).
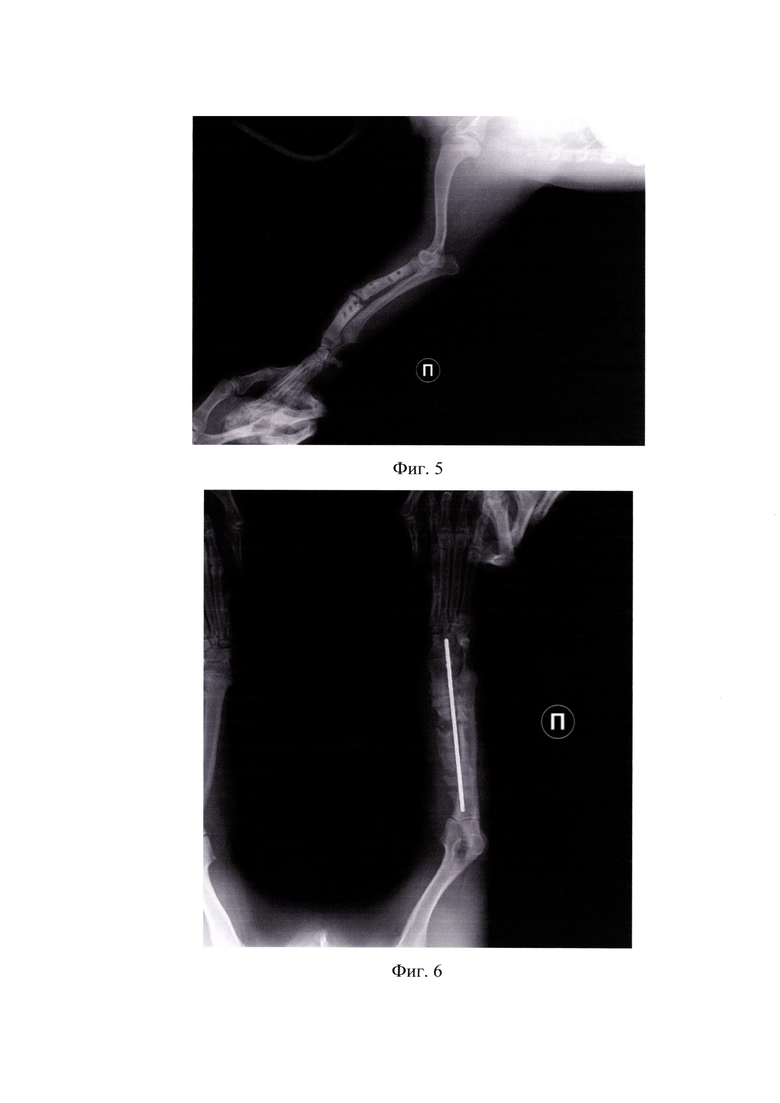
На фиг.6 представлена рентгенограмма сразу после проведения интрамедуллярного остеосинтеза имплантатом с биокомпозиционным покрытием в дорзо-вентральной проекции (пример 1).
На фиг.7 представлена рентгенограмма сразу после проведения интрамедуллярного остеосинтеза имплантатом с биокомпозиционным покрытием в латеро-медиальной проекции (пример 1).
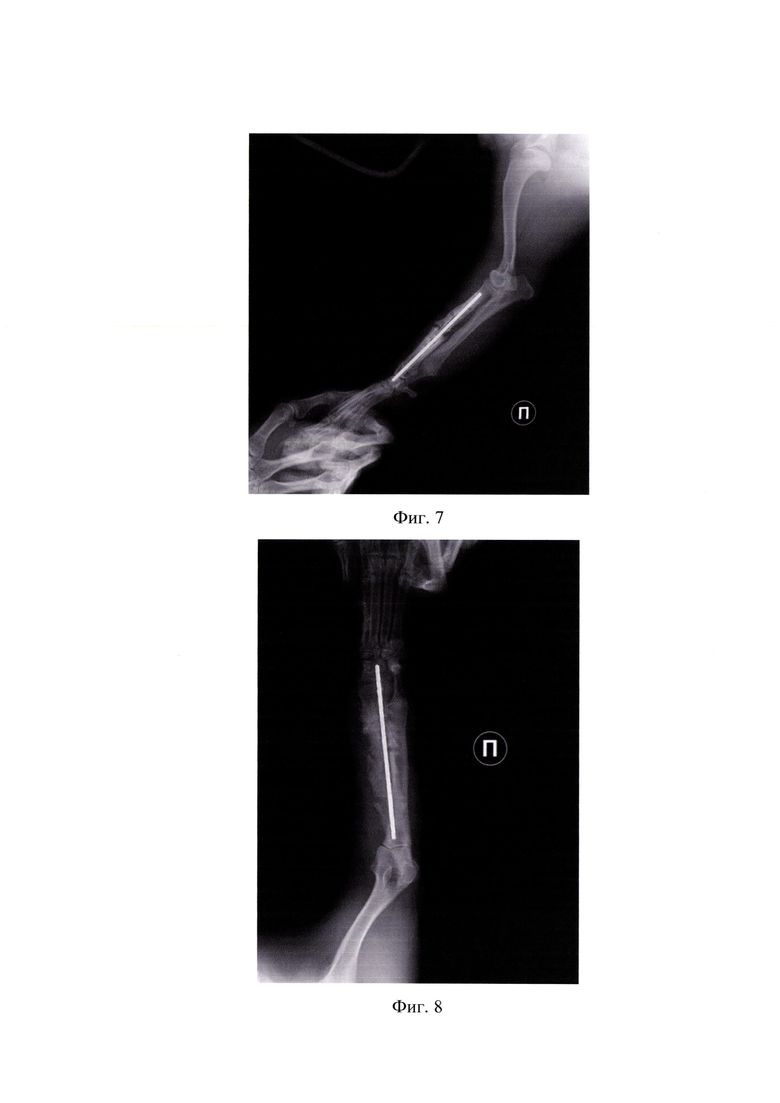
На фиг.8 представлена рентгенограмма спустя 20 дней в дорзо-вентральной проекции (пример 1).
На фиг.9 представлена рентгенограмма спустя 20 дней в латеро-медиальной проекции (пример 1).
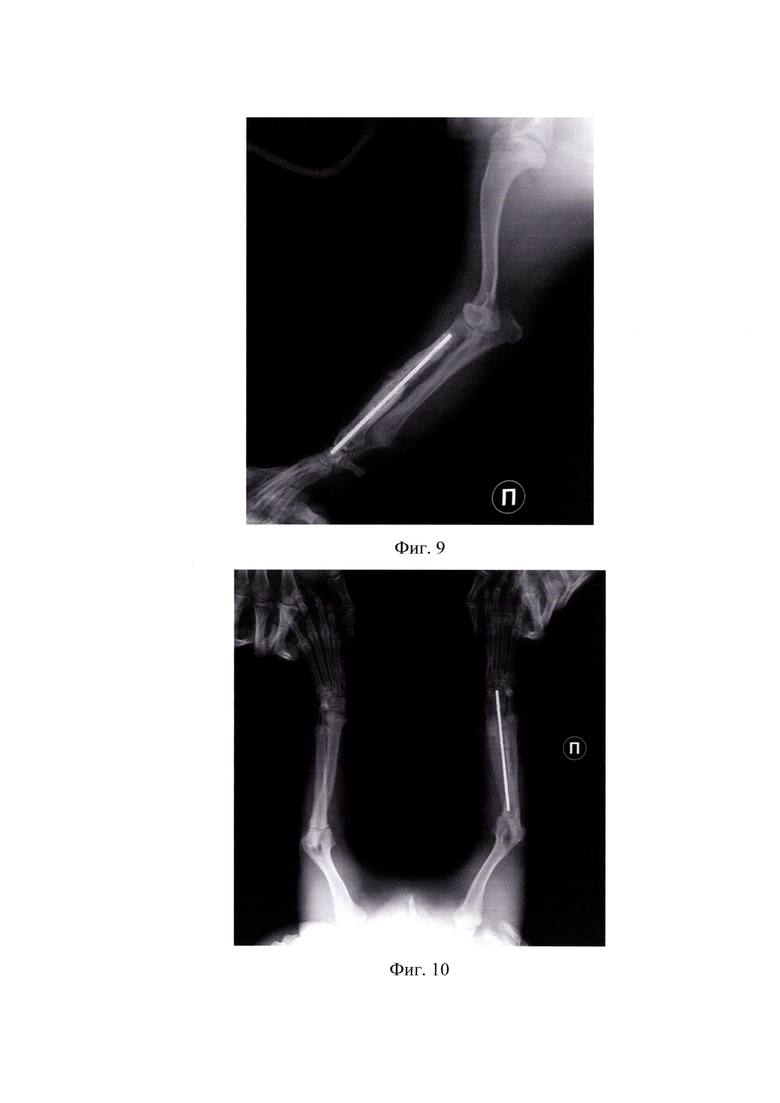
На фиг.10 представлена рентгенограмма спустя 73 дня в дорзо-вентральной проекции (пример 1).
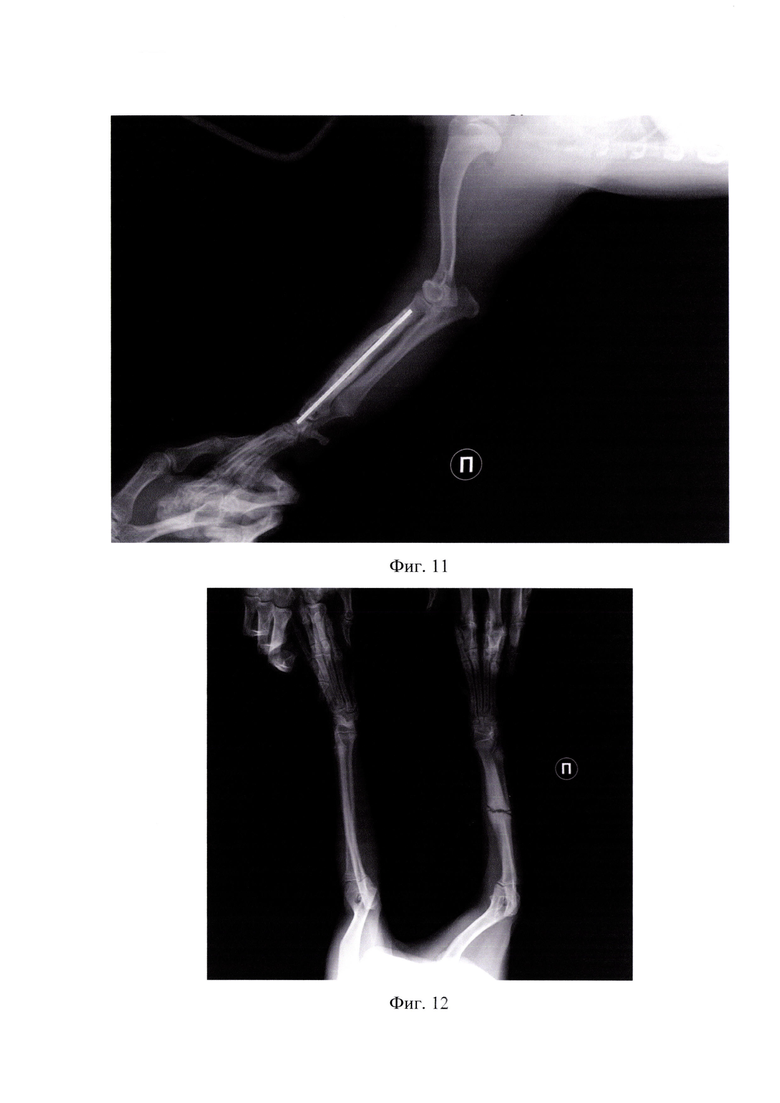
На фиг.11 представлена рентгенограмма спустя 73 дня в латеро-медиальной проекции (пример 1).
На фиг.12 представлена рентгенограмма псевдоартроза средней трети диафиза лучевой кости правой грудной конечности в дорзо-вентральной проекции (пример 2).
На фиг.13 представлена рентгенограмма псевдоартроза средней трети диафиза лучевой кости правой грудной конечности в латеро-медиальной проекции (пример 2).
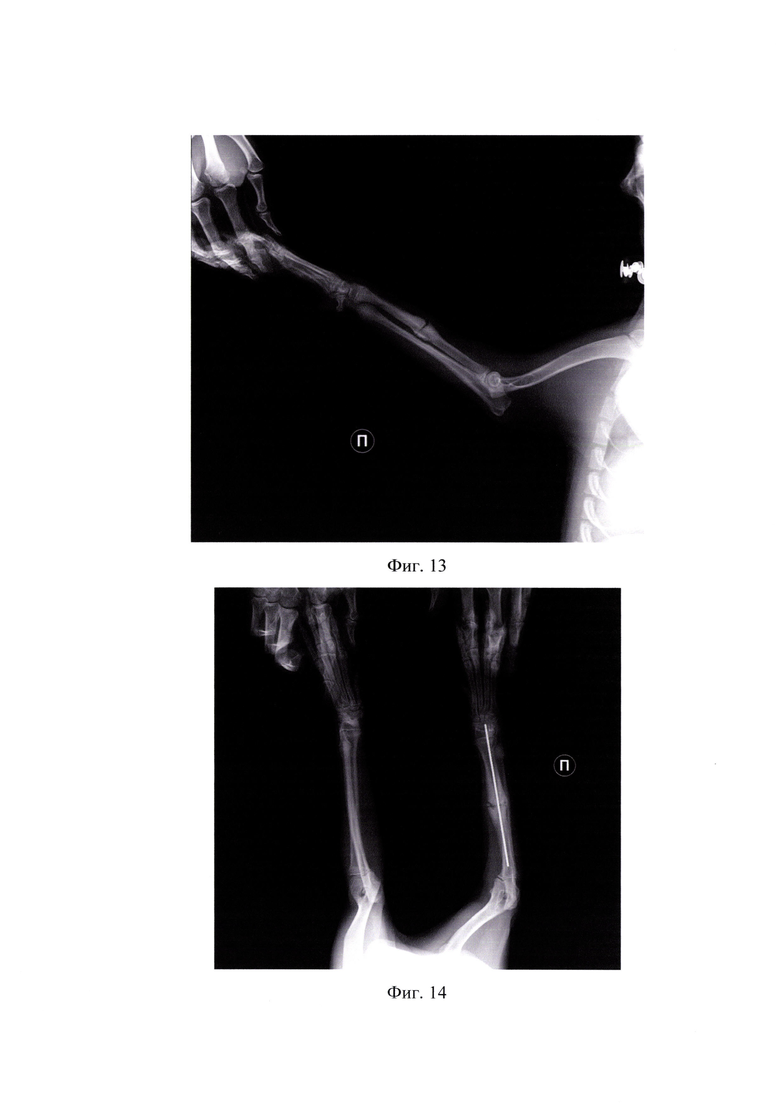
На фиг.14 представлена рентгенограмма после проведения интрамедуллярного остеосинтеза имплантатом с биокомпозиционным покрытием в дорзо-вентральной проекции (пример 2).
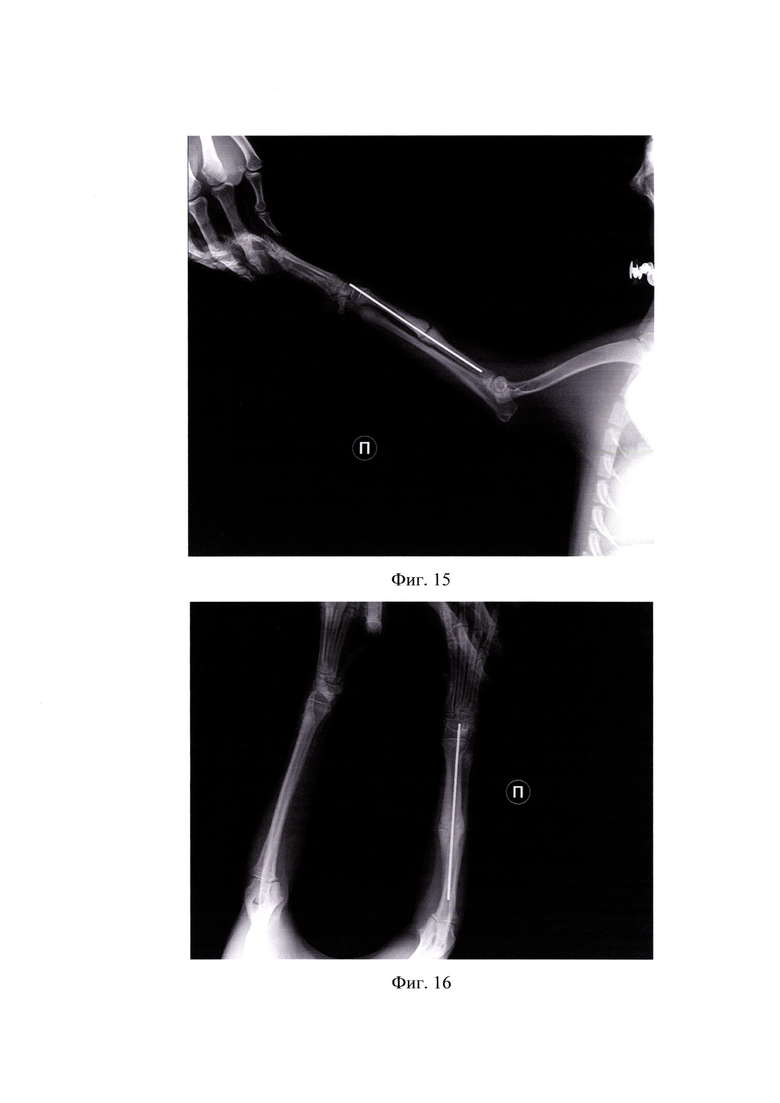
На фиг.15 представлена рентгенограмма после проведения интрамедуллярного остеосинтеза имплантатом с биокомпозиционным покрытием в латеро-медиальной проекции (пример 2).
На фиг.16 представлена рентгенограмма спустя 25 дней в дорзо-вентральной проекции (пример 2).
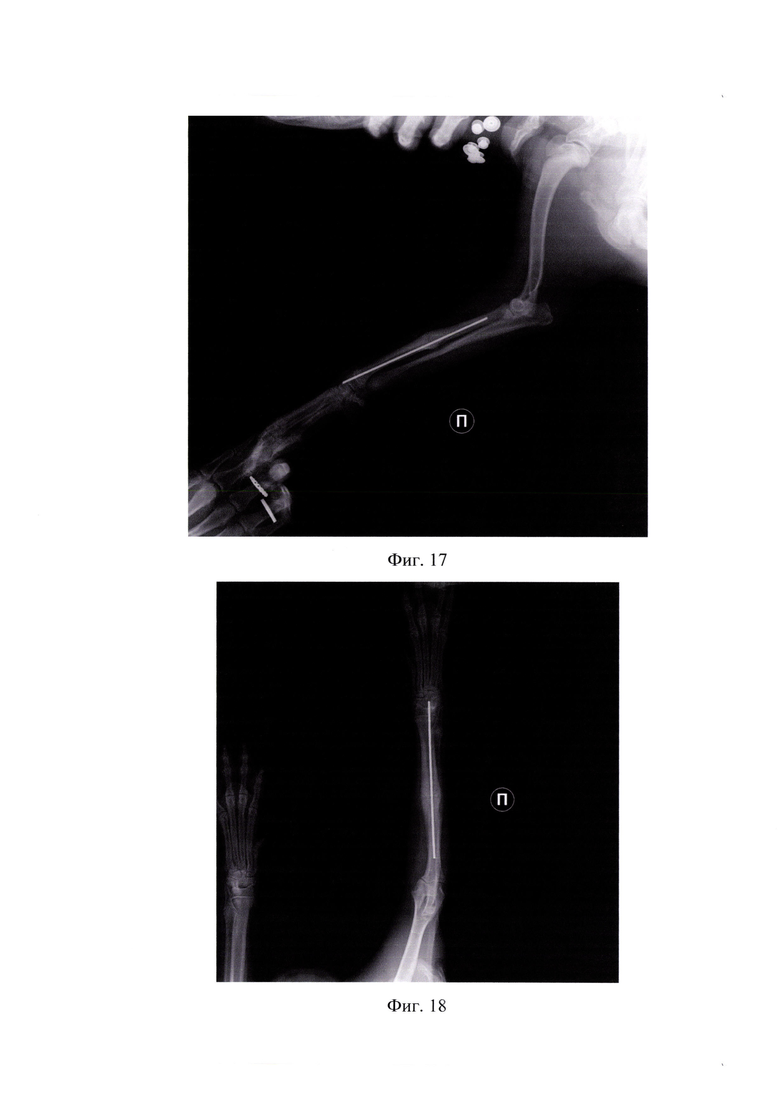
На фиг.17 представлена рентгенограмма спустя 25 дней в латеро-медиальной проекции (пример 2).
На фиг.18 представлена рентгенограмма спустя 43 дней в дорзо-вентральной проекции (пример 2).
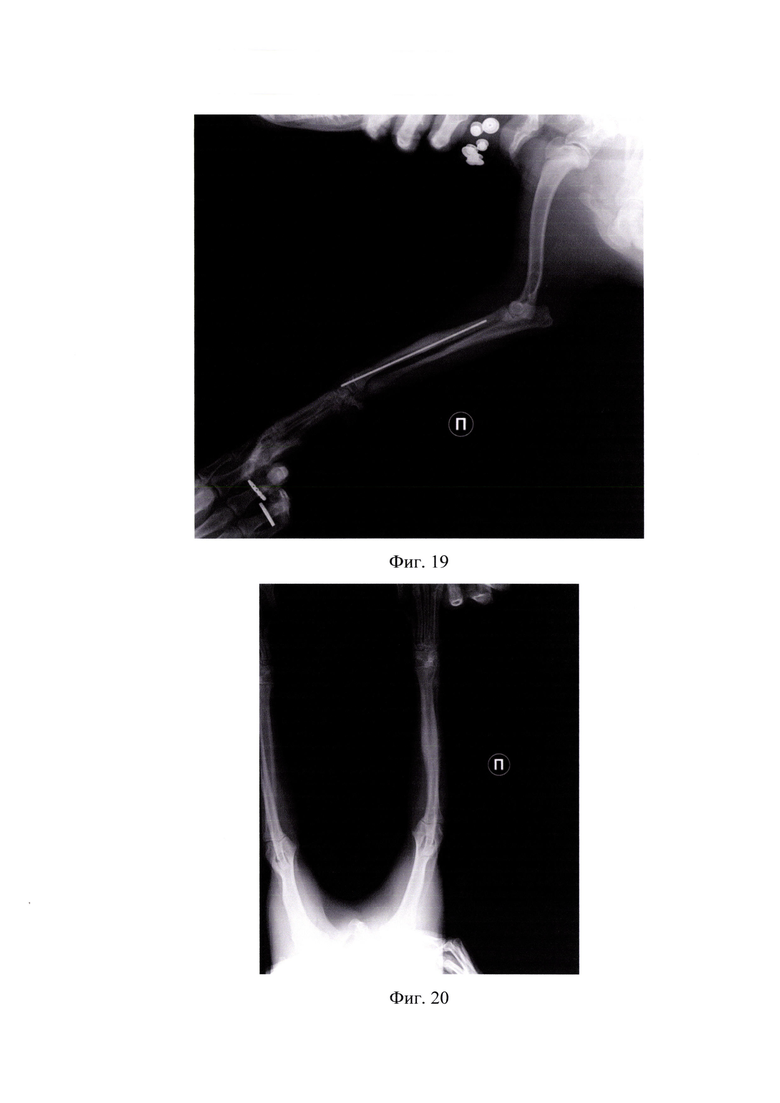
На фиг.19 представлена рентгенограмма спустя 43 дней в латеро-медиальной проекции (пример 2).
На фиг.20 представлена рентгенограмма после снятия имплантата в дорзо-вентральной проекции (пример 2).
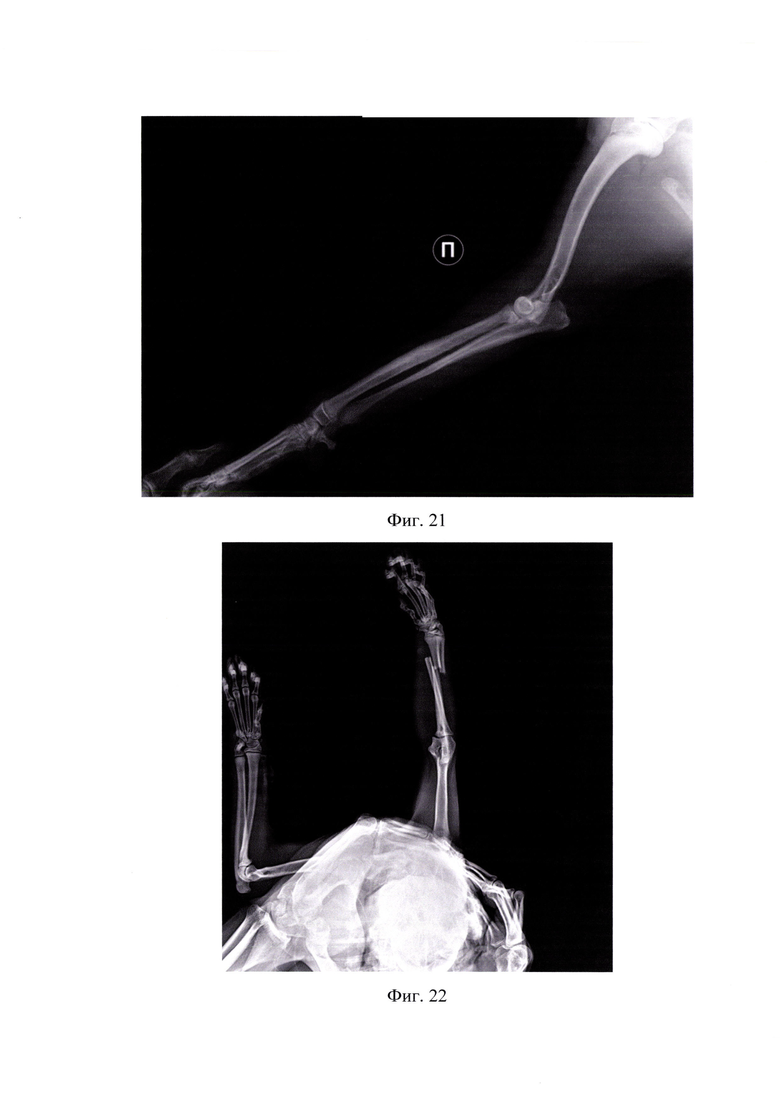
На фиг.21 представлена рентгенограмма после снятия имплантата в латеро-медиальной проекции (пример 2).
На фиг.22 представлена рентгенограмма поперечного перелома диафиза локтевой и лучевой кости справа со смещением по ширине и длине, по классификации AO/ASIF - 2 2 А2 в дорзо-вентральной проекции (пример 3).
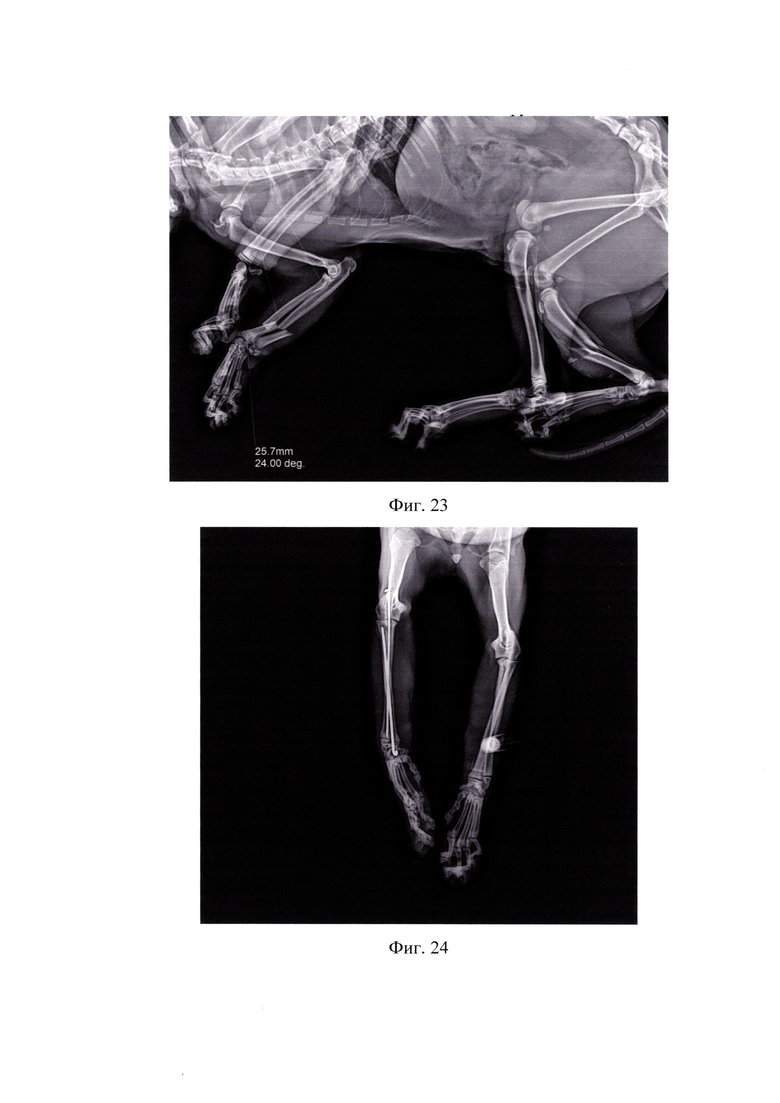
На фиг.23 представлена рентгенограмма поперечного перелома диафиза локтевой и лучевой кости справа со смещением по ширине и длине, по классификации AO/ASIF - 2 2 А2 в латеро-медиальной проекции (пример 3).
На фиг.24 представлена рентгенограмма сразу после оперативного вмешательства в дорзо-вентральной проекции (пример 3).
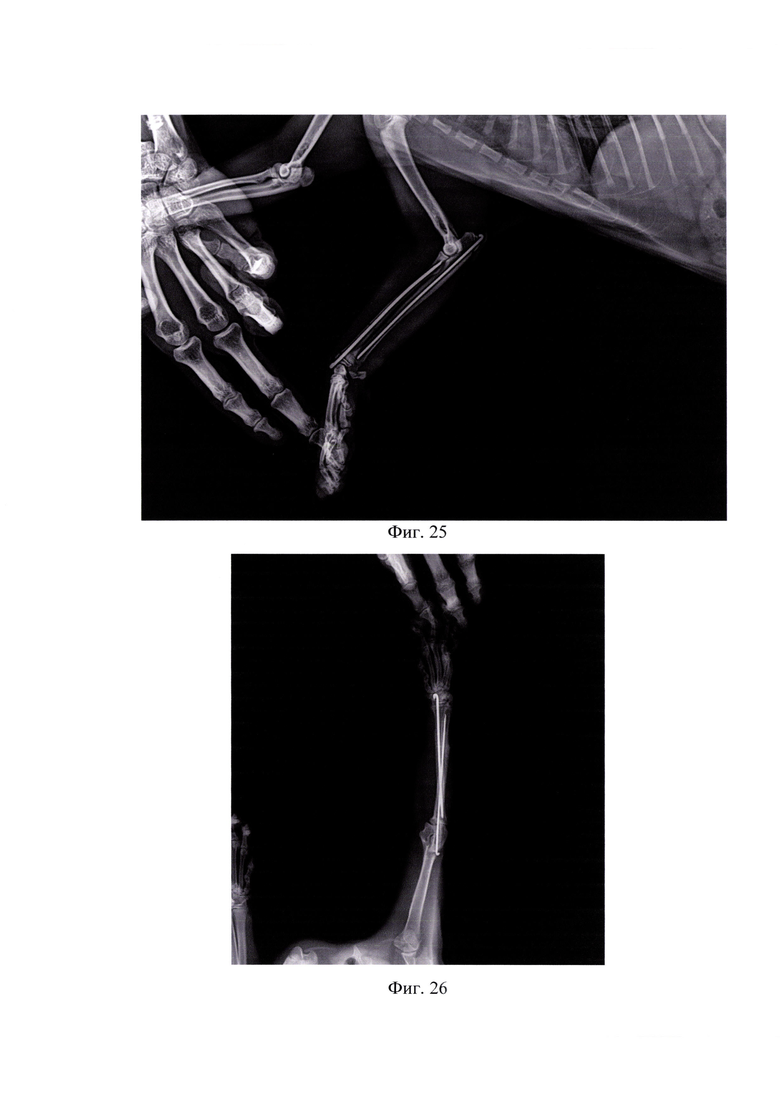
На фиг.25 представлена рентгенограмма сразу после оперативного вмешательства в латеро-медиальной проекции (пример 3).
На фиг.26 представлена рентгенограмма спустя 43 дня в дорзо-вентральной проекции (пример 3).
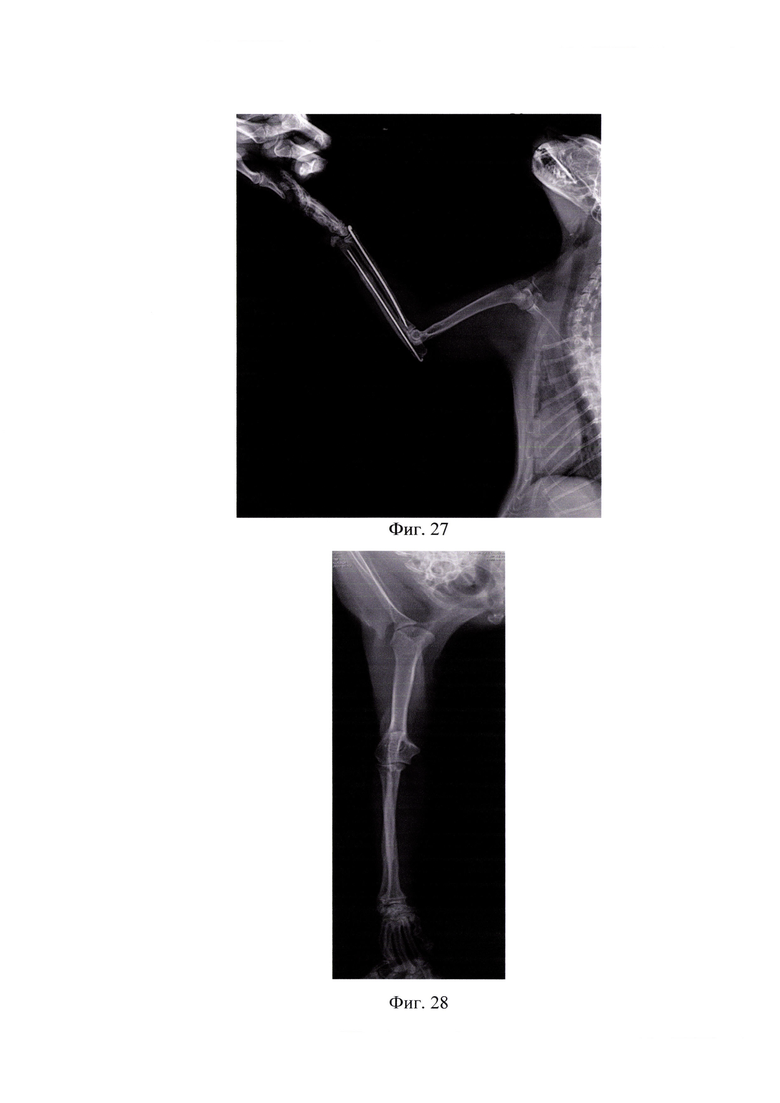
На фиг.27 представлена рентгенограмма спустя 43 дня в латеро-медиальной проекции (пример 3).
На фиг.28 представлена рентгенограмма после извлечения импланта в дорзо-вентральной проекции (пример 3).
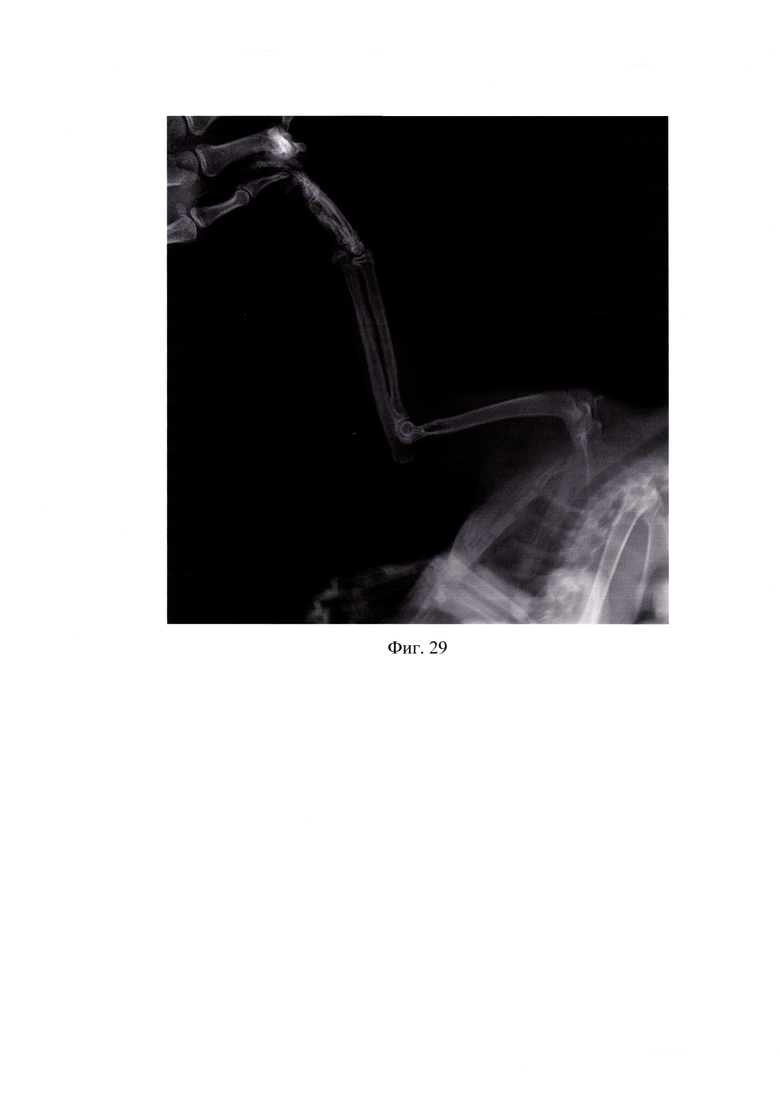
На фиг.29 представлена рентгенограмма после извлечения импланта в латеро-медиальной проекции (пример 3).
Способ осуществляется следующим образом. Производится предоперационная подготовка, определение метода остеосинтеза и применяемых для него накостных или внутрикостных имплантатов (спицы, штифты, пластины, остеофиксаторы). На используемые импланты наносится остеокондуктивное и остеоиндуктивное покрытие на основе известных веществ и метода его нанесения, с последующей их установкой (накостное/внутрикостное) в область дегенеративно-дистрофических нарушений костной системы, псевдоартрозах, замедленной консолидации, а также при первичном нарушении анатомической целостности костей.
Определено, что данное биокомпозиционное покрытие имеет стабильную плотную форму, с отменной адгезией на имплантатах, с отсутствием нарушений его целостности при механических воздействиях, образующиеся при установке имплантов в костную ткань.
Данное биокомпозиционное покрытие характеризуется следующими свойствами:
- не обладает аллергизирующим и цитостатическим эффектом;
- отсутствие реакции отторжения покрытия;
- катализатор механизмов клеточной пролиферации;
- обладает бактерицидным воздействием;
- обладает биоинтеграцией;
- стимулирует алгоритмы остеокондуктивности и остеоиндуктивности;
- активирует особенности регенерации травмированных тканей. Благодаря биоинтеграции биокомпозиционного покрытия создается
планомерное распределение компонентов в оперируемой области, что, в свою очередь, ускоряет образование ценных структур обеспечивающих активацию остеобластного процесса.
Данный способ прагматизации нашел свое применение в практическом ветеринарном здравоохранении ветеринарной клиники DoctorVet, где продемонстрировал свою эффективность, что подтверждается следующими клиническими примерами.
Пример 1.
Пациент Мальта, 2,5 года, метис, самка, 8 кг, поступила в клинику DoctorVet через 75 дней с момента травмы с диагнозом «Посттравматический псевдоартроз средней трети диафиза лучевой кости с обширной остеодеструкцией». В сторонней клинике, в первый день с момента травмы, выполнили оперативное вмешательство с постановкой внеочаговый остеосинтез аппаратом внешней фиксации. Через 70 дней после оперативного вмешательства консолидации не обнаружено, при этом хромота 3 степени, болевой синдром и снижение функции правой грудной конечности.
В результате пациент был направлен в ветеринарную клинику DoctorVet для оперативного лечения. Клиническим, ортопедическим и рентгенологическим методом исследования определен гиперпластический псевдоартроз средней трети диафиза лучевой кости, также массивная остеодеструкция из-за не правильного поставленного спицевого аппарата внешней фиксации, приводящего к патологической подвижности костных отломков. Рентгенограмма представлена на фигурах 2,3. Аппарат удален оперативным путем (фигуры 4,5).
Спустя сутки с момента поступления в клинику Doctor Vet проведена операция - интрамедуллярный остеосинтез имплантатом с остеокондуктивным и остеоиндуктивным покрытием на основе гидроксиапатита, метилурацила, амоксициллина, полилактида (фигуры 6,7).
Функция грудной конечности не была ограничена в период всего срока стабилизации, при этом питомец занимался лечебными реабилитационными методами - гимнастикой, массажем. Дополнительное время фиксации составило 73 дня (нормальные сроки консолидации от 7 до 12 недель; с учетом усугубленного анамнеза - например, при псевдоартрозе и обширной остеодеструкции, увеличивается на неопределенный срок). Рентгенографически, на разных временных промежутках (20, 73 сутки), диагностирован процесс консолидирования в зоне псевдоартроза и остеодеструкции, представленное на фигурах 8, 9, 10, 11. Произведено извлечение интрамедуллярного имплантата. Ухудшений в процессе стабилизации не было. Достигнут хороший анатомо-функциональный эффект лечения с отсутствием видимой хромоты.
Пример 2.
Пациент Тони, кобель, 2 года, метис, 8,0 кг, поступил в клинику DoctorVet через 63 дня с момента травмы с диагнозом «Посттравматический псевдоартроз средней трети лучевой кости». Благодаря анамнезу установлено, что проводили лечение перелома с помощью гипсования в сторонней клинике спустя сутки с момента травмы. В период всего срока пациента беспокоил отек, мацерация с пиодермией в области наложения гипсовой лангеты, хромата 3 степени, при прикосновении и обработки кожи беспокоил болевой синдром с ограничением функции грудной конечности. В результате владелец обратился в ветеринарную клинику DoctorVet. Клиническим, ортопедическим и рентгенологическим методом исследования определена патологическая подвижность в предплечье, псевдоартроз средней трети диафиза лучевой кости правой грудной конечности (фигуры 12, 13). Владельцем было принято решение о оперативном вмешательстве для проведения интрамедуллярного остеосинтеза имплантатом с остеокондуктивным и остеоиндуктивным покрытием на основе гидроксиапатита, метилурацила, амоксициллина, полилактида (фигуры 14, 15).
Послеоперационный период проходил без осложнений. Через 25 суток визуализируется физиологический процесс консолидации (фигуры 16, 17). Спустя 48 дней определена консолидация области псевдоартроза, установленного клинически и рентгенологически (фигуры 18, 19), также в период реабилитации занимались восстановительной физкультурой, массажем. Спустя 48 дней сняли имплантат. Период нормальной консолидации составляет 58-86 дней, однако, в процессе отягощенного анамнеза (псевдоартроз) - увеличивается на неопределенное время. Осложнений в процессе стабилизации не было. После подтверждения консолидации произвели удаление имплантатов (фигуры 20, 21). Достигнут хороший анатомо-функциональный эффект лечения с отсутствием видимой хромоты.
Пример 3.
Пациент Ролекс, 1,5 года, кот, метис, 4,3 кг, поступил через сутки с момента травмы с диагнозом «Поперечный перелом диафиза локтевой и лучевой кости справа со смещением по ширине и длине, по классификации AO/ASIF - 2 2 А2» (фигуры 22, 23). Владелец сразу обратился в ветеринарную клинику DoctorVet. При клиническом, ортопедическом и рентгенологическом исследовании выявлено отсутствие опороспособности на грудную конечность, патологическая подвижность в области предплечья. Принято решение об оперативном вмешательстве с установкой интрамедуллярных имплантатов с нанесенным биокомпозиционным покрытием. Произвели медиальный анатомический доступ в область правого диафиза, установка интрамедуллярных спиц с репозицией костных отломков, далее стандартная послойная методика закрытия мягких тканей (фигуры 24,25). Послеоперационный период проходил без осложнений. Сразу после хирургической помощи пациент начал пользоваться грудной конечностью. Хромота после оперативного вмешательства наблюдалась еще в течении 6 дней, после отсутствовала. Консолидация произошла через 43 дня (нормальные временные рамки для сращения составляют 50-84 дня, что установлено клинически и рентгенологически (фигуры 26,27). После подтверждения консолидации произвели удаление имплантатов (фигуры 28,29). Достигнут хороший анатомо-функциональный эффект лечения.
На основании вышеизложенного, предложенный способ прагматизации обладает существенными достоинствами:
1. Понижение ятрогенного фактора при затяжных дегенеративно -дистрофических процессах в связи с отсутствием необходимости в проведении дополнительных остеотомий.
2. Абсолютность использования, как при первичной, так и при вторичной хирургии.
3. Возможность нанесения на имплантаты под разные методы остеосинтеза (интрамедуллярный, интрамедуллярный блокируемый, накостная пластина).
4. Возможность прагматизации репаративного остеогенеза благодаря уменьшению времени на сращение переломов, ложных суставов, дегенеративно -дистрофических изменений, что в свою очередь восстанавливает физический статус пациентов.
5. Профилактирование бактериальных инфекций.
Заявляемое изобретение является новым и промышленно применимым, так как может быть реализовано с использованием известных компонентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оптимизации репаративного остеогенеза трубчатых костей животных | 2023 |
|
RU2816808C1 |
| Остеокондуктивное и остеоиндуктивное биокомпозиционное покрытие имплантов для ускорения консолидации переломов животных | 2022 |
|
RU2817049C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА В ЭКСПЕРИМЕНТЕ | 2022 |
|
RU2783642C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ДЕФЕКТА КЛЮЧИЦЫ | 2023 |
|
RU2807898C1 |
| Способ хирургического лечения перелома проксимального отдела плечевой кости | 2016 |
|
RU2652573C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ПЛЕЧЕВОЙ КОСТИ ПРИ ГИПОТРОФИЧНОМ ПСЕВДОАРТРОЗЕ | 2018 |
|
RU2695268C1 |
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2006 |
|
RU2315580C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗАМЕДЛЕННОЙ КОНСОЛИДАЦИИ, НЕСРАСТАЮЩИХСЯ ПЕРЕЛОМОВ, ЛОЖНЫХ СУСТАВОВ ТРУБЧАТЫХ КОСТЕЙ КОНЕЧНОСТЕЙ | 2001 |
|
RU2189193C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРЕЛОМОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2006 |
|
RU2317034C1 |
| СПОСОБ ЛЕЧЕНИЯ МНОГООСКОЛЬЧАТЫХ И МНОЖЕСТВЕННЫХ ПЕРЕЛОМОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2008 |
|
RU2370227C1 |

Изобретение относится к ветеринарной травматологии и ортопедии. Способ заключается в предварительной подготовке раствора для обработки устанавливаемых имплантатов (спицы, штифты, винты, остеофиксаторы, накостные пластины). При этом в качестве раствора используют остеокондуктивное и остеоиндуктивное покрытие на основе гидроксиапатита, метилурацила, амоксициллина, полилактида, полученное растворением в 50 мл хлороформа, при температуре окружающей среды 22°С и непрерывном перемешивании на магнитной мешалке, 1 г полилактида до образования густой суспензии прозрачного цвета. Затем при непрерывном перемешивании добавляют последовательно метилурацил, гидроксиапатит и амоксициллин по 400 мг каждого компонента каждые 20 мин по 5 раз с получением на выходе суспензии молочного цвета, в которую опускают стерильные хирургические имплантаты 5 раз, по 10 с каждый, с интервалом в 2 мин до образования тонкой пленки толщиной 1-1,5 мм. После этого имплантаты с нанесенным слоем устанавливают в штатив и проводят однократно лиофильную сушку при температуре 3-5°С и при давлении 5⋅10-1 Па в течение 30 мин с последующей предоперационной стерилизацией имплантатов автоклавированием или в сухожаровом шкафу. Достигается повышение эффективности и надежности прагматизации репаративного остеогенеза. 29 ил., 3 пр.
Способ проведения репаративного остеогенеза трубчатых костей животных, заключающийся в предварительной подготовке раствора для обработки устанавливаемых имплантатов в виде спиц, штифтов, винтов, остеофиксаторов, накостных пластин, отличающийся тем, что в качестве раствора используют остеокондуктивное и остеоиндуктивное покрытие на основе гидроксиапатита, метилурацила, амоксициллина, полилактида, полученное растворением в 50 мл хлороформа при температуре окружающей среды 22°С и непрерывном перемешивании на магнитной мешалке 1 г полилактида до образования густой суспензии прозрачного цвета, затем при непрерывном перемешивании добавляют последовательно метилурацил, гидроксиапатит и амоксициллин по 400 мг каждого компонента каждые 20 мин по 5 раз с получением на выходе суспензии молочного цвета, в которую опускают стерильные хирургические имплантаты 5 раз по 10 с каждый с интервалом в 2 мин до образования тонкой пленки толщиной 1-1,5 мм, затем имплантаты с нанесенным слоем устанавливают в штатив и проводят однократно лиофильную сушку при температуре 3-5°С и при давлении 5⋅10-1 Па в течение 30 мин с последующей предоперационной стерилизацией имплантатов автоклавированием или в сухожаровом шкафу.
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2020 |
|
RU2738406C1 |
| БИОТРАНСПЛАНТАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ И ТРАВМАТИЧЕСКИХ ЗАБОЛЕВАНИЙ КОСТНОЙ ТКАНИ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2008 |
|
RU2380105C1 |
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2006 |
|
RU2315580C2 |
| СПОСОБ ЗАМЕЩЕНИЯ КОСТНОЙ ТКАНИ | 2014 |
|
RU2553368C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА ПРИ ЛЕЧЕНИИ ПЕРЕЛОМОВ | 2008 |
|
RU2364361C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОСТНОЙ ТКАНИ ЧЕЛЮСТЕЙ ПОСЛЕ ОПЕРАЦИИ ЦИСТЭКТОМИИ | 2006 |
|
RU2311181C1 |
Авторы
Даты
2024-04-05—Публикация
2023-03-10—Подача