Область техники, к которой относится изобретение
Настоящее изобретение относится к области экстракции из растений, в частности, к способу экстракции из растений.
Уровень техники
Натуральные растительные экстракты относятся к продуктам, полученным с применением растений в качестве сырья и, в частности, к получению или концентрированию одного или нескольких действующих компонентов из растений без изменения их активной структуры посредством физической и химической экстракции и разделения в соответствии с назначением конечного экстрагированного продукта. Растительные экстракты содержат богатые и сложные органические компоненты, при этом большинство органических компонентов обладают такими биологическими активностями, как антибактериальная активность, бактериостатическая активность, антиоксидантная активность и активность по регулированию иммунитета организма. Из-за того, что они являются экологически чистыми, полезными для здоровья, безопасными, эффективными, бесшлаковыми и т.д., растительные экстракты во всем мире широко применяют в таких областях, как лекарственные препараты, продукты для здоровья, косметика, пищевые добавки, пестициды, корма и предметы первой необходимости. Китай является колыбелью шелкопрядения. Растения Moraceae с древних времен считались драгоценными материалами, применяемыми в качестве лекарственного препарата и продуктов питания из-за их высокой питательной и лекарственной ценности, что во все времена сообщалось в классических работах традиционной китайской медицины, например, еще в Compendium of Materia Medica есть следующие слова: «отваром листьев тутового дерева можно утолить жажду вместо чая» и «питьем после приготовления и настаивания можно утолить жажду вместо чая». Современная наука также привела доказательства наличия питательных и фармакологически действующих компонентов у растений Moraceae, а также изучила механизмы их действия. Исследования показали, что к химическим компонентам в растениях Moraceae в основном относятся флавоновые соединения, полисахаридные соединения, алкалоиды и аминокислоты, в дополнение к некоторым летучим маслам, таннину, янтарной кислоте, аденину, витаминам и др., и они обладают противогрибковым действием. противовоспалительным действием, гипогликемическим действием, антиоксидантным действием и др.
Способы экстракции из растений можно разделить на классические способы экстракции и современные способы экстракции. Классические способы экстракции не требуют специальных инструментов, просты и удобны в реализации, не требуют больших затрат при экстракции, и в основном к ним относятся способ экстракции растворителем, способ перегонки паром и др. Современными способами экстракции являются способы экстракции, основанные на современных передовых инструментах или недавно разработанных способов экстракции, и в основном к ним относятся способ ультразвуковой экстракции, способ микроволновой экстракции, способ ферментативной экстракции, способ твердофазной экстракции и др. Компоненты растительных экстрактов можно разделить на липофильные компоненты и гидрофильные компоненты, которые можно получить путем подбора различных растворителей и/или способов экстракции для различных растительных экстрактов. Например, что касается липофильных растительных компонентов, органические растворители можно применять для проведения перколяции, холодного выщелачивания, ультразвуковой экстракции, микроволновой экстракции, экстракции кипячением с обратным холодильником и др.; что касается водорастворимых компонентов, то обычно применяемым способом экстракции является способ водной экстракции и осаждения спиртом, который имеет большое значение в контексте переработки и очистки, увеличения содержания действующих компонентов, снижения дозы введения и удобства в производстве и формовании экстрактов в традиционной китайской медицине. Конкретные стадии включают такие стадии, как водная экстракция, концентрирование, осаждение спиртом, сушка и др., при этом осаждение спиртом обозначает добавление этанола к неочищенному экстракционному раствору до тех пор, пока концентрация этанола не достигнет соответствующей концентрации, обеспечивающей осаждение нерастворимых в этаноле примесей, а затем проведение разделения твердой и жидкой фаз для достижения цели переработки. Например, Xingjie Chang и коллеги экстрагировали действующие компоненты Forsythia в соответствии со стадиями отвара в воде, концентрирования, осаждения этанолом и удаления этанола (Xingjie Chang, Qian Ding. Forsythiaside A, Forsythin and changes of the bacteriostatic activities thereof in the preparation process of water extraction and alcohol precipitation of Forsythia [J]. Guiding Journal of Traditional Chinese Medicine and Pharmacy, 2018, 24(9):39-41.); Aiying Shen и коллеги получали полисахариды листьев тутового дерева с помощью способа водной экстракции и осаждения этанолом (Aiying Shen, Ziyu Zhu, Wenliang Zhang. Study on the extraction process of water-soluble polysaccharides from mulberry leaves [J]. Acta Sericologica Sinica, 2004, 30(3):277-279.). Для дополнительного концентрирования и обогащения действующими компонентами после осаждения спиртом можно также провести разделение на смоле, мембранное разделение, ультрафильтрацию, диализ и др. для достижения цели очистки.
Растущий спрос потребителей на продукты из растительных экстрактов подтолкнул к углубленной разработке способа экстракции из растений, и было улучшено качество продуктов. Тем не менее, по сравнению с развитыми странами, в китайских растительных экстрактах все еще есть некоторые серьезные недостатки. Среди прочих большое внимание привлекли вопросы, связанные с безопасностью продуктов, такие как остаточные количества тяжелых металлов и пестицидов. В ходе исследований было обнаружено, что некоторые растения способны обогащать окружающую среду тяжелыми металлами (такими как медь, свинец, кадмий, цинк и т.д.). Например, по результатам исследования, проведенного Xing Zhang и коллегами, было обнаружено, что в случае выращивания тутового дерева на почве, содержащей указанные далее тяжелые металлы, т.е. Cu (593,56 мг/кг), Pb (825,41 мг/кг), Cd (8,11 мг/кг), Zn (705,41 мг/кг), содержание тяжелых металлов, измеренное в корнях, составляет до следующих значений: Си: 33,13 мг/кг, Pb: 33,13 мг/кг, Cd: 4,53 мг/кг, Zn: 317,72 мг/кг, содержание тяжелых металлов в листьях до следующих значений: Си: 13,18 мг/кг, Pb: 10,32 мг/кг, Cd: 1,90 мг/кг, Zn: 186,53 мг/кг, что намного превышает соответствующие нормативы (согласно нормативам «Стандарты "зеленой" торговли лекарственными растениями и препаратами для импорта и экспорта», в сырье, отварах, экстрактах и препаратах из растений общее содержание тяжелых металлов должно составлять 20,0 мг/кг и менее, содержание Pb должно составлять 5 мг/кг и менее, содержание Cd должно составлять 0,3 мг/кг или менее, содержание Hg должно составлять 0,2 мг/кг или менее, содержание Cu должно составлять 20,0 мг/кг или менее, и содержание As должно составлять 2,0 мг/кг или менее). Важным аспектом, который необходимо учитывать при исследовании способов экстракции из растений, является то, как в максимальной степени сократить остатки вредных веществ, таких как тяжелые металлы.
Краткое описание изобретения
При общих исследованиях и способах промышленного производства водорастворимые растительные экстракты обычно получают способом водной экстракции и осаждения спиртом, после осаждения спиртом для дополнительного обогащения и очистки при рассмотрении увеличения содержания конкретного компонента проводят разделение на смоле, мембранное разделение, ультрафильтрацию, диализ и др. Тем не менее, что касается растительных экстрактов, особенно таких растений, как Moraceae, которые склонны к накоплению тяжелых металлов из окружающей среды, применение такого способа экстракции для получения экстрактов является недостаточным для удаления остатков тяжелых металлов в экстрактах. Авторами настоящего изобретения по результатам повторного исследования было обнаружено, что в ходе реализации способа экстракции из растения последовательное подвергание неочищенного экстракционного раствора разделению на смоле, концентрированию и осаждению спиртом не только способно улучшить эффективность разделения действующих компонентов, но также способно значительно уменьшить остатки тяжелых металлов в растительных экстрактах. Исходя из данных результатов, авторами настоящего изобретения предложен новый способ экстракции из растений, который позволяет эффективно снизить содержание тяжелых металлов в растительных экстрактах, при этом значительно уменьшив количество этанола, применяемого в способе экстракции, тем самым улучшив качество продукта при одновременном снижении производственных затрат и до определенной степени повышения эффективности и безопасности промышленного производства.
Ввиду этого, в первом аспекте настоящего изобретения предложен способ экстракции из растений, предусматривающий следующие стадии:
стадия 1): получение неочищенного экстракционного раствора из растений;
стадия 2): разделение неочищенного экстракционного раствора с помощью катинообменной смолы со сбором элюата, необязательно, разделение элюата с помощью анионообменной смолы со сбором выходящего потока;
стадия 3): концентрирование собранного раствора, полученного на стадии 2);
стадий 4): осаждение концентрированного раствора, полученного на стадии 3), спиртом; и
необязательно, стадия 5): концентрирование и сушка.
1) Получение неочищенного экстракционного раствора из растений
В настоящем изобретении растение предпочтительно представляет собой растение из семейства Moraceae, Liliaceae, Campanulaceae или Commelinaceae, кроме того, предпочтительно представляет собой растение из рода Moms, Hyacinthus, Adenophora или Commelina, и более предпочтительно, растение представляет собой любое растение или их комбинацию, выбранное из Morus multicaulis Perrott, Morus alba L., Morus atropurpurea Roxb, Morusmizuho Hotta, Morus wittiorum Hand Mazz., Morus laevigata Wall, Morus nigra Linn., Morus cathayana Hem si., Morus serrata Roxb., Morus mongolica Schneid., Morus bombycis Koidz., Morus notabilis Schneid., Morus nigriformis Koidz., Morusyunnanensis Koidz., Morus australis Poir., Morus mongolica (Bur.) Schneid var. diabolica Koidz., Morus alba L. var. macrophylla loud, Morus alba var.Pendula Dippel, Morus alba L. var. venosa Delili, сорта тутового дерева, выведенного из указанных выше видов тутового дерева, гибрида тутового дерева, полученного в результате избирательной внутривидовой и межвидовой селекции вышеперечисленных видов тутового дерева, Hyacinthus orientalis, Adenophora. triphylla var. japonica и Commelina communi; предпочтительно, растение представляет собой Morus atropurpurea Roxb, Morus multicaulis Perrott., Morus alba L., Morus serrata Roxb., Morus bombycis Koidz. или гибрид тутового дерева, гибрид тутового дерева предпочтительно представляет собой Yuesang №11, Guisangyou №62 или Sangteyou №2. Можно применять различные части, такие как лист, корень, ветвь, кора, почка, стебель и плод растения.
Растение можно подвергнуть грубой экстракции растворителем, таким как спирт-вода, вода, щелочной водный раствор или кислый водный раствор, предпочтительно растворителем, применяемым для грубой экстракции, является вода.
В ходе экстракции предпочтительно измельчить растение, а затем добавить полученную массу в воду для проведения тепловой экстракции, продолжительность экстракции предпочтительно составляет от 0,5 до 3 ч для каждой экстракции, а саму экстракцию проводят от 1 до 3 раз.
В предпочтительном варианте осуществления для проведения экстракции измельченное растение можно поместить в экстракционный резервуар.
В ходе экстракции, чем больше количество добавляемого растворителя, тем выше скорость экстракции из растения. Однако чрезмерное добавляемое количество растворителя может усложнить последующее разделение и очистку. Добавляемое количество растворителя предпочтительно в 3-20 раз и более предпочтительно в 4-15 раз превышает массу загружаемого растительного сырья, что позволяет в наибольшей степени получить растительный экстракт без чрезмерного увеличения объема раствора и увеличения сложности последующей обработки.
Экстракцию можно проводить с помощью способа отваривания, способа ультразвуковой экстракции или способа экстракции кипячением с обратным холодильником, предпочтительно ее проводят с помощью способа отваривания или способа экстракции кипячением с обратным холодильником, и более предпочтительно ее проводят с помощью способа отваривания, для которого имеется более проработанное промышленное оборудование.
Необязательно, экстракцию можно провести повторно, а экстрагирующие растворы объединить.
Предпочтительно, экстрагирующий раствор фильтруют для удаления нерастворимых веществ с получением неочищенного растительного экстракционного раствора.
2) Разделение с помощью катионообменной смолы и необязательной анионообменной смолы
В настоящем изобретении компоненты в неочищенном растительном экстракционном растворе разделяют с применением ионообменной смолы.
На стадии 2) неочищенный растительный экстракционный раствор загружают на катионообменную смолу и разделяют через катионообменную смолу. Предпочтительно, после забивки в колонку катионообменную смолу подвергают активации путем последовательной промывки кислым раствором, щелочным раствором и кислым раствором. Способ активации смолы также позволяет производить корректировку значения рН среды смолы, тем самым оптимизируя избирательность адсорбции катионообменной смолой и усиливая разделяющий эффект.
Предпочтительно, смолу промывают щелочным раствором до тех пор, пока рН элюата не станет 8,0-9,5, предпочтительно 8,5-9,5.
Предпочтительно, щелочной раствор представляет собой раствор аммиака, раствор гидроксида натрия, раствор гидроксида калия или раствор карбоната натрия, предпочтительно раствор аммиака или раствор гидроксида натрия. Предпочтительно, концентрация щелочного раствора составляет 0,5-4 моль/л, предпочтительно 1-2 моль/л.
Предпочтительно, смолу промывают кислым раствором до тех пор, пока рН элюата не станет 3,0-7,0, предпочтительно 4,5-6,5.
Предпочтительно, кислый раствор выбран из раствора соляной кислоты, раствора фосфорной кислоты и буфера на основе натрия фосфата двузамещенного-лимонной кислоты и более предпочтительно буфера на основе натрия фосфата двузамещенного-лимонной кислоты. Предпочтительно, концентрация кислого раствора составляет 0,5-4 моль/л, предпочтительно 1-2 моль/л.
При применении в качестве кислого раствора буфера на основе натрия фосфата двузамещенного-лимонной кислоты значение рН буфера на основе натрия фосфата двузамещенного-лимонной кислоты предпочтительно составляет 4,0-6,5 и более предпочтительно 4,5-5,0.
Необязательно, катионообменную смолу можно также промыть деионизированной водой, объем которой в 3-5 раз превышает объем колонки, после последней промывки кислым раствором.
Предпочтительно, катионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнокислотной катионообменной смолы, слабокислотной катионообменной смолы и сильнощелочной катионообменной смолы четвертичноаммониевого типа.
Предпочтительно, катионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнокислотной катионообменной смолы на основе стирола 732-го типа, сильнокислотной катионообменной смолы на основе стирола 734-го типа, сильнокислотной катионообменной смолы на основе стирола типа 002SC, макропористой и сильнокислотной катионообменной смолы на основе стирола типа D001, макропористой и слабокислотной катионообменной смолы на основе фенилпропена типа D113 и макропористой и сильнощелочной катионообменной смолы типа D254 четвертичноаммониевого типа.
Предпочтительно, катионообменная смола представляет собой сильнокислотную катионообменную смолу на основе стирола 732-го типа, сильнокислотную катионообменную смолу на основе стирола 734-го типа и макропористую и сильнокислотную катионообменную смолу на основе стирола типа D001.
В результате исследования было обнаружено, что, не ограничиваясь какой-либо теорией, способ загрузки катионообменной смолы, особенно концентрация загрузочного раствора и количество применяемой смолы, оказывает значительное влияние на адсорбционные и разделительные эффекты компонентов растений.
Предпочтительно, количество применяемой катионообменной смолы и загружаемого растительного сырья имеет массовое соотношение в диапазоне от 1:1 до 1:30, предпочтительно от 1:1 до 1:25 и более предпочтительно от 1:2 до 1:20.
После загрузки неочищенного растительного экстракционного раствора на катионообменную смолу загруженную катионообменную смолу подвергают элюированию элюентом. Предпочтительно, элюент представляет собой раствор соли или щелочной раствор, содержащий катионы, предпочтительно один или несколько, выбранных из хлорида натрия, хлорида аммония, сульфата аммония, нитрата аммония, аммиачной воды, хлорида калия и гидроксида натрия.
Предпочтительно, концентрация катионов в элюенте варьирует в диапазоне 0,04-5 моль/л, предпочтительно 0,2-3 моль/л и более предпочтительно 0,5-2,5 моль/л.
Предпочтительно, скорость потока элюента составляет 1-15 BV/h (расход ионитного фильтра в относительных объемах в час), предпочтительно 5-10 BV/h.
Предпочтительно, масса элюента, применяемого для разделения с помощью катионообменной смолы, в 0,1-30 раз превышает массу загружаемого растительного сырья. Предпочтительно, элюирование проводят элюентом, масса которого в 0,5-10 раз превышает массу загруженного растительного сырья.
Сбор начинают, когда элюат начинает вытекать из катионообменной смолы. Начальную точку сбора можно определить в соответствии с рН выходящего потока, получаемого из катионообменной смолы, например, если для осуществления элюирования применяют щелочной раствор, такой как аммиачная вода, сбор начинают, когда рН выходящего тока, получаемого из катионообменной смолы, превышает 7. Начальную точку сбора также можно определить в соответствии со свойствами разделяемых компонентов, например, начальную точку сбора выходящего потока можно определить с использованием хромогенной реакции или реакции осаждения. Также, начальную точку сбора можно определить с помощью таких способов детекции, как высокоэффективная жидкостная хроматография. Предпочтительно, сбор прекращают, когда объем собираемого раствора достигает 0,1-10-кратном массы загружаемого растительного сырья, и более предпочтительно, сбор прекращают, когда объем собираемого раствора достигает 0,2-5-кратной массы загружаемого растительного сырья.
Во время разделения с помощью катионообменной смолы можно применять способ ионного обмена с неподвижным слоем, а также можно применять способ непрерывного ионного обмена. Предпочтительно, применяют способ непрерывного ионного обмена с более высокой степенью автоматизации.
Для улучшения разделяющего эффекта у катионообменной смолы можно также провести многократное разделение с помощью катионообменной смолы, например, 2-5-кратное разделение.
Необязательно, собранный элюат разделяют с помощью анионообменной смолы. При разделении с помощью анионообменной смолы анионообменную смолу после забивки в колонку подвергают активации путем последовательной промывки щелочным раствором, кислым раствором и щелочным раствором.
Предпочтительно, аноинообменную смолу промывают кислым раствором до тех пор, пока рН элюата не станет 3,0-7,0, предпочтительно 4,5-6,5.
Предпочтительно, кислый раствор выбран из раствора соляной кислоты, раствора фосфорной кислоты и буфера на основе натрия фосфата двузамещенного-лимонной кислоты и более предпочтительно буфера на основе натрия фосфата двузамещенного-лимонной кислоты. Предпочтительно, концентрация кислого раствора составляет 0,5-4 моль/л, предпочтительно 1-2 моль/л. При применении в качестве кислого раствора буфера на основе натрия фосфата двузамещенного-лимонной кислоты значение рН буфера на основе натрия фосфата двузамещенного-лимонной кислоты предпочтительно составляет 4,0-6,5 и более предпочтительно 4,5-5,0.
Предпочтительно, аноинообменную смолу промывают щелочным раствором до тех пор, пока рН элюата не станет 8,0-9,5, предпочтительно 8,5-9,5.
Предпочтительно, щелочной раствор представляет собой раствор аммиака, раствор гидроксида натрия, раствор гидроксида калия или раствор карбоната натрия, предпочтительно раствор гидроксида натрия. Предпочтительно, концентрация раствора гидроксида натрия составляет 0,5-4 моль/л, предпочтительно 1-2 моль/л.
Предпочтительно, анионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнощелочной анионообменной смолы, слабощелочной анионообменной смолы и слабокислотной анионообменной смолы.
Предпочтительно, анионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнощелочной анионообменной смолы на основе стирола 717-го типа, сильнощелочной анионообменной смолы на основе стирола 711-го типа, макропористой смолы и сильнощелочной анионообменной смолы на основе стирола типа D201, макропористой и сильнощелочной анионообменной смолы на основе акрила типа D218, макропористой и слабокислотной анионообменной смолы на основе стирола типа D301-G и макропористой и слабощелочной анионообменной смолы на основе стирола типа D301.
Предпочтительно, анионообменная смола представляет собой сильнощелочную анионообменную смолу на основе стирола 717-го типа, макропористую и сильнощелочную анионообменную смолу на основе стирола типа D201 и макропористой и сильнощелочной анионообменной смолой на основе акрила типа D218.
Предпочтительно, количество применяемой анионообменной смолы и загружаемого растительного сырья имеет массовое соотношение в диапазоне от 1:1 до 1:80, предпочтительно от 1:1 до 1:64 и более предпочтительно от 1:1 до 1:32.
Сбор начинают, когда жидкость начинает вытекать из анионообменной смолы. Предпочтительно, сбор прекращают, когда объем собираемого раствора достигает 0,05-10-кратном массы загружаемого растительного сырья, и более предпочтительно, сбор прекращают, когда объем собираемого раствора достигает 0,1-5-кратной массы загружаемого растительного сырья.
Необязательно, для улучшения разделяющего эффекта у анионообменной смолы можно также провести многократное разделение с помощью анионообменной смолы, например, 2-4-кратное разделение.
Предпочтительно, способ экстракции дополнительно предусматривает стадию концентрирования неочищенного растительного экстракционного раствора перед разделением на стадии 2).
К способам концентрирования неочищенного экстракционного раствора относятся концентрирование при нагревании, концентрирование с помощью нанофильтрационной мембраны, концентрирование с помощью мембраны обратного осмоса и их комбинация.
Концентрирование предпочтительно проводят путем концентрирования при нагревании, концентрирования с помощью мембраны обратного осмоса или их комбинации с тем, чтобы увеличить концентрацию неочищенного растительного экстракционного раствора.
Предпочтительно, при применении мембраны для обратного осмоса и мембраны для нанофильтрации для проведения концентрирования с целью повышения эффективности концентрирования примеси можно удалить путем проведения центрифугирования, фильтрации через мембрану для ультрафильтрации или фильтрации через мембрану для микрофилтрации перед концентрированием с помощью мембраны для обратного осмоса и мембраны для нанофильтрации.
Предпочтительно, неочищенный растительный экстракционный раствор концентрируют до тех пор, пока массовая концентрация содержания твердых веществ в растворе составит от 1% до 15%, предпочтительно от 2% до 10%. Содержание твердых веществ относится к твердому веществу, оставшемуся после удаления воды из раствора.
Необязательно, концентрированный неочищенный экстракционный раствор можно также подвергнуть осаждению спиртом перед разделением на смоле на стадии 2). Во время осаждения спиртом к неочищенному экстракционному раствору добавляют этанол, смесь равномерно взбалтывают и перемешивают, перемешивание прекращают и полученную смесь выдерживают в течение определенного периода времени для осаждения в ней нерастворимых веществ. Предпочтительно, этанол добавляют к неочищенному растительному экстракционному раствору, при этом объем этанола в 0,2-20 раза превышает объем неочищенного растительного экстракционного раствора, предпочтительно в 0,4-10 раз превышает объем неочищенного растительного экстракционного раствора. Более предпочтительно, осаждение спиртом проводят с применением резервуара для осаждения спиртом. Предпочтительно, скорость перемешивания при осаждении спиртом составляет от 10 до 600 об./мин, предпочтительно от 40 до 500 об./мин и более предпочтительно от 80 до 400 об./мин.
3) Концентрирование собранного раствора, полученного на стадии 2)
К способам обработки путем концентрирования на стадии 3) относятся концентрирование при нагревании, концентрирование с помощью нанофильтрационной мембраны, концентрирование с помощью мембраны обратного осмоса и их комбинация. Предпочтительно, примеси можно удалить путем проведения центрифугирования, фильтрации через мембрану для ультрафильтрации или фильтрации через мембрану для микрофильтрации перед концентрированием через мембрану для обратного осмоса и мембрану для нанофильтрации.
Предпочтительно, удельный вес концентрированной жидкости, полученной на стадии 3), составляет от 1,0 до 1,3. Удельный вес относится к массовому соотношению концентрированной жидкости к воде в условиях, при которых концентрированная жидкость и вода имеют одинаковый объем.
4) Осаждение спиртом
При осаждении спиртом на стадии 4) концентрированный раствор со стадии 3) подвергают обработке этанолом. В частности к концентрированному раствору со стадии 3) добавляют этанол, смесь равномерно взбалтывают и перемешивают, перемешивание прекращают и полученную смесь выдерживают в течение определенного периода времени для осаждения в ней нерастворимых веществ.
Предпочтительно, на стадии 4 этанол, применяемый для осаждения спиртом, и загружаемое растительное сырье имеют массовое соотношение в диапазоне от 1:4 до 1:600, предпочтительно от 1:20 до 1:300.
Осаждение спиртом предпочтительно проводят в резервуаре для осаждения спиртом.
Предпочтительно, при осаждении спиртом на стадии 4 скорость перемешивания составляет от 10 до 600 об./мин, предпочтительно от 40 до 500 об./мин и более предпочтительно от 80 до 400 об./мин.
5) Концентрация и сушка
Необязательно, способ экстракции дополнительно предусматривает стадию 5) концентрирования и сушки.
Раствор, который был подвергнут осаждению спиртом, фильтруют для удаления нерастворимых веществ и концентрируют при пониженном давлении с получением растительного экстракта в качестве extractum или сушат с получением сухого продукта.
Во втором аспекте настоящим изобретением предложен растительный экстракт, полученный в соответствии с описанным выше способом экстракции.
Предпочтительно, растительный экстракт, полученный в соответствии с указанным выше способом экстракции по настоящему изобретению, содержит алкалоиды с массовым содержанием 3% или более (предпочтительно содержит алкалоиды с массовым содержанием от 3% до 99%, более предпочтительно содержит алкалоиды с массовым содержанием от 15% до 99% и еще более предпочтительно содержит алкалоиды с массовым содержанием от 45% до 99%, таким как от 35% до 70% или от 60% до 75%), и/или содержит полисахариды с массовым содержанием не более 70% (предпочтительно содержит полисахариды с массовым содержанием от 0,2% до 50%) и более предпочтительно содержит полисахариды с массовым содержанием от 0,2%) до 35%), и/или содержит флавоны с массовым содержанием не более 10% (предпочтительно содержит флавоны с массовым содержанием от 0,05% до 5% и более предпочтительно содержит флавоны с массовым содержанием от 0,05% до 2%), и/или содержит аминокислоты с массовым содержанием не более 50%) (предпочтительно содержит аминокислоты с массовым содержанием от 0%) до 40%) и более предпочтительно содержит аминокислоты с массовым содержанием от 0% до 25%), и/или другие компоненты (с массовым содержанием предпочтительно от 0%) до 25% и более предпочтительно от 0% до 20%). Общее содержание всех компонентов составляет 100%, где «все компоненты» относится вообще ко всем компонентам растительного экстракта, включая алкалоиды, полисахариды, флавоны и аминокислоты. То есть в растительном экстракте помимо алкалоидов, полисахаридов, флавонов и аминокислот содержатся и другие компоненты.
Предпочтительно, растительный экстракт, полученный вышеописанным способом экстракции по настоящему изобретению, содержит все компоненты в следующих массовых соотношениях:
Предпочтительно, растительный экстракт, полученный вышеописанным способом экстракции по настоящему изобретению, содержит все компоненты в следующих массовых соотношениях:
Еще предпочтительнее, растительный экстракт, полученный вышеописанным способом экстракции по настоящему изобретению, содержит все компоненты в следующих массовых соотношениях:
Предпочтительно, алкалоиды содержат 1-дезоксиноиримицин (1-DNJ) с массовым содержанием от 30% до 99%, предпочтительно от 50% до 95%, более предпочтительно от 55% до 90% и более предпочтительно от 60% до 90%.
В третьем аспекте настоящим изобретением предложена фармацевтическая композиция, содержащая вышеуказанный растительный экстракт и необязательное фармацевтически приемлемое вспомогательное вещество.
Вспомогательное вещество представляет собой неактивный компонент, который соответствует пути введения или способу введения и не оказывает токсического действия на организм человека.
Вспомогательное вещество может быть твердым вспомогательным веществом или жидким вспомогательным веществом. К твердым вспомогательным веществам относятся, например, лактат натрия, полоксамер, додецилсульфат натрия, карбоксиметилцеллюлоза натрия, желатин, ксантановая камедь, повидон, крахмал, стеарат магния, карбоксиметилкрахмал натрия и тальк. К жидким вспомогательным веществам относятся, например, вода, этанол, сироп и глицерин.
Предпочтительно, к лекарственной форме фармацевтической композиции относится препарат для перорального введения.
Предпочтительно, к лекарственной форме фармацевтической композиции относится таблетка, капсула, пероральный раствор, пероральная эмульсия, пилюля и гранула.
Могут существовать индивидуальные различия в том, что касается конкретной дозы введения в зависимости от возраста пациента, массы тела, состояния здоровья, рациона, пути введения, лекарственных средств, применяемых в комбинации, периода лечения и др.
В четвертом аспекте настоящим изобретением предложено применение вышеуказанного растительного экстракта или вышеуказанной фармацевтической композиции при получении гипогликемического лекарственного средства.
В другом аспекте настоящим изобретением предложено применение вышеуказанного растительного экстракта или вышеуказанной фармацевтической композиции при получении лекарственного средства для лечения аномальной толерантности к глюкозе.
В еще одном аспекте настоящим изобретением предложено применение вышеуказанного растительного экстракта или вышеуказанной фармацевтической композиции при получении лекарственного средства для предупреждения развития и/или лечения заболевания, связанного с аномальным уровнем глюкозы в крови. К заболеваниям относятся без ограничений диабет, диабетическая нефропатия, диабетическая стопа, осложнения со стороны органа зрения, вызванные диабетом, гипергликемия, гиперурикемия, гиперлипидемия, изменение кишечной флоры и сердечно-сосудистые и цереброваскулярные заболевания, такие как инфаркт головного мозга, кровоизлияние в головной мозг, коронарная болезнь сердца и гипертония.
Настоящим изобретением дополнительно предложено применение вышеуказанного растительного экстракта или вышеуказанной фармацевтической композиции при получении гиполипидемического лекарственного средства.
Настоящим изобретением дополнительно предложено применение вышеуказанного растительного экстракта или вышеуказанной фармацевтической композиции при получении лекарственного средства для регулировки кишечной флоры.
В еще одном аспекте настоящим изобретением предложен пищевой продукт, продукт медицинского назначения или напиток, который содержит вышеуказанный растительный экстракт и необязательное вспомогательное вещество, приемлемое для пищевого продукта, продукта медицинского назначения или напитка.
Настоящим изобретением дополнительно предложено применение вышеуказанного растительного экстракта при получении пищевого продукта, продукта медицинского назначения или напитка. Предпочтительно, пищевой продукт, продукт медицинского назначения или напиток представляет собой пищевой продукт, продукт медицинского назначения или напиток с гипогликемическим действием.
Растительное сырье по настоящему изобретению относится к растительному сырью, применяемому для экстракции, в том числе без ограничения к свежему или переработанному растению или свежим или переработанным частям растения.
В настоящем изобретении неочищенный растительный экстракционный раствор подвергают стадиям обработки, заключающимся в разделении на смоле, концентрировании и осаждении спиртом, что дает представленные далее положительные эффекты по сравнению с традиционными способами экстракции.
1. Значительно снижено содержание тяжелых металлов.
2. Масса этанола, применяемого в традиционном способе водной экстракции и осаждения спиртом, в ¼-5 раз превышает массу загруженного растительного сырья, тогда как количество этанола, применяемого в способе экстракции по настоящему изобретению, может составлять всего лишь 1/600 от массы загруженного растительного сырья, что значительно снижает количество применяемого этанола, в определенной степени снижает себестоимость, облегчает промышленное производство и повышает безопасность производственного процесса.
Краткое описание чертежей
На фигуре 1 показаны результаты теста растительных экстрактов, полученных в примерах 1, 2, 3, 5 и 6, на крысах на толерантность к сахарозе.
Подробное описание
Настоящее изобретение будет далее подробно описано в связи с прилагаемыми графическими материалами и примерами. Признаки и преимущества настоящего изобретения станут более понятными и определенными из данных иллюстративных описаний.
В настоящем документе специальный термин «иллюстративный» означает «используемый в качестве образца, или примера, или пояснения». Любой «иллюстративный» пример, представленный в настоящем документе, не обязательно должен истолковываться как превосходящий или лучший по сравнению с другими примерами.
Кроме того, технические признаки, задействованные в различных описанных ниже вариантах осуществления настоящего изобретения, можно комбинировать друг с другом, если они не противоречат друг другу.
Настоящее изобретение охватывает следующие способы обнаружения:
1. Определение содержания алкалоидов
Отбирали соответствующее количество экстракта и добавляли воду для его растворения с помощью ультразвука для получения тестируемого раствора. Наряду с этим, точно отвешивали соответствующее количество 1-дезоксиноиримицина в качестве эталонного образца и добавляли воду для его растворения с получением эталонного раствора. Точно отмеряли соответствующие объемы эталонного раствора и тестируемого раствора соответственно, добавляли растворы бикарбоната натрия и тщательно перемешивали встряхиванием. После этого добавляли раствор 9-флуоренилметоксикарбонилхлорида (FMOC-Cl) в ацетоне и нагревали при 30°С в течение 30 минут. Для прекращения реакции добавляли уксусную кислоту. Реакционную смесь тщательно перемешивали встряхиванием и подвергали фильтрации. Полученный в результате фильтрат точно отбирали и вводили впрыском в жидкостный хроматограф. По площади пика рассчитывали содержание 1-дезоксиноиримицина и содержание суммы алкалоидов в тестируемом образце способом расчета с внешним стандартом (рассчитывая хроматографические пики с относительным временем удержания в диапазоне от 0,4 до 1,7 в пересчете на 1-дезоксиноиримицин) (справочная литература: Xuejun XIA, Renyun WANG, Yuling LIU. "Determination of mulberry twig alkaloids by RP-HPLC with pre-column derivatization" [J]. Chinese Journal of New Drugs, 2008, 17(23): 2044-2047).
2. Определение содержания аминокислот
Отбирали соответствующее количество экстракта и добавляли воду для его растворения с помощью ультразвука для получения тестируемого раствора. Наряду с этим, точно отвешивали соответствующее количество смеси аминокислот в качестве эталонного образца и добавляли воду для его растворения с получением эталонного раствора. Остальные операции были такими же, как и при определении содержания алкалоидов.
3. Определение содержания полисахаридов
Точно отвешивали соответствующее количество экстракта, добавляли воду, экстрагировали ультразвуком и центрифугировали на 4000 об./мин в течение 10 мин. В качестве тестируемого раствора брали надосадочную жидкость. Отмеряли 2 мл вышеуказанного тестируемого раствора и помещали в пробирку с пробкой, в которую добавляли 6 мл 0,1% реагента антрон-серная кислота. Тестируемую пробирку нагревали на кипящей водяной бане в течение 15 минут и оставляли на ледяной бане на 15 минут. В качестве холостого опыта брали соответствующий реагент .Сразу же измеряли значение поглощения на 625 нм. Концентрацию полисахаридов в тестируемом образце по отношению к глюкозе рассчитывали по уравнению линейной регрессии глюкозы, а их содержание рассчитывали по следующему уравнению: Содержание = C*D*f/W, где W - масса образца, С - концентрация полисахарида по отношению к глюкозе, f - коэффициент преобразования (3,38), a D - коэффициент разведения (справочная литература: Zuofa ZHANG, Jie JIN, Liangen SHI. "Method for content determination of polysaccharide in Ramulus MorF, China Journal of Chinese Materia Medica [J]. 2018,33(4): 462-464).
4. Определение содержания флавонов
Взвешивали соответствующее количество эталонного образца рутина и растворяли в 60% этаноле с получением маточного эталонного раствора рутина. Точно отмеряли соответственно 0,5 мл, 1,0 мл, 3,0 мл, 5,0 мл и 7,0 мл эталонных исходных растворов рутина в мерные колбы на 25 мл, в которые добавляли соответственно 10 мл 5% раствора нитрита натрия, 10%) раствор нитрата алюминия и 1 н. раствор NaOH, а затем разводили водой до нужного масштаба и тщательно перемешивали встряхиванием в качестве эталонного раствора. В качестве эталона применяли холостой эталонный раствор. Значение поглощения измеряли на 500 нм и строили уравнение линейной регрессии.
Точно отвешивали соответствующее количество экстракта, растворяли в 60% растворе этанола с помощью ультразвука, тщательно перемешивали встряхиванием и центрифугировали на 4000 об./мин в течение 10 минут. После этого отбирали надосадочную жидкость в качестве раствора для экстракции флавонов. Точно отмеряли 2,0 мл растворов для экстракции флавонов, к которым добавляли соответственно 10 мл 5% раствора нитрита натрия, 10% раствор нитрата алюминия и 1 н. раствор NaOH, затем разводили водой до нужного масштаба, тщательно перемешивали встряхиванием, оставляли на 15 минут и центрифугировали на 5000 об./мин в течение 5 мин. После этого для определения измеряли надосадочную жидкость. Точно отмеряли еще 2,0 мл раствора для экстракции флавонов и разводили только водой до 25 мл в качестве холостого эталонного раствора в случае отсутствия цветной реакции. Значения поглощения реакционных растворов измеряли на 500 нм. Концентрации флавонов рассчитывали по уравнению линейной регрессии. Затем рассчитывали содержание флавонов в образце в пересчете на рутин по массе образца и кратности разведения.
5. Определение содержания тяжелых металлов
Общее содержание тяжелых металлов определяли вторым способом из раздела «Общие правила» 0821, из тома IV, Китайской фармакопеи, издания 2015 года. Конкретный способ заключался в следующем:
(1) Получение стандартного раствора свинца. Отвешивали 0,1599 г нитрата свинца и помещали в 1000-мл мерную колбу. После растворения с помощью 5 мл азотной кислоты и 50 мл воды раствор разводили водой до нужного масштаба и тщательно перемешивали встряхиванием в качестве маточного раствора. Точно отмеряли соответственно 0,5 мл, 1 мл, 2 мл, 5 мл и 8 мл маточных растворов в 5-мл мерные колбы, разводили водой до нужного масштаба и тщательно перемешивали встряхиванием, таким образом получая стандартные растворы свинца с концентрацией 5 ppm, 10 ppm, 20 ppm, 30 ppm, 40 ppm, 50 ppm и 80 ppm.
(2) Анализ образца. Брали 2 г образца, медленно прокаливали до полного обугливания, охлаждали, смачивали посредством точно 0,5-1 мл серной кислоты, нагревали при низкой температуре до полного удаления серной кислоты, добавляли 0,5 мл азотной кислоты, затем упаривали досуха, охлаждали после полного удаления паров оксида азота, прокаливали при температуре от 500°С до 600°С до полного озоления, охлаждали, добавляли 2 мл соляной кислоты и упаривали досуха на водяной бане с последующим добавлением 15 мл воды. По каплям добавляли раствор аммиака до тех пор, пока индикаторный раствор фенолфталеина не становился слегка розовым, а затем добавляли 2 мл ацетатного буфера (рН 3,5). После растворения материалов при слабом нагревании раствор переносили в пробирки Несслера и содержимое разводили водой по 25 мл в качестве тестируемых пробирок. Брали другой реагент для составления тестируемого раствора и упаривали досуха в фарфоровой посуде, затем добавляли 2 мл ацетатного буфера (рН 3,5) и 15 мл воды, растворяли с мягким нагревом, после этого переносили в пробирки Несслера, в которые добавляли определенное количество стандартного раствора свинца, описанного соответственно в (1), а затем разводили водой до 25 мл в качестве эталонных пробирок. Затем в тестируемые пробирки и эталонные пробирки добавляли соответственно по 2 мл тестируемого раствора тиоацетамида, тщательно перемешивали встряхиванием, оставляли на 2 минуты и одновременно помещали на белую бумагу. Тестируемые пробирки и эталонные пробирки осматривали в перспективе сверху вниз. Цвет в тестируемых пробирках сравнивали с цветом в эталонных пробирках для определения содержания тяжелых металлов в образцах.
Содержание тяжелых металлов, т.е. свинца, кадмия, ртути и мышьяка, также можно определить с помощью масс-спектрометрии с индукционной плазмой (способ ICP-MS), которая описана в «Общих правилах» 0412 из тома IV Китайской фармакопеи, издания 2015 года.
Результаты определения содержания тяжелых металлов сравнивались с данными, задокументированными в публикации «Стандарты "зеленой" торговли лекарственными растениями и препаратами для импорта и экспорта». В «Стандартах» сказано, что в растительных материалах, отварах, экстрактах и препаратах должно быть общее содержание тяжелых металлов ≤20,0 мг/кг, Pb≤5 мг/кг, Cd≤0,3 мг/кг, Hg≤2 мг/кг, Cu≤20,0 мг/кг и As≤2,0 мг/кг.
Авторы настоящего изобретения сравнивали два способа обнаружения тяжелых металлов. Из результатов было видно, что результаты обоих способов согласовывались, то есть содержание тяжелых металлов в растительных экстрактах, полученных способом по настоящему изобретению, соответствовало положениям «Стандартов "зеленой " торговли лекарственными растениями и препаратами для импорта и экспорта». Предпочтительно, содержание тяжелых металлов в растительных экстрактах, полученных способом по настоящему изобретению, составляет не более 20 ppm, более предпочтительно не более 10 ppm и еще более предпочтительно не более 5 ppm.
Пример 1
Брали и измельчали 100 г свежей шелковицы (Morus alba L.), затем за 2 раза добавляли 300 мл спиртовой воды и экстрагировали при кипячении в емкости с обратным холодильником каждый раз в течение 1 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ, в результате чего получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор содержал от 5 до 10 ppm тяжелых металлов, в том числе 5,44 ppm свинца, 0,38 ppm кадмия, 0,06 ppm ртути и 0,47 ppm мышьяка. Неочищенный экстракционный раствор концентрировали нагреванием до содержания твердого вещества 2%, выдерживали при 25°С и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 5 г сильнокислотной катионообменной смолы на основе стирола 732-го типа, промывали посредством 2,5 моль/л раствора соляной кислоты до рН элюата 3,5; промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 8,0; промывали посредством 2,5 моль/л раствора соляной кислоты до рН элюата 3,5; и затем промывали 3-кратным объемом колонки деионизированной водой для завершения активации. Концентрированный экстрагирующий раствор загружали, а затем элюировали посредством 3 л 0,1 моль/л аммиачной воды со скоростью элюирования 10 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Когда собранный раствор достигал 1 л, сбор прекращали. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 1,25 г макропористой и сильнощелочной анионообменной смолы на основе акрила типа D218, промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0; промывали посредством 1,5 моль/л раствора соляной кислоты до рН элюата 3,5; и промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0; и завершали активацию. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 1 л.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,0. Ее переносили в резервуар для осаждения спиртом и добавляли 25 г безводного этанола при скорости перемешивания мешалкой 100 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и сушили под вакуумом с получением экстракта.
Кроме того, подготавливали и экстрагировали свежие ветки тутового дерева, кору тутового дерева и листья тутового дерева (Morus alba L.). Способ и параметры экстракции были такими же, как описано выше. Содержание тяжелых металлов в неочищенных экстракционных растворах, полученных из веток тутового дерева, коры тутового дерева и листьев тутового дерева, составляло от 5 до 10 ppm, при этом содержание свинца составляло 5,51, 5,87 и 6,12 ppm соответственно, содержание кадмия составляло 0,37, 0,35 и 0,41 ppm соответственно, содержание ртути составляло 0,07, 0,08 и 0,06 ppm соответственно, содержание мышьяка составляло 0,57, 0,55 и 0,61 ppm соответственно.
Содержание компонентов и содержание тяжелых металлов в полученных экстрактах шелковицы, веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 1.

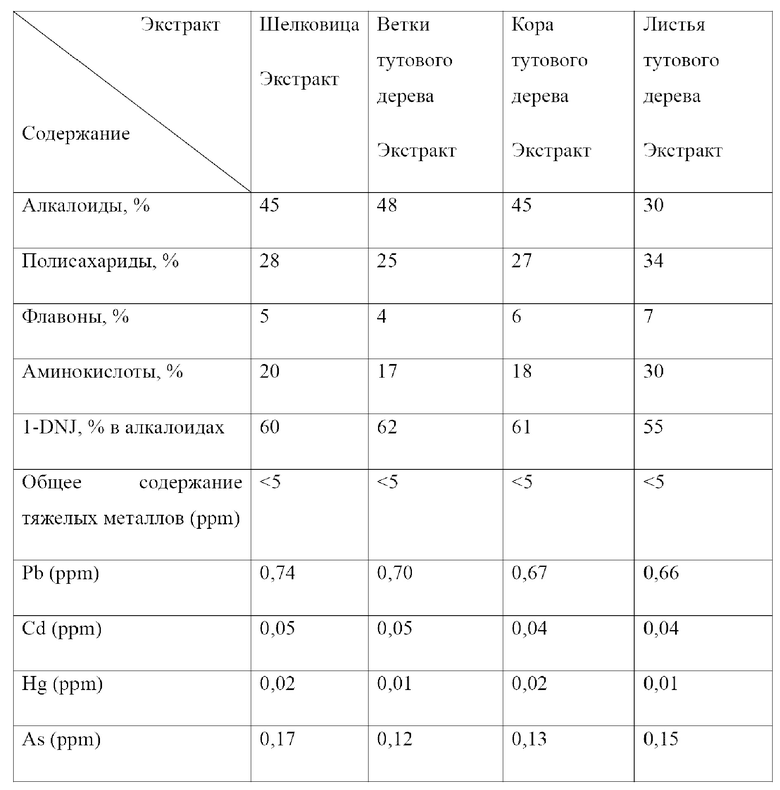
Пример 2
Брали и измельчали 100 г свежих листьев тутового дерева (Morus atropurpurea Roxb), затем за 2 раза добавляли 2000 мл кислой воды и экстрагировали способом отваривания каждый раз в течение 1 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ, в результате чего получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор содержал от 10 до 20 ppm тяжелых металлов, в том числе 13,6 ppm свинца, 0,84 ppm кадмия, 0,16 ppm ртути и 0,56 ppm мышьяка. Неочищенный экстракционный раствор центрифугировали для удаления примесей, а затем концентрировали фильтрованием через мембрану для обратного осмоса до тех пор, пока содержание твердого вещества не достигало 14,5%. Концентрированный неочищенный экстракционный раствор переносили в резервуар для осаждения спиртом и добавляли 80 г (приблизительно 100 мл) безводного этанола при скорости перемешивания мешалкой 300 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 10 г сильнокислотной катионообменной смолы на основе стирола 734-го типа, промывали посредством 2 моль/л раствора соляной кислоты до рН элюата 4,5; промывали посредством 1 моль/л раствора гидроксида натрия до рН элюата 8,5; промывали посредством 2 моль/л раствора соляной кислоты до рН элюата 4,5; и затем промывали 5-кратным объемом колонки деионизированной водой для завершения активации. Экстрагирующий раствор после концентрирования и осаждения спиртом загружали, а затем элюировали посредством 2 л 0,5 моль/л аммиачной воды со скоростью элюирования 8 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Когда собранный раствор достигал 800 мл, сбор прекращали. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 8 г сильнощелочной анионообменной смолы на основе стирола 717-го типа, промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0; промывали посредством 1,5 моль/л раствора соляной кислоты до рН элюата 3,5; и промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0 с завершением активации. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 750 мл.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,05. Ее переносили в резервуар для осаждения спиртом и добавляли 12,5 г безводного этанола при скорости перемешивания мешалкой 200 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и сушили под вакуумом с получением экстракта.
Кроме того, подготавливали и экстрагировали свежие ветки тутового дерева и кору тутового дерева (Morus atropurpurea Roxb). Способ и параметры экстракции были такими же, как описано выше. Содержание тяжелых металлов в неочищенных экстракционных растворах, полученных из веток тутового дерева и коры тутового дерева, составляло от 10 до 20 ppm, при этом содержание свинца составляло 14,5 и 15,8 ppm соответственно, содержание кадмия составляло 0,78 и 0,77 ppm соответственно, содержание ртути составляло 0,17 и 0,18 ppm соответственно, содержание мышьяка составляло 0,57 и 0,55 ppm соответственно.
Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 2.

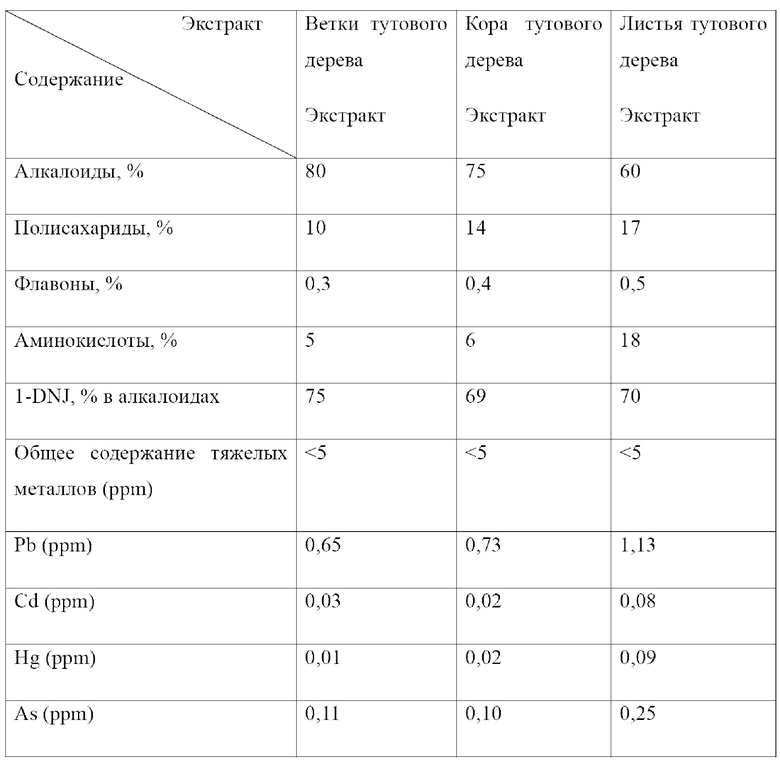
Пример 3
Брали и измельчали 1000 кг свежих веток тутового дерева (Yuesang №11), затем добавляли 4000 л воды и экстрагировали путем нагревания в емкости с обратным холодильником в течение 2 часов. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ, в результате чего получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор содержал от 40 до 80 ppm тяжелых металлов, в том числе 52 ppm свинца, 1,94 ppm кадмия, 0,88 ppm ртути и 1,11 ppm мышьяка. Неочищенный экстракционный раствор концентрировали нагреванием до содержания твердого вещества 4%, выдерживали при 50°С и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 150 кг макропористой и слабокислотной катионообменной смолы на основе фенилпропена типа D113, промывали посредством 2 моль/л раствора соляной кислоты до рН элюата 4,5; промывали посредством 1 моль/л раствора гидроксида натрия до рН элюата 8,5; промывали посредством 2 моль/л раствора соляной кислоты до рН элюата 4,5; и затем промывали 5-кратным объемом колонки деионизированной водой для завершения активации. Концентрированный экстрагирующий раствор загружали, а затем элюировали посредством 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Когда собранный раствор достигал 900 л, сбор прекращали. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 62,5 кг макропористой и сильнощелочной анионообменной смолы на основе акрила типа D218, промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0; промывали посредством 1,5 моль/л раствора соляной кислоты до рН элюата 3,5; и промывали посредством 1,5 моль/л раствора гидроксида натрия до рН элюата 9,0 с завершением активации. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 870 л.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, фильтровали через мембрану для микрофильтрации для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,1. Ее переносили в резервуар для осаждения спиртом и добавляли 15 кг безводного этанола при скорости перемешивания мешалкой 400 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Yuesang №11). Способ и параметры экстракции были такими же, как описано выше. Содержание тяжелых металлов в неочищенных экстракционных растворах, полученных из коры тутового дерева и листьев тутового дерева, составляло от 40 до 80 ppm, при этом содержание свинца составляло 48 и 53 ppm соответственно, содержание кадмия составляло 1,78 и 1,77 ppm соответственно, содержание ртути составляло 0,77 и 0,78 ppm соответственно, содержание мышьяка составляло 0,87 и 0,95 ppm соответственно.
Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 3.


Пример 4
Брали 1000 кг высушенной на воздухе коры тутового дерева (Guisangyou №62) и измельчали, затем за 2 раза добавляли 10000 л воды и экстрагировали при кипячении с обратным холодильником в течение 2,5 ч каждый раз. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ, в результате чего получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор содержал менее 5 ppm тяжелых металлов, в том числе 1,57 ppm свинца, 0,23 ppm кадмия, 0,09 ppm ртути и 0,58 ppm мышьяка. Неочищенный экстракционный раствор фильтровали через мембрану для микрофильтрации для удаления примесей, а затем концентрировали через мембрану для обратного осмоса до тех пор, пока содержание твердых веществ не достигало 6%, и он служил загрузочным раствором в колонку с катионообменной смолой.
В колонку загружали 100 кг макропористой и сильнокислотной катионообменной смолы на основе стирола типа D001. Катионообменную смолу активировали по способу, описанному в примере 3. Концентрированный экстрагирующий раствор загружали, а затем элюировали посредством 500 л 0,2 моль/л хлорида аммония со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 200 л. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 32 кг макропористой и сильнощелочной анионообменной смолы на основе стирола типа D201. Анионообменную смолу активировали по способу, описанному в примере 3. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 100 л.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,2. Ее переносили в резервуар для осаждения спиртом и добавляли 3 кг безводного этанола при скорости перемешивания мешалкой 350 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, готовили и экстрагировали высушенные на воздухе ветки тутового дерева (Guisangyou №62). Способ и параметры экстракции были такими же, как описано выше. Неочищенный экстракционный раствор, полученный из веток тутового дерева, содержал от 5 до 10 ppm тяжелых металлов, при этом содержание свинца составляло 1,66 ppm соответственно, содержание кадмия составляло 0,25 ppm соответственно, содержание ртути составляло 0,07 ppm соответственно, а содержание мышьяка составляло 0,60 ppm соответственно.
Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева и коры тутового дерева приведены в таблице 4.

Пример 5
Брали и измельчали 10 кг свежих веток тутового дерева (Sangteyou №2), затем за 2 раза добавляли 150 л кислой воды и экстрагировали способом отваривания каждый раз в течение 3 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ. Экстрагирующий раствор концентрировали нагреванием до тех пор, пока содержание твердых веществ не достигало 8%. Его переносили в резервуар для осаждения спиртом. Добавляли 2367,9 г безводного этанола (3 л) при перемешивании мешалкой со скоростью 300 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 5 кг сильнокислотной катионообменной смолы на основе стирола типа 002SC. Катионообменную смолу активировали по способу, описанному в примере 3. Экстрагирующий раствор после концентрирования и осаждения спиртом загружали, а затем элюировали посредством 100 л 5 моль/л хлорида калия со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 25 л. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 10 кг сильнощелочной анионообменной смолы на основе стирола 711-го типа. Анионообменную смолу активировали по способу, описанному в примере 3. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 15 л. Собранный раствор повторно загружали на катионообменную смолу и дважды разделяли последовательно через катионообменную смолу и анионообменную смолу в соответствии с описанными выше способами.
Собранный раствор, полученный после трех разделений на колонках, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,25. Ее переносили в резервуар для осаждения спиртом и добавляли 125 г безводного этанола при скорости перемешивания мешалкой 1000 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта. Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Sangteyou №2). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 5.


Пример 6
Брали и измельчали 1 кг свежих корней тутового дерева (Yuesang №11), затем за 3 раза добавляли 6 л спиртовой воды и экстрагировали с помощью ультразвуковой экстракции каждый раз в течение 1 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор служил загрузочным раствором для колонки с катионообменной смолой.
В колонку загружали 1 кг макропористой и сильнощелочной катионообменной смолы типа D254 четвертичноаммониевого типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством 15 л 3 моль/л хлорида натрия со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 5 л. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 1 кг макропористой и слабощелочной анионообменной смолы на основе стирола типа D301. Анионообменную смолу активировали по способу, описанному в примере 3. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 5 л. Собранный раствор повторно загружали на катионообменную смолу и еще раз разделяли последовательно через катионообменную смолу и анионообменную смолу в соответствии с описанными выше способами.
Собранный раствор, полученный после двух разделений на колонках, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,2. Ее переносили в резервуар для осаждения спиртом и добавляли 6,3 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта. Кроме того, подготавливали и экстрагировали свежие ветки тутового дерева и листья тутового дерева (Yuesang №11). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, листьев тутового дерева и корней тутового дерева приведены в таблице 6.

Пример 7
Брали и измельчали 1000 кг свежих веток тутового дерева (Morus atropurpurea Roxb), затем добавляли 11500 л воды и экстрагировали путем нагревания в емкости с обратным холодильником в течение 2 часов. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса до тех пор, пока содержание твердых веществ не достигало 1%, и он служил загрузочным раствором в колонку с катионообменной смолой.
В колонку загружали 150 кг макропористой и сильнокислотной катионообменной смолы на основе стирола типа D001. Катионообменную смолу активировали по способу, описанному в примере 3. Концентрированный неочищенный экстракционный раствор загружали и элюировали посредством 5000 л 0,04 моль/л нитрата аммония со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 1000 л.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали через мембрану для нанофильтрации. Удельный вес концентрированной жидкости составлял 1,3. Ее переносили в резервуар для осаждения спиртом и добавляли 1,7 кг безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Morus atropurpurea Roxb). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 7.

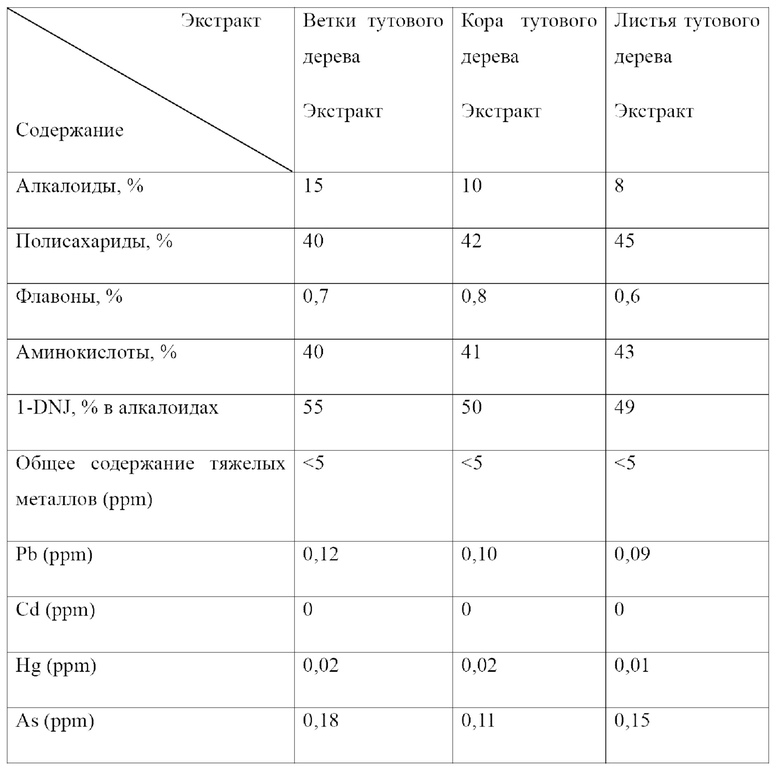
Пример 8
Брали и измельчали 1000 кг свежих веток тутового дерева (Yuesang №11), затем за 2 раза добавляли 8000 л кислой воды и экстрагировали способом отваривания каждый раз в течение 2 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор фильтровали через мембрану для микрофильтрации для удаления примесей, затем концентрировали через мембрану для обратного осмоса до тех пор, пока содержание твердых веществ не достигало 1%, и он служил загрузочным раствором в колонку с катионообменной смолой.
В колонку загружали 41,7 кг сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали и элюировали посредством 1000 л 0,1 моль/л хлорида натрия со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 500 л.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали посредством мембраны для нанофильтрации. Удельный вес концентрированной жидкости составлял 1,25. Ее переносили в резервуар для осаждения спиртом и добавляли 15 кг безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Yuesang №11). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 8.

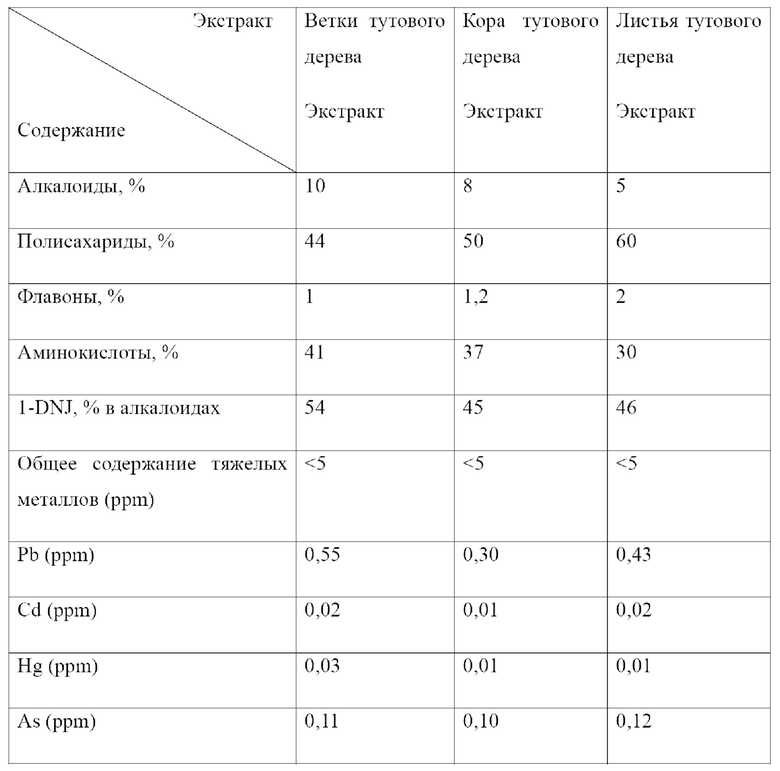
Пример 9
Брали и измельчали 100 г свежих веток тутового дерева (Moms atropurpurea Roxb), затем добавляли 600 мл воды, экстрагировали путем нагревания в емкости с обратным холодильником в течение 1 часа и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор сначала концентрировали нагреванием до содержания твердого вещества 5% и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 3,85 г сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали и элюировали посредством 700 мл 0,15 моль/л хлорида аммония со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 100 мл.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,3. Ее переносили в резервуар для осаждения спиртом и добавляли 25 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Morus atropurpurea Roxb). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 9.

Пример 10
Брали и измельчали 1000 кг свежих веток тутового дерева (Sangteyou №2), затем добавляли 5000 л воды, экстрагировали путем нагревания в емкости с обратным холодильником в течение 1 часа и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор сначала концентрировали нагреванием до содержания твердого вещества 10% и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 3,5 г макропористой и сильнощелочной катионообменной смолы D254 четвертичноаммониевого типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством 200 л 0,15 моль/л хлорида калия со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 100 л.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,05. Ее переносили в резервуар для осаждения спиртом и добавляли 15 кг безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева (Sangteyou №2). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева приведены в таблице 10.


Пример 11
Брали и измельчали 1000 г свежих веток тутового дерева (Morus bombycis Koidz.), затем за 3 раза добавляли Юл кислой воды, экстрагировали путем под ультразвуком в течение 2 часов каждый раз и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор фильтровали через мембрану для микрофильтрации для удаления примесей, затем концентрировали через мембрану для обратного осмоса до тех пор, пока содержание твердых веществ не достигало 4% и использовали в качестве загрузочного раствора в колонку с катионообменной смолой.
В колонку загружали 66,67 г макропористой и сильнокислотной катионообменной смолы на основе стирола типа D001. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством 12 л 1,5 моль/л аммиачной воды со скоростью элюирования 5 BV/h. Элюат собирали, когда с помощью высокоэффективной жидкостной хроматографии определяли, что поток, выходящий из колонки с катионообменной смолой, содержит алкалоиды. Сбор прекращали, когда объем собранного раствора составлял до 100 мл. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 13,3 г макропористой и сильнощелочной анионообменной смолы на основе стирола типа D218. Анионообменную смолу активировали по способу, описанному в примере 3. Элюат, собранный с катионообменной смолы, загружали на колонку с анионообменной смолой. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 50 мл.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, фильтровали через мембрану для микрофильтрации для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,15. Ее переносили в резервуар для осаждения спиртом и добавляли 25 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
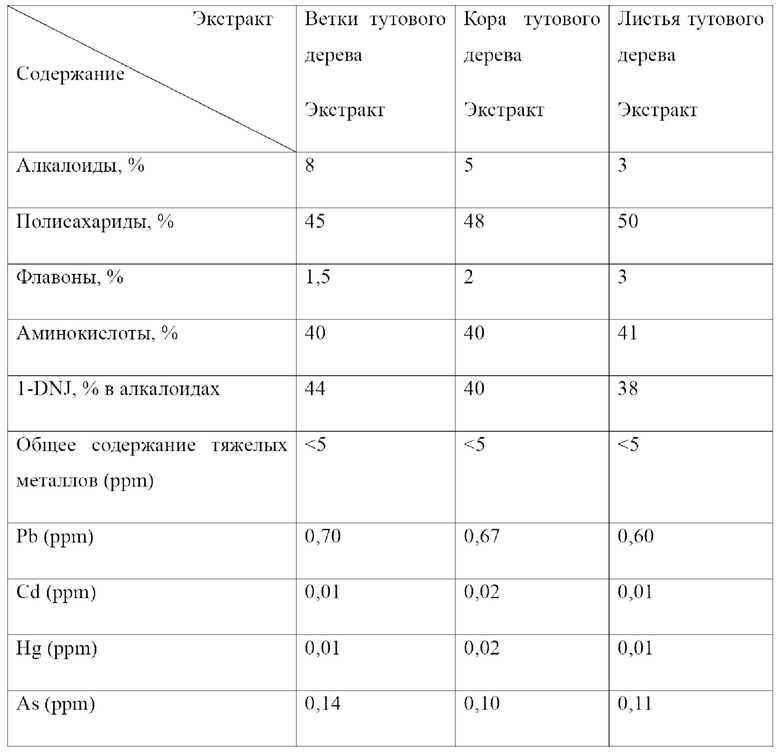
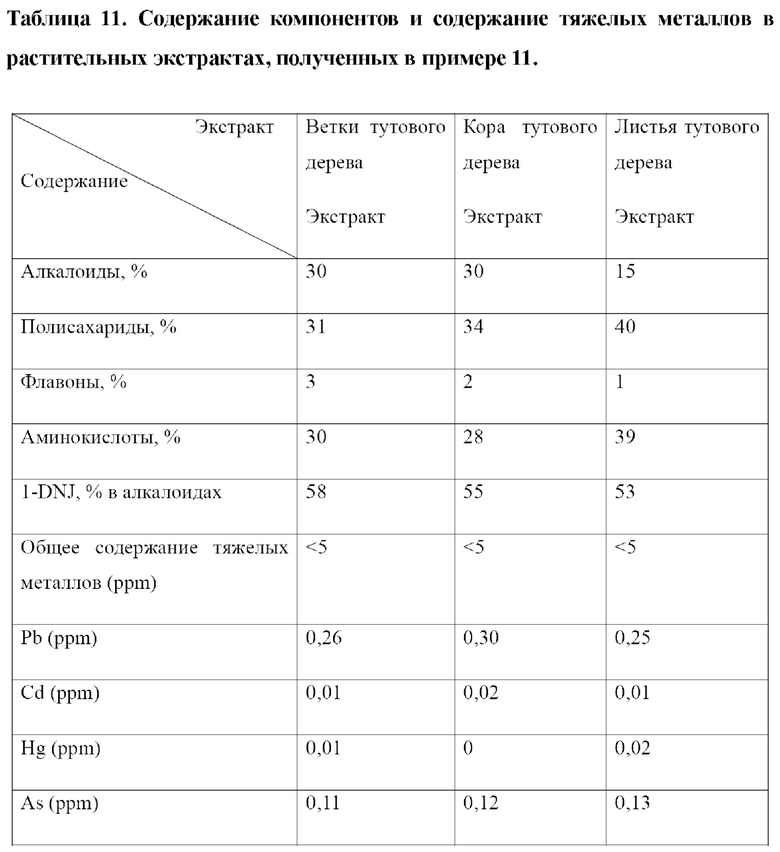
Кроме того, подготавливали и экстрагировали свежую кору тутового дерева и листья тутового дерева (Morus bombycis Koidz.). Способ и параметры экстракции были такими же, как описано выше. Содержание компонентов и содержание тяжелых металлов в полученных экстрактах веток тутового дерева, коры тутового дерева и листьев тутового дерева приведены в таблице 11.
Пример 12
Брали и измельчали 100 г свежей коры тутового дерева (Guisangyou №62), затем добавляли 1,2 л спиртовой воды, экстрагировали способом отваривания в течение 1 часа и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор сначала концентрировали нагреванием до содержания твердого вещества 8% и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 33,34 г сильнокислотной катионообменной смолы на основе стирола 734-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством 50 мл 2,5 моль/л аммиачной воды со скоростью элюирования 5 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Сбор прекращали, когда объем собранного раствора составлял до 10 мл.
Собранный раствор, полученный после разделения на колонке с катионообменной смолой, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,2. Ее переносили в резервуар для осаждения спиртом и добавляли 15 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
В экстракте коры тутового дерева содержание алкалоидов составляло 15%, содержание полисахаридов составляло 38%, содержание флавонов составляло 2%, содержание аминокислот составляло 40%. В алкалоидах содержание 1-DNJ составляло 52%.
Общее содержание тяжелых металлов составляло менее 5 ppm, в том числе 0,29 ppm свинца, 0 ppm кадмия, 0,02 ppm ртути и 0,10 ppm мышьяка.
Пример 13
Брали и измельчали 100 г свежих веток тутового дерева (Morus alba L.), затем добавляли 300 мл щелочной воды, экстрагировали путем нагревания в емкости с обратным холодильником в течение 0,5 часа и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса до тех пор, пока содержание твердых веществ не достигало 6% и использовали в качестве загрузочного раствора в колонку с катионообменной смолой.
В колонку загружали 3,34 г сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством Зл 1,0 моль/л аммиачной воды со скоростью элюирования 5 BV/h. Вытекающий поток определяли с помощью 20% кремнийвольфрамовой кислоты и начинали собирать, когда образовывался белый осадок. Сбор прекращали, когда объем собранного раствора достигал 400 мл.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,25. Ее переносили в резервуар для осаждения спиртом и добавляли 5 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
В полученном экстракте веток тутового дерева содержание алкалоидов составляло 3%, содержание полисахаридов составляло 60%, содержание флавонов составляло 5%, содержание аминокислот составляло 30%. В алкалоидах содержание 1-DNJ составляло 47%.
Общее содержание тяжелых металлов составляло менее 5 ppm, в том числе 0,31 ppm свинца, 0 ppm кадмия, 0,01 ppm ртути и 0,14 ppm мышьяка.
Пример 14
Брали и измельчали 100 г свежих листьев тутового дерева (Morus multicaulis Perrott.), затем добавляли 500 мл спиртовой воды, экстрагировали способом отваривания в течение 0,5 часа и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор концентрировали посредством мембраны для нанофильтрации до содержания твердого вещества 12% и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 25 г сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Неочищенный экстракционный раствор загружали, а затем элюировали посредством 2 л 2,0 моль/л аммиачной воды со скоростью элюирования 5 BV/h. Элюат собирали, когда с помощью высокоэффективной жидкостной хроматографии определяли, что поток, выходящий из колонки с катионообменной смолой, содержит алкалоиды. Сбор прекращали, когда объем собранного раствора составлял до 800 мл.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,14. Ее переносили в резервуар для осаждения спиртом и добавляли 5 г безводного этанола при скорости перемешивания мешалкой 600 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали под пониженным давлением с получением экстракта.
В полученном экстракте листьев тутового дерева содержание алкалоидов составляло 10%, содержание полисахаридов составляло 43%, содержание флавонов составляло 1%, содержание аминокислот составляло 37%. В алкалоидах содержание 1-DNJ составляло 50%.
Общее содержание тяжелых металлов составляло менее 5 ppm, в том числе 0,33 ppm свинца, 0,01 ppm кадмия, 0,02 ppm ртути и 0,15 ppm мышьяка.
Пример 15
Брали и измельчали 100 г свежих луковиц гиацинта восточного (Hyacinthus orientalis), затем за 2 раза добавляли 700 мл воды и экстрагировали под ультразвуком в течение 0,5 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ с получением неочищенного экстракционного раствора. Неочищенный экстракционный раствор концентрировали посредством мембраны для нанофильтрации до содержания твердого вещества 10% и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 3,5 г сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Концентрированный неочищенный экстракционный раствор загружали и элюировали посредством 10 мл 1,75 моль/л раствора гидроксида натрия со скоростью элюирования 10 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Сбор прекращали, когда объем собранного раствора составлял до 10 мл. Собранный раствор очищали непосредственно на колонке с анионообменной смолой.
В колонку загружали 4 г макропористой и сильнощелочной анионообменной смолы на основе стирола типа D218. Анионообменную смолу активировали по способу, описанному в примере 3. Элюат, собранный с катионообменной смолы, загружали на анионообменную смолу. Собирали выходящий поток и сбор прекращали, когда объем выходящего потока достигал 5 мл.
Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,1. Ее переносили в резервуар для осаждения спиртом и добавляли 0,4 г безводного этанола при скорости перемешивания мешалкой 100 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и сушили под вакуумом с получением экстракта луковиц гиацинта восточного.
В полученном экстракте луковиц гиацинта восточного содержание алкалоидов составляло 3%, содержание полисахаридов составляло 68%, содержание флавонов составляло 2%, содержание аминокислот составляло 25%.
В алкалоидах содержание 1-DNJ составляло 30%.
Общее содержание тяжелых металлов не превышало 5 ppm, в том числе 0,08 ppm свинца, 0,01 ppm ртути и 0,15 ppm мышьяка, кадмий обнаружен не был.
Пример 16
Брали и измельчали 100 г свежих листьев коммелины обыкновенной (Commelina communi), затем за 2 раза добавляли 500 мл спиртовой воды и экстрагировали при кипячении в емкости с обратным холодильником каждый раз в течение 1 ч. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ. Экстрагирующий раствор концентрировали нагреванием до содержания твердого вещества 10%, выдерживали при 30°С и использовали в качестве загрузочного раствора для колонки с катионообменной смолой.
В колонку загружали 3,5 г сильнокислотной катионообменной смолы на основе стирола 732-го типа. Катионообменную смолу активировали по способу, описанному в примере 3. Концентрированный экстрагирующий раствор загружали, а затем элюировали посредством 800 мл 2,3 моль/л аммиачной воды со скоростью элюирования 10 BV/h. Элюат собирали, когда было обнаружено, что поток, выходящий из колонки с катионообменной смолой, имеет рН>7. Сбор прекращали, когда объем собранного раствора составлял до 300 мл.
Собранный раствор, полученный в результате разделения на колонке с катионообменной смолой, фильтровали через мембрану для ультрафильтрации для удаления примесей, а затем концентрировали через мембрану для обратного осмоса. Удельный вес концентрированной жидкости составлял 1,2. Ее переносили в резервуар для осаждения спиртом и добавляли 5 г безводного этанола при скорости перемешивания мешалкой 500 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и сушили под вакуумом с получением экстракта листьев коммелины обыкновенной.
В полученном экстракте листьев коммелины обыкновенной содержание алкалоидов составляло 10%, содержание полисахаридов составляло 27%, содержание флавонов составляло 10%), содержание аминокислот составляло 50%.
В алкалоидах содержание 1-DNJ составляло 50%.
Общее содержание тяжелых металлов не превышало 5 ppm, в том числе 0,05 ppm свинца и 0,17 ppm мышьяка, кадмий и ртуть обнаружены не были.
Сравнительный пример 1
Брали 1000 кг свежих веток тутового дерева (Morus serrata Roxb.) из той же партии, что и в примере 3, и подвергали грубой экстракции в соответствии со способом, описанным в примере 3. Неочищенный экстракционный раствор концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,1. Ее переносили в резервуар для осаждения спиртом и добавляли 62 кг безводного этанола при скорости перемешивания мешалкой 400 об./мин.
После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали при пониженном давлении с получением экстракта веток тутового дерева. Содержание алкалоидов составляло 15%, содержание полисахаридов составляло 40%, содержание флавонов составляло 5,2%, содержание аминокислот составляло 30%.
В алкалоидах содержание 1-DNJ составляло 55%.
Общее содержание тяжелых металлов составляло от 30 до 40 ppm, в том числе 29,11 ppm свинца, 1,50 ppm кадмия, 0,76 ppm ртути, 1,01 ppm мышьяка, при этом содержание свинца, кадмия и ртути превышало нормы содержания.
Без стадий разделения на колонке с катионообменной смолой и колонке с анионообменной смолой в данном сравнительном примере наблюдали пониженное содержание алкалоидов, значительно повышенное содержание тяжелых металлов и 3-кратное увеличение количества этанола по сравнению с примером 3.
Сравнительный пример 2
Отвешивали 1000 кг свежих веток тутового дерева (Moms serrata Roxb.) из той же партии, что и в примере 3, и подвергали грубой экстракции, концентрированию при нагревании и разделении посредством катионообменной смолы и анионообменной смолы в соответствии со способом, описанным в примере 3. 870 л собранного раствора, полученного в результате разделения на колонке с анионообменной смолой, переносили в резервуар для осаждения спиртом и добавляли 135 кг безводного этанола при скорости перемешивания мешалкой 400 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали при пониженном давлении с получением экстракта веток тутового дерева. Содержание алкалоидов составляло 62%, содержание полисахаридов составляло 18%, содержание флавонов составляло 1,1%, содержание аминокислот составляло 12%.
В алкалоидах содержание 1-DNJ составляло 68%.
Общее содержание тяжелых металлов составляло от 10 до 20 ppm, в том числе 10,01 ppm свинца, 0,70 ppm кадмия, 0,44 ppm ртути, 0,83 ppm мышьяка, при этом содержание свинца, кадмия и ртути превышало нормы содержания.
Без стадии концентрирования между разделением на смоле и осаждением спирта в данном сравнительном примере наблюдали повышенное содержание тяжелых металлов и 8-кратное увеличение количества этанола по сравнению с примером 3.
Сравнительный пример 3
Отвешивали 1000 кг свежих веток тутового дерева (Morus serrata Roxb.) из той же партии, что и в примере 3, и подвергали грубой экстракции, концентрированию при нагревании и разделении посредством катионообменной смолы и анионообменной смолы в соответствии со способом, описанным в примере 3. 870 л собранного раствора, полученного в результате разделения на колонке с анионообменной смолой, концентрировали при пониженном давлении с получением экстракта веток тутового дерева. Содержание алкалоидов составляло 52%, содержание полисахаридов составляло 22%, содержание флавонов составляло 0,8%, содержание аминокислот составляло 20%.
В алкалоидах содержание 1-DNJ составляло 60%.
Общее содержание тяжелых металлов составляло от 20 до 40 ppm, в том числе 22,15 ppm свинца, 1,45 ppm кадмия, 0,65 ppm ртути, 0,89 ppm мышьяка, при этом содержание свинца, кадмия и ртути превышало нормы содержания.
Без стадии осаждения спиртом после разделения на смоле в данном сравнительном примере наблюдали пониженное содержание алкалоидов и значительно повышенное содержание тяжелых металлов по сравнению с примером 3.
Сравнительный пример 4
Брали и измельчали 1000 кг свежих веток тутового дерева (Morus serrata Roxb.) из той же партии, что и в примере 3, затем добавляли 4-кратный объем спиртовой воды (4000 л) и экстрагировали путем нагревания в емкости с обратным холодильником в течение 2 часов. Экстрагирующие растворы объединяли и фильтровали для удаления нерастворимых веществ. Неочищенный экстракционный раствор концентрировали при нагревании. Удельный вес концентрированной жидкости составлял 1,1. Ее переносили в резервуар для осаждения спиртом и добавляли 62 кг безводного этанола при скорости перемешивания мешалкой 400 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и загружали на катионообменную смолу. В соответствии со способом, описанным в примере 3, в колонку загружали 150 кг катионообменной смолы и подвергали разделению на катионообменной смоле и разделению на анионообменной смоле. Собранный раствор, полученный в результате разделения на колонке с анионообменной смолой, концентрировали при пониженном давлении с получением экстракта веток тутового дерева. Содержание алкалоидов составляло 51%, содержание полисахаридов составляло 25%, содержание флавонов составляло 0,5%, содержание аминокислот составляло 20%.
В алкалоидах содержание 1-DNJ составляло 55%.
Общее содержание тяжелых металлов составляло от 10 до 20 ppm, в том числе 11,11 ppm свинца, 0,82 ppm кадмия, 0,50 ppm ртути, 0,53 ppm мышьяка, при этом содержание свинца, кадмия и ртути превышало нормы содержания.
В данном сравнительном примере осуществляли осаждение спиртом перед стадией разделения на катионообменной смоле и наблюдали пониженное содержание алкалоидов, повышенное содержание тяжелых металлов и 3-кратное увеличение количества этанола по сравнению с примером 3.
Сравнительный пример 5
Брали 1000 кг свежих веток тутового дерева (Morus serrata Roxb.) из той же партии, что и в примере 3, и подвергали грубой экстракции и концентрированию при нагревании в соответствии со способом, описанным в примере 3. Концентрированный неочищенный экстракционный раствор загружали непосредственно на анионообменную смолу и подвергали разделению на анионообменной смоле в соответствии со способом, описанным в примере 3. Собирали 3000 л выходящего потока. Собранный раствор, полученный после разделения на колонке с анионообменной смолой, центрифугировали для удаления примесей, а затем концентрировали посредством мембраны для нанофильтрации. Удельный вес концентрированной жидкости составлял 1,1. Ее переносили в резервуар для осаждения спиртом и добавляли 46 кг безводного этанола при скорости перемешивания мешалкой 400 об./мин. После добавления этанола перемешивание раствора прекращали и подвергали его осаждению спиртом в течение 24 часов. Отбирали надосадочную жидкость и концентрировали при пониженном давлении с получением экстракта веток тутового дерева.
В экстракте веток тутового дерева содержание алкалоидов составляло 40%, содержание полисахаридов составляло 35%, содержание флавонов составляло 1,5%, содержание аминокислот составляло 22%.
В алкалоидах содержание 1-DNJ составляло 50%.
Общее содержание тяжелых металлов составляло от 30 до 40 ppm, в том числе 30,01 ppm свинца, 1,24 ppm кадмия, 0,21 ppm ртути, 0,85 ppm мышьяка, при этом содержание свинца, кадмия и ртути превышало нормы содержания.
Без стадии разделения на катионообменной смоле в данном сравнительном примере наблюдали пониженное содержание алкалоидов, значительно повышенное содержание тяжелых металлов и 2-кратное увеличение количества этанола по сравнению с примером 3.
Тестовый пример 1. Исследование стабильности
Экстракт шелковицы, полученный в примере 1, экстракты листьев тутового дерева, полученные в примерах 2, 8 и 9, экстракты веток тутового дерева, полученные в примерах 3 и 5-7, и экстракты коры тутового дерева, полученные в примерах 4 и 10, упаковывали в пакеты из композитной пленки и запечатывали, затем выдерживали 24 месяца при температуре 25°С±2°С и относительной влажности 60%±10%, после чего проверяли содержание в них алкалоидов. Результаты приведены в представленной ниже таблице 1.

Из таблицы 1 видно, что растительные экстракты, полученные способом экстракции по настоящему изобретению, обладают хорошей стабильностью.
Тестовый пример 2. Остаточные органические растворители
Использовали газовую хроматографию для обнаружения остаточной смолы, в том числе н-гексана, метилциклогексана, дивинилбензола, толуола, бензола, ксилола и стирола. Тестировали растительные экстракты, полученные в примерах 1-9, и ни один из них не содержал остаточной смолы.
Тестовый пример 3. Тест на эффективность
Нормальных самцов мышей ICR случайным образом разделяли на 6 групп (n=10) в зависимости от массы тела и не кормили в течение ночи перед тестированием. Одной из групп перорально вводили растворы сахарозы (4,0 г/кг) в качестве контрольной группы (норма), в то время как остальным 5 группам перорально вводили сахарозу, а также образец экстракта коры тутового дерева, полученного в примере 1, образец экстракта листьев тутового дерева, полученного в примере 2, и образцы экстракта веток тутового дерева, полученного в примерах 3, 5 и 6 (10 мг/кг каждого в пересчете на общее количество алкалоидов), в качестве групп введения. Измеряли уровни глюкозы в крови до введения (0 мин) и через 30 мин, 60 мин и 120 мин после введения. Строили кривую зависимости уровня глюкозы в крови от времени и рассчитывали площадь под кривой (AUC) уровня глюкозы в крови. Результаты были такими, как показано на фиг.1.
Из результатов видно, что растительные экстракты, полученные способом экстракции из растений по настоящему изобретению, приводят к значимому снижению повышения уровня глюкозы в крови у нормальных мышей после нагрузки сахарозой.
Настоящее изобретение выше было объяснено на основе предпочтительных вариантов осуществления, которые, тем не менее, являются лишь иллюстративными и демонстративными. Исходя из этого, в настоящее изобретение могут быть внесены различные замены и усовершенствования, и все они подпадают под объем защиты настоящего изобретения.
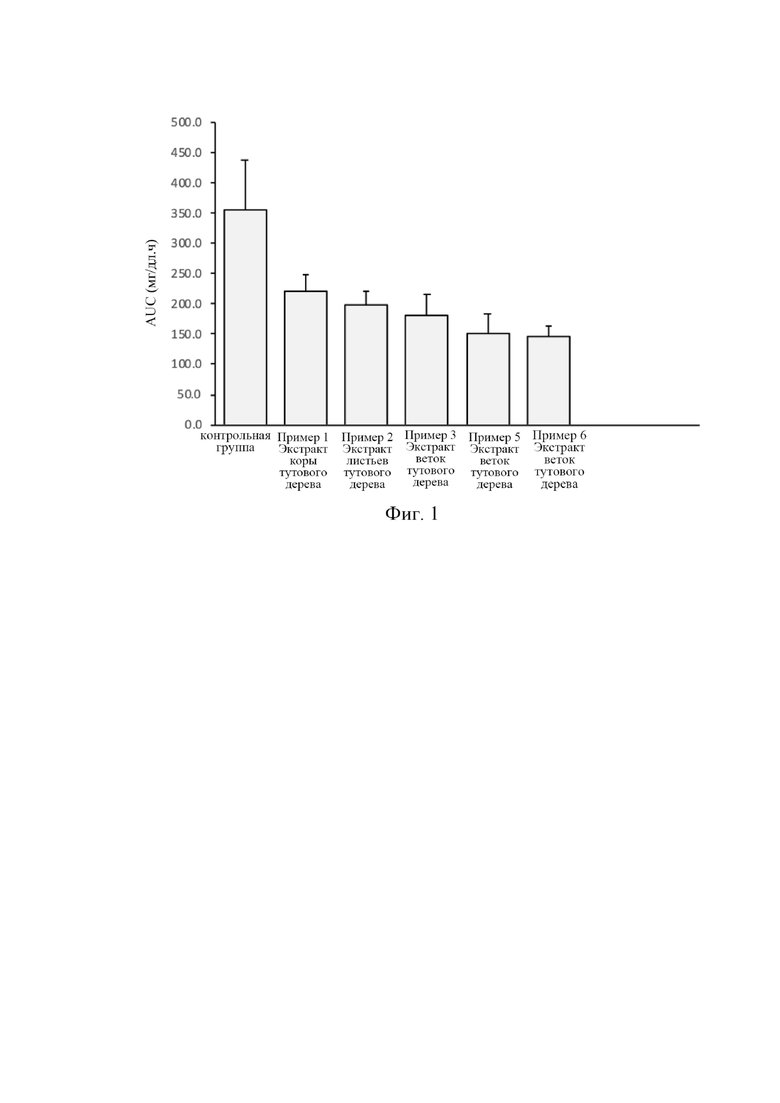
Группа изобретений относится к фармацевтической промышленности, а именно к способу получения экстракта, и к средствам на основе такого экстракта для снижения повышения уровня глюкозы в крови. Способ экстракции из растений, предусматривающий следующие стадии: стадия 1): получение неочищенного экстракционного раствора из растений путем применения растительного сырья с добавлением воды, спиртовой воды или кислой воды и экстрагирования кипячением в емкости с обратным холодильником, способом отваривания или с помощью ультразвуковой экстракции, и концентрирования неочищенного растительного экстракционного раствора; стадия 2): разделение концентрированного неочищенного экстракционного раствора с помощью катионообменной смолы и анионообменной смолы с получением собранного раствора, причем: катионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнокислотной катионообменной смолы, слабокислотной катионообменной смолы и сильнощелочной катионообменной смолы четвертичноаммониевого типа; количества применяемой катионообменной смолы и растительного сырья имеют массовое соотношение в диапазоне от 1:1 до 1:30; элюент для катионообменной смолы представляет собой солевой раствор, содержащий катионы, или щелочной раствор, содержащий катионы, причем катионы в элюенте имеют концентрацию в диапазоне от 0,04 до 5 моль/л, причем сбор с катионобменной смолы начинают, когда рН выходящего потока превышает 7, или начальную точку сбора выходящего потока определяют в соответствии со свойствами разделяемых компонентов с использованием реакции осаждения, и сбор с катионобменной смолы прекращают, когда объем собранного раствора достигает 0,1-10-кратной массы растительного сырья; масса элюента, применяемого при разделении с помощью катионообменной смолы, 0,1-30-кратна массе растительного сырья, анионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнощелочной анионообменной смолы и слабощелочной анионообменной смолы; и количества применяемой анионообменной смолы и растительного сырья имеют массовое соотношение в диапазоне от 1:1 до 1:80; сбор с анионобменной смолы прекращают, когда объем собранного раствора достигает 0,05-10-кратной массы растительного сырья; стадия 3): концентрирование собранного раствора, полученного на стадии 2); стадия 4): осаждение концентрированного раствора, полученного на стадии 3), спиртом с использованием этанола в качестве спирта, причем этанол, применяемый для осаждения спиртом, и растительное сырье имеют массовое соотношение в диапазоне от 1:4 до 1:600; и необязательно, стадия 5): концентрирование и сушка, причем растение представляет собой растение Morus, причем растительный экстракт, полученный способом экстракции из растений, содержит каждый компонент в следующих массовых соотношениях по отношению к общей массе растительного экстракта: от 30% до 99% алкалоидов; от 0,2% до 35% полисахаридов; от 0,05% до 2% флавонов; от 0% до 25% аминокислот и от 0% до 20% других компонентов; причем содержание тяжелых металлов в растительном экстракте составляет не более 10 ppm. Растительный экстракт, снижающий уровень глюкозы в крови, полученный вышеописанным способом. Фармацевтическая композиция для снижения повышения уровня глюкозы в крови, содержащая вышеописанный растительный экстракт. Применение растительного экстракта или фармацевтической композиции при получении гипогликемического лекарственного средства. Продукт медицинского назначения для снижения повышения уровня глюкозы в крови, содержащий растительный экстракт. Применение растительного экстракта при получении продукта медицинского назначения для снижения повышения уровня глюкозы в крови. Вышеописанный способ получения экстракта позволяет эффективно снизить содержание тяжелых металлов в растительных экстрактах, при этом значительно уменьшив количество этанола, применяемого в способе экстракции, тем самым улучшив качество продукта при одновременном снижении производственных затрат и до определенной степени повышения эффективности и безопасности промышленного производства. 6 н. и 5 з.п. ф-лы, 1 ил., 12 табл., 14 пр.
1. Способ экстракции из растений, предусматривающий следующие стадии:
стадия 1): получение неочищенного экстракционного раствора из растений путем применения растительного сырья с добавлением воды, спиртовой воды или кислой воды и экстрагирования кипячением в емкости с обратным холодильником, способом отваривания или с помощью ультразвуковой экстракции, и концентрирования неочищенного растительного экстракционного раствора;
стадия 2): разделение концентрированного неочищенного экстракционного раствора с помощью катионообменной смолы и анионообменной смолы с получением собранного раствора, причем:
катионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнокислотной катионообменной смолы, слабокислотной катионообменной смолы и сильнощелочной катионообменной смолы четвертичноаммониевого типа;
количества применяемой катионообменной смолы и растительного сырья имеют массовое соотношение в диапазоне от 1:1 до 1:30;
элюент для катионообменной смолы представляет собой солевой раствор, содержащий катионы, или щелочной раствор, содержащий катионы, причем катионы в элюенте имеют концентрацию в диапазоне от 0,04 до 5 моль/л;
причем сбор с катионобменной смолы начинают, когда рН выходящего потока превышает 7, или начальную точку сбора выходящего потока определяют в соответствии со свойствами разделяемых компонентов с использованием реакции осаждения, и сбор с катионобменной смолы прекращают, когда объем собранного раствора достигает 0,1-10-кратной массы растительного сырья;
масса элюента, применяемого при разделении с помощью катионообменной смолы, 0,1-30-кратна массе растительного сырья,
анионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнощелочной анионообменной смолы и слабощелочной анионообменной смолы; и
количества применяемой анионообменной смолы и растительного сырья имеют массовое соотношение в диапазоне от 1:1 до 1:80;
сбор с анионобменной смолы прекращают, когда объем собранного раствора достигает 0,05-10-кратной массы растительного сырья;
стадия 3): концентрирование собранного раствора, полученного на стадии 2);
стадия 4): осаждение концентрированного раствора, полученного на стадии 3), спиртом с использованием этанола в качестве спирта, причем этанол, применяемый для осаждения спиртом, и растительное сырье имеют массовое соотношение в диапазоне от 1:4 до 1:600; и
необязательно стадия 5): концентрирование и сушка,
причем растение представляет собой растение Morus,
причем растительный экстракт, полученный способом экстракции из растений, содержит каждый компонент в следующих массовых соотношениях по отношению к общей массе растительного экстракта: от 30% до 99% алкалоидов; от 0,2% до 35% полисахаридов; от 0,05% до 2% флавонов; от 0% до 25% аминокислот; и от 0% до 20% других компонентов; причем содержание тяжелых металлов в растительном экстракте составляет не более 10 ppm.
2. Способ экстракции по п. 1, причем растение представляет собой любое растение или их комбинацию, выбранное из Morus multicaulis Perrott., Morus alba L., Morus atropurpurea Roxb, Morusmizuho Hotta, Morus wittiorum Hand Mazz., Morus laevigata Wall, Morus nigra Linn., Morus cathayana Hemsi., Morus serrata Roxb., Morus mongolica Schneid., Morus bombycis Koidz., Morus noiabilis Schneid., Morus nigriformis Koidz., Morusyunnanensis Koidz., Morus australis Poir., Morus mongolica (Bur.) Schneid var. diabolica Koidz., Morus alba L. var. macrophylla loud, Morus alba var. Pendula Dippel, Morus alba L. var. venosa Delili, сорта тутового дерева, выведенного из указанных выше видов тутового дерева, гибрида тутового дерева, полученного в результате избирательной внутривидовой и межвидовой селекции вышеперечисленных видов тутового дерева; предпочтительно, растение представляет собой Morus atropurpurea Roxb, Morus multicaulis Perrott., Morus alba L., Morus serrata Roxb., Morus bombycis Koidz. или гибрид тутового дерева, гибрид тутового дерева предпочтительно представляет собой Yuesang №11, Guisangyou №62 или Sangteyou №2.
3. Способ экстракции по п. 1 или 2, причем катионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнокислотной катионообменной смолы на основе стирола 732-го типа, сильнокислотной катионообменной смолы на основе стирола 734-го типа, сильнокислотной катионообменной смолы на основе стирола типа 002SC, макропористой и сильнокислотной катионообменной смолы на основе стирола типа D001, макропористой и слабокислотной катионообменной смолы на основе фенилпропена типа D113 и макропористой и сильнощелочной катионообменной смолы типа D254 четвертичноаммониевого типа;
предпочтительно, катионообменная смола представляет собой сильнокислотную катионообменную смолу на основе стирола 732-го типа, сильнокислотную катионообменную смолу на основе стирола 734-го типа и макропористую и сильнокислотную катионообменную смолу на основе стирола типа D001;
предпочтительн при разделении посредством катионообменной смолы на стадии 2) катионообменная смола и растительное сырье имеют массовое соотношение в диапазоне от 1:1 до 1:25 и более предпочтительно от 1:2 до 1:20;
и
предпочтительно, масса элюента, применяемого при разделении с помощью катионообменной смолы на стадии 2), в 0,5-10 раз превышает массу растительного сырья.
4. Способ экстракции по любому из пп. 1-3, причем анионообменная смола представляет собой одну или комбинацию из нескольких, выбранных из сильнощелочной анионообменной смолы на основе стирола 717-го типа, сильнощелочной анионообменной смолы на основе стирола 711-го типа, макропористой смолы и сильнощелочной анионообменной смолы на основе стирола типа D201, макропористой и сильнощелочной анионообменной смолы на основе акрила типа D218h макропористой и слабощелочной анионообменной смолы на основе стирола типа D301; и
предпочтительно, анионообменная смола представляет собой сильнощелочную анионообменную смолу на основе стирола 717-го типа, макропористую и сильнощелочную анионообменную смолу на основе стирола типа D201 и макропористой и сильнощелочной анионообменной смолой на основе акрила типа D218; предпочтительно, при разделении посредством анионообменной смолы на стадии 2) анионообменная смола и растительное сырье имеют массовое соотношение в диапазоне от 1:1 до 1:64 и более предпочтительно от 1:1 до 1:32.
5. Способ экстракции по любому из пп. 1-4, причем этанол, применяемый для осаждения спиртом на стадии 4, и растительное сырье имеют массовое соотношение в диапазоне от 1:20 до 1:300.
6. Растительный экстракт, снижающий уровень глюкозы в крови, полученный способом экстракции по любому из пп. 1-5.
7. Фармацевтическая композиция для снижения повышения уровня глюкозы в крови, содержащая растительный экстракт по п. 6 и необязательное фармацевтически приемлемое вспомогательное вещество.
8. Фармацевтическая композиция по п. 7, где к лекарственной форме фармацевтической композиции относится пероральный твердый препарат и жидкий препарат, предпочтительно, к лекарственной форме фармацевтической композиции относится таблетка, капсула, пероральный раствор, пероральная эмульсия, пилюля и гранула.
9. Применение растительного экстракта по п. 6 или фармацевтической композиции по п. 7 или 8 при получении гипогликемического лекарственного средства.
10. Продукт медицинского назначения для снижения повышения уровня глюкозы в крови, содержащий растительный экстракт по п. 6.
11. Применение растительного экстракта по п. 6 при получении продукта медицинского назначения для снижения повышения уровня глюкозы в крови.
| Способ производства сварных труб | 1989 |
|
SU1611487A1 |
| Способ производства сварных труб | 1989 |
|
SU1611487A1 |
| CN 104402801 А, 11.03.2015 | |||
| CN 104844723 А, 19.08.2015 | |||
| CN 102462817 A, 23.05.2012. | |||
Авторы
Даты
2024-04-25—Публикация
2020-08-20—Подача