ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к применению экстракта шелковицы для получения лекарственного средства для снижения массы тела у животных.
УРОВЕНЬ ТЕХНИКИ
По мере улучшения качества жизни проблема ожирения и избыточной массы тела растет с угрожающей скоростью по всему миру. Эпидемиологические исследования показали, что ожирение и избыточная масса тела являются основными факторами риска развития диабета, сердечно-сосудистых заболеваний, рака и преждевременной смерти. Причины ожирения включают увеличение размера и количества адипоцитов, при этом увеличение количества адипоцитов вызвано дифференцировкой преадипоцитов в зрелые адипоциты, а дифференцировка преадипоцитов в зрелые адипоциты происходит за счет активации и экспрессии ряда факторов транскрипции. Данные показывают, что количество людей, страдающих диабетом, является самым большим в мире, среди них доля людей с избыточной массой тела составляет 41,0%, а доля людей с ожирением - 24,3%. По сравнению с пациентами с простым ожирением пациентам с диабетом 2 типа с ожирением сложнее похудеть и поддерживать массу тела (Experts' Consensus in China on Integrated Management of Type 2 Diabeteswith Obesity, China J Endocrinol Metab, 2016, 32(08): 623-627).
Благодаря высокой питательной и лечебной ценности растения шелковицы с древних времен считались ценным сырьем как для применения в медицине, так и для употребления в пищу. По классике традиционной китайской медицины и в рецептах разных лет имеются записи о том, что для лечения заболеваний применяли веточки шелковицы, кору шелковицы, листья шелковицы и ягоды шелковицы. Например, уже в сборнике Materia Medica есть упоминания, что «взвар листьев шелковицы с соком может утолять жажду вместо чая» и «питье после приготовления и отвара может утолять жажду вместо чая». Химические компоненты в растениях шелковицы в основном включают флавоновые соединения, полисахаридные соединения, алкалоиды и тому подобное, и в настоящее время широко применяются для приготовления гипогликемических, гиполипидемических, противовирусных и иммуномодулирующих лекарственных средств.
В уровне техники есть ряд упоминаний о влиянии экстракта шелковицы на снижение массы тела и снижение уровня липидов. Например, в заявке на патент CN 1631246 A раскрыто действие экстракта веточек шелковицы на снижение массы тела и снижение уровня липидов, и конкретно показано, что спиртовой экстракт веточек шелковицы может снижать массу тела у мышей NIH, а также снижать уровни триглицеридов и холестерина в крови, но ни способ введения, ни соотношение доза-эффект не ясны; в другой заявке на патент, CN 102370708 A, раскрыто применение водного экстракта или спиртового экстракта китайского растительного лекарственного средства из листьев шелковицы для получения лекарственных средств для снижения массы тела и снижения уровня липидов, а также раскрыто применение экстракта шелковицы для снижения массы тела и снижения уровня липидов.
Мыши ККАу представляют собой своего рода животную модель диабета 2 типа. Они появляются за счет переноса мутантного гена (ау) мышам КК; причиной этого является фактор окружающей среды, накладывающийся на генетическую восприимчивость. Эта модель очень похожа на характеристики диабета 2 типа у человека; кроме того, за счет небольших индивидуальных различий и хорошей экспериментальной повторяемости они представляют собой относительно идеальную животную модель спонтанного диабета 2 типа. Мыши ККАу имеют клинические признаки полидипсии, полифагии и полиурии с ожирением и характеризуются гипергликемией, высокой резистентностью к инсулину, недостаточностью островковых клеток, заболеваниями печени, почек и т.д. Исследования показывают, что масса тела, а также жировая масса печени и эпидидимальная жировая масса мышей ККАу значительно выше, чем у нормальных мышей. На данный момент нет сообщений об исследованиях влияния экстракта шелковицы с прозрачным составом на массу мышей ККАу.
Краткое описание изобретения
Автор настоящего изобретения провел исследования и обнаружил, что экстракт шелковицы согласно настоящему изобретению оказывает значительное влияние на снижение массы тела у животных. На основании этого в настоящем изобретении предложено применение экстракта шелковицы для получения лекарственного средства для снижения массы тела у животных.
В одном варианте реализации настоящего изобретения экстракт шелковицы содержит алкалоид, полисахарид, аминокислоту и флавон. Предпочтительно массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 3% до 99%,
полисахарид от 0,2% до 70%,
флавон от 0% до 10%,
аминокислота от 0% до 50%, и
прочие компоненты от 0% до 25%;
более предпочтительно, массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 50% до 99%,
полисахарид от 0,2% до 35%,
флавон от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%; и
еще более предпочтительно, массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 50% до 99%,
полисахарид от 0,2% до 25%,
флавон от 0% до 1%,
аминокислота от 0% до 20%, и
другие компоненты от 0% до 20%,
еще более предпочтительно, массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 30% до 99%,
полисахарид от 0,2% до 35%,
флавон от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%,
еще более предпочтительно, массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 40% до 99%,
полисахарид от 0,2% до 35%,
флавон от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%.
В одном из вариантов реализации получение экстракта шелковицы включает следующие стадии: приготовление неочищенного экстракционного раствора; необязательно, разделение с помощью катионной смолы и/или анионной смолы; необязательно, подвергание эффлюента смолы осаждению спиртом; и, необязательно, концентрирование и сушку. Предпочтительно, получение экстракта шелковицы включает следующие стадии: стадию 1): приготовление неочищенного экстракционного раствора; стадию 2): разделение с помощью катионной смолы и/или необязательно анионной смолы; необязательную стадию 3): подвергание эффлюента смолы, полученного на стадии 2), осаждению спиртом; и необязательную стадию 4): концентрирование и сушку.
В одном из вариантов реализации экстракт шелковицы получали в соответствии со следующими стадиями: измельчение веточек шелковицы, листьев шелковицы или коры шелковицы; нагревание с обратным холодильником для экстракции водой и/или спиртовым раствором или кислой водой, количество растворителя в которой в 3-20 раз превышает количество исходных лекарственных материалов; повторение экстракции 1-3 раза; объединение экстракционного раствора и концентрирование; загрузка катионообменной смолы; необязательно, вымывание неадсорбированных примесей водой (предпочтительно дистиллированной) и элюирование 0,2-3 н. гидроксидом аммония; концентрирование элюентом и загрузка анионообменной смолы; сбор неадсорбированной части, добавление этанола, осаждение для удаления примесей, центрифугирование и концентрирование (предпочтительно, концентрирование при пониженном давлении) с помощью чистого раствора или сушка (предпочтительно, распылительная сушка или лиофильная сушка) с получением экстракта.
В одном из вариантов реализации экстракт шелковицы получали в соответствии со следующими стадиями: измельчение веточек шелковицы, листьев шелковицы или коры шелковицы; нагревание с обратным холодильником для экстракции водой и/или спиртовым раствором или кислой водой, количество растворителя в которой в 3-20 раз превышает количество исходных лекарственных материалов; повторение экстракции 1-3 раза; объединение экстракционного раствора и концентрирование; загрузка катионообменной смолы; необязательно, вымывание неадсорбированных примесей водой (предпочтительно дистиллированной) и элюирование 0,2-3 н. гидроксидом аммония; концентрирование элюентом и загрузка анионообменной смолы; сбор неадсорбированной части и концентрирование (предпочтительно, концентрирование при пониженном давлении) или сушка (предпочтительно, распылительная сушка или лиофильная сушка) с получением экстракта.
В одном из вариантов реализации экстракт шелковицы получали в соответствии со следующими стадиями: измельчение веточек шелковицы, листьев шелковицы или коры шелковицы; нагревание с обратным холодильником для экстракции водой и/или спиртовым раствором или кислой водой, количество растворителя в которой в 3-20 раз превышает количество исходных лекарственных материалов; повторение экстракции 1-3 раза; объединение экстракционного раствора и концентрирование; загрузка катионообменной смолы; необязательно, вымывание неадсорбированных примесей водой (предпочтительно дистиллированной) и элюирование 0,2-3 н. гидроксидом аммония и концентрирование (предпочтительно, концентрирование при пониженном давлении) с помощью элюента или сушка (предпочтительно, распылительная сушка или лиофильная сушка) с получением экстракта.
Вид животного, обозначаемого термином «животное» в настоящем изобретении, конкретно не ограничен. Животными могут быть любые животные с интриальными (intrialinal) органами, предпочтительно млекопитающие, более предпочтительно крысы, мыши и люди, и наиболее предпочтительно люди.
В одном из вариантов реализации настоящего изобретения животные страдают диабетом. Предпочтительно, животные с диабетом имеют показатель массы тела ИМТ≥28.
Предпочтительно животные являются здоровыми.
В одном варианте реализации настоящего изобретения лекарственное средство уменьшает массу тела у животных путем уменьшения накопления жира в клетках. Предпочтительно, клетки представляют собой клетки печени и/или эпидидимальные адипоциты. Более предпочтительно, клетки представляют собой клетки печени.
Предпочтительно лекарственное средство дополнительно содержит фармацевтически приемлемый носитель. Носитель может представлять собой неактивный компонент, соответствующий путям или способам введения и нетоксичный для организма человека. Носитель может представлять собой твердое или жидкое вспомогательное вещество. Твердые вспомогательные вещества, например, включают микрокристаллическую целлюлозу, маннит, лактозу, предварительно желатинизированный крахмал, низкозамещенную гидроксипропилцеллюлозу, поливинилполипирролидон, карбоксиметилкрахмал натрия, аспартам, гидрофосфат кальция, лактат натрия, полоксамер, додецилсульфат натрия, карбоксиметилцеллюлозу натрия, желатин, ксантановую камедь, повидон, крахмал, стеарат магния, карбоксиметилкрахмал натрия и тальк; и жидкие вспомогательные вещества, например, включают воду, этанол, сироп и глицерин.
Предпочтительно лекарственное средство имеет лекарственную форму для перорального введения; более предпочтительно, указанное лекарственное средство представляет собой таблетку, капсулу, раствор для перорального приема, эмульсию для перорального приема, пилюлю, гранулу, сироп и порошок.
Экстракт шелковицы согласно настоящему изобретению может контролировать увеличение массы тела у мышей в модели спонтанного диабета с ожирением; более того, за счет понятных ингредиентов, контролируемого качества, отсутствия побочных эффектов, высокой безопасности и низкой стоимости данный экстракт обеспечивает новую возможность для людей с диабетом, страдающих ожирением, а также новые возможности для разработки и скрининга лекарственных средств для снижения массы тела.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
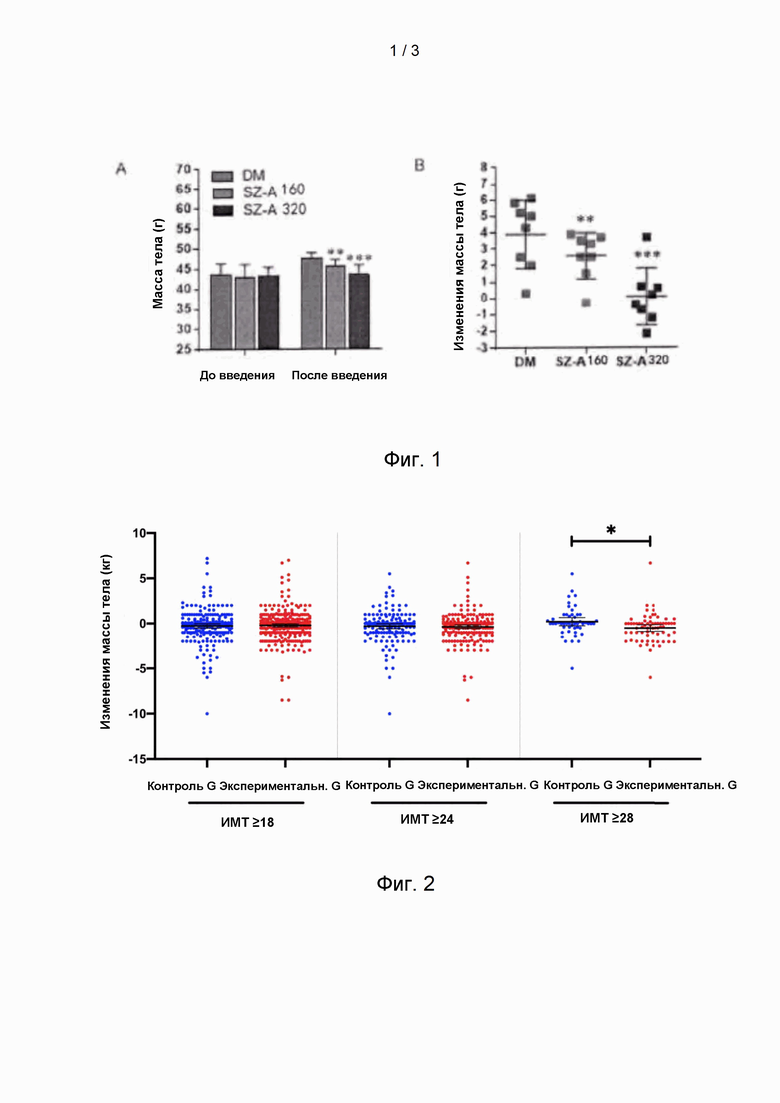
На фиг. 1 показаны эффекты долгосрочного введения экстракта шелковицы согласно варианту реализации 9 на массу тела мышей ККАу: (А) массу каждой группы до и после введения и (В) изменения массы до и после введения. **Р<0,01, ***Р<0,001 относительно группы DM.
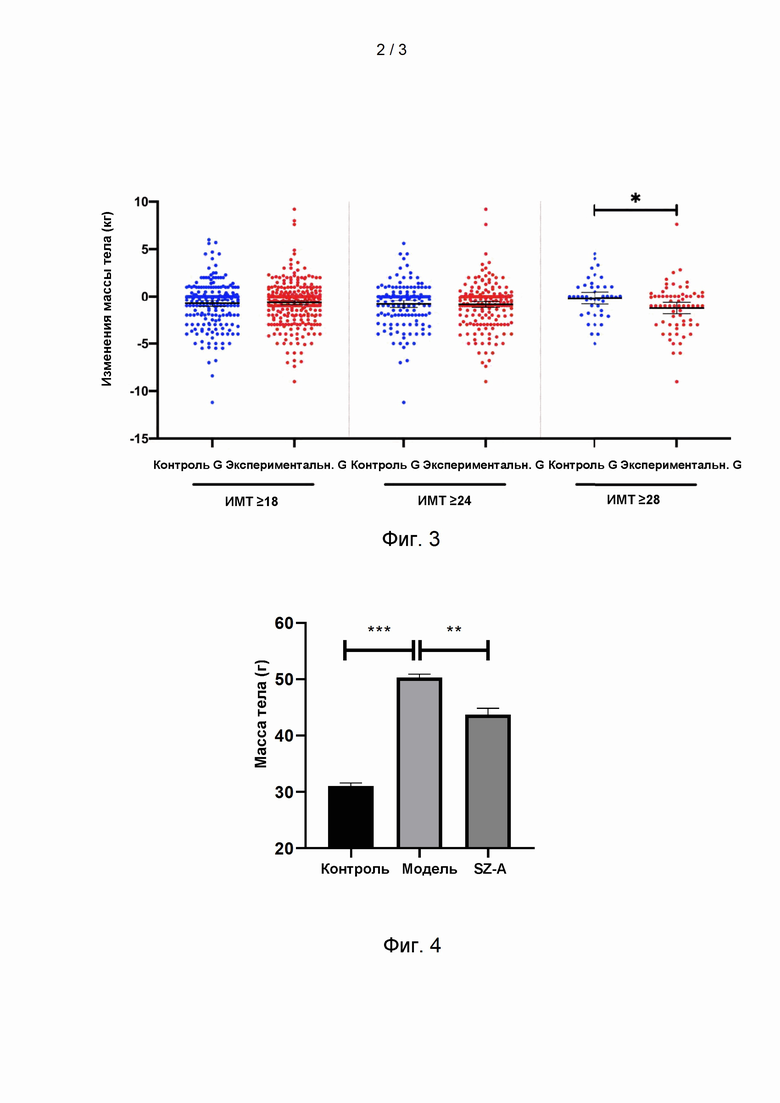
На фиг. 2 показаны индивидуальные изменения массы тела после 8 недель клинического введения в варианте реализации 11.
На фиг. 3 показаны индивидуальные изменения массы тела после 24 недель клинического введения в варианте реализации 11.
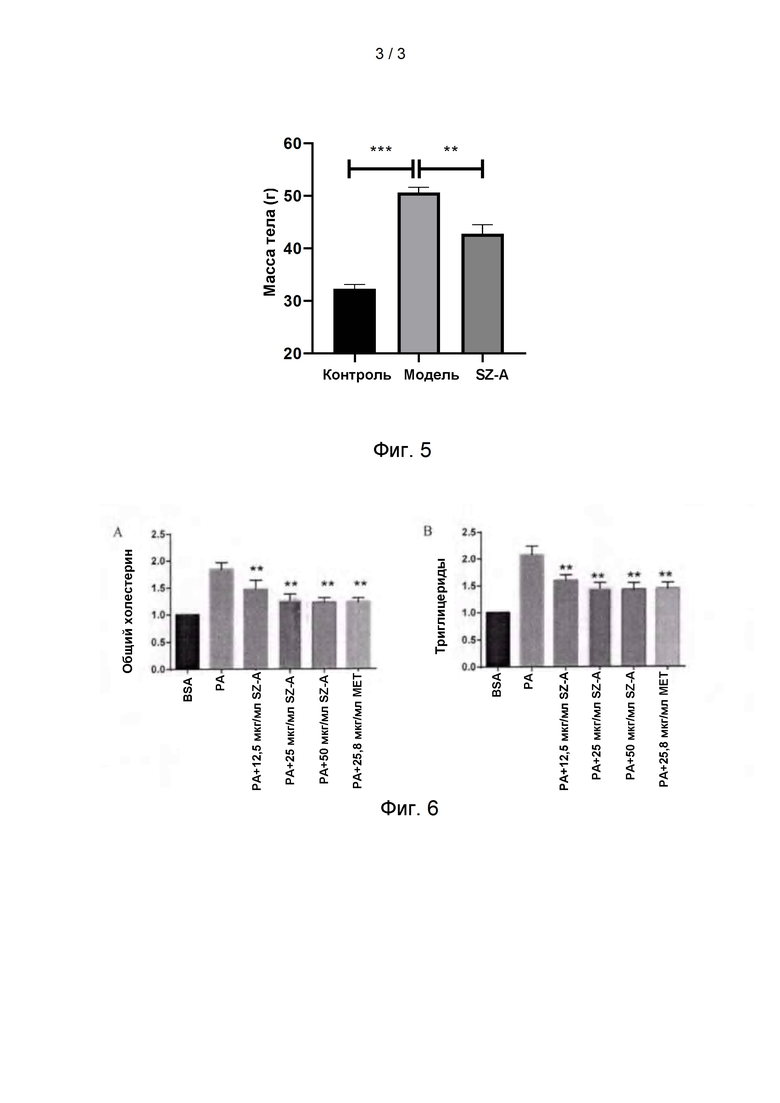
На фиг. 4 показаны изменения массы тела мышей С57 с высоким содержанием жира в варианте реализации 13 после внутрижелудочного введения.
На фиг. 5 показаны изменения массы тела мышей С57 с высоким содержанием жира в варианте реализации 13 после введения путем инъекции.
На фиг. 6 показано влияние различных доз SZ-A на накопление триглицеридов в печени и холестерина, вызванное пальмитиновой кислотой. SZ-A означает группу лечения SZ-A экстрактом веточек шелковицы, МЕТ означает группу положительного контроля метформина, РА означает модельную группу резистентности к инсулину, стимулируемую пальмитиновой кислотой, BSA означает нормальную контрольную группу клеток HepG2 (обработанную BSA0,25%). **Р<0,01 относительно нормальной контрольной группы.
Варианты реализации
Настоящее изобретение будет дополнительно подробно описано со ссылкой на графические материалы и варианты реализации изобретения. Благодаря этим иллюстративным описаниям признаки и преимущества настоящего изобретения станут более ясными и определенными.
Конкретный термин «приведенный в качестве примера» в данном документе означает «используемый в качестве примера или варианта реализации, или являющийся пояснительным». Любой вариант реализации, описанный в данном документе как «иллюстративный», не обязательно истолковывается как превосходящий или лучше других.
Кроме того, технические признаки, задействованные в различных вариантах реализации настоящего изобретения, описанных ниже, могут быть объединены друг с другом, если они не противоречат друг другу.
Содержание компонентов, используемых в настоящем изобретении, определяли в соответствии с известными способами (см. способы, раскрытые в патентах с номерами публикаций CN 11077247 А и CN 110393738 A).
Вариант реализации 1: Получение 1 экстракта шелковицы
Отбирали и измельчали 1000 кг свежих веточек шелковицы (Moms serrata Roxb-Yuesang №11), затем добавляли 4000 л воды и экстрагировали нагреванием с обратным холодильником в течение 2 ч; экстракционный раствор объединяли и фильтровали для удаления нерастворимых веществ, и таким образом получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор концентрировали путем нагревания до тех пор, пока процентное содержание твердых веществ не составляло до 4%, и выдерживали при 50°С и использовали в качестве загрузочного раствора для колонки катионной смолы.
150 кг макропористой и слабокислой катионной смолы на основе фенилпропена типа D113 использовали для набивки колонки, а раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; раствор гидроксида натрия 1 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 8,5; раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; и деионизированную воду, объем которой в 5 раз превышал объем колонки, использовали для промывки, и таким образом активацию завершали. Концентрированный экстракционный раствор загружали, а затем элюировали с применением 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 объемов слоя/ч; элюент собирали, когда было обнаружено, что эффлюент из катионной колонки имеет рН>7; сбор останавливали, когда собранный раствор составлял до 900 л, и собранный раствор очищали непосредственно через анионную колонку.
62,5 кг макропористой и сильнощелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный катионный элюент загружали на анионную смолу и собирали эффлюент до тех пор, пока эффлюент не достигнет 870 л.
Сборный раствор центрифугировали для удаления примесей, а затем концентрировали с помощью мембраны для обратного осмоса; удельный вес концентрированной жидкости составлял 1,25; концентрированную жидкость переносили в резервуар для осаждения спиртом, и добавляли 25 л безводного этанола, когда мешалка для перемешивания вращалась со скоростью 500 об/мин. После завершения добавления этанола, перемешивание прекращали, и осаждение спиртом проводили в течение 24 часов; супернатант отбирали и концентрировали при пониженном давлении, в результате чего получали вытяжку из экстракта.
Эффлюент концентрировали при пониженном давлении с получением вытяжки из экстракта веточек шелковицы, где алкалоид составлял 52%, полисахарид составлял 22%, флавон составлял 0,8%, а аминокислота составляла 20%.
Вариант реализации 2: Получение 2 экстракта шелковицы
Отбирали и измельчали 10 кг свежих веточек шелковицы (Sangteyou №2), затем добавляли 150 л воды 2 раза, и экстрагировали с помощью уваривания в течение 3 ч каждый раз; экстракционный раствор объединяли и фильтровали для удаления нерастворимых веществ. Экстракционный раствор концентрировали нагреванием до тех пор, пока процентное содержание твердых веществ не составляло до 8%, затем переносили в резервуар для осаждения спиртом и добавляли 2367,9 г (3 л) безводного этанола при скорости перемешивания 300 об/мин. После завершения добавления этанола перемешивание прекращали, и осаждение спирта проводили в течение 24 ч; супернатант брали в качестве загрузочного раствора для колонки с катионной смолой. Для заполнения колонки использовали 5 кг сильнокислотной катионной смолы на основе стирола типа 002SC, и катионную смолу активировали в соответствии со способом, описанным в варианте реализации 1. Экстракционный раствор загружали после концентрирования и осаждения спиртом, а затем элюировали 100 л 5 моль/л хлорида калия со скоростью элюирования 5 объемов слоя/ч; эффлюент обнаруживали с помощью 20% силиковольфрамовой кислоты, и сбор начинали после образования белого осадка; сбор останавливали до тех пор, пока собранный раствор не составлял до 25 л; и собранный раствор очищали непосредственно через колонку с анионной смолой.
Для заполнения колонки использовали 10 кг сильнощелочной анионной смолы на основе стирола типа 711, и анионную смолу активировали в соответствии со способом, описанным в варианте реализации 3. Собранный катионный элюент загружали на анионную смолу, и собирали эффлюент до тех пор, пока эффлюент не достигнет 15 л. Собранный раствор повторно загружали в катионную смолу и дважды разделяли с использованием катионной смолы и анионной смолы последовательно в соответствии с вышеупомянутым способом.
Собранный раствор, полученный после трех разделений на колонке, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса, при этом удельный вес концентрированной жидкости составлял 1,25; его переносили в резервуар для осаждения спиртом, и добавляли 125 г безводного этанола при скорости перемешивания 1000 об/мин. После завершения добавления этанола перемешивание прекращали, и осаждение спиртом проводили в течение 24 часов; супернатант отбирали и концентрировали при пониженном давлении, в результате чего получали вытяжку экстракта. Кроме того, снова брали и экстрагировали свежие кору шелковицы и листья шелковицы (Sangteyou №2), при этом способ и параметры экстракции были такими же, как описаны выше.
В полученном экстракте веточек шелковицы алкалоид составлял 98%, полисахарид составлял 0,2%, флавон составлял 0,05%, аминокислота составляла 0.
В полученном экстракте коры шелковицы алкалоид составлял 95%, полисахарид составлял 2%, флавон составлял 0,1%, аминокислота составляла 1%.
В полученном экстракте листьев шелковицы алкалоид составлял 90%, полисахарид составлял 4%, флавон составлял 0,1%, аминокислота составляла 3%.
Вариант реализации 3: Приготовление 3 экстракта шелковицы
Отбирали и измельчали 1000 кг свежих веточек шелковицы (Moms atropurpurea Roxb), затем добавляли 11500 л воды и экстрагировали нагреванием с обратным холодильником в течение 2 ч; экстракционный раствор объединяли и фильтровали для удаления нерастворимых веществ, и таким образом получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор центрифугировали для удаления примесей, а затем концентрировали с помощью мембраны для обратного осмоса до тех пор, пока процентное содержание твердых веществ не составляло до 1%, и он служил в качестве загрузочного раствора для колонки катионной смолы.
Для заполнения колонки использовали 300 кг макропористой и сильнокислотной катионной смолы на основе стирола типа D001, и катионную смолу активировали в соответствии со способом, описанным в варианте реализации 1. Неочищенный экстракционный раствор загружали после концентрирования, а затем элюировали 5000 л 0,04 моль/л нитрата аммония со скоростью элюирования 5 объемов слоя/ч; эффлюент обнаруживали с помощью 20% силиковольфрамовой кислоты, и сбор начинали после образования белого осадка; сбор останавливали до тех пор, пока собранный раствор не достиг 1000 л.
Собранный раствор, полученный после разделения на катионной колонке, концентрировали нанофильтрацией, а затем концентрировали при пониженном давлении с получением вытяжки экстракта.
В полученном экстракте веточек шелковицы алкалоид составлял 15%, полисахарид составлял 20%, флавон составлял 7%, аминокислота составляла 45.
Вариант реализации 4: Получение 4 экстракта шелковицы
Отбирали и измельчали 333 кг высушенных веточек шелковицы (Yuesang №11), затем добавляли 4000 л воды и дважды экстрагировали нагреванием с обратным холодильником, 1 ч для каждого обратного холодильника; экстракционный раствор объединяли и фильтровали,и концентрировали до тех пор, пока количество неочищенного лекарственного средства не достигло 1 кг/л.
150 кг макропористой и слабокислой катионной смолы на основе фенилпропена типа D113 использовали для набивки колонки, а раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; раствор гидроксида натрия 1 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 8,5; раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; и деионизированную воду, объем которой в 5 раз превышал объем колонки, использовали для промывки, и таким образом активацию завершали. Концентрированный экстракционный раствор загружали, а затем элюировали с применением 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 объемов слоя/ч; элюент собирали, когда было обнаружено, что эффлюент из катионной колонки имеет рН>7; сбор останавливали, когда собранный раствор составлял до 900 л, и собранный раствор очищали непосредственно через анионную колонку.
125 кг макропористой и сильнощелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный катионный элюент загружали на анионную смолу и собирали эффлюент, рН которого составлял более 8, до тех пор, пока эффлюент не достигнет 870 л.
Собранный раствор, полученный после разделения на анионной колонке фильтровали на микрофильтрационной мембране, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса, при этом удельный вес концентрированной жидкости составлял 1,1; его переносили в резервуар для осаждения спиртом, и добавляли 15 г безводного этанола при скорости перемешивания 400 об/мин. После завершения добавления этанола перемешивание прекращали, и осаждение спиртом проводили в течение 24 часов; супернатант отбирали и концентрировали при пониженном давлении, в результате чего получали вытяжку экстракта веточек шелковицы. Содержание в образце: алкалоид составлял 80%, полисахарид составлял 5%, флавон составлял 0,1%, аминокислота составляла 4%.
Вариант реализации 5: Получение 5 экстракта шелковицы
Отбирали и измельчали 400 кг высушенных веточек шелковицы (Yuesang №11), затем добавляли 4000 л воды и дважды экстрагировали нагреванием с обратным холодильником, 1 ч для каждого обратного холодильника; экстракционный раствор объединяли и фильтровали, и концентрировали до тех пор, пока количество неочищенного лекарственного средства не достигло 1 кг/л.
62,5 кг макропористой и сильно щелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный экстракт концентрировали и загружали в анионную смолу, и собирали эффлюент.
Собранный раствор, полученный после разделения на анионной колонке, фильтровали с помощью микрофильтрационной мембраны для удаления примесей, затем концентрировали через мембрану обратного осмоса и дополнительно концентрировали при пониженном давлении и сушили с получением вытяжки экстракта веточек шелковицы. Содержание в образце: алкалоид составлял 3%, полисахарид составлял 70%, флавон составлял 10%, аминокислота составляла 10%.
Вариант реализации 6: Получение 6 экстракта шелковицы
Отбирали и измельчали 1500 кг свежих веточек шелковицы (Moms serrata Roxb-Yuesang №11), затем добавляли 6000 л воды и экстрагировали нагреванием с обратным холодильником в течение 2 ч; экстракционный раствор объединяли и фильтровали для удаления нерастворимых веществ, и таким образом получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор концентрировали путем нагревания до тех пор, пока процентное содержание твердых веществ не составляло до 4%, и выдерживали при 50°С и использовали в качестве загрузочного раствора для колонки катионной смолы.
100 кг макропористой и слабокислой катионной смолы на основе фенилпропена типа D113 использовали для набивки колонки, а раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; раствор гидроксида натрия 1 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 8,5; раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; и деионизированную воду, объем которой в 5 раз превышал объем колонки, использовали для промывки, и таким образом активацию завершали. Концентрированный экстракционный раствор загружали, а затем элюировали с применением 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 объемов слоя/ч; элюент собирали, когда было обнаружено, что эффлюент из катионной колонки имеет рН>7; сбор останавливали, когда собранный раствор составлял до 900 л, и собранный раствор очищали непосредственно через анионную колонку.
62,5 кг макропористой и сильнощелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный катионный элюент загружали на анионную смолу и собирали эффлюент до тех пор, пока эффлюент не достигнет 870 л. Эффлюент концентрировали при пониженном давлении с получением вытяжки из экстракта веточек шелковицы, где алкалоид составлял 30%, полисахарид составлял 35%, флавон составлял 2%, а аминокислота составляла 25%.
Вариант реализации 7: Получение 7 экстракта шелковицы
Отбирали и измельчали 1000 кг свежих веточек шелковицы (Moms serrata Roxb-Yuesang №11), затем добавляли 4000 л воды и экстрагировали нагреванием с обратным холодильником в течение 2 ч; экстракционный раствор объединяли и фильтровали для удаления нерастворимых веществ, и таким образом получали неочищенный экстракционный раствор. Неочищенный экстракционный раствор концентрировали путем нагревания до тех пор, пока процентное содержание твердых веществ не составляло до 4%, и выдерживали при 50°С и использовали в качестве загрузочного раствора для колонки катионной смолы.
100 кг макропористой и слабокислой катионной смолы на основе фенилпропена типа D113 использовали для набивки колонки, а раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; раствор гидроксида натрия 1 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 8,5; раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; и деионизированную воду, объем которой в 5 раз превышал объем колонки, использовали для промывки, и таким образом активацию завершали. Концентрированный экстракционный раствор загружали, а затем элюировали с применением 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 объемов слоя/ч; элюент собирали, когда было обнаружено, что эффлюент из катионной колонки имеет рН>7; сбор останавливали, когда собранный раствор составлял до 900 л, и собранный раствор очищали непосредственно через анионную колонку.
62,5 кг макропористой и сильнощелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный катионный элюент загружали на анионную смолу и собирали эффлюент до тех пор, пока эффлюент не достигнет 870 л. Эффлюент концентрировали при пониженном давлении с получением вытяжки из экстракта веточек шелковицы, где алкалоид составлял 40%, полисахарид составлял 25%, флавон составлял 0,5%, а аминокислота составляла 25%.
Вариант реализации 8: Получение 8 экстракта шелковицы
Отбирали и измельчали 333 кг высушенных веточек шелковицы (Yuesang №11), затем добавляли 4000 л воды и дважды экстрагировали нагреванием с обратным холодильником, 1 ч для каждого обратного холодильника; экстракционный раствор объединяли и фильтровали,и концентрировали до тех пор, пока количество неочищенного лекарственного средства не достигло 1 кг/л.
150 кг макропористой и слабокислой катионной смолы на основе фенилпропена типа D113 использовали для набивки колонки, а раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; раствор гидроксида натрия 1 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 8,5; раствор хлористоводородной кислоты 2 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 4,5; и деионизированную воду, объем которой в 5 раз превышал объем колонки, использовали для промывки, и таким образом активацию завершали. Концентрированный экстракционный раствор загружали, а затем элюировали с применением 1000 л 2,5 моль/л аммиачной воды со скоростью элюирования 6 объемов слоя/ч; элюент собирали, когда было обнаружено, что эффлюент из катионной колонки имеет рН>7; сбор останавливали, когда собранный раствор составлял до 900 л, и собранный раствор очищали непосредственно через анионную колонку.
62,5 кг макропористой и сильнощелочной анионной смолы типа D218 использовали для загрузки колонки, а раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0; раствор соляной кислоты 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 3,5; и раствор гидроксида натрия 1,5 моль/л использовали для промывки до тех пор, пока рН элюента не составлял 9,0, и таким образом активацию завершали. Собранный катионный элюент загружали на анионную смолу и собирали эффлюент до тех пор, пока эффлюент не достигнет 870 л.
Собранный раствор, полученный после разделения на анионной колонке фильтровали на микрофильтрационной мембране, центрифугировали для удаления примесей, а затем концентрировали через мембрану для обратного осмоса, при этом удельный вес концентрированной жидкости составлял 1,1; его переносили в резервуар для осаждения спиртом, и добавляли 15 г безводного этанола при скорости перемешивания 400 об/мин. После завершения добавления этанола перемешивание прекращали, и осаждение спиртом проводили в течение 24 часов; супернатант отбирали и концентрировали при пониженном давлении, в результате чего получали вытяжку экстракта веточек шелковицы. Содержание в образце: алкалоид составлял 63%, полисахарид составлял 23%, флавон составлял 1%, аминокислота составляла 5%.
Вариант реализации 9: Влияние экстракта шелковицы на массу тела мышей ККАу со спонтанным диабетом 2 типа
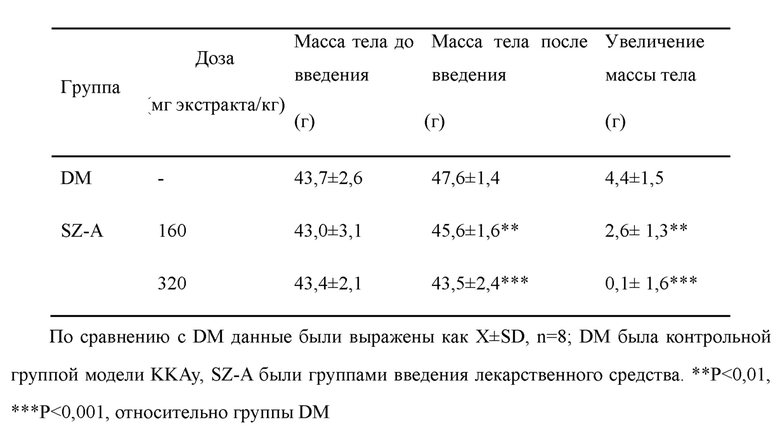
Отбирали двенадцатинедельных самок мышей ККАу; после кормления кормом с высоким содержанием жиров в течение трех недель их разделяли поровну на 3 группы (группа DM, SZ-A 160 (мг экстракта шелковицы/кг), SZ-A 320 (мг экстракта шелковицы/кг)) в соответствии со случайным уровнем глюкозы в крови, уровнем глюкозы в крови натощак, массой тела и другими показателями, по 8 мышей в каждой группе, и давали экстракт шелковицы согласно варианту реализации 8 один раз в день путем внутрижелудочного введения; лекарственное средство вводили непрерывно в течение примерно 6 недель, и регистрировали изменения массы мышей до и после введения, как показано в Таблице 1, Таблице 2 и на фиг. 1.

До введения экстракта шелковицы средняя масса тела мышей в каждой группе составляла примерно 43 г. Примерно через 6 недель после введения экстракта шелковицы масса тела мышей в двух группах дозирования экстракта шелковицы была значительно снижена, а именно, масса тела мышей в группе дозирования SZ-A160 была ниже, чем в группе DM, на 2,0 г, скорость потери массы тела составляла 4,2%, а масса тела мышей в группе дозирования SZ-A320 была ниже, чем в группе DM, на 4,1 г, скорость потери массы тела составляла 8,6%. Во время введения скорость набора массы тела мышей в двух группах дозирования SZ-A также значительно снизилась, при этом: средний прирост массы тела мышей в группе DM составлял 4,4 г, средний прирост массы тела мышей в группе дозирования SZ-A160 составлял 2,6 г, а средний прирост в группе дозирования SZ-A320 составлял 0,1 г, что указывает на то, что экстракт шелковицы может заметно контролировать прирост массы тела у мышей ККАу.
Таблица 2 Изменения массы тела у мышей ККАу со спонтанным диабетом 2 типа
Вариант реализации 10: Клинический эксперимент 1
Брали экстракт веточек шелковицы согласно варианту реализации 1 и добавляли подходящее количество вспомогательного материала; после равномерного смешивания и добавления воды получали мягкий материал, а затем гранулировали и сушили; добавляли стеарат магния и равномерно перемешивали, и получали таблетки путем прессования, тем самым получая экстракт веточек шелковицы, причем каждая таблетка содержала суммарно 50 мг алкалоидов.
Клинические случаи и лечение:
(1) 43-летний китаец мужского пола (84,2 кг, 170 см, сахарный диабет 2 типа в течение 3 месяцев) перорально принимал таблетки, содержащие экстракт шелковицы согласно варианту реализации 1 (три раза в день и по две таблетки каждый раз перорально в течение 24 недель), и сбросил 10,2 кг массы тела.
(2) Мужчина в возрасте 65 лет (68,3 кг, 173 см, сахарный диабет 2 типа в течение 7 месяцев с гиперлипидемией) перорально принимал таблетки, содержащие экстракт шелковицы согласно варианту реализации 1 (три раза в день и по две таблетки каждый раз непрерывно в течение 24 недель), и сбросил 6,3 кг массы тела.
(3) Мужчина в возрасте 64 лет (75,0 кг, 168 см, диабет 2 типа в течение 12 месяцев) принимал акарбозу в течение двух месяцев, а затем прекратил; 8 месяцев спустя он перорально принимал таблетки, содержащие экстракт шелковицы, согласно варианту реализации 1 (три раза в день и по две таблетки каждый раз непрерывно в течение 24 недель) и сбросил 7 кг массы тела.
(4) 48-летняя женщина (81,0 кг, 164 см, сахарный диабет 2 типа в течение 8 месяцев с гиперлипидемией) перорально принимала таблетки, содержащие экстракт шелковицы согласно варианту реализации 1 (три раза в день и по две таблетки каждый раз непрерывно в течение 24 недель), и сбросила 7 кг массы тела.
Вариант реализации 11: Клинический эксперимент 2
1. Задача
Влияние экстракта веточек шелковицы на снижение массы тела у больных диабетом.
2. Метод эксперимента
2.1 Группирование
Был принят следующий дизайн исследования: случайное двойное слепое и с двойным моделированием, параллельным контролем таблетками акарбозы, многоцентровое, не меньшей эффективности, чем у контроля. Всего было включено 600 пациентов с сахарным диабетом 2 типа (в возрасте от 18 до 70 лет, 19 кг/м2 ≤ИМТ≤30 кг/м2, 7%≤HbA1C≤10%) и плохим контролем уровня глюкозы в крови, которые были случайным образом разделены на группу, получавшую таблетки алкалоида (SZ-A, N=360), и группу, получавшую акарбозу (Glucobay®) (CON, N=240). Все подписали информированные согласия.
Основными критериями исключения представляли собой следующие: 1) аллергия или непереносимость ингибиторов а-глюкозидазы; 2) изменение уровней FBS между первым и вторым последующим наблюдением превышало 2,5 ммоль/л (>45 мг/дл); 3) история тяжелых диабетических осложнений (пролиферативная стадия диабетической ретинопатии, диабетическая нефропатия V стадии, диабетический кетоацидоз, диабетическая гипертоническая кома, диабетический лактоацидоз); 4) комбинированная лекарственная терапия, влияющая на метаболизм глюкозы, такая как антидиабетическая китайская медицина или глюкокортикоиды; 5) гиперлипидемия, сопровождающаяся нерегулярным приемом липидоснижающих препаратов в анамнезе; 6) хроническая дисфункция желудочно-кишечного тракта, очевидные нарушения пищеварения и всасывания или эндокринные нарушения, такие как гипертиреоз, гиперкортизолизм и акромегалия; 7) тяжелое заболевание сердца, инфаркт миокарда, неустойчивая стенокардия, хроническая сердечная недостаточность или плохой контроль артериального давления; 8) нарушение функции печени или почек; и 9) беременность. 2.2 Способ введения
Экспериментальные группы принимали таблетки перорально (таблетки получали следующим образом: отбирали экстракт согласно варианту реализации 1 и добавляли соответствующее количество вспомогательных веществ; после равномерного смешивания и добавления воды получали мягкий материал, а затем гранулировали и сушили; добавляли стеарат магния и равномерно перемешивали, и таблетки получали путем прессования, тем самым получая экстракт веточек шелковицы, каждая таблетка содержала 50 мг общих алкалоидов) с начальной дозой одна таблетка каждый раз и три раза в день; четыре недели спустя дозу последовательно увеличивали до двух таблеток каждый раз и три раза в день; контрольная группа принимала акарбозу перорально по одной таблетке каждый раз и три раза в день.
3. Обнаружение и обработка данных эксперимента
3.1 Индекс обнаружения
(1) С 1-й по 24-ю неделю введения наблюдали и регистрировали рост, массу тела и увеличение массы тела в каждой группе каждый день.
3.2 Статистический анализ
Для обработки данных использовали программное обеспечение SPSS 20.0, а различия между группами проверяли с помощью Т-критерия.
4. Результаты
Через 8 недель и 24 недели введения были получены экспериментальные данные для различных групп ИМТ больных сахарным диабетом 2 типа в каждой группе, как показано в Таблицах 3 и 4 и на фиг.2 и 3.
После 8 недель введения, как и у пациентов с ИМТ≥28 кг/м2, масса тела в экспериментальной группе была явно снижена, по сравнению с контрольной группой, в среднем на -0,503 кг и 0,210 кг соответственно (Р=0,016); после 24 недель введения, как и у пациентов с ИМТ≥28 кг/м2, масса тела в экспериментальной группе была явно снижена, по сравнению с контрольной группой, в среднем на -1,228 кг и -0,182 кг соответственно (Р=0,022); для других групп ИМТ изменения массы тела не были статистически значимыми.
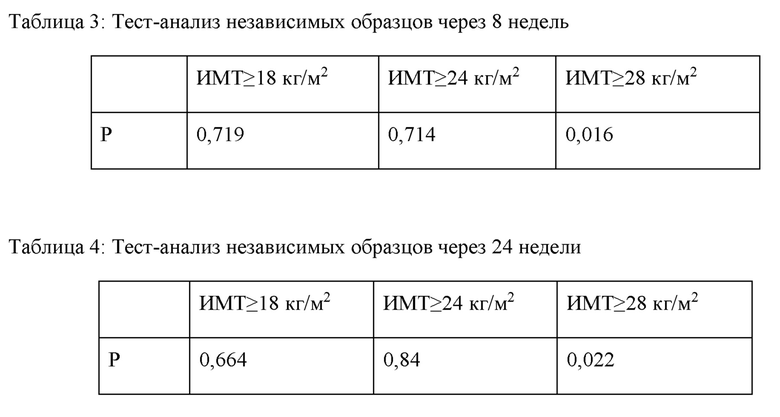
Показано, что применение экстракта веточек шелковицы у больных диабетом с ИМТ≥28 кг/м2 может способствовать лечению сахарного диабета 2 типа, а также снижению массы тела.
Вариант реализации 12: Клинический экспериментальный пример 3
1. Задача
Влияние экстракта веточек шелковицы на снижение массы тела у здоровых людей
2. Способ эксперимента
2.1 Экспериментальные приборы и материалы
Весы
2.2 Дизайн эксперимента
В группе без диабета общей сложности 17 человек, включая 11 мужчин и 6 женщин, были здоровыми людьми; они получали обычное питание в течение периода приема лекарственного средства; период приема лекарственного средства составлял от 0,7 до 8 месяцев, доза составляла 50 или 100 мг/раз, а частота приема лекарственного средства составляла от 2 до 3 раз/сут.
2.3 Индекс обнаружения
До и в конце экспериментов измеряли следующие показатели тела: масса, рост.
Критерии оценки снижения массы тела: (1) отлично, при этом процент потери массы больше или равен 10%; (2) хорошо, при этом процент потери массы больше или равен 5% и меньше 10%; (3) эффективно, при этом процент потери массы больше или равен 3% и меньше 5%; и (4) неэффективно, при этом процент потери массы меньше 3%.
3. Результаты
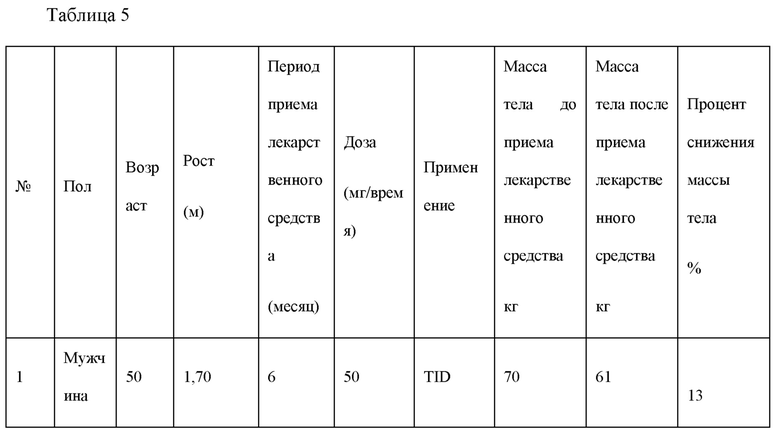
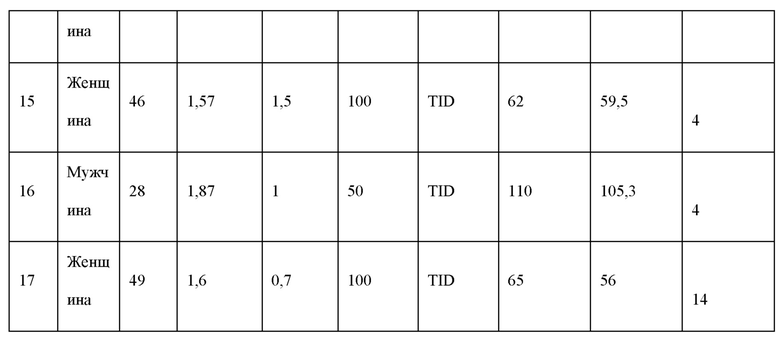
Было зарегистрировано 2 случая «отлично», 9 случаев «хорошо», 5 случаев «эффективно» и 1 случай «неэффективно», а общая эффективная частота составила 94%. Кроме того, у всех испытуемых не наблюдалось нежелательных реакций после приема лекарственного средства, что свидетельствует о том, что лекарственного средство оказывает значительное влияние на снижение массы тела у пациентов, не страдающих диабетом. Информация и экспериментальные результаты для субъектов приведены ниже в Таблице 5.
Общая степень эффективности = (Отличный случай + Очевидные случаи + Эффективные случаи)/Случаи*100%.
ТШ: лекарственное средство принимают три раза в сутки BID: лекарственное средство принимают 2 раза в сутки.

Вариант реализации 13: Эксперимент по снижению массы тела у мышей С57, которые питались кормом с высоким содержанием жиров
1. Внутрижелудочное введение
Тридцать здоровых 6-недельных самцов мышей С57 случайным образом разделяли на нормальную группу, модельную группу и группу SZ-A, по 10 мышей в каждой группе, при этом: мышей в нормальной группе кормили основным кормом, а мыши в модельной группе и группе SZ-A получали корм с высоким содержанием жиров. После 14 недель кормления мышам в каждой группе вводили соответствующее лекарственное средство путем внутрижелудочного введения каждый день в течение 6 недель подряд, при этом: группе SZ-A осуществляли внутрижелудочное введение в дозе 400 мг/кг/сут в соответствии с общим количеством алкалоидов экстракта веточек шелковицы, а нормальной группе и модельной группе вводили внутрижелудочное введение соответствующей дозы растворителя. Во время лечения лекарственным средством контролировали массу мышей. После окончания введения лекарственного средства всех мышей взвешивали натощак в течение 12 часов.
Как показано на Фиг. 4, средняя масса тела мышей в модельной группе составляла 50,3 г, а у мышей в группе введения - 43,7 г, что указывает на то, что SZ-A может значительно снизить массу тела мышей, получавших корм с высоким содержанием жиров.
2. Инъекционное введение
(1) Моделирование на животных: тридцать 6-недельных мышей С57 были случайным образом разделены на три группы, где: первую группу кормили основным кормом, вторую и третью группы кормили кормом с высоким содержанием жиров, и кормление продолжали в течение 14 недель.
(2) Введение: исходя из массы тела, третьей группе вводили внутрибрюшинную инъекцию 200 мг/кг общих алкалоидов экстракта веточек шелковицы, и период введения инъекции составлял 6 недель. Первой и второй группам индивидуально вводили один раз в день физиологический раствор в соответствии с массой тела.
(3) Измерение массы тела: после введения массу тела мышей измеряли с помощью весов и регистрировали.
Как показано на Фиг. 5, средняя масса модельной группы составляла 50,6 г, а группы введения - 42,8 г, что указывает на то, что инъекция SZ-A может значительно снизить ожирение, вызванное кормом с высоким содержанием жиров.
Вариант реализации 14: Эксперимент с клетками in vitro
1. После расщепления клеток HepG2 на логарифмической стадии роста плотность клеток доводили до 2×105 клеток/мл с помощью полной культуральной среды DMEM (с высоким содержанием глюкозы), содержащей 10% FBS, и клетки переносили в 6-луночный планшет по 2 мл/лунку.
2. После культивирования в течение 24 часов модельные клетки случайным образом разделяли на группу SZ-A (экстракт веточек шелковицы SZ-A в варианте реализации 1 при 50 мкг/мл, 25 мкг/мл и 12,5 мкг/мл), группу метформина (200 мкмоль/л МЕТ) и модельную группу, стимулированную пальмитиновой кислотой (РА); в то же время клетки HepG2 служили в качестве нормальной контрольной группы (0,25% BSA). В дополнение к нормальной контрольной группе (0,25% BSA) и модельной группе (РА) в другие группы по отдельности добавляли соответствующие лекарственные средства и пальмитиновую кислоту, реплицировали модель стимуляции пальмитиновой кислотой и предоставляли три повтора для каждой группы.
3. После культивирования в течение 24 часов для промывки один раз добавляли предварительно нагретую PBS, а затем в каждую лунку 6-луночного планшета добавляли 400 мкл лизата Triton х-100, содержащего 1% PMSF. 6-луночный планшет постукивали по льду или при 4°С в течение 1 часа с осторожным продуванием с помощью пипетки, и взбивая так, чтобы лизат и клетки находились в полном контакте. Лизированную жидкость не центрифугировали, и непосредственно измеряли 10 мкл триглицерида и 10 мкл общего холестерина после взбалтывания.
Как показано на Фиг. 6, чрезмерное накопление жира в печени может легко вызвать ожирение печени. Образование жировой ткани печени можно моделировать путем стимуляции клеток печени HepG2 пальмитиновой кислотой РА. При добавлении различных доз SZ-A можно было наблюдать накопление триглицеридов и холестерина в печени, вызванное ингибированием пальмитиновой кислоты посредством SZ-A. Эффект SZ-A аналогичен эффекту МЕТ.
Со ссылкой на вышеупомянутый способ модельные клетки обрабатывали экстрактом шелковицы (доза составляла 25 мкг/мл), полученным в вариантах реализации 2-7, и измеряли уровень триглицеридов и общий холестерин в клетках, соответственно. Согласно результатам, по сравнению с группой РА, накопление триглицеридов и холестерина в печени, вызванных пальмитиновой кислотой, было в определенной степени уменьшено после лечения экстрактом шелковицы. Конкретные результаты показаны ниже в Таблице 6.
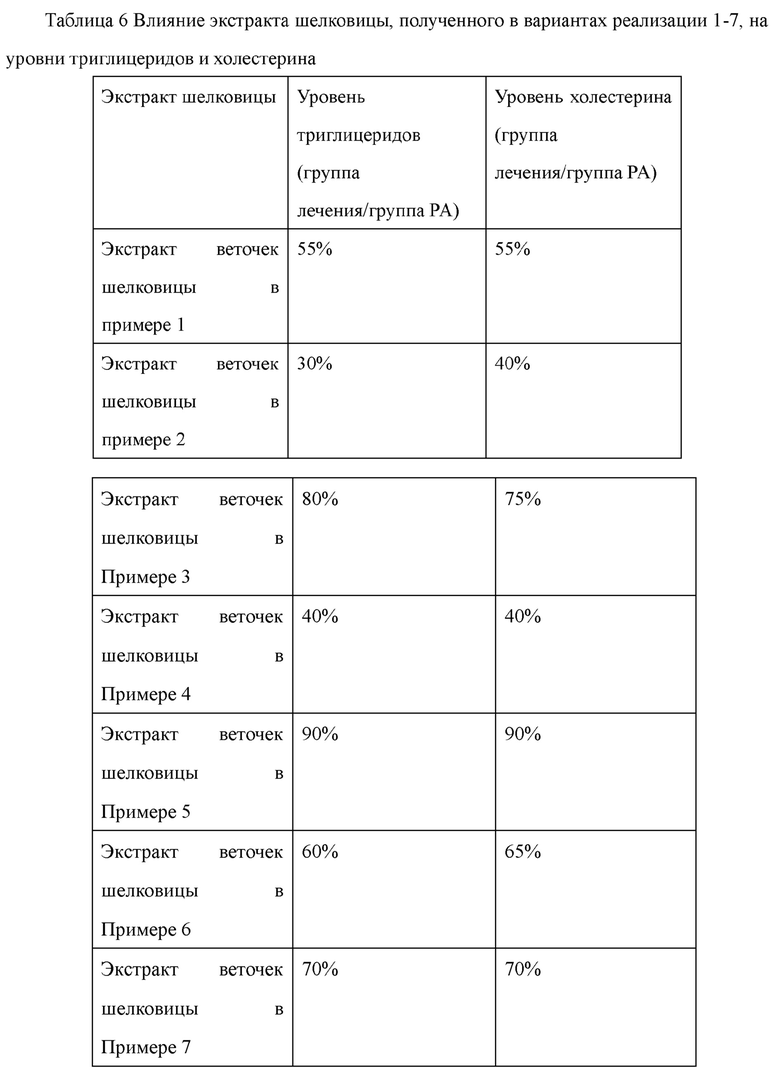
Вышеуказанные варианты реализации показывают, что экстракт шелковицы играет хорошую роль в контроле массы тела. Длительное введение экстракта шелковицы может подавлять рост массы тела у мышей и людей и подавлять увеличение массы тела у мышей с диабетом 2 типа и пациентов с диабетом; кроме того, оно может подавлять накопление жира в органах.
Со ссылкой на предпочтительные варианты реализации настоящее изобретение объясняется вышеприведенным образом. Однако эти варианты реализации изобретения являются лишь примерными и иллюстративными. Таким образом, в настоящее изобретение могут быть внесены различные замены и усовершенствования, и все эти замены и усовершенствования подпадают под объем защиты настоящего изобретения.
Изобретение относится к области медицины, а именно к применению экстракта шелковицы для получения лекарственного средства для снижения массы тела у животных. Применение экстракта шелковицы для получения лекарственного средства для снижения массы тела у животных, при этом указанный экстракт шелковицы содержит алкалоид, полисахарид, аминокислоту и флавоноид, и при этом массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим: алкалоид от 3% до 99%, полисахарид от 0,2% до 70%, флавоноид от 0% до 10%, аминокислота от 0% до 50% и прочие компоненты от 0% до 25%. Указанное изобретение обеспечивает эффективное средство для снижения массы тела у животных. 11 з.п. ф-лы, 6 ил., 6 табл.
1. Применение экстракта шелковицы для получения лекарственного средства для снижения массы тела у животных, при этом указанный экстракт шелковицы содержит алкалоид, полисахарид, аминокислоту и флавоноид, и при этом массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 3% до 99%,
полисахарид от 0,2% до 70%,
флавоноид от 0% до 10%,
аминокислота от 0% до 50%, и
прочие компоненты от 0% до 25%.
2. Применение по п. 1, отличающееся тем, что массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 50% до 99%,
полисахарид от 0,2% до 35%,
флавоноид от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%.
3. Применение по п. 1, отличающееся тем, что массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 50% до 99%,
полисахарид от 0,2% до 25%,
флавоноид от 0% до 1%,
аминокислота от 0% до 20%, и
другие компоненты от 0% до 20%.
4. Применение по п. 1, отличающееся тем, что массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 30% до 99%,
полисахарид от 0,2% до 35%,
флавоноид от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%.
5. Применение по п. 1, отличающееся тем, что массовое содержание каждого компонента, в расчете на массу экстракта шелковицы, является следующим:
алкалоид от 40% до 99%,
полисахарид от 0,2% до 35%,
флавоноид от 0% до 2%,
аминокислота от 0% до 30%, и
другие компоненты от 0% до 20%.
6. Применение по любому из пп. 1-5, отличающееся тем, что указанные животные представляют собой млекопитающих, включая людей и грызунов.
7. Применение по любому из пп. 1-6, отличающееся тем, что указанные животные страдают диабетом.
8. Применение по любому из пп. 1-6, отличающееся тем, что указанные животные являются здоровыми.
9. Применение по любому из пп. 1-8, отличающееся тем, что указанное лекарственное средство дополнительно содержит фармацевтически приемлемый носитель.
10. Применение по любому из пп. 1-9, отличающееся тем, что указанное лекарственное средство имеет лекарственную форму для перорального введения.
11. Применение по п. 10, отличающееся тем, что указанное лекарственное средство представляет собой таблетку, капсулу, раствор для перорального приема, эмульсию для перорального приема, пилюлю, гранулу, сироп и порошок.
12. Применение по п. 7, отличающееся тем, что указанные животные, страдающие диабетом, имеют ИМТ≥28.
| CN 111658692 A, 15.09.2020 | |||
| WEISELL, R.C | |||
| Body mass index as an indicator of obesity | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| COMERFORD, K.B | |||
| et al | |||
| The Beneficial Effects α-Cyclodextrin on Blood Lipids and Weight Loss in Healthy Humans | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| СЕЛИНА И.И | |||
| Сравнительное изучение аминокислотного состава листьев | |||
Авторы
Даты
2024-09-17—Публикация
2022-03-11—Подача