Область техники
Изобретение относится к области медицины, фармацевтики, ветеринарии, биологии, биотехнологии и может быть использовано при лечении ран и ожогов.
Уровень техники
Хиноны нашли применение в медицине как противовирусные, противогрибковые, антигипоксические, антибактериальные, антиишемические и противоопухолевые лекарственные соединения. Интерес к применению хинонов в медицине, косметологии и косметике неизменно растет (Ferreira et al., 2021). Примерами исследований, связанных с применением хинон-содержащих препаратов для различных фармацевтических целей, могут служить патент WO 2011/137126 А1 на применение хинонов в области офтальмологии и патент ES 2663709 Т3 на применение фармацевтической композиции, содержащей токотриенолхинон, выбранный из группы, состоящей из альфа-триготриенолхинона, бета-токотриенолхинона, гамма-токотриенолхинона и дельта-токотриенолхинона, или смесь токотриенолхинонов при лечении или уменьшении повреждений нейронов, связанных с эпизодом церебральной ишемии или гипоксией у млекопитающих. Патент US 9,090,576 В2 раскрывает составы и способы применения производных 2-замещенного п-хинона для лечения и профилактики заболеваний, связанных с окислительным стрессом. К таким заболеваниям относятся митохондриальные расстройства, нарушение клеточной энергетики, нейродегенеративные заболевания и болезни, связанные со старением. Убихиноны и пластохиноны относятся к полипренилированным 1,4-бензохинонам, присутствуют в растениях и животных, выполняя важные функции в транспорте электронов в митохондриях и хлоропластах и действуя как антиоксиданты (Pennock In: Pridham 1967; Thomson, 1971).
Существует ряд патентов на изобретения, где биологически активным веществом, позитивно влияющим на организм, является именно пластохинон. В патенте US 8999939 В2 пластохиноны применяются как дополнение к олигопептидам в средстве ухода за волосами для придания пышности волосам, для усиления действия против перхоти и выпадения волос. Также в патенте RU 2411229 С2 было заявлено применение некоторых известных 1,4-бензохинонов и 1,4-гидрохинонов для приготовления лекарственного средства, фармацевтической композиции на их основе, к методу лечения онкологических заболеваний, к методу индуцирования в клетке АР-1-зависимой или NF-κВ-зависимой транскрипционной активности или обеих активностей одновременно и к методу индуцирования апоптоза в клетке. В патенте US 2018/0250208 раскрывается топическое применение косметических композиций, содержащих хиноны, способных усиливать репарацию ДНК и/или предотвращать повреждения ДНК и/или повышать регуляцию генов, связанных с заживлением ран. Под понятием хиноны в патенте авторы указывают тимохинон, лапахол, миртукоммулон С или их смеси, которые могут быть включены в состав косметических композиций, предназначенных для топического применения, чтобы улучшить внешний вид кожи. Тимохинон является фотохимическим соединением, присутствующим в растении черный тмин (Nigella Sativa), и может также встречаться в растении дикий бергамот (Monarda Fistulosa), лапахол - природное фенольное соединение, выделенное из коры дерева лапачо (Handroanthus impetiginosa), миртукоммулон выделяется из растения мирт обыкновенный (Myrtus communis). В патенте СА 2986941 предлагается применение производных изохинолина для лечения диабетических ран.
Данное изобретение основывается на открытом нами феномене, связанным со способностью пластохинона защищать эритроциты крови от деформации и гемолиза при его применении для лечения ран и ожогов, с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов на пораненном участке. Для таргетной доставки вещества к мембранным структурам клеток пластохинон инкапсулируется в липосомы. Какая-либо информация в предшествующем уровне техники о защите эритроцитов крови от деформации и гемолиза путем применения пластохинона, влиянии пластохинона на сохранение толщины эпидермиса и снижение количества поврежденных волосяных фолликулов при лечении ран и ожогов отсутствует.
Сущность изобретения
Одним из аспектов изобретения является способ защиты эритроцитов крови от деформации и гемолиза путем применения пластохинона при лечении ран и ожогов.
Другим аспектом изобретения является способ применения пластохинона для сохранения толщины эпидермиса на пораненном участке при лечении ран и ожогов.
Другим аспектом изобретения является способ применения пластохинона для снижения количества поврежденных волосяных фолликулов при лечении ран и ожогов.
Другим аспектом изобретения является применение в настоящем изобретении инкапсулированного в липосомы пластохинона для увеличения эффективности действия вещества и его таргетной доставки в мембранные структуры клеток.
Другим аспектом изобретения является достижение технического результата способа защиты эритроцитов крови от деформации и гемолиза путем применения пластохинона при лечении ран и ожогов, сохранения толщины эпидермиса и снижения количества поврежденных волосяных фолликулов путем использования биологически активного вещества пластохинона в чистом виде, в виде пластохинона, инкапсулированного в липосомы, или применение фармацевтической композиции, содержащей в своем составе пластохинон.
Другим аспектом изобретения является достижение технического результата способа защиты эритроцитов крови от деформации и гемолиза путем применения пластохинона при лечении ран и ожогов, сохранения толщины эпидермиса и снижения количества поврежденных волосяных фолликулов путем топического и внутривенного применения биологически активного вещества пластохинона в чистом виде, в виде пластохинона, инкапсулированного в липосомы, или применение фармацевтической композиции, содержащей в своем составе пластохинон.
Следующим аспектом изобретения является то, что выделение из растительных тканей пластохинона, используемого при осуществлении технического результата, не привязано ни к какому определенному виду растений, что определяет широкую доступность сырья в течение всего года, включая растения, выращенные в оранжереях, сезонные сельскохозяйственные культуры, а также сорные растения и листву парковых деревьев.
Дополнительным аспектом изобретения является то, что в изобретении применяется пластохинон в неизмененной форме, полученный путем ступенчатого элюирования при хроматографировании при слабом рассеянном освещении, что позволяет снизить образование хлорофиллом синглетного кислорода, инициирующего окислительные модификации пластохинона.
Еще одним аспектом изобретения является то, что продукты гидроксилирования пластохинона по боковой изопреноидной цепи, включая моно-гидроксилированные формы пластохинона в положениях звеньев изопреноидной цепи от 1 до 9; а также ди-, три-, тетра-, пента-, гекса-, гепта-, окта-, нона-гидроксилированные формы пластохинона в положениях звеньев изопреноидной цепи от 1 до 9; а также сложные эфиры пластохинона или его гидроксилированных форм с жирными кислотами могут применяться как в качестве биологически активного вещества в чистом виде, так и в виде биологически активного вещества, инкапсулированного в липосомы, или содержащегося в составе фармацевтической композиции, применяемой для обеспечения защиты эритроцитов от деформации и гемолиза, сохранения толщины эпидермиса на поврежденном участке и снижения количества поврежденных волосяных фолликулов при лечении ран и ожогов.
Таким образом, сущность предлагаемого способа основана на способности пластохинона защищать эритроциты крови от деформации и гемолиза, сохранять толщину эпидермиса на пораненном участке кожи и снижать количество поврежденных волосяных фолликулов.
Краткое описание чертежей
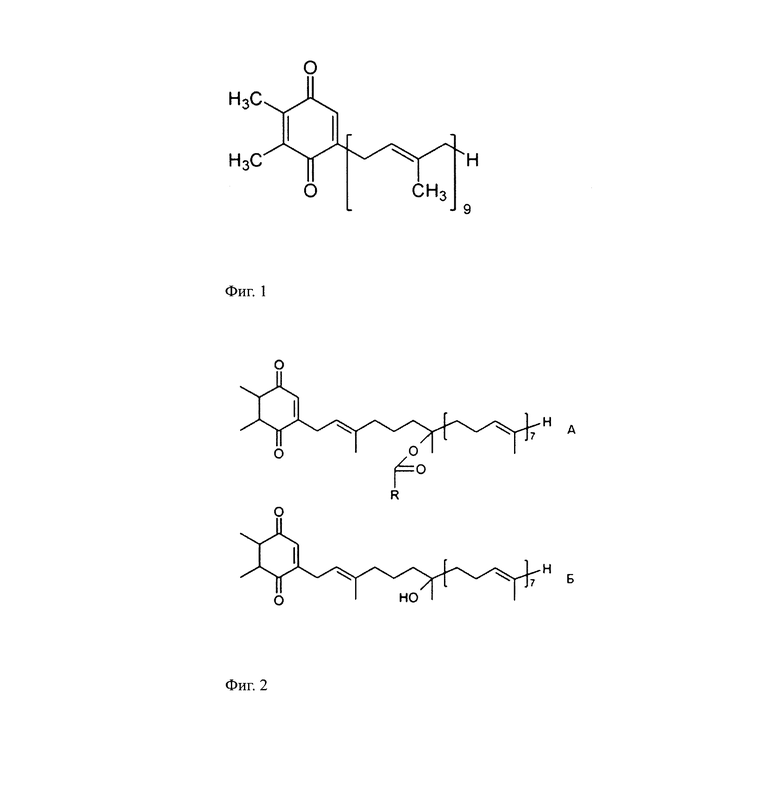
Структурная формула пластохинона иллюстрируется фиг. 1.
Структурная формула производных пластохинона где R - это гидроксилированная боковая изопреноидная цепь пластохинона, включая моно-гидроксилированные формы изопреноидной цепи в положениях звеньев от 1 до 9, а также ди-, три-, тетра-, пента-, гекса-, гепта-, окта-, нона-гидроксилированные формы изопреноидной цепи в положениях звеньев цепи от 1 до 9 или это боковая изопреноидная цепь пластохинона, содержащая от 1 до 9 сложноэфирных связей с жирными кислотами, или гидроксилированная боковая изопреноидная цепь пластохинона, содержащая одну или несколько сложноэфирных связей с жирными кислотами иллюстрируется фиг. 2.
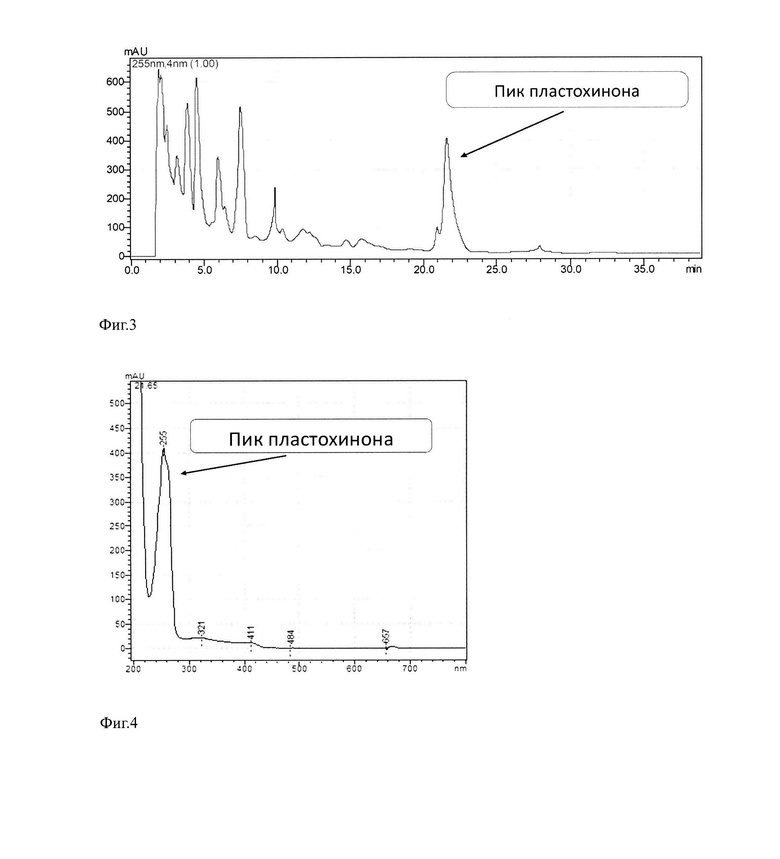
Хроматограмма очищенного от хлорофилла экстракта из растительной ткани, полученная с помощью высокоэффективной жидкостной хроматографии с показанным пиком с максимумом выхода на 22 минуте, соответствующим пластохинону, иллюстрируется фиг. 3.
Спектр поглощения пластохинона в 99% этаноле с максимум поглощения пластохинона - 255 нм иллюстрируется фиг. 4.
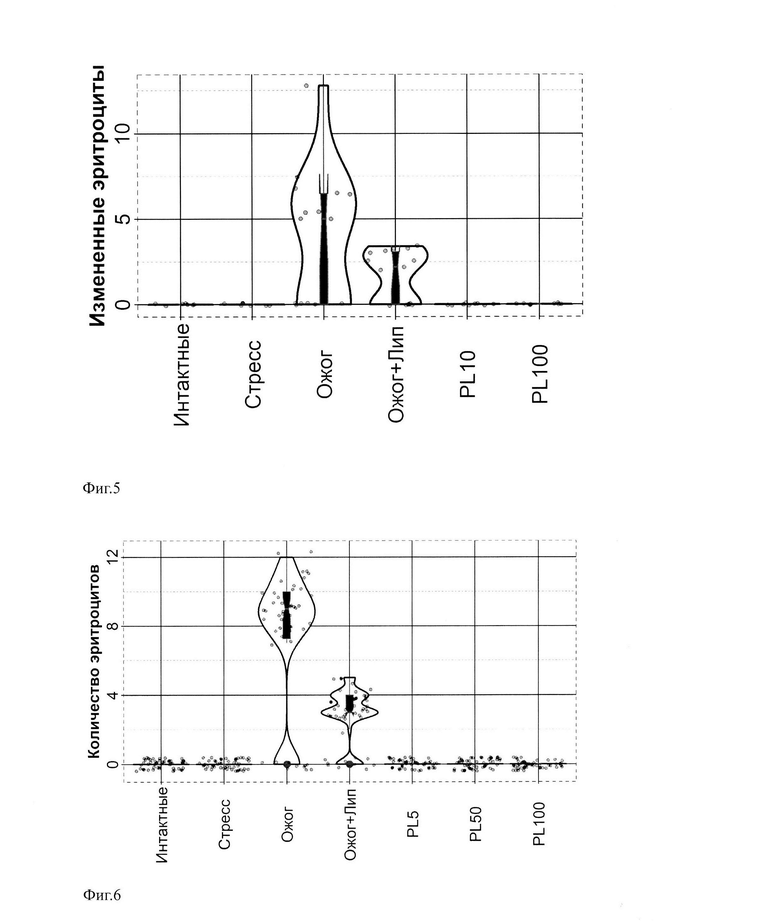
Фиг. 5 иллюстрирует графическое представление показателя Количество эритроцитов с измененной формой, число ×1012 единиц на литр крови, у интактных животных и животных через 24 часа после ультрафиолетового ожога. Относительная площадь ожога составила 8-9%. PL 10 - липосомы с 10 мкМ пластохиноном; PL 100 - липосомы со 100 мкМ пластохиноном. Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором крови. Форму эритроцитов оценивали в камере Горяева на микроскопе Leica DM 2000.
Фиг. 6 иллюстрирует графическое представление показателя Количество эритроцитов с измененной формой, число ×1012 единиц на литр крови, у интактных животных и животных через 24 часа после термического ожога II-IIIA степени. Относительная площадь ожога составила 8-9%. 1 группа - интактные животные (n=7), 2 группа - стресс-контроль (n=7) - манипуляции с животными без ожога и нанесения испытуемого вещества. Крысам 4, 5, 6 и 7 экспериментальных групп непосредственно после моделирования ожога либо i) на поврежденную кожу наносили по 0,45 мл липосомального раствора (4 группа) или липосомального раствора с 50 мкМ (PL 50) и 100 мкМ (PL 100) пластохиноном (6 и 7 группа, соответственно), либо ii) вводили липосомальный раствор с 5 мкМ пластохиноном (PL 5) внутривенно в латеральную хвостовую вену (5 группа). Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором крови. Форму эритроцитов оценивали в камере Горяева на микроскопе Leica DM 2000.
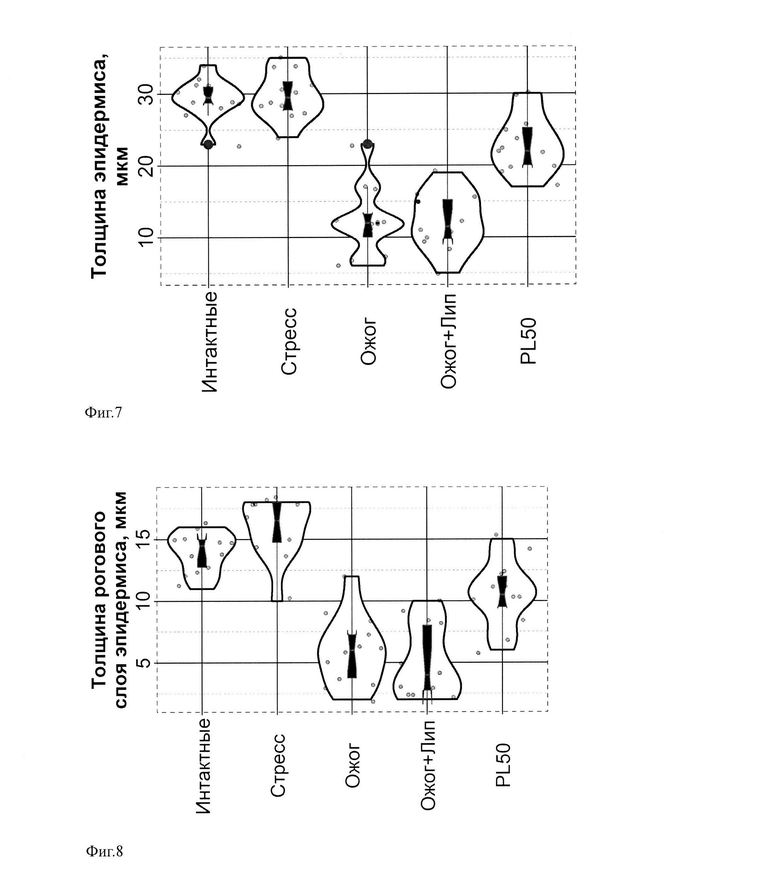
Фиг. 7 иллюстрирует графическое представление показателя Толщина эпидермиса, мкм, у интактных животных и животных через 24 часа после термического ожога II-IIIA степени. Относительная площадь ожога составила 8-9%. PL 50 - липосомы с 50 мкМ пластохиноном. Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором биоптата кожи. Гистологические срезы окрашивали гематоксилином-эозином и исследовали на микроскопе Leica DM 2500.
Фиг. 8 иллюстрирует графическое представление показателя толщины рогового слоя эпидермиса, мкм, у интактных животных и животных через 24 часа после термического ожога II-IIIA степени. Относительная площадь ожога составила 8-9%. PL 50 - липосомы с 50 мкМ пластохиноном. Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором биоптата кожи. Гистологические срезы окрашивали гематоксилином-эозином и исследовали на микроскопе Leica DM 2500.
Фиг. 9 иллюстрирует графическое представление показателя Толщина эпидермиса (без рогового слоя), мкм, у интактных животных и животных через 24 часа после термического ожога II-IIIA степени. Относительная площадь ожога составила 8-9%. PL 50 - липосомы с 50 мкМ пластохиноном. Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором биоптата кожи. Гистологические срезы окрашивали гематоксилином-эозином и исследовали на микроскопе Leica DM 2500.
Фиг. 10 иллюстрирует графическое представление показателя Количество поврежденных волосяных фолликулов (в поле зрения), штук, у интактных животных и животных через 24 часа после термического ожога II-IIIA степени. Относительная площадь ожога составила 8-9%. PL 50 - липосомы с 50 мкМ пластохиноном. Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором биоптата кожи. Гистологические срезы окрашивали гематоксилином-эозином и исследовали на микроскопе Leica DM 2500.
Описание изобретения
Определение "ран и ожогов" подразумевает повреждения тканей организма, вследствие чего запускается процесс их заживления, состоящий из серии взаимозависимых стадий - гемостаза, воспаления, пролиферации и эпителизации.
Ожог - повреждение тканей организма, возникшее от теплового, химического, электрического или радиационного воздействия.
Рана - нарушение целости кожи, тканей организма или слизистых оболочек на всю их толщину (часто и глубжележащих тканей и органов), (Kujath and Michelsen, 2008).
Фармацевтическая композиция - вещество, содержащее в своем составе пластохинон, готовое к применению и отвечающее всем требованиям фармакопеи.
Современное лечение ожоговых ран включает местное применение антибактериальных препаратов, регулярную санацию, иногда кожную пластику, а основными способами для их заживления являются наложение традиционных, антимикробных, противовоспалительных и обезболивающих повязок, доставка лекарственного препарата в рану, усовершенствованные повязки, содержащие биологические или природные агенты, лекарственные швы (Сизоненко 2003; Алексеев 2012; Rennekampf 2010; Jae На Gwak and So Young Sohn, 2017). Лечение ожогов, возникших в результате избыточного воздействия на кожу ультрафиолетового (УФ) излучения аналогично таковому при термических ожогах.
Процесс заживления повреждений тканей организма, полученных вследствие местного механического, теплового, химического, электрического или радиационного воздействия, представляет собой хорошо организованную и высоко регулируемую серию из взаимозависимых стадий - гемостаза, воспаления, пролиферации и эпителизации. Эти стадии ведут к репарации поврежденной ткани и ее восстановлению до нормального здорового и функционального состояния (Anitua et al., 2004; Monaco et al., 2003; Broughton et al., 2006; Enoch and Leaper, 2008; Singer and Clark, 1999). Основной функцией эритроцитов в крови является транспортировка кислорода к тканям для поддержания обмена веществ, а также выведение углекислоты. При заживлении поврежденных тканей, эритроциты участвуют в усилении активации и высвобождении биоактивных факторов из тромбоцитов (Santos et al., 1986; Vallles et al., 1991; Valles et al., 2002; Whelihan et al., 2012).
Эритроциты играют важную роль в усилении выработки тромбина, являющегося критически важным звеном между гемостазом и воспалением и обеспечивающим эффективное и действенное выполнение обеих стадий заживления ран (Parrish and Roides, 2017). Тромбоциты являются одними из первых реагирующих клеток, которые играют ключевую роль в формировании гемостатической пробки повреждения. Они секретируют несколько хемокинов, таких как эпидермальный фактор роста, фибронектин, фибриноген, гистамин, тромбоцитарный фактор роста, серотонин и фактор фон Виллебранда. Эти факторы также привлекают и активируют макрофаги и фибробласты (Heldin and Westermark, 1996), останавливают кровотечение и ограничивают степень повреждения. Высокие концентрации тромбина требуются для ускорения полимеризации фибрина в стабильный сгусток (Wolberg, 2007; Weisel, 2007).
Технический результат данного изобретения заключается в предоставлении способа защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов путем применения пластохинона или его производных. Применение пластохинона подразумевает использование биологически активного вещества пластохинона в чистом виде, в виде пластохинона, инкапсулированного в липосомы, или применение фармацевтической композиции, содержащей в своем составе пластохинон для обеспечения защиты эритроцитов от деформации и гемолиза, сохранения толщины эпидермиса на поврежденном участке и снижения количества поврежденных волосяных фолликулов при лечении ран и ожогов, а также подразумевает возможность использования всех природных пластохинонов в чистом виде или применение фармацевтической композиции, содержащей в своем составе природные модификации пластохинона, для обеспечения защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов. Пластохинон является хиноном, структурно представляющим собой 2,3-диметил-1,4-бензохинон с боковой цепью из девяти изопреновых единиц (фиг. 1). Наиболее часто встречающимися производными являются гидроксипроизводные пластохинона и сложные эфиры пластохинона и жирных кислот (фиг. 2). Данное изобретение включает возможность использования всех природных пластохинонов и их производных при осуществлении данного способа. Заместителями пластохинона как биологически активного вещества в чистом виде, в виде биологически активного вещества, инкапсулированного в липосомы, или содержащегося в составе фармацевтической композиции, применяемой для обеспечения защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса на поврежденном участке и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов, являются его производные - продукты гидроксилирования пластохинона по боковой изопреноидной цепи, включая моно-гидроксилированные формы пластохинона в положениях звеньев изопреноидной цепи от 1 до 9; а также ди-, три-, тетра-, пента-, гекса-, гепта-, окта-, нона-гидроксилированные формы пластохинона в положениях звеньев изопреноидной цепи от 1 до 9; а также сложные эфиры пластохинона или его гидроксилированных форм с жирными кислотами.
Источником для выделения пластохинона служат зеленые растительные ткани, которые могут быть доступны круглогодично (при выращивании в оранжерее), сезонные сельскохозяйственные культуры, а также сорные растения и листва парковых деревьев. Таким образом, выделение пластохинона не привязано ни к какому определенному виду растений, как это применено в патенте US 2018/0250208, что определяет широкую доступность сырья. Используемые при выделении пластохинона ступенчатое элюирование и слабое рассеянное освещение при хроматографировании снизило образование хлорофиллом используемых растений синглетного кислорода, инициирующего окислительные модификации пластохинона и позволило применить пластохинон в неизмененной форме (фиг. 3 и фиг. 4).
Примеры осуществления способа
В процессе работы над изобретением проводили экспериментальное моделирование термических и ультрафиолетовых ожогов на лабораторных животных (крысах). Для исследования были использованы беспородные белые крысы, у которых в течение эксперимента были взяты кровь и биоптат кожи. Были проведены исследования формы и количества эритроцитов, а также морфологические исследования биоптата кожи экспериментальных животных. Было показано положительное действие при применении пластохинона, инкапсулированного в липосомы: снижение изменения формы эритроцитов и выраженности повреждения эпидермиса и волосяных фолликулов у крыс, подвергнутых ожогу.
Липосомы с пластохиноном получили методом гидратации тонких пленок, пластохинон был инкапсулирован в липосомы методом пассивной загрузки. Способ получения липосом с пластохиноном включает стадии: а) смешивания в органических растворителях 90% фосфатидилхолина и холестерина в соотношении 5:1, а также пластохинона (в заданном количестве), б) выпаривания органических растворителей с помощью роторного испарителя из смеси, содержащей фосфатидилхолин, холестерин и пластохинон, в) ресуспендирования образовавшейся липидной пленки в фосфатном буфере (для накожного нанесения) или физрастворе (для внутривенного введения), г) экструдирования полученной суспензии на лабораторном экструдере с целью получения моноламмелярных липосом диаметром 345-455 нм. В состав 90% фосфатидилхолина входили жирные кислоты: С16:0 - 13,63%, С18:0 - 3,68%, С18:1n9 с - 11,36%, С18:2n6 с - 62,88%, С18:3n3 - 6,12%.
Эксперимент с ультрафиолетовыми ожогами был проведен на белых беспородных крысах, разделенных на 6 групп: 1 - интактные животные, 2 - стресс-контроль (манипуляции с животными без ожога и нанесения испытуемого состава), 3 - ожог без лечения, 4 - ожог+липосомы без пластохинона накожно, 5 - ожог+липосомы с 10 мкМ пластохиноном накожно, 6 - ожог+липосомы со 100 мкМ пластохиноном накожно. Шерсть животных в области ожога (спина) предварительно выбривалась до кожных покровов. Крыс наркотизировали кетамином в дозе 150 мкл из расчета на 1 крысу. Ультрафиолетовый ожог вызывали однократным облучением ультрафиолетовым светом при длине волны 280 нм, с мощностью излучения 5 мВТ/см2 в течение 4 минут. Относительная площадь ожога составила 8-9% от площади поверхности тела. Непосредственно после ультрафиолетового облучения на поврежденные кожные покровы животных экспериментальных групп 5 и 6 наносили по 0,45 мл раствора пластохинона, инкапсулированного в липосомы, с концентрацией пластохинона 10 мкМ (PL 10) и 100 мкМ (PL 100) соответственно.
При работе с термическими ожогами эксперимент был проведен на белых беспородных крысах, разделенных на 7 групп: 1 - интактные животные, 2 - стресс-контроль (манипуляции с животными без ожога и нанесения испытуемого состава), 3 - ожог без лечения, 4 - ожог+липосомы без пластохинона накожно, 5 - ожог+липосомы с 5 мкМ пластохиноном внутривенно, 6 - ожог+липосомы с 50 мкМ пластохиноном накожно, 7 - ожог+липосомы со 100 мкМ пластохиноном накожно. Шерсть животных в области ожога (спина) предварительно выбривалась до кожных покровов. Крыс наркотизировали кетамином в дозе 150 мкл из расчета на 1 крысу и подвергали контактному действию сфокусированного источника термического ожогового повреждения. Термический ожог вызывали прибором для моделирования термических ожогов, что соответствовало, согласно морфологическим исследованиям, ожогу II-III степени. Непосредственно после термического воздействия на поврежденные кожные покровы животных экспериментальных групп 6 и 7 наносили по 0,45 мл раствора пластохинона, инкапсулированного в липосомы с концентрацией пластохинона 50 мкМ (PL 50) и 100 мкМ (PL 100), соответственно. Животным 5 группы после нанесения ожога вводили физраствор с 5 мкМ пластохиноном, инкапсулированным в липосомы, внутривенно в латеральную хвостовую вену.
Животных декапитировали под эфирным наркозом через 24 часа после нанесения ожога с последующим забором крови. Кровь животных забиралась в гепаринизированные пробирки. Количество эритроцитов и их форму оценивали в камере Горяева на микроскопе Leica DM2000. Подсчет эритроцитов проводили по следующей формуле: N=m*4000*200/80=m*10000, где N - искомое количество эритроцитов в 1 мкл крови, m - число эритроцитов в 5 больших квадратов камеры Горяева (в 1 большом квадрате - 16 малых квадратов), 80 - количество подсчитанных маленьких квадратов камеры Горяева (5*16=80); 200 - степень разведения крови; 4000 - множитель, который приводит результат объема в 1 мкл крови, поскольку объем маленького квадратика составляет 1/4000 мм (сторона 1/20, а внутри 1/10 мм). Для определения количества эритроцитов полученную цифру умножали на 106. Количество эритроцитов выражали в 1012 в 1 л крови. Эритроцитами с измененной формой считали эритроциты одноконтурные или двухконтурные, в виде лимонной дольки, в виде овального кольца, эллипсоида (вытянутые) и в виде песочных часов.
Биоптат кожи до обработки фиксировали в 10%-м растворе нейтрального формалина. Гистологические срезы окрашивали гематоксилином-эозином и исследовали на микроскопе Leica DM 2500 (окуляр ×10, объективы ×20 и ×40), оснащенном цифровой камерой Leica DFC 320. Количество поврежденных элементов подсчитывали в 10 полях зрения и рассчитывали средний показатель исследуемых элементов кожи.
Предварительная обработка и статистический анализ данных был выполнен при помощи пакета прикладных программ R version 4.1.2 (2021-11-01). Распределение исследуемых признаков оценивали согласно критерию Шапиро-Уилка, и при условии наличия гауссовского распределения для сравнения использовались методы параметрической статистики, в обратном случае - непараметрические методы. Парное сравнение осуществляли на основании критерия Стьюдента или критерия Вилкоксона-Манна-Уитни. Множественное сравнение выполняли при помощи ANOVA (в случае гетерогенности дисперсий исследуемых признаков применяли поправку Уэлча) или Н-критерия Краскела-Уоллиса. Анализ post hoc выполняли согласно критерию Тьюки или Н-критерию Краскела-Уоллиса в модификации Данна с поправкой на множественные сравнения по методу Бенджамини-Иекутиели. Отличия считали статистически значимыми при р-значении <0.05. Визуализация данных выполнена при помощи пакета ggplot2 3.3.6. Расчет критериев Шапиро-Уилка, Стьюдента, Вилкокосона-Манна-Уитни, Краскела-Уоллиса, Тьюки, ANOVA выполнен при помощи пакета base 4.1.2. Оценка критерия Краскела-Уоллиса в модификации Данна с поправкой Бенджамини-Иекутиели осуществлена на основе пакета FSA 0.9.3.
Пример 1
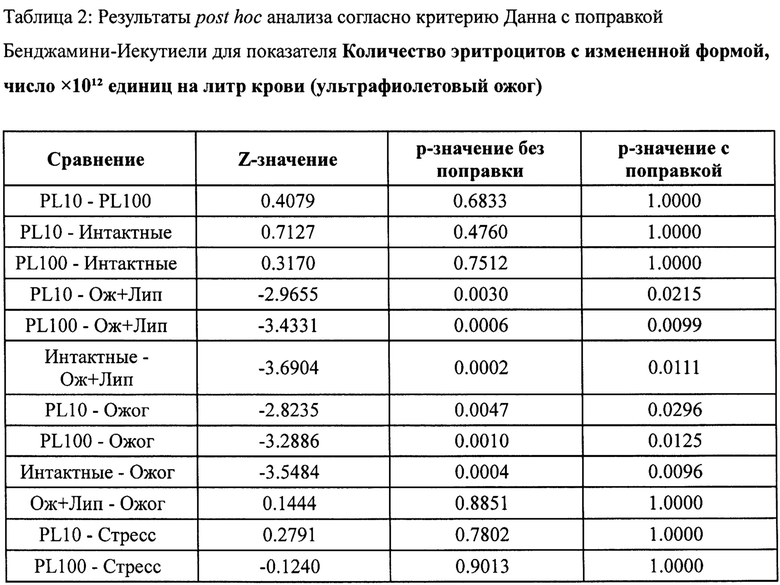
Ультрафиолетовый ожог статистически значимо увеличивал количество эритроцитов с измененной формой как по сравнению с интактными животными, так и по сравнению с группой стресс-контроля (фиг. 5, табл. 1, 2). После нанесения пластохинона, инкапсулированного в липосомы (10 мкМ и 100 мкМ), на кожные покровы животных, эритроциты с измененной формой не обнаруживались, что свидетельствует о защитном эффекте пластохинона на эритроциты при ожогах, в частности защите эритроцитов от деформации и последующего гемолиза.
Описательная статистика (в формате Среднее значение ± среднеквадратическое отклонение) представлена ниже:


Пример 2
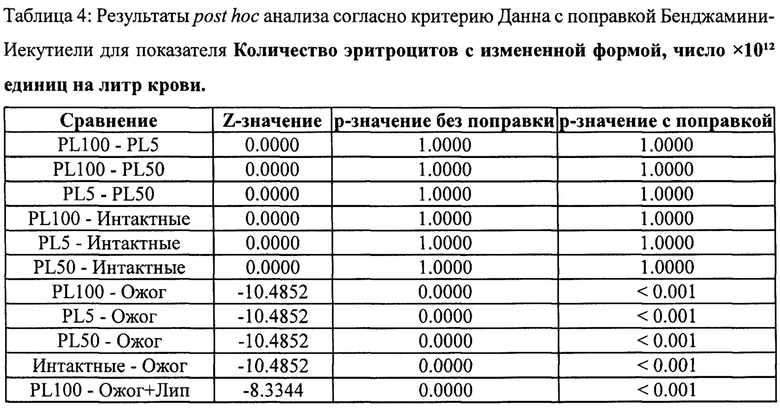
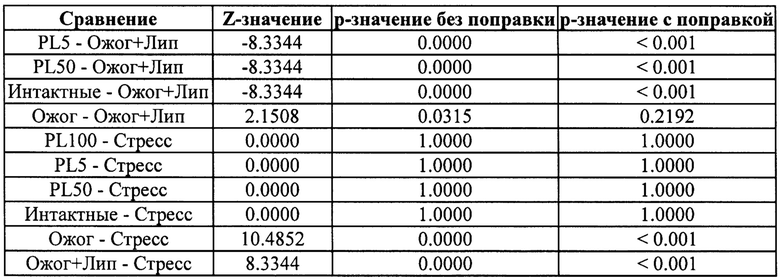
Термический ожог также статистически значимо увеличивал количество эритроцитов с измененной формой, как по сравнению с интактными животными, так и по сравнению с группой стресс-контроля (фиг. 6, табл. 3, 4). Как после нанесения пластохинона, инкапсулированного в липосомы, на кожные покровы животных (50 мкМ), так и после внутривенного введения физраствора с 5 мкМ пластохиноном, инкапсулированным в липосомы, эритроциты с измененной формой не обнаруживались, что также свидетельствует о защитном эффекте пластохинона на эритроциты при ожогах.

Для показателя Количество эритроцитов с измененной формой, число ×1012 единиц на литр крови, в исследуемых группах найдены статистически значимые отличия (согласно критерию Краскела-Уоллиса, χ2-статистика: 257.61, р-значение <0.001).
Пример 3
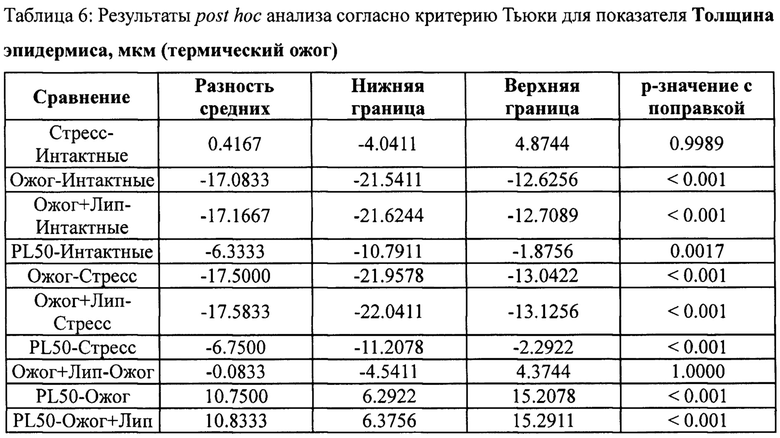
Толщина эпидермиса (фиг. 7, табл. 5, 6), включая толщину рогового слоя эпидермиса (фиг. 8, табл. 7, 8) и толщину эпидермиса без рогового слоя (фиг. 9, табл. 9, 10), а также повреждение волосяных фолликулов (фиг. 10, табл. 11, 12) увеличивались в группе животных с термическим ожогом, как по сравнению с интактными животными, так и по сравнению с группой животных стресс-контроля; соответственно, ожог вызвал негативные статистически значимые изменения всех исследуемых показателей. Добавка пластохинона, инкапсулированного в липосомы, оказывала защитный эффект на исследуемые структуры кожи, подтверждая протекторную роль пластохинона при ожогах кожных покровов. Описательная статистика (в формате Среднее значение±среднеквадратическое отклонение) представлена ниже:

Для показателя Толщина эпидермиса, мкм в исследуемых группах найдены статистически значимые отличия (согласно критерию ANOVA, F-статистика: 60.87, р-значение <0.001).
Описательная статистика (в формате Среднее значение ± среднеквадратическое отклонение) представлена ниже:

Для показателя Толщина рогового слоя эпидермиса, мкм в исследуемых группах найдены статистически значимые отличия (согласно критерию Краскела-Уоллиса, χ2-статистика: 44.76, р-значение <0.001).
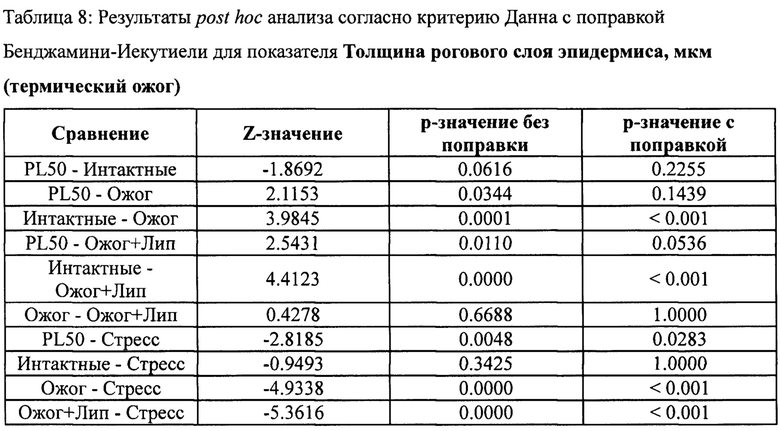
Описательная статистика (в формате Среднее значение ± среднеквадратическое отклонение) представлена ниже:

Для показателя Толщина эпидермиса (без рогового слоя), мкм в исследуемых группах найдены статистически значимые отличия (согласно критерию ANOVA, F-статистика: 53.54, р-значение <0.001).

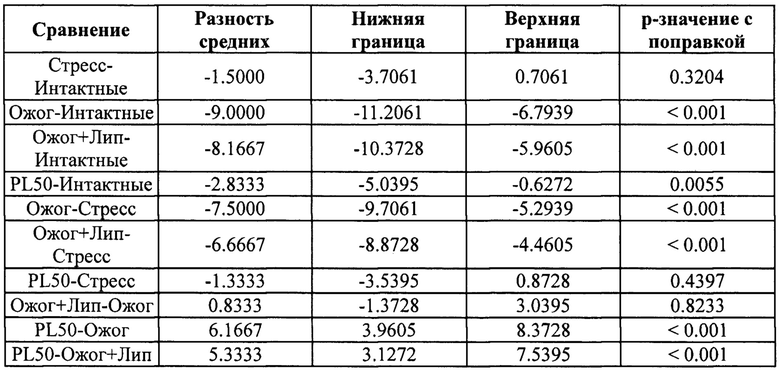
Описательная статистика (в формате Среднее значение ± среднеквадратическое отклонение) представлена ниже:

Для показателя Количество поврежденных волосяных фолликулов (в поле зрения) в исследуемых группах найдены статистически значимые отличия (согласно критерию Краскела-Уоллиса, χ2-статистика: 57.49, р-значение <0.001).
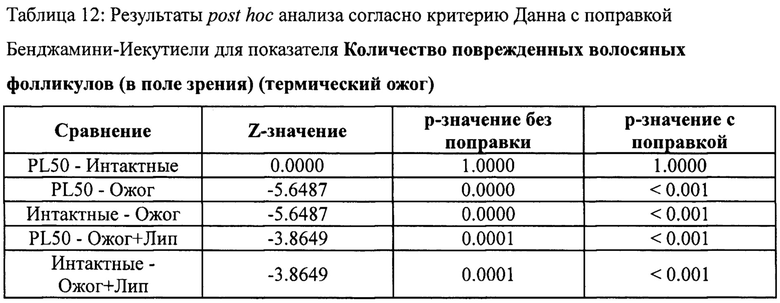
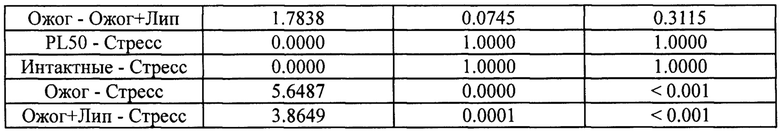
Промышленная воспроизводимость
Различные повреждения тканей организма человека и расходы на их лечение являются одной из основных проблем здравоохранения. Только в странах Северной Америки более 8,2 млн человек страдают от ран, а стоимость лечения варьируется от 28,1 до 97,6 млрд долларов. В 2018 году объем мирового рынка средств для лечения ран оценивался в 18,4 млрд долларов США, и ожидается, что с 2019 по 2026 год он будет расти с годовым темпом роста 3,9% (Chandan K. Sen, 2021). Способ защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса на пораненном участке и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов путем применения пластохинона характеризуется надежностью и воспроизводимостью эффектов, что подтверждено в результате проведения большого числа экспериментов на протяжении нескольких лет исследований. Применяемые вещества для осуществления способа являются естественными пластохинонами, а сырьем для их получения служат зеленые растительные ткани, которые доступны круглогодично (при выращивании в оранжерее), сезонные сельскохозяйственные культуры, сорные растения и листва парковых деревьев, что определяет широкую доступность и дешевизну вышеупомянутого сырья.
Источники информации
Ferreira, V.F., de Carvalho, A.S., Ferreira, P.G., Lima, C.G.S., de С da Silva F. (2021) Quinone-Based Drugs: An Important Class of Molecules in Medicinal Chemistry. Med Chem 17(10): 1073-1085. Pennock, J.F. (1967) Chemistry of isoprenoid quinones In: Terpenoids in Plants. Pridham, J.B. (ed.), pp.129-146.
Thomson, R.H. (1971) Naturally Occurring Quinones Academic Press, London, pp. 1-197.
Сизоненко, B.A., Цепелев, В.Л. (2003) Биорегулирующая терапия в комплексном лечении больных с тяжелыми ожогами Сибирский медицинский журнал 36(1):55-58.
Алексеев, А.А., Салахиддинов, К.З., Гаврилюк, Б.К., Тюрников, Ю.И. (2012) Комплексное лечение глубоких ожогов на основе применения хирургической некрэктомии и современных биотехнологических методов, Аналы хирургии 6:41- 45.
Rennekampf Н.О. Debridement of the burn wound /Н.О. Rennekampf, M. Tenenhaus //In: H. Hyakusoku et al. (eds.) (2010) Color Atlas of Burn Reconstructive Surgery/Springer-Verlag Berlin Heidelberg. - P. 10-15.
Gwak, J. H., Sohn, S.Y. (2017) Identifying the trends in wound-healing patents for successful investment strategies PloS One 12(3): e0174203.
Anitua, E., Andia, I., Ardanza, В., Nurden, P., Nurden, A.T. (2004)Autologous platelets as a source of proteins for healing and tissue regeneration. The Journal of Thrombosis and Haemostasis 91(1):4-15.
Monaco, J.L., Lawrence, W.T. (2003) Acute wound healing an overview. Clinics in Plastic Surgery 30(1): 1-12.
Broughton, G., Janis, J.E., Attinger, C.E. (2006) The basic science of wound healing. Plastic and Reconstructive Surgery 117(7 Suppl):12S-34S.
Enoch, S., Leaper, D.J. (2008) Basic science of wound healing. Surgery (Oxford) 26(2):31-37.
Singer, A.J., Clark, R.A. (1999) Cutaneous wound healing. The New England Journal of Medicine 341(10):738-746.
Santos, M.T., Valles, J., Aznar, J., Perez-Requejo, J.L. (1986) Role of red blood cells in the early stages of platelet activation by collagen. The Journal of Thrombosis and Haemostasis 56(3):376-381.
Valles, J., Santos, M.T., Aznar, J., Marcus, A.J., Martinez-Sales, V, Portoles, M., Broekman, M.J., Safier, L.B. (1991) Erythrocytes metabolically enhance collagen-induced platelet responsiveness via increased thromboxane production, adenosine diphosphate release, and recruitment. Blood Reviews 78(1): 154-162.
Valles, J., Santos, M.T., Aznar, J., Martínez, M., Moscardó, A., Piñón, M., Broekman, M.J., Marcus, A.J. (2002) Platelet-erythrocyte interactions enhance alpha (IIb) beta (3) integrin receptor activation and P-selectin expression during platelet recruitment: down-regulation by aspirin ex vivo. Blood Reviews 99(11):3978-3984.
Whelihan, M.F., Zachary, V., Orfeo, Т., Mann, K.G. (2012) Prothrombin activation in blood coagulation: the erythrocyte contribution to thrombin generation. Blood Reviews 120(18):3837-3845.
Parrish, W.R., Roides, B. (2017) Physiology of Blood Components in Wound Healing: An Appreciation of Cellular Co-Operativity in Platelet Rich Plasma Action. Journal of Exercise, Sports & Orthopedics 4:1-14.
Heldin, C., Westermark, B. (1999) Mechanism of action and in vivo role of platelet-derived growth factor Physiological Reviews 79(4):1283-316.
Wolberg, A.S. (2007) Thrombin generation and fibrin clot structure. Blood Reviews 21(3): 131-142.
Weisel, J.W. (2007) Structure of fibrin: impact on clot stability. The Journal of Thrombosis and Haemostasis 5 Suppl 1:116-124.
Kujath, P., Michelsen, A. (2008) Wounds - from physiology to wound dressing. Deutsches Ärzteblatt International 03;105(13):239-48.
Chandan, S.K. (2021) Human Wound and Its Burden: Updated 2020 Compendium of Estimates. Advances in wound care 10(5):281-292.
Патентный поиск был произведен в поисковых системах и патентных базах данных PATENTSCOPE, Espacenet, ИПС ФИПС.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛИПОСОМА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ МЕСТНЫХ РАДИАЦИОННЫХ ПОРАЖЕНИЙ КОЖИ, ПРИМЕНЕНИЕ ЛИПОСОМ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ МЕСТНЫХ РАДИАЦИОННЫХ ПОРАЖЕНИЙ КОЖИ | 2016 |
|
RU2642957C2 |
| Применение водно-солевого раствора фуллерена Cв качестве терапевтического средства при заболеваниях атопическим дерматитом | 2016 |
|
RU2641091C1 |
| КОМПОЗИЦИЯ ДЛЯ УЛУЧШЕНИЯ СОСТОЯНИЯ КОЖИ, СОДЕРЖАЩАЯ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА ГОРМОНЫ РОСТА ЧЕЛОВЕКА | 2005 |
|
RU2401099C2 |
| Способ моделирования термического поражения кожи степени IIIA | 2019 |
|
RU2712051C1 |
| ПРОТИВООЖОГОВОЕ СРЕДСТВО НА ОСНОВЕ НАСТОЯ ЛИСТЬЕВ ОСИНЫ ОБЫКНОВЕННОЙ, ЦВЕТКОВ КАЛЕНДУЛЫ ЛЕКАРСТВЕННОЙ, РОМАШКИ ЛЕКАРСТВЕННОЙ | 2016 |
|
RU2618087C1 |
| Средство для профилактики образования патологических кожных рубцов | 2018 |
|
RU2691647C1 |
| ВВЕДЕНИЕ КЛЕТОК И КЛЕТОЧНЫХ ЭКСТРАКТОВ ДЛЯ ОМОЛАЖИВАНИЯ | 2011 |
|
RU2453301C1 |
| ВВЕДЕНИЕ КЛЕТОК И КЛЕТОЧНЫХ ЭКСТРАКТОВ ДЛЯ ОМОЛАЖИВАНИЯ | 2007 |
|
RU2421208C2 |
| СПОСОБ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ ДЕФЕКТОВ КОЖИ И СЛИЗИСТЫХ ОБОЛОЧЕК И ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2011 |
|
RU2447082C1 |
| Липосомальное лекарственное средство для лечения местных радиационных поражений кожи | 2019 |
|
RU2712079C1 |

Настоящее изобретение относится к способу защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов путем применения пластохинона, имеющего структурную формулу
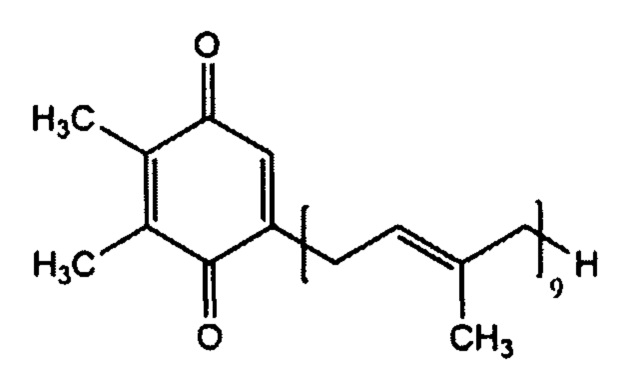
или производных пластохинона, имеющих структурную формулу
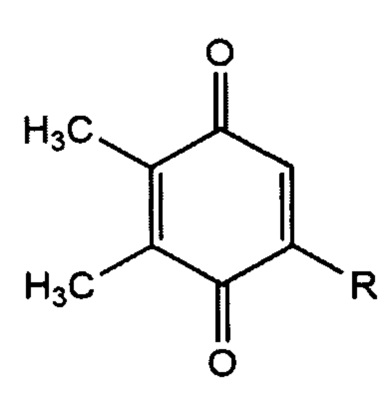 ,
,
где R - это гидроксилированная боковая изопреноидная цепь пластохинона, включая моно-гидроксилированные формы изопреноидной цепи в положениях звеньев от 1 до 9, а также ди-, три-, тетра-, пента-, гекса-, гепта-, окта-, нона-гидроксилированные формы изопреноидной цепи в положениях звеньев цепи от 1 до 9 или это боковая изопреноидная цепь пластохинона, содержащая от 1 до 9 сложноэфирных связей с жирными кислотами, или гидроксилированная боковая изопреноидная цепь пластохинона, содержащая одну или несколько сложноэфирных связей с жирными кислотами. Настоящее изобретение обеспечивает способ защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов путем применения пластохинона или его производных. 3 з.п. ф-лы, 10 ил., 12 табл., 3 пр.
1. Способ защиты эритроцитов от деформации и гемолиза с сохранением толщины эпидермиса и снижением количества поврежденных волосяных фолликулов при лечении ран и ожогов путем применения пластохинона, имеющего структурную формулу
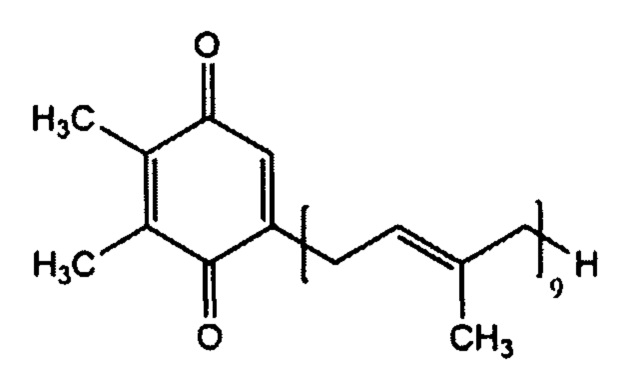
или производных пластохинона, имеющих структурную формулу
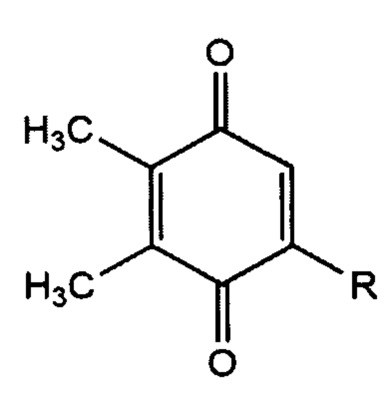 ,
,
где R - это гидроксилированная боковая изопреноидная цепь пластохинона, включая моно-гидроксилированные формы изопреноидной цепи в положениях звеньев от 1 до 9, а также ди-, три-, тетра-, пента-, гекса-, гепта-, окта-, нона-гидроксилированные формы изопреноидной цепи в положениях звеньев цепи от 1 до 9 или это боковая изопреноидная цепь пластохинона, содержащая от 1 до 9 сложноэфирных связей с жирными кислотами, или гидроксилированная боковая изопреноидная цепь пластохинона, содержащая одну или несколько сложноэфирных связей с жирными кислотами.
2. Способ по п. 1, отличающийся тем, что для обеспечения защиты эритроцитов крови от деформации и гемолиза при лечении ран и ожогов пластохинон или производные пластохинона применяют в чистом виде, в виде пластохинона или производных пластохинона, инкапсулированных в липосомы, или в виде фармацевтической композиции, содержащей в своем составе пластохинон или производные пластохинона.
3. Способ по п. 1, отличающийся тем, что для обеспечения сохранения толщины эпидермиса на пораненном участке при лечении ран и ожогов пластохинон или производные пластохинона применяют в чистом виде, в виде пластохинона или производных пластохинона, инкапсулированных в липосомы, или в виде фармацевтической композиции, содержащей в своем составе пластохинон или производные пластохинона.
4. Способ по п. 1, отличающийся тем, что для снижения количества поврежденных волосяных фолликулов при лечении ран и ожогов пластохинон или производные пластохинона применяют в чистом виде, в виде пластохинона или производных пластохинона, инкапсулированных в липосомы, или в виде фармацевтической композиции, содержащей в своем составе пластохинон или производные пластохинона.
| Liliya G | |||
| Vasilchenko et al | |||
| Phenolic antioxidants and their role in quenching of reactive molecular species in the human skin injury / Lipid Technology, 2015, vol | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| US 2010292625 A1, 18.11.2010 | |||
| М.М | |||
| Боpиcова-Мубаpакшина и др | |||
| Антиокcидантные cвойcтва плаcтоxинона и пеpcпективы его пpактичеcкого пpименения / Биофизика, 2018, | |||
Авторы
Даты
2024-05-23—Публикация
2023-05-05—Подача