Изобретение относится к области экспериментальной медицины, а именно, к экспериментальному моделированию патологических состояний, в частности, псориаза, и может применяться при изучении механизмов патогенеза этого хронического дерматоза и разработке этиопатогенетического лечения псориаза.
Изучение молекулярных механизмов индукции и развития воспаления на животных моделях позволяет оптимизировать методы лечения различных хронических воспалительных заболеваний. Одним из тяжелых воспалительных иммуно-ассоциированных заболеваний человека мультифакторной природы является псориаз, распространенность которого в популяции составляет от 1% до 3% [Greb JE, Goldminz AM, Elder JT, Lebwohl MG, Gladman DD, Wu JJ, Mehta NN, Finlay AY, Gottlieb AB. Psoriasis. Nat Rev Dis Primers. (2016) 2:16082. doi: 10.1038/nrdp.2016.82]. В патогенезе псориаза на фоне ускоренной пролиферации эпидермоцитов и нарушения их дифференцировки происходят иммунные реакции в дерме и синовиальных оболочках, возникает дисбаланс между провоспалительными и противовоспалительными цитокинами. За последние три десятилетия значительно расширилось использование доклинических животных моделей псориаза, и благодаря многим из них были получены ценные данные о патогенезе заболевания.
Известно, что с 2009 года одной из самых используемых моделей для изучения псориазоподобного воспаления у мышей является местное применение имиквимода, агониста рецепторов TLR 7/8. В течение 4-10 дней накожного применения этого препарата у мышей развивается воспалительная реакция с признаками, сходными с псориазом у человека, включающая гиперплазию эпидермиса и накопление воспалительных клеток в эпидермисе и дерме, которое опосредуется IL-17A и IL-22.
Воспаление, вызванное имиквимодом, имитирует определенные признаки псориаза, демонстрируя развитие иммунного ответа с преобладанием Th17-лимфоцитов и IL-23 в качестве ключевых факторов, а также значение плазмацитоидных дендритных клеток в роли первичных сенсоров [Garzorz-Stark N, Lauffer F, Krause L, Thomas J, Atenhan A, Franz R, Roernneberg S, Boehner A, Jargosch M, Batra R, Mueller NS, Haak S, Groβ C, Groβ O, Traidl-Hoffmann C, Theis FJ, Schmidt-Weber CB, Biedermann T, Eyerich S, Eyerich K. Toll-like receptor 7/8 agonists stimulate plasmacytoid dendritic cells to initiate TH17-deviated acute contact dermatitis in human subjects. J Allergy Clin Immunol. (2018) 141(4):1320-1333.ell. doi: 10.1016/j.jaci.2017.07.045]. Эта модель используется для изучения молекулярных и клеточных механизмов патогенеза псориаза, а также в доклинических исследованиях для оценки потенциальных методов лечения и имеет два главных преимущества - простоту воспроизведения и экономичность. Недостатком модели можно считать ее неприспособленность для изучения хронического псориазиформного воспаления. [Singh TP, Zhang НН, Hwang ST, Farber JM. IL-23- and Imiquimod-Induced Models of Experimental Psoriasis in Mice. Curr Protoc Immunol. (2019) 125(l):e71. doi: 10.1002/cpim. 71; Moos S, Mohebiany AN, Waisman A, Kurschus FC. Imiquimod-Induced Psoriasis in Mice Depends on the IL-17 Signaling of Keratinocytes. J Invest Dermatol. (2019), 139(5):1110-1117. doi: 10.1016/j.jid.2019.01.006; van der Fits L, Mourits S, Voerman JS, Kant M, Boon L, Laman JD, Cornelissen F, Mus AM, Florencia E, Prens EP, Lubberts E. Imiquimod-induced psoriasis-like skin inflammation in mice is mediated via the IL-23/IL-17 axis. J Immunol. (2009) 182(9):5836-45. doi: 10.4049/jimmunol.0802999].
В отечественной и зарубежной литературе представлены разные модификации этой модели с применением разных линий мышей и различной продолжительностью воспроизведения воспаления.
Известен «Способ формирования лабораторной модели псориаза при имиквимод-индуцированном воспалении у экспериментальных животных» [патент РФ №2736000, 03.04.2020]. Он описывает формирование острой лабораторной модели псориаза с помощью наружного применения имиквимода на предварительно побритую кожу спины мышей линии Balb/c возраста 7-8 недель в течение 10 дней 1 раз в день (в ежедневной дозе 62,5 мг). Основными недостатками способа являются невозможность моделирования длительного или хронического воспаления, характерного для псориаза, и выбор мышей линии Balb/c, в то время как оптимальны для воспроизведения такого воспаления мыши линии C57/BL6J [Schön MP, Manzke V, Erpenbeck L. Animal models of psoriasis-highlights and drawbacks. J Allergy Clin Immunol. (2021), 147(2):439-455. doi:10.1016/j.jaci.2020.04.034; Swindell WR, Michaels KA, Sutter AJ, Diaconu D, Fritz Y, Xing X, Sarkar MK, Liang Y, Tsoi A, Gudjonsson JE, Ward NL. Imiquimod has strain-dependent effects in mice and does not uniquely model human psoriasis. Genome Med. (2017), 9(1):24. doi: 10.1186/sl3073-017-0415-3; Hawkes JE, Gudjonsson JE, Ward NL. The Snowballing Literature on Imiquimod-Induced Skin Inflammation in Mice: A Critical Appraisal. J Invest Dermatol. (2017), 137(3):546-549. doi: 10.1016/j.jid.2016.10.024].
Известен также способ формирования псориазиформных высыпаний при нанесении 5% крема имиквимода на кожу спины мышей линии Balb/c 1 раз в день в течение 5 дней [van der Fits L, Mounts S, Voerman JS, Kant M, Boon L, Laman JD, Comelissen F, Mus AM, Florencia E, Prens EP, Lubberts E. Imiquimod-induced psoriasis-like skin inflammation in mice is mediated via the IL-23/IL-17 axis. J Immunol. (2009) 182(9):5836-45. doi: 10.4049/jimmunol.0802999]. Недостатком метода является слабая выраженность псориазоподобных высыпаний и патогистологических изменений в пораженной коже.
Известен патент CN114568386, 28.02.2022, согласно которому используют самок мышей линии C57BL/6 в возрасте 6-7 недель. За два дня до подготовки модели спину мыши условно разделяют как минимум на две части, сначала удаляют шерсть с первой части и наносят 5% крем имиквимода в дозе 45-55 мг в течение 5 дней, далее прекращают нанесение и наблюдают. При этом по времени опыт делится на циклы по 5 дней с перерывом в 2 дня. Итак, когда во время второго цикла шерсть на подвергнутой опыту коже начинают отрастать, выбривают следующий участок кожи и наносят на него крем имиквимод подобным же образом в течение 5 дней, после чего мышей подвергают исследованиям. Недостатком этого метода является хронологическая сжатость, малая площадь поражения кожи в опыте (менее 2 см2).
Известен также ряд аналогичных методов формирования модели псориазиформного воспаления у мышей. Например, по данным статьи Horváth и др. [Horváth S, Kemény Á, Pintér Е, Gyulai R. A Localized Aldara (5% Imiquimod)-Induced Psoriasiform Dermatitis Model in Mice Using Finn Chambers. Curr Protoc Pharmacol. (2020), 90(l):e78. doi: 10.1002/cpph.78] авторами использовались мыши-самки в возрасте 8-10 недель, массой 20-25 г. В этой модели крем имиквимод наносят на кожу спины мышей с помощью небольших (диаметром 8 мм) камер Финна, чтобы вызвать типичные симптомы псориаза и гистопатологические изменения при минимизации системного воспаления. При этом уменьшается вероятность проглатывания крема, существует возможность исследовать обработанную и контрольную кожу на одном и том же животном. Кожу мышей под анестезией выбривают и обрабатывают кремом для депиляции, а на следующий день начинают нанесение имиквимода на выбритый участок. При этом заполняют одну камеру 25 мг крема Aldara, а другую - 25 мг вазелина (контроль). Камеры Финна размещают на коже спины на расстоянии не менее 2 см друг от друга. Через 24 часа камеры удаляют пинцетом и накладывают на прежние места свежие камеры с имиквимодом и вазелином. Продолжают опыт в течение 4 дней, на 5-й день мышей подвергают исследованию. Недостатками этой модели является отсутствие формирования хронического воспаления, данная модель ограничивается острым воспалением.
Авторы статьи Karamani и др. [Karamani С, Antoniadou IT, Dimou А, Andreou Е, Kostakis G, Sideri A, Vitsos A, Gkavanozi A, Sfiniadakis I, Skaltsa H, Papaioarnou GT, Rallis MC, Maibach H. Optimization of psoriasis mouse models. J Pharmacol Toxicol Methods. (2021), 108:107054. doi: 10.1016/ j.vascn.2021. 107054] использовали самцов мышей линий BALB/c, C57BL/6J, АроЕ и ApoE/SKH-hr2 в возрасте от 6 до 15 недель. Мышей анестезировали внутрибрюшинной инъекцией смеси кетамина (100 мг/кг) и ксилазина (7 мг/кг). Затем с помощью электробритвы на спине каждой мыши выбривали участок площадью около 3,0×2,5 см. Эта процедура не выполнялась в случае безволосых мышей ApoE/SKH-hr2. Через 24 часа мышей каждой линии случайным образом делили на 4 группы (по 5 особей). Мышам контрольной группы наносили на кожу вазелин, группы IMQ ежедневно наносили 62,5 мг 5% крема имиквимод, группа IMQ+АсОН (местно) получала 62,5 мг 5% крема имиквимода, в который была добавлена уксусная кислота до концентрации 2% по массе; мышей группы IMQ+АсОН (наружно) ежедневно мазали кремом имиквимод, в то время как питьевая вода содержала 200 ммоль/л уксусной кислоты. Эксперимент проводился в течение 6 дней. Достоинством модели является использование уксусной кислоты для усиления воспаления. Недостатком этого способа является отсутствие варианта модели хронического воспаления.
Наиболее близким к заявляемому изобретению является способ, описанный в статье [Liu N, Qin Н, Cai Y, Li X, Wang L, Xu Q, Xue F, Chen L, Ding С, Hu X, Tieri D, Rouchka EC, Yan J, Zheng J. Dynamic trafficking patterns of IL-17-producing γδ T cells are linked to the recurrence of skin inflammation in psoriasis-like dermatitis. EBioMedicine. (2022), 82:104136. doi: 10.1016/ j.ebiom.2022.104136], принятый нами за прототип. Этот способ демонстрирует воспроизведение аналогичной модели на мышах C57BL/6 дикого типа (WT) (RRID:IMSR_JAX:000664) и трансгенных мышах (на основе C57BL/6): Tcrd-/- (RRID:IMSR_JAX:002120), Ccr6-/-(RRID:IMSR_JAX:005793) и Ccr2-/- (RRID:IMSR_JAX:004999). Согласно этому методу, мышам ежедневно в течение 5 дней наносят на каждое ухо 10 мг 5% крема имиквимода, чтобы вызвать псориазоподобное воспаление. Начиная с 6-го дня мыши подвергаются лечению галометазоном, редуцирующим воспаление, в качестве контроля используют вазелин, в течение 10 дней одновременно с продолжением нанесения имиквимода. После курса применения имиквимода все мыши «отдыхают» в течение 2 недель. Затем мышей повторно подвергают воздействию имиквимода в течение 7 дней. Данное исследование проводилось с целью адоптивного переноса γδ Т-клеток, изолированных из шейных лимфатических узлов от мышей с имиквимод-индуцированным воспалением наивным мышам (6-8 недель) через ретроокулярную вену. Недостатком этой модели является отсутствие сравнения модели острого и хронического воспаления, отсутствие учета пола животных (авторы не указывают пол), а, как известно, наиболее хорошо воспроизводима модель имиквимод-индуцированного воспаления на линейных мышах C57BL/6, самках. Также недостатком этой модели является небольшая площадь воспроизведенного воспаления - нанесение крема осуществлялось только в области ушей.
Задачей заявляемого изобретения является создания адекватной модели хронического псориазоподобного воспаления с максимально сформированным и выраженным воспалением, носящим хронический характер, с минимальным риском отрастания шерсти у мышей на стадиях оценки воспаления, с объективной оценкой воспаления на разных этапах и с минимальным системным действием препарата.
Решение поставленной задачи обеспечивается тем, что предложен способ формирования экспериментальной модели псориазоподобного дерматита, заключающийся в нанесении 5% крема имиквимод по 2-х этапной схеме с первичным нанесением препарата 1 раз в день в ежедневной дозе 62,5 мг/см2 на мышь в течение 7 дней на предварительно эпилированную гипоаллергенным кремом кожу спины самок мышей линии C57BL/6J возрастом 9 недель, с последующим 14-ти дневным перерывом, за время которого у животных успевает отрасти шерсть и полностью редуцироваться воспаление, и дальнейшим повторным 7-ми дневным курсом нанесения препарата в той же дозе с последующей оценкой клинических и патогистологических признаков воспаления на 7-й день воспроизведения вторичного (хронического) воспаления.
Сходство прототипа с заявляемым изобретением заключается в выборе модели имиквимод-индуцированного псориазоподобного воспаления кожи мышей, применении мышей C57BL/6J, наличии 14-дневного перерыва между первым и вторым воспроизведением воспаления.
Преимуществами заявленного изобретения в сравнении с прототипом являются: 1) использование для создания модели локализации в области спины животных, что позволяет получить большую площадь поражения, оптимальную для проведения оценки выраженности воспаления, для осуществления забора биоптата кожи как для проведения патогистологического и иммуногистохимического исследования (для патогистологического исследования оптимален размер образца кожи от 1 см х 1 см с ровными краями квадратной формы), так и для изоляции клеток для проведения цитометрического анализа; 2) возможность проведения сравнительного анализа острого и хронического псориазоподобного имиквимод-индуцированного воспаления; 3) использование самок линейных мышей, что обусловлено лучшей воспроизводимостью модели на самках; 4) использование особей в более зрелом возрасте 9 недель, что позволяет добиться максимально выраженного воспаления в сжатые сроки; 5) нанесение индуктора воспаления имиквимода в течение 7 дней, так как признаки воспаления продолжают нарастать к 7-му дню, а риск начала отрастания шерсти еще невысок, и побочные эффекты в результате системного действия имиквимода в эти сроки (до 7 дней включительно) не продемонстрированы.
Техническим результатом настоящего изобретения является то, что предложена модель хронического псориазоподобного имиквимод-индуцированного воспаления на мышах, характеризующаяся более выраженными признаками воспаления, сходными с псориазом человека. Наиболее значимыми преимуществами данного изобретения являются более высокая точность моделирования, оптимальная площадь поражения, максимальное для данной модели сходство с псориазом человека, удобство воспроизведения, универсальность модели для изучения действия топических и системных препаратов, обладающих противовоспалительными свойствами.
Заявляемое изобретение иллюстрируется таблицами 1-3 и примерами 1-2.
На табл. 1 представлена сравнительная характеристика первичного и вторичного воспроизведения по показателям эритемы, инфильтрации, шелушения и площади поражения на 7-день воспроизведения модели.
На табл. 2 представлена сравнительная характеристика первичного и вторичного воспроизведения по массе тела и толщине кожи в очаге воспаления в ходе формирования экспериментальной модели псориазоподобного дерматита в ходе вторичного воспроизведения по показателям эритемы, инфильтрации, шелушения и площади поражения в начале исследования и на 7-день воспроизведения модели.
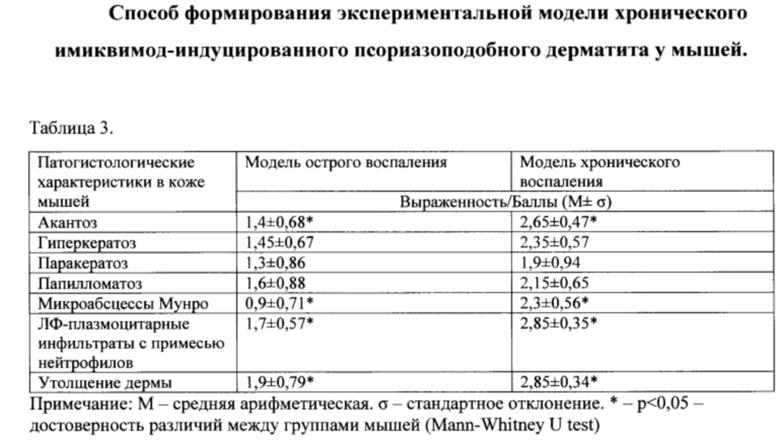
На табл. 3 представлена сравнительная характеристика первичного и вторичного воспроизведения по патогистологической картине.
Пример 1. Воспроизведение модели хронического псориазоподобного воспаления, индуцированного имиквимодом с заявленными характеристиками.
В опыт были взяты самки мышей линии C57BL/6J массой тела 20±0,6 г и возрастом 9 недель к первому дню исследования. Животные прошли карантинизацию в течение 14 дней до включения в исследование. Животных во время карантина и во время проведения опыта содержали в стандартных условиях: 20-26°С и относительной влажности воздуха 30-70%, NH3≤10 мг/м3 СО2≤0,15 об. %. Световой режим составлял 12 часов света и 12 часов темноты. Далее всем животным удаляли шерсть площадью равной примерно 2×3 см с помощью гипоаллергенного эпилирующего крема. На следующий день равномерно на кожу эпилированного участка наносили 5% имиквимод крем в ежедневной дозе 62,5 мг/см2 на животное в течение 7 дней. Аккуратно массажными движениями крем втирали до полного впитывания в кожу. В начале исследования и на 7-й день проводилась оценка выраженности воспаления с помощью измерения толщины кожи, выраженности эритемы, шелушения и инфильтрации по системе баллов, а также с помощью фотографирования области спины в месте нанесения препарата. Также регистрировали массу тела. После воспроизведения острой патологии на 7-й день мыши были оставлены без применения наружных средств на 14 дней для купирования воспаления. Спустя 14 дней отдыха на 21-й день исследования всем мышам после проведения измерений массы тела и толщины кожи было проведено 7-ми дневное нанесение индуктора патологии в тех же дозах. Проведенная сравнительная характеристика острого и хронического воспаления показала, что хроническое воспаление характеризуется более выраженными эритемой, инфильтрацией, шелушением, общим индексом тяжести псориаза (mPASI) (табл. 1). Помимо этого было отмечено, что мыши в начале индукции хронического воспаления имели более толстую кожу, чем в начале индукции острого воспаления, при этом в ходе опыта индукции хронического воспаления ее утолщение было более выраженным, чем в опыте с острым воспалением. При этом системное действие имиквимода, выраженное в уменьшении массы тела мышей, в опыте с хроническим воспалением было менее выраженным (табл. 2).
Пример 2. Различия острого и хронического псориазоподобного воспаления, индуцированного имиквимодом, по патогистологической картине.
Образцы кожи вырезали так, чтобы в микроскопическом срезе сохранялись топографические соотношения, характерные для исследуемого материала. Биоптат кожи помещали в емкость с фиксатором, объем фиксирующей жидкости превышал в 20 раз объем фиксируемого объекта. Если объект был разрезан на фрагменты толщиной более 5-6 мм, его оставляли в фиксаторе на 2-3 часа для уплотнения, после чего ткань рассекали на пластины толщиной 2-3 мм и помещали в свежий раствор фиксатора. Ткани для гистологического исследования фиксировались в 10%-ом растворе нейтрального формалина в течение 24 часов. Далее производилась проводка материала на аппарате вакуумного типа Excelsior AS (Thermo Shandon): парафин - ксилол - парафин. Суммарное время проводки 13 часов 30 минут. После по общепринятой методике фрагменты тканей заливались в парафин. Затем изготавливали срезы толщиной 3 мкм, с последующим окрашиванием гематоксилином и эозином. Анализ гистологических препаратов проводили при помощи светооптического микроскопа Carl Zeiss Axio Imager A2 (Германия) при увеличении х400. Микрофотографирование проводили при помощи цифровой фотокамеры AxioCam 105 Color 1 и программного обеспечения ZEN 2.5 (blue edition) (Германия). Для оценки воспаления кожи была применена полуколичественная оценка поражения 0-3 баллов, где: 0 - отсутствие воспаления; 1 - воспаление слабой степени: небольшое количество лимфоцитов определяется в эпидермисе, дерме и в подлежащей жировой клетчатке, носит очаговый характер, гиперкератоз незначителен; 2 - воспаление умеренной степени: увеличение количества клеток воспаления, увеличение площади поражения, небольшие участки некроза в пределах эпидермиса; 3 - выраженное воспаление: большое количество воспалительных элементов, может наблюдаться некроз, процесс распространяется обширно вплоть до подкожно-жировой клетчатки и мышечного слоя, выраженный гиперкератоз. Также каждый морфологический признак был оценен по шкале баллов от 0 до 3. Для морфометрической оценки изменений в коже была измерена толщина эпидермиса.
Результаты патогистологического исследования продемонстрировали в модели хронического воспаления более выраженные акантоз, гиперкератоз, паракератоз, папилломатоз, микроабсцессы Мунро, лимфоцитарно-плазмоцитарные инфильтраты с примесью нейтрофилов, утолщение дермы, особенно видны различия в отношении толщины кожи, акантоза, формирования микроабсцессов Мунро и лимфоцитарно-плазмоцитарных инфильтратов (табл.3).
Заявленное изобретение позволяет воспроизвести хроническое псориазоподобное воспаление, индуцированное имиквимодом с повторным нанесении имиквимода в течение 7 дней после 14-дневного интервала, у самок линейных мышей C57BL/6 в возрасте 9 недель в области спины, характеризующееся максимально выраженными признаками воспаления, оптимальной площадью поражения, отсутствием системного действия индуктора воспаления. Изобретение отличается высокой точностью моделирования хронического псориазоподобного воспаления кожи по сравнению с аналогами, характеризуется оптимальными условиями для оценки эффективности наружных и системных препаратов, проведения патогистологического, иммуногистохимического исследования и цитометрического анализа клеток кожи, и может быть использовано для оценки эффективности топических и системных препаратов, обладающих противовоспалительными свойствами, в доклинических исследованиях на мышах.
Способ формирования экспериментальной модели хронического имиквимод-индуцированного псориазоподобного дерматита у мышей.
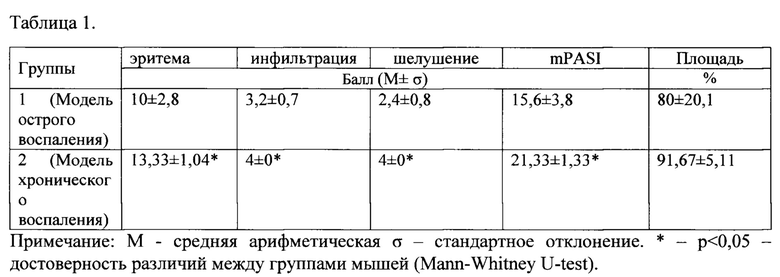
При поведении сравнительного анализа первичного (острого) и вторичного (хронического) воспаления под действием индуктора патологии имиквимода было выявлено, что хроническое воспаление характеризуется более выраженными эритемой, инфильтрацией, шелушением, общим индексом тяжести псориаза (mPASI).
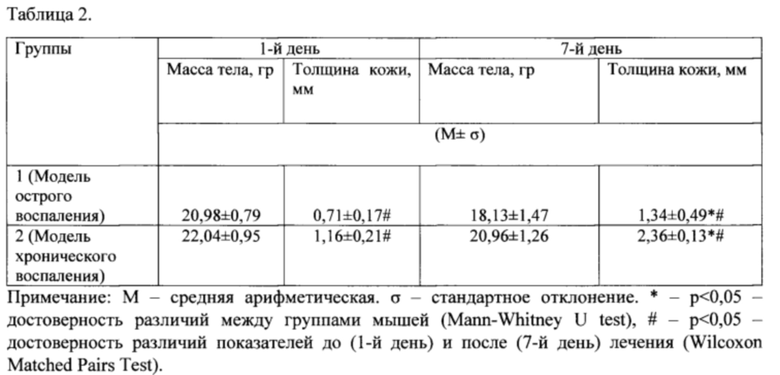
При сравнении динамики толщины кожи мышей в местах воспроизводимой патологии выявлено увеличение толщины кожи при хроническом воспалении (группа 2) (2,36±0,13) см - в 2,03 раза по сравнению с острым (группа 1) - (1,34±0,49) см - в 1,88 раз соответственно. Однако отмечены исходно разные значения толщины кожи мышей в 1-й день исследования. Так, индекс (толщина кожи 2/толщина кожи 1) в первый день составил 1,63.
Способ формирования экспериментальной модели хронического имиквимод-индуцированного псориазоподобного дерматита у мышей.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки эффективности терапии in vitro и in vivo в мышиной экспериментальной модели имиквимод-индуцированного псориазоподобного дерматита | 2023 |
|
RU2829630C1 |
| Способ формирования лабораторной модели псориаза при имиквимод-индуцированном воспалении у экспериментальных животных | 2020 |
|
RU2736000C1 |
| Способ оценки противопсориатического действия наружного препарата на лабораторной модели имиквимод-индуцированного псориаза | 2021 |
|
RU2764549C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЗМЕТИОНИНОВОГО РЕЦЕПТОРНОГО АНТАГОНИСТА ИНТЕРЛЕЙКИНА-36, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI BL21[DE3] - ПРОДУЦЕНТ БЕЗМЕТИОНИНОВОГО РЕЦЕПТОРНОГО АНТАГОНИСТА ИНТЕРЛЕЙКИНА-36 (ВАРИАНТЫ), СПОСОБ ИХ ПОЛУЧЕНИЯ, ПЛАЗМИДНЫЕ ВЕКТОРЫ pBAD15A и pET15A И ПОСЛЕДОВАТЕЛЬНОСТЬ ДНК ДЛЯ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2672816C9 |
| Фармацевтическая композиция, обладающая лечебным действием при различных кожных патологиях | 2019 |
|
RU2694059C1 |
| Фармацевтическая композиция для лечения псориаза | 2020 |
|
RU2742879C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ПСОРИАЗА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2785038C2 |
| Способ отмены генетически детерминированного ингибирования роста злокачественной опухоли в эксперименте | 2019 |
|
RU2718671C1 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| Биомедицинский клеточный продукт со специфической противоопухолевой активностью, представленный популяциями лимфокин-активированных киллеров и анти-HER2 CAR-γδΤ-ОИЛ и анти-HER2 CAR-T-NK | 2022 |
|
RU2786210C1 |
Изобретение относится к экспериментальной медицине, а именно к дерматологии. Наносят 5 % крем имиквимод на эпилированную кожу спины самок мышей возрастом 9 недель в ежедневной дозе 62,5 мг/см2 на мышь в течение 7 дней. Семидневный курс повторяют с нанесением 5% крема имиквимода в той же дозе. Способ удобен в воспроизведении, хорошо переносится животными, позволяет создать адекватную модель хронического псориазоподобного воспаления с максимально сформированным и выраженным воспалением, носящим хронический характер, и минимальным риском отрастания шерсти у мышей на стадиях оценки воспаления, позволяет объективно оценить воспаление на разных этапах без системного действия препарата на организм животного. 3 табл., 1 пр.
Способ формирования экспериментальной модели хронического имиквимод-индуцированного псориазоподобного дерматита у мышей линии C57BL/6J, характеризующийся индукцией псориазоподобного дерматита путем нанесения 5% крема имиквимода двумя курсами с 14-ти дневным перерывом, отличающийся тем, что 5% крем имиквимод наносят на эпилированную кожу спины самок мышей возрастом 9 недель в ежедневной дозе 62,5 мг/см2 на мышь в течение 7 дней, затем семидневный курс повторяют с нанесением 5% крема имиквимода в той же дозе.
| LIU N | |||
| et al | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| EBioMedicine | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Способ формирования лабораторной модели псориаза при имиквимод-индуцированном воспалении у экспериментальных животных | 2020 |
|
RU2736000C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПСОРИАЗА У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2014 |
|
RU2575338C1 |
| CN 109172576 A, 11.01.2019 | |||
| CN 112136764 A, 29.12.2020 | |||
| ЗУЕВА А.А | |||
| и др | |||
| Апробация модели | |||
Авторы
Даты
2024-06-03—Публикация
2023-07-21—Подача