Изобретение относится к области медицины, а именно к экспериментальной медицине и онкогинекологии, и может быть использовано для моделирования злокачественной опухоли тела матки в экспериментальной онкологии.
Саркомы матки представляют собой группу относительно редких злокачественных опухолей, происходящих из тканей матки, с агрессивным течением и плохим прогнозом (см. Liu J., Wang Z. Advances in preoperative identification of uterine sarcoma. Cancer diseases (Basel). 2022;14(14):3517. doi: 10.3390/cancers14143517; см. He H., Don Q., Weng S., Gu J., Yang Q., Yang G. Trends in incidence, survival, and initial treatments for gynecological sarcoma: a United States subpopulation retrospective analysis. BMC Women's Health. 2023;23(1):10. doi: 10.1186/s12905-023-02161-1). Напротив, миомы матки являются распространенными доброкачественными опухолями матки, которые поражают 40-80% женщин в течение их жизни (см. Pavone D., Clemenza S., Sorbi F., Fambrini M., Petraglia F. Epidemiology and risk factors for uterine fibroids. Best practice. RES. Clinic. Obstetrics. Gynecology. 2018;46:3-11. doi: 10.1016/j.bpobgyn.2017.09.004).
Минимально инвазивная хирургия имеет меньше послеоперационных осложнений и позволяет быстрее восстановиться, а лапароскопическое измельчение миомы матки стало широко используемой минимально инвазивной хирургической процедурой. Однако при опухолях матки, которые не диагностированы как злокачественные, до операции или интраоперационно лапороскопические вмешательства/приемы могут привести к тазово–абдоминальной диссеминации опухоли, увеличивая частоту рецидивов заболевания и сокращая выживаемость без прогрессирования и общую выживаемость (см Rein-Bennett T., Tucker L.Yu., Zaritsky E., Littell R.D., Palen T., Neugebauer R., Akstell A., Schulze P., Kronbach D., Embry-Schubert J. and al. Occult uterine sarcoma and leiomyosarcoma: incidence and survival associated with morcellation. Obstetrics. Gynecol. 2016;127:29-39. doi:10.1097/AOG.0000000000001187). Для оценки риска развития лейомиосаркомы (LMS) до хирургического лечения Kohler G. с коллегами провели анализ и опубликовали критерий на основе предоперационной оценки риска возникновения LMS. Этот показатель позволяет оценить риск LMS и адекватные хирургические варианты для каждой пациентки (см. Kohler G., Vollmer M., Nath N., Hessler P.A., Dennis K., Lehr A., Koller M., Riechmann C., Bralo H., Trojnarska D., et al. Benign uterine mass-discrimination from leiomyosarcoma by a preoperative risk score: A multicenter cohort study. Arch. Gynecol. Obstet. 2019;300:1719–1727. doi:10.1007/s00404-019-05344-0). Хотя большинство LMS диагностируется на ранней стадии (60%), 5-летняя выживаемость на всех стадиях заболевания варьируется от 25% до 76%. При первоначальном диагнозе, который свидетельствует о наличии метастатического поражения прогноз 5-летней выживаемости ухудшается до минимальных 10-15% (см Reichert V.M., Alvafay Z., Zygmunt M.T., Volmer M., Köhler G. Incidental morcellation of uterine leiomyosarcoma affects disease-free survival but does not adversely affect overall survival. J Clinic Med. 2023 Jan 11;12(2):591. doi: 10.3390/jcm12020591).
Существуют исследования, показывающие, что саркомы матки поражают примерно от 1 из 225 до 1 из 580 женщин, перенесших операцию по поводу миомы матки (см. Yorgancı A., Meydanlı M.M., Kadıoğlu N., Taşkın S., Kayıkçıoğlu F., Altın D., Atasoy L., Haberal A.N., Kınay T., Akgül M.A., et al. Incidence and outcome of occult uterine sarcoma: a multicentre study of 18,604 operations performed for suspected uterine leiomyoma. J. Gynecol. obstet. Hum. Repetition. 2020;49:101631. doi: 10.1016/j.jogoh.2019.101631), предупреждая при этом о риске распространения, связанного с внутрибрюшинной морцелляцией. В ряде исследований и мета-анализах сообщалось о частоте 0,12‰ (1:8300) и 1,43‰ (1:700) сарком, прооперированных как миома матки (см. Brohl A.S., Li L., Andikyan V., Obican S.G., Cioffi A., Hao K., Dudley J.T., Ascher-Walsh C., Kasarskis A., Maki R.G. Age-stratified risk of unexpected uterine sarcoma following surgery for presumed benign leiomyoma. Oncologist. 2015;20:433–439. doi: 10.1634/theoncologist.2014-0361; см. Nugent W., Engelke G., Reicke S., Soder R., Hennefrund J., Hasskamp T., Bung P., Weisbach W., Kohler G. Laparoscopic Supracervical Hysterectomy or Myomectomy with Power Morcellation: Risk of Uterine Leiomyosarcomas. A Retrospective Trial Including 35.161 Women in Germany. J. Minim. Invasive Gynecol. 2015;22:S2–S3. doi:10.1016/j.jmig.2015.08.013; см. Pritts E.A., Vanness D.J., Berek J.S., Parker W., Feinberg R., Feinberg J., Olive D.L. The prevalence of occult leiomyosarcoma at surgery for presumed uterine fibroids: A meta-analysis. Gynecol. Surg. 2015;12:165–177. doi:10.1007/s10397-015-0894-4). Следовательно, это редкое заболевание, связанное с плохим прогнозом и в результате у женщин появлялся высокий риск возникновения местного рецидива и отдаленных метастазов в случаях морцеллированных злокачественных образований. Тем самым появлялась неизлечимая фаза заболевания, при которой ни химиотерапия, ни лучевая терапия при данном виде рака не являются эффективными методами лечения, приводящими к выздоровлению. Кроме того, известно, что неадекватные хирургические приемы связаны с отрицательной безрецидивной и общей выживаемостью (OS) (см Raspagliesi F., Maltese G., Bogani G., Fuca G., Lepori S., De Iaco P., Perrone M., Scambia G., Cormio G., Bogliolo S., et al. Morcellation worsens survival outcomes in patients with undiagnosed uterine leiomyosarcomas: A retrospective MITO group study. Gynecol. Oncol. 2017;144:90–95. doi:10.1016/j.ygyno.2016.11.002). Предоперационная постановка морфологического диагноза с уточнением доброкачественной и злокачественной природы новообразований матки может помочь выбрать подходящий хирургический подход, избежать распространения инфекции и улучшить прогноз и общую выживаемость пациентов.
Ежегодная заболеваемость саркомами матки составляет примерно 1,7 на 100 000 женщин, при этом пик заболеваемости приходится на молодой возраст начала заболевания, на долю которого приходится 3-10% злокачественных новообразований матки (см. Mallmann P. Sarcoma of the uterus - difficult to diagnose, difficult to treat. Oncol. RES. Treatment. 2018;41:674. doi: 10.1159/000494393; см. He H., Don Q., Weng S., Gu J., Yang Q., Yang G. Trends in incidence, survival, and initial treatments for gynecological sarcoma: a United States subpopulation retrospective analysis. BMC Women's Health. 2023;23(1):10. doi: 10.1186/s12905-023-02161-1). Подтипами сарком матки являются LMS, эндометриальные стромальные саркомы (ESS) и аденосаркомы (AS). Факторы риска связаны с ожирением, приемом эстрогена и прогестерона в период менопаузы, оральных контрацептивов, лучевой терапией органов малого таза в анамнезе, генетическими дефектами и приемом тамоксифена (см. Liu J., Wang Z. Advances in preoperative identification of uterine sarcoma. Cancer diseases (Basel). 2022;14(14):3517. doi: 10.3390/cancers14143517). Клиническая картина саркомы матки аналогична клинической картине миомы матки, которая может проявляться нерегулярными вагинальными кровотечениями, образованиями в области таза и болями в области таза и живота.
LMS является наиболее распространенным типом сарком матки, на долю которого приходится более 60% случаев, со средним возрастом начала заболевания 48 лет, а опухоль в основном представляет собой единичные крупные образования с мягкими, «рыбообразными» на разрезе поверхностями, в основном расположенные в миометрии или подсерозным слоем матки (см. Roberts M.E., Ainardi J.T., Chu K.S. Uterine leiomyosarcoma: literature review and update on management options. Gynecol. oncol. 2018;151:562-572. doi: 10.1016/j.ygyno.2018.09.010). Мезенхимальные саркомы эндометрия далее подразделяются на стромальные саркомы эндометрия низкой степени злокачественности (LG-ESS), стромальные саркомы эндометрия высокой степени злокачественности (HG-ESS) и недифференцированные стромальные саркомы эндометрия (USS). Являясь вторым по распространенности типом саркомы матки, LG-ESS менее злокачественна, возраст начала заболевания в последние годы стал моложе, и более 50% случаев приходится на женщин в пременопаузе. Опухоли могут располагаться в эндометрии, миометрии и субплазме, а яичник является наиболее частым местом внематочных поражений, обычно связанных с эндометриозом (см. Arend R., Doneza J.A., Wright J.D. Uterine carcinosarcoma. Further. Opinion. oncol. 2011;23:531-536. doi: 10.1097/CCO.0b013e328349a45b). HG-ESS был вновь включен в качестве отдельного объекта в классификацию Всемирной организации здравоохранения 2014 года, как редкий, со средним возрастом пациенток начиная с 50 лет, а по биологическомц поведению и прогнозу, промежуточный между LG-ESS и UUS (см. Konklin K.M., Longakr T.A. Endometrial stromal tumors: A new WHO classification. Adv. Anat. Pathologist. 2014;21:383-393. doi: 10.1097/PAP.0000000000000046).
Опухоли часто проявляются в виде внутриматочных полипоподобных выпуклостей или узелков миометрия. Разрезанные участки опухолей имеют вид «рыбьей мякоти», а кровоизлияния и некроз являются обычным явлением. UUS представляет собой высокогетерогенную интерстициальную опухоль матки с высокой злокачественностью, встречается редко и обычно встречается у женщин в постменопаузе, а патологический диагноз не требует специфического дифференциального диагноза и диагностируется путем исключения (см. Cotzia P., Benaid R., Mullani K., Oliva E., Felix A., Ferreira J., Soslow R.A., Antonescu C.R., Ladanya M., Chiang S. Undifferentiated uterine sarcomas are poorly recognized high-grade endometrial stromal sarcomas. Am. J. Surg. Pathologist. 2019;43:662-669. doi: 10.1097/PAS.0000000000001215). Опухоль образует коричневую или белую полиповидную массу в полости матки с нечеткими границами и «рыбообразной» поверхностью разреза; часто встречаются некроз и кровотечение (см. Nucci M.R. Practical issues related to uterine pathology: endometrial stromal tumors. Maud. Pathologist. 2016;29:92–103. doi: 10.1038/modpathol.2015.140). Аденосаркома (АС) представляет собой смешанную опухоль с низким злокачественным потенциалом, состоящую из смеси доброкачественного железистого эпителия и саркомы низкой степени злокачественности, с широким возрастным диапазоном начала заболевания, встречающуюся в основном у женщин в постменопаузе. Подавляющее большинство АС происходит из эндометрия (85%), тогда как другие происходят из шейки матки или вне матки и имеют полиповидный вид, со средним диаметром 5 см (см. Natenson M.J., Ravi W., Fleming N., Van W.L., Conley A. Uterine adenosarcoma: a review. Curr. Oncol. Rep. 2016;18:68. doi: 10.1007/s11912-016-0552-7).
Несмотря на их относительную редкость, саркомы матки являются агрессивными с различными патологическими типами, нетипичными клиническими симптомами и крайне неблагоприятным прогнозом. Поэтому раннее их выявление имеет большое значение для улучшения прогноза пациентки. Успешное предоперационное прогнозирование саркомы матки и направление пациенток в специализированное медицинское учреждение, значительно улучшит выживаемость пациенток (см. Benson S., Miah A.B. Sarcoma of the uterus - modern perspectives. Int. J. Women's health. 2017;9:597-606. doi: 10.2147/IJWH.S117754).
В настоящее время существуют преимущества и недостатки каждого из клинических методов, используемых для предоперационной идентификации саркомы матки. Повышенные сывороточные маркеры CA-125, LDH, CRP и D-димер могут указывать на саркому матки, но они чувствительны к другим факторам и не обладают специфичностью. Ультразвук доступен и является лучшим методом скрининга, но не позволяет точно определить доброкачественность или злокачественность новообразований матки. Хотя МРТ имеет хорошее разрешение для мягких тканей, некоторые дегенеративные типы миомы матки имеют схожую интенсивность сигнала, и существует определенная вероятность ошибочного диагноза. ПЭТ-КТ обладает высочайшей точностью, но является дорогостоящей и требует специальных технических условий. Патология, связанная с предоперационной биопсией, является золотым стандартом диагностики, но необходим высокий уровень квалификации врача, чтобы исключить медицинский посев и неадекватный отбор проб при обследованиях.
Учитывая растущий объем знаний о саркоме матки, предлагается все больше методов предоперационной диагностики, но врачи по-прежнему сталкиваются со многими проблемами. Во-первых, большинство исследований являются одноцентровыми, которые не полностью отражают ситуацию из-за недостаточного объема данных, отсутствия внешней валидации и низкой надежности модели. Во-вторых, большинство исследований основаны на ретроспективном анализе данных, не имеют стандартизированных протоколов и наблюдения проводились в короткое время. Наконец, с ростом междисциплинарной интеграции гинекологи должны разбираться в новых областях, таких как искусственный интеллект и молекулярная биология, в дополнение к своим превосходным клиническим навыкам, что ставит перед клиницистами более сложную задачу (см. Zhang L., Huang J., Liu L. Advanced deep learning network based combined with cost-sensitive learning for early detection of ovarian cancer in a color ultrasound system. J. Med. Syst. 2019;43:251. doi: 10.1007/s10916-019-1356-8). Pergialiotis V. et al. (2018) сообщили, что эти проблемы будут постепенно решаться при более широком междисциплинарном сотрудничестве. Можно облегчить исследования, создав экспериментальные модели гинекологического рака для изучения патогенеза злокачественного процесса, выявления патогномоничных эффективных факторов ранней диагностики и привлекая специалистов в области компьютерных наук и базовой медицины (см. Pergialiotis V., Pouliakis A., Parthenis C., Damaskou V, Chrelias C, Papantoniou N, Panayiotides I. The utility of artificial neural networks and classification and regression trees for the prediction of endometrial cancer in postmenopausal women. Public Health. 2018;164:1-6. doi: 10.1016/j.puhe.2018.07.012).
В целом, учитывая ухудшение результатов, связанных с лапароскопической гистерэктомией с силовым морцеллятором или миомэктомией, возрастает необходимость выявления саркомы матки до операции. Потребуется некоторое время, чтобы новые тесты на онкомаркеры были внедрены в медицинских учреждениях. Недавние результаты, основанные на многопараметрической визуализации и гистологии МРТ для дифференциации сарком матки от миомы матки, обнадеживают, но все еще являются сложными. Долгосрочные результаты предоперационной пункционной биопсии также находятся под наблюдением. Необходимо продолжать изучать саркомы матки в будущем.
За последние два десятилетия экспериментальные модели сыграли жизненно важную роль в продвижении понимания патогенетических основ канцерогенеза. В моделирование внедряются новые технологии, продвинувшие наше понимание генеза, прогрессирования и метастазирования опухолей. Несколько основных направлений остаются недооцененными и недостаточно изученными. Базисом экспериментальной онкологии является создание различных экспериментальных моделей злокачественного процесса на животных. Объектом изучения в эксперименте, как правило, являются грызуны – крысы и мыши, на которых перевивают различные штаммы опухолей.
Перевиваемые опухоли имеют ряд значительных преимуществ перед спонтанными и индуцированными. Прежде всего, они делают возможной постановку массовых экспериментов, так как легко и быстро могут быть получены в большом количестве. Другим преимуществом штаммов перевиваемых опухолей является относительное постоянство их строения и биологических свойств.
Известно, что ортотопические модели лучше воспроизводят клинический рак, особенно в отношении микроокружения опухоли, по сравнению с подкожными моделями (см. Zhang W., Fan W., Rachagani S., Zhou Z., Lele S.M., Batra S.K., Garrison J.C. Comparative Study of Subcutaneous and Orthotopic Mouse Models of Prostate Cancer: Vascular Perfusion, Vascular Density, Hypoxic Load, and Effectiveness of BB2r Targeting. sci. Rep. 2019;9:11117. doi: 10.1038 / s41598-019-47308-zet).
Техническим результатом настоящего изобретения является создание модели саркомы матки у самок белых беспородных крыс.
Технический результат достигается тем, что самкам белых беспородных крыс в просвет правого маточного рога с помощью внутривенного катетера с инъекционным портом 22G, 0,9 х 25 mm вводят 0,5 мл опухолевой взвеси саркомы М1 в количестве 2,5-3,5х106 клеток.
Изобретение «Способ создания модели саркомы матки» является новым, так как оно неизвестно в области экспериментальных исследований в онкологии о развитии трансплантированной саркомы М1 в матке самок крыс.
Новизна изобретения заключается в том, что фрагмент растущей подкожной саркомы М1 трансплантируют в правый рог матки самкам крыс, где она растет и развивается.
Для лучшего понимания способа приводим фигуры.
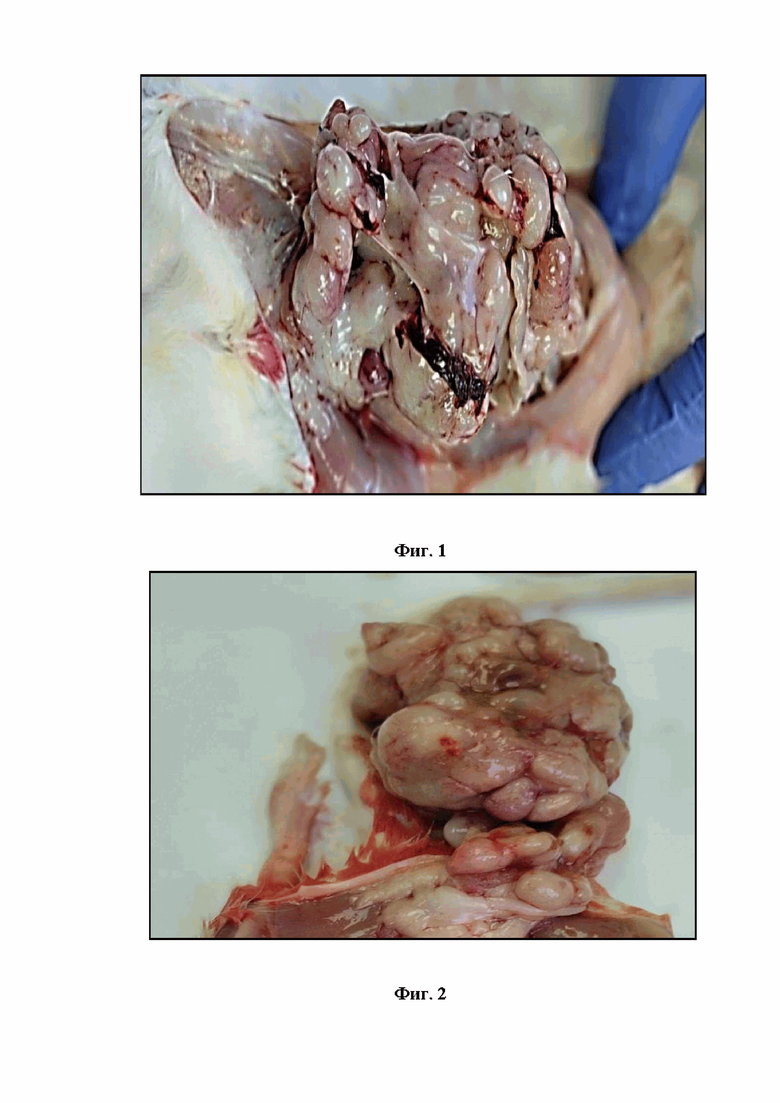
Фиг. 1. Опухолевые узлы в брюшной полости.
Фиг. 2. Опухолевые образования в полости матки.
Фиг. 3. Опухолевое поражение брыжейки (лимфоузлы).
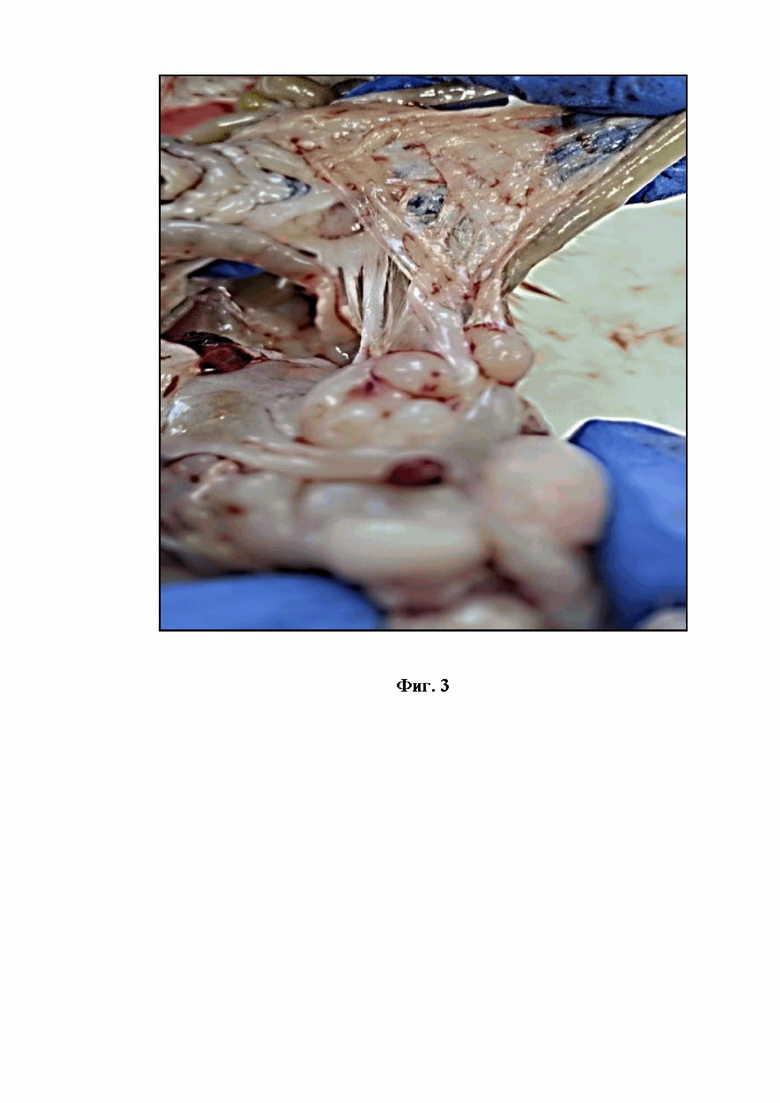
Фиг. 4. Опухолевые образования в печени.
Способ создания модели саркомы матки является промышленно применимым, так как может быть использован в научно-исследовательских учреждениях онкологического профиля для воспроизведения экспериментальной модели роста злокачественной стромальной опухоли в матке, как модель саркомы матки для изучения ее роста, особенностей метастазирования.
В эксперименте in vivo нами использовались белые беспородные лабораторные крысы, в качестве экспериментальной модели опухоли использовали штамм крысиной саркомы М1. Выбор опухолевого штамма обусловлен тем, что саркома М1 относится к числу быстрорастущих, агрессивных опухолей с достаточно коротким инкубационным периодом, отличается большой биомассой и высокой степенью перевиваемости (98-100%). Штамм перевиваемой опухоли получили из банка опухолевых штаммов НМИЦ онкологии им. Н.Н. Блохина и поддерживали in vivo в виварии ФГБУ «НМИЦ онкологии» Минздрава России. Работа выполнена с соблюдением международных рекомендаций по проведению исследований с использованием лабораторных животных, изложенных в «Европейской конвенции по защите позвоночных животных, используемых в экспериментальных и других научных целях».
Способ создания модели саркомы матки выполняется следующим образом.
Подготовка саркомы М1 к перевивке. Инструменты, посуду, руки дезинфицируют обычным способом. Помощник декапитирует крысу с растущей подкожной саркомой М1, обрабатывает кожу над опухолью 70% спиртом. Отступив от опухоли 1 – 2 см экспериментатор отсепаровывает кожу и отгибает её таким образом, чтобы шерсть не попала внутрь. Подкожный опухолевый узел саркомы М1 выделяют, промывают стерильным физиологическим раствором и разрезают вдоль. Вырезают кусочки жизнеспособной ткани, имеющей серовато-розовый цвет, и переносят в стерильную чашку Петри, после чего иссекают оставшиеся мелкие участки некроза, прослойки соединительной ткани, сгустки крови, наличие которых ухудшает условия последующего приживления; кусочки ополаскивают стерильным физиологическим раствором. Опухолевую ткань пропускают через пресс для измельчения и разводят стерильным физиологическим раствором. Для перевивки используют 2,5-3,5 млн. опухолевых клеток в 0,5 мл физиологического раствора.
Трансплантация саркомы М1 в матку самок крыс.
Анестезию проводили стандартно ксилазин-золетиловым наркозом. Ксиланит (ЗАО «НИТА-ФАРМ, Россия, г. Саратов) вводили внутримышечно 0,1 мл/100г веса животного. Далее через 10-15 минут вводили золетил («Virbac» Франция) в дозе 5мг/100г веса животного. Через 1-2 минуты пропадал рефлекс переворачивания, максимальный эффект достигался через 5-7 минут после инъекции. Наркоз верифицировали по исчезновению реакции на болевые раздражители (укол лапы) и угнетению роговичного рефлекса. Ксила-золетиловый наркоз использовался для сопровождения крупных оперативных вмешательств, средней продолжительностью от 30 минут до 2-х часов.
В качестве объекта оперативного вмешательства выступали нелинейные белые лабораторные крысы-самки, общим числом 20, массой 250 ± 25 грамм. Белым беспородным крысам-самкам в условиях наркоза в асептических условиях (удаление шерсти и двукратная обработка дезинфицирующим раствором операционного поля) скальпелем проводится лапаротомия. Длина разреза 2 см. Мочевой пузырь, как правило, наполненный, выводится в рану и отклоняется кпереди. Осторожно, потягивая за дольки сальника, в рану выводятся маточные рога. Правый маточный рог фиксируется мягким пинцетом. В просвет правого маточного рога с помощью внутривенного катетера с инъекционным портом 22G (0,9 х 25 mm) вводят 0,5 мл опухолевой взвеси саркомы М1, т.е. вводится 2,5-3,5х106 клеток. Рог матки перевязывают кетгутом для предотвращения излития взвеси в брюшную полость.
После этого рана трижды обрабатывается антисептическим раствором (фурациллин 1:5000). Матка с ее рогами, мочевой пузырь, доли сальника возвращаются в брюшную полость. Кетгутом 4/0 на атравматической игле тремя одиночными узловыми швами ушивается дефект брюшины. Таким же способом ушивается кожа, операционная рана обрабатывается 2% раствором Н2O2. Повязка на рану не накладывается в связи со сложностью ее фиксации и низким риском нагноения раны.
Наблюдение за развитием опухолевого процесса проводилось в течение 14 суток. После умерщвления животных под эфирным наркозом по стандартной методике производили лапаротомию и фиксировали рост саркомы матки.
Указанным образом было прооперировано 20 самок крыс.
Через 7 суток с момента прививки 3 животных были подвергнуты эвтаназии для контроля роста саркомы. В этот срок макроскопически определяется опухолевый узел в области дна правого рога матки крыс, его размеры составляют 25,5 ±2,3 мм.
Через 14 суток у оставшихся животных диагностировано увеличение живота в объеме. Животные были подвергнуты эвтаназии. При вскрытии: в брюшной полости определялось большое количество узловых образований (см. Фиг. 1). Макроскопически матка была представлена опухолевыми узлами, имеющими на разрезе вид «рыбьего мяса» (см. Фиг. 2). На брыжейке определялись пораженные опухолевыми отсевами участки – лимфоузлы (см. Фиг.3). Опухолевые образования в печени (см. Фиг. 4).
Технико-экономическая эффективность способа создания модели саркомы матки заключается в том, что воспроизведение модели в условиях эксперимента путем трансплантации саркомы М1 обеспечивает быстрый злокачественный рост саркомы в теле матки. Это дает возможность изучать патогенез злокачественного процесса и влияния на него любой коморбидной патологии, а также проводить поиск мишеней для таргетной терапии. Способ экономичен, доступен для исполнения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ создания ортотопической модели рака эндометрия | 2024 |
|
RU2818464C1 |
| Способ моделирования карциномы Герена в матке на фоне сахарного диабета | 2024 |
|
RU2833143C1 |
| Способ дифференциальной диагностики доброкачественных и злокачественных новообразований яичников | 2018 |
|
RU2686180C1 |
| СПОСОБ СТИМУЛЯЦИИ ХРОНИЧЕСКОЙ БОЛЬЮ ЗЛОКАЧЕСТВЕННОГО РОСТА В ЛЁГКИХ КРЫС | 2018 |
|
RU2676641C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАЛИЧИЯ САРКОМЫ У ЖЕНЩИН С ПРОЛИФЕРИРУЮЩЕЙ МИОМОЙ МАТКИ | 2018 |
|
RU2682801C1 |
| Способ прогнозирования высокого риска рецидива у пациенток с IB стадией рака шейки матки, получивших комбинированное лечение | 2020 |
|
RU2732769C1 |
| Способ прогнозирования длительности безрецидивного периода сарком мягких тканей конечностей у женщин среднего и пожилого возраста | 2022 |
|
RU2778616C1 |
| Способ создания полинеоплазии со стимуляцией опухолевого роста в условиях первичного иммунодефицита в эксперименте | 2021 |
|
RU2751930C1 |
| Способ создания экспериментальной модели опухолевого роста в условиях гипотиреоза | 2021 |
|
RU2779358C1 |
| Способ хирургического лечения миомы матки у женщин репродуктивного возраста | 2020 |
|
RU2750911C1 |
Изобретение относится к области медицины, а именно к экспериментальной медицине и онкогинекологии, и может быть использовано для моделирования саркомы матки. Самкам белых беспородных крыс в просвет правого маточного рога с помощью внутривенного катетера с инъекционным портом 22G, 0,9×25 мм, вводят 0,5 мл опухолевой взвеси саркомы М1 в количестве 2,5-3,5×106 клеток. Изобретение обеспечивает быстрый злокачественный рост саркомы в теле матки. 4 ил.
Способ создания модели саркомы матки, заключающийся в том, что самкам белых беспородных крыс в просвет правого маточного рога с помощью внутривенного катетера с инъекционным портом 22G, 0,9×25 мм, вводят 0,5 мл опухолевой взвеси саркомы М1 в количестве 2,5-3,5×106 клеток.
| СПОСОБ МОДЕЛИРОВАНИЯ ОПУХОЛИ ТЕЛА МАТКИ ДЛЯ ИССЛЕДОВАНИЯ ЕЕ РЕГИОНАРНОГО ЛИМФАТИЧЕСКОГО РУСЛА | 2002 |
|
RU2220459C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ РАКА ЯИЧНИКА В ЭКСПЕРИМЕНТЕ У КРЫС | 2020 |
|
RU2743219C1 |
| КАПЛАН М.А | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Веникодробильный станок | 1921 |
|
SU53A1 |
| ФРАНЦИЯНЦ Е.М | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-06-03—Публикация
2024-02-27—Подача