Рак шейки матки (РШМ) - одна из наиболее распространенных злокачественных опухолей органов малого таза у женщин. Согласно мировой статистике, РШМ занимает четвертое место в структуре онкозаболеваемости у женщин и седьмое в структуре общей онкозаболеваемости [16]. В России эта патология находится на пятом месте в структуре заболеваемости злокачественными новообразованиями женского населения. Несмотря на успехи в диагностике (в 2017 году у 65,7% пациенток диагноз был установлен на I-II стадиях), летальность в течение первого года с момента установления диагноза остается высокой (14,3%) [2]. В связи с этим, снижение смертности от РШМ представляется одной из приоритетных задач здравоохранения РФ. Для решения этой проблемы важны как своевременная диагностика, так и эффективное лечение, что невозможно без точной оценки прогноза заболевания, необходимой для выбора оптимальной тактики лечения каждой конкретной пациентки [3,5,7,12,17].
Следует отметить, что РШМ является не только медицинской, но и социально-экономической проблемой. В.Н. Журман и соавторы (2016) отметили, что в 2013 г. экономические потери, связанные с преждевременной смертью от злокачественных новообразований женских половых органов, были максимальными при раке шейки матки и составили 488,6 млн рублей, опередив экономические потери при раке яичников (329,1 млн) и при раке эндометрия (101,1 млн) [1]. Таким образом, диагностика РШМ на ранних стадиях имеет решающее значение не только для снижения смертности от данной патологии, но и для оптимизации экономических затрат на ее лечение.
Известно, что РШМ отличается агрессивным течением. Уже при IB стадии РШМ, при наличии факторов высокого риска прогрессирования заболевания, показано проведение адъювантной лучевой терапии. Однако комбинированное лечение, не всегда гарантирует благоприятный прогноз. У части пациентов, несмотря на то, что лучевое лечение назначается им с учетом гистологии, стадии заболевания и локализации процесса, данный вид терапии оказывается неэффективным. Неудачный выбор тактики лечения приводит к потере времени и дальнейшей опухолевой прогрессии. Таким образом, прогнозирование эффекта проводимой комбинированной терапии у каждой конкретной пациентки имеет огромное значение, как для определения оптимального плана лечения пациента (выбор самостоятельного, комбинированного или комплексного лечения), так и для оценки его эффективности [2]. Определение риска рецидива РШМ позволило бы избегать назначения неэффективных схем лечения, корректировать индивидуальные планы терапии пациентов и, тем самым, способствовать улучшению результатов их лечения.
Уровень техники
Известны способы прогнозирования повышенного риска рецидива РШМ по клиническим характеристикам патологического процесса. При I стадии РШМ более высокий риск рецидива заболевания прогнозируют у пациенток моложе 35 лет [9,11]; при IB стадии заболевания [9,12,14]; при аденокарциномах [8,9,10,13,14]; при поражении всех слоев шейки матки [11,13]; при размерах опухоли больше 4 см [10,11,13,18]; при наличии опухолевых клеток по линии резекции [11,12,13]; при наличии метастазов в тазовых лимфоузлах [9,10,11]; при наличии параметральной инвазии [9,11]. Отмеченные способы просты в исполнении и не требуют дополнительных затрат. Недостатком отмеченных способов является их низкая чувствительность и специфичность, не позволяющая оценить риск развития рецидива у конкретного больного.
Известен способ определения высокого риска рецидива РШМ (патент RU 2247377 С2 Приходько Е.В. Способ прогнозирования возникновения рецидивов рака шейки матки), который заключается в том, что после сочетанной лучевой терапии определяют отношение абсолютного числа лимфоцитов к абсолютному числу моноцитов периферической крови, полученное соотношение делят на 4,05. При значениях полученного результата выше единицы констатируют отсутствие вероятности рецидива заболевания в течение первого года наблюдения, а при значениях ниже единицы констатируют наличие продолженного роста опухоли и возникновение рецидива рака в первый год после лечения. Недостатком этого способа является низкая специфичность, так как показатели периферической крови изменяются при наличии даже незначительного воспалительного процесса, а проведение лучевой терапии вызывает различной степени дозозависимое угнетение всех показателей периферической крови. Кроме того, способ может быть использован только у пациентов, получивших сочетанную лучевую терапию, и не может быть использован для оценки эффективности комбинированного лечения раннего РШМ.
Известен способ прогнозирования возникновения рецидивов РШМ, в ближайшие сроки после окончания комплексного или комбинированного методов лечения, включающий биохимическое исследование суточной мочи пациенток (патент RU 2485523 C2 Розенко Л.Я., Рубцов В.Р., Родионова О.Г. Способ прогнозирования ранних рецидивов или/и метастазов рака шейки матки). Способ заключается в том, что в суточной моче определяют андростерон и этиохоланолон, вычисляют отношение между ними, и при величине отношения 0,75 мг/сут и ниже прогнозируют рецидив болезни в первые 2 года, а при величине, превышающей 0,75 мг/сут, - длительный безрецидивный период до 10 лет и более. Недостатком метода является его высокая стоимость, и необходимость сбора суточного объема мочи, что не всегда возможно. Кроме того, на синтез стероидных гормонов влияют различные факторы и, следовательно, уровень их метаболитов в моче зависит от особенностей обмена веществ, общего состояния организма, здоровья эндокринной системы, образа жизни и других факторов.
В качестве прототипа взят способ прогнозирования высокого риска рецидива РШМ по наличию периневральной инвазии в строме опухоли [Tang M, Liu Q, Yang X, Chen L, Yu J, Qi X et al. Perineural invasion as a prognostic risk factor in patients with early cervical cancer]. При гистологическом исследовании образцов ткани опухоли, в случаях наличия периневральной инвазии, прогнозируют высокий риск рецидива РШМ. Способ обладает высокой специфичностью (93,8%), простотой выполнения и низкой стоимостью. Существенным недостатком описанного способа является его низкая чувствительность (40,4%), что снижает его ценность при планировании адьювантной терапии пациенток с РШМ.
Задача изобретения - создание способа позволяющего прогнозировать высокий риска рецидива у пациенток с IB стадией РШМ, получивших комбинированное лечение.
Новизна изобретения
Новизной предлагаемого способа является то, что прогнозирование высокого риска рецидива раннего РШМ осуществляется путем выявления в гистологических препаратах, окрашенных иммуногистохимически с использованием антител к CD34, наличия фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками.
Раскрытие изобретения
Прогнозирование риска рецидива у пациенток с IB стадией РШМ, получивших комбинированное лечение, осуществляют путем выявления в гистологических препаратах, окрашенных иммуногистохимически с использованием антител к CD34, наличия фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками, и в тех случаях, когда в исследуемых образцах выявляют оба признака, прогнозируют высокий риск рецидива заболевания.
Технический результат
Предложенный способ позволяет выявлять группу пациентов с IB стадией РШМ, получивших комбинированное лечение, с высоким риском развития рецидива заболевания и вносить коррективы в проводимое лечение. Метод легко реализуется, не требует значительных финансовых затрат и отличается высокой эффективностью, что было подтверждено результатами исследования образцов опухолей 75 пациенток с I стадией РШМ. Чувствительность метода составляет 75,0%, специфичность - 94,9% и точность - 91,3%. Внедрение метода в клиническую практику будет способствовать повышению точности прогноза заболевания с целью оптимизации проводимого лечения.
Способ осуществляется следующим образом
После радикальной операции по поводу РШМ выполняют иммуногистохимическое исследование образцов ткани опухоли с использованием антител к CD34. При обнаружении в исследуемых образцах фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками, с вероятностью 75% прогнозируют риск рецидива заболевания.
Пример клинического применения
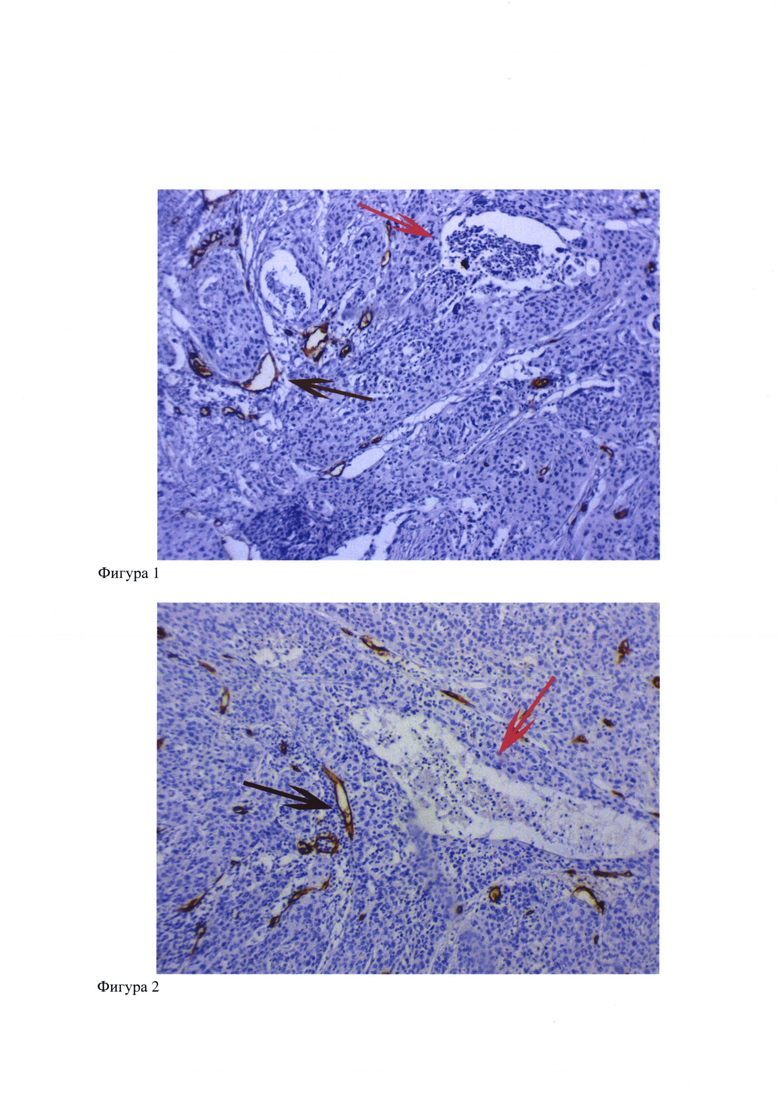
1. Пациентка А. 28 лет, находилась на лечении с диагнозом: «Рак шейки матки, стадия T1бN0M0». 25.04.13 г. ей была выполнена расширенная гистерэктомия (по Вертгейму) с транспозицией яичников. Гистология: Плоскоклеточный ороговевающий рак цервикального канала с прорастанием шейки матки на всю толщу. В лимфоузлах метастазов не найдено. Послеоперационный период протекал без осложнений. При иммуногистохимическом исследовании в образцах опухолевой ткани (Фиг. 1) выявлена фрагментация клеток в солидном компоненте опухоли (красная стрелка) и дилятированные капилляры, непосредственно контактирующие с опухолевыми клетками (коричневая стрелка), что позволяет прогнозировать высокий риск рецидива заболевания. После операции пациентка получила сочетанную лучевую терапию по стандартной схеме. 16.12.13 г у пациентки выявлены диссеминация в малом тазу и метастазы в печень.
Пациентка А. 51 год, находилась на лечении с диагнозом: «Рак шейки матки, стадия T1бN0M0». 07.08.12 г. ей была выполнена расширенная гистерэктомия с придатками (по Вертгейму). Гистология: Плоскоклеточный ороговевающий рак шейки матки, глубина инвазии до 15 мм. В лимфоузлах метастазов не найдено. Послеоперационный период протекал без осложнений. При иммуногистохимическом исследовании в образцах опухолевой ткани (Фиг. 2) выявлена фрагментация клеток в солидном компоненте опухоли (красная стрелка) и дилятированные капилляры, непосредственно контактирующие с опухолевыми клетками (коричневая стрелка), что указывает на высокий риск рецидива заболевания. После операции пациентка получила сочетанную лучевую терапию по стандартной схеме. 25.03.16 г у пациентки выявлены метастазы в легких.
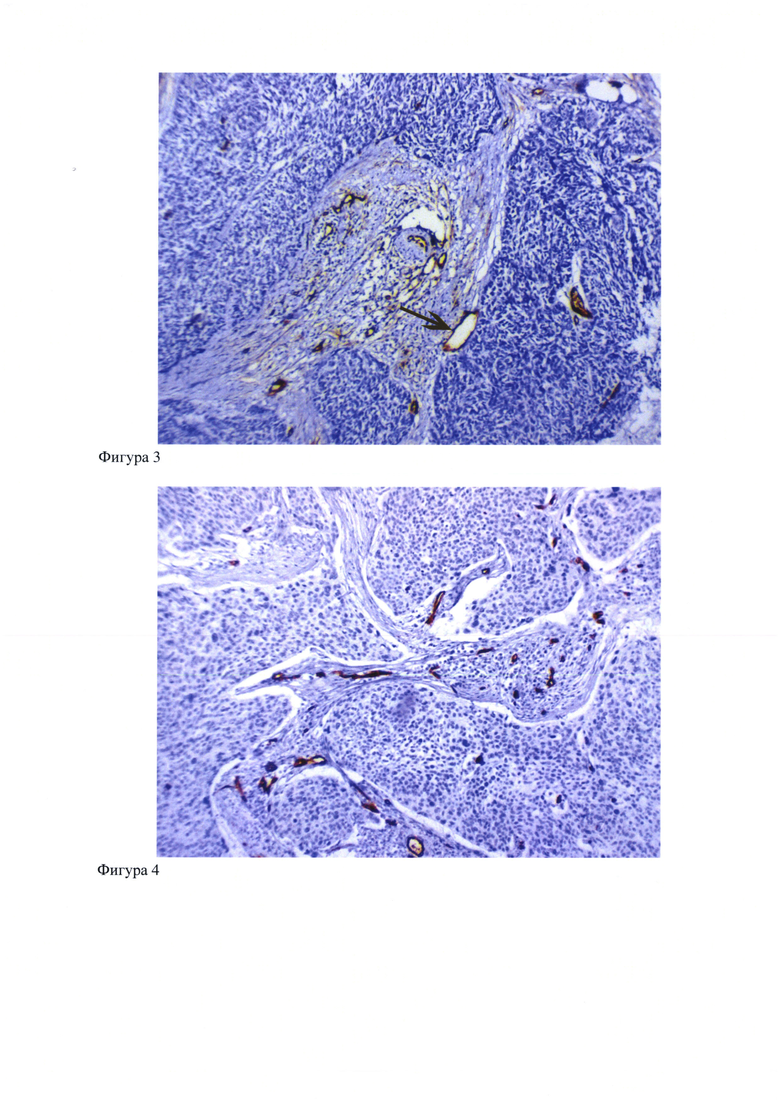
3. Пациентка Г. 59 лет, находилась на лечении с диагнозом: «Рак шейки матки, стадия T1бN0M0». 07.04.11 г. ей была выполнена расширенная гистерэктомия с придатками (по Вертгейму). Гистология: Плоскоклеточный ороговевающий рак шейки матки, глубина инвазии до 8мм. В лимфоузлах метастазов не найдено. Послеоперационный период протекал без осложнений. При иммуногистохимическом исследовании, в образцах опухолевой ткани (Фиг. 3) выявлены дилятированные капилляры, непосредственно контактирующие с опухолевыми клетками (коричневая стрелка). Фрагментации клеток в солидном компоненте опухоли не выявлено, что указывает на низкий риск рецидива заболевания. После операции пациентка получила сочетанную лучевую терапию по стандартной схеме. В настоящее время пациентка находится под наблюдением в ГБУЗ «ООКОД», данных за рецидив не получено.
4. Пациентка Б. 42 года, находилась на лечении с диагнозом: «Рак шейки матки, стадия T1бN0M0». 07.04.11 г. ей была выполнена расширенная гистерэктомия с придатками (по Вертгейму). Гистология: Плоскоклеточный ороговевающий рак шейки матки, глубина инвазии до 10мм. В лимфоузлах метастазов не найдено. Послеоперационный период протекал без осложнений. При иммуногистохимическом исследовании в образцах опухолевой ткани (Фиг. 4) фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками, не выявлено, что указывает на низкий риск рецидива заболевания. После операции пациентка получила сочетанную лучевую терапию по стандартной схеме. В настоящее время пациентка находится под наблюдением в ГБУЗ «ООКОД» данных за рецидив не получено.
Литература:
1. Журман В.Н., Елисеева Е.В., Гулевич А.П., Слободенюк Е.В. Социально-экономические последствия смертности женщин от злокачественных новообразований женских половых органов. Дальневосточный медицинский журнал. 2016.N 1:С. 89-91.
2. Состояние онкологической помощи населению России в 2017 году. Под ред. Каприна А.Д., Старинского В.В., Петровой Г.В. М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИРЦ» Минздрава России; 2018. - илл. - 236 с.
3. Рак шейки матки. Клинические рекомендации по диагностике и лечению. МЗ РФ / Кравец А., Кузнецов В.В., Морхов К.Ю., Нечушкина В.М., Хохлова С.В.- М.- 2018. - 44 с.
4. Приходько Е. В. Способ прогнозирования возникновения рецидивов рака шейки матки // Патент на изобретение RU 2485523 C2
5. Прошин А.А., Березовская Т.П., Крикунова Л.И, Шавладзе З.Н. Рак шейки матки: магнитно-резонансные и клинические факторы прогноза. Опухоли женской репродуктивной системы. 2012(3), № 4:102-7.
6. Розенко Л.Я., Рубцов В.Р., Родионова О.Г. Способ прогнозирования ранних рецидивов или/и метастазов рака шейки матки // Патент на изобретение RU 2247377 С2
7. Atahan IL, Onal C, Ozyar E, Yiliz F, Selek U, Kose F. Long-term outcome and prognostic factors in patients with cervical carcinoma: a retrospective study. Int J Gynecol Cancer. 2007;17(4):833-42. doi:10.1111/j.1525-1438.2007.00895.x
8. Gadducci A., Guerrieri M.E., Cosio S. Adenocarcinoma of the uterine cervix: Pathologic features, treatment options, clinical outcome and prognostic variables. Crit Rev Oncol Hematol. 2019; 135:103-14. doi: 10.1016/j.critrevonc.2019.01.006
9. Hou Y, Guo S, Lyu J, Lu Z, Yang Z, Liu D. et al. Prognostic factors in Asian and white American patients with cervical cancer, considering competing risks. Curr Oncol. 2019 Jun; 26(3):277-85. doi: 10.3747/co.26.4473
10. Landoni F, Colombo A, Milani R, Placa F, Zanagnolo V, Mangioni C. Randomized study between radical surgery and radiotherapy for the treatment of stage IB-IIA cervical cancer: 20-year update. J Gynecol Oncol. 2017 May;28(3):34. doi: 10.3802/jgo.2017.28.e34
11. Marnitz S,  C, Affonso RJ, Schneider A, Chiantera V, Tsounoda A. et al. Validity of Laparoscopic Staging to Avoid Adjuvant Chemoradiation following Radical Surgery in Patients with Early Cervical Cancer. Oncology. 2012; 83(6):346-53. doi: 10.1159/000341659
C, Affonso RJ, Schneider A, Chiantera V, Tsounoda A. et al. Validity of Laparoscopic Staging to Avoid Adjuvant Chemoradiation following Radical Surgery in Patients with Early Cervical Cancer. Oncology. 2012; 83(6):346-53. doi: 10.1159/000341659
12. Miyauchi R, Itoh Y, Kawamura M, Hirakawa A, Shibata K, Kajiyama H. et al. Postoperative chemoradiation therapy using high dose cisplatin and fluorouracil for high- and intermediate-risk uterine cervical cancer. Nagoya J Med Sci. 2017 Feb;79(2):211-20. doi: 10.18999/nagjms.79.2.211.
13. Noh JM, Park W, Kim YS, Kim JY, Kim HJ, Kim J. et al. Comparison of clinical outcomes of adenocarcinoma and adenosquamous carcinoma in uterine cervical cancer patients receiving surgical resection followed by radiotherapy: a multicenter retrospective study (KROG 13-10). Gynecol Oncol. 2014 Mar; 132(3):618-23.
doi: 10.1016/j.ygyno.2014.01.043
14. Shimamoto K, Saito T, Kitade S, Tomita Y, Nagayama R, Yamaguchi S. et al. A study of treatments and outcomes in elderly women with cervical cancer. Eur J Obstet Gynecol Reprod Biol. 2018 Sep; 228:174-79.
doi: 10.1016/j.ejogrb.2018.06.032
15. Tang M, Liu Q, Yang X, Chen L, Yu J, Qi X et al. Perineural invasion as a prognostic risk factor in patients with early cervical cancer. Oncol Lett. 2019 Jan;17(1):1101-07. doi: 10.3892/ol.2018.9674.
16. Torre LA, Bray F, Siegel RL, Ferlay J, Lortet-Tieulent J, Jemal A.Global cancer statistics 2012. CA Cancer J Clin. 2015 Mar; 65(2):87-108.
doi: 10.3322/caac.21262.
17. Wiebea E, Dennyb L, Thomasa G. FIGO cancer report 2012. Cancer of the cervix uteri. Int J Gynaecol Obstet. 2012 Oct;119 Suppl 2:100-9.
doi: 10.1016/S0020-7292(12)60023-X.
18. Wu SG, Zhang WW, He ZY, Sun JY, Wang Y, Zhou J. Comparison of survival outcomes between radical hysterectomy and definitive radiochemotherapy in stage IB1 and IIA1 cervical cancer. Cancer Manag Res. 2017 Dec 11; 9:813-19. doi: 10.2147/CMAR.S145926
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования прогрессирования рака шейки матки у больных IIB стадии | 2022 |
|
RU2789500C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НЕБЛАГОПРИЯТНОГО ТЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННЫХ ФОРМ РАКА ШЕЙКИ МАТКИ, АССОЦИИРОВАННОГО С ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА | 2012 |
|
RU2504326C1 |
| Способ комбинированного термохимиолучевого лечения больных местнораспространенным раком шейки матки | 2016 |
|
RU2622633C1 |
| Способ лучевой терапии местнораспространенного рака шейки матки | 2019 |
|
RU2719902C1 |
| Способ ранней диагностики цервикальных интраэпителиальных неоплазий (ЦИН) на основе изучения метаболических маркеров | 2016 |
|
RU2629632C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ КЛИНИЧЕСКОГО ИСХОДА МЕСТНОРАСПРОСТРАНЕННЫХ ФОРМ РАКА ШЕЙКИ МАТКИ | 2018 |
|
RU2674675C2 |
| Способ прогнозирования риска раннего рецидива плоскоклеточного рака эндометрия у больных с I стадией заболевания | 2023 |
|
RU2812609C1 |
| СПОСОБ ДИАГНОСТИКИ МЕТАСТАЗОВ В ЛИМФАТИЧЕСКИЕ УЗЛЫ МАЛОГО ТАЗА У БОЛЬНЫХ РЕЗЕКТАБЕЛЬНЫМ РАКОМ ШЕЙКИ МАТКИ | 2020 |
|
RU2750769C2 |
| Способ прогнозирования ранних рецидивов светлоклеточной карциномы тела матки | 2022 |
|
RU2784775C1 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННЫХ ФОРМ РАКА ШЕЙКИ МАТКИ IIB-IIIB(T2b-T3bN0(1)M0) СТАДИЙ | 2020 |
|
RU2748135C2 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для прогнозирования высокого риска рецидива у пациенток с IB стадией рака шейки матки, получивших комбинированное лечение. Предлагается способ прогнозирования высокого риска рецидива у пациенток с IB стадией рака шейки матки путем иммуногистохимического исследования образцов ткани опухоли, заключающийся в том, что в препаратах, окрашенных с использованием антител к CD34, определяют наличие фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками, и в тех случаях, когда в исследуемых образцах выявляют оба признака, прогнозируют высокий риск рецидива заболевания. 4 ил., 4 пр.
Способ прогнозирования высокого риска рецидива у пациенток с IB стадией рака шейки матки путем гистологического исследования образцов ткани опухоли, отличающийся тем, что в препаратах, окрашенных иммуногистохимически с использованием антител к CD34, определяют наличие фрагментации клеток в солидном компоненте опухоли и дилятированных капилляров, непосредственно контактирующих с опухолевыми клетками, и в тех случаях, когда в исследуемых образцах выявляют оба признака, прогнозируют высокий риск рецидива заболевания.
| Tang M, Liu Q, Yang X, Chen L, Yu J, Qi X et al | |||
| Perineural invasion as a prognostic risk factor in patients with early cervical cancer | |||
| Oncol Lett | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАННИХ РЕЦИДИВОВ ИЛИ/И МЕТАСТАЗОВ РАКА ШЕЙКИ МАТКИ | 2003 |
|
RU2247377C2 |
| СПОСОБ ДИАГНОСТИКИ РЕЦИДИВОВ И МЕТАСТАЗОВ РАКА | 1993 |
|
RU2082984C1 |
| US 5989815 А, 23.11.1999 | |||
| WO 9525429 А1, 28.07.1995 | |||
| ГУСЬКОВА Е.А., НЕРОДО Г.А., ГУСЬКОВА | |||
Авторы
Даты
2020-09-22—Публикация
2020-01-10—Подача