Изобретение относится к медицине, в частности, к гинекологии и онкологии, может быть использовано в практике гинекологов и гинекологов-онкологов для дифференциальной диагностики доброкачественных и злокачественных новообразований яичников на этапе предоперационного обследования пациентов.
Объемные образования яичников, являющиеся наиболее часто выявляемой патологией при обследовании женщин репродуктивного и постменопаузального возраста, могут быть как доброкачественными, так и злокачественными. Злокачественные опухоли яичников являются наименее доступными для ранней диагностики среди всех злокачественных новообразований репродуктивной системы, в связи с бессимптомным течением заболевания на ранних стадиях. Определение характера опухоли яичника – доброкачественная (ДОЯ) или злокачественная (ЗОЯ) на этапе предоперационной диагностики является, несомненно, важным, так как имеются принципиальные различия в тактике ведения и лечения больных. Однозначных критериев для направления больных в гинекологический или онкологический стационар до настоящего времени не существует. Общепринятым является алгоритм диагностики ЗОЯ, включающий клинический осмотр, лучевые методы визуализации и иммунологический метод (определение уровня опухолевых маркеров в сыворотке крови). С целью повышения диагностической значимости в последние годы является актуальной разработка комплексных диагностических панелей (платформ).
В 2011 году FDA разработан алгоритм ROMA (Risk Ovarian Malignacy Algorithm), учитывающий уровни двух опухолевых маркеров (СА-125 и HЕ-4) и репродуктивный статус пациентки. ROMA позволяет оценить статистическую вероятность злокачественного характера новообразований яичников, разделяя женщин репродуктивного и постменопаузального периода на группы высокого и низкого риска [14]. В основе расчета ROMA лежит определение так называемого прогностического индекса (ПИ, Predictive Index, PI). Недостатком данного метода является то, что? формула подсчета разработана отдельно для женщин репродуктивного возраста и в постменопаузе.
Известен также способ дифференциальной диагностики ДОЯ и ЗОЯ с помощью специальной программы для ЭВМ «Risk Ovarian Cancer v.2.2» (Свидетельство о государственной регистрации программы для ЭВМ №2015619866 от 15.09.2015 г.). Математическая модель нейронной сети прямого распространения, позволяющая на основе данных о конкретной пациентке и результатах ее обследования прогнозировать наличие у нее ДОЯ или ЗОЯ. Построение модели проводилось путем проведения 37 итераций обучения. На 1 итерации использовалось 46 параметров пациенток (все исследуемые показатели из историй болезней), в ходе обучения остались 9 параметров, имеющих наибольшее значение. Такими параметрами оказались: возраст и длительность постменопаузы, индекс массы тела (ИМТ), количество родов в анамнезе, концентрация креатинина и глюкозы крови, число баллов при УЗИ, концентрация CA125 и HE4 и результат по формуле ROMA. На основе данной модели была разработана компьютерная диагностическая система «Risk Ovarian Cancer v.2.2», которая позволяет оценить вероятность наличия у пациенток ЗОЯ с чувствительностью - 94%, специфичностью - 80% [20]. Однако применение данного метода требует специального технического оснащения.
В 1990 году Jacobs и соавторы [1] для того, чтобы провести количественную оценку риска малигнизации объемного образования в яичнике на основе ультразвукового исследования (УЗИ), менопаузального статуса и уровня онкомаркера СА-125 (cancer antigen 125), разработали алгоритм – Risk of Malignancy Index (RMI). Он представляет собой множество между цифровыми значениями онкомаркера и вышеуказанных показателей, выраженных в условных баллах.
Усовершенствованной версией индекса является более современная формула, разработанная в 1996 году доктором Tingulstad. При этом при отсутствии или наличии одного ультразвукового признака присваивается 1 балл, при наличии от двух до пяти признаков – 4 балла. Женщинам в постменопаузе также присваивается 4 балла. После чего все баллы перемножаются между собой и показателем онкомаркера СА-125. Это и будет усовершенствованным индексом малигнизации, более точным, специфичным и обладающим большим процентом прогностической ценности. По данным зарубежных авторов (Bast R.C. Jr, Skates S., Lokshin A.,Moore R.G. ) RMI обладает чувствительностью 71-88% при специфичности 74-97% [2, 3].
Преимущество RMI над остальными диагностическими системами заключается в том, что он включает в себя три наиболее важных клинико-лабораторных показателя в определении риска рака яичников (РЯ), в том числе данные ультразвукового исследования. Индекс малигнизации RMI является наиболее близким к заявляемому техническому решению по сущности и достигаемому результату. Описанный способ принят за прототип изобретения.
Недостатки метода RMI: включение в расчет абсолютного значения уровня СА125 может снижать его диагностическую ценность в связи с тем, что чувствительность определения уровня СА-125 зависит от стадии заболевания и гистологической структуры опухоли и варьирует от 31 % до 95 % [4, 5]. Диагностическая чувствительность СА-125 для РЯ серозного типа варьирует от 42 % (I–II стадии) до практически 100 % (IV стадия) [6]. Продолжающееся более 30 лет (с момента открытия) исследование СА-125 выявило ряд ограничений для его применения. Несмотря на то, что СА-125 часто повышен при распространенных стадиях РЯ, онкомаркер повышается менее чем в 50 % случаев при I стадии заболевания и часто остается в норме при муцинозных (32 %), эндометриоидных (30–60 %) и светлоклеточных (40 %) аденокарциномах [7, 8]. В то же время уровень СА-125 может быть повышен при эндометриозе, миоме матки, циррозе печени, остром панкреатите, опухолях желудочно-кишечного тракта, карциноме молочной железы и бронхов. У молодых женщин концентрация СА-125 может колебаться в течение менструального цикла [9].
Технической задачей изобретения является улучшения дифференциальной диагностики ДОЯ и ЗОЯ на амбулаторном этапе путем применения неинвазивного, доступного в техническом и финансовом отношении метода, обладающего высокой чувствительностью и специфичностью, что могло бы способствовать более точному определению тактики ведения и лечения пациенток. Уже доказано, что выживание женщин после хирургического и последующего химиотерапевтического лечения гораздо выше и прогноз лучше, если оно проводится в специализированных центрах специалистами гинекологами-онкологами [21]. По приблизительным оценкам, если бы 75% случаев злокачественных опухолей яичников были бы обнаружены на I или II стадии, то смертность снизилась бы на 50 % [22] , тем не менее, до настоящего времени не существует единственного стандарта оценки риска малигнизации при обследовании женщин с образованиями в области придатков матки.
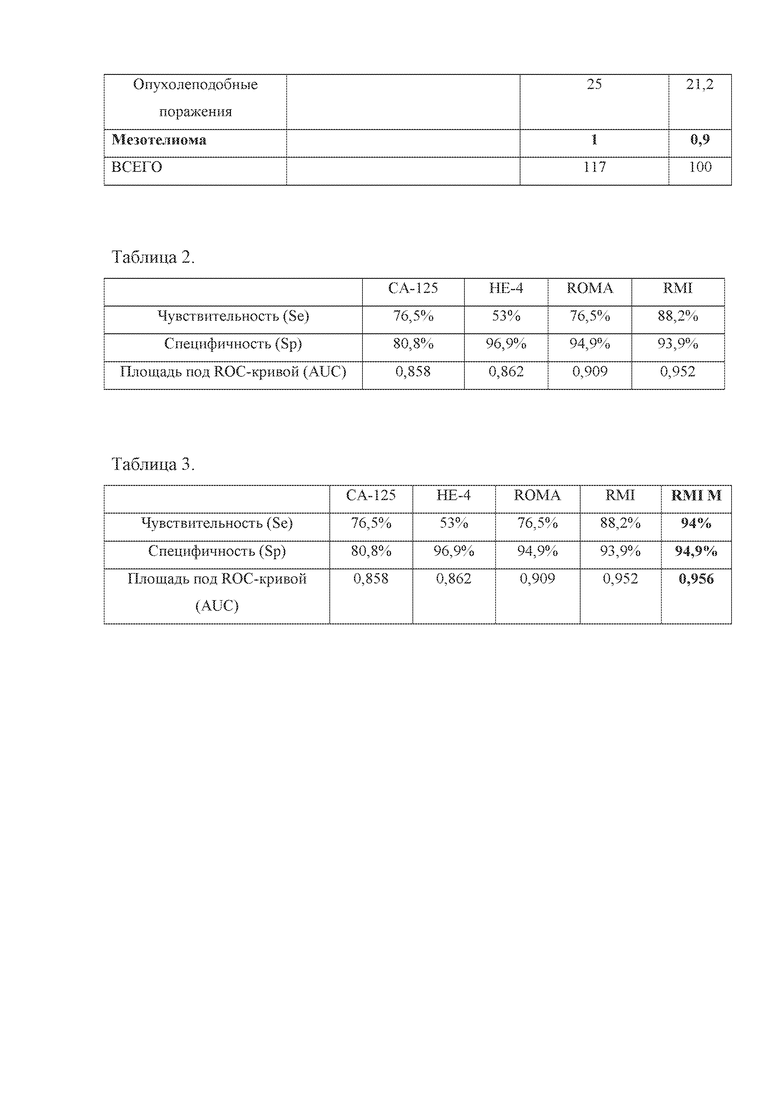
Поставленная задача решается следующим образом: рассчитывается «модифицированный» индекс малигнизации яичников, основанный на данных УЗИ ОМТ, концентрации опухолевого маркера НЕ-4, определенного методом хемилюминесцентного иммуноанализа (Architect, Abbott), и возрастном периоде пациентки. Формула для расчёта схожа с формулой RMI, предложенной в 1990 году Jacobs [1]: RMI =АхВхС, где А – особенности возрастного периода женщины (репродуктивный возраст – 1 балл, постменопауза – 4 балла), В – наличие таких ультразвуковых признаков как многокамерное образование, солидное образование, двустороннее поражение, наличие асцита, наличие метастазов (при отсутствии или выявлении одного ультразвукового признака - 1 балл, при наличии от двух до пяти признаков – 4 балла), но отличающаяся тем, что в качестве третьего множителя С – концентрация опухолевого маркера НЕ-4 (а не СА-125, как в формуле Jacobs) сыворотке крови (пмоль/л). Значение «модифицированного RMI» более 170 у пациенток репродуктивного возраста и более 340 у женщин в постменопаузе указывает на наличие злокачественных опухолей яичников. Чувствительность (Se) метода составила 94%, специфичность (Sp) – 94,9%, площадь под ROC-кривой (AUC) – 0,956 (таблица 3).
Пример осуществления изобретения.
Проведено исследование, целью которого было провести сравнительный анализ чувствительности и специфичности СА-125, НЕ-4, RMI, «модифицированного RMI» и ROMA в дифференциальной диагностике доброкачественных и злокачественных объемных образований яичников на этапе предоперационного обследования. Диагностическая значимость исследуемых онкомаркеров и методов оценивалась на основе анализа их чувствительности (Se), специфичности (Sp) и значения площади под ROC-кривой (AUC).
В проспективном исследовании приняли участие 117 пациенток, поступившие для хирургического лечения по поводу объёмных образований яичников. В группу исследования вошли 67 (57,3%) женщин репродуктивного периода и 50 (42,7%) – постменопаузального. Возраст пациенток варьировал от 18 до 82 лет (45 [33; 56]). На основании менопаузального статуса, результатов УЗИ органов малого таза и уровня онкомаркера СА-125 в сыворотке крови был рассчитан индекс малигнизации RMI. Расчет алгоритма ROMA проводился на основании менопаузального статуса и уровней онкомаркеров СА-125 и НЕ-4 в сыворотке крови. После этапа хирургического лечения и получения результатов гистологического исследования операционного материала проводилась статистическая обработка полученных данных с помощью компьютерной программы SPSS. По результатам гистологического исследования операционного материала в группе исследования было идентифицировано 98 (83,7%) ДОЯ, 1 (0,9%) пограничная опухоль яичника, 17 (14,5%) ЗОЯ и 1 (0,9%) мезотелиома брюшины. Морфологическая структура объемных образований яичников в группе исследования (согласно классификации ВОЗ, 2013 г) представлена в таблице 1.
У большинства (75 (64,2%)) пациенток были идентифицированы эпителиальные опухоли яичников. Помимо этого, встречались герминогенные опухоли – зрелая тератома у 10 пациенток; опухоли стромы полового тяжа в варианте фибромы у 5 и текомы у 1 женщины. У 25 пациенток были выявлены опухолеподобные поражения, представленные фолликулярными кистами, кистами желтого тела, стромальным гипертекозом и фиброматозом яичников. Все злокачественные новообразования яичников, выявленные в группе исследования, были представлены эпителиальными опухолями.
Данные о чувствительности (Se), специфичности (Sp) площади под ROC-кривой (AUC) для методов СА-125, НЕ4, RMI и ROMA представлены в таблице 2.
Согласна таблицы 2, индекс малигнизации RMI в проведенном исследовании характеризовался наибольшими значениями чувствительности и площади под ROC-кривой, несмотря на то, что его определение основано на данных УЗИ ОМТ и концентрации СА-125 (онкомаркера, чувствительность и специфичность которого варьирует от 31 до 95% [28]). В формуле расчета индекса малигнизации СА-125 заменен на более специфичный онкомаркер НЕ4 с учетом различных дискриминационных уровней (ДУ) последнего для пациенток репродуктивного (70 пмоль/л) и постменопаузального периодов (140 пмоль/л). При этом отмечено, что у пациенток репродуктивного возраста с РЯ значения «модифицированного RMI» превышали 170, а у пациенток в постменопаузе (за исключением больной со светлоклеточной карциномой яичника, у которой все методы оказались ложноотрицательными) – превышали 340.
Приняв за ДУ значения 170 для женщин репродуктивного возраста и 340 для пациенток в постменопаузе, рассчитаны показатели прогностической ценности и для «модифицированного RMI: чувствительность (Se) метода составила 94%, специфичность (Sp) – 94,9%, площадь под ROC-кривой (AUC) – 0,956. Таким образом, метод определения «модифицированного RMI» характеризовался наибольшей чувствительностью и площадью под ROC-кривой; специфичность была сопоставима с таковой для ROMA и уступала по значению лишь специфичности онкомаркера НЕ4 (таблица 3).
Клинический пример 1.
Пациентка А., 33 года, поступила в гинекологическую клинику с жалобами на периодические боли ноющего характера средней интенсивности внизу живота в течение 8 месяцев. Менструальный цикл регулярный. Беременностей в анамнезе у пациентки не было. Наследственность по онкологическим заболеваниям не отягощена. По данным протокола УЗИ ОМТ, в проекции левого яичника определяется объемное образование с гомогенной взвесью размером 43х40х40 мм; эхоскопически патологии матки и правых придатков не выявлено; в позадиматочном пространстве жидкость высотой 24 мм. Концентрации опухолевых маркеров в сыворотке крови на этапе предоперационного обследования были следующими: СА-125 = 9,7 Ед/мл (в пределах референсных значений (менее 35 ЕД/мл)), НЕ-4 = 44 пмоль/л ( в пределах референсных значений (70 пмоль/л)). При эзофагогастродуоденоскопии (ЭГДС) была диагностирована очаговая атрофия слизистой антрального отдела желудка, дуоденогастральный рефлюкс. На основании данных УЗИ ОМТ и значений опухолевых маркеров, были рассчитаны RMI (9,7),ROMA (5,5%) и модифицированный RMI (44), результаты не выходили за границы референсных значений. Данных за злокачественное новообразование по результатам предоперационного обследования получено не было. Пациентке выполнена операция: лапароскопия, цистэктомия слева. Материал отправлен на гистологическое исследование. Результат гистологического исследования послеоперационного материала: эндометриоидная киста (доброкачественное эпителиальное
Клинический пример 2.
Пациентка Б., 76 лет, поступила в стационар онкологического диспансера с жалобами на тянущие боли внизу живота в течение длительного времени, склонность к запорам. Постменопауза 23 года. Репродуктивная функция не реализована, беременностей в анамнезе не было. В возрасте 55 лет пациентка перенесла оперативное лечение по поводу миомы матки больших размеров в объеме лапаротомии, субтотальной гистерэктомии без придатков. Наследственность по онкологическим заболеваниям не отягощена. Со слов больной, объемное образование в малом тазу выявлено 12 месяцев назад. При повторном УЗИ ОМТ в малом тазу определялось кистозно-солидное образование 157х112х160 мм с пристеночными папиллярными разрастаниями и единичными цветовыми локусами по периферии, в позадиматочном пространстве – жидкость в большом количестве, яичники достоверно не определялись. На предоперационном этапе было проведено определение уровней опухолевых маркеров в сыворотке крови: СА-125 = 1,5 Eд/мл (в пределах референсных значений (менее 35 ЕД/мл)), НЕ-4 = 63,4 пмоль/л ( в пределах референсных значений (140 пмоль/л)). На основании данных УЗИ ОМТ и значений опухолевых маркеров, были рассчитаны RMI (24), ROMA (3,0%), результаты не выходили за границы референсных значений. Таким образом, данных за злокачественное новообразование по результатам предоперационного определения опухолевых маркеров и расчета комплексных диагностических тестов, получено не было. Но, рассчитав модифицированный индекс малигнизации, нами было получено значение 1014,4, что значительно превышает установленный нами дискриминационный уровень (340), указывает на риск того, что описываемое при УЗИ ОМТ образование является злокачественным. Пациентке была выполнена операция: лапаротомия, двусторонная аднексэктомия, лимфодиссекция. Материал отправлен на гистологическое исследование. Заключение гистологического исследования: муцинозная цистаденокарцинома правого яичника умеренной степени дифференцировки с разрастаниями опухоли на поверхности капсулы яичника (злокачественная эпителиальная опухоль).
Клинический пример 3.
Пациентка В.,55 лет, поступила в стационар онкологического диспансера с жалобами умеренно выраженную слабость в течение месяца. Постменопауза 5 лет. В анамнезе 7 беременностей, 4 родов, 2 аборта и 1 выкидыш. Наследственность отягощена по онкологическим заболеваниям со стороны матери. При УЗИ ОМТ в проекции яичников с двух сторон определялись объемные образования кистозно-солидного строения диаметром около 5 см, окруженные жидкостью. На предоперационном этапе было проведено определение уровней опухолевых маркеров в сыворотке крови: СА-125 = 17 Eд/мл (в пределах референсных значений (менее 35 ЕД/мл)), НЕ-4 = 39,5пмоль/л ( в пределах референсных значений (140 пмоль/л)). На основании данных УЗИ ОМТ и значений опухолевых маркеров, были рассчитаны RMI (272), ROMA (10%) и модифицированный RMI (632). Таким образом, только RMI и модифицированный индекс малигнизации указывали на высокий риск злокачественных опухолей яичников. Пациентке была выполнена операция: лапаротомия, тотальная гистерэктомия с маточными придатками. Материал отправлен на гистологическое исследование. Заключение гистологического исследования: серозная аденокарцинома низкой дифференцировки правого и левого яичников (злокачественные эпителиальные опухоли).
Техническим результатом является новый способ дифференциальной диагностики доброкачественных и злокачественных объемных образований яичников на предоперационном этапе.
Изобретение позволяет на амбулаторном приеме провести дифференциальную диагностику между ДОЯ и ЗОЯ у пациенток с объемными образованиями в проекции маточных придатков и, при получении данных за злокачественный процесс, направить женщину в специализированное учреждение онкологического профиля, а при отсутствии данных за РЯ – направить на лечение в гинекологический стационар.
Источники информации:
1. Jacobs I, Oram D, Fairbanks J, et al. A risk of malignancy index incorporating CA 125, ultrasound and menopausal status for the accurate preoperative diagnosis of ovarian cancer. British Journal of Obstetrics and Gynecology. 1990; 97 (10): 922-929.
2. Никогосян С.О., Кадагидзе З.Г., Шелепова В.М., Кузнецов В.В. Современные методы иммунодиагностики злокачественных новообразований яичников // Онкогинекология. - 2014. - № 3. - С. 49–54.
3. Altasas M.M., Golderg G.L., Levin W., Radio F.F., Blosh B., Darg L., Smith J.A. The role of cancer antigen 125 in management of ovarian epittelial carcinomas // Gynecol.oncol. 1988. V. 30. № 1. P. 26–34.
4. Kenemans P, Verstraeten AA, van Kamp GJ, von Mensdorff-Pouilly S. The second generation CA 125 assays. Annals of Medicine. 1995; 27 (1): 107–113.
5. Никогосян С.О. Серозная цистаденокарцинома яичников (факторы риска, клиника, прогноз). Дисс. … канд. мед. наук. - М., 1991. [Nikogosyan SO. Seroznaya tsistadenokartsinoma yaichnikov (faktory riska, klinika, prognoz). Moscow; 1991. (In Russ).]
6. Онкология: национальное руководство. Под ред. В.И. Чиссова, М.И. Давыдова. М.:ГЭОТАР-Медиа, 2008. 1072 с.
7. Подзолкова Н.М., Львова А.Г., Зубарев А.Р., Осадчев В.Б. Дифференциальная диагностика опухолей и опухолевидных образований яичников: клиническое значение трехмерной эхографии // Вопросы гинекологии, акушерства и перинатологии. - 2009. - Т. 8. - № 1. - С. 7 – 16.
8. Barbati A., Lauro V., Orlacchio A., Cosmi E.V.Immunoblotting characterization of CA 125 in biological fluids: difference between pregnancy and cancer CA 125 origin. Anticancer Res 1996;16(6В):3621–4.
9. Алексеева М.Л., Гусарова Е.В., Муллабаева С.М. и др. Онкомаркеры, их характеристика и некоторые аспекты клинико-диагностического использования // Проблемы репродукции. - 2005. - № 3. - С. 43-45.
10. Havrilesky LJ, Whitehead CM, Rubatt JM, et al. Evaluation of biomarker panels for early stage ovarian cancer detection and monitoring for disease recurrence. Gynecologic Oncology. 2008; 110 (3): 374-382.
11. Lin J, Qin J, Sangvatanakul V. Human epididymis protein 4 for differential diagnosis between benign gynecologic disease and ovarian cancer: a systematic review and meta-analysis. European Journal of Obstetrics and Gynecology and Reproductive Biology. 2013; 167 (1): 81–85.
12. Huhtinen K, Suvitie P, Hiissa J, et al. Serum HE4 concentration differentiates malignant ovarian tumours from ovarian endometriotic cysts. British Journal of Cancer. 2009; 100 (8): 1315–1319.
13. Macedo A.C., da Rosa M.I., Lumertz S., Medeiros L.R. Accuracy of serum human epididymis protein 4 in ovarian cancer diagnosis: a systematic review and meta-analysis. Int J Gynecol Cancer. — 2014. — Sep;24(7):1222–31.
14. Moore RG, McMeekin DS, Brown AK, et al. A novel multiple marker bioassay utilizing HE4 and CA125 for the prediction of ovarian cancer in patients with a pelvic mass. Gynecologic Oncology. 2009, 112 (1): 40–46.
15. Huhtinen K., Suvitie P., Hiissa J. et al. Serum HE4 concentration differentiates malignant ovarian tumours from ovarian endometriotic cysts. Br J Cancer. 2009; 100 (8): 1315-19.
16. Holcomb K., Vucetic Z., Miller M.C., Knapp R.C. Human epididymis protein 4 offers superior specifi city in the differentiation of benign and malignant adnexal masses in premenopausal women. Am J Obstet Gynecol 2011;205(4):358.e1–6.
17. DePriest P.D., Shenson D., Fried A., Hunter J.E., Andrews S.J., Gallion H.H. et al. A morphology index based on sonographic findings in ovarian cancer. Gynecol. Oncol. 1993; 51(1): 7-11.
18. Ferrazzi E., Zanetta G., Dordoni D., Berlanda N., Mezzopane R., Lissoni A.A. Transvaginal ultrasonographic characterization of ovarian masses: comparison of five scoring systems in a multicenter study. Ultrasound Obstet. Gynecol. 1997; 10(3): 192-7.
19. Guerriero S, Alcazar JL, Ajossa S, Galvan R, Laparte C, Garcia-Manero M et al. Transvaginal color Doppler imaging in the detection of ovarian cancer in a large study population. Int J Gynecol Cancer. 2010;20(5):781-786.
20. Наркевич А.Н., Борисова Е.А., Макаренко Т.А., Система дифференциальной диагностики злокачественных опухолей придатков матки на основе нейронной сети// Медицинская техника. - 2017. - №5.- С.- 49-52.
21. Paulsen T., Kjaerheim K., Kaern J., Tretli S., Trope C. Improved short-term survival for advanced ovarian, tubal, and peritoneal cancer patients operated at teaching hospitals. Int. J. Gynecol. Cancer. 2006; 16(supрl. 1): S11–17.
22. Siegel R., Ward E., Brawley O., Jemal A.Cancer statistics 2011: the impact of eliminating socioeconomic and racial disparities on premature cancer deaths. CA Cancer J Clin 2011;61(4):212–36.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРОВАНИЯ СЕРОЗНОЙ КАРЦИНОМЫ ЯИЧНИКОВ | 2020 |
|
RU2749361C1 |
| Способ прогнозирования развития доброкачественных опухолей яичников у женщин постменопаузального возраста | 2025 |
|
RU2840309C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ АСЦИТНО-ИНФИЛЬТРАТИВНОЙ ФОРМЫ РАКА ЯИЧНИКОВ И АБДОМИНАЛЬНОГО ТУБЕРКУЛЁЗА | 2015 |
|
RU2585959C1 |
| Способ диагностики I-II стадий серозного рака яичников высокой степени злокачественности по липидному профилю сыворотки крови | 2022 |
|
RU2807396C1 |
| Способ прогнозирования перитонеального распространения рака яичников | 2019 |
|
RU2722654C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗМОЖНОСТИ ОЗЛОКАЧЕСТВЛЕНИЯ ОПУХОЛИ ЯИЧНИКА У ЖЕНЩИН РЕПРОДУКТИВНОГО ВОЗРАСТА | 2019 |
|
RU2713795C1 |
| Способ определения риска развития рецидива эндометриоидных кист яичников после оперативного лечения | 2023 |
|
RU2811890C1 |
| Способ определения эффективности химиотерапии препаратами платины при раке яичников III-IV стадии | 2020 |
|
RU2738167C1 |
| Способ ранней диагностики серозной карциномы яичника высокой степени злокачественности на основании изменения клеточного состава эпителия маточной трубы | 2016 |
|
RU2641094C1 |
| Способ дифференциальной диагностики рака яичников, кистозных образований яичника и рака тела матки | 2024 |
|
RU2836527C1 |

Изобретение относится к медицине, а именно к гинекологии и онкологии, и может быть использовано для дифференциальной диагностики доброкачественных и злокачественных образований яичников. Проводят количественную оценку в баллах риска малигнизации по формуле АхВхС. А – это особенности возрастного периода женщины: репродуктивный возраст – 1 балл, постменопауза – 4 балла. В – наличие таких ультразвуковых признаков, как многокамерное образование, солидное образование, двустороннее поражение, наличие асцита, наличие метастазов. При отсутствии или выявлении одного ультразвукового признака В равен 1 баллу. При наличии от двух до пяти признаков В равен 4 баллам. С – концентрация опухолевого маркера НЕ-4 (пмоль/л) в сыворотке крови. Значение индекса более 170 у пациенток репродуктивного возраста и более 340 у пациенток в постменопаузе позволяет прогнозировать злокачественный характер образований яичников. Способ обеспечивает дифференциальную диагностику доброкачественных и злокачественных образований яичников за счет использования данных УЗИ и использования в качестве опухолевого маркера в сыворотке крови НЕ-4. 3 табл., 3 пр.
Способ дифференциальной диагностики доброкачественных и злокачественных образований яичников, включающий количественную оценку в баллах риска малигнизации по формуле АхВхС, где А – особенности возрастного периода женщины: репродуктивный возраст – 1 балл, постменопауза – 4 балла, В – наличие таких ультразвуковых признаков, как многокамерное образование, солидное образование, двустороннее поражение, наличие асцита, наличие метастазов: при отсутствии или выявлении одного ультразвукового признака – 1 балл, при наличии от двух до пяти признаков – 4 балла, С – концентрация опухолевого маркера в сыворотке крови, отличающийся тем, что в качестве опухолевого маркера в сыворотке крови определяют уровень НЕ-4 (пмоль/л); значение индекса более 170 у пациенток репродуктивного возраста и более 340 у пациенток в постменопаузе позволяет прогнозировать злокачественный характер образований яичников.
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ АСЦИТНО-ИНФИЛЬТРАТИВНОЙ ФОРМЫ РАКА ЯИЧНИКОВ И АБДОМИНАЛЬНОГО ТУБЕРКУЛЁЗА | 2015 |
|
RU2585959C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕПОДОБНЫХ ОБРАЗОВАНИЙ И ОПУХОЛЕЙ ЯИЧНИКОВ У БЕРЕМЕННЫХ | 2007 |
|
RU2325118C1 |
| US 20140193919 A1, 10.07.2014 | |||
| ЕВТУШЕНКО И | |||
| Д | |||
| и др | |||
| Объемные образования яичников в постменопаузе: морфологическая структура и дифференциальная диагностика на предоперационном этапе | |||
| Доктор.Ру | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| JACOBS I | |||
| et al | |||
| Плуг с фрезерным барабаном для рыхления пласта | 1922 |
|
SU125A1 |
| Rritisli Jourrial oJ Obstetrics and Gynuecology | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Водяное колесо со складными лопастями | 1924 |
|
SU922A1 |
Авторы
Даты
2019-04-24—Публикация
2018-05-08—Подача