Ссылка на список последовательностей, представленный в электронном виде
[001] Заверенная копия файла со списком последовательностей под названием «PD034766IN-SC sequence listing.txt», созданного 30 июля 2019 г., имеющего размер 11 кБ и поданного в электронном виде одновременно с описанием настоящей заявки, является частью настоящей заявки.
Область изобретения
[002] Настоящее изобретение относится к оптимизированным по кодонам синтетическим нуклеотидным последовательностям, кодирующим инсектицидный кристаллический белок Bacillus thuringiensis (Bt), обладающий инсектицидной активностью против насекомых-вредителей. Настоящее изобретение также относится к экспрессии этих последовательностей в растениях.
Предшествующий уровень техники
[003] Насекомые-вредители являются основным фактором гибели сельскохозяйственных культур во всем мире и, по мнению специалистов, ответственны за уничтожение одной пятой общемирового урожая сельскохозяйственных культур ежегодно. В процессе искусственного отбора культур, подходящих для употребления человеком в пищу, также попадаются растения, в высокой степени чувствительные к заражению насекомыми, что в конечном итоге, снижает их экономическую ценность и повышает стоимость производства.
[004] Традиционно, борьба с насекомыми-вредителями осуществляется с помощью химических и/или биологических пестицидов. Использование химических пестицидов создает определенные проблемы, связанные с загрязнением окружающей среды, вызываемым производством и использованием этих пестицидов. Из-за таких проблем, Регуляторными органами было запрещено или ограничено использование некоторых наиболее опасных пестицидов.
[005] Кроме того, хорошо известен тот факт, что насекомые-вредители способны со временем эволюционировать в процессе естественного отбора, который может адаптироваться к новым ситуациям, например, преодолевать влияние токсичных веществ или обходить естественную или искусственную устойчивость растений к вредителям, что еще больше усугубляет имеющиеся проблемы.
[006] Биологические пестициды являются экологически и коммерчески приемлемой альтернативой химическим пестицидам. Они представляют меньший риск загрязнения и опасности для окружающей среды и обеспечивают большую целевую специфичность, чем традиционные химические инсектициды широкого спектра действия.
[007] Известно, что некоторые виды микроорганизмов рода Bacillus, например Bacillus thuringiensis (Bt), обладают инсектицидной активностью против широкого круга насекомых-вредителей. Инсектицидная активность, по-видимому, сосредоточена в параспоральных тельцах включения кристаллического белка, хотя инсектицидные белки также были выделены на стадии вегетативного роста Bacillus thuringiensis.
[008] Экспрессия генов инсектицидного кристаллического белка (cry) Bacillus thuringiensis (Bt) в растениях известна специалистам в данной области, однако, было обнаружено, что чрезвычайно трудно экспрессировать нативный ген Bt в растениях. Были предприняты попытки экспрессировать ген белка cry Bt в растениях в сочетании с различными промоторами, функционирующими в растениях. Однако, в трансгенных растениях были достигнуты только низкие уровни этого белка.
[009] Одной из причин низкого уровня экспрессии гена cry Bt в растении является высокое содержание A/T в последовательности ДНК Bt по сравнению с генами растений, в которых соотношение G/C выше, чем A/T. Общее значение A/T для бактериальных генов составляет 60-70%, а для генов растений - 40-50%. Как следствие, соотношение GC при использовании кодонов генов cry явно недостаточно для их экспрессии на оптимальном уровне. Более того, A/T-богатая область может также содержать сайты терминации транскрипции (полиаденилирования AATAAA), мотив нестабильности мРНК (ATTTA) и скрытые сайты сплайсинга мРНК. Было обнаружено, что использование кодонов нативного гена cry Bt значительно отличается от использования кодонов гена растения. В результате, использование мРНК этого гена может оказаться неэффективным. Использование кодонов может влиять на экспрессию генов на уровне трансляции, транскрипции или процессинга мРНК. В целях оптимизации инсектицидного гена для экспрессии в растениях были предприняты попытки изменить ген так, чтобы он был максимально похож на природные гены, содержащиеся в трансформируемом растении-хозяине.
[0010] Однако, создание сортов сельскохозяйственных культур, экспрессирующих высокий/оптимальный уровень белка cry Bt, сообщающего устойчивость к определенным насекомым-вредителям, все еще остается серьезной проблемой в сельском хозяйстве. Повышенная экспрессия генов инсектицидных белков имеет решающее значение для выращивания генетически улучшенных растений с агрономически приемлемыми уровнями устойчивости к насекомым. Были предприняты различные попытки регулировать или предотвращать заражение сельскохозяйственных культур насекомыми, однако, некоторые насекомые-вредители все еще представляют серьезную проблему для специалистов в области сельского хозяйства. Следовательно, потребность в выращивании устойчивых к насекомым трансгенных сельскохозяйственных культур с желаемыми уровнями экспрессии инсектицидных белков в трансгенных растениях остается актуальной.
[0011] Настоящее изобретение позволяет решить существующие проблемы, связанные с заражением растений насекомыми-вредителями, путем получения оптимизированной по кодонам синтетической последовательности ДНК растений, кодирующей белок Cry2Ai Bt, обладающий инсектицидной активностью против насекомых-вредителей.
Краткое описание сущности изобретения
[0012] Настоящее изобретение относится к оптимизированным по кодонам синтетическим нуклеотидным последовательностям, кодирующим белок B. thuringiensis, обладающий инсектицидной активностью против насекомых-вредителей. Настоящее изобретение относится к способам усиления экспрессии гетерологичных генов в клетках растений. Ген или кодирующую область гена cry2Ai конструируют так, чтобы получить предпочтительную последовательность кодона, характерную для данного растения. Таким образом, кодоны для белка Cry2Ai оптимизируют для его экспрессии в растении. Такие оптимизированные для растений кодирующие последовательности могут быть функционально связаны с промотором, способным регулировать экспрессию кодирующих последовательностей в клетке растения. Трансформированные клетки-хозяева и трансгенные растения, содержащие оптимизированные по кодонам синтетические нуклеотидные последовательности B. thuringiensis, также являются аспектами настоящего изобретения.
[0013] Одной из целей настоящего изобретения является получение оптимизированных по кодонам синтетических нуклеотидных последовательностей, кодирующих инсектицидный белок, где нуклеотидные последовательности были оптимизированы для экспрессии в растениях.
[0014] Другой целью настоящего изобретения является получение оптимизированных по кодонам синтетических нуклеотидных последовательностей, кодирующих инсектицидный белок Bt для максимизации экспрессии белков Bt в растении, а предпочтительно в растении, выбранном из группы, состоящей из баклажанов, хлопчатника, риса, томатов, пшеницы, кукурузы, сорго, овса, проса, бобовых, капусты, цветной капусты, брокколи, Brassica sp., фасоли, гороха, голубиного гороха, картофеля, перца, тыквы, салата-латука, сладкого картофеля, канолы, сои, люцерны, арахиса и подсолнечника.
[0015] В соответствии с настоящим изобретением, авторами настоящего изобретения были синтезированы гены кристаллического инсектицидного белка Cry2Ai Bt, кодоны которых были оптимизированы для повышения уровня экспрессии в растении. Однако, вместо оптимизации кодонов так, чтобы они были похожи на ген растения с точки зрения общего распределения кодонов, авторами настоящего изобретения были оптимизированы кодоны так, чтобы они были наиболее предпочтительными в растениях при синтезе нуклеотидных последовательностей согласно изобретению. Оптимизация по кодонам, предпочтительная для конкретных растений, является эффективной для экспрессии высокого уровня инсектицидного белка Bt в двудольных растениях, таких как хлопчатник, баклажаны и томаты; в однодольных растениях, таких как рис, и в бобовых растениях, таких как нут и голубиный горох.
[0016] Оптимизированные по кодонам синтетические нуклеотидные последовательности согласно изобретению были получены из белка Cry2Ai Bacillus thuringiensis, имеющего аминокислотную последовательность, представленную в SEQ ID NO: 1 (NCBI GenBank: ACV97158.1). Белок с аминокислотной последовательностью, представленной в SEQ ID NO: 1, является активным против различных чешуекрылых насекомых, включая Helicoverpa armigera - хлопковую совку и кукурузную уховертку, Cnaphalocrocis medinalis - рисовую листовертку и Scirpophaga incertulas - рисового желтого стеблевого сверлильщика и Pectinophora gossypiella.
[0017] Хотя настоящее изобретение было проиллюстрировано на синтезе оптимизированных по кодонам нуклеотидов Cry2Ai Bt для экспрессии в растениях, однако, известно, что оптимизированные по кодонам нуклеотиды Cry2Ai Bt могут быть использованы для оптимизации экспрессии белка в таких растениях, как хлопчатник, баклажаны, томаты, рис и кукуруза.
[0018] Соответственно, в одном из своих аспектов, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, кодирующей белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1, где указанная нуклеотидная последовательность выбрана из группы, состоящей из: (а) нуклеотидной последовательности, представленной в SEQ ID NO: 2; (b) нуклеотидной последовательности, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положения нуклеотида 262 до 402 и/или от 1471 до 1631; и (c) нуклеотидной последовательности, комплементарной нуклеотидной последовательности (a) и (b).
[0019] В другом своем аспекте, настоящее изобретение относится к молекуле нуклеиновой кислоты, содержащей оптимизированную по кодонам последовательность для экспрессии в растении, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, представленной в SEQ ID NO: 2; (b) нуклеотидной последовательности, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положений нуклеотидов 262 до 402 и/или от 1471 до 1631; и (c) нуклеотидной последовательности, комплементарной нуклеотидной последовательности (a) и (b).
[0020] В другом своем аспекте, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, кодирующей белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1, где указанная нуклеотидная последовательность представляет собой:
а. последовательность, представленную в SEQ ID NO: 2, или комплементарную ей нуклеотидную последовательность; или
b. нуклеотидную последовательность, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положения нуклеотида 262 до 402 и/или от 1471 до 1631, или комплементарную ей нуклеотидную последовательность.
[0021] В другом своем аспекте, настоящее изобретение относится к рекомбинантной ДНК, содержащей раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность, где указанная нуклеотидная последовательность функционально связана с гетерологичным регуляторным элементом.
[0022] В другом своем аспекте, настоящее изобретение относится к конструкции ДНК для экспрессии представляющего интерес инсектицидного белка, содержащей 5'-нетранслируемую последовательность; кодирующую последовательность, кодирующую инсектицидный белок Cry2Ai, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее инсектицидную часть, и 3'-нетранслируемую область, где указанная 5'-нетранслируемая последовательность включает промотор, функциональный в клетке растения; указанная кодирующая последовательность представляет собой раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность; а указанная 3'-нетранслируемая последовательность включает последовательность терминации транскрипции и сигнал полиаденилирования.
[0023] В другом своем аспекте, настоящее изобретение относится к плазмидному вектору, содержащему раскрытую здесь рекомбинантную ДНК или раскрытую здесь конструкцию ДНК.
[0024] В другом своем аспекте, настоящее изобретение относится к клетке-хозяину, содержащей раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность.
[0025] В другом своем аспекте, настоящее изобретение относится к способу сообщения растению устойчивости к насекомым, где указанный способ включает:
(а) встраивание в клетку растения раскрытой здесь оптимизированной по кодонам синтетической нуклеотидной последовательности, где нуклеотидная последовательность функционально связана с (i) промотором, функциональным в клетке растения, и (ii) терминатором;
(b) получение трансформированной клетки растения из клетки растения стадии (а), где указанная трансформированная клетка растения содержит указанную оптимизированную по кодонам синтетическую нуклеотидную последовательность, раскрытую в настоящей заявке; и
(с) получение трансгенного растения из указанной трансформированной клетки растения на стадии (b), где указанное трансгенное растение содержит указанную раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность.
[0026] В другом своем аспекте, настоящее изобретение относится к трансгенному растению, содержащему раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность.
[0027] В другом своем аспекте, настоящее изобретение относится к композиции, содержащей Bacillus thuringiensis, включающую раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность, кодирующую белок Cry2Ai, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1.
[0028] В другом своем аспекте, настоящее изобретение относится к способу борьбы с заражением насекомыми сельскохозяйственных культур и обеспечения устойчивости к насекомым, где указанный способ включает контактирование указанного сельскохозяйственного растения с инсектицидно эффективным количеством раскрытой здесь композиции.
[0029] Еще одним аспектом настоящего изобретения является применение оптимизированной по кодонам синтетической нуклеотидной последовательности, конструкции ДНК или плазмиды, раскрытой в настоящей заявке, для получения трансгенных растений, устойчивых к насекомым.
[0030] Еще одним аспектом изобретения является применение раскрытой здесь оптимизированной по кодонам синтетической нуклеотидной последовательности для получения инсектицидной композиции, где указанная композиция содержит клетки Bacillus thuringiensis, включающие указанные нуклеотидные последовательности.
Краткое описание чертежей
[0031] На фигуре 1 показана карта конструкции Т-ДНК pGreen0029-CaMV35S-201D1.
[0032] На фигуре 2 показана генетическая трансформация и регенерация трансгенных растений хлопчатника.
Краткое описание последовательностей
[0033] SEQ ID NO: 1 представляет собой аминокислотную последовательность белка Cry2Ai (NCBI GenBank: ACV97158.1).
[0034] SEQ ID NO: 2 представляет собой оптимизированную по кодонам синтетическую нуклеотидную последовательность cry2Ai (201D1), кодирующую белок Cry2Ai (SEQ ID NO: 1).
[0035] SEQ ID NO: 3 представляет собой оптимизированную по кодонам синтетическую нуклеотидную последовательность cry2Ai (201D2), кодирующую белок Cry2Ai (SEQ ID NO: 1).
[0036] SEQ ID NO: 4 представляет собой оптимизированную по кодонам синтетическую нуклеотидную последовательность cry2Ai (201D3), кодирующую белок Cry2Ai (SEQ ID NO: 1).
[0037] SEQ ID NO: 5 представляет собой оптимизированную по кодонам синтетическую нуклеотидную последовательность cry2Ai (201D4), кодирующую белок Cry2Ai (SEQ ID NO: 1).
[0038] SEQ ID NO: 6 представляет собой оптимизированную по кодонам синтетическую нуклеотидную последовательность cry2Ai (201D5), кодирующую белок Cry2Ai (SEQ ID NO: 1).
[0039] SEQ ID NO: 7 представляет собой последовательность прямого праймера для амплификации последовательности ДНК 201D1 (SEQ ID NO: 2).
[0040] SEQ ID NO: 8 представляет собой последовательность обратного праймера для амплификации последовательности ДНК 201D1 (SEQ ID NO: 2).
[0041] SEQ ID NO: 9 представляет собой последовательность прямого праймера для амплификации гена ДНК nptII.
[0042] SEQ ID NO: 10 представляет собой последовательность обратного праймера для амплификации гена ДНК nptII.
Подробное описание
[0043] Подробное описание, представленное в настоящей заявке, приводится для облегчения осуществления настоящего изобретения специалистами в данной области и не должно рассматриваться как чрезмерно ограничивающее объем изобретения, и специалисты в данной области могут внести в обсуждаемые здесь варианты осуществления изобретения модификации и изменения, не выходящие за рамки существа и объема изобретения. Настоящее изобретение будет более подробно описано ниже со ссылкой на прилагаемые чертежи и/или список последовательностей, в которых показаны и/или описаны некоторые, но не все варианты осуществления изобретения. Настоящее изобретение может быть осуществлено во многих различных формах и не должно ограничиваться представленными здесь вариантами.
[0044] Хотя в настоящей заявке используются конкретные термины, однако, они употребляются только в общем и описательном смысле, но не в целях ограничения изобретения. Нижеследующие определения представлены для лучшего понимания вариантов осуществления изобретения.
[0045] Следует отметить, что, в описании и в прилагаемой формуле изобретения, артикли «a», «an» и «the», употребляемые с существительными в единственном числе, могут относиться к одному или более, чем одному (то есть, по меньшей мере к одному) грамматическому объекту, с которым употребляется данный артикль, если из контекста описания не следует обратное. Так, например, ссылка на «зонд» означает, что в композиции может присутствовать более, чем один такой зонд. Аналогичным образом, ссылка на «элемент» означает один или более элементов.
[0046] Во всем описании изобретения, слово «содержит» или «содержащий» следует понимать как включение указанного элемента, целого числа или стадии, или группы элементов, целых чисел или стадий, но не исключение любого другого элемента, целого числа или стадии, или группы элементов, целых чисел или стадий.
[0047] Единицы, префиксы и символы могут быть обозначены в их общепринятой форме СИ. Если это не оговорено особо, то нуклеиновые кислоты записаны слева направо в ориентации от 5' до 3', а аминокислотные последовательности записаны слева направо в ориентации от амино- до карбокси-конца, соответственно. Числовые диапазоны включают числа, определяющие диапазон. Аминокислоты могут обозначаться здесь либо их общеизвестными трехбуквенными символами, либо однобуквенными символами, рекомендованными Комиссией по биохимической номенклатуре IUPAC-IUB. Аналогичным образом, нуклеотиды могут также обозначаться их общепринятыми однобуквенными кодами. Вышеуказанные термины будут более полно определены со ссылкой на описание в целом.
[0048] Термин «нуклеиновая кислота» обычно означает крупные полинуклеотиды. Термин «нуклеиновая кислота» и «нуклеотидная последовательность» используются здесь как синонимы. Этот термин включает ссылку на дезоксирибонуклеотидный или рибонуклеотидный полимер в одноцепочечной или двухцепочечной форме и, если это не оговорено особо, охватывает известные аналоги (например, пептид-содержащие нуклеиновые кислоты), имеющие, в основном, природные нуклеотиды, поскольку они гибридизуются с одноцепочечными нуклеиновыми кислотами по механизму, аналогичному механизмам гибридизации природных нуклеотидов. Нуклеотиды представляют собой субъединицу, которая полимеризуется (соединяется в длинную цепь) с образованием нуклеиновых кислот (ДНК и РНК). Нуклеотиды состоят из трех более мелких компонентов: сахара рибозы, азотистого основания и фосфатной(ых) группы (групп).
[0049] «Полинуклеотид» означает одиночную цепь или параллельные и антипараллельные цепи нуклеиновой кислоты. Таким образом, полинуклеотид может представлять собой одноцепочечную или двухцепочечную нуклеиновую кислоту.
[0050] Термин «олигонуклеотид» обычно означает короткие полинуклеотиды, длина которых, в основном не превышает приблизительно 50 нуклеотидов. Следует отметить, что если нуклеотидная последовательность представлена последовательностью ДНК (то есть, A, T, G, C), то этот термин также включает последовательность РНК (то есть, A, U, G, C), где «U» заменяет «Т».
[0051] Термины «оптимизированные по кодонам синтетические нуклеотидные последовательности» означают негеномные нуклеотидные последовательности и используются здесь как синонимы для обозначения синтетических нуклеотидных последовательностей или молекулы нуклеиновой кислоты, которая имеет одно или более изменений в нуклеотидной последовательности по сравнению с нативной или геномной нуклеотидной последовательностью. В некоторых вариантах осуществления изобретения, изменение нативной или геномной молекулы нуклеиновой кислоты включает, но не ограничивается ими, изменения в последовательности нуклеиновой кислоты вследствие оптимизации по кодонам последовательности нуклеиновой кислоты для экспрессии в конкретном организме, например, в растении, и вследствие вырожденности генетического кода; изменения в последовательности нуклеиновой кислоты для введения по меньшей мере одной аминокислотной замены, инсерции, делеции и/или добавления по сравнению с нативной или геномной последовательностью; изменения в последовательности нуклеиновой кислоты для введения сайтов рестриктирующих ферментов, удаления одного или нескольких интронов, ассоциированных с последовательностью геномной нуклеиновой кислоты, вставки одного или более гетерологичных интронов, делеции одной или более вышерасположенных или нижерасположенных регуляторных областей, связанных с последовательностью геномной нуклеиновой кислоты, инсерции одной или более гетерологичных вышерасположенных или нижерасположенных регуляторных областей, делеции 5'- и/или 3'-нетранслируемой области, связанной с последовательностью геномной нуклеиновой кислоты, инсерции гетерологичной 5'- и/или 3'-нетранслируемой области и модификации сайта полиаденилирования.
[0052] В описании настоящего изобретения используются нижеследующие сокращения для часто встречающихся оснований нуклеиновых кислот. «А» означает аденозин, «С» означает цитидин, «G» означает гуанозин, «Т» означает тимидин, а «U» означает уридин.
[0053] В некоторых вариантах осуществления изобретения, молекула не-геномной нуклеиновой кислоты представляет собой кДНК. В некоторых вариантах осуществления изобретения, молекула негеномной нуклеиновой кислоты представляет собой синтетическую нуклеотидную последовательность. Оптимизированные по кодонам нуклеотидные последовательности могут быть получены для любого прдставляющего интерес организма с применением способов, известных специалистам в данной области, например, Murray et al. (1989) Nucleic Acids Res. 17:477-498. Оптимизированные нуклеотидные последовательности могут быть использованы для повышения уровня экспрессии пестицидного белка в растении, например, в однодольных и двудольных растениях, таких как рис, томат и хлопчатник.
[0054] Недавно разработанные последовательности ДНК cry2Ai, раскрытые в настоящей заявке, называются «оптимизированными по кодонам синтетическими нуклеотидными последовательностями cry2Ai».
[0055] Термины «конструкция ДНК», «нуклеотидные конструкции» и «кластер для экспрессии ДНК» используются здесь как синонимы и не ограничиваются вариантами осуществления изобретения, относящимися к нуклеотидным конструкциям, содержащим ДНК. Специалистам в данной области будет очевидно, что нуклеотидные конструкции, а в частности, полинуклеотиды и олигонуклеотиды, состоящие из рибонуклеотидов и комбинаций рибонуклеотидов и дезоксирибонуклеотидов, также могут быть использованы в раскрытых здесь способах.
[0056] Используемые здесь термины «рекомбинантная» молекула нуклеиновой кислоты или ДНК, или «рекомбинантный» полинуклеотид означают молекулу нуклеиновой кислоты или полинуклеотид ДНК, которые были изменены или получены человеком и находятся в рекомбинантной бактериальной или растительной клетке-хозяине. Так, например, рекомбинантный полинуклеотид может представлять собой полинуклеотид, выделенный из генома; кДНК, полученную путем обратной транскрипции РНК; синтетическую молекулу нуклеиновой кислоты или искусственную комбинацию двух иным образом разделенных сегментов последовательности, например, путем химического синтеза или путем модификации выделенных сегментов полинуклеотидов методами генной инженерии.
[0057] Используемый здесь термин «гомологичный» относится к сходству нуклеотидных последовательностей между двумя областями одной и той же цепи нуклеиновой кислоты или между областями двух различных цепей нуклеиновой кислоты. Если положение нуклеотидного остатка в обеих областях занято одним и тем же нуклеотидным остатком, то эти области являются гомологичными в этом положении. Первая область гомологична второй области, если по меньшей мере одно положение нуклеотидного остатка каждой области занято одним и тем же остатком. Гомология между двумя областями выражается отношением положений нуклеотидных остатков в двух областях, которые заняты одним и тем же нуклеотидным остатком. Так, например, область с нуклеотидной последовательностью 5'-ATTGCC-3' и область с нуклеотидной последовательностью 5'-TATGGC-3' имеют 50% гомологию. Предпочтительно, первая область включает первую часть, а вторая область включает вторую часть, при этом, по меньшей мере приблизительно 50%, а предпочтительно по меньшей мере приблизительно 75%, по меньшей мере приблизительно 90% или, по меньшей мере, приблизительно 95% положений нуклеотидных остатков в каждой из частей заняты одним и тем же нуклеотидным остатком. Более предпочтительно, чтобы все положения нуклеотидных остатков каждой из частей были заняты одним и тем же нуклеотидным остатком.
[0058] Оптимальное выравнивание последовательностей для сравнения может быть проведено с помощью компьютеризированных реализаций алгоритмов, известных специалистам в данной области (GAP, BESTFIT, BLAST, PASTA и TFASTA в пакете программ Wisconsin Genetics Software Package, Genetics Computer Group (GCG), 575 Science Dr., Madison, WI) или путем визуального наблюдения.
[0059] «Процент идентичности последовательностей», используемый в настоящем описании, определяют путем сравнения двух оптимально выровненных последовательностей в окне сравнения, где фрагмент полинуклеотидной или аминокислотной последовательности в окне сравнения может содержать добавления или делеции (например, пробелы или выступы) по сравнению с эталонной последовательностью (которая не содержит добавлений или делеций) для оптимального выравнивания двух последовательностей. Процент рассчитывают путем определения числа положений, в которых присутствуют одинаковые основания нуклеиновых кислот или аминокислотные остатки в обеих последовательностях, для получения количества совпадающих положений, деления количества совпадающих положений на общее количество положений в окне сравнения и умножения результата на 100 с получением процента идентичности последовательностей.
[0060] Оптимальное выравнивание последовательностей для сравнения может быть проведено с помощью компьютеризированных реализаций алгоритмов, известных специалистам в данной области (GAP, BESTFIT, BLAST, PASTA и TFASTA в пакете программ Wisconsin Genetics Software Package, Genetics Computer Group (GCG), 575 Science Dr., Madison, WI) или путем визуального наблюдения.
[0061] Используемый здесь термин «по существу идентичные нуклеотидные последовательности» означает полинуклеотид, содержащий последовательность, которая по меньшей мере на 65%, а предпочтительно по меньшей мере на 69%-77% идентична эталонной последовательности.
[0062] Используемый здесь термин «промотор/регуляторная последовательность» означает последовательность нуклеиновой кислоты, которая необходима для экспрессии продукта гена, функционально связанного с промоторной/регуляторной последовательностью. В некоторых случаях, эта последовательность может представлять собой последовательность корового промотора, а в других случаях, эта последовательность может также включать энхансерную последовательность и другие регуляторные элементы, которые необходимы для экспрессии продукта гена. Промоторная/регуляторная последовательность может, например, представлять собой последовательность, которая экспрессирует продукт гена по тканеспецифическому механизму.
[0063] «Конститутивный» промотор представляет собой промотор, который регулирует экспрессию гена, с которым он функционально связан в клетке по конститутивному механизму. Так, например, промоторы, которые регулируют экспрессию генов домашнего хозяйства в клетках, называются конститутивными промоторами.
[0064] «Индуцибельный» промотор представляет собой нуклеотидную последовательность, которая, если она функционально связана с полинуклеотидом, который кодирует или определяет продукт гена, вызывает образование продукта гена в живой клетке, по существу только в том случае, когда в клетке присутствует индуктор, который соответствует промотору.
[0065] «Тканеспецифический» промотор представляет собой нуклеотидную последовательность, которая, если она функционально связана с полинуклеотидом, который кодирует или определяет продукт гена, вызывает образование продукта гена в живой клетке, по существу только в том случае, когда клеткой является клетка ткани, тип которой соответствует типу промотора.
[0066] Используемый здесь термин «функционально связанный» означает любую связь, независимо от ориентации или расстояния, между регуляторной последовательностью и кодирующей последовательностью, где такая связь позволяет регуляторной последовательности регулировать экспрессию кодирующей последовательности. Термин «функционально связанный» также означает, что связываемые последовательности нуклеиновой кислоты являются смежными и, если это необходимо для соединения двух областей, кодирующих белок, смежными и находящимися в одной и той же рамке считывания. Термин «функционально связанный» также относится к функциональной связи между промотором и второй последовательностью, где промоторная последовательность инициирует и опосредует транскрипцию последовательности ДНК, соответствующей второй последовательности.
[0067] Используемый здесь термин «гетерологичная кодирующая последовательность ДНК», или «гетерологичная нуклеиновая кислота», или «гетерологичный полинуклеотид» означает любую кодирующую последовательность, отличающуюся от последовательности, которая в природе кодирует белок Cry2Ai, или любой гомолог белка Cry2Ai.
[0068] Используемый здесь термин «кодирующая область» означает часть гена, ДНК или нуклеотидной последовательности, которая кодирует белок. Термин «некодирующая область» означает часть гена, ДНК или нуклеотидной последовательности, которая не является кодирующей областью.
[0069] Используемые здесь термины «кодирующий» или «кодируемый» при их использовании в отношении конкретной нуклеиновой кислоты означают, что нуклеиновая кислота содержит необходимую информацию для прямой трансляции нуклеотидной последовательности в конкретный белок. Информация, посредством которой кодируется белок, определяется использованием кодонов. Нуклеиновая кислота, кодирующая белок, может содержать нетранслируемые последовательности (например, интроны) в пределах транслируемых областей нуклеиновой кислоты или может не содержать таких промежуточных нетранслируемых последовательностей (например, как в кДНК).
[0070] Термины «полипептид», «пептид» и «белок» используются здесь как синонимы и означают полимер, состоящий из аминокислотных остатков, связанных с встречающимися в природе структурными вариантами, и его синтетических не встречающихся в природе аналогов, связанных пептидными связями. Синтетические полипептиды могут быть синтезированы, например, с использованием автоматического синтезатора полипептидов. Эти термины применяются к аминокислотным полимерам, в которых один или несколько аминокислотных остатков представляют собой искусственный химический аналог соответствующей встречающейся в природе аминокислоты, а также к встречающимся в природе аминокислотным полимерам. Термины «остаток», «аминокислотный остаток» или «аминокислота» используются здесь как синонимы и означают аминокислоты, которые включены в белок, полипептид или пептид (в целом, «белок»). Аминокислота может представлять собой природную аминокислоту и, если это не оговорено особо, то она может включать известные аналоги природных аминокислот, которые могут действовать таким же образом, как и встречающиеся в природе аминокислоты.
[0071] Термин «белок» обычно означает крупные полипептиды. Термин «пептид» обычно означает короткие полипептиды. Однако, термин «полипептид» используется здесь для обозначения любого аминокислотного полимера, состоящего из двух или более аминокислотных остатков, связанных пептидными связями.
[0072] Используемый здесь термин «экспрессионный кластер» означает генетический модуль, содержащий ген и регуляторные области, необходимые для его экспрессии, которые могут быть включены в вектор.
[0073] «Вектор» представляет собой композицию веществ, которая содержит молекулу нуклеиновой кислоты, и которая может быть использована для доставки выделенной нуклеиновой кислоты вовнутрь клетки. Специалистам в данной области известно множество векторов, включая, но не ограничиваясь ими, линейные полинуклеотиды, полинуклеотиды, связанные с ионными или амфифильными соединениями, плазмиды и вирусы. Таким образом, термин «вектор» включает автономно реплицирующуюся плазмиду или вирус. Этот термин также следует понимать как включающий не-плазмидные и не-вирусные соединения, которые облегчают перенос нуклеиновой кислоты в клетки, такие как, например, соединения полилизина, липосомы и т.п. Примеры вирусных векторов включают, но не ограничиваются ими, аденовирусные векторы, аденоассоциированные вирусные векторы, ретровирусные векторы и т.п.
[0074] Термин «экспрессионный вектор» означает вектор, содержащий рекомбинантную нуклеиновую кислоту, включающую последовательности регуляции экспрессии, функционально связанные с нуклеотидной последовательностью, которая должна быть экспрессирована. Экспрессионный вектор содержит достаточное количество цис-действующих элементов для экспрессии; другие элементы для экспрессии могут поставляться клеткой-хозяином или в системе экспрессии in vitro. Векторы для экспрессии включают все векторы, известные специалистам в данной области, такие как космиды, плазмиды (например, «оголенные» или содержащиеся в липосомах) и вирусы, которые включают рекомбинантную нуклеиновую кислоту.
[0075] Используемый здесь термин «клетка-хозяин» означает клетку, которая содержит вектор и поддерживает репликацию и/или экспрессию экспрессионного вектора. Клетки-хозяева могут представлять собой прокариотические клетки, такие как E. coli, или эукариотические клетки, такие как клетки дрожжей, насекомых, амфибий или млекопитающих, или клетки однодольных или двудольных растений. Примером клетки-хозяина однодольного растения является клетка-хозяин риса, а примером клетки-хозяина двудольного растения является клетка-хозяин баклажана или томата. Если это возможно, то последовательность модифицируют во избежание образования предсказанных вторичных шпилечных структур мРНК.
[0076] Используемый здесь термин «токсин» означает полипептид, обладающий пестицидной активностью или инсектицидной активностью. Термин «токсин Bt» или «Bacillus thuringiensis» охватывает более широкий класс токсинов Cry, обнаруженных в различных штаммах Bt, которые включают такие токсины.
[0077] Термин «зонд» или «пробный зонд» означает молекулу, которая распознается своим комплементом или конкретным элементом микроматрицы. Примеры зондов, которые могут быть исследованы в соответствии с настоящим изобретением, включают, но не ограничиваются ими, ДНК, РНК, олигонуклеотиды, олигосахариды, полисахариды, сахара, белки, пептиды, моноклональные антитела, токсины, вирусные эпитопы, гормоны, рецепторы гормонов, ферменты, субстраты ферментов, кофакторы и лекарственные средства, включая агонисты и антагонисты рецепторов клеточной поверхности.
[0078] Используемый здесь термин «комплементарный» или «комплемент» относится к спариванию оснований, пуринов и пиримидинов, которые связываются посредством водородных связей в двухцепочечной нуклеиновой кислоте. Комплементарными являются следующие пары оснований: гуанин и цитозин; аденин и тимидин; и аденин и урацил. Используемые здесь термины включают полную и частичную комплементарность.
[0079] Используемый здесь термин «гибридизация» относится к процессу, в котором цепь нуклеиновой кислоты связывается с комплементарной цепью посредством спаривания оснований. Условия, используемые при гибридизации двух неидентичных, но очень похожих комплементарных нуклеиновых кислот, различаются в зависимости от степени комплементарности двух цепей и длины цепей. Таким образом, этот термин подразумевает как частичную, так и полную гибридизацию. Такие методы и условия хорошо известны специалистам в данной области.
[0080] Термины «инсектицидная активность» и «пестицидная активность» используются здесь как синонимы для обозначения активности организма или вещества (такого как, например, белок), которая может быть оценена по таким параметрам, но не ограничивается ими, как степень уничтожения вредителей, потеря массы вредителей, отпугивание вредителей и другие поведенческие и физические изменения вредителей после кормления и воздействия на них в течение соответствующего периода времени. Таким образом, организм или вещество, обладающие пестицидной активностью, негативно влияют по меньшей мере на один измеряемый параметр приспособляемости вредителей. Так, например, «инсектицидные белки» представляют собой белки, которые проявляют инсектицидную активность сами по себе или в сочетании с другими белками.
[0081] Используемый здесь термин «воздействие на насекомых-вредителей» относится к контролю изменений в питании, росте и/или поведении насекомых на любой стадии развития, включая, но не ограничиваясь ими, уничтожение насекомого, замедление его роста, подавление репродуктивной способности, антифидинговую активность и т.п.
[0082] Используемый здесь термин «пестицидно эффективное количество» означает количество вещества или организма, которые обладают пестицидной активностью, если они присутствуют в среде обитания вредителя. Для каждого вещества или организма, пестицидо эффективное количество определяют эмпирически для каждого вредителя, действующего в конкретной среде. Аналогичным образом, «инсектицидно эффективное количество» может использоваться для обозначения «пестицидо эффективного количества», если вредителем является насекомое-вредитель.
[0083] Используемые здесь термины «трансформированное растение» и «трансгенное растение» означают растение, геном которого содержит один или более гетерологичных полинуклеотидов. Гетерологичный(е) полинуклеотид(ы) стабильно интегрируется(ются) в геном трансгенного или трансформированного растения, в результате чего полинуклеотид передается последующим поколениям. Гетерологичный полинуклеотид может быть интегрирован в геном отдельно или как часть рекомбинантной молекулы ДНК.
[0084] Следует отметить, что используемый здесь термин «трансгенный» включает любую клетку растения, линию растительных клеток, каллус, ткань, часть растения или растение, генотип которого был изменен в результате присутствия одной или более гетерологичных нуклеиновых кислот. Этот термин включает трансгены, которые изначально были получены с применением метода генетической трансформации, известного специалистам в данной области, а также трансгены, которые были получены путем полового скрещивания или бесполого размножения из исходного трансгена.
[0085] Используемый здесь термин «исходное трансгенное растение» не включает модификацию генома (хромосомного или внехромосомного) обычными методами селекции растений или в результате естественных событий, таких как случайное перекрестное оплодотворение, не-рекомбинантное инфицирование вирусом, не-рекомбинантная бактериальная трансформация, не-рекомбинантная транспозиция или спонтанная мутация.
[0086] Используемый здесь термин «растение» включает целые растения, клетки растений, протопласты растений, культуры тканей клеток растений, из которых растения могут быть регенерированы, каллусы растений, скопления растений и клетки растений, которые являются интактными в растениях или в частях растений, таких как зародыши, пыльца, семяпочки, семена, листья, цветки, ветви, плоды, зерна, початки, стержни початков, шелуха, стебли, корни, кончики корней, пыльники и т.п. и их потомство. Части трансгенных растений входят в объем вариантов осуществления изобретения и включают, например, клетки растений, протопласты, ткани, каллус, зародыши, а также цветки, стебли, плоды, листья и корни, происходящие от трансгенных растений или их потомства, ранее трансформированных с использованием молекулы ДНК согласно изобретению и, следовательно, состоящих по меньшей мере частично из трансгенных клеток.
Ген cry Bacillus thuringiensis и оптимизация по кодонам
[0087] В настоящее время секвенировано приблизительно 400 генов cry, кодирующих δ-эндотоксины (Crickmore, N. 2005. Using worms to better understand how Bacillus thuringiensis kills insects. Trends in Microbiology, 13(8): 347-350). Различные δ-эндотоксины были подразделены на классы (Cry 1, 2, 3, 4 и т.п.) на основе сходства аминокислотных последовательностей. Эти классы состоят из нескольких подклассов (Cry1A, Cry1B, Cry1C и т.п.), которые сами подразделяются на подсемейства или варианты (Cry1Aa, Cry1Ab, Cry1Ac и т.п.). Гены каждого класса идентичны друг другу более, чем на 45%. Продукт каждого отдельного гена cry обычно имеет спектр активности, ограниченный личиночными стадиями небольшого числа видов. Однако, пока не удалось установить корреляцию между степенью идентичности белков Cry и их спектром активности. Белки Cry1Aa и Cry1Ac идентичны на 84%, но только Cry1Aa токсичен для Bombyx mori (L.). И напротив, Cry3Aa и Cry7Aa, которые идентичны только на 33%, оба активны против колорадского жука Leptinotarsa decemlineata. Другие токсины Cry вообще не активны против насекомых, но активны против других беспозвоночных. Так, например, белки классов Cry5 и Cry6 активны против нематод. Совсем недавно были охарактеризованы бинарные токсины Bt, обозначенные как Cry34Ab1/Cry35Ab1, которые являются активными против различных жесткокрылых насекомых-вредителей семейства Chrysomelidae. Им было присвоено обозначение Cry, хотя они имеют небольшую гомологию с другими членами семейства токсинов Cry.
[0088] Было обнаружено, что для достижения желаемых уровней экспрессии гетерологичных белков в трансгенных растениях было бы желательно изменять кодирующую последовательность нативной геномной ДНК, иногда называемой последовательностью дикого типа или исходной последовательностью, различными способами так, чтобы использование кодонов более точно соответствовало использованию кодонов в видах растения-хозяина, и аналогично, содержание G+C в кодирующей последовательности более точно соответствовало содержанию G+C растения-хозяина того же вида.
[0089] Специалисту в области молекулярной биологии растений известно, что несколько последовательностей ДНК могут быть сконструированы для кодирования одной аминокислотной последовательности. Распространенным средством повышения уровня экспрессии области, кодирующей представляющий интерес белок, является модификация кодирующей области таким образом, чтобы ее состав кодонов напоминал общий состав кодонов хозяина, в котором данный ген должен быть экспрессирован.
[0090] Геномная/нативная нуклеиновая кислота может быть оптимизирована для увеличения уровня экспрессии в организме-хозяине. Таким образом, если организм-хозяин представляет собой растение, то синтетические нуклеиновые кислоты могут быть синтезированы с использованием предпочтительных для растений кодонов для повышения уровня экспрессии. Так, например, хотя последовательности нуклеиновых кислот согласно вариантам осуществления изобретения могут быть экспрессированы как в однодольных, так и в двудольных растениях, однако, последовательности могут быть модифицированы с учетом конкретных предпочтений кодонов и предпочтений содержания GC однодольных или двудольных растений, поскольку эти предпочтения, как было показано, различаются (Murray et al. (1989) Nucleic Acids Res. 17: 477-498). Таким образом, предпочтительный кодон риса для конкретной аминокислоты может происходить из известных последовательностей генов риса, а предпочтительный кодон для баклажанов для конкретной аминокислоты может происходить из известных последовательностей генов баклажана.
[0091] Известно, что дополнительные модификации последовательности повышают уровень экспрессии генов в клетке-хозяине. Такие модификации включают удаление последовательностей, кодирующих ложные сигналы полиаденилирования, сигналы экзон-интронных сайтов сплайсинга, транспозоноподобные повторы и другие хорошо охарактеризованные последовательности, которые могут оказывать негативное влияние на экспрессию генов. Содержание GC в последовательности может быть доведено до средних уровней для данной клетки-хозяина, вычисленных по отношению к известным генам, экспрессированным в клетке-хозяине.
[0092] Vaeck и др. (Vaeck M, Reynaerts A, Höfte H, Jansens S, De Beukeleer M, Dean C, Zabeau M, Van Montagu M, Leemans J (1987) Transgenic plants protected from insect attack. Nature 327:33-37) сообщили о создании устойчивых к насекомым трансгенных растений табака, экспрессирующих ген cry1Ab Bt для защиты от европейского кукурузного пилильщика, то есть, одного из основных вредителей, поражающих кукурузу в США и Европе. Однако, несмотря на использование сильных промоторов, продуцирование токсинов в растениях было изначально слишком слабым для их эффективного использования в сельском хозяйстве (Koziel G M, Beland G L, Bowman C, Carozzi N B, Crenshaw R, Crossland L, Dawson J, Desai N, Hill M, Kadwell S, Launis K, Maddox D, McPherson K, Heghji M, Merlin E, Rhodes R, Warren G, Wright M, Evola S (1993) Field performance of elite transgenic maize plants expressing an insecticidal protein derived from Bacillus thuringiensis. Biotechnology 11:194-200). В отличие от генов растений, гены Bt имеют высокое содержание A+T (66%), что является неоптимальным использованием кодонов для растений и потенциально приводит к неправильному сплайсингу или к преждевременной терминации транскрипции (De la Riva and Adang, 1996).
[0093] Perlak и др. (Perlak F J, Fuchs R L, Dean D A, McPherson S L, Fishhoff D A (1991) Modification of the coding sequences enhances plant expression of insect control protein genes, Proc. Natl. Acad. Sci. (USA) 88:3324-3328) модифицировали кодирующую последовательность генов cry без изменения последовательности кодируемых пептидов так, чтобы обеспечивалось оптимальное использование кодонов для растений и позволяло в два раза увеличить продуцирование токсинов в растениях по сравнению с нативным геном. Эта стратегия была успешно применена на многих растениях, таких как хлопчатник, рис и кукуруза, трансформированных модифицированными генами cry1, и картофель, трансформированный модифицированным геном cry3A. Bt-кукуруза и Bt-хлопчатник выращиваются в больших масштабах по всему миру.
[0094] Таким образом, естественное смещение кодонов среди организмов приводит к субоптимальной экспрессии генов в гетерологичном организме. В настоящем изобретении, нативный ген cry2Ai Bacillus thuringiensis был реконструирован in silico для оптимальной экспрессии рекомбинантного белка в растениях, включая двудольные и однодольные растения. При конструировании методом многомерного анализа, редкие и очень редкие кодоны были заменены наиболее предпочтительными кодонами двудольных/однодольных растений. Реконструированный синтетический ген, созданный методом генной инженерии, был вручную оценен на использование редких кодонов, стабильность вторичной структуры мРНК, и любое начало вторичной транскрипции гена во избежание экспрессии усеченных белков. Структура и стабильность оптимизированной мРНК была проверена и подтверждена путем оптимизации мРНК.
[0095] В своем конкретном аспекте, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеиновой кислоте, кодирующей инсектицидные белки Cry2Ai, к инсектицидным композициям, к полинуклеотидныя конструкциям, к рекомбинантной нуклеотидной последовательности, к рекомбинантному вектору, к трансформированным микроорганизмам и к растениям, содержащим молекулу нуклеиновой кислоты согласно изобретению. Эти композиции находят применение в способах борьбы с насекомыми-вредителями, а особенно с насекомыми-вредителями сельскохозяйственных культур.
[0096] Раскрытая здесь оптимизированная по кодонам синтетическая нуклеотидная последовательность может быть присоединена к различным промоторам, включая конститутивные, индуцибельные, регулируемые по времени, регулируемые в процессе развития, тканевые и тканеспецифичные промоторы для получения рекомбинантных молекул ДНК. Раскрытые здесь оптимизированные по кодонам синтетические нуклеотидные последовательности cry2Ai (кодирующие последовательности) обеспечивают существенно более высокие уровни экспрессии в трансформированном растении по сравнению с нативным геном cry2Ai. Соответственно, могут быть получены растения, устойчивые к чешуекрылым вредителям, таким как Helicoverpa armigera - хлопковая совка и кукурузная уховертнка, Cnaphalocrocis medinalis - рисовый листоверт и Scirpophaga incertulas - рисовый желтый стеблевой пилильщик и Pectinophora gossypiella.
[0097] В одном из своих вариантов, настоящее изобретение относится к оптимизированным по кодонам синтетическим нуклеотидным последовательностям cry2Ai с кодонами, предпочтительными для растений. В другом своем варианте, настоящее изобретение относится к экспрессии оптимизированной(ых) по кодонам синтетической(их) нуклеотидной(ых) последовательности(ей) cry2Ai в растениях, таких как хлопчатник, баклажан, рис, томат и кукуруза. В другом своем варианте, настоящее изобретение относится к кластерам для экспрессии ДНК, и к векторам для трансформации растений, содержащим синтетическую(ие) нуклеотидную(ые) последовательность(и) cry2Ai согласно изобретению. В другом своем варианте, настоящее изобретение относится к композициям, содержащим раскрытую(ые) здесь оптимизированную(ые) по кодонам синтетическую(ие) нуклеотидную(ые) последовательность(и) cry2Ai, или инсектицидный полипептид, кодируемый описанной здесь оптимизированной по кодонам синтетической нуклеотидной последовательностью cry2Ai. Раскрытая здесь композиция может представлять собой пестицидные и/или инсектицидные композиции, содержащие пестицидные и/или инсектицидные белки/полипептиды согласно изобретению. В другом своем варианте, настоящее изобретение относится к трансгенным растениям, содержащим оптимизированную(ые) по кодонам синтетическую(ие) нуклеотидную(ые) последовательность(и) cry2Ai согласно изобретению, экспрессирующую(ие) белок токсина Cry2Ai.
[0098] В частности, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, представленной в SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6, где указанный нуклеотид кодирует инсектицидный белок Cry2Ai, имеющий аминокислотную последовательность, представленную в SEQ ID NO:1.
[0099] В некоторых своих вариантах, настоящее изобретение относится к растениям и микроорганизмам, трансформированным с использованием раскрытой(ых) здесь оптимизированной(ых) по кодонам синтетической(их) нуклеотидной(ых) последовательности(ей) cry2Ai и к способам, включающим применение такой(их) нуклеотидной(ых) последовательности(ей), пестицидных композиций, трансформированных организмов и их продуктов для борьбы с насекомыми-вредителями.
[00100] Полинуклеотидные последовательности вариантов осуществления изобретения могут быть использованы для трансформации любого организма, например, растений и микроорганизмов, таких как Bacillus thuringiensis, для получения кодируемых инсектицидных и/или пестицидных белков. Были предложены способы, которые включают использование таких трансформированных организмов для уничтожения насекомых-вредителей растений или борьбы с ними. Нуклеиновые кислоты и нуклеотидные последовательности согласно вариантам осуществления изобретения могут быть также использованы для трансформации органелл, таких как хлоропласты. Способ трансформации нужного организма хорошо известен специалистам в данной области, что позволяет специалисту осуществлять трансформацию с использованием нуклеотидных последовательностей, раскрытых в настоящем изобретении.
[00101] Нуклеотидные последовательности вариантов осуществления изобретения включают последовательности нуклеиновых кислот или нуклеотидов, которые были оптимизированы для экспрессии в клетках конкретного организма, например, последовательности нуклеиновых кислот, которые были подвергнуты возвратной трансляции (то есть, обратной трансляции) с использованием предпочтительных для растений кодонов на основе аминокислотной последовательности полипептида, обладающего пестицидной активностью.
[00102] Настоящее изобретение относится к оптимизированным по кодонам синтетическим последовательностям нуклеиновых кислот/нуклеотидов, кодирующих инсектицидные белки Cry2Ai. Синтетические кодирующие последовательности являются особенно адаптированными для их использования при экспрессии белков в растениях с двумя семядолями (в двудольных растениях) и в растениях с одной семядолей (в однодольных растениях), таких как рис, томаты, баклажаны, кукуруза, хлопчатник и бобовые.
[00103] Настоящее изобретение относится к синтетическим нуклеотидным последовательностям, кодирующим белок Cry2Ai, которые были, в частности, адаптированы для эффективной экспрессии в растениях. В описанных синтетических нуклеотидных последовательностях с оптимизированными кодонами используются кодоны, оптимизированные для растений, приблизительно с той же частотой, с которой они используются, в среднем, в генах, встречающихся в природе у растений этих видов. Настоящее изобретение дополнительно включает оптимизированную по кодонам синтетическую нуклеотидную последовательность для сообщения растениям устойчивости к насекомым.
[00104] Для трансформации растений, в настоящем изобретении используются селективные маркерные гены. В настоящей заявке раскрываются конструкции ДНК и трансгенные растения, содержащие синтетические последовательности, а также способы и композиции, применяемые для выращивания агнономически ценных растений.
[00105] Каждый белок, кодируемый оптимизированными по кодонам синтетическими нуклеотидными последовательностями, обладает биологической активностью, подавляющей насекомых видов Чешуекрылых. Двудольные и/или однодольные растения могут быть трансформированы каждой из раскрытых здесь нуклеотидных последовательностей, отдельно или в комбинациях с другими нуклеотидными последовательностями, кодирующими инсектицидные агенты, такие как белки, кристаллические белки, токсины и/или специфичные для вредителей двухцепочечные РНК, необходимые для подавления генов у одного или более вредителей-мишеней и т.п., для разработки средств борьбы с резистентностью насекомых в полевых условиях, что было ранее недостижимым путем простого использования известных инсектицидных белков против Чешуекрылых, полученных из штаммов Bacillus thuringiensis.
[00106] Оптимизированные по кодонам синтетические нуклеотидные последовательности согласно изобретению могут быть также использованы в растениях в комбинации с другими типами нуклеотидных последовательностей, кодирующих инсектицидные токсины, для получения растений, трансформированных так, чтобы они содержали по меньшей мере одно средство для борьбы с одним или несколькими распространенными вредителями растений, выбранными из групп, состоящих из чешуекрылых насекомых-вредителей, жесткокрылых насекомых-вредителей, колющих и сосущих насекомых-вредителей и т.п.
Регуляторные последовательности
[00107] Сигналы регуляции транскрипции и трансляции включают, но не ограничиваются ими, промоторы, сайты инициации транскрипции, операторы, активаторы, энхансеры, другие регуляторные элементы, сайты связывания с рибосомой, кодон инициации, сигналы терминации и т.п.
[00108] Конструкция полинуклеотид/ДНК будет включать в направлении транскрипции от 5'- до 3'-конца: область инициации транскрипции и трансляции (то есть, промотор), последовательность ДНК согласно вариантам осуществления изобретения и область терминации транскрипции и трансляции (то есть, область терминации), которые являются функциональными в организме-хозяине. Область инициации транскрипции (то есть, промотор) может быть нативной, аналогичной, чужеродной или гетерологичной области организма-хозяина и/или последовательности согласно изобретению. Кроме того, промотор может представлять собой природную последовательность или альтернативно, синтетическую последовательность. Используемый здесь термин «чужеродный» означает, что этот промотор не был обнаружен в нативном организме, в который его вводят. Если промотор является «чужиродным» или «гетерологичным» последовательности вариантов осуществления изобретения, то подразумевается, что этот промотор не является нативным или встречающимся в природе промотором для функционально связанной последовательности согласно вариантам осуществления изобретения.
[00109] Для практического осуществления вариантов изобретения может быть использован ряд промоторов. Промоторы могут быть выбраны в зависимости от желаемого результата. Оптимизированная по кодонам нуклеотидная последовательность согласно изобретению может быть объединена с конститутивными, тканеспецифическими, индуцибельными или другими промоторами для экспрессии в организме-хозяине. Подходящие конститутивные промоторы для использования в клетке растения-хозяина включают, например, коровый промотор 35S CaMV; актин риса; убихитин; промотор ALS и т.п.
[00110] В зависимости от желаемого результата может оказаться предпочтительным экспрессировать ген из индуцибельного промотора. Особый интерес для регуляции экспрессии нуклеотидных последовательностей согласно вариантам осуществления изобретения в растениях представляют промоторы, индуцируемые повреждением. Такие индуцируемые повреждением промоторы могут реагировать на повреждение, вызванное поеданием насекомыми, и включают ген ингибитора протеиназы картофеля (pin II); wun1 и wun2, win1 и win2; WIP1; ген MPI и т.п.
[00111] Кроме того, в способах и в нуклеотидных конструкциях вариантов осуществления изобретения могут быть использованы индуцируемые патогенами промоторы. Такие индуцируемые патогенами промоторы включают промоторы, происходищие от белков, ассоциированных с патогенезом (PR-белков), которые индуцируются после инфицирования патогеном; например, белков PR, белков SAR, β-1,3-глюканазы, хитиназы и т.п.
[00112] Химически регулируемые промоторы могут быть использованы для модуляции экспрессии гена в растении посредством применения экзогенного химического регулятора. В зависимости от цели применения, промотор может быть химически индуцируемым промотором, где применение химического вещества индуцирует экспрессию гена, или химически репрессируемым промотором, где применение химического репрессора подавляет экспрессию гена. Химически индуцируемые промоторы известны специалистам в данной области и включают, но не ограничиваются ими, промотор In2-2 кукурузы, который активируется бензолсульфонамидными гербицидами; промотор GST кукурузы, который активируется гидрофобными электрофильными соединениями, используемыми в качестве предшественников-гербицидов; и промотор табака PR-1a, который активируется салициловой кислотой. Другие представляющие интерес химически регулируемые промоторы включают промоторы, чувствительные к стероиду.
[00113] Промотор, который «предпочтительно» экспрессируется в конкретной ткани, экспрессируется в этой ткани в большей степени, чем по меньшей мере в одной другой ткани растения. Некоторые предпочтительные для ткани промоторы экспрессируются почти исключительно в конкретной ткани. Промоторы, предпочтительные для ткани, могут быть использованы для повышения уровня экспрессии пестицидного белка в конкретной ткани растения. При необходимости, такие промоторы могут быть модифицированы для ослабления экспрессии.
[00114] Примеры некоторых тканеспецифических промоторов включают, но не ограничиваются ими, промоторы, предпочтительные для листьев, корне-специфические промоторы или промоторы, предпочтительные для корней; семяспецифические промоторы или промоторы, предпочтительные для семян; промоторы, специфичные для пыльцы, и промоторы, специфичные для сердцевины.
[00115] Предпочтительные для корней промоторы или корне-специфические промоторы известны специалистам и могут быть выбраны из промоторов, описанных в литературе, или выделены de novo из различных совместимых видов.
[00116] «Предпочтительные для семян» промоторы включают как «семяспецифические» промоторы (промоторы, активные во время развития семян, такие как промоторы запасных белков семян), так и промоторы «прорастания семян» (промоторы, активные во время прорастания семян). Гамма-зеин и Glob-1 являются промоторами, специфичными для эндосперма. Для двудольных растений, семяспецифические промоторы включают, но не ограничиваются ими, β-фазеолин, β-конглицинин, соевый лектин, круциферин и т.п. Для однодольных растений, семяспецифические промоторы включают, но не ограничиваются ими, зеин 15 кДа кукурузы, зеин 22 кДа кукурузы, зеин в 27 кДа кукурузы, g-зеин, зеин восковидной кукурузы, зеин, активный при сморщивании зерна 1, зеин, активный при сморщивании зерна 2, глобулин 1 и т.п.
[00117] Если желателен низкий уровень экспрессии, то могут быть использованы слабые промоторы. Обычно, используемый здесь термин «слабый промотор» относится к промотору, который регулирует экспрессию кодирующей последовательности на низком уровне. Такие слабые конститутивные промоторы включают, например, коровый промотор Rsyn7, коровый промотор 35S CaMV и т.п.
[00118] Области терминации выделяют из Ti-плазмиды A. tumefaciens, такие как области терминации октопинсинтазы (OCS) и нопалинсинтазы (NOS).
[00119] Кластеры для экспрессии ДНК могут дополнительно содержать 5'-лидерные последовательности. Такие лидерные последовательности могут усиливать трансляцию. Лидерные последовательности трансляции известны специалистам в данной области и включают: лидерные последовательности пикорнавируса, например, лидерную последовательность EMCV (5'-некодирующую область вируса энцефаломиокардита); лидерные последовательности потивирусов, например, лидерную последовательность TEV (вируса гравировки табака), лидерную последовательность MDMV (вируса карликовой мозаики кукурузы), нетранслируемую лидерную последовательность мРНК белка оболочки вируса мозаики люцерны (РНК 4 AMV); лидерную последовательность вируса мозаики табака (ВТМ); и лидерную последовательность вируса хлоротической крапчатости кукурузы (MCMV).
[00120] В одном из конкретных раскрытых и заявленных здесь вариантов осуществления изобретения, промотор, предпочтительный для ткани или тканеспецифический промотор функционально связан с синтетической последовательностью ДНК согласно изобретению, кодирующей инсектицидный белок, и трансгенное растение стабильно трансформируют по меньшей мере одной такой рекомбинантной молекулой. Полученное в результате растение будет резистентным к определенным насекомым, которые питаются теми частями растения, в которых экспрессируется ДНК.
Селективный маркерный ген
[00121] Обычно, экспрессионный кластер будет содержать селективный маркерный ген для отбора трансформированных клеток. Селективные маркерные гены используют для отбора трансформированных клеток или тканей. Маркерные гены включают гены, кодирующие резистентность к антибиотикам, такие как гены, кодирующие неомицинфосфотрансферазу II (nptII) и гигромицинфосфотрансферазу (hptII), а также гены, сообщающие резистентность к гербицидным соединениям, таким как глюфозинат аммония, бромоксинил, имидазолиноны и 2,4-дихлорфеноксиацетат (2,4-D). Дополнительные примеры подходящих селектируемых маркерных генов включают, но не ограничиваются ими, гены, кодирующие резистентность к хлорамфениколу, метотрексату, стрептомицину, спектиномицину, блеомицину, сульфонамиду, бромоксинилу, глифосату, фосфинотрицину.
Приведенный выше список селективных маркерных генов не является ограничивающим. В вариантах осуществления изобретения может быть использован любой селективный маркерный ген.
ДНК-конструкции и векторы
[00122] Оптимизированные по кодонам синтетические нуклеотидные последовательности согласно изобретению представлены в конструкциях ДНК для экспрессии в представляющем интерес организме. Конструкция включает 5'- и 3'-регуляторные последовательности, функционально связанные с последовательностью согласно изобретению.
[00123] Такая полинуклеотидная конструкция имеет множество рестрикционных сайтов для встраивания последовательностей ДНК, кодирующих последовательность белка токсина Cry2Ai и находящихся под транскрипционным контролем регуляторных областей. Полинуклеотидная конструкция может дополнительно содержать селективные маркерные гены. Конструкция может дополнительно содержать по меньшей мере один дополнительный ген, который будет котрансформирован в желаемый организм. Альтернативно, дополнительный(е) ген(ы) может (могут) присутствовать во множестве полинуклеотидных конструкций.
[00124] При получении конструкции ДНК/экспрессионного кластера, различные фрагменты ДНК могут быть модифицированы так, чтобы последовательности ДНК находились в правильной ориентации и, при необходимости, в соответствующей рамке считывания. Для этой цели, адаптеры или линкеры могут быть использованы для соединения фрагментов ДНК, либо могут быть проведены другие манипуляции для создания удобных рестрикционных сайтов, удаления лишней ДНК, удаления рестрикционных сайтов и т.п. Для этой цели могут быть проведены мутагенез in vitro, репарация праймеров, рестрикция, отжиг, повторные замены, например, транзиции и трансверсии.
[00125] Согласно настоящему изобретению, раскрытая здесь конструкция ДНК/экспрессионный кластер может быть встроена в рекомбинантный экспрессионный вектор. Термин «рекомбинантный экспрессионный вектор» означает бактериальную плазмиду, фаг, дрожжевую плазмиду, вирус клетки растения, вирус клетки млекопитающего или другой вектор. Вообще говоря, могут быть использованы любая плазмида или любой вектор при условии, что они могут реплицироваться и стабилизироваться в хозяине. Важной характеристикой экспрессионного вектора является то, что он имеет ориджин репликации, промотор, маркерный ген и элемент регуляции трансляции.
[00126] Для встраивания чужеродных генов в высшие растения используется большое количество клонирующих векторов, содержащих систему репликации E.coli и маркер, позволяющий проводить отбор трансформированных клеток. Векторы включают, например, pBR322, серию pUC, серию M13mp, pACYC184 и т.п. Соответственно, фрагмент ДНК, имеющий последовательность, кодирующую белок токсина Bt, может быть встроен в вектор в подходящем рестрикционном сайте. Полученную плазмиду используют для трансформации в E. coli. Клетки E. coli культивируют в подходящей питательной среде, а затем собирают и подвергают лизису. Затем плазмиду выделяют. В качестве методов анализа обычно проводят анализ последовательности, рестрикционный анализ, электрофорез и другие биохимические и молекулярно-биологические методы. После каждой манипуляции, используемая последовательность ДНК может быть расщеплена и присоединена к следующей последовательности ДНК. Каждая последовательность плазмиды может быть клонирована в той же самой или в других плазмидах. В зависимости от метода введения желаемых генов в растение могут потребоваться другие последовательности ДНК. Если, например, плазмида Ti или Ri используется для трансформации клетки растения, то, по меньшей мере правая граница, а часто правая и левая границы Т-ДНК плазмиды Ti или Ri должны быть соединены как фланкирующие области генов, которые необходимо вставить.
[00127] Экспрессионный вектор, содержащий оптимизированную по кодонам нуклеотидную последовательность согласно изобретению и подходящий сигнал регуляции транскрипции/трансляции, может быть сконструирован способом, хорошо известным специалисту в данной области. Примеры такого способа включают метод рекомбинации ДНК in vitro, метод синтеза ДНК и метод рекомбинации in vivo. Последовательность ДНК может быть эффективно связана с подходящим промотором в экспрессионном векторе для индуцирования синтеза мРНК. Кроме того, экспрессионный вектор может содержать в качестве сайта инициации трансляции сайт связывания с рибосомой и терминатор транскрипции.
[00128] Предпочтительным примером рекомбинантного вектора согласно изобретению является Ti-плазмидный вектор, который может переносить одну из своих частей, то есть, так называемую Т-область, в клетку растения, если этот вектор присутствует в подходящем хозяине, таком как Agrobacterium tumefaciens. Другие типы Ti-плазмидного вектора в настоящее время используют для переноса гибридного гена в протопласты, которые могут давать новое растение, путем соответствующего встраивания гибридного гена в клетку растения или гибридной ДНК в геном растения.
[00129] Экспрессионный вектор может содержать по меньшей мере один селективный маркерный ген. Селективный маркерный ген представляет собой нуклеотидную последовательность, обладающую свойством, основанным на том, что она может быть выбрана обычным химическим методом. Каждый ген, который может быть использован для дифференциации трансформированных клеток от нетрансформированных, может быть селективным маркером. Пример включает ген резистентности к гербицидам, таким как глифосат и фосфинотрицин, и ген резистентности к антибиотикам, таким как, но не ограничивающимся ими, канамицин, гигромицин, G418, блеомицин и хлорамфеникол.
[00130] Для рекомбинантного вектора согласно изобретению, промотором может быть любой из промоторов, которыми являются, но не ограничиваются ими, промотор CaMV 35S, актина или убихитина. Поскольку трансформант может быть выбран с помощью различных механизмов на различных стадиях, то конститутивный промотор может быть предпочтительным для осуществления настоящего изобретения. Таким образом, в данном случае, возможность выбора конститутивного промотора не ограничена.
[00131] Для рекомбинантного вектора согласно изобретению может быть использован любой обычный терминатор. Примерами таких терминаторов являются, но не ограничиваются ими, терминатор нопалинсинтазы (NOS), терминатор α-амилазы RAmy1 A риса, терминатор фазеолина и терминатор гена оптопина Agrobacterium tumefaciens и т.п. Хорошо известно, что при использовании терминатора, такая область может повысить надежность и эффективность транскрипции в клетках растения. Следовательно, использование терминатора может быть в высокой степени предпочтительным исходя из контекста настоящего изобретения.
[00132] Специалисту в данной области известно, что описанные здесь ДНК-конструкция и вектор могут быть использованы для получения трансгенных растений, резистентных к насекомым, и/или для получения инсектицидной композиции, где такая композиция может содержать клетки Bacillus thuringiensis, включающие указанную нуклеотидную последовательность, или любой другой микроорганизм, способный экспрессировать раскрытую здесь нуклеотидную последовательность, для продуцирования инсектицидного белка Cry2Ai.
Рекомбинантная клетка
[00133] Варианты осуществления изобретения дополнительно охватывают микроорганизм, который трансформируют по меньшей мере одной оптимизированной по кодонам нуклеиновой кислотой согласно изобретению с использованием экспрессионного кластера, содержащего нуклеиновую кислоту, или вектора, содержащего экспрессионный кластер. В некоторых вариантах осуществления изобретения, микроорганизм представляет собой микроорганизм, который размножается на растениях. Вариант осуществления изобретения относится к инкапсулированному пестицидному белку, который содержится в трансформированном микроорганизме, способном экспрессировать белок Cry2Ai согласно изобретению.
[00134] Еще один вариант осуществления изобретения относится к трансформированному организму, такому как организм, выбранный из группы, состоящей из клеток растений и насекомых, бактерий, дрожжей, бакуловирусов, простейших, нематод и водорослей. Трансформированный организм содержит оптимизированную по кодонам синтетическую молекулу ДНК согласно изобретению, экспрессионный кластер, содержащий указанную молекулу ДНК, или вектор, содержащий указанный экспрессионный кластер, которые могут быть стабильно включены в геном трансформированного организма.
[00135] Известно, что гены, кодирующие белок Cry2Ai, могут быть использованы для трансформации патогенных организмов насекомых. Такие организмы включают бакуловирусы, грибы, простейшие, бактерии и нематоды.
[00136] Оптимизированная(ые) по кодонам синтетическая(ие) нуклеотидная(ые) последовательность(и), кодирующая(ие) белок Cry2Ai согласно изобретению, может (могут) быть введена(ы) с помощью подходящего вектора хозяину-микробу, и указанного хозяина вносят в окружающую среду, или на растения или на животных. Термин «введенный», если он относится к встраиванию нуклеиновой кислоты в клетку, означает «трансфекцию», или «трансформацию», или «трансдукцию» и включает введение нуклеиновой кислоты в эукариотическую или прокариотическую клетку, где нуклеиновая кислота может быть введена в геном клетки (например, в хромосому, в плазмиду, в пластиду или в митохондриальную ДНК), превращена в автономный репликон или временно экспрессирована (например, трансфецированная мРНК).
[00137] Для стабильного поддержания и экспрессии ДНК имеется ряд способов введения чужеродной ДНК, экспрессирующей пестицидный белок, микроорганизму-хозяину в условиях, которые обеспечивают такое поддержание и экспрессию ДНК. Так, например, экспрессионные кластеры могут быть сконструированы так, чтобы они включали представляющие интерес нуклеотидные конструкции, функционально связанные с сигналами регуляции транскрипции и трансляции для экспрессии нуклеотидных конструкций, и нуклеотидную последовательность, гомологичную последовательности в организме-хозяине, в результате чего будет происходить интеграция, и/или интеграция системы репликации, которая будет функционировать у хозяина, посредством чего будет происходить интеграция или стабильное сохранение.
Способы трансформации растений и получение трансгенных растений
[00138] Оптимизированная по кодонам синтетическая нуклеотидная последовательность (последовательность ДНК) согласно изобретению, кодирующая белок токсина Cry2Ai Bt, может быть встроена в клетки растений с применением ряда методов, хорошо известных специалистам в данной области. После встраивания ДНК, она интегрируется в геном растения и становится относительно стабильной. Вектор для трансформации обычно содержит селективный маркер, который сообщает трансформированным клеткам растения резистентность к биоциду или антибиотику, такому как канамицин, биалафос, G418, блеомицин или гигромицин. Соответственно, индивидуально используемый маркер позволяет проводить отбор только трансформированных клеток, а не клеток, не содержащих встроенную ДНК.
[00139] Существует большое число методов встраивания ДНК в клетку растения-хозяина. Эти методы включают трансформацию Т-ДНК с использованием Agrobacterium tumefaciens или Agrobacterium rhizogenes в качестве агента для трансформации, слияние, инъекцию, биобаллистические методы (бомбардировку микрочастицами) или электропорацию, а также другие возможные методы. Если для трансформации используют агробактерии, то встраиваемую ДНК необходимо клонировать в специальные плазмиды, а именно, либо в промежуточный вектор, либо в бинарный вектор. Промежуточные векторы могут быть интегрированы в плазмиду Ti или Ri путем гомологичной рекомбинации благодаря последовательностям, которые гомологичны последовательностям в Т-ДНК. Плазмида Ti или Ri также содержит область vir, необходимую для переноса Т-ДНК.
[00140] Промежуточные векторы не могут реплицироваться в агробактериях. Промежуточный вектор может быть перенесен в Agrobacterium tumefaciens с помощью вспомогательной плазмиды (посредством конъюгигования). Бинарные векторы могут реплицироваться как в E. coli, так и в Agrobacteria. Они содержат селективный маркерный ген и линкер или полилинкер, которые фланкированы правой и левой пограничными областями Т-ДНК. Они могут быть преобразованы непосредственно в Agrobacteria. Agrobacteria, используемая в качестве клетки-хозяина, должна содержать плазмиду, несущую область вирулентности (vir). Область vir необходима для переноса Т-ДНК в клетку растения. При этом, может также присутствовать и дополнительная Т-ДНК. Трансформированную таким образом бактерию используют для трансформации клеток растений. Растительные эксплантаты можно преимущественно культивировать с Agrobacterium tumefaciens или Agrobacterium rhizogenes для переноса ДНК в клетку растения. Затем из инфицированного растительного материала (например, кусочков листьев, сегментов стебля, корней, а также протопластов или культивируемых в суспензии клеток) можно регенерировать целые растения в подходящей среде, которая может содержать антибиотики или биоциды для отбора. Полученные таким образом растения могут быть затем протестированы на наличие встроенной ДНК. При этом, никаких особых требований к плазмидам в случае инъекции и электропорации не предъявляется. Можно использовать обычные плазмиды, такие как, например, производные pUC.
[00141] Трансформированные клетки могут быть культивированы в растениях обычными способами. Затем эти растения можно выращивать и опылять одним и тем же трансформированным штаммом или различными штаммами, и идентифицировать полученный гибрид, имеющий конститутивную или индуцибельную экспрессию желаемого фенотипического свойства. Можно культивировать два или более поколений, для гарантии того, что экспрессия желаемой фенотипического свойства будет стабильно сохраняться и наследоваться, а затем можно собрать семена для гарантии достижения экспрессии желаемого фенотипического свойства. Эти семена могут образовывать зародышевые клетки и передавать трансформированный(е) признак(и) потомству. Такие растения могут быть культивированы обычным способом и скрещены с растениями, которые имеют такие же трансформированные наследственные признаки или другие наследственные признаки. Полученные гибридные растения обладают соответствующими фенотипическими свойствами.
[00142] Способы трансформации растений согласно изобретению включают введение полинуклеотида(ов) согласно изобретению в растение и не зависят от конкретного метода введения полинуклеотида(ов) в растение. Способы введения полинуклеотида(ов) в растения известны специалистам в данной области, включая, но не ограничиваясь ими, методы стабильной трансформации, методы временной трансформации и методы, опосредованные вирусами.
[00143] В одном варианте осуществления изобретения, растения были трансформированы раскрытой(ыми) здесь оптимизированной(ыми) по кодонам синтетической(ими) нуклеотидной(ыми) последовательностью(ями). Некоторыми неограничивающими примерами трансформированных растений являются фертильные трансгенные растения риса и томата, содержащие оптимизированную(ые) по кодонам синтетическую(ие) нуклеотидную(ые) последовательность(и) согласно изобретению, кодирующую(ие) белок Cry2Ai. Способы трансформации риса и томата известны специалистам в данной области. Различные другие растения могут быть также трансформированы с использованием раскрытой(ых) здесь оптимизированной(ых) по кодонам синтетической(их) нуклеотидной(ых) последовательности(ей).
[00144] Термин «стабильная трансформация» означает, что нуклеотидная конструкция, введенная в растение, интегрируется в геном растения и способна наследоваться его потомством. Термин «временная трансформация» означает, что полинуклеотид вводится в растение и не интегрируется в геном растения, либо в растение вводится полипептид.
[00145] Протоколы трансформации, а также протоколы введения нуклеотидных последовательностей в растения могут варьироваться в зависимости от типа растения или клетки растения, то есть, от того, предназначены ли для трансформации однодольные или двудольные растения. Подходящие способы введения нуклеотидных последовательностей в клетки растения и последующего введения в геном растения включают микроинъекцию, электропорацию, трансформацию, опосредованную Agrobacterium, и биобаллистическое ускорение частиц.
[00146] В одном варианте осуществления изобретения, оптимизированная(ые) по кодонам синтетическая(ие) нуклеотидная(ые) последовательность(и) согласно изобретению, кодирующая(ие) токсин Cry2Ai, экспрессируется(ются) в высшем организме, например в растении, посредством оптимизированной по кодонам нуклеотидной последовательности согласно изобретению. В этом случае, трансгенные растения, экспрессирующие эффективное количество токсина, защищают себя от насекомых-вредителей. Если насекомое начинает питаться таким трансгенным растением, то оно также проглатывает выделенный токсин. Это удерживает насекомое от дальнейшего укуса ткани растения или даже может нанести вред насекомому или убить это насекомое. Нуклеотидную последовательность согласно изобретению встраивают в экспрессионный кластер, который затем стабильно интегрируется в геном растения.
[00147] Варианты настоящего изобретения также охватывают трансформированные или трансгенные растения, содержащие по меньшей мере одну нуклеотидную последовательность вариантов осуществления изобретения. В некоторых вариантах осуществления изобретения, растение стабильно трансформируют нуклеотидной конструкцией, содержащей по меньшей мере одну нуклеотидную последовательность вариантов осуществления изобретения, функционально связанную с промотором, который регулирует экспрессию в клетке растения.
[00148] Хотя варианты осуществления изобретения не зависят от конкретного биологического механизма повышения резистентности растения к вредителям, однако, экспрессия нуклеотидных последовательностей вариантов осуществления изобретения в растении может приводить к продуцированию пестицидных белков вариантов осуществления изобретения и к повышению резистентности растения к вредителям. Растения согласно вариантам осуществления изобретения находят свое применение в способах борьбы с насекомыми-вредителями в сельском хозяйстве. Некоторые варианты осуществления изобретения относятся к трансформированным сельскохозяйственным растениям, таким как, например, рис и томат, которые применяются в способах борьбы с насекомыми-вредителями растения, такими как, например, различные чешуекрылые насекомые, включая Cnaphalocrocis medinalis - рисовую листовертку и Scirpophaga incertulas - рисового желтого стеблевого пилильщика.
[00149] «Исследуемое растение или клетка растения» представляет собой растение, в котором генетическое изменение, такое как трансформация, было осуществлено в отношении представляющего интерес гена, или растение или клетка растения, происходящие от растения или клетки, измененных таким образом и содержащих такое изменение. Термин «контроль», или «контрольное растение», или «контрольная клетка растения» относится к контрольному объекту для оценки изменений фенотипа рассматриваемого растения или клетки растения. Контрольное растение или клетка растения могут включать, например: (а) растение или клетку дикого типа, то есть, того же генотипа, что и исходный материал для генетического изменения, которое приводит к получению нужного растения или клетки; (b) растение или клетку растения, которое имеет такой же генотип, как и исходный материал, но которое было трансформировано «нулевой» конструкцией (то есть, конструкцией, которая не оказывает какого-либо известного действия на представляющий интерес признак, такой как конструкция, содержащая маркерный ген); (c) растение или клетку растения, которые представляют собой нетрансформированный сегрегант среди потомства рассматриваемого растения или клетки растения; (d) растение или клетку растения, который были генетически идентичны рассматриваемому растению или клетке растения, но не подвергались воздействию условий или раздражителей, которые могли бы индуцировать экспрессию представляющего интерес гена; или (e) рассматриваемое растение или клетку самого растения в условиях, в которых представляющий интерес ген не экспрессируется.
[00150] Перенос (или интрогрессия) нуклеотидов cry2Ai, описанных в настоящей заявке, и собщающих признак инбредным растениям, таким как хлопчатник, рис, баклажаны (бринджал), томаты и бобовые, может быть достигнут путем рекуррентного селекционного скрещивания, например, путем возвратного скрещивания. В этом случае, желаемого рекуррентного родителя сначала скрещивают с инбредным донором (нерекуррентным родителем), который несет раскрытую здесь нуклеотидную последовательность, которая определяет признаки для cry2Ai. Потомство от этого скрещивания затем подвергают возвратному скрещиванию с рекуррентным родителем с последующим отбором полученного потомства по желаемому(ым) признаку(ам), который(е) должен (должны) быть передан(ы) от нерекуррентного родителя. После трех, предпочтительно четырех, более предпочтительно пяти или более поколений возвратных скрещиваний с рекуррентным родителем с отбором по желаемому(ым) признаку(ам), потомство будет гетерозиготным по локусам, регулирующим переносимый(е) признак(и), но будет похоже на рекуррентный родитель для большинства или почти всех других генов.
[00151] Варианты осуществления изобретения также относятся к материалу для размножения трансформированного растения согласно вариантам осуществления изобретения, включая, но не ограничиваясь ими, семена, клубни, клубнелуковицы, луковицы, листья и черенки корней и побегов.
[00152] Класс растений, которые могут быть использованы в способах вариантов осуществления изобретения, обычно является таким же широким, как и класс высших растений, поддающихся методам трансформации, включая, но не ограничиваясь ими, однодольные и двудольные растения. Примеры представляющих интерес растений включают, но не ограничиваются ими, зерна, злаки, овощные культуры, масличные культуры, плодовые культуры, декоративные растения, дерновые травы и т.п. Так, например, ими являются рис (Oryza sativa, Oryza spp.), кукуруза (Zea mays), рожь (Secale cereale), сорго (Sorghum bicolor, Sorghum vulgare), просо (например, просо жемчужное (Pennisetum glaucum), просо метельчатое (Panicum miliaceum), просо лисохвостное (Setaria italica), пальцевидное просо (Eleusine coracana)), пшеница (Triticum aestivum, Triticum sp.), овес (Avena sativa), ячмень (Hordeum vulgare L), сахарный тростник (Saccharum spp.), хлопчатник (Gossypium hirsutum, Gossypium barbadense, Gossypium зр.), томаты (Lycopersicon Esculentum), бринджал/баклажан (Solanum melongena), картофель (Solanum tuberosum), сахарная свекла (Beta vulgaris), сладкий картофель (Ipomoea batatus), маниокa (Manihot esculenta), салат-латук (Lactuca sativa), капуста (Brassica oleracea, сорт capitata), цветная капуста (Brassica oleracea, сорт botrytis), брокколи (Brassica oleracea, сорт indica), Brassica sp. (например, B. napus, B. rapa, B. juncea), а в частности, виды Brassica, которые используются в качестве источников масл из семян, соя (Glycine max), подсолнечник (Helianthus annuus), сафлор (Carthamus tinctorius), арахис (Arachis hypogaea), голубиный горох (Cajanus cajan), нут (Cicer arietinum), стручковая фасоль (Phaseolus vulgaris), фасоль Лима (Phaseolus limensis), горох (Pisum sativum), горох посевной (Lathyrus spp.), огурец (Cucumis sativus), канталупская дыня (Cucumis cantalupensis) и мускусная дыня (Cucumis melo), люцерна (Medicago sativa), табак (Nicotiana tabacum) и резушка Таля (Arabidopsis thaliana).
[00153] Представляющие интерес растения включают зерновые культуры, дающие представляющие интерес семена, масличные растения и растения семейства бобовых. Представляющие интерес семена включают семена зерновых, таких как кукуруза, пшеница, ячмень, рис, сорго, рожь, просо и т.п. Масличные растения включают хлопчатник, сою, сафлор, подсолнечник, капусту, кукурузу, люцерну, пальму, кокос, лен, клещевину, оливу и т.п. Бобовые растения включают фасоль и горох. К бобам относятся гуаровое дерево, рожковое дерево, пажитник, соя, садовые бобы, вигна, маш, фасоль Лима, бобы фава, чечевица, нут и т.п.
[00154] В некоторых вариантах осуществления изобретения, по меньшей мере одна оптимизированная по кодонам синтетическая нуклеотидная последовательность согласно изобретению может быть объединена с любой комбинацией представляющих интерес полинуклеотидных последовательностей для создания растений с желаемым фенотипом. Так, например, оптимизированная по кодонам синтетическая нуклеотидная последовательность может быть объединена с любым другим полинуклеотидом, кодирующим полипептид, обладающий пестицидной и/или инсектицидной активностью, такой как другие токсичные белки Bt и т.п. Полученные комбинации могут также включать множество копий любого представляющего интерес полинуклеотида. Нуклеотидные последовательности согласно вариантам осуществления изобретения могут быть также объединены с любым другим геном или комбинацией генов для получения растений с различными комбинациями желаемых признаков, включая, но не ограничиваясь ими, признаки, желательные для приготовления корма для животных, такие как гены с высоким содержанием масла; сбалансированный аминокислотный состав; резистентность к абиотическому стрессу и т.п.
[00155] Нуклеотидные последовательности согласно изобретению также могут быть объединены с признаками, желательными для генов резистентности к болезням или гербицидам, генов авирулентности и генов устойчивости к болезням, для генов ацетолактатсинтазы (ALS), генов ингибиторов глутаминсинтазы, таких как фосфинотрицин или basta (например, ген bar), генов резистентности к глифосату; с признаками, желательными для процессинга или продуктов обработки, таких как продукты с высоким содержанием масла, модифицированные масла, модифицированные крахмалы (например, ADPG-пирофосфорилазы (AGPазы), крахмал-синтазы (SS), крахмал-ветвящие ферменты (SBE) и крахмал-деветвящие ферменты (SDBE)). Полинуклеотиды согласно вариантам осуществления могут быть также объединены с полинуклеотидами, обеспечивающими агрономические признаки, такие как мужская стерильность, прочность стебля, время цветения, или признаки, сообщаемые методами трансформации, такие как регуляция клеточного цикла или нацеливание на гены.
[00156] Эти совмещенные комбинации могут быть созданы любым способом, включая, но не ограничиваясь ими, скрещивание растений с применением любой традиционной генетической трансформации или любого другого метода, известного специалистам в данной области. Если признаки объединяют путем генетической трансформации растений, то представляющие интерес полинуклеотидные последовательности могут быть комбинированы в любое время и в любом порядке. Так, например, трансгенное растение, имеющее один или более желаемых признаков, может быть использовано в качестве мишени для сообщения ему дополнительных признаков путем последующей трансформации. Признаки могут быть сообщены одновременно в соответствии с протоколом котрансформации представляющими интерес полинуклеотидами, обеспечиваемыми любой комбинацией кластеров для трансформации. Так, например, если будут введены две последовательности, то эти две последовательности могут содержаться в отдельных кластерах для трансформации (в транс-ориентации) или в одном кластере для трансформации (в цис-ориентации). Экспрессия последовательностей может запускаться одним и тем же промотором или различными промоторами. В некоторых случаях, может оказаться желательным введение кластера для трансформации, который будет подавлять экспрессию представляющего интерес полинуклеотида. Этот кластер может быть объединен с любой комбинацией других кластеров для ингибирования или кластеров для сверхэкспрессии в целях создания растения с желаемой комбинацией признаков. Кроме того, известно, что полинуклеотидные последовательности могут быть объединены в желаемом положении генома с использованием системы сайт-специфической рекомбинации.
Анализ трансгенных растений
Полимеразная цепная реакция (ПЦР)
[00157] Настоящее изобретение относится к способу ПЦР-амплификации фрагмента раскрытой здесь оптимизированной по кодонам нуклеотидной последовательности, представленной в SEQ ID NO: 2, и кодирующей белок Cry2Ai с аминокислотной последовательностью, представленной в SEQ ID NO: 1, где указанный способ включает амплификацию ДНК с помощью ПЦР в присутствии праймера, представленного в SEQ ID NO: 7-8. Аналогичным образом, фрагмент раскрытой здесь оптимизированной по кодонам нуклеотидной последовательности, представленной в SEQ ID NO: 3-6, может быть амплифицирован с использованием праймеров, специфичных для указанной нуклеотидной последовательности. Специалист в данной области может разработать набор праймеров для амплификации указанных нуклеотидов. Протоколы и условия для ПЦР-амплификации фрагмента ДНК из матричной ДНК представлены в настоящей заявке или описаны в литературе и известны специалистам.
[00158] Олигонуклеотидные праймеры могут быть сконструированы для использования в ПЦР-реакциях в целях амплификации соответствующих последовательностей ДНК из оптимизированных по кодонам последовательностей ДНК согласно изобретению. Способы конструирования ПЦР-праймеров и способы ПЦР-клонирования, в основном, известны специалистам в данной области и описаны в руководстве Sambrook et al. (1989) Molecular Cloning: A Laboratory Manual (2nd ed., Cold Spring Harbor Laboratory Press, Plainview, NY), далее называемом просто руководством «Sambrook». Известные методы ПЦР включают, но не ограничиваются ими, методы с использованием парных праймеров, гнездовых праймеров, отдельных специфических праймеров, вырожденных праймеров, ген-специфических праймеров, вектор-специфических праймеров, праймеров с частичным ошибочным спариванием и т.п.
[00159] В одном своем варианте, настоящее изобретение относится к набору праймеров, подходящих для ПЦР-амплификации фрагмента оптимизированной по кодонам синтетической нуклеотидной последовательности согласно изобретению, которая кодирует пестицидный полипептид, и к способам использования набора праймеров в ПЦР-амплификации ДНК. Наборы праймеров содержат прямые и обратные праймеры, которые были сконструированы для отжига с нуклеотидными последовательностями согласно изобретению.
[00160] Наборы праймеров для амплификации нуклеотидной последовательности, представленной в SEQ ID NO: 2, согласно изобретению, включают прямые и обратные праймеры, представленные в SEQ ID NO: 7 и SEQ ID NO: 8.
[00161] Саузерн-гибридизация
[00162] В методах гибридизации, вся или часть известной нуклеотидной последовательности используется в качестве зонда, который селективно гибридизуется с другими соответствующими нуклеотидными последовательностями, присутствующими в популяции клонированных фрагментов геномной ДНК или в выбранном организме. Зонды для гибридизации зонды могут представлять собой ПЦР-амплифицированные ДНК-фрагменты оптимизированной(ых) по кодонам последовательности(ей) ДНК согласно изобретению или линеаризованную плазмиду, содержащую нуклеотидную(ые) последовательность(и), или другие олигонуклеотиды, способные гибридизоваться с соответствующими последовательностями раскрытого здесь синтетического нуклеотида, и могут быть помечены детектируемой группой, такой как 32P, или любым другим детектируемым маркером. Так, например, зонды для гибридизации могут быть получены путем мечения синтетических олигонуклеотидов, полученных на основе последовательностей вариантов осуществления изобретения. Способы получения зондов для гибридизации по существу известны специалистам в данной области и описаны в руководстве Sambrook.
[00163] Так, например, вся описанная здесь последовательность или одна или несколько ее частей могут быть использованы в качестве зонда, способного специфически гибридизоваться с соответствующими последовательностями. Для достижения специфической гибридизации в различных условиях, такие зонды включают последовательности, которые являются уникальными для последовательностей вариантов осуществления изобретения, и обычно имеют длину по меньшей мере приблизительно 10 или 20 нуклеотидов. Такие зонды могут быть использованы для амплификации соответствующих нуклеотидных последовательностей cry2Ai с помощью ПЦР.
[00164] Гибридизация таких последовательностей может быть проведена в жестких условиях. Используемый здесь термин «жесткие условия» или «жесткие условия гибридизации» относится к условиям, при которых зонд будет гибридизоваться со своей последовательностью-мишенью в значительно большей степени, чем с другими последовательностями (например, по меньшей мере в 2 раза, в 5 раз или в 10 раз выше фона). Жесткие условия зависят от последовательности и могут быть различными при различных обстоятельствах. Путем регуляции жесткости условий гибридизации и/или промывки можно идентифицировать последовательности-мишени, которые на 100% комплементарны зонду (гомологичное зондирование). Альтернативно, условия жесткости могут быть скорректированы так, чтобы допускались некоторые несоответствия в последовательностях для обнаружения более низких степеней сходства (гетерологичное зондирование).
[00165] Обычно, жесткими условиями являются условия, при которых концентрация соли составляет менее, чем приблизительно 1,5 М иона Na, обычно приблизительно от 0,01 до 1,0 М иона Na (или других солей) при рН от 7,0 до 8,3, а температура составляет по меньшей мере приблизительно 30°C для коротких зондов (например, от 10 до 50 нуклеотидов) и по меньшей мере приблизительно 60°C для длинных зондов (например, более 50 нуклеотидов). Жесткие условия могут быть также достигнуты путем добавления дестабилизирующих агентов, таких как формамид. Примеры условий низкой жесткости включают гибридизацию с буферным раствором, содержащим от 30% до 35% формамида, 1M NaCl, 1% ДСН (додецилсульфата натрия) при 37°C и промывку в 1-2× SSC (20× SSC=3,0 M NaCl/0,3 М тринатрийцитрата) при температуре от 50°C до 55°C. Примеры условий умеренной жесткости включают гибридизацию в 40-45% формамиде, 1,0 M NaCl, 1% ДСН при 37°C и промывку в 0,5-1× SSC при 55-60°C. Примеры условий высокой жесткости включают гибридизацию в 50% формамиде, 1 M NaCl, 1% ДСН при 37°C и конечную промывку в 0,1× SSC при 60-65°C в течение по меньшей мере приблизительно 20 минут. Промывочные буферы могут содержать, но необязательно, от приблизительно 0,1% до приблизительно 1% ДСН. Продолжительность гибридизации обычно составляет менее, чем приблизительно 24 часа, а обычно от приблизительно 4 до приблизительно 12 часов.
[00166] Специфичность обычно зависит от промывок после гибридизации, причем, основными факторами являются ионная сила и температура конечного промывочного раствора. Для гибридов ДНК-ДНК, Tm (температура плавления) может быть аппроксимирована по уравнению Meinkoth and Wahl (1984) Anal. Biochem. 138: 267-284: Tm=81,5°C+16,6 (log M) + 0,41 (%GC) - 0,61 (% формамида) -500/л; где M означает молярность одновалентных катионов, % GC означает процентное содержание гуанозиновых и цитозиновых нуклеотидов в ДНК, «% формамида» означает процентное содержание формамида в растворе для гибридизации, а L означает длину гибрида в парах оснований. Tm означает температуру (при определенной ионной силе и pH), при которой 50% комплементарной последовательности-мишени гибридизуются с идеально подобранным зондом. Промывки обычно проводят по меньшей мере до тех пор, пока не будет достигнуто равновесие и не будет достигнут низкий фоновый уровень гибридизации, например, в течение 2 часов, 1 часа или 30 минут. Tm снижается приблизительно на 1°C на каждый 1% ошибочного спаривания; и таким образом, Tm в условиях гибридизации и/или промывки может быть скорректирована для гибридизации с последовательностями желаемой идентичности. Так, например, если нужно найти последовательности с 90% идентичностью, то Tm можно снизить до 10°C. Обычно выбирают жесткие условия, при которых Т должна быть приблизительно на 5°C ниже, чем Tm для конкретной последовательности и ее комплемента при определенной ионной силе и при определенном pH. Однако, в очень жестких условиях, гибридизация и/или промывка могут быть проведены при температуре на 1, 2, 3 или 4°C ниже, чем Tm; в условиях умеренной жесткости, гибридизация и/или промывка могут быть проведены при температуре на 6°C, 7°C, 8°C, 9°C или 10°C ниже, чем Tm; а в условиях низкой жесткости, гибридизация и/или промывка могут быть проведены при температуре на 11°C, 12°C, 13°C, 14°C, 15°C или 20°C ниже, чем Tm.
[00167] Используя это уравнение, композиции для гибридизации и промывки, а также желаемую Tm, специалисты в данной области поймут, что по существу здесь описаны различные варианты жесткости растворов для гибридизации и/или промывки. Если желаемая степень ошибочного спаривания требует Tm менее 45°C (водного раствора) или 32°C (раствора формамида), то концентрацию SSC можно увеличить так, чтобы можно было использовать более высокую температуру. Подробное руководство по гибридизации нуклеиновых кислот можно найти в публикациях Tijssen (1993) Laboratory Techniques in Biochemistry and Molecular Biology - Hybridization with Nucleic Acid Probes, Part I, Chapter 2 (Elsevier, New York); и Ausubel et al., eds. (1995) Current Protocol in Molecular Biology, Chapter 2 (Greene Publishing and Wiley-Interscience, New York). См. также Sambrook et al.
[00168] Настоящее изобретение охватывает нуклеотидную последовательность, комплементарную нуклеотидной последовательности, представленной в SEQ ID NO: 2, или нуклеотидную последовательность, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положения нуклеотидов от 262 до 402 и/или от 1471 до 1631 или последовательности, комплементарной этой последовательности. Специалистам в данной области известен способ получения зонда на основе раскрытых здесь нуклеотидных последовательностей для гибридизации нуклеиновых кислот.
Анализы на экспрессию белков
[00169] Для количественного определения уровней экспрессии представляющего интерес белка могут быть проведены различные анализы. Уровень экспрессии представляющего интерес белка может быть оценен непосредственно, например, путем анализа уровня кодируемого белка в растении. Методы проведения таких анализов хорошо известны специалистам в данной области. Так, например, для оценки уровней транскриптов могут быть проведены Нозерн-блот-анализ или количественная ПЦР с обратной транскриптазой (кол.ОТ-ПЦР), а для оценки уровней белка могут быть проведены Вестерн-блот-анализ, ELISA (твердофазный иммуноферментный анализ) или анализы с использованием ферментов.
[00170] В настоящем изобретении, уровень экспрессии белка Cry2Ai в трансгенных растениях, содержащих раскрытую здесь оптимизированную по кодонам нуклеотидную последовательность, определяли с помощью ELISA, и неожиданно было обнаружено, что раскрытые здесь оптимизированные по кодонам синтетические последовательности ДНК демонстрируют значительное повышение уровня кспрессии белка Cry2Ai в трансгенных растениях. Достигнутый повышенный уровень экспрессии белка Cry2Ai в трансгенных растениях может быть оптимальным для эффективного обеспечения наивысшего уровня защиты от насекомых-мишеней. Таким образом, раскрытые здесь оптимизированные по кодонам синтетические последовательности ДНК могут быть использованы для эффективной борьбы с насекомыми в растениях для повышения их устойчивости к насекомым-вредителям, и тем самым для повышения урожайности сельскохозяйственных культур.
Биоанализ
[00171] Специалисту в данной области известно множество различных методов биоанализа. Общие процедуры включают добавление экспериментального соединения или организма к источнику питания в закрытом контейнере. Пестицидная активность может быть оценена по таким параметрам, которыми являются, но не ограничиваются ими, изменения процента гибели, потеря массы, привлекательность, отталкивание и другими поведенческие и физические изменения после поедания и другого воздействия в течение соответствующего периода времени. Биоанализы, описанные в настоящей заявке, могут быть проведены с использованием любого кормящегося насекомого-вредителя на стадии личинок или имаго.
Инсектицидная композиция
[00172] Биологический пестицид является одной из наиболее перспективных альтернатив традиционным химическим пестицидам, и этот биологический пестицид наносит меньший вред окружающей среде и биоте или вообще не наносит никакого вреда. Bacillus thuringiensis (широко известная как Bt) представляет собой инсектицидную грамположительную спорообразующую бактерию, продуцирующую кристаллические белки, называемые дельта-эндотоксинами (δ-эндотоксином), во время стационарной фазы или фазы старения. Первоначально, бактерия Bt была обнаружена Шигетане Ишиватари в 1902 г. в организме больного тутового шелкопряда (Bombyx mori). Но формально, она была охарактеризована Эрнстом Берлинером на примере больных гусениц мучной моли (Ephestia kuhniella) в 1915 г. Первое упоминание о ее применении для борьбы с насекомыми было сделано в Венгрии в конце 1920-х гг., а в Югославии, в начале 1930-х гг., ее применяли для борьбы с европейским кукурузным мотыльком. Bt, то есть, основной биорациональный пестицид, был первоначально охарактеризован как патоген у насекомых, и его инсектицидная активность в значительной степени или полностью приписывалась параспоральным кристаллам. Он является активным в отношении более 150 видов насекомых-вредителей. Токсичность культуры Bt заключается в ее способности продуцировать кристаллический белок, и это наблюдение привело к разработке биоинсектицидов на основе Bt для борьбы с некоторыми видами насекомых отрядов Чешуекрылых, Двукрылых и Жесткокрылых.
[00173] Композиции согласно вариантам осуществления изобретения находят применение для защиты растений, семян и растительных продуктов во множестве способов. Так, например, композиции могут быть использованы в способе, который включает размещение эффективного количества пестицидной композиции в среде обитания вредителя с помощью процедуры, выбранной из группы, состоящей из опрыскивания, опудривания, рассыпания или покрытия семян.
[00174] Перед тем как материал для размножения растений (плоды, клубни, луковицы, клубнелуковицы, зерна, семена), а особенно семена, будет продан в качестве коммерческого продукта, его обычно обрабатывают защитным покрытием, содержащим гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскоциды или смеси некоторых из этих препаратов, и если это желательно, вместе с другими носителями, поверхностно-активными веществами или адъювантами, способствующими нанесению и обычно используемыми при приготовлении препаратов для обеспечения защиты от повреждений, вызываемых бактериями, грибами или паразитами животных. Для обработки семян, защитное покрытие может быть нанесено на семена либо путем пропитки клубней или зерен жидким составом, либо путем покрытия их комбинированным влажным или сухим составом. Кроме того, в особых случаях возможны и другие методы обработки растений, например, обработка почек или плодов.
[00175] Семена растений согласно изобретению, содержащие нуклеотидную последовательность, кодирующую пестицидный белок согласно изобретению, могут быть обработаны защитным покрытием для семян, содержащим соединение для обработки семян, такое как, например, каптан, карбоксин, тирам, металаксил, пиримифос-метил и другие соединения, которые обычно используются при обработке семян. В одном варианте осуществления изобретения, защитное покрытие семян, содержащее пестицидную композицию согласно изобретению, используют отдельно или в комбинации с одним из защитных покрытий семян, обычно используемых при обработке семян. Композиции согласно изобретению могут быть получены в форме, подходящей для непосредственного применения или в виде концентрата первичной композиции, который требует разведения подходящим количеством воды или другого разбавителя перед применением. Концентрация пестицида будет варьироваться в зависимости от природы конкретного состава, особенно от того, является ли он концентратом или предназначен для непосредственного использования. Композиция содержит от 1 до 98% твердого или жидкого инертного носителя и от 0 до 50% или от 0,1 до 50% поверхностно-активного вещества. Эти композиции могут быть введены в дозе, указанной на этикетке для коммерческого продукта, например, приблизительно от 0,01 до 5,0 фунтов на акр в сухой форме и приблизительно от 0,01 до 10 долей на акр в жидкой форме.
[00176] Описанная здесь оптимизированная по кодонам синтетическая нуклеотидная последовательность может быть также использована для получения трансформированных Bacillus thuringiensis, способных продуцировать белок Cry2Ai. Затем трансформированная Bacillus thuringiensis может быть использована для получения инсектицидной и/или пестицидной композиции, применимой для сельскохозяйственной деятельности, такой как борьба с насекомыми-вредителями.
[00177] В некоторых вариантах осуществления изобретения, трансформированный микроорганизм (который включает целые организмы, клетки, споры, такие как Bacillus thuringiensis, трансформированные оптимизированными по кодонам синтетическими нуклеотидными последовательностями, описанными в настоящей заявке, пестицидный(е) белок (белки), пестицидный(е) компонент(ы), компонент(ы), поражающий(е) вредителя, мутант(ы), живые или мертвые клетки и клеточные компоненты, включая смеси живых и мертвых клеток и клеточных компонентов, включая разрушенные клетки и клеточные компоненты) или выделенный пестицидный белок могут быть приготовлены вместе с приемлемым носителем в виде пестицидной(ых) композиции(й), которая(ые) представляет(ют) собой, например, суспензию, раствор, эмульсию, присыпку, диспергируемые гранулы или таблетки, смачиваемый порошок и эмульгируемый концентрат, аэрозоль или спрей, пропитанные гранулы, адъювант, пасту для нанесения покрытия, коллоид, а также соединения, инкапсулированные, например, в полимерных веществах. Эти составленные композиции могут быть получены такими общепринятыми способами, как сушка, лиофилизация, гомогенизация, экстракция, фильтрация, центрифугирование, седиментация или концентрирование культуры клеток, содержащих полипептид.
[00178] Такие описанные выше композиции могут быть получены путем добавления поверхностно-активного вещества, инертного носителя, консерванта, увлажнителя, стимулятора поедания, аттрактанта, инкапсулирующего агента, связующего вещества, эмульгатора, красителя, УФ-защитного средства, буфера, агента для улучшения текучести или удобрений, доноров микроэлементов или других препаратов, влияющих на рост растений. Один или несколько агрохимикатов, включая, но не ограничиваясь ими, гербициды, инсектициды, фунгициды, бактерициды, нематоциды, моллюскоциды, акарициды, регуляторы роста растений, вспомогательные средства для сбора урожая и удобрения, могут быть объединены с носителями, поверхностно-активными веществами или адъювантами, обычно используемыми специалистами по приготовлению композиций или других компонентов для облегчения работы с продуктом и его применения для борьбы с конкретными вредителями. Подходящие носители и адъюванты могут быть твердыми или жидкими и соответствовать веществам, обычно используемым в технологии приготовления рецептур, например, природным или регенерированным минеральным веществам, растворителям, диспергаторам, смачивающим агентам, веществам, повышающим клейкость, связующим веществам или удобрениям. Активные ингредиенты согласно изобретению обычно применяются в форме композиций, и могут быть нанесены на обрабатываемую площадь сельскохозяйственных культур, на растения или на семена. Так, например, композиции согласно изобретению могут быть нанесены на зерно при подготовке или во время хранения в зерновом бункере или в силосном бункере и т.п. Композиции согласно вариантам осуществления изобретения могут применяться одновременно или последовательно с другими соединениями. Способы нанесения активного ингредиента согласно изобретению или агрохимической композиции согласно изобретению, которая содержит по меньшей мере один из пестицидных белков, продуцируемых бактериальными штаммами согласно изобретению, включают, но не ограничиваются ими, нанесение на листья, покрытие семян и внесение в почву. Количество применений и норма внесения зависят от интенсивности заражения соответствующим вредителем.
[00179] В другом варианте осуществления изобретения, композиции, а также трансформированные микроорганизмы и пестицидный белок согласно изобретению могут быть обработаны перед приготовлением препарата для продления пестицидной активности при внесении в среду обитания вредителя, при условии, что предварительная обработка не будет негативно влиять на пестицидную активность. Такая обработка может быть осуществлена химическими и/или физическими средствами при условии, что она не будет негативно влиять на свойства композиции(й). Примеры химических реагентов включают, но не ограничиваются ими, галогенирующие агенты; альдегиды, такие как формальдегид и глутаральдегид; противоинфекционные средства, такие как хлорид зефирана; спирты, такие как изопропанол и этанол.
[00180] В других вариантах осуществления изобретения может оказаться предпочтительной обработка полипептидов токсина Cry протеазой, например трипсином, для активации белка перед нанесением пестицидной белковой композиции согласно вариантам осуществления изобретения в среду обитания вредителя-мишени. Способы активации протоксина сериновой протеазой хорошо известны специалистам в данной области.
[00181] Композиции (включая трансформированные микроорганизмы и пестицидный белок согласно вариантам осуществления изобретения) могут быть внесены в среду обитания насекомых-вредителей, например, путем распыления, аэрозольного распыления, опудривания, разбрасывания, нанесения покрытия или выливания, внесения в почву или нанесения на нее, внесения в воду для полива, обработки семян или общего применения или опудривания во время появления вредителей или до появления вредителей в качестве защитной меры. Так, например, пестицидный белок и/или трансформированные микроорганизмы согласно вариантам осуществления изобретения могут быть смешаны с зерном для защиты зерна во время хранения. Обычно, важно обеспечить хорошую защиту от вредителей на ранних стадиях роста растений, так как именно в это время растение может быть наиболее серьезно повреждено. Композиции согласно вариантам осуществления изобретения могут, если это необходимо, содержать и другой инсектицид. В одном варианте осуществления изобретения, композицию вносят непосредственно в почву во время посадки в гранулированной форме, содержащей носитель и мертвые клетки штамма Bacillus или трансформированного микроорганизма согласно вариантам осуществления изобретения. Другой вариант осуществления изобретения представляет собой гранулированную форму композиции, содержащей агрохимикат, такой как, например, гербицид, инсектицид, удобрение, инертный носитель и мертвые клетки штамма Bacillus или трансформированного микроорганизма согласно вариантам осуществления изобретения.
[00182] Для специалиста в данной области очевидно, что не все соединения одинаково эффективны против всех вредителей. Соединения в соответствии с вариантами осуществления изобретения проявляют активность против насекомых-вредителей, которые могут включать вредителей, наносящих сильный экономический и агрономический урон, вредителей леса, вредителей в теплицах, вредителей в питомниках, вредителей декоративных растений, пищевых продуктов и волокна, вредителей, наносящих ущерб здоровью населения и животных, вредителей, обитающих в домах и магазинах, вредителей домашних хозяйств и хранящихся продуктов.
[00183] К насекомым-вредителям относятся насекомые отряда Чешуекрылых, Двукрылых, Жесткокрылых, Полужесткокрылых и Равнокрылых.
[00184] Насекомыми-вредителями отряда Чешуекрылых являются, но не ограничиваются ими, походные черви, совки, пяденицы и гелиотины семейства Noctuidae Spodoptera frugiperda JE Smith (осенняя совка); S. exigua Hubner (свекольная совка); S. litura Fabricius (табачная совка, гусеницы, образующие скопления); Mamestra configurata Walker (совка-берта); M. brassicae Linnaeus (капустная моль); Agrotis ipsilon Hufnagel (совка-ипсилон); A. orthogonia Morrison (совка западная); A. subterranea Fabricius (совка круглая); Alabama argillacea Hubner (хлопковый листовой червь); Trichoplusia ni Hubner (капустная пяденица); Pseudoplusia includens Walker (соевая пяденица); Anticarsia gemmatalis Hubner (бархатная гусеница); Hypena scabra Fabricius (зеленый клеверный червь); Heliothis virescens Fabricius (табачный почковый червь); Pseudaletia unipuncta Haworth (походный червь); Athethis mindara Barnes and Mcdunnough (совка с грубой кожей); Euxoa messoria Harris (темнополосная совка); Earias insulana Boisduval (игловидная совка); E. vittella Fabricius (пятнистая совка); Helicoverpa armigera Hubner (американская совка); H. zea Boddie (кукурузная уховертка или хлопковая совка); Melanchra picta Harris (зебровидная гусеница); Egira (Xylomyges) curialis Grote (совка цитрусовых); пилильщики, гусеницы, паутинные черви, хищные черви и скелетообразующие черви семейства Pyralidae Ostrinia nubilalis Hubner (европейский кукурузный мотылек); Amyelois transitella Walker (червь «пупка» апельсина); Anagasta kuehniella Zeller (средиземноморская мучная моль); Cadra cautella Walker (миндальная моль); Chilo suppressalis Walker (рисовый стеблевой пилильщик); C. partellus, (мотылек, обитающий на сорго); Corcyra cephalonica Stainton (рисовая моль); Crambus caliginosellus Clemens (паутинный червь корней кукурузы); C. teterrellus Zincken (паутинный червь мятлика); Cnaphalocrocis medinalis Guenee (листовой червь риса); Desmia funeralis Hubner (виноградный листовой червь); Diaphania hyalinata Linnaeus (дынный червь); D. nitidalis Stoll (червь обитающий на огурцах); Diatraea grandiosella Dyar (юго-западный кукурузный мотылек), D. saccharalis Fabricius (мотылек сахарного тростника); Eoreuma loftini Dyar (мексиканский рисовый мотылек); Ephestia elutella Hubner (табачная моль (моль какао)); Galleria mellonella Linnaeus (большая восковая моль); Herpetogramma licarsisalis Walker (дерновый паутинный червь); Homoeosoma electellum Hulst (подсолнечная моль); Elasmopalpus lignosellus Zeller (малый пилильщик стеблей кукурузы); Achroia grisella Fabricius (малая восковая моль); Loxostege sticticalis Linnaeus (паутинный свекольный червь); Orthaga tyrisalis Walker (паутинная моль чайного дерева); Maruca testulalis Geyer (пилильщик бобов фасоли); Plodia interpunctella Hubner (индийская мучная моль); Scirpophaga incertulas Walker (желтостебельный пилильщик); Udea rubigalis Guenee (вредитель сельдерея); и листовертки, почковые черви, семенные черви и плодовые черви семейства Tortricidae Acleris gloverana Walsingham (западный черноголовый почковый червь); A. variana Fernald (восточный черноголовый почковый червь); Archips argyrospila Walker (листоверт плодовых деревьев); A. rosana Linnaeus (европейский листоверт); и другие виды Archips, Adoxophyes orana Fischer von Rosslerstamm (летняя плодовая моль); Cochylis hospes Walsingham (полосатая моль подсолнечника); Cydia latiferreana Walsingham (ореховый червь); C. pomonella Linnaeus (моль-плодожорка); Platynota flavedana Clemens (пестрый листоверт); P. stultana Walsingham (всеядный листоверт); Lobesia botrana Denis & Schiffermuller (европейская виноградная моль); Spilonota ocellana Denis & Schiffermuller (пятнистая почковая моль); Endopiza viteana Clemens (виноградная моль); Eupoecilia ambiguella Hubner (моль виноградной лозы); Bonagota salubricola Meyrick (бразильский яблочный листоверт); Grapholita Molesta Busck (восточная плодовая моль); Suleima helianthana Riley (почковая моль подсолнечника); Argyrotaenia spp.; Choristoneura spp.
[00185] Другими выбранными агрономическими вредителями отряда Чешуекрылых являются, но не ограничиваются ими, Alsophila pometaria Harris (осенний ядовитый червь); Anarsia lineatella Zeller (пилильщик побегов персика); Anisota senatoria JE Smith (дубовый червь с оранжевыми полосками); Antheraea pernyi Guerin-Meneville (китайский дубовый шелкопряд); Bombyx mori Linnaeus (шелкопряд); Bucculatrix thurberiella Busck (точильщик листьев хлопчатника); Collas eurytheme Boisduval (гусеница люцерны); Datana integerrima Grote & Robinson (гусеница грецкого ореха); Dendrolimus sibiricus Tschetwerikov (сибирский шелкопряд), Ennomos subsignaria Hubner (паутинная вязовая совка); Erannis tiliaria Harris (липовая пяденица); Euproctis chtysorrhoea Linnaeus (моль лисохвоста); Harrisina americana Guerin-Meneville (вредитель, скелетирующий виноградные листья); Hemileuca oliviae Cockrell (гусеница, обитающая на больших ареалах); Hyphantria cunea Drury (осенний паутинный червь); Keiferia lycopersicella Walsingham (томатный червь); Lambdina fiscellaria fiscellaria Hulst (восточная пяденица); L. fiscellaria lugubrosa Hulst (западная пяденица болиголова); Leucoma salicis Linnaeus (атласная моль); Lymantria dispar Linnaeus (непарный шелкопряд); Manduca quinquemaculata Haworth (пятнистая ястребиная моль, томатный рогатый червь); M. sexta Haworth (томатный рогатый червь, табачный рогатый червь); Operophtera brumata Linnaeus (озимая моль); Paleacrita vemata Peck (весенний плодовый червь); Papilio cresphontes Cramer (червь, поражающий гигантский лисохвост, оранжевый собачий червь; Phryganidia californica Packard (калифорнийский дубовый червь); Phyllocnistis citrella Stainton (цитрусовый минер); Phyllonotycter blancardella Fabricius (пятнистый тентиформный минер); Pieris brassicae Linnaeus (большая белая бабочка); P. rapae Linnaeus (малая белая бабочка); P. napi Linnaeus (белая бабочка с зелеными прожилками); Platyptilia carduidactyla Riley (моль артишока и сливы); Plutella xylostella Linnaeus (пяденица обыкновенная); Pectinophora gossypiella Saunders (гвоздичная совка); Pontia protodice Boisduval & Leconte (южная капустная совка); Sabulodes aegrotata Guenee (всеядная пяденица); Schizura concinna JE Smith (красногорбая гусеница); Sitotroga cerealella Olivier (зерновая моль Angoumois); Thaumetopoea pityocampa Schiffermuller (гусеница соснового шелкопряда); Tineola bisselliella Hummel (паутинная тканевая моль); Tuta absolute Meyrick (томатный минер); Yponomeuta padella Linnaeus (горностаевая моль); Heliothis subflexa Guenee; Malacosoma spp. и Orgyia spp.
[00186] Насекомые-вредители могут быть протестированы на пестицидную активность композиций согласно изобретению на ранних стадиях развития, например, в виде личинок или других незрелых форм. Насекомые могут быть выращены в полной темноте при температуре от приблизительно 20°C до приблизительно 30°C и при относительной влажности от приблизительно 30% до приблизительно 70%. Способы выращивания личинок насекомых и проведения биоанализов хорошо известны специалисту в данной области.
[00187] Способ борьбы с насекомыми, в частности с Чешуекрылыми, в соответствии с настоящим изобретением может включать нанесение (например, распыление) раскрытой здесь инсектицидной/пестицидной композиции на участок или растение, подлежащее защите, на участок (ареал), который должен быть защищен, где указанный способ включает трансформацию клеток-хозяев оптимизированными по кодонам нуклеотидными последовательностями cry2Ai согласно изобретению. Защищаемый участок может включать, например, среду обитания насекомых-вредителей или произрастающую на ней растительность или территорию, на которой она будет выращиваться.
[00188] Настоящее изобретение относится к способу борьбы с насекомыми-вредителями баклажанов, где указанный способ включает нанесение раскрытой здесь инсектицидной/пестицидной композиции, на участок или растение, подлежащее защите, путем посадки растений баклажанов, трансформированных нуклеотидной(ыми) последовательностью(ями) cry2Ai согласно изобретению, или распыление композиции, содержащей белок Cry2Ai согласно изобретению. Настоящее изобретение также относится к применению композиции согласно изобретению для борьбы с Чешуекрылыми вредителями баклажанов для минимизации повреждения растений баклажанов.
[00189] Настоящее изобретение также относится к способу борьбы с насекомыми-вредителями риса, такими как чешуекрылые стеблевые пилильщики риса, рисовые листовертки, рисовые прыгуны, рисовые совки, рисовые походные черви или рисовые чехлоноски, а предпочтительно насекомые, выбранные из группы, состоящей из: Chilo suppressalis, Chilo partellus, Scirpophaga incertulas, Sesamia inferens, Cnaphalocrocis medinalis, Marasmia patnalis, Marasmia exigua, Marasmia farmalis, Scirpophaga innotata, где указанный способ включает нанесение раскрытой здесь инсектицидной/пестицидной композиции на участок или растение, подлежащее защите, путем посадки растения риса, трансформированного нуклеотидной(ыми) последовательностью(ями) cry2Ai согласно изобретению, или путем опрыскивания композицией, содержащей белок Cry2Ai согласно изобретению. Настоящее изобретение также относится к применению раскрытой здесь композиции против насекомых-вредителей риса для минимизации повреждения растений риса.
[00190] Настоящее изобретение также относится к способу борьбы с насекомыми-вредителями томатов, такими как чешуекрылые насекомые Helicoverpa armigera, где указанный способ включает нанесение раскрытой здесь инсектицидной/пестицидной композиции на участок или растение, подлежащее защите, путем посадки растения томата, трансформированного нуклеотидной(ыми) последовательностью(ями) cry2Ai согласно изобретению, или путем опрыскивания композицией, содержащей белок Cry2Ai согласно изобретению. Настоящее изобретение также относится к применению раскрытой здесь композиции против насекомых-вредителей томатов для минимизации повреждения растений томатов.
[00191] Настоящее изобретение также относится к способу борьбы с насекомыми-вредителями хлопчатника, где указанный способ включает нанесение раскрытой здесь инсектицидной/пестицидной композиции на участок или растение, подлежащее защите, путем посадки растения хлопчатника, трансформированного нуклеотидной(ыми) последовательностью(ями) cry2Ai согласно изобретению, или путем опрыскивания композицией, содержащей белок Cry2Ai согласно изобретению. Настоящее изобретение также относится к применению раскрытой здесь композиции против насекомых-вредителей хлопчатника для минимизации повреждения растений хлопчатника.
[00192] Для получения белка-токсина Cry2Ai (SEQ ID NO:1), клетки рекомбинантных хозяев, экспрессирующих белок Cry2Ai, могут быть культивированы обычным способом в подходящей культуральной среде, а затем подвергуты лизису с использованием обычных средств, таких как ферментативное разложение, использование детергентов и т.п. Затем токсин может быть выделен и очищен стандартными способами, такими как хроматография, экстракция, электрофорез или т.п.
[00193] Соответственно, настоящее изобретение относится к композициям и способам борьбы с насекомыми-вредителями, а в частности, с вредителями растений. Более конкретно, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, которая кодирует биологически активные инсектицидные полипептиды против насекомых-вредителей, таких как, но не ограничивающихся ими, насекомые-вредители отряда Чешуекрылых, таких как Helicoverpa armigera - хлопковая совка и кукурузная уховертка, Cnaphalocrocis medinalis - рисовый листоверт и Scirpophaga incertulas - рисовый желтостеблевой пилильщик и Spectinophora gossypiella.
[00194] В соответствии с настоящим изобретением, в одном из своих вариантов, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, кодирующей белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1, где указанная нуклеотидная последовательность выбрана из группы, состоящей из: (а) нуклеотидной последовательности, представленной в SEQ ID NO:2; (b) нуклеотидной последовательности, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положений нуклеотидов 262 до 402 и/или от 1471 до 1631; и (c) нуклеотидной последовательности, комплементарной нуклеотидной последовательности (a) и (b).
[00195] В другом своем варианте, настоящее изобретение относится к молекуле нуклеиновой кислоты, содержащей оптимизированную по кодонам последовательность для экспрессии в растении, выбранную из группы, состоящей из: (а) нуклеотидной последовательности, представленной в SEQ ID NO:2; (b) нуклеотидной последовательности, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, от положений нуклеотидов 262 до 402 и/или от 1471 до 1631; и (c) нуклеотидной последовательности, комплементарной нуклеотидной последовательности (a) и (b).
[00196] В одном из своих вариантов, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности, кодирующей белок, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1, где указанная нуклеотидная последовательность представляет собой:
а. последовательность, представленную в SEQ ID NO: 2, или комплементарную ей нуклеотидную последовательность; или
b. нуклеотидную последовательность, которая специфически гибридизуется по меньшей мере с 10 нуклеотидами нуклеотидной последовательности, представленной в SEQ ID NO: 2, в положениях нуклеотидов от 262 по 402 и/или от 1471 до 1631, или комплементарную ей нуклеотидную последовательность.
[00197] В другом своем варианте, настоящее изобретение относится к оптимизированной по кодонам синтетической нуклеотидной последовательности согласно изобретению, где указанная нуклеотидная последовательность, которая специфически гибридизуется с нуклеотидной последовательностью, представленной в SEQ ID NO: 2, выбрана из группы, состоящей из SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
[00198] В другом своем варианте, настоящее изобретение относится к рекомбинантной ДНК, содержащей оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению, где нуклеотидная последовательность функционально связана с гетерологичным регуляторным элементом. Другой вариант осуществления изобретения относится к рекомбинантной ДНК, раскрытой в настоящей заявке, где указанная оптимизированная по кодонам синтетическая нуклеотидная последовательность содержит, но необязательно, селективный маркерный ген, репортерный ген или их комбинацию. Еще один вариант осуществления изобретения относится к раскрытой здесь рекомбинантной ДНК, где указанная оптимизированная по кодонам синтетическая нуклеотидная последовательность содержит, но необязательно, последовательность ДНК, кодирующую нацеливающий или транспортный пептид для нацеливания на вакуоль, митохондрию, хлоропласт, пластиду, или для секреции.
[00199] В другом своем варианте, настоящее изобретение относится к конструкции ДНК для экспрессии представляющего интерес инсектицидного белка, содержащей 5'-нетранслируемую последовательность; кодирующую последовательность, кодирующую инсектицидный белок Cry2Ai, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее инсектицидную часть, и 3'-нетранслируемую область, где указанная 5'-нетранслируемая последовательность содержит промотор, функциональный в клетке растений; указанная кодирующая последовательность представляет собой раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность, а указанная 3'-нетранслируемая последовательность содержит последовательность терминации транскрипции и сигнал полиаденилирования.
[00200] В одном из своих вариантов, настоящее изобретение относится к плазмидному вектору, содержащему раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность. В другом своем варианте, настоящее изобретение относится к плазмидному вектору, содержащему рекомбинантную ДНК, включающую оптимизированную по кодонам синтетическую нуклеотидную последовательность, раскрытую в настоящей заявке. В другом своем варианте, настоящее изобретение относится к плазмидному вектору, содержащему конструкцию ДНК, включающую оптимизированную по кодонам синтетическую нуклеотидную последовательность, раскрытую в настоящей заявке.
[00201] В другом своем варианте, настоящее изобретение относится к клетке-хозяину, содержащей оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению. Клетка-хозяин согласно изобретению охватывает растительную клетку, бактериальную клетку, вирус-содержащую клетку, клетку грибов и дрожжевую клетку. В другом варианте осуществления изобретения, описанная клетка-хозяин представляет собой клетку растения, Agrobacterium или E.coli.
[00202] В другом своем варианте, настоящее изобретение относится к способу сообщения растению резистентности к насекомым, где указанный способ включает:
(а) встраивание в клетку растения раскрытой здесь оптимизированной по кодонам синтетической нуклеотидной последовательности, где нуклеотидная последовательность функционально связана с (i) промотором, функциональным в растительной клетке, и (ii) терминатором;
(b) получение трансформированной клетки растения из клетки растения на стадии (а), где указанная трансформированная клетка растения содержит указанную оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно настоящему изобретению; и
(с) получение трансгенного растения из указанной трансформированной клетки растения стадии (b), где указанное трансгенное растение содержит указанную оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению.
[00203] В другом своем варианте, настоящее изобретение относится к трансгенному растению, полученному способом сообщения резистентности к насекомым, как описано в настоящей заявке. Еще один вариант осуществления изобретения относится к трансгенному растению, содержащему оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению. Еще один вариант осуществления изобретения относится к трансгенному растению, содержащему оптимизированную по кодонам синтетическую нуклеотидную последовательность, где нуклеотидная последовательность выбрана из группы, состоящей из SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6. Еще один вариант осуществления изобретения относится к трансгенному растению, раскрытому в настоящей заявке, где указанное растение выбрано из группы, состоящей из хлопчатника, баклажана, риса, пшеницы, кукурузы, сорго, овса, проса, бобовых, томатов, капусты, цветной капусты, брокколи, Brassica sp., фасоли, гороха, голубиного гороха, картофеля, перца, тыквы, салата-латука, сладкого картофеля, канолы, сои, люцерны, арахиса, подсолнечника, сафлора, табака, сахарного тростника, маниоки, кофе, ананаса, цитрусовых, какао, чая, банана и дыни.
[00204] В другом своем варианте, настоящее изобретение относится к ткани, семенам или потомству, полученным из трансгенного растения согласно изобретению, где указанные семена или потомство содержат раскрытую здесь оптимизированную по кодонам синтетическую нуклеотидную последовательность. В другом своем варианте, настоящее изобретение относится к биологическому образцу, полученному из раскрытых здесь тканей, семян или потомства, где указанный образец содержит детектируемое количество указанной оптимизированной по кодонам синтетической нуклеотидной последовательности согласно изобретению. Дополнительный вариант осуществления изобретения относится к продукту потребления, полученному из трансгенного растения, раскрытого в настоящей заявке, где указанный продукт содержит детектируемое количество указанной оптимизированной по кодонам синтетической нуклеотидной последовательности согласно изобретению.
[00205] В другом своем варианте, настоящее изобретение относится к композиции, содержащей Bacillus thuringiensis, включающую оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению, кодирующую белок Cry2Ai, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1. Композиция, раскрытая в настоящей заявке, может содержать, но необязательно, дополнительный инсектицидный агент, токсичный для тех же насекомых-вредителей, но проявляющий инсектицидный эффект, отличающийся от эффекта указанного инсектицидного белка. Инсектицидный агент композиции согласно изобретению выбран из группы, состоящей из токсина Bacillus, токсина Xenorhabdus, токсина Photorhabdus и дцРНК, специфичной для подавления одного или более основных генов указанного насекомого-вредителя.
[00206] В еще одном своем варианте, настоящее изобретение относится к способу борьбы с заражением насекомыми сельскохозяйственных культур и к способу обеспечения устойчивости к насекомым, где указанный способ включает контактирование указанного сельскохозяйственного растения с инсектицидно эффективным количеством композиции, как описано выше.
[00207] В другом своем варианте, настоящее изобретение относится к применению оптимизированной по кодонам синтетической нуклеотидной последовательности, ДНК-конструкции или плазмиды согласно изобретению для получения трансгенных растений, устойчивых к насекомым. В еще одном своем варианте, настоящее изобретение относится к применению раскрытой здесь оптимизированной по кодонам синтетической нуклеотидной последовательности для получения инсектицидной композиции, где композиция содержит клетки Bacillus thuringiensis, содержащие указанные нуклеотидные последовательности.
[00208] В другом своем варианте, настоящее изобретение относится к трансгенным растениям, которые экспрессируют по меньшей мере одну оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению. В другом своем варианте, настоящее изобретение относится к трансгенному растению, полученному способом, описанным в настоящей заявке. Трансгенное растение, раскрытое в настоящей заявке, выбрано из группы, состоящей из риса, пшеницы, кукурузы, сорго, овса, проса, бобовых, хлопчатника, томатов, баклажана, капусты, цветной капусты, брокколи, Brassica sp., фасоли, гороха, голубиного гороха, картофеля, перца, тыквы, салата-латука, сладкого картофеля, канолы, сои, люцерны, арахиса, подсолнечника, сафлора, табака, сахарного тростника, маниоки, кофе, ананаса, цитрусовых, какао, чая, банана и дыни. В некоторых своих вариантах, настоящее изобретение относится к ткани, семенам или потомству, полученным из трансгенного(ых) растения(й) согласно изобретению, где указанные семена или потомство содержат оптимизированную по кодонам синтетическую нуклеотидную последовательность, описанную в настоящей заявке. В некоторых своих вариантах, настоящее изобретение относится к биологическим образцам, полученным из тканей или семян или потомства, где образец содержит детектируемое количество указанной оптимизированной по кодонам синтетической нуклеотидной последовательности. Один из вариантов изобретения охватывает продукт потребления, полученный из трансгенного растения согласно изобретению, где указанный продукт содержит детектируемое количество оптимизированной по кодонам синтетической нуклеотидной последовательности.
[00209] В одном своем варианте, настоящее изобретение относится к композиции, содержащей Bacillus thuringiensis, включающую по меньшей мере одну оптимизированную по кодонам синтетическую нуклеотидную последовательность согласно изобретению, где указанная нуклеотидная последовательность кодирует белок Cry2Ai, имеющий аминокислотную последовательность, представленную в SEQ ID NO: 1. Эта композиция содержит, но необязательно, дополнительный инсектицидный агент, токсичный для тех же насекомых-вредителей, но проявляющий инсектицидный эффект, отличающийся от эффекта указанного инсектицидного белка. Инсектицидный агент выбран из группы, состоящей из токсина Bacillus, токсина Xenorhabdus, токсина Photorhabdus и дцРНК, специфичной для подавления одного или более основных генов указанного насекомого-вредителя.
[00210] В другом своем варианте, настоящее изобретение относится к способу борьбы с заражением насекомыми сельскохозяйственных культур и к способу обеспечения устойчивости к насекомым, где указанный способ включает контактирование указанного сельскохозяйственного растения с инсектицидно эффективным количеством композиции, описанной в настоящей заявке.
[00211] В другом своем варианте, настоящее изобретение относится к применению оптимизированной по кодонам синтетической нуклеотидной последовательности, ДНК-конструкции или плазмиды согласно изобретению для получения трансгенных растений, устойчивых к насекомым. В еще одном своем варианте, настоящее изобретение относится к применению раскрытой здесь оптимизированной по кодонам синтетической нуклеотидной последовательности для получения инсектицидной композиции, где указанная композиция содержит клетки Bacillus thuringiensis, включающие указанные нуклеотидные последовательности.
[00212] Эти и/или другие варианты осуществления изобретения отражены в формуле изобретения, которая составляет часть описания изобретения.
[00213] Различные модификации и другие варианты осуществления настоящего изобретения могут быть представлены специалистом в области, к которой относятся это изобретение, с учетом принципов, представленных в описании и прилагаемых чертежах. Следовательно, следует отметить, что настоящее изобретение не должно ограничиваться конкретными вариантами его осуществления, раскрытыми в настоящей заявке, и что в настоящее изобретение могут быть внесены модификации и другие варианты его осуществления, не выходящие за рамки объема прилагаемой формулы изобретения.
[00214] Представленные ниже примеры иллюстрируют изобретение и не должны рассматриваться как ограничение объема изобретения или требуемой защиты.
ПРИМЕРЫ
[00215] Нижеследующие примеры представлены для полного раскрыия и описания способа осуществления и применения настоящего изобретения, и эти примеры не рассматриваются как ограничение объема изобретения и указывают на то, что все нижеследующие эксперименты представляют собой все или только некоторые проведенные эксперименты. Были предприняты попытки обеспечения точности используемых чисел (например, количеств, температур и т.п.), но при этом, следует учитывать некоторые экспериментальные ошибки и отклонения.
Общие методы
[00216] Манипуляции с ДНК осуществляли в соответствии со стандартными процедурами, применяемыми в данной области. Эти процедуры часто допускают некоторые изменения или замены без существенного изменения результата. Если это не оговорено особо, то большинство из этих процедур описано в руководстве Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, второе издание, 1989.
Пример 1: Конструирование оптимизированной по кодонам последовательности, кодирующей белок CRY2Ai (SEQ ID NO: 1)
[00217] Последовательность ДНК, имеющая смещение по кодонам растений, была сконструирована и синтезирована для экспрессии белка Cry2Ai, имеющего аминокислотную последовательность, представленную в SEQ ID NO: 1, в трансгенных растениях. Таблицу использования кодонов для растений составляли исходя из кодирующих последовательностей, происходящих от последовательности белка Cry2Ai SEQ ID NO: 1 (NCBI GenBank ACV97158.1). Последовательность ДНК была оптимизирована с использованием алгоритма Монте-Карло (Villalobos A, Ness J E, Gustafsson C, Minshull J and Govindarajan S (2006) Gene Designer: a synthetic biology tool for constructing artificial DNA segments; BMC Bioinformatics 67:285-293) в качестве первичных критериев выбора кодонов. При оптимизации последовательности ДНК учитывались вероятности, представленные в таблице использования кодонов. Редко и менее часто встречающиеся кодоны были заменены наиболее распространенными кодонами. Взвешенная средняя набора кодонов растений была вычислена после исключения любого избыточного кодона, встречающегося с вероятностью менее, чем приблизительно 10% от общего количества кодонов, используемых для этой аминокислоты. Средневзвешенное представление для каждого кодона рассчитывали по формуле:
[00218] Средневзвешенный % ДИ=1/(%C1 + %C2 + %C3+и т.п.) × %C1 × 100, где CI представляет собой рассматриваемый кодон, а %C2, %C3 и т.п. представляют средние значения % использования остальных синонимичных кодонов.
[00219] Для получения последовательности ДНК с оптимизированными кодонами растений, кодирующей белок Cry2Ai SEQ ID NO: 1, замены кодонов в последовательности ДНК, кодирующей белок Cry2Ai, были сделаны так, чтобы полученная последовательность ДНК имела общий состав кодонов растений, оптимизированных как показано в таблице смещения оптимизированных кодонов для растений. Дальнейшие уточнения последовательностей были сделаны для устранения нежелательных сайтов распознавания рестриктирующих ферментов, потенциальных сайтов сплайсинга интронов растений, длинных последовательностей остатков A/T или C/G и других мотивов, которые могут негативно влиять на стабильность РНК, транскрипцию или трансляцию кодирующей области в клетках растений. Ген был оптимизирован in silico с использованием программного обеспечения для создания генов с пороговым значением 6,0 ккал/моль для образования стабильной вторичной структуры мРНК. Другие изменения были внесены для включения желаемых сайтов распознавания рестриктирующих ферментов и исключения длинных внутренних открытых рамок считывания (рамок, не являющихся +1). Сайты распознавания рестриктирующих ферментов XbaI, NcoI и BamHI были включены перед старт-кодоном ATG, а сайт распознавания рестриктирующего фермента SmaI был встроен перед стоп-кодоном для обеспечения клонирования оптимизированного гена в прокариотическом векторе для присоединения С-концевых белковых меток. Сайты распознавания рестриктирующих ферментов EcoRI и HindIII были включены после стоп-кодона. Стоп-кодон TGA использовали в оптимизированном гене.
[00220] Все эти изменения были внесены в рамках ограничений, связанных с сохранением приблизительного состава кодонов, смещенных в данных растениях. Полная последовательность, оптимизированная по кодонам растений и кодирующая белок Cry2Ai (SEQ ID NO: 1), представлена в SEQ ID NO: 2-6. Трансляция in silico последовательности ДНК, оптимизированной по смещению кодонов растений, показала 100% идентичность с нативным белком Cry2Ai (SEQ ID NO: 1). Последовательности ДНК с оптимизированными кодонами растений (SEQ ID NO: 2-6) были обозначены как 201D1, 201D2, 201D3, 201D4 и 201D5. Синтез фрагментов ДНК 201D1-D5 (SEQ ID NO: 2-6) был выполнен коммерческим поставщиком (Genscript Inc, USA). Фрагмент ДНК 201D1 был клонирован в вектор pUC57 с применением метода, известного специалистам в данной области и обозначенного как pUC57-201D1. Аналогичным образом, фрагменты ДНК 201D2, ДНК 201D3, ДНК 201D4 и ДНК 201D5 были клонированы в вектор pUC57 и обозначены как pUC57-201D2, pUC57-201D3, pUC57-201D4 и pUC57-201D5, соответственно.
Пример 2: Конструирование экспрессионного вектора
[00221] Вектор pUC57-201D1 Примера 1 расщепляли BamHI и HindIII с получением фрагмента ДНК 201D1 (SEQ ID NO: 2) (реакционный объем - 20 мкл, плазмидная ДНК - 8,0 мкл, буфер 10× - 2,0 мкл, рестриктирующий фермент BamHI - 0,5 мкл, рестриктирующий фермент HindIII - 0,5 мкл, дистиллированная вода - 9,0 мкл). Все реагенты смешивали с получением реакционной смеси и инкубировали при 37°C в течение 30 минут, после чего реакционную смесь анализировали с помощью гель-электрофореза на 2% агарозном геле, и фрагмент ДНК 201D1 вырезали из агарозного геля чистым острым скальпелем под УФ-излучением. Фрагмент ДНК элюировали из геля с использованием набора для элюирования геля. Срез геля, содержащий фрагмент ДНК, переносили в пробирку Эппендорфа объемом 2 мл и добавляли 3-кратный объем буфера DE-A для образцов. Гель ресуспендировали в буфере DE-A путем встряхивания, и содержимое нагревали до 75°C до полного растворения геля с последующим добавлением 0,5× буфера DE-A и DE-B, смешанных вместе. Пробирку Эппендорфа подготавливали путем ее помещения в колонку, и в эту колонку переносили смесь для связывания. Пробирку Эппендорфа, встроенную в колонку, быстро центрифугировали. Затем в колонку помещали свежую пробирку Эппендорфа и добавляли 500 мкл промывочного буфера -WI (набор Qiagen) с последующим центрифугированием. Супернатант отбрасывали и добавляли 700 мкл промывочного буфера -W2 вдоль стенок колонки для смывания всего остаточного буфера с последующим центрифугированием. Эту стадию повторяли с аликвотой 700 мкл буфера W2. В колонку переносили свежую пробирку Эппендорфа и центрифугировали при 6000 об/мин в течение 1 минуты для удаления остаточного буфера. В колонку снова помещали новую пробирку Эппендорфа и в центр мембраны добавляли 40 мкл элюирующего буфера. Колонку с элюирующим буфером оставляли на 1 минуту при комнатной температуре и пробирки центрифугировали при 12000 об/мин в течение 1 минуты. Элюированный фрагмент ДНК 201D1 хранили при -20°С до последующего использования.
[00222] Полученный таким образом выделенный и очищенный фрагмент ДНК 201D1 лигировали в линеаризованный вектор pET32a. Лигирование проводили с использованием фермента ДНК-лигазы Т4 (реакционный объем - 30 мкл, 10× буфер для лигирования - 3,0 мкл, векторная ДНК - 5,0 мкл, ДНК-вставка - 15,0 мкл, фермент ДНК-лигаза Т4-1,0 мкл, дистиллированная вода - 6,0 мкл). Реагенты тщательно перемешивали, и полученную реакционную смесь инкубировали при 16°C в течение 2 часов. Затем, компетентные клетки штамма E. coli BL21 (DE3) трансформировали лигированной смесью, содержащей вектор pET32a, несущий ДНК 201D1, путем добавления 10 мкл смеси для лигирования к 100 мкл компетентных клеток BL21 DE3. Полученную таким образом смесь клеток помещали на лед на 30 минут, инкубировали при 42°C в течение 60 секунд на водяной бане для достижения теплового шока и снова помещали на лед на 5-10 минут. Затем к смеси добавляли 1 мл бульона LB и дополнительно инкубировали при 37°C в течение 1 часа в шейкере инкубатора при 200 об/мин. Смесь клеток наносили на агар LB плюс 50 мкг/мл карбенициллина и инкубировали при 37°C в течение ночи. Позитивные клоны идентифицировали с помощью анализа на расщепление рестриктирующими ферментами. Полученный таким образом экспрессионный вектор был обозначен как pET32a-201D1.
[00223] Аналогичным образом были сконструированы экспрессионные векторы, несущие другие последовательности ДНК, оптимизированные по кодонам растений и представленные в SEQ ID NO: 3-6, и эти векторы были обозначены как pET32a-201D2, pET32a-201D3, pET32a-201D4 и pET32a-201D5.
Пример 3: Экспрессия CRY2Ai в E. coli .
[00224] ДНК 201D1 (SEQ ID NO: 2), клонированная в pET32a и обозначенная как pET32a-201D1, была экспрессирована в E. coli BL 21 D3. Экспрессию индуцировали 1 мМ IPTG при плотности клеток приблизительно при OП на длине волны=0,5-1,0 нм. После индуцирования, клетки E. coli инкубировали в шейкере от 24 до 40 часов при 16°C для продуцирования белка. Белок Cry2Ai (SEQ ID NO: 1) экспрессировался в клетке в растворимой форме. Затем культуру переносили в центрифужную пробирку и центрифугировали при 10000 об/мин в течение 5 минут. Супернатант сливали, 10 мл клеток обрабатывали лизоцимом и инкубировали в течение 1 часа при комнатной температуре. Образцы центрифугировали при 10000 об/мин в течение 5 минут и супернатант отбрасывали. Осадок суспендировали в стерильной дистиллированной воде и центрифугировали при 10000 об/мин в течение 10 минут. Эту стадию повторяли дважды, и осадок хранили при -20°C. Осадок, содержащий белки из индуцированного рекомбинантного штамма, анализировали с помощью электрофореза в 10% ПААГ с ДСН.
[00225] Аналогичным образом, последовательности ДНК, представленные в SEQ ID NO: 3-6, были клонированы в pET32a и экспрессированы в E. coli BL 21 D3.
Пример 4: Конструирование вектора для трансформации растений, содержащего ДНК 201D1 (SEQ ID NO: 2), кодирующую белок CRY2Ai (SEQ ID NO: 1)
[00226] Вектор pUC57-201D1, несущий ДНК 201D1 (SEQ ID NO: 2), расщепляли рестриктирующими ферментами для высвобождения фрагмента ДНК 201D1 (реакционный объем - 20 мкл, плазмидная ДНК - 8,0 мкл, буфер 10 × - 2,0 мкл, рестриктирующий фермент EcoRV - 0,5 мкл, дистиллированная вода - 9,5 мкл). Все реагенты смешивали, и смесь инкубировали при 37°C в течение 30 минут. Продукт, полученный после расщепления рестриктирующими ферментами, анализировали с помощью гель-электрофореза и дополнительно очищали.
[00227] Вектор Ti плазмиды pGreen0029 получали путем расщепления рестриктирующим ферментом EcoRV (реакционный объем - 20 мкл, плазмидная ДНК - 8,0 мкл, буфер 10× - 2,0 мкл, рестриктирующий фермент EcoRV - 0,5 мкл, дистиллированная вода - 9,5 мкл). Все реагенты смешивали, и смесь инкубировали при 37°С в течение 30 минут. Продукт, полученный после гидролиза рестриктирующими ферментами, анализировали с помощью гель-электрофореза.
[00228] Очищенный фрагмент ДНК 201D1 (SEQ ID NO: 2) лигировали в линеаризованный вектор pGreen0029. Лигирование проводили с использованием фермента ДНК-лигазы Т4 (реакционный объем - 30 мкл, 10× буфер для лигирования - 3,0 мкл, вектор ДНК - 5,0 мкл, ДНК-вставка - 15,0 мкл, фермент ДНК-лигаза Т4-1,0 мкл, дистиллированная вода - 6,0 мкл). Реагенты тщательно перемешали и полученную реакционную смесь инкубировали при 16°С в течение 2 часов. Затем компетентные клетки штамма E. coli BL21 (DE3) трансформировали смесью для лигирования, содержащей вектор pGreen0029, несущий ДНК 201D1 (SEQ ID NO: 2), путем добавления 10 мкл смеси для лигирования к 100 мкл компетентных клеток BL21 DE3. Полученную таким образом клеточную смесь помещали на лед на 30 минут и инкубировали при 42°С в течение 60 секунд на водяной бане для теплового шока, и клеточную смесь снова помещали на лед на 5-10 минут. Затем к смеси добавляли 1 мл бульона LB и дополнительно инкубировали при 37°C в течение 1 часа в шейкере-инкубаторе при 200 об/мин. Суспензию клеток (100 мкл) равномерно распределяли на среде с агаром LB, содержащей 50 мкг/мл карбенициллина. Планшеты инкубировали при 37°C в течение ночи. Позитивные клоны подтверждали путем анализа на расщепление рестриктирующими ферментами. Полученный таким образом рекомбинантный вектор был обозначен как pGreen0029 CaMV35S-201D1.
[00229] Таким образом, рекомбинантная плазмида pGreen0029-CaMV35S-201D1 содержит оптимизированную для растений последовательность ДНК 201D1 (SEQ ID NO: 2) под транскрипционным контролем промотора 35SCaMV. Кроме того, pGreen0029-CaMV35S-201D1 содержит ген nptII, селективный маркерный ген растений под транскрипционным контролем промотора NOS (фиг. 1). Физическое расположение компонентов Т-области pGreen0029-CaMV35S-201D1 показано как:
[00230] RB>35SCaMV: 201D1 CDS: CaMV polyA> Промотор NOS: nptII CDS: NOS Poly A> LB
[00231] Аналогичным образом, последовательности ДНК, представленные в SEQ ID NO: 3-6, были клонированы в плазмиде Ti pGreen0029, и полученные таким образом рекомбинантные векторы были обозначены как pGreen0029-CaMV35S-201D2, pGreen0029-CaMV35S-201D3, pGreen0029-CaMV35S-201D4 и pGreen0029-CaMV35S-201D5. Физическое расположение компонентов pGreen0029-CaMV35S, несущих указанные последовательности ДНК (SEQ ID NO: 3-6) в Т-области, проиллюстрировано ниже:
[00232] RB> 35SCaMV: 201D2 CDS: CaMV polyA> Промотор NOS: nptII CDS: NOS Poly A> LB
[00233] RB> 35SCaMV: 201D3 CDS: CaMV polyA> Промотор NOS: nptII CDS: NOS Poly A> LB
[00234] RB> 35SCaMV: 201D4 CDS: CaMV polyA> Промотор NOS: nptII CDS: NOS Poly A> LB
[00235] RB> 35SCaMV: 201D5 CDS: CaMV polyA> Промотор NOS: nptII CDS: NOS Poly A> LB
Трансформация Agrobacterium tumefaciens рекомбинантным вектором pGreen0029-CaMV35S-201D1
[00236] Штамм LBA440 Agrobacterium tumefaciens трансформировали рекомбинантной плазмидой pGreen0029-CaMV35S-201D1, несущей последовательность ДНК, представленную в SEQ ID NO: 2. 200 нг плазмидной ДНК pGreen0029-CaMV35S-201D1 добавляли к аликвоте 100 мкл клеток, компетентных по штамму LBA440 А. tumefaciens. Смесь инкубировали на льду в течение 30 минут и переносили в жидкий азот на 20 минут с последующим оттаиванием при комнатной температуре. Затем клетки Agrobacterium переносили в 1 мл бульона LB и инкубировали при 28°C в течение 24 часов в шейкере с водяной баней при 200 об/мин. Суспензию клеток равномерно распределяли на среде с агаром LB, содержащей 50 мкг/мл рифампицина, 30 мкг/мл канамицина и 5 мкг/мл тетрациклина. Планшеты инкубировали при 28°C в течение ночи. Трансформированные клетки Agrobacterium анализировали методом экстракции плазмид и методом расщепления рестриктирующими ферментами, а затем отбирали позитивные колонии A. tumefaciens и хранили для дальнейшего использования.
Пример 5. (А) Agrobacterium -опосредованная трансформация хлопчатника конструкцией pGreen0029-CaMV35S-201D1
[00237] Подробное описание эксперимента по трансформации хлопчатника приводится ниже. Для специалистов в области трансформации хлопчатника будет очевидно, что для трансформации хлопчатника и отбора трансформированных растений могут быть применены и другие методы, если используются другие экспрессируемые растением селективные маркерные гены.
Материалы
Штаммы Agrobacterium tumefaciens и селективный маркер
[00238] Agrobacterium tumefaciens LBA4404 и ген неомицинфосфотрансферазы II (nptII) в качестве селективного маркера были использованы для эксперимента по трансформации и регенерации хлопчатника, описанного в настоящей заявке.
Среды для культивирования и другие среды
[00239] Среда Луриа-Бертани (LB) (Himedia); LB-агар (Himedia); макросоли MS (Himedia), микросоли MS (Himedia), FeEDTA, витамины B5, тиамин-HCl (Duchefa), пиридоксин-HCl (Duchefa), никотиновая кислота (Duchefa)], миоинозит (Sigma), сахароза (Sigma), агар (Duchefa); 2,4-дихлорфеноксиуксусная кислота (2,4-D) (Duchefa): исходный раствор - 1 мг/мл; кинетин (Duchefa); индол-3-масляная кислота/IBA (Duchefa); ацетосирингон (3',5'-диметокси-4'-гидроксиацетофенон) (Sigma); аугментин (Duchefa); моносульфат канамицина (Duchefa);
Растительный материал
[00240] Хлопчатник (Gossypium hirsutum) L. сорт Coker 310
Проращивание семян in vitro и предварительное культивирование
[00241] Семена хлопчатника сорта Coker 310 погружали в стерильную воду с 0,1% Твина-20 в шейкере при 28°C±2°C, 200 об/мин в течение 20 минут и обрабатывали 0,1% HgCl2 в шейкере в течение 20 минут. Семена пять раз промывали стерильной водой. Стерилизованные семена замачивали в стерильной воде и оставляли на ночь. Стерилизованные семена проращивали в среде MS при фотопериоде 16/8 свет/темнота при 25°C±2°C. Семядольные эксплантаты получали из 7-дневных проростков и предварительно культивировали на среде MS, содержащей соли MS, витамины B5, глюкозу: 30,0 г/л; фитагель: 2,5 г/л, pH=5,8) с 2,4-D (1,0 мг/л) и кинетином (5,0 мг/л), где абаксиальная сторона касается среды.
Совместное культивирование, отбор и регенерация растений
[00242] Через 24 часа, эксплантаты, выделенные из предварительной культуральной среды, были инфицированы в течение 20 минут суспензионной культурой A. tumefaciens LBA4404, несущей плазмиду pGreen0029-CaMV35S-201D1. Суспензионная культуральная среда состояла из 100 мкМ ацетосирингона. Избыток суспензионной культуры удаляли путем сушки методом блоттинга на стерильной фильтровальной бумаге и переносили в среду для совместного культивирования, содержащую среду MS с 2,4-D (1,0 мг/л) и кинетином (5,0 мг/л) + ацетосирингон (100 мкМ). После 48-часового совместного культивирования в темноте при 25°C±2°C, эксплантаты промывали стерильной дистиллированной водой и водным раствором, содержащим 300 мг/л аугментина. Совместно культивированные эксплантаты сушили методом блоттнга на стерильной фильтровальной бумаге и культивировали на селективной среде, содержащей среду MS с 2,4-D (1,0 мг/л) и кинетином (5,0 мг/л) + канамицин (50 мг/л) + аугментин (300 мг/л). Эксплантаты подвергали субкультивированию на одной и той же среде каждые две недели до тех пор, пока не появлялись каллусы. Каллусы собирали и субкультивировали на среде MS+канамицин (50 мг/л) + аугментин (300 мг/л). Пролиферирующиеся каллусы субкультивировали через каждый 21 день на той же самой среде. Эмбриогенные каллусы были идентифицированы и субкультивированы на среде MS с добавлением KNO3 (1,9 г/л) + аугментин (300 мг/л) с получением соматических эмбрионов. Соматические эмбрионы, возникающие из эмбриогенных каллусов, были еще раз субкультивированы на среде MS+аугментин (300 мг/л). Эмбрионы вместе с прилипшим каллусом помещали на фильтровальную бумагу и оставляли в культуральной среде. Развившиеся соматические эмбрионы затем переносили в стеклянные бутыли, содержащие среду MS с половинной концентрацией. Соматические эмбрионы развивались нормально и превращались в проростки за 14-25 дней. Ростки тщательно вынимали из бутылей с тканевой культурой и закаляли в маленьких пластиковых горшках, содержащих реагент соилрит, и выдерживали при температуре 28±2°C в течение 7-8 дней. Затем проростки переносили в теплицу (фиг. 2).
[00243] Специалистам в области трансформации и регенерации хлопчатника очевидно, что для трансформации и регенерации хлопчатника могут быть применены и другие методы. Кроме того, для отбора трансформированных растений могут быть использованы и другие селективные маркерные гены, экспрессируемые в растениях.
Пример 5 (B) Молекулярные анализы предполагаемых трансгенных растений хлопчатника, трансформированных последовательностью ДНК 201D1 (SEQ ID NO: 2)
(i) Выделение геномной ДНК
[00244] Полную геномную ДНК экстрагировали из тканей листьев предполагаемых трансгенных растений хлопчатника, полученных как описано в Примере 5 (A), и контрольных нетрансгенных растений Coker 310. Листья собирали с предполагаемых трансгенных растений хлопчатника и нетрансгенных растений хлопчатника и гомогенизировали с 300 мкл буфера для экстракции (1M Трис-HCl, pH 7,5, 1M NaCl, 200 мМ EDTA и 10% ДСН) с использованием QIAGEN TissueLyser II (Retsch) и центрифугировали при 12000 об/мин в течение 10 минут. Супернатант переносили в стерильную микроцентрифужную пробирку. К супернатанту добавляли хлороформ-изоамиловый спирт (24:1) и центрифугировали при 12000 об/мин в течение 10 минут. Водный слой переносили в микроцентрифужную пробирку. К этому слою добавляли равный объем охлажденного льдом изопропанола и выдерживали при -20°C в течение 20 минут. Затем супернатант сливали и к осадку добавляли 300 мкл этанола. После центрифугирования при 10000 об/мин в течение 5 минут, супернатант отбрасывали и осадок ДНК сушили на воздухе в течение 15 минут, а затем растворяли в 40 мкл 0,1 × TE-буфера (Трис - pH 8,0:10,0 мМ и EDTA - pH 8,0:1,0 мМ). Качественный и количественный анализ геномной ДНК проводили на спектрофотометре Nanodrop 1000® (Thermo Scientific, USA) путем измерения OП на длине волны 260 нм. Затем, целостность ДНК оценивали путем проведения электрофореза в 0,8% агарозном геле.
(ii) ПЦР-анализ
[00245] Полимеразную цепную реакцию (ПЦР) проводили на геномной ДНК (100 нг) предполагаемых трансгенных растений хлопчатника и нетрансгенных контрольных растений хлопчатника для анализа синтетической ДНК cry2Ai-201D1 с использованием праймеров, представленных в SEQ ID NO: 7 и SEQ ID NO: 8, и гена nptII с использованием праймеров, представленных в SEQ ID NO: 9 и SEQ ID NO: 10.
Условия ПЦР
94°C в течение 5 минут: 1 цикл
94°C в течение 45 секунд
58°-62°C в течение 45 секунд: 30 циклов
72°C в течение 45 секунд
72°C в течение 10 мин: 1 цикл
[00246] Было обнаружено, что все предполагаемые трансгенные растения хлопчатника были позитивными по ДНК cry2Ai-201D1 (1500 п.о.), имеющей нуклеотидную последовательность, представленную в SEQ ID NO: 2, и гену nptII (698 п.о.).
(iii) Саузерн-гибридизация
[00247] Все ПЦР-позитивные растения хлопчатника были отобраны для проведения Саузерн-гибридизации. Геномную ДНК (5 мкг каждой) ELISA-позитивных трансгенных растений хлопчатника Т0 гидролизовали рестриктирующими ферментами NcoI или XbaI или BamHI и подвергали Саузерн-блот-гибридизации с использованием [α-32P]-dCTP-меченного ДНК-зонда 201D1.
[00248] Геномную ДНК ПЦР- и ELISA-позитивных трансгенных растений хлопчатника и нетрансгенных растений хлопчатника гидролизовали рестриктирующим ферментом NcoI при 37°C в течение 16 часов. Плазмидную ДНК pGreen0029-CaMV35S-201D1 использовали в качестве позитивного контроля. Расщепленные образцы геномной ДНК и плазмидную ДНК разделяли в 0,8% агарозном геле при 20 В в течение ночи в 1× буфере TAE, визуализировали путем окрашивания бромидом этидия под УФ-трансиллюминатором и результаты заносили в систему документации геля (SYNGENE).
[00249] Расщепленную рестриктирующими ферментами и электрофоретически разделенную геномную ДНК денатурировали путем погружения гелей в два объема денатурирующего раствора на 30 минут при осторожном встряхивании. Гели подвергали нейтрализации, погружая их в два объема нейтрализующего раствора на 30 минут при осторожном перемешивании. Гель кратковременно промывали стерильной деионизированной водой, и ДНК переносили в положительно заряженную найлоновую мембрану (Sigma) посредством восходящего капиллярного переноса в 20-кратном буфере SSC в течение 16 часов в соответствии со стандартным протоколом. После полного переноса геномной ДНК, найлоновую мембрану кратковременно промывали 2× буфером SSC и сушили на воздухе в течение 5 минут. ДНК подвергали поперечному сшиванию путем экспонирования мембраны в УФ-сшивающем линкере (UV Stratalinker® 1800 Stratagene, CA, USA) при 1100 мкДж в течение 1 минуты. Перекрестносшитую мембрану запечатывали в пластиковые пакеты и хранили при 4°C до использования для Саузерн-блот-гибридизации.
Денатурирующий раствор:
NaCl: 1M
NaOH: 0,5 н
Нейтрализующий раствор:
NaCl: 1,5 М
Трис: 0,5 М
20 × SSC:
NaCl: 3,0 М
Цитрат натрия: 0,3 М
pH: 7,0, полученный путем добавления концентрированной HCl
Раствор 20 × SSC может быть разведен следующим образом:
Получение зонда
[00250] Приблизительно 100 нг фрагмента ДНК 201D1 размером 1500 п.о., амплифицированного из вектора и очищенного с помощью набора miniprep для гель-экстракции (Bio Basic Inc., Canada), радиоактивно метили [α-32P]-dCTP и использовали в качестве зонда для мечения.
[00251] Зонд для мечения: 4 мкл амплифицированных и очищенных ПЦР-фрагментов использовали в качестве ДНК-матрицы для мечения. ДНК-матрицу смешивали с 10 мкл рандомизированного праймера (DecaLabel DNA Labeling Kit, Thermo Fisher Scientific Inc., USA) в микроцентрифужной пробирке. Объем доводили до 40 мкл стерильной дистиллированной водой и денатурировали путем нагревания в течение 5 минут на кипящей водяной бане и охлаждения на льду. К денатурированной ДНК добавляли 5 мкл смеси для мечения, содержащей dATP, dGTP, dTTP, 5 мкл [α-32P]-dCTP (50 мкКи) и 1 мкл фрагмента Кленова ДНК-полимеразы I, и инкубировали при 37°C в течение 10 минут на водяной бане. Реакцию прекращали путем добавления 1 мкл 0,5 М EDTA, инкубировали на кипящей водяной бане в течение 4 минут и переносили на лед на 4-5 минут.
Предварительная гибридизация и гибридизация с зондом
[00252] Мембрану, перекрестносшитую с ДНК как описано выше, осторожно помещали в бутыль для гибридизации, содержащую 30 мл буферного раствора для гибридизации. Бутыль плотно закрывали и помещали в печь при 65°C на период от 45 минут до 1 часа для обработки перед гибридизацией.
[00253] Буфер для гибридизации выливали из бутыли и заменяли 30 мл раствора для гибридизации (поддерживаемого при 65°C), содержащего денатурированный ДНК-зонд, меченный [α-32P]-dCTP. Бутыль с раствором для гибридизации плотно закрывали и помещали в печь при 65°C на 16 ч.
Раствор для гибридизации:
Na2HPO4, pH 7,2: 0,5M
ДСН: 7% (масс./об.)
EDTA, pH 7,2: 1 мМ
[00254] Буфер для гибридизации выливали из бутыли. Затем добавляли Раствор для промывки I, и бутыль помещали в печь на медленно вращающуюся платформу при 65°C на 10 минут. Через 10 минут, Раствор для промывки I заменяли 30 мл Раствора для промывки II и инкубировали при 65°C в течение 5-10 минут при осторожном перемешивании. Затем, Раствор для промывки II выливали, и количество радиоактивности в мембране оценивали с помощью счетчика Грегора-Мюллера. В зависимости от количества, в бутыль добавляли 30 мл Раствора для промывки III и инкубировали при 65°C в течение периода времени от 30 секунд до 1 минуты при осторожном перемешивании. Затем Раствор для промывки III удаляли, и мембрану сушили на фильтровальной бумаге Whatman № 1 в течение 5-10 минут при комнатной температуре и экспонировали рентгеновской пленкой (Kodak XAR) в темной комнате с использованием экрана усилителя сигнала (Hyper cassette® от Amersham, USA) в течение 2 дней при -80°C.
[00255] Через 2 дня после экспонирования, рентгеновскую пленку переносили в темную комнату и погружали в проявитель на 1 минуту, а затем в воду на 1 минуту. И наконец, рентгеновскую пленку погружали в раствор фиксатора на 2 минуты, затем промывали водой в течение 1-2 минут и сушили на воздухе.
Раствор для промывки
Раствор для промывки I: 3× SSC+0,1% ДСН
Раствор для промывки II: 0,5× SSC+0,1% ДСН
Раствор для промывки III: 0,1× SSC+0,1% ДСН
Проявитель:
13,2 г содержимого пакета A растворяли в 800 мл дистиллированной воды, и после полного растворения добавляли 89 г компонента пакета B и растворяли при медленном перемешивании. После полного растворения, объем доводили до 1000 мл и хранили во флаконе из янтарного стекла.
Фиксатор:
268 г фиксатора растворяли в 800 мл дистиллированной воды при медленном перемешивании, и после полного растворения, объем доводили до 1000 мл, фильтровали через фильтровальную бумагу и хранили во флаконе из янтарного стекла.
[00256] Все ПЦР-позитивне трансгенные растения хлопчатника продемонстрировали сигналы гибридизации различной величины, что указывало на интеграцию трансгена в геном хлопчатника. Некоторые трансгенные растения хлопчатника показали интеграцию последовательности ДНК 201D1 в одном локусе (единственная копия ДНК 201D1), в то время как несколько трансгенных растений хлопчатника показали интеграцию последовательности ДНК 201D1 в нескольких локусах. Сигнал гибридизации также обнаруживался в позитивном контроле, тогда как нетрансгенные растения хлопчатника не показали никакого сигнала гибридизации.
[00257] Трансгенные растения хлопчатника (T0) с единственной копией трансгенной ДНК (SEQ ID NO: 2-201D1) были впоследствии отобраны для последующих экспериментов. Семена растений Т0 выращивали для получения потомства поколений от Т1 до Т4.
Пример 6: Биохимические анализы предполагаемых трансгенных растений хлопчатника (T0) с помощью ELISA
[00258] Сэндвич-ELISA, проводимый с использованием набора EnviroLogix Quantiplate (EnviroLogix Inc., США), осуществляли в соответствии с инструкциями производителя для количественной оценки белка Cry2Ai (SEQ ID NO: 1) в предполагаемых трансгенных ПЦР-позитивных растениях хлопчатника (последовательность ДНК 201D1 - SEQ ID NO 1). В качестве эталона использовали позитивный и негативный контроли, представленные вместе с набором. Для этого эксперимента использовали второй настоящий лист предполагаемого трансгенного растения хлопчатника. Приблизительно 30 мг ткани листа гомогенизировали в 500 мкл буфера для экстракции и центрифугировали при 6000 об/мин при 4°C в течение 7 минут, и супернатант использовали для анализа. Супернатант (100 мкл) загружали в планшет, предварительно покрытый антителом против белка Cry2Ai. Планшет покрывали парафильмом и инкубировали при комнатной температуре (24±2°C) в течение 15 минут. В каждую лунку добавляли конъюгат фермента (100 мкл). Через один час, лунки тщательно промывали промывочным буфером 1×. В каждую лунку добавляли субстрат (100 мкл) и инкубировали в течение 30 минут. Реакцию прекращали добавлением блокирующего раствора (0,1 н соляной кислоты). Оптическую плотность (ОП) культуры планшета определяли на 450 нм с использованием негативного контроля. Эксперимент проводили дважды для каждого образца, и каждая лунка рассматривалась как лунка с репликацией.
[00259] Был построен график по данным оптических плотностей и различных концентраций калибраторов (поставляемых с набором). Концентрацию белка Cry2Ai (SEQ ID NO: 1) определяли путем нанесения его значения OП против соответствующего уровня концентрации на графике. Концентрацию вычисляли как описано ниже.

[00260] Количество белка Cry2Ai (SEQ ID NO: 1), присутствующего в образцах, выражали в микрограммах на грамм свежей ткани листа. Из 15 ПЦР-позитивных растений хлопчатника (T0), скринированных с помощью набора для проведения количественного ELISA Cry2Ai, все растения оказались позитивными по экспрессии белка Cry2Ai (SEQ ID NO: 1) в ткани молодых листьев трансгенного хлопчатника.
[00261] Оценка результатов ELISA, систематизированных в Таблице 1, дала неожиданное и удивительные данные, указывающие на то, что большинство трансгенных растений хлопчатника, несущих конструкции, содержащие ДНК 201D1, экспрессировали белок Cry2Ai (SEQ ID NO: 1) в диапазоне от 10 мкг/г до 20 мкг/г свежей ткани листьев во время вегетативной стадии у разных поколений, и неожиданно стабильную экспрессию белка в последующих поколениях трансгенных растений, и при этом, не наблюдалось значительных различий между поколениями (T1-T4). Хотя было обнаружено, что экспрессия белка Cry1Ac составляет от 5 мкг/г до 10 мкг/г свежей ткани листа во время вегетативной стадии у разных поколений, однако, такая экспрессия не показывала значительных различий между поколениями (T1-T4). Таким образом, оптимизированные по кодонам синтетические последовательности ДНК, кодирующие белок Cry2Ai, обнаруживали значительное усиление экспрессии белка в трансгенных растениях по сравнению с обычными растениями.
[00262] Хотя вышеизложенное изобретение было подробно описано с помощью иллюстраций и примеров, используемых для лучшего понимания изобретения, однако, будет очевидно, что в него могут быть внесены определенные изменения и модификации, не выходящие за рамки объема настоящего изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> DCM SHRIRAM LIMITED
<120> ПОСЛЕДОВАТЕЛЬНОСТИ СИНТЕТИЧЕСКИХ НУКЛЕОТИДОВ, КОДИРУЮЩИХ
ИНСЕКТИЦИДНЫЙ КРИСТАЛЛИЧЕСКИЙ БЕЛОК И ИХ ПРИМЕНЕНИЯ
<130> PD034766IN-SC
<160> 10
<170> PatentIn version 3.5
<210> 1
<211> 633
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> аминокислотная последовательность белка Cry2Ai (NCBI GenBank:
ACV97158.1)
<400> 1
Met Asn Asn Val Leu Asn Ser Gly Arg Asn Ile Thr Cys His Ala His
1 5 10 15
Asn Val Val Ala His Asp Pro Phe Ser Phe Glu His Lys Ser Leu Asn
20 25 30
Thr Ile Glu Lys Glu Trp Lys Glu Trp Lys Arg Thr Asp His Ser Leu
35 40 45
Tyr Val Ala Pro Ile Val Gly Thr Val Gly Ser Phe Leu Leu Lys Lys
50 55 60
Val Gly Ser Leu Val Gly Lys Arg Ile Leu Ser Glu Leu Gln Asn Leu
65 70 75 80
Ile Phe Pro Ser Gly Ser Ile Asp Leu Met Gln Glu Ile Leu Arg Ala
85 90 95
Thr Glu Gln Phe Ile Asn Gln Arg Leu Asn Ala Asp Thr Leu Gly Arg
100 105 110
Val Asn Ala Glu Leu Ala Gly Leu Gln Ala Asn Val Ala Glu Phe Asn
115 120 125
Arg Gln Val Asp Asn Phe Leu Asn Pro Asn Gln Asn Pro Val Pro Leu
130 135 140
Ala Ile Ile Asp Ser Val Asn Thr Leu Gln Gln Leu Phe Leu Ser Arg
145 150 155 160
Leu Pro Gln Phe Gln Ile Gln Gly Tyr Gln Leu Leu Leu Leu Pro Leu
165 170 175
Phe Ala Gln Ala Ala Asn Leu His Leu Ser Phe Ile Arg Asp Val Ile
180 185 190
Leu Asn Ala Asp Glu Trp Gly Ile Ser Ala Ala Thr Val Arg Thr Tyr
195 200 205
Arg Asp His Leu Arg Asn Phe Thr Arg Asp Tyr Ser Asn Tyr Cys Ile
210 215 220
Asn Thr Tyr Gln Thr Ala Phe Arg Gly Leu Asn Thr Arg Leu His Asp
225 230 235 240
Met Leu Glu Phe Arg Thr Tyr Met Phe Leu Asn Val Phe Glu Tyr Val
245 250 255
Ser Ile Trp Ser Leu Phe Lys Tyr Gln Ser Leu Met Val Ser Ser Gly
260 265 270
Ala Asn Leu Tyr Ala Ser Gly Ser Gly Pro Gln Gln Thr Gln Ser Phe
275 280 285
Thr Ala Gln Asn Trp Pro Phe Leu Tyr Ser Leu Phe Gln Val Asn Ser
290 295 300
Asn Tyr Ile Leu Ser Gly Ile Ser Gly Thr Arg Leu Ser Ile Thr Phe
305 310 315 320
Pro Asn Ile Gly Gly Leu Pro Gly Ser Thr Thr Thr His Ser Leu Asn
325 330 335
Ser Ala Arg Val Asn Tyr Ser Gly Gly Val Ser Ser Gly Leu Ile Gly
340 345 350
Ala Thr Asn Leu Asn His Asn Phe Asn Cys Ser Thr Val Leu Pro Pro
355 360 365
Leu Ser Thr Pro Phe Val Arg Ser Trp Leu Asp Ser Gly Thr Asp Arg
370 375 380
Glu Gly Val Ala Thr Ser Thr Asn Trp Gln Thr Glu Ser Phe Gln Thr
385 390 395 400
Thr Leu Ser Leu Arg Cys Gly Ala Phe Ser Ala Arg Gly Asn Ser Asn
405 410 415
Tyr Phe Pro Asp Tyr Phe Ile Arg Asn Ile Ser Gly Val Pro Leu Val
420 425 430
Ile Arg Asn Glu Asp Leu Thr Arg Pro Leu His Tyr Asn Gln Ile Arg
435 440 445
Asn Ile Glu Ser Pro Ser Gly Thr Pro Gly Gly Ala Arg Ala Tyr Leu
450 455 460
Val Ser Val His Asn Arg Lys Asn Asn Ile Tyr Ala Ala Asn Glu Tyr
465 470 475 480
Gly Thr Met Ile His Leu Ala Pro Glu Asp Tyr Thr Gly Phe Thr Ile
485 490 495
Ser Pro Ile His Ala Thr Gln Val Asn Asn Gln Thr Arg Thr Phe Ile
500 505 510
Ser Glu Lys Phe Gly Asn Gln Gly Asp Ser Leu Arg Phe Glu Gln Ser
515 520 525
Asn Thr Thr Ala Arg Tyr Thr Leu Arg Gly Asn Gly Asn Ser Tyr Asn
530 535 540
Leu Tyr Leu Arg Ala Ser Ser Ile Gly Asn Ser Thr Ile Arg Val Thr
545 550 555 560
Ile Asn Gly Arg Ala Tyr Thr Val Ser Asn Val Asn Thr Thr Thr Asn
565 570 575
Asn Asp Gly Val Asn Asp Asn Gly Ala Arg Phe Ser Asp Ile Asn Ile
580 585 590
Gly Asn Ile Val Ala Ser Asp Asn Thr Asn Val Thr Leu Asp Ile Asn
595 600 605
Val Thr Leu Asn Ser Gly Thr Pro Phe Asp Leu Met Asn Ile Met Phe
610 615 620
Val Pro Thr Asn Leu Pro Pro Leu Tyr
625 630
<210> 2
<211> 1944
<212> ДНК
<213> Искусственная последовательность
<220>
<223> 201D1
<400> 2
tctagaccat ggggatccat gaataatgtt cttaactctg gaaggaatat tacctgccat 60
gcacataatg ttgttgcaca tgacccattc agttttgaac ataagagtct aaacactata 120
gaaaaagagt ggaaggagtg gaaaaggaca gatcattctc tatacgtagc tccaatcgtg 180
gggactgtgg gttcttttct attaaagaag gtaggttcct tagtgggtaa gagaatactg 240
tctgaacttc aaaatctgat cttcccatct ggtagtattg acctgatgca ggaaatactt 300
cgtgctactg agcaattcat taaccaacgt ttgaatgctg atacacttgg tagggtaaat 360
gccgaactcg ctggattgca ggccaatgtt gctgagttta acaggcaagt ggataacttt 420
ttaaacccta accaaaatcc agtcccactt gctattattg attccgtcaa cacattacag 480
cagttattcc tttcacgact gcctcaattc caaatccagg ggtatcaact cctactattg 540
ccgctattcg ctcaagccgc taacttgcac ctgagtttta tcagagatgt tattttgaat 600
gcagacgaat gggggatttc agccgcaact gtgagaactt atagagatca tctacgtaac 660
tttacaagag attactctaa ctactgtatt aacacatatc aaacagcttt tagaggcttg 720
aacactaggc ttcacgatat gcttgagttt aggacataca tgtttttgaa cgttttcgag 780
tatgttagta tttggtcact atttaagtat caatccctta tggtatcctc tggagcaaac 840
ctatacgcct ccggttcagg cccccaacaa acccaatcct ttacagcaca gaactggcca 900
tttttgtatt cattgtttca agtgaactct aattacattc tctcaggtat tagcggtaca 960
agactttcta ttacattccc caatatagga ggactcccag gttcaacaac aactcattca 1020
ttgaacagtg caagggttaa ctattctggc ggagtcagtt caggtcttat tggcgcaaca 1080
aatcttaatc acaatttcaa ctgttcaacc gtgttaccac cgttaagcac accattcgta 1140
aggagttggt tagactcagg gacagataga gaaggagtcg caacatcaac gaattggcag 1200
actgagtctt tccaaacaac tctttcactt aggtgtggag cctttagcgc tagggggaac 1260
agcaactatt ttcctgacta ctttataaga aacatatcag gtgtcccatt ggttattagg 1320
aacgaggatt taacaaggcc cctacattac aaccagataa gaaatattga gtcaccgtcc 1380
ggtactccag gtggtgctag ggcttattta gtgagcgtgc ataataggaa gaataacatt 1440
tacgccgcaa acgaatatgg aactatgata catcttgctc cggaggatta taccgggttt 1500
accattagtc caatccacgc aacacaagtg aataatcaga caaggacttt tatatctgaa 1560
aaattcggca atcaaggaga ttctcttagg tttgagcaat ctaacacgac cgctcgttac 1620
acccttcgtg gcaacggaaa tagctacaat ttgtatctcc gtgcttcatc tatcgggaac 1680
tcaactattc gtgttacaat caatggtaga gcatacaccg ttagtaatgt aaatacaact 1740
actaacaatg atggcgtaaa tgataatgga gcaaggttca gcgacataaa catagggaac 1800
attgtcgcaa gtgacaacac taacgttacc ttggatataa atgttacatt aaactccggc 1860
actccttttg acttgatgaa tattatgttc gtaccaacta atctcccacc gctgtatccc 1920
gggtgagaat tcaagcttga gctc 1944
<210> 3
<211> 1944
<212> ДНК
<213> Искусственная последовательность
<220>
<223> 201D2
<400> 3
tctagaccat ggggatccat gaataatgtt ttgaattctg gaagaaatat tacttgtcat 60
gctcataatg ttgttgctca tgatcctttt tcttttgaac ataagtcttt gaatactatt 120
gaaaaggaat ggaaggaatg gaagagaact gatcattctt tgtatgttgc tcctattgtt 180
ggaactgttg gatctttttt gttgaagaag gttggatctt tggttggaaa gagaattttg 240
tctgaattgc aaaatctgat cttcccatct ggtagtattg acctgatgca ggaaatactt 300
cgtgctactg agcaattcat taaccaacgt ttgaatgctg atacacttgg tagggtaaat 360
gccgaactcg ctggattgca ggccaatgtt gctgagttta acaggcaagt ggataacttt 420
ttaaacccta accaaaatcc agtcccactt gctattattg attctgtcaa cacattacag 480
cagttattcc tttcaagact gcctcaattc caaatccagg ggtatcaact cctactattg 540
ccgctattcg ctcaagctgc taacttgcac ctgagtttta tcagagatgt tattttgaat 600
gcagacgaat gggggatttc agctgcaact gtgagaactt atagagatca tctacgtaac 660
tttacaagag attactctaa ctactgtatt aacacatatc aaacagcttt tagaggattg 720
aacactaggc ttcacgatat gcttgagttt aggacataca tgtttttgaa cgttttcgag 780
tatgttagta tttggtcact atttaagtat caatctctta tggtatcttc tggagcaaac 840
ctatacgctt ctggttcagg acctcaacaa acccaatctt ttacagcaca gaactggcca 900
tttttgtatt cattgtttca agtgaactct aattacattc tctcaggtat tagcggtaca 960
agactttcta ttacattccc taatatagga ggactcccag gttcaacaac aactcattca 1020
ttgaacagtg caagggttaa ctattctgga ggagtcagtt caggtcttat tggagcaaca 1080
aatcttaatc acaatttcaa ctgttcaacc gtgttaccac cgttaagcac accattcgta 1140
aggagttggt tagactcagg gacagataga gaaggagtcg caacatcaac gaattggcag 1200
actgagtctt tccaaacaac tctttcactt aggtgtggag cttttagcgc tagggggaac 1260
agcaactatt ttcctgacta ctttataaga aacatatcag gtgtcccatt ggttattagg 1320
aacgaggatt taacaaggcc tctacattac aaccagataa gaaatattga gtcaccgtct 1380
ggtactccag gtggtgctag ggcttattta gtgagcgtgc ataataggaa gaataacatt 1440
tacgctgcaa acgaatatgg aactatgata catcttgctc cggaggatta taccgggttt 1500
accattagtc caatccacgc aacacaagtg aataatcaga caaggacttt tatatctgaa 1560
aaattcggca atcaaggaga ttctcttagg tttgagcaat ctaacacgac cgctcgttac 1620
acccttcgtg gaaatggaaa ttcttataat ttgtatttga gagcttcttc tattggaaat 1680
tctactatta gagttactat taatggaaga gcttatactg tttctaatgt taatactact 1740
actaataatg atggagttaa tgataatgga gctagatttt ctgatattaa tattggaaat 1800
attgttgctt ctgataatac taatgttact ttggatatta atgttacttt gaattctgga 1860
actccttttg atttgatgaa tattatgttt gttcctacta atttgcctcc tttgtatcct 1920
ggataagaat tcaagcttga gctc 1944
<210> 4
<211> 1944
<212> ДНК
<213> Искусственная последовательность
<220>
<223> 201D3
<400> 4
tctagaccat ggggatccat gaataatgtt ttaaactctg gtcgtaacat tacatgtcat 60
gcacataacg tagtagcaca tgatccattc tctttcgaac ataaatcttt aaacacaatt 120
gaaaaagaat ggaaagaatg gaaacgtaca gatcattctt tatacgtagc accaattgta 180
ggtacagtag gttctttctt attaaaaaaa gtaggttctt tagtaggtaa acgtatttta 240
tctgaattac aaaacttaat tttcccatct ggtagtattg acctgatgca ggaaatactt 300
cgtgctactg agcaattcat taaccaacgt ttgaatgctg atacacttgg tagggtaaat 360
gccgaactcg ctggattgca ggccaatgtt gctgagttta accgtcaagt agataacttt 420
ttaaacccta accaaaatcc agtaccactt gctattattg attctgtaaa cacattacaa 480
caattattcc tttcacgttt acctcaattc caaatccaag gttatcaatt actactatta 540
ccactattcg ctcaagcagc taacttacac ttaagtttta tccgtgatgt tattttaaat 600
gcagacgaat ggggtatttc agcagcaact gtacgtactt atcgtgatca tctacgtaac 660
tttacacgtg attactctaa ctactgtatt aacacatatc aaacagcttt tcgtggctta 720
aacactcgtc ttcacgatat gcttgagttt cgtacataca tgtttttaaa cgttttcgag 780
tatgttagta tttggtcact atttaagtat caatctctta tggtatcttc tggagcaaac 840
ctatacgcat ctggttcagg cccacaacaa acacaatctt ttacagcaca aaactggcca 900
tttttatatt cattatttca agtaaactct aattacattt tatcaggtat tagcggtaca 960
cgtctttcta ttacattccc aaatattgga ggattaccag gttcaacaac aactcattca 1020
ttaaacagtg cacgtgttaa ctattctggc ggagtaagtt caggtcttat tggcgcaaca 1080
aatcttaatc acaatttcaa ctgttcaaca gtattaccac cattaagcac accattcgta 1140
cgtagttggt tagactcagg tacagatcgt gaaggagtag caacatcaac gaattggcaa 1200
actgagtctt tccaaacaac tctttcactt cgttgtggag catttagcgc tcgtggtaac 1260
agcaactatt ttcctgacta ctttattcgt aacatttcag gtgtaccatt agttattcgt 1320
aacgaggatt taacacgtcc actacattac aaccaaattc gtaatattga gtcaccatct 1380
ggtactccag gtggtgctcg tgcttattta gtaagcgtac ataatcgtaa gaataacatt 1440
tacgcagcaa acgaatatgg aactatgata catcttgctc cggaggatta taccgggttt 1500
accattagtc caatccacgc aacacaagtg aataatcaga caaggacttt tatatctgaa 1560
aaattcggca atcaaggaga ttctcttagg tttgagcaat ctaacacgac cgctcgttac 1620
acccttcgtg gtaacggtaa ctcttacaac ttatacttac gtgcatcttc tattggtaac 1680
tctacaattc gtgtaacaat taacggtcgt gcatacacag tatctaacgt aaacacaaca 1740
acaaacaacg atggtgtaaa cgataacggt gcacgtttct ctgatattaa cattggtaac 1800
attgtagcat ctgataacac aaacgtaaca ttagatatta acgtaacatt aaactctggt 1860
acaccattcg atttaatgaa cattatgttc gtaccaacaa acttaccacc attataccca 1920
ggttaagaat tcaagcttga gctc 1944
<210> 5
<211> 1944
<212> ДНК
<213> Искусственная последовательность
<220>
<223> 201D4
<400> 5
tctagaccat ggggatccat gaataatgtt ctgaacagcg gccgcaacat cacgtgccat 60
gcccataacg tcgtcgccca tgacccgttt agctttgaac ataaaagcct gaacacgatc 120
gaaaaagaat ggaaagaatg gaaacgcacg gaccatagcc tgtatgtcgc cccgatcgtc 180
ggcacggtcg gcagctttct gctgaaaaaa gtcggcagcc tggtcggcaa acgcatcctg 240
agcgaacttc aaaatctgat cttcccatct ggtagtattg acctgatgca ggaaatactt 300
cgtgctactg agcaattcat taaccaacgt ttgaatgctg atacacttgg tagggtaaat 360
gccgaactcg ctggattgca ggccaatgtt gctgagttta acaggcaagt ggataacttt 420
ttaaacccta accaaaatcc ggtcccgctt gctattattg attccgtcaa cacattacag 480
cagttattcc tttcacgcct gcctcaattc caaatccagg ggtatcaact cctgctgttg 540
ccgctgttcg ctcaagccgc taacttgcac ctgagcttta tcagagatgt tattttgaat 600
gcagacgaat gggggatttc agccgcaacg gtgagaacgt atagagatca tctgcgcaac 660
tttacaagag attactctaa ctactgtatt aacacatatc aaacagcttt tagaggcttg 720
aacacgaggc ttcacgatat gcttgagttt aggacataca tgtttttgaa cgttttcgag 780
tatgttagca tttggtcact gtttaagtat caatccctta tggtatcctc tggagcaaac 840
ctgtacgcct ccggttcagg cccgcaacaa acccaatcct ttacagcaca gaactggccg 900
tttttgtatt cattgtttca agtgaactct aattacattc tctcaggtat tagcggtaca 960
agactttcta ttacattccc gaatatcgga ggactcccgg gttcaacaac aacgcattca 1020
ttgaacagcg caagggttaa ctattctggc ggagtcagct caggtcttat tggcgcaaca 1080
aatcttaatc acaatttcaa ctgttcaacc gtgttaccgc cgttaagcac accgttcgta 1140
aggagctggt tagactcagg gacagataga gaaggagtcg caacatcaac gaattggcag 1200
acggagtctt tccaaacaac gctttcactt aggtgtggag cctttagcgc tagggggaac 1260
agcaactatt ttcctgacta ctttatcaga aacatctcag gtgtcccgtt ggttattagg 1320
aacgaggatt taacaaggcc gctgcattac aaccagatca gaaatattga gtcaccgtcc 1380
ggtacgccgg gtggtgctag ggcttattta gtgagcgtgc ataataggaa gaataacatt 1440
tacgccgcaa acgaatatgg aactatgata catcttgctc cggaggatta taccgggttt 1500
accattagtc caatccacgc aacacaagtg aataatcaga caaggacttt tatatctgaa 1560
aaattcggca atcaaggaga ttctcttagg tttgagcaat ctaacacgac cgctcgttac 1620
acccttcgtg gcaacggcaa cagctataac ctgtatctgc gcgccagcag catcggcaac 1680
agcacgatcc gcgtcacgat caacggccgc gcctatacgg tcagcaacgt caacacgacg 1740
acgaacaacg acggcgtcaa cgacaacggc gcccgcttta gcgacatcaa catcggcaac 1800
atcgtcgcca gcgacaacac gaacgtcacg ctggacatca acgtcacgct gaacagcggc 1860
acgccgtttg acctgatgaa catcatgttt gtcccgacga acctgccgcc gctgtatccg 1920
ggctaagaat tcaagcttga gctc 1944
<210> 6
<211> 1944
<212> ДНК
<213> Искусственная последовательность
<220>
<223> 201D5
<400> 6
tctagaccat ggggatccat gaataatgtt ctgaactctg gtcgtaacat cacttgtcac 60
gctcacaacg tagtagctca cgatccgttc tctttcgaac acaaatctct gaacactatc 120
gaaaaagaat ggaaagaatg gaaacgtact gatcactctc tgtacgtagc tccgatcgta 180
ggtactgtag gttctttcct gctgaaaaaa gtaggttctc tggtaggtaa acgtatcctg 240
tctgaactgc aaaatctgat cttcccatct ggtagtattg acctgatgca ggaaatactt 300
cgtgctactg agcaattcat taaccaacgt ttgaatgctg atacacttgg tagggtaaat 360
gccgaactcg ctggattgca ggccaatgtt gctgagttta accgtcaagt ggataacttt 420
ttaaacccta accaaaatcc ggtaccgctt gctattattg attctgtaaa cacattacag 480
cagttattcc tttcacgtct gcctcaattc caaatccagg gttatcaact cctgctgttg 540
ccgctgttcg ctcaagccgc taacttgcac ctgagtttta tcagagatgt tattttgaat 600
gcagacgaat ggggtatttc agccgcaact gtgagaactt atagagatca tctgcgtaac 660
tttacaagag attactctaa ctactgtatt aacacatatc aaacagcttt tagaggcttg 720
aacactcgtc ttcacgatat gcttgagttt cgtacataca tgtttttgaa cgttttcgag 780
tatgttagta tttggtcact gtttaagtat caatctctta tggtatcttc tggagcaaac 840
ctgtacgcct ctggttcagg cccccaacaa acccaatctt ttacagcaca gaactggccg 900
tttttgtatt cattgtttca agtgaactct aattacattc tctcaggtat tagcggtaca 960
agactttcta ttacattccc caatatcgga ggactcccgg gttcaacaac aactcattca 1020
ttgaacagtg cacgtgttaa ctattctggc ggagtaagtt caggtcttat tggcgcaaca 1080
aatcttaatc acaatttcaa ctgttcaacc gtgttaccgc cgttaagcac accgttcgta 1140
cgtagttggt tagactcagg tacagataga gaaggagtag caacatcaac taattggcag 1200
actgagtctt tccaaacaac tctttcactt cgttgtggag cctttagcgc tcgtggtaac 1260
agcaactatt ttcctgacta ctttatcaga aacatctcag gtgtaccgtt ggttattcgt 1320
aacgaggatt taacacgtcc cctgcattac aaccagatca gaaatattga gtcaccgtct 1380
ggtactccgg gtggtgctcg tgcttattta gtgagcgtgc ataatcgtaa gaataacatt 1440
tacgccgcaa acgaatatgg aactatgatc catcttgctc cggaggatta taccgggttt 1500
accattagtc caatccacgc aacacaagtg aataatcaga caaggacttt tatatctgaa 1560
aaattcggca atcaaggaga ttctcttagg tttgagcaat ctaacacgac cgctcgttac 1620
acccttcgtg gtaacggtaa ctcttacaac ctgtacctgc gtgcttcttc tatcggtaac 1680
tctactatcc gtgtaactat caacggtcgt gcttacactg tatctaacgt aaacactact 1740
actaacaacg atggtgtaaa cgataacggt gctcgtttct ctgatatcaa catcggtaac 1800
atcgtagctt ctgataacac taacgtaact ctggatatca acgtaactct gaactctggt 1860
actccgttcg atctgatgaa catcatgttc gtaccgacta acctgccgcc gctgtacccg 1920
ggttaagaat tcaagcttga gctc 1944
<210> 7
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> представляет собой последовательность прямого праймера
для амплификации последовательности ДНК 201D1 (SEQ ID NO: 2)
<400> 7
ctccaatcgt ggggactgtg 20
<210> 8
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> представляет собой последовательность обратного праймера
для амплификации последовательности ДНК 201D1 (SEQ ID NO: 2)
<400> 8
cccgatagat gaagcacgga 20
<210> 9
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> представляет собой последовательность прямого праймера
для амплификации последовательности ДНК гена nptii
<400> 9
acgaggaagc ggtcagccca 20
<210> 10
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> представляет собой последовательность обратного праймера
для амплификации последовательности ДНК гена nptII
<400> 10
ttgcacgcag gttctccggc 20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОДОН-ОПТИМИЗИРОВАННЫЕ СИНТЕТИЧЕСКИЕ НУКЛЕОТИДНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ, КОДИРУЮЩИЕ БЕЛОК Cry2Ai, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2799821C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2017 |
|
RU2765722C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2017 |
|
RU2765304C2 |
| ИНСЕКТИЦИДНЫЕ ПОЛИПЕПТИДЫ С ШИРОКИМ СПЕКТРОМ АКТИВНОСТИ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2750459C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2015 |
|
RU2745322C2 |
| СКОНСТРУИРОВАННЫЕ ПЕСТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2017 |
|
RU2817591C2 |
| СКОНСТРУИРОВАННЫЕ ПЕСТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2017 |
|
RU2816526C2 |
| КОМПОЗИЦИИ И СПОСОБЫ КОНТРОЛЯ ВРЕДИТЕЛЕЙ РАСТЕНИЙ | 2015 |
|
RU2741833C2 |
| ГЕН АХМ1554, КОДИРУЮЩИЙ ДЕЛЬТА-ЭНДОТОКСИН, И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2755282C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ | 2019 |
|
RU2810220C2 |
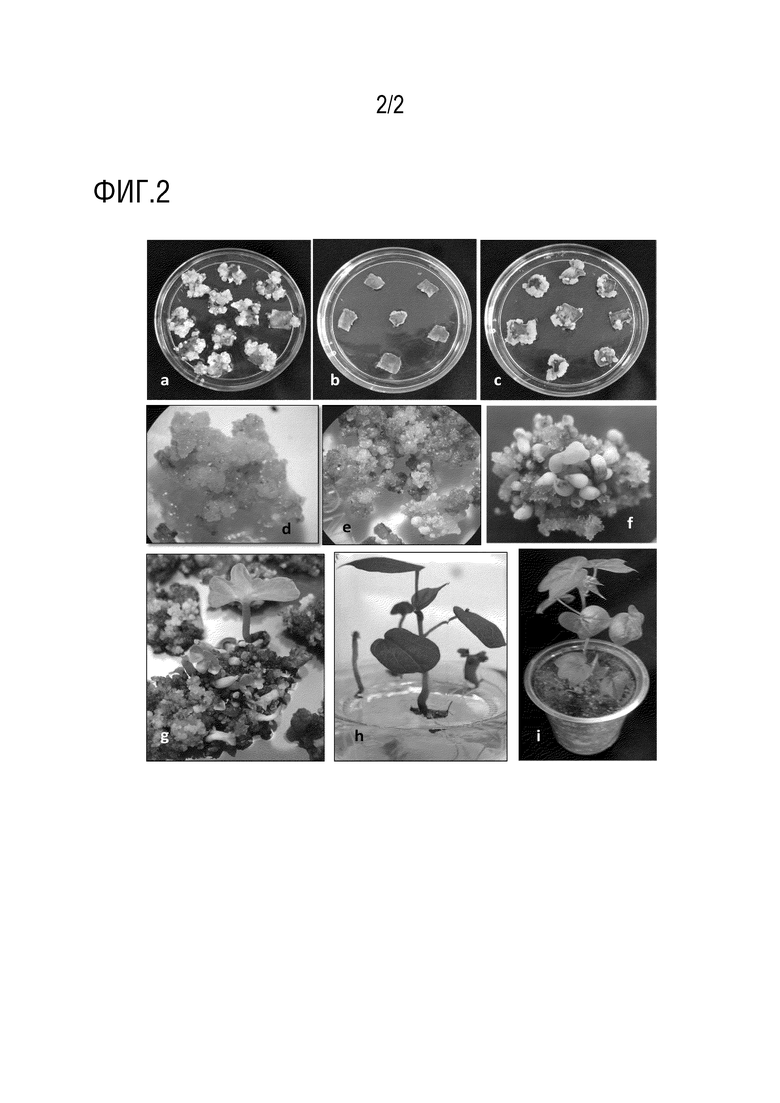
Изобретение относится к области биохимии, в частности к молекуле нуклеиновой кислоты, обладающей инсектицидной активностью. Также раскрыты конструкция ДНК, плазмидный вектор, клетка-хозяин, трансгенное растение, семя, продукт потребления, содержащие указанную молекулу нуклеиновой кислоты. Изобретение позволяет эффективно бороться с насекомыми-вредителями. 9 н. и 6 з.п. ф-лы, 2 ил., 1 табл., 1 пр.
1. Молекула нуклеиновой кислоты, обладающая инсектицидной активностью против насекомых-вредителей, содержащая оптимизированную по кодонам синтетическую нуклеотидную последовательность, кодирующую белок с аминокислотной последовательностью, представленной в SEQ ID NO: 1, где нуклеотидная последовательность выбрана из группы, состоящей из последовательности, представленной в SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
2. Рекомбинантная ДНК, кодирующая белок Cry2Ai, содержащая молекулу нуклеиновой кислоты по п. 1, где оптимизированная по кодонам синтетическая нуклеотидная последовательность функционально связана с гетерологичным регуляторным элементом.
3. Рекомбинантная ДНК по п. 2, где указанная оптимизированная по кодонам синтетическая нуклеотидная последовательность включает, но необязательно, селективный маркерный ген, ген-репортер или их комбинацию.
4. Рекомбинантная ДНК по п. 2, где указанная оптимизированная по кодонам синтетическая нуклеотидная последовательность содержит, но необязательно, последовательность ДНК, кодирующую нацеливающий или транспортный пептид для нацеливания на вакуоль, митохондрию, хлоропласт, пластиду, или для секреции.
5. Конструкция ДНК для экспрессии инсектицидного белка в растении, содержащая 5'-нетранслируемую последовательность, кодирующую последовательность, кодирующую инсектицидный белок Cry2Ai, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее инсектицидную часть, и 3'-нетранслируемую область, где указанная 5'-нетранслируемая последовательность включает промотор, функциональный в клетке растения; указанная кодирующая последовательность представляет собой последовательность молекулы нуклеиновой кислоты по п. 1, а указанная 3'-нетранслируемая последовательность содержит последовательность терминации транскрипции и сигнал полиаденилирования.
6. Плазмидный вектор для экспрессии белка Cry2Ai в растениях, содержащий молекулу нуклеиновой кислоты по п. 1.
7. Клетка-хозяин для экспрессии белка Cry2Ai в растениях, содержащая молекулу нуклеиновой кислоты по п. 1.
8. Клетка-хозяин по п. 7, где указанная клетка-хозяин представляет собой клетку растения, бактериальную клетку, вирус-содержащую клетку, клетку грибов или дрожжевую клетку.
9. Клетка-хозяин по п. 8, где указанной бактериальной клеткой является Agrobacterium или E. coli.
10. Трансгенное растение, устойчивое к насекомым-вредителям, содержащее молекулу нуклеиновой кислоты по п. 1.
11. Трансгенное растение по п. 10, где указанное растение выбрано из группы, состоящей из риса, пшеницы, кукурузы, сорго, овса, проса, бобовых, хлопчатника, томатов, баклажанов, капусты, цветной капусты, брокколи, Brassica sp., фасоли, гороха, голубиного гороха, картофеля, перца, тыквы, салата-латука, сладкого картофеля, канолы, сои, люцерны, арахиса, подсолнечника, сафлора, табака, сахарного тростника, маниоки, кофе, ананаса, цитрусовых, какао, чая, банана и дыни.
12. Ткань, устойчивая к насекомым-вредителям, полученная от трансгенного растения по п. 10, где указанная ткань содержит молекулу нуклеиновой кислоты по п. 1.
13. Семя, устойчивое к насекомым-вредителям, полученное от трансгенного растения по п. 10, где указанное семя содержит молекулу нуклеиновой кислоты по п. 1.
14. Биологический образец, устойчивый к насекомым-вредителям, полученный из ткани по п. 12 или семени по п. 13, где указанный образец содержит детектируемое количество указанной молекулы нуклеиновой кислоты по п. 1.
15. Продукт потребления, полученный из трансгенного растения по п. 10, где указанный продукт содержит детектируемое количество указанной молекулы нуклеиновой кислоты по п. 1.
| WO 2018075269 A1, 26.04.2018 | |||
| WO 2009109123 A1, 03.09.2008 | |||
| RU 2017124613 A, 15.01.2019. |
Авторы
Даты
2024-06-07—Публикация
2020-07-28—Подача