Настоящее изобретение относится к области здравоохранения. Более конкретно, изобретение относится к раствору аминодигидрофталазиндиона натрия для внутривенного введения и способу его приготовления.
Аминодигидрофталазиндион натрия является действующим веществом в составе коммерчески доступных лекарственных средств, относящихся к классу иммуномодуляторов и противовоспалительных препаратов, применяемых для лечения язвенной болезни желудка и 12-перстной кишки; вирусных гепатитов; хронических рецидивирующих заболеваний, вызванных вирусом герпеса; заболеваний, вызванных вирусом папилломы человека; инфекционно-воспалительных урогенитальных заболеваний, таких как уретрит хламидийной и трихомонадной этиологии, хламидийный простатит, острый и хронический сальпингоофорит, эндометрит; гнойно-воспалительных заболеваний органов малого таза; послеоперационной реабилитации больных с миомой матки; осложнений послеоперационного периода у женщин репродуктивного возраста; послеоперационныз гнойно-септическиз осложнений и их профилактики; хронического рецидивирующего фурункулеза и рожи; стенических состояний, невротических и соматоформных расстройств, снижения физической работоспособности; психических, поведенческих и постабстинентных расстройств при алкогольной и наркотической зависимости; воспалительных заболеваний слизистой оболочки полости рта и горла, заболеваний пародонта; острых и хронических инфекционно-воспалительных заболеваний желудочно-кишечного тракта, сопровождающихся интоксикацией и/или диареей; хронических урогенитальных инфекций, в том числе при проведении иммунореабилитационных мероприятий в межрецидивный период с целью поддержания клинической ремиссии. Инструкция к применению препарата Тамерит®, реестр лекарственных средств России. https://www.rlsnet.ru/drugs/tamerit-84753.
Воспалительные заболевания, на лечение которых направлены препараты, содержащие аминодигидрофталазиндион натрия, обычно сопровождаются повышением вязкости крови, связанной с агрегацией эритроцитов в крови. Эритроциты – это высокоспециализированные клетки, осуществляющие транспорт кислорода, содержание которых в крови составляет примерно 3,9-5,5⋅1012 клеток на литр. При воспалении эритроциты образуют агрегаты в крови, что вызывает уменьшение кровотока на уровне микрососудов вплоть до полной закупорки и ведет к снижению эффективности доставки кислорода в ткани. Meiselman H.J. Biorheology. 2009; 46(1):1-19. Морозов М.А. и др. Агрегация эритроцитов: Роль в патологии и пути профилактики: пособие для врачей. М., 2010. 12 с. Поэтому, снижение агрегации эритроцитов необходимо для улучшения транспортной функции крови и снабжения тканей кислородом.
Растворы аминодигидрофталазиндиона натрия для внутримышечного введения известны из уровня техники. Инструкция к применению препарата Тамерит®, реестр лекарственных средств России. https://www.rlsnet.ru/drugs/tamerit-84753. Инструкция к применению препарата Галавит®, реестр лекарственных средств России. https://www.rlsnet.ru/drugs/galavit-691.
Однако, растворы аминодигидрофталазиндиона натрия для внутривенного введения неизвестны из уровня техники.
Авторы изобретения обнаружили, что внутривенное введение раствора аминодигидрофталазиндиона натрия имеет существенное преимущество перед внутримышечным введением, так как имеет лучший профиль безопасности и обеспечивает снижение агрегации эритроцитов у пациентов с воспалением, тогда как внутримышечное введение таким эффектом не обладает.
Настоящее изобретение относится к раствору для внутривенного введения, содержащему аминодигидрофталазиндион натрия и растворитель, выбранный из группы, состоящей из воды для инъекций и раствора 0,9 мас.% хлорида натрия в воде, при следующем соотношении ингредиентов, мг/мл:
Кроме того, настоящее изобретение относится к способу приготовления раствора для внутривенного введения настоящего изобретения, включающему растворение аминодигидрофталазиндиона натрия в растворителе, выбранном из группы, состоящей из воды для инъекций и раствора 0,9 мас.% хлорида натрия в воде.
Техническим результатом настоящего изобретения является повышение безопасности парентеральной терапии с использованием растворов аминодигидрофталазиндиона натрия, что достигается снижением среднего времени удержания препарата в крови при внутривенном введении раствора настоящего изобретения в сравнении с внутримышечным введением.
Термин «среднее время удержания» означает среднее время пребывания действующего вещества в организме, обозначаемое далее как MRT0-t. Каркищенко НН и др. Фармакокинетика, Ростов-на-Дону, 2001, 384 с.
Аминодигидрофталазиндион натрия, химическое название 5-амино-1,2,3,4-тетрагидрофталазин-1,4-диона натриевая соль, относится к классу иммуномодулирующих и противовоспалительных средств, имеет брутто-формулу C8H5Na2N3O2 и структурную формулу:
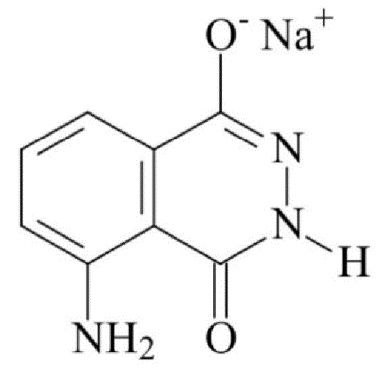
Раствор настоящего изобретения приготавливается растворением аминодигидрофталазиндиона натрия в подходящем растворителе.
Предпочтительно, раствор для внутривенного введения настоящего изобретения приготавливается смешением аминодигидрофталазиндиона натрия с растворителем, выбранным из группы, состоящей из воды для инъекций и раствора 0,9 мас.% хлорида натрия в воде, непосредственно перед введением пациенту, нуждающемуся в этом.
Термин «вода для инъекций» относится к воде, произведенной в соответствии с требованиями фармакопейной статьи ФС.2.2.0019.15 «Вода для инъекций».
Раствор 0,9 мас.% хлорида натрия в воде, представляет собой изотонический раствор, известный также как «физиологический раствор».
Введение раствора настоящего изобретения пациенту осуществляется путем внутривенной инъекций или инфузии.
Раствор настоящего изобретения может быть использован для лечения пациентов, страдающих от язвенной болезни желудка и 12-перстной кишки; вирусных гепатитов; хронических рецидивирующих заболеваний, вызванных вирусом герпеса; заболеваний, вызванных вирусом папилломы человека; инфекционно-воспалительных урогенитальных заболеваний, таких как уретрит хламидийной и трихомонадной этиологии, хламидийный простатит, острый и хронический сальпингоофорит, эндометрит; гнойно-воспалительных заболеваний органов малого таза; послеоперационной реабилитации больных с миомой матки; осложнений послеоперационного периода у женщин репродуктивного возраста; послеоперационныз гнойно-септическиз осложнений и их профилактики; хронического рецидивирующего фурункулеза и рожи; стенических состояний, невротических и соматоформных расстройств, снижения физической работоспособности; психических, поведенческих и постабстинентных расстройств при алкогольной и наркотической зависимости; воспалительных заболеваний слизистой оболочки полости рта и горла, заболеваний пародонта; острых и хронических инфекционно-воспалительных заболеваний желудочно-кишечного тракта, сопровождающихся интоксикацией и/или диареей; хронических урогенитальных инфекций, в том числе при проведении иммунореабилитационных мероприятий в межрецидивный период с целью поддержания клинической ремиссии.
Количество раствора настоящего изобретения, вводимого пациенту, нуждающемуся в этом, устанавливается практикующим врачом и может обеспечить введение аминодигидрофталазиндиона натрия в количестве от 25 до 1000 мг.
Кроме того, настоящее изобретение относится к способу снижения агрегации эритроцитов, включающему внутривенное введение раствора настоящего изобретения субъекту, нуждающемуся в этом. Техническим результатом настоящего изобретения при этом является снижение агрегации эритроцитов в крови, что достигается внутривенным введением раствора настоящего изобретения субъекту, нуждающемуся в этом.
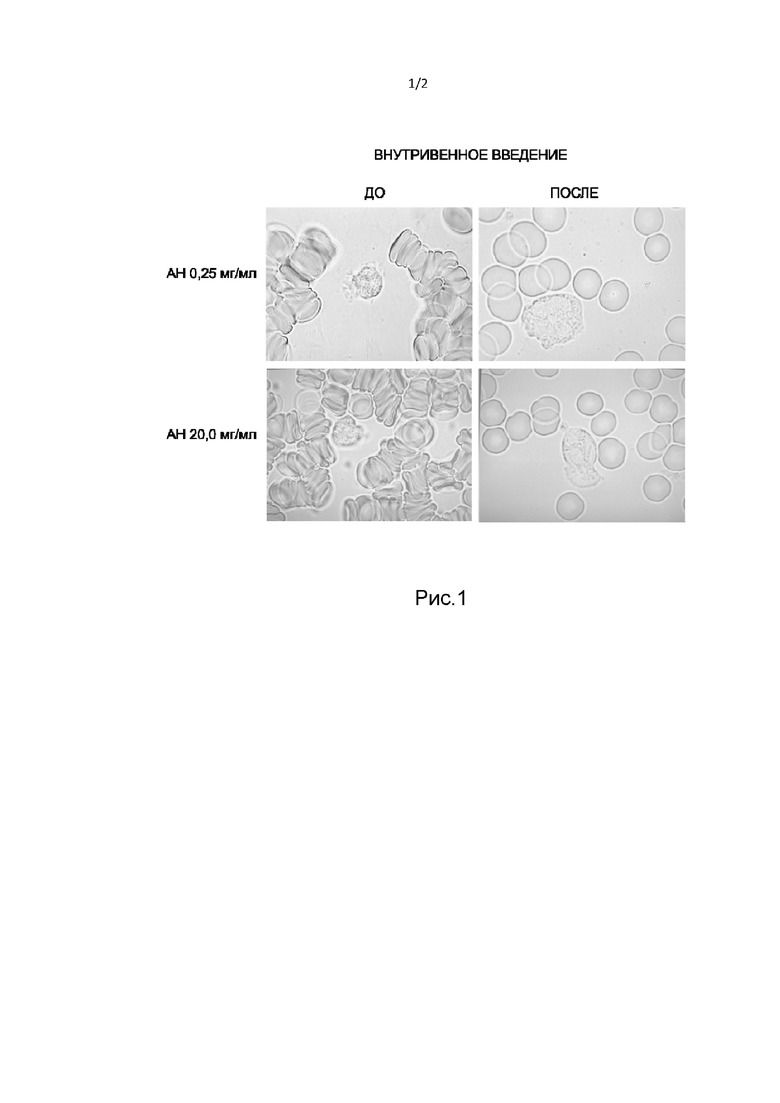
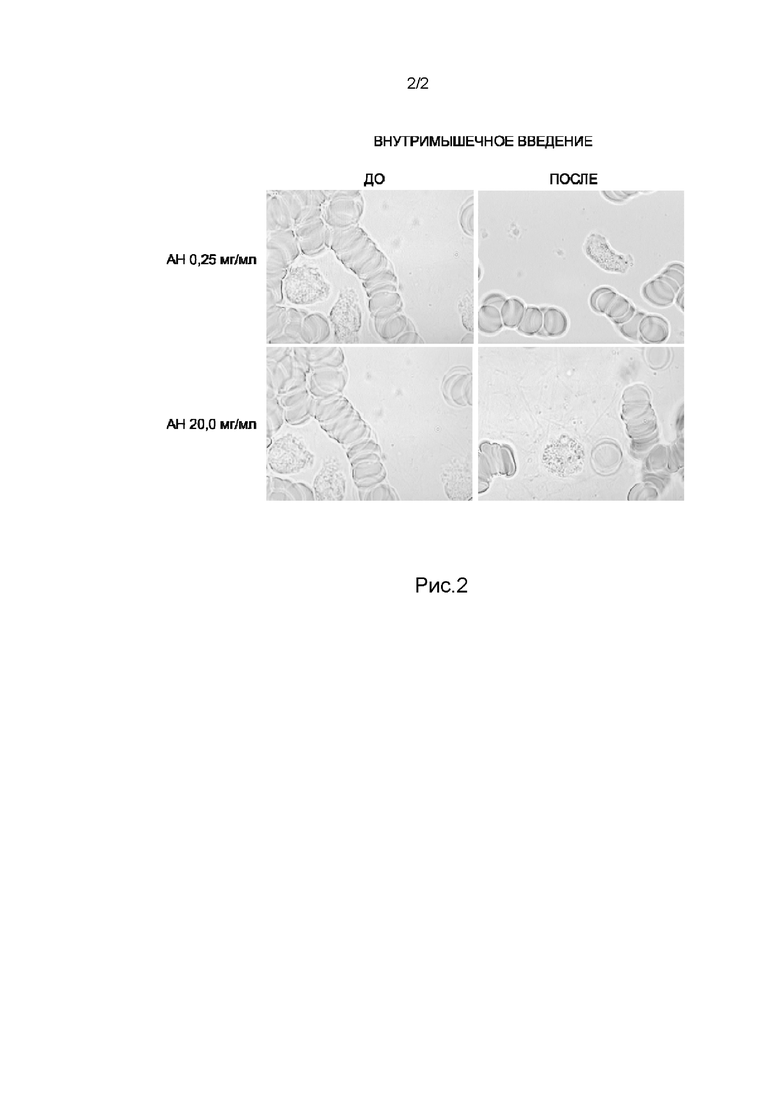
На рис. 1 показан репрезентативный пример фотомикроскопии крови до и после в/в введения препарата в указанных концентрациях, на рис. 2 - репрезентативный пример фотомикроскопии крови до и после в/м введения препарата в указанных концентрациях.
Следующие примеры имеют иллюстративное значение и не предназначены для ограничения объема изобретения.
Пример 1.
Таблица 1 показывает состав раствора для внутривенного введения, приготовленного растворением аминодигидрофталазиндиона натрия (АН) в воде для инъекций (вода).
Таблица 1. Состав раствора для внутривенного введения.
Для приготовления раствора для внутривенного введения аминодигидрофталазиндион натрия (АН) растворяют в воде для инъекций (вода) в пропорциях, как указано в таблице 1. Полученный раствор стерильно переносят во флакон/пакет для проведения внутривенной инфузии пациенту, нуждающемуся в этом.
Пример 2.
Таблица 2 показывает состав раствора для внутривенного введения, приготовленного растворением аминодигидрофталазиндиона натрия (АН) в физиологическом растворе (физ. раствор).
Таблица 2. Состав раствора для внутривенного введения.
Для приготовления раствора для внутривенного введения аминодигидрофталазиндион натрия (АН) растворяют в физиологическом растворе (физ. раствор) в пропорциях, как указано в таблице 2. Полученный раствор стерильно переносят во флакон/пакет для проведения внутривенной инфузии пациенту, нуждающемуся в этом.
Пример 3.
Фармакокинетические исследования растворов для парентерального введения аминодигидрофталазиндиона натрия (АН), полученных растворением АН в воде для инъекций, проводили на кроликах при однократном внутривенном (в/в) и внутримышечном (в/м) введениях АН в дозе 9,1 мг/кг в виде растворов с разной концентрацией. Для этого животных рандомизировали в восемь групп (n=6). В первой группе животные получали в/в инъекцию раствора АН 0,25 мг/мл (раствор №1, пример 1); во второй в/в инъекцию раствора АН 1,0 мг/мл (раствор №2, пример 1); в третьей в/в инъекцию раствора АН 5,0 мг/мл (раствор №3, пример 1); в четвертой в/в инъекцию раствора АН 20,0 мг/мл (раствор №4, пример 1); в пятой в/м инъекцию раствора АН 0,25 мг/мл (раствор №1, пример 1); в шестой в/м инъекцию раствора АН 1,0 мг/мл (раствор №2, пример 1); в седьмой в/м инъекцию раствора АН 5,0 мг/мл (раствор №3, пример 1); в восьмой в/м инъекцию раствора АН 20,0 мг/мл (раствор №4, пример 1), после чего измеряли концентрации АН в крови во времени и определяли среднее время удерживания (MRT0-t) АН в организме. Результаты представлены в таблице 3 как среднее ± стандартное отклонение MRT0-t.
Таблица 3. Среднее время удержания АН в организме (MRT0-t)
*Статистически значимое отличие от внутримышечного введения (p<0,05).
Таблица 3 показывает, что среднее время удержания АН в крови существенно ниже (примерно на 45 мин) при внутривенном введении по сравнению с внутримышечным введением, что свидетельствует о большей безопасности раствора для внутривенного введения настоящего изобретения в сравнении с внутримышечным введением при той же дозе вводимого препарата во всем диапазоне исследованных концентраций (0,25-20,0 мг/мл).
Пример 4
Фармакокинетические исследования растворов настоящего изобретения, полученных растворением аминодигидрофталазиндиона натрия (АН) в воде для инъекций, проводили на добровольцах в ходе первой фазы клинических испытаний. Для этого добровольцев рандомизировали в три группы (n=6 в каждой). В первой группе добровольцы получали в/в инъекцию раствора АН 0,25 мг/мл (раствор №6, пример 2); во второй в/в инъекцию раствора АН 0,5 мг/мл (раствор №7, пример 2); в третьей в/в инъекцию раствора АН 1,0 мг/мл (раствор №8, пример 2), после чего измеряли концентрации АН в крови во времени и определяли среднее время удерживания (MRT0-t) действующего вещества в организме. Результаты представлены в таблице 4 как среднее ± стандартное отклонение среднего MRT0-t.
Таблица 4. Среднее время удержания АН в организме (MRT0-t)
Таблица 4 показывает, что среднее время удержания АН в крови при внутривенном введении добровольцам составляет 0,18-0,24 ч во всем диапазоне исследуемых доз, что существенно ниже среднего времени удержания АН в крови человека при внутримышечном введении 0,55-0,84 ч, известном из уровня техники (Кузнецова Е.Г. и др. Вестник трансплантологии и искусственных органов, т.23, №2, стр.114-121, г. 2021). Таким образом, раствор для внутривенного введения настоящего изобретения обеспечивает наибольшую безопасность парентеральной терапии с использованием растворов аминодигидрофталазиндиона натрия, что достигается снижением среднего времени удержания препарата в крови при внутривенном введении раствора настоящего изобретения в сравнении с внутримышечным введением.
Кроме того, для всех 18 добровольцев популяции безопасности в составе 3 когорт дозирования параметры физикального осмотра, осмотра места введения исследуемого препарата, ЭКГ в 12 отведениях, значения основных жизненно-важных показателей и лабораторных параметров крови и мочи на протяжении исследования были в пределах нормы, и не было выявлено признаков дозолимитирующей токсичности, не зарегистрировано каких-либо нежелательных явлений, не зарегистрировано случаев досрочного прекращения участия, что свидетельствует о высокой общей безопасности раствора настоящего изобретения.
Пример 5
Сравнительная эффективность раствора для внутривенного введения настоящего изобретения и раствора для внутримышечного введения сравнивалась в тесте агрегации эритроцитов. Для этого, у добровольцев проводили исследование крови под микроскопом с фото и видеофиксацией до и после введения соответствующих растворов.
У всех добровольцев (n=10), получавших внутривенно аминодигидрофталазиндион натрия (АН) в дозе 100 мг в виде растворов с концентрацией 0,25 и 20,0 мг/мл (растворы №№6 и 9 из примера 2) был получен достоверный эффект значительного уменьшения агрегации эритроцитов после ведения. Рис. 1 показывает репрезентативный пример фотомикроскопии крови до и после в/в введения препарата в указанных концентрация. Агрегаты эритроцитов в виде стопок легко различимы на фото до введения, но их практически нет на фото после введения.
У всех добровольцев (n=10), получавших внутримышечно аминодигидрофталазиндион натрия (АН) в дозе 100 мг в виде растворов с концентрацией 0,25 и 20,0 мг/мл (растворы №№6 и 9 из примера 2) не был выявлен эффект уменьшения агрегации эритроцитов. Рис. 2 показывает репрезентативный пример фотомикроскопии крови до и после в/м введения препарата в указанных концентрация. Агрегаты эритроцитов в виде стопок легко различимы на фото как до введения, так и после, что указывает на отсутствие эффекта.
Таким образом, внутривенное введение раствора настоящего изобретения имеет существенное преимущество перед внутримышечным введением раствора той же концентрации, так как улучшает реологические свойства крови путем снижения агрегации эритроцитов, тогда как внутримышечное введение нет.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТА И ПИРИДОКСИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2383331C1 |
| Пероральные композиции аминодигидрофталазиндиона и их применение в лечении невирусного гепатита | 2019 |
|
RU2834494C2 |
| РАСТВОР ДЛЯ ВНУТРИВЕННОГО И ВНУТРИМЫШЕЧНОГО ВВЕДЕНИЯ НА ОСНОВЕ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2605825C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЦИДИВИРУЮЩЕГО ВУЛЬВОВАГИНАЛЬНОГО КАНДИДОЗА | 2016 |
|
RU2642666C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2216328C1 |
| Препарат для профилактики и лечения воспалительных процессов у животных | 2019 |
|
RU2725773C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ЦИСТИТА | 2008 |
|
RU2386440C1 |
| Радиопротекторное, радиомитигаторное и радиосенсибилизирующее средство на основе натриевой соли аминодигидрофталазиндиона натрия (лекарственного препарата Тамерон) и других солей щелочных и щелочноземельных металлов аминодигидрофталазиндиона | 2022 |
|
RU2804886C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИ-CD20 АНТИТЕЛА И ЕЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2824627C2 |
| СПОСОБ ЛЕЧЕНИЯ КРОВОИЗЛИЯНИЙ ВО ВНУТРЕННИЕ СРЕДЫ И ОБОЛОЧКИ ГЛАЗА, СОПРОВОЖДАЮЩИХСЯ ГИПЕРАГРЕГАЦИЕЙ ТРОМБОЦИТОВ | 1998 |
|
RU2161020C2 |
Изобретение относится к области медицины, а именно к способу снижения агрегации эритроцитов. Способ снижения агрегации эритроцитов включает внутривенное введение субъекту, нуждающемуся в этом, раствора, содержащего аминодигидрофталазиндион натрия и растворитель, выбранный из группы, состоящей из воды для инъекций и раствора 0,9 мас.% хлорида натрия в воде, при следующем соотношении ингредиентов мг/мл: аминодигидрофталазиндион натрия - 0,25-20,0; растворитель - остальное. Вышеописанный способ имеет лучший профиль безопасности и позволяет снижать агрегацию эритроцитов при внутривенном введении раствора аминодигидрофталазиндиона натрия. 2 ил., 4 табл., 5 пр.
Способ снижения агрегации эритроцитов, включающий внутривенное введение субъекту, нуждающемуся в этом, раствора, содержащего аминодигидрофталазиндион натрия и растворитель, выбранный из группы, состоящей из воды для инъекций и раствора 0,9 мас.% хлорида натрия в воде, при следующем соотношении ингредиентов, мг/мл:
| Инструкция к применению препарата Тамерит, реестр лекарственных средств России, найдено в Интернет 28.11.2022, ссылка на источник: https://web.archive.org/web/20221128045154/https://www.rlsnet.ru/drugs/tamerit-84753 | |||
| Вода для инъекций, Фармсинтез, Найдено в Интернет 02.12.2022, ссылка на источник: |
Авторы
Даты
2024-06-17—Публикация
2023-04-28—Подача