Изобретение относится к медицине, а именно к гематологии и трансфузиологии, и может быть использовано при подготовке пациентов к аферезу аутологичных гемопоэтических стволовых клеток периферической крови.
Аутологичная трансплантация гемопоэтических стволовых клеток (ауто-ТГСК) периферической крови в настоящее время является обязательным этапом терапии многих онкологических и неонкологических заболеваний у взрослых и детей. Для мобилизации гемопоэтических стволовых клеток (ГСК) в периферическую кровь рутинно применяется гранулоцитарный колониестимулирующий фактор (Г-КСФ), а также, в некоторых случаях, добавляется плериксафор (Baldomero H., Gratwohl M., Gratwohl A., et al. The EBMT activity survey 2009: trends over the past 5 years // Bone Marrow Transplantation. - 2011. - Vol. 46. - P. 485-501; Gianni A.M., Siena S., Bregni M., et al. Granulocyte-macrophage colony-stimulating factor to harvest circulating haemopoietic stem cells for autotransplantation // Lancet. - 1989. - Vol. 334 (8663). - P. 580-5; DiPersio J.F., Stadtmauer E.A., Nademanee A. et al. Plerixafor and G-CSF versus placebo and G-CSF to mobilize hematopoietic stem cells for autologous stem cells transplantation in patients with multiple myeloma // Blood. - 2009. - Vol. 113(23). - P. 5720-5726).
Наиболее эффективно стимулирующие факторы действуют после курсов химиотерапии, в состав которых входят препараты, обладающие мобилизирующим потенциалом, такие как циклофосфомид, винорельбин и т.д. (Nowrousian M.R., Washke S., Bojko P., et al. Impact of chemotherapy regimen and hematopoietic growth factor on mobilization and collection of peripheral blood stem cells in cancer patients // Annals of Oncology. - 2003. - Vol. 14(1); Bargetzi M.J., Passweg J., Baertschi E., et al. Mobilization of peripheral blood progenitor cells with vinorelbine and granulocyte colony-stimulating factor in multiple myeloma patients is reliable and cost effective // Bone Marrow Transplantation. - 2003. - Vol. 31(2). - P. 99-103; Marr K., Ronsley R., Nadel H., et al. Ifosfamide, gemcitabine, and vinorelbine is an effective salvage regimen with excellent stem cell mobilization in relapsed or refractory pediatric Hodgkin lymphoma / // Pediatric Blood & Cancer. - 2020. - Vol. 67(4). - P. e28167).
CD34 - это гликопротеин, экспрессирующийся на поверхности ГСК, - наиболее часто использующаяся в клинической практике молекула для идентификации и подсчета стволовых клеток и клеток-предшественников. Измерение концентрации CD34+ клеток используется для определения качества мобилизации и предсказания успешности сбора ГСК (J. Delgado, M.C. Fernandez-Jimenez, A. Martinez, et al. Analysis of factors affecting PBPC collection in low-weight children with malignant disorders // Cytotherapy. - 2004. - Vol. 6(1). - P. 43-49; Schots R, Van Riet I, Damiaens S, et al. The absolute number of circulating CD34+ cells predicts the number of hematopoietic stem cells that can be collected by apheresis // Bone Marrow Transplant. - 1996. - Vol.17 - Р. 509-515; Furlong E., Jensen J., Woodard M., et al. Optimized peripheral blood progenitor cell mobilization for autologous hematopoietic cell transplantation in children with high-risk and refractory malignancies // Pediatric transplantation. - 2020. - Vol. 24(1). - P. e13602; Gidron A., Singh V., Egan K., et al. Significance of low peripheral blood CD34+ cell numbers prior to leukapheresis: What should the threshold required for apheresis be? // Bone marrow transplantation. - 2008. - Vol. 42(7). - P. 439-442). Концентрация (число) циркулирующих в периферической крови (ПК) перед аферезом CD34+ клеток является максимально точным маркером-предиктором успешного сбора, и чем больше количество CD34+ клеток в ПК, тем лучше результат.
Для определения оптимальной концентрации CD34+ клеток в ПК перед процедурой афереза и получения максимально достоверного предсказательного результата требуется большая выборка пациентов. Общепринятым методом получения этих данных является построение Receiver operating characteristic (ROC) кривых. Благодаря этому методу можно выделить значение, позволяющее достичь искомого результата с определённой специфичностью и чувствительностью (Truong T.H., Prokopishyn N.L., Luu H., et al. Predictive factors for successful peripheral blood stem cell mobilization and collection in children // Journal of Clinical Apheresis. - 2019. - Vol. 34(5). - P. 598-606. - DOI: 10.1002/jca.21738; Гальцева И.В., Давыдова Ю.О., Гапонова Т.В. и др. Абсолютное количество гемопоэтических стволовых клеток CD34+ в периферической крови перед процедурой лейкафереза как параметр, прогнозирующий эффективность сбора стволовых клеток // Терапевтический архив. - 2017. - №07. - С. 18-24).
Основной недостаток данного метода заключается в том, что он представляет ответ только на один заданный вопрос - сколько циркулирующих в ПК CD34+ клеток оптимально для сбора той дозы ГСК, которая была задана. При этом метод не позволяет предсказать успех и эффективность мобилизации ГСК на основе определения количества циркулирующих CD34+ клеток.
Технический результат заключается в способе определения вероятности сбора целевой дозы ГСК в зависимости от числа циркулирующих CD34+ клеток.
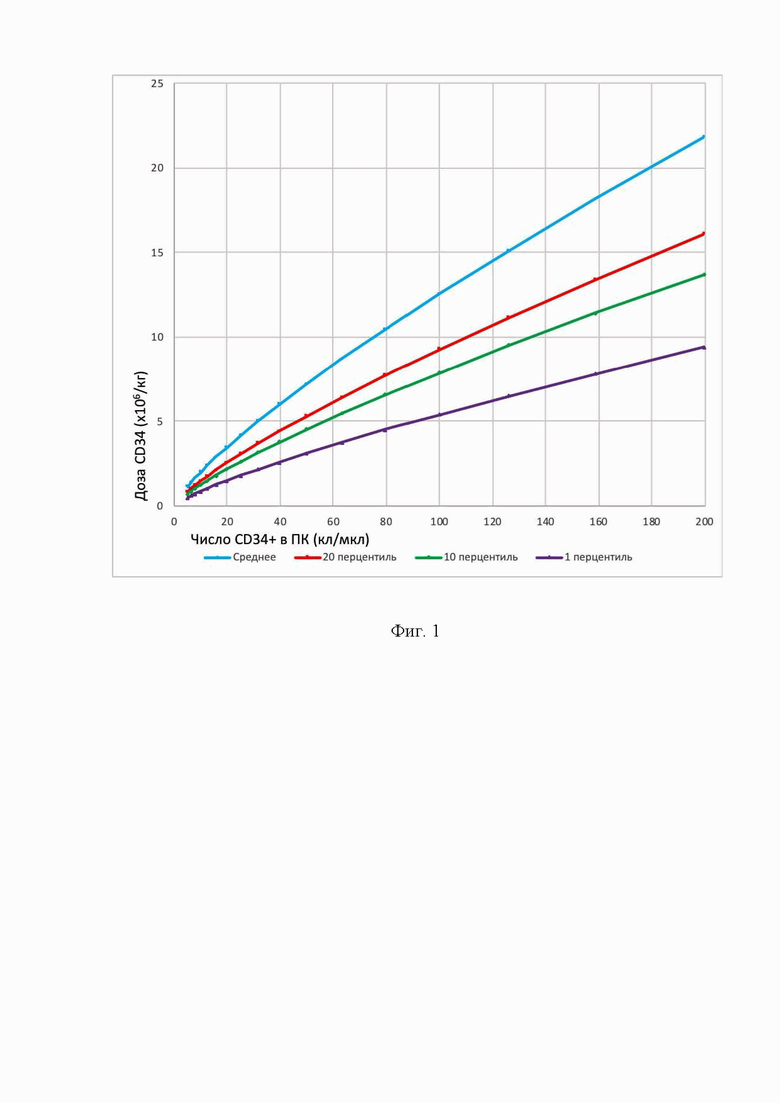
Технический результат достигается тем, что подсчитывают число циркулирующих CD34+ клеток до афереза ГСК, после чего по номограмме, составленной на основе линейной регрессионной модели зависимости дозы собранных ГСК от количества циркулирующих CD34+ клеток, с нанесенными на нее линиями, соответствующими 1, 10, 20 и 50 перцентилям, осуществляют прогнозирование вероятности получения эффективной дозы CD34+ клеток таким образом, что при значении числа CD34+ перед аферезом, указанном на оси абсцисс, вероятность сбора дозы ГСК менее значений, указанных на линиях 1, 10, 20 и 50 перцентилей по оси ординат, составляет не более 1%, 10%, 20% и 50% соответственно.
Способ осуществляется следующим образом: на первом этапе на основе анализа массива парных данных о концентрации в периферической крови CD34+ клеток перед аферезом в кл/мкл (независимая переменная), и значения дозы ГСК, полученных по завершении процедуры сбора (х106 CD34+ клеток/кг тела пациента, зависимая переменная), с использованием метода линейной регрессии и применением логарифмического преобразования для достижения линейной зависимости между переменными строят номограмму с нанесением на нее линий, соответствующих 1, 10, 20 и 50 перцентилям, при этом, 1 перцентиль соответствует 99% вероятности успеха сбора дозы ГСК, соответствующей точке пересечения перпендикуляра от оси абсцисс с перцентильной линией, 10 перцентилей соответствуют 90% вероятности успеха сбора дозы ГСК, соответствующей точке пересечения перпендикуляра от оси абсцисс с перцентильной линией, 20 перцентилей соответствуют 80% вероятности успеха сбора дозы ГСК, соответствующей точке пересечения перпендикуляра от оси абсцисс с перцентильной линией, среднее (50 перцентилей) соответствует 50% вероятности успеха сбора дозы ГСК, соответствующей точке пересечения перпендикуляра от оси абсцисс с перцентильной линией; на втором этапе у конкретного пациента подсчитывают число циркулирующих CD34+ клеток до афереза ГСК, после чего по номограмме прогнозируют вероятность получения эффективной дозы CD34+ клеток таким образом, что от точки на оси значений концентрации CD34+ клеток перед аферезом проводится перпендикуляр до пересечения с перцентильными линиями, затем от каждой точки пересечения этого перпендикуляра с перценцильными кривыми проводят перпендикуляры к оси ординат со значениями дозы ГСК; на заключительном этапе результат интерпретируют так, что при значении числа CD34+ перед аферезом, указанном на оси абсцисс, вероятность сбора дозы ГСК менее значений, указанных на линиях 1, 10, 20 и 50 перцентилей по оси ординат, составляет не более 1%, 10%, 20% и 50% соответственно.
Описываемый результат подтверждается в следующих клинических примерах.
Клинический пример 1. В ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России за период с марта 2012 г по июль 2021 г. включительно было выполнено 538 первых аферезов ГСК для 523 пациентов (вторые аферезы не учитываются при построении номограммы).
Стандартный график лечения: мобилизация гемопоэтических стволовых клеток в периферическую кровь начиналась при помощи Г-КСФ в стандартной дозе 10 мкг/кг в день. При необходимости доза Г-КСФ увеличивалась в 2 раза. Аферез планировался на следующий день после фиксации выброса CD34+ клеток в ПК > 20 кл/мкл (4 - 6-й день от начала стимуляции); или 15 кл/мкл при невозможности достигнуть лучшего результата, 17% пациентов дополнительно назначался плериксафор. Перед началом процедуры сбора ГСК обязательно брался образец крови пациента для определения концентрации CD34+ клеток. В зависимости от полученного результата, а также массы тела реципиента и количества запланированных аутологичных трансплнтаций гемопоэтических стволовых клеток (ауто-ТГСК), пациенту выполнялся аферез стандартного объёма (<3 объема циркулирующей крови (ОЦК)) или большого объёма (≥3 ОЦК). Целевая задача для каждого пациента определялась как доза ГСК ≥ 5 х 106 CD34+ клеток /кг, минимум ≥ 2 х 106/кг.
На основе линейного регрессионного анализа данных была построена номограмма (Фиг. 1). Модель построена без учета массы тела, возрастной или нозологической группы пациентов. В соответствии с номограммой сбор дозы ГСК ≥ 5 х 106/кг с 50% вероятностью возможен если у пациента в ПК перед аферезом циркулирует ≥ 35 кл/мкл CD34+, с 80% вероятностью - если циркулирует ≥ 45 кл/мкл, с 90% вероятностью - ≥ 55 кл/мкл, с 99% вероятностью требуется ≥ 90 кл/мкл. С 50% вероятностью доза ГСК ≥ 10 х 106/кг собиралось, если у пациента было перед аферезом CD34+ клеток было ≥ 70 кл/мкл. Для сбора дозы ГСК ≥ 10 х 106/кг с 80% вероятностью требуется ≥ 110 кл/мкл, с 90% вероятностью требуется ≥ 130 кл/мкл.
Данный график значительно упрощает восприятие данных пользователем, позволяет получить больше информации -- какой должна быть независимая переменная, чтобы получить искомое значение зависимой переменной с любой долей вероятности (нами были заданы 50%, 80%, 90%, 99%). Также доступна обратная интерпретация - с какая величина зависимой переменной достижима с разными степенями вероятности при имеющемся значении независимой переменной.
Клинический пример 2. Пациент №1, девочка 3-х лет, с диагнозом нейробластома, терапия по протоколу NB2004, масса тела 13 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии N5(3) - стандартная терапия Г-КСФ 10 мкг/кг, аферез на 4 день стимуляции, концентрация CD34+ 126 кл/мкл. По номограмме прогноз сбора дозы ГСК >5х106/кг - 99% и 80% вероятности сбора дозы ГСК >10х106/кг. Пациентке выполнен аферез стандартного объёма (обработано 0,8 объёма циркулирующей крови, 110 минут), эффективность сбора была 72%. Получена доза ГСК 6,0 х 106/кг CD34+ клеток.
Клинический пример 3. Пациент №2, мальчик 13 лет, с диагнозом лимфома Беркитта, терапия по протоколу B-NHL-2010 с ритуксимабом, масса тела 50 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии ВВ(5) - стандартная терапия Г-КСФ 10 мкг/кг, аферез на 4 день стимуляции, концентрация CD34+ 46 кл/мкл. По номограмме прогноз сбора дозы ГСК >2х106/кг - 99% и 80% вероятности сбора дозы ГСК >5х106/кг. Пациенту выполнен аферез стандартного объёма (обработано 2,7 объёма циркулирующей крови, 310 минут), эффективность сбора была 71%. Получена доза ГСК 6,3 х 106/кг CD34+ клеток.
Клинический пример 4. Пациент №3, мальчик 13 лет, с диагнозом саркома Юинга, терапия по протоколу Euro-Ewing 2008, масса тела 50 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии VIDE(5) - комбинированная терапия Г-КСФ 10 мкг/кг + плериксафор 0,24 мг/кг, аферез на 5 день стимуляции, концентрация CD34+ 17 кл/мкл. По номограмме прогноз сбора дозы ГСК >2х106/кг - 50% и вероятности сбора дозы ГСК >5х106/кг - 0%. Пациенту выполнен аферез большого объёма (обработано 4,4 объёма циркулирующей крови, 492 минуты), эффективность сбора была 40%. Получена доза ГСК 2,5 х 106/кг CD34+ клеток.
Клинический пример 5. Пациент №4, девочка 15 лет, с диагнозом герминогенная опухоль, терапия по протоколу TIGER, масса тела 50 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии TICE(1) - комбинированная терапия Г-КСФ 10-20 мкг/кг + плериксафор 0,24 мг/кг, аферез на 6 день стимуляции, концентрация CD34+ 119 кл/мкл. Цель сбора - 15 х 106/кг CD34+ клеток. По номограмме прогноз сбора дозы ГСК >10х106/кг - 80% и вероятность сбора дозы ГСК >15х106/кг - менее 50%. Пациентке выполнен аферез большого объёма (обработано 3,9 объёма циркулирующей крови, 314 минут), эффективность сбора была 59%. Получена доза ГСК 18,5 х 106/кг CD34+ клеток.
Клинический пример 6. Пациент №5, мальчик 17 лет, с диагнозом лимфома Ходжкина, рецидив, противорецидивная терапия, масса тела 61 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии бендамустин + брентуксимаб ведотин - комбинированная терапия Г-КСФ 10-20 мкг/кг + плериксафор 0,24 мг/кг, аферез на 6 день стимуляции, концентрация CD34+ 48 кл/мкл. По номограмме прогноз сбора дозы >2х106/кг - 99% и 80% вероятности сбора дозы ГСК >5х106/кг. Пациенту выполнен аферез большого объёма (обработано 4,1 объёма циркулирующей крови, 487 минут), эффективность сбора была 40%. Получена доза ГСК 5,5 х 106/кг CD34+ клеток.
Клинический пример 7. Пациент №6, мальчик 2-х лет, с диагнозом нейробластома, терапия по протоколу NB2004, масса тела 14 кг. Мобилизация ГСК инициирована после завершения блока химиотерапии N5(3) - комбинированная терапия Г-КСФ 10 мкг/кг + плериксафор 0,24 мг/кг, аферез на 5 день стимуляции, концентрация CD34+ 46 кл/мкл. По номограмме прогноз сбора дозы >2х106/кг - 99% и 80% вероятности сбора дозы ГСК >5х106/кг. Пациенту выполнен аферез большой по продолжительности (обработано 2,5 объёма циркулирующей крови, 320 минут), эффективность сбора была 34%. Получена доза ГСК 3,3 х 106/кг CD34+ клеток.
Исследование проведено в соответствии с действующими нормативными правовыми и этическими требованиями, предъявляемыми к клиническим исследованиям с участием детей (Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 г. №323-ФЗ в действующей редакции, Приказ Министерства здравоохранения Российской Федерации от 01.04.2016 г. №200н «Об утверждении правил надлежащей клинической практики») и одобрены Независимым этическим комитетом ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России.
Таким образом, применение заявляемого способа, построенного на основе результатов мобилизации и аферезов ГСК большой выборки пациентов, позволяет достаточно точно прогнозировать вероятность сбора любой целевой дозы ГСК у пациентов с любой реальной концентрацией CD34+ клеток перед аферезом. Также шкала может использоваться как вспомогательный инструмент для определения желаемого количества CD34+ клеток, добиться которого можно модифицируя терапию мобилизации.
Фиг. 1. Номограмма, отображающая вероятность сбора целевой дозы ГСК в среднем (50% вероятность), 80% вероятность (20 перцентилей), 90% вероятность (10 перцентилей) и 99% вероятность (1 перцентиль)
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования эффективной мобилизации гемопоэтических стволовых клеток у пациентов с множественной миеломой | 2020 |
|
RU2757964C1 |
| БИОМЕДИЦИНСКИЙ КЛЕТОЧНЫЙ ПРОДУКТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2741769C2 |
| ПРЕПАРАТ АУТОЛОГИЧНЫХ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК, СПОСОБ ЕГО ПОЛУЧЕНИЯ, КРИОКОНСЕРВАЦИИ И ИСПОЛЬЗОВАНИЯ ДЛЯ ЛЕЧЕНИЯ ТРАВМАТИЧЕСКОЙ БОЛЕЗНИ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2005 |
|
RU2283119C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ БЕЗРЕЦИДИВНОЙ ВЫЖИВАЕМОСТИ У БОЛЬНЫХ МНОЖЕСТВЕННОЙ МИЕЛОМОЙ ПОСЛЕ ПРОВЕДЕНИЯ АУТОЛОГИЧНОЙ ТРАНСПЛАНТАЦИИ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК | 2015 |
|
RU2580648C1 |
| Способ лечения впервые диагностированной нейробластомы 4 стадии группы высокого риска у детей старше 18 месяцев на основе индукционной химиоиммунотерапии | 2024 |
|
RU2839951C1 |
| Биомедицинский клеточный препарат | 2017 |
|
RU2647429C1 |
| БИОМЕДИЦИНСКИЙ КЛЕТОЧНЫЙ ПРОДУКТ ДЛЯ ЛЕЧЕНИЯ НЕРВНЫХ БОЛЕЗНЕЙ И ПСИХИЧЕСКИХ РАССТРОЙСТВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2720002C1 |
| ПРОТИВООПУХОЛЕВЫЙ ТАРГЕТНЫЙ КЛЕТОЧНЫЙ ПРОДУКТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2757812C2 |
| Персонализированный способ реституции костного мозга для борьбы с прогрессированием и рецидивами различных болезней цивилизации, профилактики старения и внезапной смерти | 2023 |
|
RU2817892C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ТРАНСПЛАНТАЦИИ СТВОЛОВЫХ КЛЕТОК | 2019 |
|
RU2809803C2 |
Изобретение относится к медицине, а именно к гематологии и трансфузиологии. После процедуры мобилизации и перед проведением сбора ГСК берут образец крови пациента. Определяют концентрацию CD34+ клеток в образце крови. Прогнозируют сбор дозы ГСК от 5 х 106/кг до 10 х 106/кг и дозы ГСК 10 х 106/кг и выше в зависимости от определенной концентрации CD34+ клеток в образце крови. Способ обеспечивает эффективное определение вероятности сбора целевой дозы ГСК в зависимости от числа циркулирующих CD34+ клеток. 1 ил., 7 пр.
Способ прогнозирования эффективности сбора гемопоэтических стволовых клеток (ГСК), отличающийся тем, что после процедуры мобилизации и перед проведением сбора ГСК берут образец крови пациента, определяют концентрацию CD34+ клеток в образце крови и прогнозируют сбор дозы ГСК от 5 х 106/кг до 10 х 106/кг с 50% вероятностью при концентрации CD34+ от 35 до 45 кл/мкл, с 80% вероятностью при концентрации CD34+ от 45 до 55 кл/мкл, с 90% вероятностью – от 55 до 90 кл/мкл, с 99% вероятностью – от 90 и выше кл/мкл; прогнозируют сбор дозы ГСК 10 х 106/кг и выше с 50% вероятностью при концентрации CD34+ от 70 до 110 кл/мкл, с 80% вероятностью при концентрации CD34+ от 110 до 130 кл/мкл, с 90% вероятностью – от 130 и выше кл/мкл.
| ПРЕПАРАТ АУТОЛОГИЧНЫХ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК, СПОСОБ ЕГО ПОЛУЧЕНИЯ, КРИОКОНСЕРВАЦИИ И ИСПОЛЬЗОВАНИЯ ДЛЯ ЛЕЧЕНИЯ ТРАВМАТИЧЕСКОЙ БОЛЕЗНИ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2005 |
|
RU2283119C1 |
| Центробежный фильтр | 1929 |
|
SU23367A1 |
| WO 2017096347 A1, 08.06.2017 | |||
| ГАЛЬЦЕВА И.В | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| КУРНИКОВА Е.Е | |||
| Результаты | |||
Авторы
Даты
2024-06-18—Публикация
2023-05-12—Подача