Настоящее изобретение относится к области бактериологии и вакцинологии. В частности, изобретение относится к жидкой композиции живых бактерий Mollicutes и стабилизатора, к производству указанной жидкой композиции, к применению NADES в качестве стабилизатора в указанной композиции и к различным медицинским применениям указанной композиции.
Живые бактерии используются в широком множестве применений; хорошо известны классические и современные биотехнологические процессы, способы диагностики и вакцины. Для всех этих применений являются важными способы стабилизации таких бактерий в ходе хранения и применения для поддержания их жизнеспособности. Обычные способы основаны на хранении в условиях глубокой заморозки с использованием криопротектора, такого как глицерин или богатая среда для стабилизации. Альтернативно живые бактерии можно лиофилизировать и хранить в лиофилизированной форме в условиях охлаждения или замораживания. Однако все эти способы стабилизации имеют ряд недостатков: богатая среда для хранения обеспечивает компоненты неопределенного и переменного качества, такие как сыворотки, гидролизаты и экстракты. Такой неопределенный ингредиент может иметь непредсказуемый эффект на стабильность. Кроме того, замороженные продукты требуют трудоемкой холодовой цепи для хранения и доставки. Однако даже эти процессы не обеспечивают полного выживания живых бактериальных клеток, поскольку стадии замораживания сами по себе индуцируют значительное снижение количества жизнеспособных клеток. Также, лиофилизация является очень дорогостоящим и времязатратным процессом. Таким образом, являются в высокой степени желательными улучшенные способы эффективной стабилизации количества живых клеток бактерий в ходе хранения и применения.
Группой бактерий с сельскохозяйственным и медицинским значением является класс Mollicutes. Их таксономически относят к роду Tenericutes (Ludwig et al., 2009: Bergey’s Manual of Systematic Bacteriology, 2nd ed, vol. 3. Springer: New York, USA, pp 1-13.). Этот род включает бактерии, которые происходят из грамположительных бактерий, но утратили их клеточную стенку. Они, как правило, являются паразитами или комменсалами эукариотических хозяев.
Инфекции животных бактериями Mycoplasma, либо в качестве первичного, либо в качестве вторичного патогена, часто вызывают респираторное заболевание и/или различные другие симптомы, которые вместе взятые могут вызывать заболевание от мягкого до тяжелого, вызывая значительный дискомфорт у пораженного хозяина, а также экономический ущерб. Эффекты инфекций Mycoplasma в сельском хозяйстве описаны в: "The Merck veterinary manual" (11th ed., 2016, ISBN-10: 9780911910612).
В то время как инфекцию бактериями Mycoplasma можно терапевтически лечить определенными типами антибиотиков, часто вакцины используются профилактически. Такие вакцины могут быть основаны на живых ослабленных штаммах или на инактивированных бактеринах (убитые бактерии). Вакцина на основе бактеринов против M. bovis представляет собой MpB GuardTM (Agrilabs). Большинство используемых коммерческих вакцин против Mycoplasma предназначены для птиц; примерами являются следующие: живые аттенуированные вакцины против M. gallisepticum: Vaxsafe®MG (Bioproperties) (замороженная) и Nobilis MG 6/85 (MSD Animal Health) (лиофилизированная, охлажденная); и вакцины на основе бактеринов против M. gallisepticum: MG-Bac® (Zoetis) и Nobilis® MG inac (MSD Animal Health), обе из которых являются эмульсиями с масляным адъювантом. Живыми аттенуированными вакцинами против M. synoviae являются: Vaxsafe® MS (Bioproperties) (замороженная) и Nobilis® MS Live (MSD Animal Health) (лиофилизированная, охлажденная). Несколько других живых аттенуированных вакцин против Mycoplasma известно и используется в более ограниченном масштабе, например ContavaxTM, лиофилизированная вакцина против M. mycoides жвачных животных, которая используется в некоторых африканских странах. Также в Китае используется живая аттенуированная вакцина против M. hyopneumoniae у свиней. Обзоры по вакцинации против Mycoplasma приведены в: Whithear (1996, Rev. Sci. Tech. Off. Int. Epiz., vol. 15, p. 1527-1553); Kleven (2008, Av. Dis., vol. 52, p. 367-374); и Perez-Casal et al. (2017, Vaccine, vol. 35, p. 2902-2907).
Вследствие их ассоциации с клеточной мембраной или даже инвазии ими клеток-хозяев, Mollicutes являются хорошо известными контаминирующими организмами для клеточных культур различных эукариотических клеток in vitro. Таким образом, несколько видов живых бактерий Mollicutes используется для диагностических целей и контроля качества. Это также является формальным требованием при биологическом производстве, находящемся под правительственным регулированием, например, в соответствии с Фармакопеей Европы и American 9 CFR.
Mollicutes представляют собой наименьшие из известных самореплицирующихся организмов: бактерии некоторых видов имеют диаметр только 0,2 микрометра, и некоторые имеют геном только 580 т.п.н. Наличие настолько малого количества генов вынуждает эти бактерии Mollicutes сильно зависеть от ресурсов их окружающей среды, так что при культивировании in vitro они, как правило, требуют очень богатой среды. Также отсутствие клеточной стенки выставляет их клеточную мембрану для физических и химических воздействий внешней среды, что приводит к низкой стабильности при хранении и в ходе применения.
Таким образом, важной проблемой вакцинной промышленности является то, как сохранить жизнеспособность таких живых бактерий Mollicutes в качестве бактериальных исходных культур, в ходе хранения готового продукта и в ходе применения, например, в диагностике или вакцинации. Одним из решений является производство и использование неживых вакцин типа бактеринов. Однако такие вакцины являются относительно дорогостоящими вследствие необходимости в относительно высокой их дозе, повторяющемся введении и применении адъюванта.
Вакцины на основе живых бактерий Mollicutes хранят глубоко замороженными или лиофилизированными, и в богатой стабилизирующей среде. Как описано, такая среда является менее желательной по ряду причин. Также значительные снижения количеств жизнеспособных клеток все еще происходят в ходе самого процесса заморозки, вызывающего потерю вплоть до 10^3 колониеобразующих единиц (кое) за несколько дней. Следовательно, являются в высокой степени желательными способы и материалы для улучшения стабилизации живых бактерий Mollicutes.
Глубокие эвтектические растворители (DES) представляют собой хорошо известные жидкие композиции, которые сочетают в себе ряд примечательных свойств. Как правило, они представляют собой смеси соединений, которые являются жидкими при температуре окружающей среды, но имеют низкое содержание воды. Также, небольшое количество воды, которое присутствует, является прочно связанным, ограничивая ее доступность для химических или биологических процессов. Это отражается очень низкими величинами водной активности. DES описаны, например, Abbott et al., 2003, Chem. Commun., vol. 1, p. 70-71, и в WO 2009/120839.
Являясь в высокой степени ионными, но в то же время обладая очень низкой водной активностью, DES являются в высокой степени эффективными в качестве растворителей для полярных гидрофобных соединений. Примеры находится в диапазоне от добычи газов, минералов или производства промышленной массовой продукции до солюбилиации фармацевтических веществ. DES также используются для экстракции и стабилизации биомолекул, таких как ферменты и РНК, см. US 8247198 и WO 2011/155829, соответственно.
Приблизительно с 2011 года рассматривается специальная форма DES, состоящая из встречающихся в природе веществ. Эти так называемые "природные DES", или NADES, описаны, например, в: Choi et al., 2011, Plant Physiol., vol. 156, p. 1701-1705; и Dai et al. 2013, Anal. Chim. Acta, vol. 766, p. 61-68. NADES в настоящее время представляют большой интерес в качестве "зеленых" растворителей, которые могут использоваться для экстракции натуральных продуктов и в качестве растворителей для применения, например, в натуральных пестицидах.
В WO 2011/155829 описана экстракция биологических материалов с использованием NADES. Одной из указанных возможностей является экстракция белковых материалов, таких как субъединичные вакцины.
Аналогично, в WO 2014/131906 описан, среди прочих, фиксаж для вируса в крови или ткани, отдельно фокусируясь на экстракции и стабилизации вирусной РНК для клинической диагностики. Фиксаж представляет собой DES, и, в то время как в WO 2014/131906 приводится большое количество возможных композиций DES, фактически используются только композиции, содержащие мочевину или трифторацетамид в качестве акцептора протонов, и холин или бетаин в качестве донора протонов. В WO 2014/131906 наиболее предпочтительный DES состоит из холинхлорида и трифторацетамида, таким образом, не являясь NADES, и трифторацетамид не является приемлемым фармацевтическим эксципиентом.
В WO 2016/108083 описано применение NADES вследствие их бактерицидной активности: было обнаружено, что некоторые NADES способны эффективно уничтожать или инактивировать грамположительные и грамотрицательные бактерии, а также клетки грибов Candida.
В WO 2016/162703 описано применение NADES, полученных, например, из бетаина и органической кислоты или многоатомного спирта, для экстракции биологических молекул, в частности из растительных материалов.
В WO 2017/222377 описано применение геля NADES в смеси с кормом для животных для обеспечения источника воды, который не высыхает в жару. Конкретно описано применение для вновь вылупившихся цыплят.
В WO 2015/121463 описаны жидкие стабильные вакцины для птиц, в частности, против вирусов птиц, в композиции из 5-40% сахарного спирта и 0,15-0,75 M аминокислоты, выбранной из аргинина, глутаминовой кислоты или глицина. Однако наиболее важно, в WO 2015/121463 и сходных публикациях, таких как WO 2014/029702 и WO 2014/140239, не описаны NADES, а описаны водные растворы, которые содержат по меньшей мере 60% масс./об. воды и имеют водную активность (aw) выше 0,85. В разделе "Примеры" приведены сравнительные данные.
В Gutierrez et al. (2010, Angew. Chem. Int. Ed., vol. 49, p. 2158-2162) описана криоконсервация грамотрицательных бактерий Escherichia coli с использованием разведения NADES, полученного из холинхлорида и глицерина в молярном соотношении 1:2 с 20% масс./об. растворенного вещества. Для получения NADES смесь бактерий и разведения NADES лиофилизировали.
Qiao et al. (2018, Appl. Microbiol. Biotechnol., vol. 102, p. 5695-5705) протестировали стабилизацию молочнокислых бактерий с использованием композиций, происходящих из NADES. Эти бактерии являются грамположительным и содержат клеточную стенку. Жизнеспособность двух видов из рода Lactobacillus не стабилизировалась или даже нарушалась при использовании NADES для хранения в замороженном состоянии. Streptococcus thermophilus могли быть стабилизированы в замороженной форме с использованием NADES из пролина:глицерина в молярном соотношении 1:3. Однако с использованием смеси 1+1 по объему NADES и бактериальной культуры, Qiao et al. разбавили их NADES до состояния, при котором сеть водородных связей перестала быть интактной. Это очевидно из профиля дифференциальной сканирующей калориметрии (DSC) (Qiao et al., фиг. 4), показавшего плавление и рост ледяных кристаллов. Это является свойством водной композиции, в то время как интактный NADES продемонстрировал бы температуру перехода в стеклообразное состояние.
Qiao et al. также описывают, что наличие клеточной стенки обеспечивает резистентность бактерий к эффектам токсичности NADES, а именно: дегидратации и повреждению клеточной мембраны.
Задачей настоящего изобретения является устранение недостатков уровня техники и удовлетворение потребности в данной области посредством предоставления композиции, содержащей живые бактерии Mollicutes, которые могут быть получены без лиофилизации и не должны храниться замороженными, а обеспечивают достаточную стабилизацию в ходе хранения и манипулирования при температурах выше 0 °C.
Неожиданно было обнаружено, что эта задача может быть решена, и, следовательно, один или несколько недостатков уровня техники могут быть преодолены, путем предоставления жидкой композиции, которая способна стабилизировать живые бактерии Mollicutes без замораживания или лиофилизации. Этого достигают с использованием NADES в качестве стабилизатора.
Это открытие открывает ряд очень полезных применений: живые Mollicutes теперь можно хранить без замораживания или лиофилизации, которые нарушают жизнеспособность. Также такие процессы являются трудоемкими, времязатратными и дорогостоящими. Кроме того, в жидкой композиции по настоящему изобретению не используются компоненты неопределенного или переменного качества, такие как гидролизаты для стабилизации, а напротив, используются соединения, которые имеют природное происхождение и являются химически определенными. Кроме того, жидкая форма позволяет простоту использования в различных применениях, таких как диагностика, контроль качества, а также в применении в качестве живых аттенуированных вакцин. Это является следствием того, что NADES являются приемлемыми в качестве фармацевтического носителя. Такую вакцинацию теперь можно проводить с использованием жидкой композиции, содержащей бактерии Mollicutes, либо прямо, либо после разведения.
Было неожиданным, что NADES способны стабилизировать живые бактерии Mollicutes: ожидалось, что в качестве мощных ионных растворителей NADES будут растворять тонкие и экспонированные мембраны бактериальных клеток и экстрагировать их цитоплазматические белки и нуклеиновые кислоты. В действительности, Qiao et al. (выше) предупреждают, что бактерии без клеточной стенки являются чувствительными к токсичности NADES. Также в WO 2016/108083 (выше) NADES фактически используются для уничтожения бактерий.
Таким образом, авторы изобретения неожиданно обнаружили, что составы NADES были способны обеспечить значительную стабилизацию жизнеспособности живых бактерий Mollicutes без замораживания или лиофилизации. Стабилизация была значительно лучшей, чем стабилизация, наблюдаемая для водных жидких композиций. Например, M. synoviae могли храниться в жидкой композиции по изобретению при 4 °C в течение вплоть до 24 недель с потерей менее 3 Log10 CFU, и в некоторых композициях потеря составляла даже менее 1 Log10 CFU. Даже при комнатной температуре обнаруживалась значительная стабилизация в течение вплоть до 8 недель, демонстрируя потерю только 4 Log10 CFU, в то время как культура в фосфатно-солевом буфере полностью утрачивалось в течение одной недели при этой температуре.
Точно неизвестно, как и почему NADES является настолько эффективным стабилизатором для живых бактерий Mollicutes. Хотя авторы изобретения не желают быть связанными какой-либо теорией или моделью, которая может объяснить эти данные, они полагают, что низкое количество доступной воды в NADES является полезным для поддержания жизнеспособности бактерий. Также бактерии Mollicutes, по-видимому, взаимодействуют с NADES способом, отличным от способа взаимодействия с ним бактерий, которые имеют клеточную стенку. Поскольку из уровня техники не известна стабилизация бактерий Mollicutes в NADES, этот эффект нельзя было предвидеть.
Таким образом, в одном аспекте изобретение относится к жидкой композиции, содержащей живые бактерии Mollicutes и стабилизатор, характеризующейся тем, что стабилизатор представляет собой натуральный глубокий эвтектический растворитель (NADES).
Термин "жидкий" используется в его обычном значении, указывая на композицию, которая может течь при определенной температуре и в определенный период времени. Одним из способов определения жидких свойств является тилт-тест, где контейнер с композицией при определенной температуре наклоняют, и, когда после определенного количества времени определяют любое изменение формы композиции, эту композицию классифицируют как жидкость. В рамках изобретения композиция является жидкой, если она изменяет форму в пределах 15 минут после наклона ее контейнера на 90° при комнатной температуре.
Подразумевают, что термин "содержащий" (а также варианты, такие как "содержать", "содержит" и "содержал"), как используют в рамках изобретения, относится ко всем элементам и в любой возможной комбинации, допустимой в рамках изобретения, которые охватываются или включены во фрагмент текста, абзац, пункт формулы изобретения и т. д., в которых этот термин используется, даже если такие элементы или комбинации не указаны в явной форме; и не исключая никакой такой элемент(ы) или комбинации.
Таким образом, любой такой фрагмент текста, абзац, пункт формулы изобретения и т. д. также относится к одному или нескольким варианту(ам) осуществления, где термин "содержащий" (или его варианты) заменен терминами, такими как "состоять из", "состоящий из" или "по существу состоит из".
Термин "живой" используется в настоящем описании в его обычно значении в отношении бактерий, указывающем на их способность расти, двигаться, поглощать и ферментировать питательные вещества и/или реплицироваться в соответствующих условиях. Способы определения того, являются бактерии погибшими или живыми, хорошо известны в данной области. Это можно определять in vivo, однако более удобно in vitro, например, посредством культивирования в подходящей среде и детекции повышения оптической плотности культуры, или путем посева на подходящие чашки с агаром и подсчета к.о.е. Альтернативой является использование селективного окрашивания живые/погибшие и подсчет.
Термин "Mollicutes" относится к бактериям, имеющим характерные признаки их таксономического класса, такие как морфологические, геномные и биохимические характеристики, а также биологические характеристики, такие как физиологическое, иммунологическое или патологическое поведение. То же самое применимо для указания на бактериальный отряд, семейство, род или на наименования индивидуальных видов бактерий.
Класс Mollicutes включает отряды Acholeplasmatales, Anaeroplasmatales, Entomoplasmatales и Mycoplasmatales. Отряд Acholeplasmatales включает хорошо известных вредителей растений Mollicutes рода Phytoplasma (Candidatus). Отряд Entomoplasmatales включает комменсалов насекомых и патогенов растений рода Spiroplasma.
Наиболее известным является отряд Mycoplasmatales, поскольку он включает хорошо известные патогенные для человека или животных бактерии рода Mycoplasma: например, M. pneumoniae, M. bovis, M. hyopneumoniae, M. meleagridis и M. gallisepticum, которые (в основном) инфицируют, соответственно: людей, жвачных животных, свиней, индеек и кур.
Как известно в данной области, отнесение микроорганизма к конкретной таксономической группе основано на комбинации таких признаков. Изобретение, таким образом, также относится к видам бактерий Mollicutes из отрядов, семейств, родов и видов, которые относят к классу Mollicutes. Аналогично, оно относится к бактериям, которые подклассифицированы из них каким-либо образом, например, в качестве подвида, штамма, изолята, генотипа, варианта, подтипа или подгруппы и т. п.
Кроме того, специалисту в области изобретения будет понятно, что, в то время как конкретный отряд, семейство, род или вид бактерий Mollicutes по изобретению может быть отнесен к этой группе, эта классификация является таксономической, которая может изменяться с течением времени, поскольку новые данные могут приводить к переклассификации в новую или отличающуюся таксономическую группу. Однако, поскольку это не изменяет сами бактерии или их антигенный репертуар, а изменяет только их научное название или классификацию, такие переклассифицированные бактерии остаются входящими в объем изобретения. Например, Gupta et al. (2018, Antonie van Leeuwenhoek, vol. 111, p. 1583-1630) предложили новую организацию рода Tenericutes на основе последних геномных данных.
Образцы бактерий Mollicutes для применения в рамках изобретения могут быть получены из различных источников, например, в качестве полевого изолята от человека или от не являющегося человеком животного в дикой среде или на ферме, или из различных лабораторий, (депозитарных) учреждений или (ветеринарных) университетов.
"Стабилизатор" в рамках изобретения представляет собой композицию, способную уменьшать снижение количества жизнеспособных клеток бактерий Mollicutes в рамках изобретения в результате манипулирования или применения и/или в результате хранения при определенной температуре на протяжении определенного периода времени.
"Стабилизацию" в рамках изобретения выражают в качестве эффекта на разность к.о.е. до и после определенной обработки композиции, содержащей живые бактерии Mollicutes, например, после инкубации в течение определенного периода времени при определенной температуре. Выживаемость в различных жидких композициях согласно изобретению, таким образом, сравнивают с выживаемостью в стандартном буфере PBS (10 мМ Na2PO4, 1,8 мМ KH2PO4, 2,7 мМ KCl и 137 мМ NaCl, в воде при pH 7,4). Следовательно, любая выживаемость выше выживаемости, наблюдаемой в PBS в сходных условиях хранения, считается эффектом на выживаемость, обеспечиваемым жидкой композицией по изобретению.
"Глубокий эвтектический растворитель" (DES) хорошо известен в данной области в качестве ионной жидкости, содержащей смесь по меньшей мере двух соединений в молярном соотношении, которое образует эвтектическую смесь, причем эвтектическая точка смеси является значительно более низкой, чем температуры плавления индивидуальных соединений.
Эта сниженная температура плавления смеси вызывается взаимодействием соединений, одно из которых выступает в качестве донора водородных связей, а другое из которых выступает в качестве акцептора водородных связей, которое обеспечивает сеть стабильных водородных связей. В то время как эта сеть включает небольшое количество воды, она не может кристаллизоваться при замораживании. Это позволяет смеси быть в жидкой форме при температурах, значительно более низких, чем температуры плавления компонентов. Часто "эвтектический" означает легкоплавкий.
NADES для применения в рамках изобретения имеет интактную сеть водородных связей. Это может быть удобным образом подтверждено посредством термического анализа профиля фазового перехода с использованием DSC. Следовательно, NADES для применения в рамках изобретения имеет профиль DSC, который демонстрирует температуру перехода в стеклообразное состояние.
Определение профиля DSC хорошо известно и может проводиться с использованием стандартного оборудования. Иллюстративный профиль представлен на фиг. 1.
Сеть водородных связей может обеспечить ограниченный уровень разведения. Однако когда используют слишком большое разведение, "DES" превращается в обычный водный раствор. В этом случае профиль DSC демонстрирует энтальпию плавления и кристаллизации, как в Qiao et al., выше, фиг. 4.
Индивидуальные соединения (за исключением воды), используемые для получения NADES в рамках изобретения, имеют температуру плавления выше приблизительно 80 °C, и полученный NADES имеет температуру плавления ниже приблизительно 40 °C. Например: температуры плавления бетаина и сорбита составляют 310 °C и 95 °C соответственно, в то время как NADES, полученный при молярном соотношении бетаина, сорбита и воды 1:1:2,5, имеет температуру перехода в стеклообразное состояние -50 °C и не демонстрирует кристаллизации льда и/или температуры плавления льда в его профиле DSC.
Термин "натуральный" служит для указания на то, что соединения, используемые для получения натурального DES (NADES) по изобретению, представляют собой органические соединения, которые в нормальных условиях могут встречаться в материале из биологических источников, таких как растения или животные, в количествах, значительно превышающих следовые количества. Как правило, такое натуральное соединение представляет собой или происходит из первичного метаболита, который присутствует в определенном материале растительного или животного происхождения. Как будет понятно специалисту в данной области, термин "натуральный" используется в настоящем описании для охарактеризации первоначального происхождения соединения для применения в NADES по изобретению, и не для охарактеризации истинного источника соединения для применения в рамках изобретения. Таким образом, натуральное соединение также может использоваться в рамках изобретения, когда оно получено посредством (полу-)синтетического способа получения.
Примерами натуральных соединений, которые могут использоваться для получения NADES по изобретению, представляют собой органические кислоты, амины, сахара, сахарные спирты, аминокислоты и четвертичные соли аммония, такие как производные холина.
Специалисту в данной области будет понятно, что в варианты осуществления, описанные в настоящем описании для изобретения, охватывают комбинации определенного типа NADES и типа бактерий Mollicutes, которые имеют более благоприятные свойства, чем другие комбинации, в отношении стабильности бактерий. Тем не менее, специалист в данной области способен без труда выбирать, оптимизировать и корректировать комбинации и композицию в соответствии с настоящим изобретением с использованием только стандартных способов и материалов, и информации, как описано в настоящем описании.
Дальнейшие детали предпочтительных вариантов осуществления и других аспектов изобретения описаны ниже.
Вода, которая присутствует в NADES для применения в рамках изобретения, прочно связана в структуре сети водородных связей NADES, что значительно снижает доступность воды для химических или биологических процессов, которые могут влиять на стабильность бактерий Mollicutes. Этот признак часто выражают путем указания количеств воды и свободной воды. На доступность этой воды (свободной воды) указывает величина водной активности, указываемая символом: aw. Водная активность варьируется между верхней границей 1,0 для чистой воды и нижней границей 0. Водную активность часто измеряют путем сравнения (при одной и той же температуре) давления пара тестируемой композиции относительно давления пара чистой воды и количества насыщенных солевых растворов с известной водной активностью. Это описано в различных справочниках, обзорах и руководствах, например, по консервации фруктов и овощей в бюллетене сельскохозяйственной службы FAO № 149 (Cánovas et al., FAO, Rome, 2003, ISBN 92-5-104861-4); и обзор приведен в: "Fundamentals of water activity", Decagon Devices Inc., Washington, 2015 (http://pdf.directindustry.com/pdf/decagon-devices-inc/fundamentals-water-активность/64142-634433.html).
При водной активности ниже приблизительно 0,8 рост большинства бактерий прекращается; ниже 0,7 прекращается рост большинства дрожжей и плесеней; и при водной активности ниже 0,4 эффективно останавливается активность большинства ферментов.
Оборудование и методики для измерения водной активности хорошо известны и доступны, например, с использованием анализа давления в свободном пространстве.
Было обнаружено, что эффективная стабилизация бактерий Mollicutes в жидких композициях по изобретению может быть достигнута, когда композиция имеет водную активность ниже чем приблизительно 0,85.
Таким образом, в одном варианте осуществления жидкой композиции по изобретению композиция имеет водную активность 0,85 или менее.
В рамках изобретения указанная водная активность относится к водной активности жидкой композиции согласно изобретению в форме конечного продукта, например, которая предлагается коммерческим производителем и в которой она может храниться в течение длительного времени. При применении этой композиции ее можно разбавлять или смешивать с другими компонентами, которые затем могут изменять величину водной активности.
В одном варианте осуществления жидкой композиции согласно изобретению водная активность композиции составляет менее чем приблизительно 0,8; более предпочтительно менее чем приблизительно 0,7, приблизительно 0,6, приблизительно 0,5, приблизительно 0,4, приблизительно 0,3 или даже менее чем приблизительно 0,2, в указанном порядке предпочтительности.
Предпочтительно водная активность жидкой композиции согласно изобретению составляет от 0,8 до 0,1. Более предпочтительно, она составляет от 0,7 до 0,1, от 0,6 до 0,1, от 0,5 до 0,1, от 0,4 до 0,1, от 0,3 до 0,1, или даже от 0,2 до 0,1, в указанном порядке предпочтительности.
В рамках изобретения указание на диапазон предполагает включение указанных конечных точек.
В рамках изобретения "приблизительно" указывает на то, что число может отличаться на ±10% от указанной величины. Предпочтительно "приблизительно" означает ±9% от указанной величины, более предпочтительно "приблизительно" означает ±8, 7, 6, 5, 4, 3, 2, 1 или даже 0% от указанной величины в указанном порядке предпочтительности.
Вода, используемая для жидкой композиции по изобретению, предпочтительно представляет собой воду высокого качества и чистоты, такую как (многократно) дистиллированная вода или обратноосмотическая вода. Более предпочтительно вода представляет собой воду фармацевтического качества и пригодную для парентеральной инъекции; вода такого качества предпочтительно является стерильной и по существу свободной от пирогенов, как например, вода для инъекций (WFI).
NADES для применения в жидкой композиции согласно изобретению получают с ограниченным количеством воды. Путем варьирования содержания воды в жидкой композиции, ее свойства можно адаптировать и оптимизировать, например, в отношении вязкости жидкой композиции. Эффективные содержащие NADES композиции с небольшой вязкостью можно получать с общим содержанием воды вплоть 50% масс./масс. (Dai et al., 2015, vol. 187, p. 14-19). Более высокие количества воды могут нарушать сеть водородных связей NADES.
Таким образом, в одном из вариантов осуществления жидкой композиции согласно изобретению композиция имеет содержание воды 50% масс./масс. или менее.
Содержание воды в жидкой композиции согласно изобретению выражают в качестве процента массы по массе "масс./масс.", который соответствует массе общего количества воды в жидкой композиции согласно изобретению в качестве части массы жидкой композиции. Содержание воды можно определять с использованием различных методик, например, посредством титрования по методу Карла Фишера, хорошо известного в данной области.
Что касается водной активности, жидкая композиция в этом контексте представляет собой композицию в форме конечного продукта перед применением какого-либо смешения или разбавления.
Предпочтительно жидкая композиция согласно изобретению имеет содержание воды 40% масс./масс. или менее, более предпочтительно 30, 25, 20, 15, 10, 8, 7, 6 или даже 5% масс./масс. или менее, в этом порядке предпочтительности.
Нижняя граница содержания воды в жидкой композиции согласно изобретению определяется практическими факторами, такими как следующие: насколько мало воды достаточно для солюбилизации соединений, которые образуют NADES. Также она определяется следующим: насколько много воды требуется для достижения приемлемого уровня вязкости NADES, чтобы его было удобно обрабатывать или использовать.
Таким образом, в одном варианте осуществления жидкой композиции согласно изобретению содержание воды в жидкой композиции составляет от 50 до 0,5% масс./масс.; от 40 до 1% масс./масс.; от 30 до 1,5% масс./масс.; от 20 до 2% масс./масс.; или даже от 10 до 3% масс./масс., в этом порядке предпочтительности.
Кроме того, некоторое количество воды добавляется в смесь путем смешения NADES с образцом живых бактерий Mollicutes с получением жидкой композиции согласно изобретению. Однако жидкая композиция по изобретению не должна быть чрезмерно разбавленной.
Таким образом, в одном варианте осуществления жидкой композиции согласно изобретению соотношение объемов NADES и объемов образца бактерий, подлежащих комбинированию, предпочтительно составляет по меньшей мере 3:1 об./об. NADES:бактериальный образец; более предпочтительно по меньшей мере 5:1 об./об. NADES:бактериальный образец; или даже по меньшей мере 10:1 об./об. NADES:бактериальный образец, в указанном порядке предпочтительности. Примечание: соотношение 10:1 означает комбинацию 9 частей NADES с 1 частью бактериального образца. Например: NADES из пролина, сорбита и воды в молярном соотношении 1:1:2,5 имеет общее количество воды 13,1% масс./масс. После смешения с образцом бактерий Mycoplasma по изобретению в соотношении 9 частей NADES+1 часть бактерий, общее количество воды конечной жидкой композиции согласно изобретению составляет 21,8% масс./масс.
Для ограничения чрезмерного разбавления NADES по изобретению в водную композицию, бактериальный образец, подлежащий комбинированию, может быть необходимо концентрировать.
Было обнаружено, что NADES, эффективный в качестве стабилизатора для живых бактерий Mollicutes в жидкой композиции согласно изобретению, образовывался из различных комбинаций и соотношений органической соли и/или многоатомного спирта, или образовывался из нескольких многоатомных спиртов.
Таким образом, в одном варианте осуществления жидкой композиции согласно изобретению NADES содержит органическую соль и многоатомный спирт.
В альтернативном варианте осуществления жидкой композиции согласно изобретению NADES содержит два или более соединений, которые являются многоатомными спиртами.
В некоторых из этих вариантов осуществления сеть водородных связей образуется органической солью в качестве ионной структуры, которая выступает в качестве донора водородных связей, и многоатомного спирта в качестве акцептора водородных связей. Альтернативно, когда NADES содержит только многоатомные спирты, между этими молекулами образуется сеть посредством водородных связей.
В рамках изобретения "многоатомный спирт" представляет собой органическое соединение, содержащее две или более гидроксильных групп. Однако очень крупные полимеры, входящие в определение многоатомного спирта, такие как целлюлоза, не являются в высокой степени эффективными в отношении образования NADES, как определено в настоящем описании, и, таким образом, предпочтительно не должны использоваться в рамках изобретения. Следовательно, многоатомные спирты для применения в рамках изобретения предпочтительно имеют молекулярную массу менее чем приблизительно 10000 граммов на моль.
В следующем предпочтительном варианте осуществления многоатомные спирты для применения в рамках изобретения имеют молекулярную массу менее 5000 или даже менее 1000 граммов на моль.
Соединения для применения NADES для применения в рамках изобретения являются хорошо доступными в различной степени чистоты и качестве от различных коммерческих поставщиков. Предпочтительно соединения используют в фармацевтическом качестве. Такие эксципиенты описаны, например, в рамках государственного регулирования, как например, в фармакопее Европы и в American 9 CFR, и в справочниках, таких как: The Handbook of Pharmaceutical Excipients (R. Rowe et al., Pharmaceutical press 2012, ISBN 0857110276); Remington: the science and practice of pharmacy (2000, Lippincot, USA, ISBN: 683306472), и: "Veterinary vaccinology" (P. Pastoret et al. ed., 1997, Elsevier, Amsterdam, ISBN 0444819681).
Предпочтительными многоатомным спиртами для применения в рамках изобретения являются сахара или сахарные спирты, поскольку было продемонстрировано, что они являются универсальными компонентами, которые позволяют получение различных эффективных NADES для применения в рамках изобретения.
В предпочтительном варианте осуществления сахар представляет собой невосстанавливающий сахар.
В одном варианте осуществления невосстанавливающего сахара для применения в жидкой композиции согласно изобретению невосстанавливающий сахар выбран из сахарозы и трегалозы.
Предпочтительно невосстанавливающий сахар представляет собой трегалозу. Трегалоза предпочтительно представляет собой CAS № 6138-23-4.
В рамках изобретения "сахарные спирты" представляют собой гидрогенизированные сахара, которые содержат 3 или более атомов углерода, и они могут быть основаны на моно-, ди- или полисахаридах.
В одном варианте осуществления сахарного спирта для применения в жидкой композиции согласно изобретению, сахарный спирт представляет собой один или несколько, выбранных из: эритрита, ксилита и сорбита.
Предпочтительно эритрит представляет собой CAS № 149-32-6. Ксилит предпочтительно представляет собой CAS № 87-99-0. Сорбит предпочтительно представляет собой D-сорбит, CAS № 50-70-4.
В одном варианте осуществления сахарного спирта для применения в жидкой композиции согласно изобретению, сахарный спирт представляет собой один или несколько, выбранных из ксилита и сорбита.
В более предпочтительном варианте осуществления сахарный спирт представляет собой сорбит.
Многоатомный спирт для применения в жидкой композиции в соответствии с изобретением может использоваться в качестве различных солей, изомерных форм, форм гидратов или безводных форм, и т. д. Специалист в данной области без труда способен выбрать и протестировать подходящую форму многоатомного спирта для применения в рамках изобретения.
В рамках изобретения "органическая соль" представляет собой соль любой органической кислоты или основания, включая цвиттерионы, которая входит в определение натурального соединения, как описано в настоящем описании выше, и которая способна образовывать глубокий эвтектический растворитель в рамках изобретения, как описано в настоящем описании. Специалист в данной области способен без труда выбрать органическую соль в рамках настоящего изобретения и использовать ее для получения NADES.
В одном варианте осуществления жидкой композиции согласно изобретению органическая соль представляет собой одну или несколько, выбранных из солей бетаина, пролина, холина, метионина и аргинина.
В рамках изобретения "бетаин" предпочтительно представляет собой соединение N, N,N-триметилглицин, CAS № 107-43-7, который также известен как глицин-бетаин. Пролин предпочтительно представляет собой CAS № 609-36-9. Холин предпочтительно представляет собой CAS № 62-49-7. Метионин предпочтительно представляет собой L-метионин, CAS № 63-68-3.
В предпочтительном варианте осуществления холин представляет собой холинхлорид, CAS № 67-48-1.
Что касается многоатомного спирта, описанного выше, органическую соль можно использовать в различных изомерных формах, формах гидратов или безводных формах, и т. д. Специалист в данной области способен без труда выбрать и протестировать подходящую форму органической соли для применения в рамках изобретения.
В одном варианте осуществления жидкой композиции согласно изобретению, когда органическая соль представляет собой аргинин, аргинин используется в качестве смеси L-аргинина (CAS № 74-79-3) и L-аргинина-HCl (CAS № 1119-34-2), причем L-аргинин-HCl составляет основную часть смеси.
Такая смесь соединений аргинина позволяет довести величину pH жидкой композиции согласно изобретению ближе к физиологическим величинам, когда композицию разбавляют, например, перед применением в качестве вакцины или при посеве для подсчета.
Предпочтительно молярное соотношение L-аргинина и L-аргинина-HCl составляет от 1:1 до 1:100; более предпочтительно молярное соотношение L-аргинина и гидрохлорида L-аргинина составляет от 1:1 до 1:50, более предпочтительно молярное соотношение составляет приблизительно 1:19.
В одном варианте осуществления жидкой композиции согласно изобретению NADES содержит три многоатомных спирта.
В предпочтительном варианте осуществления три многоатомных спирта представляют собой сорбит, ксилит и трегалозу.
В одном варианте осуществления NADES для применения в жидкой композиции согласно изобретению органическая соль выбрана из солей бетаина, пролина, холина и аргинина; и многоатомный спирт выбран из ксилита и сорбита.
В рамках изобретения органическую соль и многоатомный спирт, или многоатомные спирты, можно использовать в различных молярных соотношениях для обеспечения NADES с различными свойствами. Они могут быть оптимизированы специалистом в данной области для обеспечения оптимальной стабилизации живых бактерий Mollicutes в жидкой композиции согласно изобретению.
Таким образом, в одном варианте осуществления жидкой композиции согласно изобретению молярное соотношение между органической солью и многоатомным спиртом, как определено в настоящем описании, составляет от 1:5 до 5:1.
В предпочтительном варианте осуществления жидкой композиции согласно изобретению молярное соотношение между органической солью и многоатомным спиртом, как определено в настоящем описании, составляет от 1:4 до 4:1, от 1:3 до 3:1, или даже от 1:2 до 2:1, в указанном порядке предпочтительности.
В одном варианте осуществления жидкой композиции согласно изобретению молярное соотношение между любым из трех многоатомных спиртов: ксилита, трегалозы и сорбита, во всех случаях как определено в настоящем описании, может быть от 1-кратного до 5-кратного. Следовательно, молярное соотношение сорбит : ксилит : трегалоза составляет от 1:1:1 до одного из: 1:1:5, 1:5:1, 5:1:1, 1:5:5, 5:1:5, 5:5:1 и 5:5:5.
Одним типом преимущественного применения жидкой композиции согласно изобретению является применение в качестве вакцины. В таком применении бактерии Mollicutes используются в качестве активного ингредиента живой бактериальной вакцины, что требует, чтобы они были аттенуированными, чтобы не вызывать неприемлемую реакцию на вакцинацию у целевого животного.
Таким образом, в одном варианте осуществления жидкой композиции согласно изобретению бактерии Mollicutes являются аттенуированными в отношении их патогенных свойств.
Термин "аттенуированный" в рамках изобретения используются в его обычном значении, указывающем на бактерию, которая вызывает более низкий уровень патогенных эффектов в результате снижения частоты инфицирования и/или репликации в хозяине по сравнению с немодифицированной, неаттенуированной формой или формой "дикого типа" таких бактерий Mollicutes. Такие аттенуированные живые бактерии также называют "модифицированными живыми" бактериями.
Аттенуация бактерий Mollicutes может быть достигнута различными способами, например, посредством пассирования бактерий дикого типа через экспериментальных животных или в клеточной культуре, с использованием мутагенов или посредством технологии рекомбинантных ДНК, как хорошо известно в данной области.
Жидкая композиция согласно изобретению является эффективной в отношении стабилизации жизнеспособности различных бактерий из класса Mollicutes.
Таким образом, в одном варианте осуществления бактерии Mollicutes представляют собой одни или несколько, выбранных из отряда бактерий: Acholeplasmatales, Anaeroplasmatales, Entomoplasmatales и Mycoplasmatales.
В одном варианте осуществления бактерии Mollicutes в рамках изобретения являются одними или несколькими, выбранными из семейства бактерий: Acholeplasmataceae, Anaeroplasmataceae, Entomoplasmataceae, Spiroplasmataceae и Mycoplasmataceae.
В одном варианте осуществления бактерии Mollicutes в рамках изобретения являются одними или несколькими, выбранными из рода бактерий: Acholeplasma, Phytoplasma, Anaeroplasma, Asteroleplasma, Entomoplasma, Mesoplasma, Spiroplasma, Hepatoplasma, Marinoplasma, Moeniiplasma, Mycoplasma и Ureaplasma.
Предпочтительно бактерии Mollicutes в рамках изобретения являются одними или несколькими, выбранными из рода бактерий: Acholeplasma, Spiroplasma и Mycoplasma.
Более предпочтительно бактерии Mollicutes в рамках изобретения происходят из рода бактерий Mycoplasma.
В одном варианте осуществления жидкой композиции согласно изобретению бактерии Mollicutes являются одними или несколькими, выбранными из M. pneumoniae, M. bovis, M. hyopneumoniae, M. meleagridis, M. gallisepticum и M. synoviae.
В предпочтительном варианте осуществления бактерии Mollicutes представляют собой M. gallisepticum и/или M. synoviae.
В одном варианте осуществления жидкой композиции согласно изобретению бактерии Mollicutes представляют собой M. gallisepticum и M. synoviae.
Эксперименты показали, что M. gallisepticum и M. synoviae могут храниться в комбинации в жидкой композиции согласно изобретению, причем не может быть обнаружен значительный эффект одних из них на стабильность других при тестировании в течение вплоть до 23 недель при 2-8 °C. В таких смесях может быть обнаружено и подсчитано два вида бактерий при посеве того же смешанного образца на два различных типа чашек с агаром: один тип чашки с NAD (никотинамидадениндинуклеотид), а другой тип без NAD, и сравнении подсчитанных количеств колоний. Как описано в литературе (Olson & Kish Meadows, 1972, Avian Dis., vol. 16, p. 387-396), M. synoviae требуют NAD для их роста, таким образом, на чашках без NAD все выявленные колонии были из M. gallisepticum.
В предпочтительном варианте осуществления жидкая композиция согласно изобретению способна обеспечивать стабилизацию живых бактерий Mollicutes, причем количество к.о.е. Mollicutes не снижается более чем на 3 Log10 после инкубации при 4 °C в течение 12 недель. Еще более предпочтительно количество к.о.е. не снижается более чем на 7 Log10 после инкубации при комнатной температуре в течение 8 недель.
Комнатная температура представляет собой температуру 20±5 °C; 4 °C соответствует от 2 до 8 °C.
В одном варианте осуществления жидкой композиции согласно изобретению выполняется одно, или несколько, или все из условий, выбранных из группы, состоящей из:
- жидкая композиция имеет водную активность 0,85 или менее;
- водная активность жидкой композиции составляет менее чем приблизительно 0,8; более предпочтительно менее чем приблизительно 0,7, приблизительно 0,6, приблизительно 0,5, приблизительно 0,4, приблизительно 0,3 или даже менее чем приблизительно 0,2, в указанном порядке предпочтительности;
- водная активность жидкой композиции составляет от 0,8 до 0,1; более предпочтительно от 0,7 до 0,1, от 0,6 до 0,1, от 0,5 до 0,1, от 0,4 до 0,1, от 0,3 до 0,1 или даже от 0,2 до 0,1, в указанном порядке предпочтительности;
- жидкая композиция имеет содержание воды 50% масс./масс. или менее;
- жидкая композиция имеет содержание воды 40% масс./масс. или менее, более предпочтительно 30, 25, 20, 15, 10, 8, 7, 6 или даже 5% масс./масс. или менее, в указанном порядке предпочтительности;
- содержание воды в жидкой композиции составляет от 50 до 0,5% масс./масс.; от 40 до 1% масс./масс.; от 30 до 1,5% масс./масс.; от 20 до 2% масс./масс.; или даже от 10 до 3% масс./масс., в указанном порядке предпочтительности;
- соотношение объемов NADES и объемов бактериального образца, подлежащих комбинированию, предпочтительно составляет по меньшей мере 3:1 об./об. NADES:бактериальный образец; более предпочтительно по меньшей мере 5:1 об./об. NADES:бактериальный образец; или даже по меньшей мере 10:1 об./об. NADES:бактериальный образец, в указанном порядке предпочтительности;
- NADES содержит органическую соль и многоатомный спирт;
- NADES содержит два или более соединений, все из которых являются многоатомными спиртами;
- многоатомные спирты для применения в рамках изобретения имеют молекулярную массу менее 5000 или даже менее 1000 граммов на моль;
- многоатомный спирт представляет собой сахар или сахарный спирт;
- сахар представляет собой невосстанавливающий сахар;
- невосстанавливающий сахар выбран из сахарозы и трегалозы; предпочтительно невосстанавливающий сахар представляет собой трегалозу; трегалоза предпочтительно соответствует CAS № 6138-23-4;
- сахарный спирт представляет собой один или несколько выбранных из: эритрита, ксилита и сорбита;
- эритрит предпочтительно соответствует CAS № 149-32-6; ксилит предпочтительно соответствует CAS № 87-99-0; сорбит предпочтительно представляет собой D-сорбит, CAS № 50-70-4;
- сахарный спирт представляет собой один или несколько, выбранных из группы из ксилита и сорбита; в более предпочтительном варианте осуществления сахарный спирт представляет собой сорбит;
- органическая соль представляет собой одну или несколько, выбранных из солей бетаина, пролина, холина, метионина и аргинина;
- бетаин предпочтительно представляет собой соединение N,N,N-триметилглицин, CAS № 107-43-7, которое также известно как глицин-бетаин; пролин предпочтительно представляет собой CAS № 609-36-9; холин предпочтительно представляет собой CAS № 62-49-7; метионин предпочтительно представляет собой L-метионин, CAS № 63-68-3; аргинин предпочтительно представляет собой L-аргинин, CAS № 74-79-3;
- холин представляет собой холинхлорид, CAS № 67-48-1;
- когда органическая соль представляет собой аргинин, аргинин используют в качестве смеси L-аргинина (CAS № 74-79-3) и гидрохлорида L-аргинина (CAS № 1119-34-2);
- молярное соотношение L-аргинина и L-аргинина-HCl составляет от 1:1 до 1:100; более предпочтительно молярное соотношение L-аргинина и гидрохлорида L-аргинина составляет от 1:1 до 1:50, более предпочтительно молярное соотношение составляет приблизительно 1:19;
- органическая соль выбрана из солей бетаина, пролина, холина и аргинина; и многоатомный спирт выбран из ксилита и сорбита;
- молярное соотношение между органической солью и многоатомным спиртом составляет от 1:5 до 5:1;
- молярное соотношение между органической солью и многоатомным спиртом составляет от 1:4 до 4:1, от 1:3 до 3:1 или даже от 1:2 до 2:1, в указанном порядке предпочтительности;
- NADES содержит три многоатомных спирта; в предпочтительном варианте осуществления три многоатомных спирта представляют собой сорбит, ксилит и трегалозу;
- молярное соотношение сорбит : ксилит : трегалоза составляет между 1:1:1 и одним из 1:1:5, 1:5:1, 5:1:1, 1:5:5, 5:1:5, 5:5:1 и 5:5:5;
- бактерии Mollicutes являются аттенуированными в отношении их патогенных свойств;
- бактерии Mollicutes являются одними или несколькими, выбранными из отряда бактерий: Acholeplasmatales, Anaeroplasmatales, Entomoplasmatales и Mycoplasmatales;
- бактерии Mollicutes являются одними или несколькими, выбранными из семейства бактерий: Acholeplasmataceae, Anaeroplasmataceae, Entomoplasmataceae, Spiroplasmataceae и Mycoplasmataceae;
- бактерии Mollicutes являются одними или несколькими, выбранными из рода бактерий: Acholeplasma, Phytoplasma, Anaeroplasma, Asteroleplasma, Entomoplasma, Mesoplasma, Spiroplasma, Hepatoplasma, Marinoplasma, Moeniiplasma, Mycoplasma и Ureaplasma;
- бактерии Mollicutes являются одними или несколькими, выбранными из рода бактерий: Acholeplasma, Spiroplasma и Mycoplasma;
- бактерии Mollicutes происходят из рода бактерий Mycoplasma;
- бактерии Mollicutes являются одними или несколькими, выбранными из M. pneumoniae, M. bovis, M. hyopneumoniae, M. meleagridis, M. gallisepticum и M. synoviae;
- бактерии Mollicutes представляют собой M. gallisepticum и/или M. synoviae; и
- бактерии Mollicutes представляют собой M. gallisepticum и M. synoviae.
В одном варианте осуществления жидкой композиции согласно изобретению жидкая композиция имеет водную активность 0,85 или менее, и содержание воды 50% масс./масс. или менее; NADES содержит органическую соль и многоатомный спирт, где многоатомный спирт представляет собой ксилит или сорбит, и органическая соль выбрана из бетаина, пролина, холина и аргинина; бактерии Mollicutes являются аттенуированными в отношении их патогенных свойств и бактерии Mollicutes являются одними или несколькими, выбранными из M. pneumoniae, M. bovis, M. hyopneumoniae, M. meleagridis, M. gallisepticum и M. synoviae.
В предпочтительном варианте осуществления бактерии Mollicutes представляют собой M. gallisepticum и/или M. synoviae, и NADES содержит бетаин и сорбит.
В одном варианте осуществления жидкой композиции согласно изобретению жидкая композиция имеет водную активность 0,85 или менее, и содержание воды 50% масс./масс. или менее; NADES содержит три многоатомных спирта, которые представляют собой сорбит, ксилит и трегалозу; бактерии Mollicutes являются аттенуированными в отношении их патогенных свойств, и бактерии Mollicutes являются одними или несколькими, выбранными из M. pneumoniae, M. bovis, M. hyopneumoniae, M. meleagridis, M. gallisepticum и M. synoviae.
Как описано, жидкая композиция согласно изобретению может быть получена с использованием обычных способов и материалов. Детали и примеры такого способа, применения или процесса получения жидкой композиции согласно изобретению описаны в настоящем описании, и такие методики без труда могут применяться специалистом в данной области с использованием стандартных материалов и способов.
Например, NADES в рамках изобретения можно производить в промышленном масштабе, а затем составлять в жидкую композицию согласно изобретению путем смешения с препаратом живых бактерий Mollicutes. Затем смесью заполняют контейнеры соответствующего размера. Мониторинг различных стадий процесса производства можно осуществлять посредством соответствующих тестов, например, посредством биохимических или иммунологических тестов качества и количества бактерий.
Таким образом, в следующем аспекте изобретение относится к способу производства жидкой композиции согласно изобретению, причем способ включает стадии:
a. получения NADES, и
b. смешения указанного NADES с живыми бактериями Mollicutes.
Удобно, чтобы две стадии способа согласно изобретению можно было осуществлять с разделением во времени и/или в пространстве и с промежуточными стадиями хранения, транспортировки или даже дополнительными стадиями. Это позволит гибкость действий в отношении планирования и логистики.
Производство NADES для применения в способе согласно изобретению можно проводить с использованием стандартных инструментов и способов. Одним из удобных способов является использование нагрева объединенных соединений до температуры, которая позволяет им смешаться и раствориться, например, как при автоклавировании. Однако некоторые соединения или композиции NADES для применения в рамках изобретения могут не выдерживать слишком высоких температур; специалист в данной области может оптимизировать и адаптировать такой процесс. Нагрев можно проводить, например, в комбинации с перемешиванием или обработкой ультразвуком.
Также один из компонентов для получения NADES изначально может быть растворен в воде в более или менее концентрированной форме, после чего его можно смешивать с дополнительным компонентом(ами). Затем формируют структуру NADES путем удаления избытка воды. Предпочтительно такое удаление не проводят посредством лиофилизиации. Альтернативным способом является, например, ротационное испарение на водяной бане при 70°C в течение нескольких часов при пониженном атмосферном давлении.
Композиция, содержащая живые бактерии Mollicutes для применения в способе согласно изобретению, в подходящем случае может быть получена различными способами из культуры in vivo, однако предпочтительно из культуры in vitro бактерий в подходящей среде. Такие бактериальные культуры можно получать в любом желаемом размере или объеме вплоть до нескольких 1000 литров в крупномасштабных ферментерах промышленного размера с использованием способов автоматизированного контроля и мониторинга.
Затем бактерии собирают из культуры способом, который зависит от характеристик бактерий: в качестве супернатанта, клеточного осадка или цельной культуры. Далее бактерии смешивают с NADES, либо прямо, либо непрямо, путем первоначального смешения бактерий с жидкостью, например, буфером или средой.
Бактериальную композицию для применения в способе по изобретению можно получать с использованием дополнительных стадий процесса, таких как концентрирование, например, с использованием пропускания через ультрафильтрационные мембраны. Затем бактериальную композицию проверяют в отношении жизнеспособности и количества. Все это хорошо известно специалисту в данной области.
Смешение NADES и бактериальной композиции в способе согласно изобретению предпочтительно проводят с использованием асептических способов.
Порядок и способ смешения не является критичным, поскольку NADES можно добавлять к бактериальной композиции или наоборот. Предпочтительно любое используемое механическое перемешивание происходит при низкой скорости или является низкоударным для предотвращения чрезмерных сдвиговых усилий в отношении бактерий. Кроме того, смешение и/или заполнение можно проводить в защитной атмосфере из инертного газа (например, азота) для уменьшения воздействия кислорода.
Удобное оборудование для перемешивания и заполнения относительно вязких жидкостей доступно от различных поставщиков технологического оборудования.
В следующем аспекте изобретение относится к применению NADES, как описано в рамках изобретения, в качестве стабилизатора в жидкой композиции, содержащей живые бактерии Mollicutes.
Все из "стабилизатора", "жидкой композиции", "живых бактерий Mollicutes" являются такими, как определено в любом одном или нескольких из вариантов осуществления, как описано в настоящем описании для изобретения.
Как описано, преимущественное применение в рамках настоящего изобретения представляет собой медицинское применение жидкой композиции согласно изобретению в качестве бактериальной вакцины.
Таким образом, в следующем аспекте изобретение относится к жидкой композиции согласно изобретению или получаемой способом производства согласно изобретению для применения в качестве вакцины против инфекции или заболевания, вызываемых бактериями Mollicutes.
Аналогично, в следующем аспекте изобретение относится к жидкой вакцине для применения против инфекции или заболевания, вызываемых бактериями Mollicutes, причем вакцина содержит жидкую композицию согласно изобретению или получена способом согласно изобретению.
Кроме того, в следующем аспекте изобретение относится к применению NADES, как описано в рамках изобретения, в качестве фармацевтически приемлемого носителя в жидкой вакцине согласно изобретению.
Хорошо известно, что "вакцина" представляет собой композицию, которая имеет медицинский эффект. Вакцина содержит иммунологически активный компонент и фармацевтически приемлемый носитель. Иммунологически активный компонент в данном случае представлен живыми бактериями Mollicutes. Вакцина распознается иммунной системой целевого животного, у которого индуцируется защитный иммунологический ответ. Ответ может осуществляться врожденной и/или приобретенной иммунной системой целевого животного, и может быть клеточного и/или гуморального типа.
Вакцина, как правило, является эффективной в отношении снижения тяжести инфекции, например, путем уменьшения количества присутствующих патогенов или уменьшения длительности репликации патогена в животном-хозяине.
Также или возможно в результате этого, вакцина, как правило, является эффективной в отношении снижения или облегчения (клинических) симптомов заболевания, которое может вызываться такой инфекцией или репликацией, или ответом целевого организма на эту инфекцию или репликацию.
"Фармацевтически приемлемый носитель" в рамках изобретения представляет собой жидкость высокой степени чистоты, и предпочтительно он является стерильным. В данном случае носитель представляет собой NADES, как определено в настоящем описании. Носитель может включать дополнительные добавки, такие как стабилизаторы, антиоксиданты или консерванты.
Детали, касающиеся "инфекции или заболевания, вызываемых бактериями Mollicutes", хорошо известны в данной области и описаны, например, в справочниках, таких как: Merck veterinary manual (выше), и Diseases of Poultry, 12th edition, 2008, Wiley-Blackwell, ISBN: 0813807182.
Жидкая вакцина согласно изобретению содержит количество живых бактерий Mollicutes, которое является иммунологически эффективным.
Специалист в области изобретения способен без труда определить и оптимизировать такое иммунологически эффективное количество живых бактерий Mollicutes в жидкой вакцине по изобретению, например, посредством мониторинга иммунологического ответа после вакцинации. Также, в случае целевого не являющегося человеком животного можно проводить контрольное заражение с последующим мониторингом признаков заболевания у целевого организма, клинической оценки и распространения и диссеминирования патогена, и сравнением этих результатов с ответом вакцинация-заражение, наблюдаемым у животных с имитирующей вакцинацией.
Способы определения количества живых бактерий в дозе вакцины или в образце от животного хорошо известны в данной области, и, как правило, в них используются способы культивирования и подсчета бактерий. Удобно, чтобы такое количество бактерий могло быть выражено в качестве числовой величины, например, в качестве к.о.е.
Целевыми организмами для жидкой вакцины по изобретению являются люди или не являющиеся человеком животные, нуждающиеся в вакцинации против инфекции или заболевания, вызываемых патогенной формой конкретных живых бактерий Mollicutes, которые присутствуют в вакцине. Возраст, масса тела, пол, иммунологический статус и другие параметры целевого организма, подлежащего вакцинации, не являются критическими, хотя является целесообразным вакцинировать здоровые неинфицированные целевые организмы и вакцинировать настолько рано, насколько это возможно, чтобы предотвратить какую-либо полевую инфекцию.
Жидкая вакцина согласно изобретению, кроме того, может содержать другие соединения, такие как дополнительный антиген или микроорганизм, цитокин или иммуностимулирующая нуклеиновая кислота, содержащая неметилированный CpG, адъювант и т. д. Альтернативно жидкая вакцина согласно изобретению может быть сама по себе добавлена к вакцине.
Жидкую вакцину согласно изобретению можно преимущественно комбинировать с одним или несколькими дополнительными антигенами или микроорганизмом, например, происходящим из микроорганизма, патогенного для предполагаемых целевых человека или не являющегося человеком животного. Такой дополнительный антиген сам по себе может представлять собой инфекционный микроорганизм, живой, аттенуированный или инактивированный, или может представлять собой субъединицу, экстракт или фракцию и т. д. Дополнительный антиген может состоять из биологической или синтетической молекулы, такой как белок, углевод, липополисахарид, липид или молекула нуклеиновой кислоты.
Жидкая вакцина согласно изобретению может содержать консервант, такой как тимеросал, мертиолат, фенольные соединения и/или гентамицин. Предпочтительно консервант не используют.
Жидкая вакцина согласно изобретению может содержать стабилизатор, хотя предпочтительно такой стабилизатор не является переменным или неопределенным соединением, как описано в настоящем описании.
Жидкая вакцина согласно изобретению может содержать антиоксидант, такой как аскорбиновая кислота, цитрат, метионин или токоферол.
Жидкую вакцину согласно изобретению можно использовать либо в качестве профилактического, либо в качестве терапевтического способа лечения, либо в качестве обоих из них.
Жидкая вакцина согласно изобретению может служить в качестве эффективной примирующей вакцинации, после которой далее может следовать одна или несколько бустерная вакцинация(ий), той же самой или отличающейся вакциной.
Жидкая вакцина согласно изобретению может быть получена с использованием хорошо известных способов, которые включают способы производства жидкой композиции согласно изобретению.
Таким образом, в следующем аспекте изобретение относится к применению NADES, как описано в рамках изобретения, для производства жидкой вакцины согласно изобретению.
Такое производство включает микробиологические тесты стерильности и отсутствия посторонних агентов; и в конечном итоге испытания с вакцинацией у животных для подтверждения эффективности и безопасности. После завершения тестирования качества, количества, стерильности, безопасности и эффективности, вакцинный продукт может быть выпущен для продажи.
Все они хорошо известны специалисту в данной области, и основные способы и факторы, которые применимы для производства вакцин в соответствии с хорошо известными стандартами производства фармацевтических средств, описаны в правительственных предписаниях и нормах (Фармакопея, 9CFR) и в хорошо известных справочниках (Pastoret, Lippincot, оба выше).
Жидкую вакцину согласно изобретению можно вводить человеку или не являющемуся человеком животному в форме, в которой она предоставляется, например, фармацевтическим производителем. Однако в зависимости от конкретного состава конкретного варианта осуществления жидкой вакцины согласно изобретению, может быть целесообразным проведение разведения жидкой вакцины. Это может облегчать фактическое введение целевому организму, например, путем уменьшения вязкости, или может уменьшать локальные реакции при вакцинации целевого организма.
Разбавитель для такого разбавления, как правило, представляет собой жидкость, и он может быть предоставлен отдельно от жидкой вакцинной композиции согласно изобретению. Предпочтительно, разбавитель предоставляют вместе с жидкой вакциной согласно изобретению, например, в качестве набора.
Таким образом, в следующем аспекте изобретение относится к набору, содержащему по меньшей мере два контейнера: один контейнер, содержащий жидкую вакцину согласно изобретению, и один контейнер, содержащий жидкий разбавитель.
"Жидкий разбавитель" для разбавления жидкой вакцины согласно изобретению, например, для включения в набор согласно изобретению, представляет собой жидкость, которая пригодна для разбавления жидкой вакцины согласно изобретению. Таким образом, жидкий разбавитель может быть водным, таким как вода или буфер. Однако, вследствие низкого содержания воды в жидкой вакцине согласно изобретению, разбавитель также может быть масляным или он может представлять собой эмульсию масла и воды, например, типа "масло в воде", "вода в масле" или двойную эмульсию.
В одном варианте осуществления жидкий разбавитель сам по себе может представлять собой жидкую вакцину, например, восстановленную лиофилизированную живую вакцину или эмульсионную вакцину.
Выбор жидкого разбавителя для разбавления жидкой вакцины согласно изобретению, например, для включены в набор согласно изобретению, зависит от нескольких факторов, таких как: предполагаемое применение вакцины после ее разбавления; бактерий Mollicutes, которые она содержит; предполагаемые целевые человек или животное для вакцинации и т. д. Специалист в данной области абсолютно способен выбрать, получить и применять такой разбавитель.
В одном варианте осуществления набора согласно изобретению набор содержит инструкции по применению набора и/или его компонентов. В предпочтительных вариантах осуществления инструкции по применению предоставлены на или с одним или несколькими компонентами набора; или предоставлены посредством отсылки к инструкциям в электронной форме, таким как информация, которая может быть просмотрена или загружена с веб-сайта в интернете, например, от производителя или поставщика набора.
В одном варианте осуществления набор представляет собой коробку, содержащую по меньшей мере два контейнера и содержащую инструкции по применению, которые отображены на носителе информации (например, карточка или листок), присутствующем на, с или в коробке.
В одном варианте осуществления набор также может представлять собой предложение компонентов (касающееся коммерческой продажи), например, на веб-сайте интернета, для применения в способе вакцинации по изобретению.
Жидкая вакцина согласно изобретению или жидкая вакцина, которая может быть произведена посредством способа или применения согласно изобретению, или жидкая вакцина в разбавленной форме, которая может быть получена, например, с использованием набора согласно изобретению, предназначена для введения целевым человеку или не являющегося человеком животному, нуждающимся в такой вакцинации. Вакцинация индуцирует активную иммунизацию для снижения инфекции и/или признаков заболевания, которое может вызваться инфекцией неаттенуированным аналогом живых бактерий Mollicutes по изобретению. В свою очередь это приводит у целевых человека или не являющегося человеком животного к уменьшению количества, интенсивности или тяжести очагов повреждения и последующих клинических признаков заболевания, вызываемого бактериальной инфекцией. Такая вакцина в разговорной речи называется: вакциной "против" конкретной бактерии Mollicutes, или "вакциной Mollicutes".
Таким образом, в следующем аспекте изобретение относится к жидкой вакцине согласно изобретению для применения в способе защиты человека или не являющегося человеком животного против инфекции и/или заболевания, вызываемых патогенной формой живых бактерий Mollicutes, содержащихся в указанной жидкой вакцине.
Такая "патогенная форма живых бактерий Mollicutes, содержащихся в указанной жидкой вакцине", представляет собой, например, неаттенуированную родительскую бактерию Mollicutes, из которой была получена аттенуированная форма бактерий Mollicutes по изобретению. Альтернативно такая патогенная форма бактерий может быть без труда получена из различных источников, как описано в настоящем описании. Специалист в данной области по изобретению способен без труда определить, является ли бактерия Mollicutes патогенной формой, например, посредством сравнительного тестирования in vitro или in vivo, как описано в настоящем описании.
"Способ защиты" вовлекает введение жидкой вакцины согласно изобретению указанным целевым человеку или не являющемуся человеком животному, так что вакцина может "приобретать" (т. е. установление защитной функции) и демонстрировать ее благоприятные иммунологические эффекты у целевого организма.
В следующем аспекте изобретение относится к способу вакцинации целевых человека или не являющегося человеком животного против инфекции или заболевания, вызываемых бактериями Mollicutes, причем способ включает введение указанному целевому организму жидкой композиции согласно изобретению или включает применение набора согласно изобретению.
В способе вакцинации согласно изобретению жидкая вакцина согласно изобретению может использоваться для прямого введения целевым человеку или не являющемуся человеком животному. Альтернативно жидкую вакцину согласно изобретению можно вводить целевым человеку или не являющемуся человеком животному в разбавленной форме. Этот последний вариант осуществления способа вакцинации согласно изобретению может облегчать манипулирование и введение посредством инъекции вследствие сниженной вязкости. Альтернативно или дополнительно, введение в разбавленной форме может снижать локальные реакции у целевых человека или не являющегося человеком животного, например, в результате раздражения тканей в области инокуляции.
Вакцинацию согласно изобретению можно проводить парентеральным путем, т. е. через кожу, например: внутримышечным, внутрибрюшинным, внутрикожным, субмукозальным или подкожным. Предпочтительным путем парентерального введения жидкой вакцинной композиции согласно изобретению является внутримышечная или подкожная инъекция.
Кроме того, жидкую вакцину по изобретению можно вводить энтеральным или мукозальным путем, т. е. через глазные капли, капли для носа, перорально, путем кишечного введения, посредством ороназальных капель, спрея, аэрозоля и т. д.
Альтернативно жидкую вакциную согласно изобретению можно вводить целевому организму способом массового введения, например, посредством питьевой воды, крупнораспыленной струи, распыления, с кормом и т. д. Следующей альтернативой является введение эмбрионам птиц посредством введения в яйцо.
Естественно, оптимальный путь введения жидкой вакцины согласно изобретению зависит от специфики используемой вакцины и от конкретных характеристик целевого организма. Специалист в данной области способен без труда выбрать и оптимизировать такой путь и способ введения.
Жидкую вакцину согласно изобретению можно вводить парентеральным путем в объеме, который является приемлемым для целевых человека или не являющегося человеком животного и, например, ее можно вводить в объеме от приблизительно 0,01 мл до приблизительно 10 мл. Предпочтительно одна доза представляет собой объем от приблизительно 0,05 мл до приблизительно 5 мл, более предпочтительно одна доза составляет от 0,1 мл до 3 мл.
При введении внутримышечным путем объем одной дозы предпочтительно составляет от приблизительно 0,5 мл до приблизительно 3 мл, более предпочтительно от приблизительно 1 мл до приблизительно 2 мл.
При введении внутрикожным путем объем одной дозы предпочтительно составляет от приблизительно 0,1 мл до приблизительно 0,5 мл, более предпочтительно приблизительно 0,2 мл.
При введении в яйцо объем одной дозы предпочтительно составляет от приблизительно 0,01 мл до приблизительно 0,5 мл, более предпочтительно приблизительно 0,05 мл.
Способ, расписание и объем введения жидкой вакцины согласно изобретению предпочтительно интегрируется в существующие планы вакцинации другими вакцинами, которые могут потребоваться целевым человеку или не являющемуся человеком животному для уменьшения стресса для целевого организма и снижения затраты на оплату труда. Эти другие вакцины могут быть введены одновременно, совместно или последовательно или способом, совместимым с их зарегистрированным применением.
Специалист в данной области без труда способен далее оптимизировать жидкую вакцину согласно изобретению. Как правило, это вовлекает адаптацию эффективности вакцины для дальнейшего улучшения ее предусматриваемой иммунной защиты. Это можно осуществлять, например, посредством адаптации дозы, объема или антигенного содержания вакцины, или путем применения посредством отличающегося пути, способа или режима. Все они входят в объем изобретения.
Далее изобретение описано посредством следующих неограничивающих примеров.
Примеры
Пример 1: Способы и материалы
1.1 Получение составов NADES
NADES можно получать путем смешения желаемых компонентов, которое может быть ускорено нагреванием и/или добавлением небольшого количества воды. Образцы NADES, которые далее тестировали и которые описаны в настоящем описании ниже, получали путем растворения соответствующих соединений в воде посредством обработки ультразвуком на водяной бане. Требуемые количества соединений добавляли в колбу. Колбу кратковременно качали или встряхивали для смешения порошков. Далее добавляли требуемое количество воды. Эту смесь помещали на водяную баню с обработкой ультразвуком, установленную на 45 °C, обрабатывая ультразвуком в течение вплоть до нескольких часов до получения NADES. В ходе обработки ультразвуком можно было достигнуть температур обработки ультразвуком вплоть до 80°.
1.2 Измерение водной активности
Образцы
Для целей биологический защиты измеряли водную активность образцов препаратов NADES без живых бактерий. Однако, зная количество водной бактериальной композиции, которое будет добавлено к NADES для получения жидкой вакцинной композиции согласно изобретению, может быть вычислена конечная водная активность комбинации NADES и бактериальной композиции согласно Dai et al. (2015, Food Chem., vol. 187, p. 14-19).
Получение образцов
Некоторое количество образца NADES переносили в 10-мл стеклянный флакон для достижения высоты заполнения приблизительно 1/4 флакона. Для каждого образца флаконы с кодом заполняли в двух экземплярах. Флаконы закрывали с использованием алюминиевой обжимной крышки с пробкой из PTFE и помещали при комнатной температуре в течение 12 ч для достижения равновесия между образцом и свободным пространством.
Оборудование
Давление водяного пара в свободном пространстве образцов определяли с использованием анализатора влажности/давления LighthouseTM FMS-1400. Образцы помещали в камеру для образцов как есть. Перед измерением в образце систему откалибровывали с использованием стандартов калибровки давления свободного пространства в диапазоне aw 0-0,2. Также использовали насыщенные солевые стандарты для калибровки и перевычисления нелинейного диапазона aw 0,2-1.
Калибровка
Для калибровки устройства на протяжении полного диапазона aw 0-1 и для получения эталонной линии величин водной активности проводили измерение для ряда стандартных образцов: помимо чистой воды использовали 5 образцов конкретных насыщенных солевых растворов, и для каждого из 6 стандартов проводили 3-кратное измерение дублированных образцов. Путем установки измеренной величины для чистой воды на 1000, другие стандартные величины были определены как aw 0,8511, 0,7547, 0,5438, 0,3307 и 0,1131. Также проводили измерение для серии сертифицированных стандартов давления пара.
Результаты измерений aw включены в таблицу 1.
1.3 Тестирование профиля DSC для NADES
Анализ посредством дифференциальной сканирующей калориметрии (DSC) проводили на устройстве Q2000 DSC от TA Instruments программного обеспечения Thermal Analysis. Для полного профиля DSC образцы сначала уравновешивали при 40 °C и охлаждали до -90 °C при 5 °C/мин с последующим уравновешиванием в течение 5 мин при -90 °C, после чего образцы вновь нагревали до 40 °C при 5 °C/мин. Этот цикл охлаждения и нагрева повторяли второй раз для того же образца для изучения фазового гистерезиса. Tg образца определяли посредством программного обеспечения из кривой нагрева по средней точки пошагового сдвига от исходного уровня, указывающей на изменение термической проводимости вследствие повышенной подвижности в ходе перехода в стеклообразное состояние.
Репрезентативный профиль DSC NADES в рамках изобретения представлена на фиг.1 для NADES, образованного при молярном соотношении пролина, сорбита и воды 1:1:2,5.
На фиг. 1 представлен резкий сдвиг исходной линии, в данном случае между -41 и -45 °C, который указывает на переход в стеклообразное состояние, который соответствует свойствам эффективного NADES по изобретению. Этот профиль по существу отличается от профиля, представленного Qiao et al. (выше) на их фиг.4 для NADES, который был чрезмерно разбавлен и стал водной композицией; который демонстрирует по существу ровную исходную линию с повышением и снижением теплового потока при образовании и плавлении ледяных кристаллов воды; так называемой "холодовой кристаллизации".
1.4 Смешение NADES и бактериальных композиций
Препараты NADES смешивали 9+1 об./об. с бактериальными композициями в ламинарном боксе. Образцы либо осторожно перемешивали с использованием роликового наклонного смесителя; либо встряхивали; либо кратковременно перемешивали с использованием стерильной инокуляционной петли, в зависимости от размера образца. Из этих образцов 1-миллилитровыми аликвотами заполняли 3-миллилитровые стеклянные флаконы, которые закрывали резиновой пробкой и металлической крышкой.
1.5 Анализ стабильности
Для каждого тестируемого образца уникальный флакон хранили в условиях охлаждения (2-8 °C), условиях замораживания (-20 °C) или при комнатной температуре (20 °C). После определенного периода флакон открывали и получали серийное десятикратное разведение в PBS от 10^-1 до 10^-10. Для по меньшей мере трех разведений 50-микролитровый образец высевали на чашки с агаром, поддерживающие рост определенных бактерий, в двух экземплярах. Затем чашки инкубировали при 37 °C и 5% CO2 в течение 5-8 сут. до тех пор, пока размер колоний не становился достаточным для подсчета. Из этого вычисляли титр Mollicutes, тем самым было подсчитано от 30 до 300 колоний. Титр выражали в качестве колониеобразующих единиц на мл образца (к.о.е./мл). Из точек данных для различных флаконов, которые были протестированы в различные моменты времени, строили график данных стабильности, как представлено на фиг. 2 и 3.
Пример 2: Композиция NADES для применения в рамках изобретения
Получали большое количество различных композиций NADES для применения в рамках изобретения с различными соединениями, с различными молярными соотношениями и с различным содержанием воды.
В таблице 1 ниже приведено количество наиболее эффективных составов NADES; эти составы обеспечивали прозрачные жидкие растворы, которые были жидкими при комнатной температуре (приблизительно 20 °C). Представлены детали, касающиеся их состава и содержания воды. Для нескольких из полученных образцов определяли водную активность, и результаты включены.
Таблица 1. Композиции и свойства репрезентативного количества NADES по изобретению
масс.)
Пример 3: Результаты анализа стабильности бактерий
Для бактерий M. synoviae и M. gallisepticum, находившихся в жидких композициях согласно изобретению проводили анализ стабильности на протяжении длительного периода времени, и при температурах 2-8 °C и при комнатной температуре (приблизительно 20 °C).
Инкубация при комнатной температуре в течение 8 недель может служить в качестве ускоренного теста стабильности, указывающего на эффект инкубации в течение 1-2 лет при 4 °C. Таким образом, это является очень существенным воздействием на жизнеспособность бактерий, и ожидалось, что не все образцы выживут в этих условиях.
Заключения из результатов стабильности
Присущая как бактериям M. synoviae, так и бактериям M. gallisepticum, низкая стабильность в ходе хранения была продемонстрирована посредством контроля, представляющего собой смесь 1+9 об./об. в стандартном фосфатно-солевом буфере (PBS). См. фиг. 2 и 3 для иллюстративных деталей. В этой контрольной жидкой композиции уже в первый протестированный момент времени нельзя было выявить бактериальные колонии ни в одном из исследованных разведений. Это относилось к условиям хранения как при 2-8 °C, так и при к.т.
Для этих контрольных образцов было сделано заключение, что отсутствовала поддающаяся обнаружению выживаемость либо M. synoviae, либо M. gallisepticum, в PBS.
Неожиданно, и в противоположность контролям в виде PBS, как M. synoviae, так и M. gallisepticum продемонстрировали поразительную выживаемость при комбинировании с NADES в жидкой композиции согласно изобретению. При смешении 1+9 об./об. с различными NADES были получены поддающиеся измерению титры при хранении при 20 °C вплоть до 8 недель.
Для M. synoviae стабилизирующий эффект при 20 °C был наиболее выраженным для NADES с бетаином:сорбитом:WFI в молярном соотношении 1:1:2,5, и сорбитом:ксилитом:трегалозой:WFI в молярном соотношении 2:2:1:10. При хранении при 2-8 °С в течение вплоть до 6 месяцев были обнаружены поразительные титры выживаемости с потерями менее чем 3 Log10 к.о.е./мл для нескольких NADES.
Для M. gallisepticum стабилизирующий эффект при 20 °C был наиболее выраженным в случае NADES с аргинином:сорбитом:WFI в молярном соотношении 1:2:6, и с пролином:сорбитом:WFI в молярном соотношении 1:1:2,5. При хранении при 2-8 °C в течение вплоть до 3 месяцев были обнаружены поразительные титры выживаемости с потерями менее 3 Log10 к.о.е./мл для нескольких NADES.
Пример 4: Введение NADES экспериментальным животным
Для оценки простоты введения и безопасности NADES для применения в рамках изобретения у целевых животных, иллюстративные NADES вводили экспериментальным животным и обрабатывали посмертные материалы.
Для этой цели получали и тестировали два варианта NADES на основе пролина : сорбита: один с высокой вязкостью (NADES 3A) и один с низкой вязкостью (NADES 3B). Они служили для сравнения свойств NADES при введении по изобретению в двух крайних точках спектра вязкости. Характеристики NADES 3A приведены в таблице 2. Кроме того, его вязкость измеряли с использованием стандартных условий: при приблизительно 20 °C с использованием вискозиметра BrookfieldTM DV-I+, используя веретено типа № 62, в течение 30 секунд при 60 об/мин в стандартной чаше для измерения объемом приблизительно 80 мл.
Манипулирование
Высоковязкий NADES 3A можно было протолкнуть через иглу для подкожных инъекций размера 21G или менее, т. е. иглу с наружным диаметром 0,8 мм или более.
Таблица 2. Составы NADES, протестированные посредством введения животным
Подкожное введение in vivo
Составы NADES 3B и 3C вводили посредством подкожной инъекции в исследовании безопасности у собак. Особое внимание уделяли неблагоприятным реакциям, которые могли возникнуть после введения составов стабилизаторов, либо локально, либо системно.
Оба состава получали, как описано выше, путем нагрева и обработки ультразвуком пролина, сорбита и воды для инъекций в закрытом флаконе, получая прозрачную и однородную жидкость. Кроме того, их подвергали стерилизации фильтрованием, и определяли их биологическую нагрузку и уровни эндотоксинов. Было обнаружено, что оба состава имели показатели ниже стандарта с наиболее низким разведением 1 единица/мл, удовлетворяя основным критериям соответствия для стерильных составов. Состав NADES 3C получали путем разбавления 1 объемной части NADES 3A 9 объемными частями WFI, получая состав с соотношением пролин:сорбит:WFI 1:1:5 и вязкостью 289 мПа⋅с. NADES 3B имеет вязкость 33,4 мПа⋅с.
Шесть здоровых собак породы бигль в возрасте 7 месяцев разделяли на две группы по 3 собаки. Каждой группе назначали состав NADES, и им проводили введение двух доз по 1 мл назначенного состава с использованием 1-миллилитрового шприца и иглы 21G 5/8 посредством подкожной инокуляции с двухнедельным интервалом. Собакам группы 1 вводили низковязкий NADES 3B, и собакам группы 2 вводили высоковязкий NADES 3C. Всех собак подвергали клиническому мониторингу каждые сутки на протяжении испытания, включая локальные реакции в области инокуляций.
Вакцинации проводили в загривок шеи; первую вакцинацию проводили в шею слева, а вторую вакцинацию проводили в шею справа. Области вакцинации выбривали перед каждым введением, и область инъекции обводили фломастером. Не наблюдали дискомфорта в ходе какой-либо из инъекций. Через 4 ч после инъекции области инъекции пальпировали, и мало материала пальпировалсь или материал не пальпировался в областях инъекций, и не наблюдали опухания или покраснения.
Ректальные температуры измеряли на сутки -3, -2, -1 перед каждой из вакцинаций; в день вакцинации: непосредственно перед вакцинацией и через 4 ч после вакцинации; и каждые сутки в течение семи суток после вакцинации.
На протяжении всего исследования не наблюдали значительного повышения температуры тела у каких-либо из собак и не наблюдали клинических неблагоприятных эффектов.
Заключение: инокуляция NADES составов 3C или 3B посредством подкожного пути собакам не индуцировала никакой неблагоприятной реакции после инокуляции, ни локально, ни системно.
Интраназальное введение
Два состава NADES: 3A и 3B тестировали в отношении их паттерна распределения на поверхности слизистой оболочки носа при введении интраназально. Оба состава NADES тестировали как есть без добавления воды. Следовательно, NADES 3A имеет вязкость 5197 мПа⋅с, и NADES 3B имеет вязкость 33,4 мПа⋅с. К 30 мл каждого состава NADES добавляли краситель "запатентованный синий" на кончике шпателя для достижения темно-синего цвета. В качестве контроля использовали PBS без красителя.
Головы телят получали посмертно от телят в возрасте приблизительно 2-4 недель. Введение проводили удерживая голову в прямом положении, имитирующем положение теленка в ходе и/н вакцинации в полевых условиях с наклоном ноздрей несколько вверх.
Затем жидкости вводили в соответствии со стандартной методикой интраназальной вакцинации, при которой 2,5-миллилитровый шприц без иглы, содержавший 1,5 мл жидкости, помещали в ноздрю, а затем жидкость впрыскивали одним равномерным потоком. Далее голову рассекали на две половины и перегородку извлекали и исследовали в отношении наличия синего цвета во внутриносовых путях.
Для всех образцов было обнаружено, что синяя жидкость легко проходила через носовые пути. Низкая вязкость образца PBS обеспечивала простоту инъекции, однако вся жидкость проходила насквозь быстро. Синий цвет наблюдали по всей носовой полости, включая начало трахеи.
Инъекция NADES 3A с очень высокой вязкостью через шприц отнимала мало усилий. Также, как и ожидалось, больше времени уходило на появление синей жидкости ниже головы. После рассечения головы было обнаружено, что также эта вязкая жидкость распределилась равномерно во внутриносовых путях, где оказалось, что она образовывала толстый слой, оставляя больше материала в носовых путях. Это указывает на то, что будет происходить лучшее удержание и меньший переход в верхние дыхательные пути при введении живому теленку в ходе и/н вакцинации.
Эффект введения состава NADES 3B с низкой вязкостью в высокой степени напоминал эффект введения образца PBS, где жидкость проходила через носовую полость.
Заключение: было возможно осуществить мониторинг распределения окрашенных препаратов с различной вязкостью после интраназальной инъекции в головы телят. Распределение жидкости, судя по синему цвету, было сравнимым для двух препаратов NADES и PBS, причем существовало некоторое отличие в отношении простоты введения и количества остаточного материала и состав NADES 3A было несколько труднее впрыскивать, но он обеспечивал более густой слой остатка в носовых путях. Это указывает на то, что может быт достигнуто замедленное высвобождение антигена из таких вязких составов NADES.
Пример 5: Сравнительное измерение на водном стабилизаторе
Получали композицию водного стабилизатора, как описано в WO 2015/121463, имевшую: 30% масс./масс. сорбита+0,6 M аргинина в 0,04 M PBS. Эту композицию тестировали в отношении ее свойств, таких как водная активность и профиль DSC, чтобы уточнить, что она не обладает характерными признаками, которые определяют композицию композиция NADES, как определено и описано выше.
Водная активность
Определение aw проводили посредством измерения давления пара в свободном пространстве, как описано в WO 2019/122329, пример 1. Результат водной активности определяли в двух повторениях с получением среднего aw 0,89. Очевидно, этот высокий уровень доступной воды демонстрирует, что эта композиция не является NADES. Определение aw проводили посредством измерения давления пара в свободном пространстве, как описано в WO 2019/122329, пример 1. Результат водной активности определяли в двух повторениях с получением среднего aw 0,89. Очевидно, этот высокий уровень доступной воды демонстрирует, что эта композиция не является NADES.
Профиль DSC
Определение профиля DSC в водном стабилизаторе уровня техники проводили, как описано в настоящем описании в примере 1.3.
Результаты представлены на фиг.4, причем (как на фиг. 1 настоящего описания) на верхней горизонтальной части графика представлена фаза охлаждения от 40 °C до -90 °C при 5 °C/мин (справа налево), и на нижней горизонтальной части фазы нагревания от -90 °C до 40 °C при 5 °C/мин (слева направо).
В ходе охлаждения наблюдается массивная и внезапная кристаллизация свободной воды в воду при температуре приблизительно -27 °C. Далее при повторном нагревании наблюдался типичный профиль плавления кристаллов льда при -5,5 °C.
Кроме того, на фиг. 4, в ходе фазы нагрева горизонтальная исходная линия после плавления льда возвращается на тот же уровень, на котором она была до плавления. Это означает, что не происходило изменения теплоемкости в этом образце, что прямо отличается от пошагового сдвига от исходного уровня, который обычно наблюдается в случае перехода в стеклообразное состояние.
Также является значительным, что плавление льда на фиг.4 происходит при значительно более высокой температуре (-5 °C), чем переход в стеклообразное состояние согласно фиг. 1 (-45 °C), вновь иллюстрируя, что образец, протестированный согласно фиг.4, не был глубокой эвтектической смесью.
На фиг. 4 все из обоих пиков, высокой температуры плавления и возвращения исходной линии к ее предшествующему уровню указывают на образование и плавление кристаллов льда и, таким образом, демонстрируют, что протестированная композиция имела значительное количество присутствующей свободной воды, и, таким образом, не была NADES.
Однако напротив, в образце согласно фиг.1 (NADES согласно изобретению) не происходило образование или плавления ледяных кристаллов, и был обнаружен отчетливый сдвиг перехода в стеклообразное состояние.
Пример 6: Дополнительные результаты стабильности: M. bovis
Следующий вид бактерий Mollicutes тестировали в отношении стабилизации в жидких композициях согласно изобретению: Mycoplasma bovis. Эксперименты проводили, по существу как описано в настоящем описании в примерах 1-3 для M. synoviae и M. gallisepticum.
Результаты анализов стабильности в различных композициях согласно изобретению либо при комнатной температуре, либо при 2-8°C, представлены на фиг.5:
панель A: комнатная температура, вплоть до 10 недель; и
панель B: 2-8 °C, инкубация вплоть до 26 недель.
Начальный титр составлял 9,9 Log10 к.о.е./мл. В PBS (отрицательный контроль) наблюдали некоторую выживаемость в ходе инкубации в течение двух недель, как при комнатной температуре, так и при охлаждении. Однако из образцов, инкубированных в течение более длительных периодов в PBS, более нельзя было извлечь жизнеспособных клеток.
При комнатной температуре была достигнута хорошая первоначальная стабильность (инкубация в течение 2-4 недель) в нескольких из композиций NADES. Однако наилучшие результаты были выявлены при использовании аргинина : сорбита : воды (2:1:6), которые были способны стабилизировать эти бактерии в течение по меньшей мере 10 недель при комнатной температуре.
При инкубации при охлаждении наблюдали сходную картину: хорошая первоначальная стабилизация в течение 6-13 недель наблюдалась для нескольких протестированных композиций. Наилучшим длительным стабилизатором (инкубация в течение 26 недель) также был аргинин : сорбит : вода (2:1:6), хотя отличия, наблюдаемые между различными протестированными композициями, не были настолько значительными, как и в случае инкубации при комнатной температуре.
В целом, M. bovis могли быть эффективно стабилизированы без лиофилизации в жидких композициях согласно изобретению при различных температурах хранения, превышающих заморозку.
Пример 7: Результаты расширенного теста стабильности
Результаты теста стабильности для M. synoviae и M. gallisepticum в жидких композициях согласно изобретению получали после продолжительной инкубации вплоть до 1 года при 2-8 °C. Эти данные получены для серии образцов, как описано в примере 3, и распространяются на результаты, представленные на фиг. 2B и 3 B настоящего описания.
Расширенные результаты представлены на фиг. 6:
панель A: M. synoviae при 2-8 °C вплоть до 54 недель; и
панель B: M. gallisepticum при 2-8 °C при инкубации вплоть до 52 недель.
Для M. synoviae, три из протестированных жидких композиций согласно изобретению могут стабилизировать жизнеспособность этих бактерий в течение по меньшей мере года при 2-8 °C; причем пролин : сорбит : вода (1:1:2,5) и бетаин : сорбит : вода (1:1:2,5) продемонстрировали те же конечные результаты.
Для M. gallisepticum, жизнеспособные бактерии сохранялись только до 52 недель инкубации при 2-8 °C в бетаине : сорбите : воде (1:1:2,5).
Описание чертежей
Фиг. 1
Профиль дифференциальной сканирующей калориметрии NADES, полученного при молярном соотношении пролина, сорбита и воды 1:1:2,5.
Фиг. 2
Результаты стабильности для Mycoplasma synoviae в жидких композициях с различными NADES.
Панель A: инкубация при комнатной температуре; панель B: инкубация при 2-8 °C.
Фиг. 3
Результаты стабильности для Mycoplasma gallisepticum в жидких композициях с различными NADES.
Панель A: инкубация при комнатной температуре; панель B: инкубация при 2-8 °C.
Фиг. 4
Профиль DSC для водного стабилизатора уровня техники, содержащего 30% масс./масс. сорбита и 0,6 M аргинина в 0,04 M PBS.
Фиг. 5
Данные стабильности для M. bovis в NADES при комнатной температуре (A) и при 2-8 °C (B).
Фиг. 6
Данные длительной стабильности M. synoviae (A) и M. gallisepticum (B) в NADES при 2-8 °C.

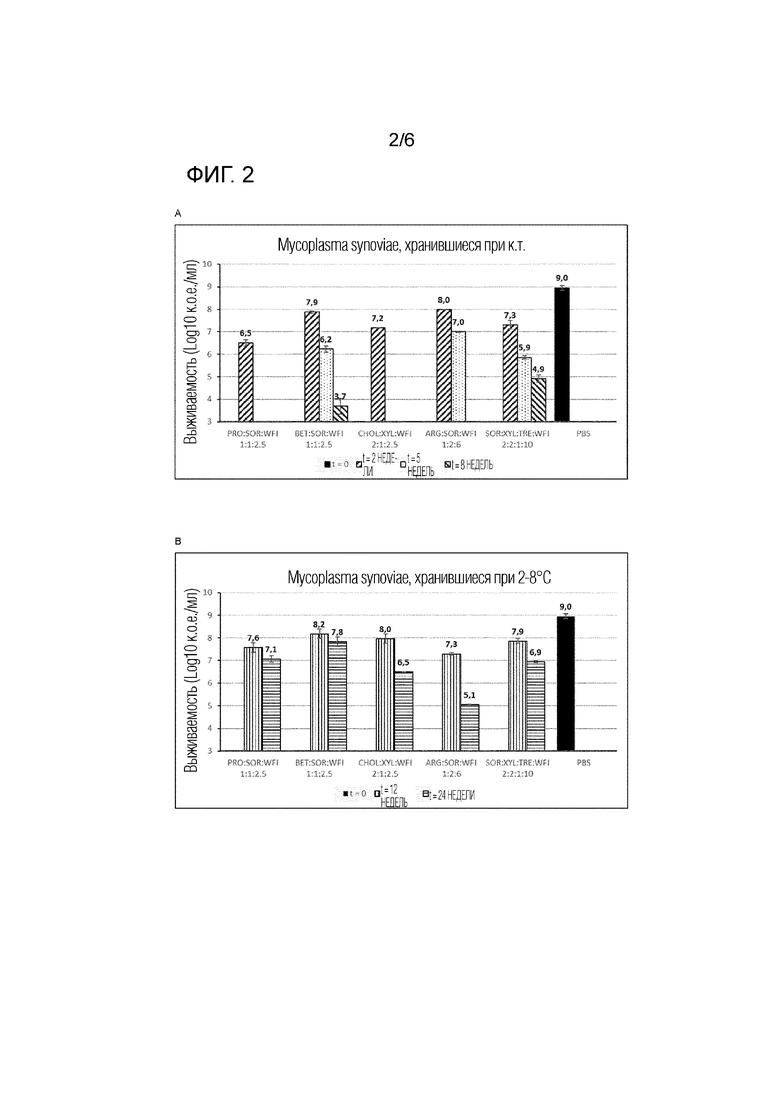


Группа изобретений относится к фармацевтике и медицине, и может быть использована для вакцинации против инфекции или заболевания, вызываемых бактериями Mollicutes. Предложена жидкая композиция для защиты от инфекции или заболевания, вызываемых бактериями Mollicutes, содержащая живые бактерии Mollicutes и стабилизатор, представляющий собой натуральный глубокий эвтектический растворитель (NADES), причем композиция имеет водную активность 0,85 или менее и содержание воды 50% масс./масс. или менее. Предложены также способ получения указанной композиции и применение ее в качестве вакцины, применение NADES в качестве фармацевтически приемлемого носителя для получения указанной вакцины, набор для вакцинации и способ вакцинации. Изобретение обеспечивает эффективную стабилизацию живых бактерий Mollicutes без необходимости замораживания или лиофилизации. 9 н. и 6 з.п. ф-лы, 6 ил., 2 табл., 7 пр.
1. Жидкая композиция для защиты от инфекции или заболевания, вызываемых бактериями Mollicutes, содержащая живые бактерии Mollicutes и стабилизатор, отличающаяся тем, что стабилизатор представляет собой натуральный глубокий эвтектический растворитель (NADES), тем, что композиция имеет водную активность 0,85 или менее, и тем, что композиция имеет содержание воды 50% масс./масс. или менее.
2. Жидкая композиция по п. 1, отличающаяся тем, что NADES содержит органическую соль и многоатомный спирт.
3. Жидкая композиция по п. 1, отличающаяся тем, что NADES содержит два или более соединений, все из которых являются многоатомными спиртами.
4. Жидкая композиция по п. 2 или 3, отличающаяся тем, что многоатомный спирт представляет собой сахар или сахарный спирт.
5. Жидкая композиция по любому из пп. 2-4, отличающаяся тем, что сахар выбран из сахарозы и трегалозы, или тем, что сахарный спирт является одним или несколькими, выбранными из эритрита, ксилита и сорбита.
6. Жидкая композиция по п. 2, отличающаяся тем, что органическая соль является одной или несколькими, выбранными из солей бетаина, пролина, холина, метионина и аргинина.
7. Жидкая композиция по любому из пп. 1-6, отличающаяся тем, что бактерии Mollicutes являются аттенуированными в отношении их патогенных свойств.
8. Способ получения жидкой композиции по любому из пп. 1-7, включающий стадии:
a) получения NADES и
b) смешения указанного NADES с живыми бактериями Mollicutes.
9. Применение жидкой композиции по любому из пп. 1-7 или которая может быть получена способом по п. 8 в качестве вакцины против инфекции или заболевания, вызываемых бактериями Mollicutes.
10. Жидкая вакцина для применения против инфекции или заболевания, вызываемых бактериями Mollicutes, причем вакцина содержит жидкую композицию по любому из пп. 1-7 или которая может быть получена способом по п. 8.
11. Применение NADES в качестве фармацевтически приемлемого носителя в жидкой вакцине по п. 10.
12. Применение NADES для получения жидкой вакцины по п. 10.
13. Набор для вакцинации против инфекции или заболевания, вызываемых бактериями Mollicutes, содержащий по меньшей мере два контейнера, причем один из контейнеров содержит жидкую вакцину по п. 10, а другой контейнер содержит жидкий разбавитель.
14. Применение жидкой вакцины по п. 10 для защиты целевых человека или не являющегося человеком животного против инфекции и/или заболевания, вызываемых патогенной формой живых бактерий Mollicutes, содержащихся в указанной жидкой вакцине.
15. Способ вакцинации мишени, представляющей собой человека или не являющегося человеком животного, против инфекции или заболевания, вызываемых бактериями Mollicutes, включающий введение указанной мишени жидкой вакцины по п. 10 или включает применение набора по п. 13.
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| K.RADOŠEVIĆ et al | |||
| Antimicrobial, cytotoxic and antioxidative evaluation of natural deep eutectic solvents | |||
| Environmental Science and Pollution Research, 2018, 25:14188-14196 | |||
| Y.QIAO et al | |||
| Effects of natural deep eutectic solvents on lactic acid | |||
Авторы
Даты
2024-07-01—Публикация
2020-03-27—Подача