Изобретение относится к медицине, а именно экспериментальной онкологии, конкретно к способам подавления роста опухолевых клеток рака простаты.
В настоящее время онкологические заболевания являются одной из ведущих причин смертности во всем мире. В порядке убывания рак молочной железы, рак легких и бронхов, рак предстательной железы, толстой и прямой кишки, анальный, меланома кожи, рак мочевого пузыря, неходжкинская лимфома, рак почек и малого таза, рак эндометрия, лейкемия, рак поджелудочной железы, рак щитовидной железы и печени являются наиболее распространенными новыми случаями рака в 2018 году.
Основная причина возникновения злокачественных новообразований заключается в перерождении клетки из-за изменения функций генов, контролирующих рост клетки. В результате чего трансформированная клетка начинает неконтролируемо делиться, избегая пути восстановления и апоптоза (запрограммированной гибели клеток). Имеющиеся способы терапии злокачественных новообразований базируются на разрушении клеточных мембран, энергетических депо клеток, представленных митохондриями, генетического аппарата опухолевых клеток и др., то есть на прекращении различных путей становления проопухолевой активации клетки. У существующих методов, включающих использование различных физических факторов, существует явный недостаток - уничтожение нормальных тканей, окружающих опухоль, которые приводят к негативным последствиям. Следовательно, проблема повышения эффективности лечения злокачественных новообразований и снижения побочных эффектов является чрезвычайно актуальной.
В настоящее время известно несколько способов торможения роста опухолевых клеток с применением низкотемпературной плазмы, при которых рабочим газом выступает гелий [1]. Известен метод разрушения солидных опухолей посредством плазмы [2], при котором проводится интраоперационная плазменная обработка ложа опухоли. В этом случае без предварительного использования радио- или химиотерапии настоящий способ осуществить нельзя.
Наиболее близким к предлагаемому выбран способ, описанный в патенте US №20170319256, опубл. 2017 [3]. В известном способе в качестве повреждающего агента используется холодная плазма с импульсным напряжением 1-2 кВт, скоростью воздушного потока 400-600 мл/мин, частотой следования импульсов 40-60 кГц. Подобного рода низкотемпературная плазма позволяет снижать рост опухолевых клеток рака кожи, головы и шеи, лейкоза, мезотелиомы, рака легкого, колоректального рака, рака шейки матки и других. Область применения известного способа ограничена, поскольку его использование включает предварительную подготовку клеток, путем обработки клеток ингибиторами киназ и синхронизацию с циркадным ритмом нормальных клеток, что трудно выполнить в условиях целого организма, либо трудно выполнимо без хирургического вмешательства. Кроме того, недостатком описанных способов является невозможность исключить влияние электромагнитных полей и ультрафиолетового излучения.
Новый технический результат - расширение арсенала способов позволяющих для подавлять пролиферативную активности опухолевых клеток простаты.
Для достижения нового технического результата в способе подавления роста опухолевых клеток рака предстательной железы воздействуют плазмой на культуру клеток, причем воздействуют низкотемпературной неравновесной плазменной струей с разрядом в воздушном потоке, с параметрами источника: импульсным напряжением до 15 кВ, длительностью импульса 1 мкс, частотой следования импульсов в диапазоне от 0,5 кГц до 4,2 кГц, воздушный поток до 0,05 г/с со скоростью 3 мл/мин.
Способ осуществляют следующим образом.
Использовали культуру опухолевых клеток РС-3 (аденокарцинома простаты, Российская коллекция клеточных культур позвоночных, ИНЦ РАН, Санкт-Петербург), которые культивировали в чашках Петри площадью 9,2 см2 в полной питательной среде RPMI-1640, содержащей 10% инактивированной эмбриональной телячьей сыворотки и антибиотики (50 ед/мл пенициллина и 50 мкг/мл стрептомицина), при температуре 37°С с 5% содержанием СО2, во влажной среде с концентрацией клеток 150 тыс/мл. Опухолевые клетки рака простаты обрабатывали с использованием генератора плазменных струй с определенными режимами, имеющими частоту следования импульсов напряжения в диапазоне от 0,5 до 4,2 кГц и время экспозиции 120 с, осуществляемых при стандартной температуре и давлении.
Через 24 часа опухолевые клетки в РС-3 обрабатывали с использованием генератора плазменных струй.
Для получения низкотемпературной неравновесной плазменной струи используют разряд в воздушном потоке. Параметры источника: импульсное напряжение - до 15 кВ, длительность импульса - 1 мкс, частота следования импульсов в диапазоне от 0,5 кГц до 4,2 кГц, воздушный поток - до 0,05 г/с со скоростью 3 мл/мин.
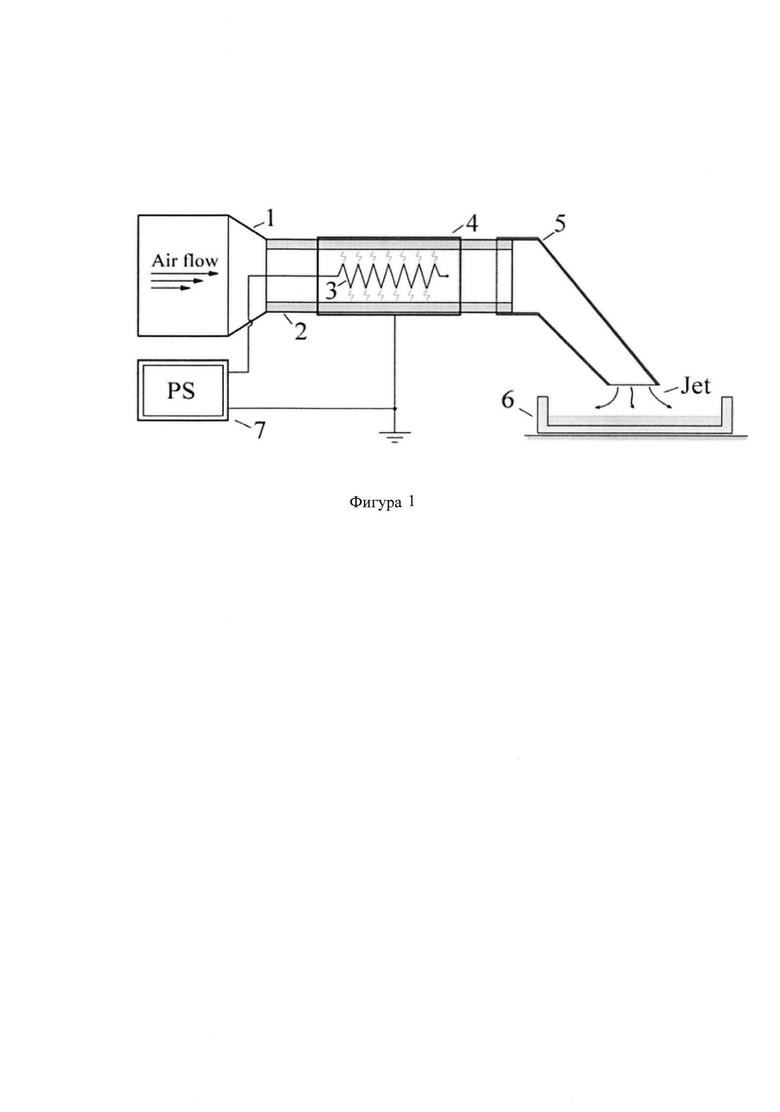
Способ реализуют с помощью экспериментального плазменного струйного устройства, схема которого изображена на Фиг. 1, где: 1 - компрессор, 2 - кварцевая трубка, 3 - потенциальный электрод, 4 - заземленный электрод, 5 - сопло (силикон), 6 - чашка Петри с обрабатываемой средой, 7 - высоковольтный источник питания.
Плазменное струйное устройство на Фиг. 1 состоит из кварцевой трубки внутренний диаметр 10 мм, толщина стенки около 1 мм, которая имеет спиралевидный внутренний электрод из нержавеющей стали диаметром проволоки 0,5 мм, диаметр катушки 5 мм, длина катушки 25 мм и внешний электрод из алюминиевой фольги. Источник питания 7 обеспечивает импульсное напряжение величиной до 15 кВ и длительность импульса около 1 мкс. Частоту следования импульсов в диапазоне от 0,5 кГц до 4,2 кГц. Воздушный поток до 0,05 г/с, создаваемый компрессором 1, позволяет формировать плазменную струю и обеспечивать перенос плазмоактивированной среды через сопло 5 на подложку с чашкой Петри 6.
Заземленный электрод 4, в виде изогнутой насадки изготовлен из силиконовой трубки длиной 15 см с внутренним диаметром 10 мм. Таким образом, область плазмы разряда расположена на расстоянии 1 см от выходного отверстия сопла, поэтому на выходе из системы отсутствуют электрические поля или заряженные частицы. В результате обработка клеток производится образующимися в плазме химически активными соединениями, например, озоном с расчетной концентрацией менее 0,1 промилле, оксидами азота и другими формами. Эти соединения обладают высокой реакционной способностью и могут изменять физиологическое состояние клеток.
На выходе сопла устройства получается смесь из заряженных ионов и радикалов, в частности, соединений кислорода и азота, которые активно вступают в реакцию с компонентами питательной среды RPMI-1640 и попадают внутрь клеток, находящихся в ней, тем самым воздействуя на структурные компоненты клеток и их метаболизм.
Для оценки пролиферативной активности клеток использовали несколько методов. Метод МТТ-теста, основанный на превращении водорастворимого соединения МТТ (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида) в нерастворимый продукт формазана в процессе клеточного дыхания. Оценка апоптической/некротической гибели основана на соединении флуоресцентных меток с соответствующими клеточными компонентами. Установлено, что предлагаемый способ позволяет тормозить пролиферативную активность опухолевых клеток на 85%.
Основная причина возникновения злокачественных новообразований заключается в перерождении клетки из-за изменения функций генов, контролирующих рост клетки. В результате чего трансформированная клетка начинает неконтролируемо делиться, избегая пути восстановления и апоптоза (запрограммированной гибели клеток). Имеющиеся способы терапии злокачественных новообразований базируются на разрушении клеточных мембран, энергетических депо клеток, представленных митохондриями, генетического аппарата опухолевых клеток и др., то есть на прекращении различных путей становления проопухолевой активации клетки. У существующих методов, включающих использование различных физических факторов, существует явный недостаток - уничтожение нормальных тканей, окружающих опухоль, которые приводят к негативным последствиям. Следовательно, проблема повышения эффективности лечения злокачественных новообразований и снижения побочных эффектов является чрезвычайно актуальной.
Решением проблемы может послужить использование нового способа терапии онкологических заболеваний, который бы позволил сохранить противоопухолевый эффект при минимальном негативном влиянии на окружающие опухоль здоровые ткани - применение низкотемпературных плазменных струй, получаемых на основе разрядов атмосферного давления в потоке газа как физического фактора воздействия на опухоль. Плазменные струи формируются на выходе электродной системы в условиях, когда газ проходит через область плазмы разряда [4]. В струе содержится различные химически и биологически активные частицы, что обуславливает широкий спектр применения таких систем [5]. Установлено, что благодаря наличию в плазме свободных радикалов и активных молекул она может применяться в биомедицинских исследованиях, связанных со стерилизацией, изменением свойств поверхности биоматериала, заживлением ран, свертыванием крови, а также лечением рака [5-8]. Обзор имеющейся литературы в области терапии злокачественных новообразований показал, что после прямого воздействия низкотемпературной плазмой в различных дозах на опухолевые клетки наблюдается противоопухолевый эффект для различных типов рака in vitro и in vivo [9-13]. Было отмечено, что плазма может не только продуцировать активные радикалы в окружающую среду, но и индуцировать генерацию активных форм кислорода (АФК) в клетках, приводя к их гибели [7, 27]. Кроме того, отличительной особенностью плазмы является ее селективное воздействие на различные типы клеток, выраженное в подавлении роста опухолевых клеток за счет индукции апоптоза и стимуляции функций здоровых, например, стволовых [14, 15 + Арндт, С., М. + Lee, J. II., J. Y Om, Y Н. Ким и др.,].
В предлагаемом способе воздействие плазмой включает нанесение ионизированного газа, получаемого на выходе из системы на опухолевые клетки простаты, т.е. действие производится за счет химически активных агентов, включающих в себя соединения кислорода и азота, а не за счет вышеприведенных факторов. Полученная композиция реакционноспособных соединений является избирательно действующим цитотоксическим агентом в отношении разных линий опухолевых клеток, в частности, в настоящем изобретении использовалась культура опухолевых клеток РС-3 (аденокарцинома простаты, Российская коллекция клеточных культур позвоночных, ИНЦ РАН, Санкт-Петербург),
Результаты воздействия представлены на Фиг 2-5
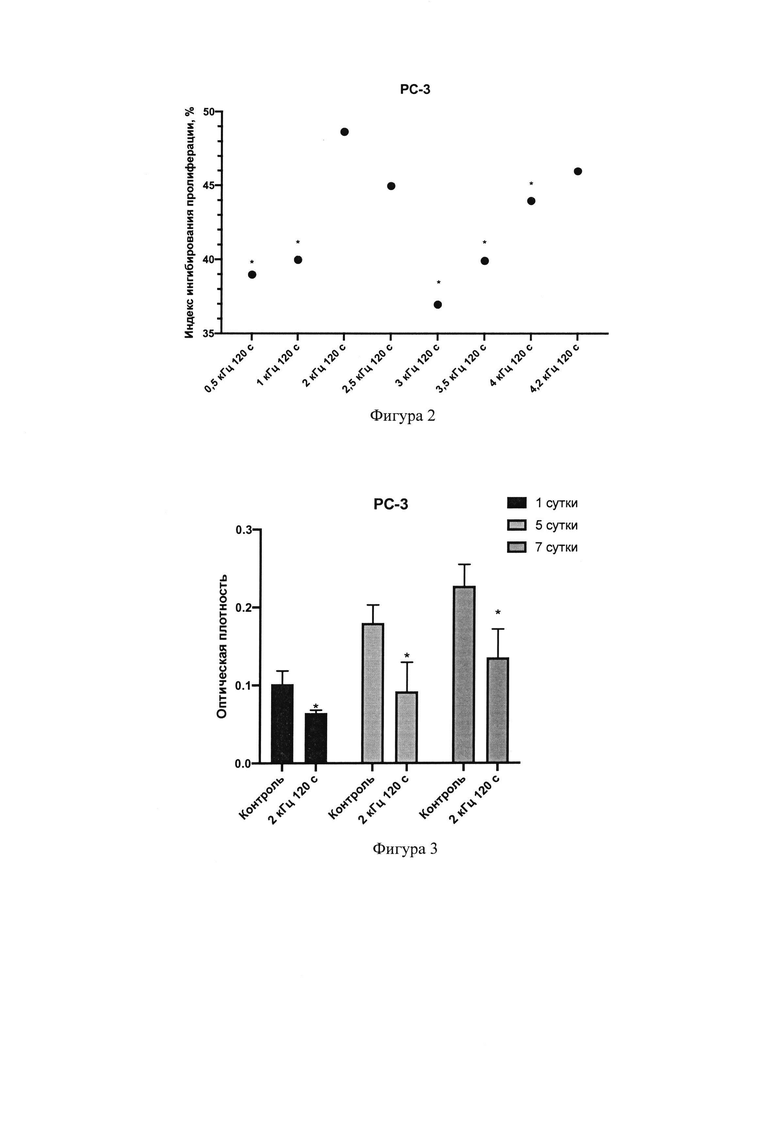
Фигура 2 - Индекс ингибирования пролиферативной активности клеток на 1-е сутки после воздействия плазменной струи атмосферного давления с разными частотами разряда.
Примечание: * - статистически значимые различия при р<0,05 по сравнению с группой 2 кГц 120 с.
Фигура 3 - Пролиферативная активность клеток РС-3 на 1-е, 5-е и 7-е сутки после однократного воздействия плазменной струи атмосферного давления.
Примечание: * - статистически значимые различия при р<0,05 по сравнению с группой контроля.
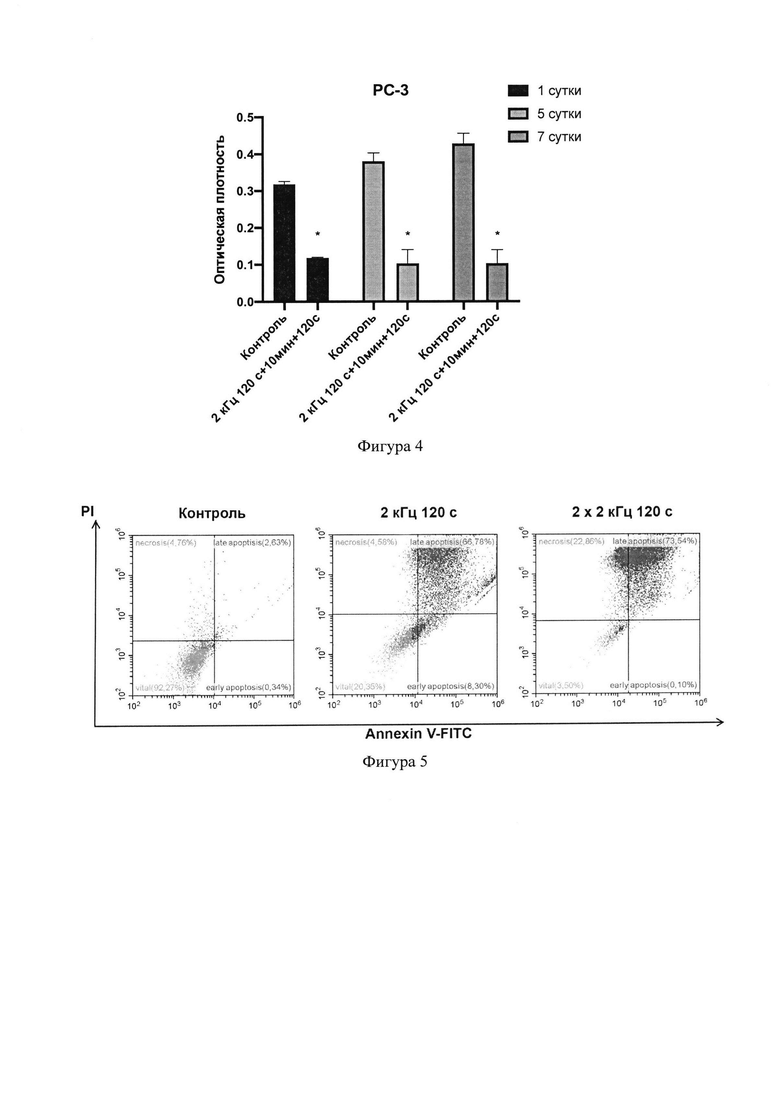
Фигура 4 - Пролиферативная активность клеток РС-3 на 1-е, 5-е и 7-е сутки после двукратного воздействия плазменной струи атмосферного давления.
Примечание: * - статистически значимые различия при р<0,05 по сравнению с группой контроля.
Фигура 5 - Процент апоптотических и некротических клеток РС-3 через 24 часа после обработки низкотемпературной плазмой, подсчитанный методом проточной цитометрии.
Пример 1
Клетки культивировали в чашках Петри площадью 9,2 см2 в полной питательной среде RPMI-1640, содержащей 10% инактивированной эмбриональной телячьей сыворотки и антибиотики (50 ед/мл пенициллина и 50 мкг/мл стрептомицина), при температуре 37°С с 5% содержанием СО2, во влажной среде с концентрацией клеток 150 тыс/мл. Опухолевые клетки рака простаты обрабатывали с использованием генератора плазменных струй с определенными режимами, имеющими частоту следования импульсов напряжения в диапазоне от 0,5 до 4,2 кГц и время экспозиции 120 с, осуществляемых при стандартной температуре и давлении
Через 24 часа после посева клеток производили плазменную обработку в стерильных условиях, определение жизнеспособности опухолевых клеток осуществляли по истечении 24 часов с помощью МТТ-теста. Данный колориметрический метод основан на определении оптической плотности растворов с помощью спектрофотометра при длине волны 620 нм. В качестве группы сравнения использовали опухолевые клетки, подвергавшиеся всем аналогичным манипуляциям, что и обработанные плазмой, за исключением самого фактора воздействия. Пролиферативная активность клеток представлена в виде оптической плотности и индекса ингибирования (в процентах), который рассчитывали по следующей формуле: X=(A+B)/A*100, где А - значение оптической плотности в группе контроля; В - значение оптической плотности в опытной группе. Статистическую обработку полученных данных проводили в программе Statistica 8.
Было установлено, что воздействие низкотемпературными плазменными струями ингибировало пролиферативную активность опухолевых клеток, наибольшее ингибирование клеточного роста наблюдалось в группах с частотой 2 кГц и временем экспозиции 120 с и составляло 50% (Фиг. 2).
Пример 2
Аналогично первому примеру, опухолевые клетки РС-3 обрабатывали с использованием вышеописанного генератора плазменных струй в следующих режимах - однократная и двукратная плазменная обработка с частотой следования импульсов напряжения 2 кГц и временем экспозиции 120 сек. Клетки культивировались в стандартных условиях в чашках Петри, обработка производилась через 24 часа после пассажа. Определение пролиферативной активности клеток проводилась на 1, 5 и 7 сутки методом МТТ-теста, полученные данные приведены в значениях оптической плотности, полученных на спектрофотометре.
Значение оптической плотности было отличным при разной кратности повторов обработки. При однократной обработке наблюдалось снижение клеточного роста, не превышающее 50% (Фиг. 3). Однако, ингибирование пролиферативной активности клеток РС-3 после двукратного воздействия плазменными струями было максимальным и наиболее выраженным на 5-е сутки после обработки (до 85%) (Фиг. 4).
Пример 3
Производили обработку опухолевых клеток рака простаты РС-3 в одном режиме - при двукратной обработке с частотой следования импульсов напряжения 2 кГц, времени экспозиции 120 с. Клетки росли в аналогичных предыдущим примерам условиях, плазменная обработка проводилась также через 24 часа культивирования в полной питательной среде RPMI-1640. Оценка типа клеточной гибели осуществлялась с помощью проточного цитофлюориметра через 24 часа после плазменной обработки клеток (Аннексии V+PI). Результаты наблюдения представлены на графике (Фиг. 5).
Полученные данные свидетельствуют о том, что однократное воздействие на клетки приводит к гибели 80% клеток в культуре, в то время как при повторной обработке количество мертвых клеток составляет 97%
Таким образом, предлагаемый способ позволяет эффективно воздействовать на клетки опухоли простаты и может быть перспективен для внедрения в клиническую практику.
Источники информации, принятые во внимание при составлении описания:
1. System and method for cold atmospheric plasma treatment on cancer stem cells // Патент USA №10329535. 2019 / Trink В., Keidar M., Canady J.
2. Method for treatment for combination cold atmospheric plasma therapy of solid tumors // Патент USA №20210196337. 2021 / Canady J., Cheng X., Murthy S., Zhuang T. Ly L., Jones O.
3. Method of selectively killing cancer cells using low-temperature plasma jet device and method of treating tumors using the same // Патент USA №20170319256. 2017 / Kang Т., Choi J.
4. Lu X., Laroussi M., Puech V. On atmospheric-pressure non-equilibrium plasma jets and plasma bullets // Plasma Sources Science and Technology. 2012. Vol.21, №3.
5. Laroussi M. Low-Temperature Plasma Jet for Biomedical Applications: A Review // IEEE Transactions on Plasma Science. Institute of Electrical and Electronics Engineers Inc., 2015. Vol.43, №3. P. 703-712.
6. Winter J., Brandenburg R., Weltmann K.D. Atmospheric pressure plasma jets: An overview of devices and new directions // Plasma Sources Science and Technology. Institute of Physics Publishing, 2015. Vol.24, №6.
7. Korolev Y.D. Low-current discharge plasma jets in a gas flow. Application of plasma jets // Russian Journal of General Chemistry. Maik Nauka Publishing / Springer SBM, 2015. Vol.85, №5. P. 1311-1325.
8. Laroussi M. Sterilization of contaminated matter with an atmospheric pressure plasma // IEEE Transactions on Plasma Science. 1996. Vol.24, №3. P. 1188-1191.
9. Schoenbach K.H. et al. Microhollow cathode discharges // Appl. Phys. Lett. 1996. Vol.68, №LP. 13-15.
10. Tornin J. et al. Evaluation of the effects of cold atmospheric plasma and plasma-treated liquids in cancer cell cultures // Nature Protocols 2021 16:6. Nature Publishing Group, 2021. Vol.16, №6. P. 2826-2850.
11. Yan X. et al. Plasma medicine for neuroscience - An introduction // Chinese Neurosurgical Journal. BioMed Central Ltd., 2019. Vol.5, №1. P. 1-8.
12. Keidar M. et al. Cold plasma selectivity and the possibility of a paradigm shift in cancer therapy // British Journal of Cancer 2011 105:9. Nature Publishing Group, 2011. Vol.105, №9. P. 1295-1301.
13. Schneidera C. et al. Cold atmospheric plasma treatment inhibits growth in colorectal cancer cells // Biol Chem. Biol Chem, 2018. Vol.400, №1. P. 111-127.
14. Utsumi F. et al. Effect of Indirect Nonequilibrium Atmospheric Pressure Plasma on Antiproliferative Activity against Chronic Chemo-Resistant Ovarian Cancer Cells In Vitro and In Vivo // PLoS ONE. Public Library of Science, 2013. Vol.8, №12. P. 81576.
15. Dobrynin D. et al. Physical and biological mechanisms of direct plasma interaction with living tissue // New Journal of Physics. 2009. Vol.11, №11. P. 115020.
16. Yan D. et al. The role of aquaporins in the anti-glioblastoma capacity of the cold plasma-stimulated medium // Journal of Physics D: Applied Physics. Institute of Physics Publishing, 2017. Vol.50, №5.
17. Arndt S. et al. Cold atmospheric plasma (CAP) activates angiogenesis-related molecules in skin keratinocytes, fibroblasts and endothelial cells and improves wound angiogenesis in an autocrine and paracrine mode // J Dermatol Sci. J Dermatol Sci, 2018. Vol.89, №2. P. 181-190.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения плазменной струи и устройство для его осуществления | 2016 |
|
RU2633705C1 |
| Источник плазменной струи | 2015 |
|
RU2616445C1 |
| УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ ПЛАЗМЕННОЙ СТРУИ | 2021 |
|
RU2764165C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2014 |
|
RU2552305C1 |
| СПОСОБ ЭКСПРЕСС-ДИАГНОСТИКИ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2016 |
|
RU2661098C1 |
| Способ прогнозирования риска опухолевой прогрессии у больных раком молочной железы | 2024 |
|
RU2838618C1 |
| СПОСОБ СТЕРИЛИЗАЦИИ ГАЗОРАЗРЯДНОЙ ПЛАЗМОЙ АТМОСФЕРНОГО ДАВЛЕНИЯ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2016 |
|
RU2638569C1 |
| Способ прогнозирования эволюции церебральных глиом | 2020 |
|
RU2740194C1 |
| Способ определения риска злокачественной трансформации эпителиальных клеток гортани у больных предопухолевыми заболеваниями гортани | 2022 |
|
RU2803858C1 |
| Газоразрядное устройство для обработки плазмой при атмосферном давлении поверхности биосовместимых полимеров | 2020 |
|
RU2751547C1 |
Изобретение относится к медицине, а именно к экспериментальной онкологии, конкретно к способам подавления роста опухолевых клеток рака аденокарциномы простаты in vitro. На опухолевые клетки воздействуют низкотемпературной неравновесной плазменной струей с использованием в качестве рабочего газа атмосферного воздуха с параметрами источника: импульсным напряжением 15 кВ, длительностью импульса 1 мкс, воздушным потоком 0,05 г/с со скоростью 3 мл/мин, частотой следования импульсов в диапазоне от 0,5 до 4,2 кГц, временем экспозиции 120 с и кратностью повторов обработки от 1 до 2. Изобретение позволяет эффективно воздействовать на клетки опухоли простаты. 5 ил., 3 пр.
Способ подавления роста опухолевых клеток рака аденокарциномы простаты in vitro, характеризующийся тем, что на опухолевые клетки воздействуют низкотемпературной неравновесной плазменной струей с использованием в качестве рабочего газа атмосферного воздуха с параметрами источника: импульсным напряжением 15 кВ, длительностью импульса 1 мкс, воздушным потоком 0,05 г/с со скоростью 3 мл/мин, частотой следования импульсов в диапазоне от 0,5 до 4,2 кГц, временем экспозиции 120 с и кратностью повторов обработки от 1 до 2.
| Способ воздействия холодной плазменной струей на биологический объект и установка для его реализации | 2020 |
|
RU2764619C1 |
| ФРОЛОВА А.А | |||
| и др | |||
| ИЗБИРАТЕЛЬНОЕ ДЕЙСТВИЕ НИЗКОТЕМПЕРАТУРНЫХ ПЛАЗМЕННЫХ СТРУЙ НА ОПУХОЛЕВЫЕ И НОРМАЛЬНЫЕ КЛЕТКИ / АКТУАЛЬНЫЕ ВОПРОСЫ ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ МЕДИЦИНЫ, 2022, Томск, стр | |||
| Льночесальная машина | 1923 |
|
SU245A1 |
| АШУРБЕКОВ Н.А | |||
| и др | |||
| Взаимодействие низкотемпературной плазменной струи атмосферного давления в смеси воздуха и аргона с | |||
Авторы
Даты
2024-07-24—Публикация
2023-02-28—Подача