Изобретение относится к химии комплексонов, а именно - к новым соединениям на основе амидов аминокислот и нитрилотриуксусной кислоты общей формулы I, обладающим способностью промотировать образование газовых гидратов. Соединения могут найти применение в нефтегазовой отрасли в процессах добычи, транспортировки и хранения природного газа.


Природный газ, являясь самым экологически чистым ископаемым топливом, играет огромную роль в удовлетворении глобального спроса на энергию, обеспечивая 24% ее мирового потребления [H.P. Veluswamy, A. Kumar, Y. Seo, J.D. Lee, P. Linga, A review of solidified natural gas (SNG) technology for gas storage via clathrate hydrates, Applied Energy, 216, 262-285, 2018.]. Использование природного газа для выработки электроэнергии приводит к снижению выбросов CO2 примерно на 50% и 33% по сравнению с использованием угля и нефти, соответственно [Leveraging natural gas to reduce greenhouse gas emissions, Center for climate and energy solutions, June, 2013.]. Учитывая тот факт, что по прогнозам потребность в природном газе до 2040 года будет расти со скоростью 2% в год, встает актуальный вопрос эффективного способа его хранения и транспортировки. На дату представления заявочных материалов известны несколько подходов в решении данной задачи.
Наиболее распространенным подходом является транспорт через газопровод, который не всегда практичен, учитывая расстояние до места назначения и его доступность.
В качестве другого известного подхода к транспортировке и хранению газа можно обозначить технологию сжатого природного газа. Недостатками этого подхода являются проблемы безопасности и низкая емкость хранилищ. Адсорбированный природный газ - это еще один возможный подход к транспортировке и хранению газа путем адсорбции на сорбентах, таких как углеродные нанотрубки, графен, металлоорганические каркасы и т.д.
Однако такие факторы, как механическая стабильность, теплопроводность, наличие примесей и, самое главное, высокая стоимость материала сорбента будут препятствовать развертыванию данной технологии в промышленном масштабе.
Транспортировка природного газа в сжиженном виде (СПГ) считается приемлемым подходом для крупномасштабных и дальних перевозок, однако данная технология требует очень низких температур (минус 162°C) и сталкивается с проблемой постоянного выкипания газа, что накладывает ограничения на время хранения.
Газовые гидраты представляют собой класс соединений включения, в которых пористый кристаллический каркас образован молекулами воды, а молекулы газов заполняют поры этого каркаса. Хранение и транспортировка природного газа в форме его клатратных гидратов (далее - гидратов) на сегодняшний день является многообещающей альтернативой рассмотренных выше технологий [H.P. Veluswamy, A. Kumar, Y. Seo, J.D. Lee, P. Linga, A review of solidified natural gas (SNG) technology for gas storage via clathrate hydrates, Applied Energy, 216, 262-285, 2018.] из-за некоторых характерных преимуществ, рассмотренных ниже:
1) Процесс образования гидрата газа является экологически приемлемым, поскольку в нем участвуют только вода, газ и очень малая доля промотора (в случае использования промотора);
2) Газ легко извлекается из гидрата путем снижения давления или минимального нагрева;
3) Умеренные значения температуры и давления, необходимые для формирования и хранения гидрата (при наличии промотора в низкой концентрации);
4) Относительно высокое содержание энергии на единицу объема;
5) Данный способ хранения газа является безопасным, поскольку газогидраты не относятся к взрывоопасным веществам [H.P. Veluswamy, A. Kumar, Y. Seo, J.D. Lee, P. Linga, A review of solidified natural gas (SNG) technology for gas storage via clathrate hydrates, Applied Energy, 216, 262-285, 2018.].
Возможность хранения и транспортировки газа в виде гидратов требует решения таких вопросов, как эффективное снижение адгезии гидратов к внутренним поверхностям технологических аппаратов, управление кинетикой образования и разложения гидратов и пр. [Ф. А. Кузнецов, В. А. Истомин, Т. В. Родионова, Газовые гидраты: исторический экскурс, современное состояние, перспективы исследований, Российский химический журнал (Журнал Росийского химического общества им. Д.И. Менделеева) XLVII, № 3, 5-18, 2003.].
Одним из подходов к решению данных вопросов может быть использование веществ, целенаправленно влияющих на физико-химические свойства гидратов.
Например, для развития гидратных технологий транспортировки и хранения газа необходимо создание эффективных способов промотирования гидратообразования.
Промоторы бывают двух типов - термодинамические и кинетические.
Термодинамические промоторы представляют собой соединения, которые изменяют/сдвигают условия равновесия образования гидрата газа. К известным промоторам этого типа относятся тетрагидрофуран, циклопентан, йодистый метил, метилтретбутиловый эфир, 1,4-диоксан, 1,3-диоксолан и др. [Y. Sowjanya, P.S.R. Prasad, Formation kinetics & phase stability of double hydrates of C4H8O and CO2/CH4: A comparison with pure systems, Journal of Natural Gas Science and Engineering, 18, 58-63, 2014. B. Tohidi, A. Danesh, A.C. Todd, R.W. Burgass, K.K. Østergaard, Equilibrium data and thermodynamic modelling of cyclopentane and neopentane hydrates, Fluid Phase Equilibria, 138, 241-50, 1997.]. Использование термодинамических промоторов позволяет получать газогидраты при более низком давлении и высокой температуре. Однако конверсия газа при их использовании снижается.
Кинетические промоторы представляют собой добавки, которые помогают повысить скорость образование гидратов без влияния на температуру и давление. Таким образом, условия образования гидратов (температура и давление) и структура гидратов не будут затронуты включением кинетических промоторов. К известным промоторам этого типа относятся некоторые ПАВ (анионные, катионные и неионогенные, например, додецилсульфат натрия [US-6389820-B1; RU2293907C2; Y. Zhong, R.E. Rogers, Surfactant effects on gas hydrate formation, Chemical Engineering Science, 55, 4175-87, 2000.], цетилтриметиламмонийбромид [J. Du, H. Li, L. Wang, Effects of ionic surfactants on methane hydrate formation kinetics in a static system, Advanced Powder Technology, 25(4), 1227-1233, 2014.] и др.), аминокислоты (лейцин [H.P. Veluswamy, Q.W. Hong, P. Linga, Morphology study of methane hydrate formation and dissociation in the presence of amino acid, Crystal Growth and Design, 16(10), 5932-5945, 2016.] и гистидин [G. Bhattacharjee, N. Choudhary, A. Kumar, S. Chakrabarty, R. Kumar, Effect of the amino acid l-histidine on methane hydrate growth kinetics, Journal of Natural Gas Science and Engineering, 35, 1453-1462, 2016.]), некоторые полимеры (различные целлюлозы [M. Mohammad-Taheri, A.Z. Moghaddam, K. Nazari, N.G. Zanjani, Methane hydrate stability in the presence of water-soluble hydroxyalkyl cellulose, Journal of Natural Gas Chemistry, 21(2), 119-125, 2012.], крахмалы [H. Fakharian, H. Ganji, A. Naderi Far, M. Kameli, Potato starch as methane hydrate promoter, Fuel, Volume 94, 2012, Pages 356-360.], поливиниловый спирт [U. Karaaslan, M. Parlaktuna, Promotion effect of polymers and surfactants on hydrate formation rate, Energy Fuels, 16, 1413-6, 2002.].
Использование кинетических промоторов как в индивидуальном виде, так и в виде композиций приводит в большей или меньшей степени к ускорению образования газогидратов. Однако следует отметить, что кинетические промоторы обладают рядом отрицательных свойств. Так, для ПАВ характерно сильное вспенивание при извлечении газа из гидрата, что сильно усложняет данный процесс. Нативные природные аминокислоты и полимеры обладают низкой стабильностью за счет того, что являются питательным субстратом для микроорганизмов - бактерий и грибов. Помимо этого, многие из них дороги в производстве и не всегда обладают достаточной эффективностью.
Также известны гетерогенные промоторы гидратообразования, такие как нано-частицы серебра [Samad Arjang, Mehrdad Manteghian, Abolfazl Mohammadi, Effect of synthesized silver nanoparticles in promoting methane hydrate formation at 4.7MPa and 5.7MPa, Chemical Engineering Research and Design, Volume 91, Issue 6, 2013, Pages 1050-1054], оксиды различных металлов [Himangshu Kakati, Ajay Mandal, Sukumar Laik, Promoting effect of Al2O3/ZnO-based nanofluids stabilized by SDS surfactant on CH4+C2H6+C3H8 hydrate formation, Journal of Industrial and Engineering Chemistry, Volume 35, 2016, Pages 357-368], а также различные комбинированные промоторы, например, нано-оксид железа покрытый ПАВ (додецилсульфат натрия) [Guo-Qiang Liu, Fei Wang, Sheng-Jun Luo, Dong-Yan Xu, Rong-Bo Guo, Enhanced methane hydrate formation with SDS-coated Fe3O4 nanoparticles as promoters, Journal of Molecular Liquids, Volume 230, 2017, Pages 315-321], графен [Yan, S.; Dai, W.; Wang, S.; Rao, Y.; Zhou, S. Graphene Oxide: An Effective Promoter for CO2 Hydrate Formation, Energies, 2018, 11, 1756.], однако их использование требует предварительной специальной обработки и стабилизации дисперсности (очень высокие скорости перемешивания). Также стоит отметить абразивные свойства гетерогенных промоторов, которые снижают эксплуатационные характеристики оборудования.
Так же близким по назначению является промотор гидратообразования на основе сульфированного касторового масла (далее - COS) по патенту на изобретение RU 2755790 «Промотор гидратообразования на основе касторового масла». Сущностью известного изобретения является «Промотор гидратообразования на основе касторового масла формулы (I):
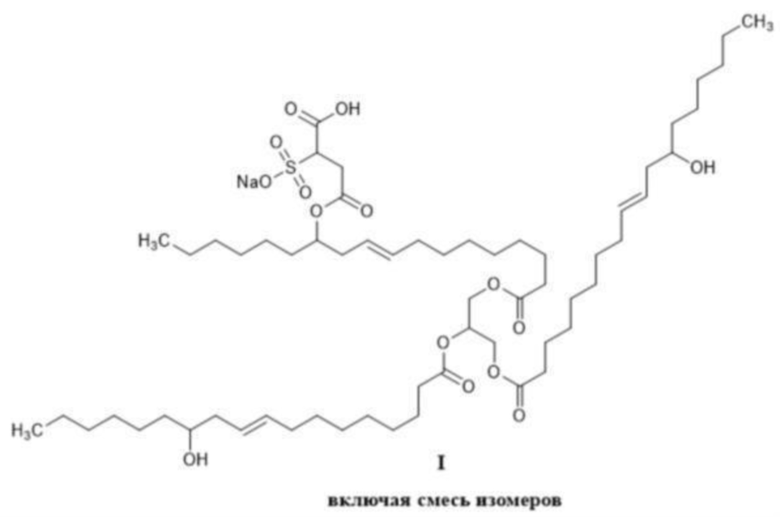
»
Недостатком известного технического решения по сравнению с заявленным является более низкая промотирующая гидратообразующая способность.
Так же близким по назначению и строению являются промоторы на основе бисамидов ЭДТА и алифатических аминов [Pavelyev, Roman S., et al. "Dual Promotion-Inhibition Effects of Novel Ethylenediaminetetraacetic Acid Bisamides on Methane Hydrate Formation for Gas Storage and Flow Assurance Applications." Energy & Fuels 36.1, 2021, Pages 290-297. / https://doi.org/10.1021/acs.energyfuels.1c03381], которые увеличивали конверсию газа в гидрат, однако при этом значительно увеличивали время индукции. Так же известен этилендиаминтетрацетамид [Farhadian, A., Varfolomeev, M. A., Abdelhay, Z., Emelianov, D., Delaunay, A., & Dalmazzone, D. Accelerated methane hydrate formation by ethylene diamine tetraacetamide as an efficient promoter for methane storage without foam formation. Industrial & Engineering Chemistry Research, 58(19), 2019, 7752-7760. https://pubs.acs.org/doi/10.1021/acs.iecr.9b00803], уменьшающий время индукции и увеличивающий конверсию газа в гидрат, однако его необходимо использовать в большой (0,5 мас.% и более) концентрации.
В качестве прототипа заявленных соединений можно рассматривать промоторы гидратообразования на основе амидов аминокислот и этилендиаминтетрауксусной кислоты по патенту на изобретение RU 2798318 «Промоторы гидратообразования на основе амидов аминокислот и этилендиаминтетрауксусной кислоты», сущностью является промоторы гидратообразования на основе амидов аминокислот и этилендиаминтетрауксусной кислоты формулы (I):
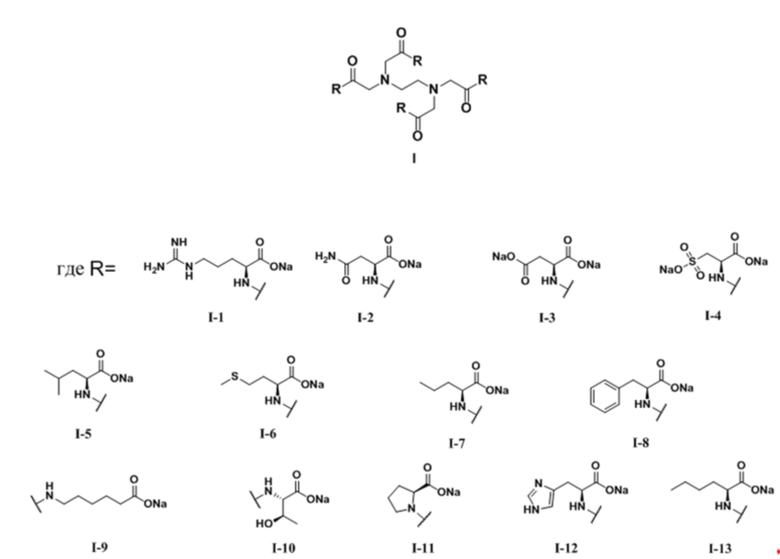
Основой известного изобретения являются амиды аминокислот и полиаминокарбоновой кислоты, которыми являются нитрилотриуксусная кислота (НТК), этилендиаминтетрауксусная кислота (ЭДТА).
В отличие от ЭДТА, молекула НТК имеет меньшую молекулярную массу и иную симметрию. Меньшее расстояние между карбоксильными группами и присутствие только одного атома азота изменяет свойства амидов аминокислот и полиаминокарбоновой кислоты, что влияет на способность промотировать образование гидратов. В качестве соединения сравнения использовался амид лейцина и этилендиаминтетрауксусной кислоты (далее - ЭДТА+Лей), который обладает лучшими промотирующими способностями среди соединений, которые представлены в патенте на изобретение RU 2798318 C1. Стоит отметить, что недостатком патента на изобретение RU 2798318 C1 является отсутствие данных о времени индукции представленных в нем промоторов, которое является ключевой характеристикой при изучении промотирующей активности образования газовых гидратов. Поэтому сравнение проводится только по конверсии воды в гидрат. Далее показано, что ЭДТА+Лей менее эффективен некоторых представленных амидов аминокислот и нитрилотриуксусной кислоты формулы I.
Таким образом, по итогам анализа российских и зарубежных патентных баз данных, научной литературы, Интернет-ресурсов заявителем не выявлены аналоги к заявленному техническому решению как по химической структуре, так и по составу.
Вместе с тем, заявителем выявлены соединения, которые являются аналогами заявленного технического решения по назначению, но которые, однако, обладают указанными выше недостатками, а именно - недостаточно высокой эффективностью или же высокой стоимостью производства при использовании по назначению на фоне слишком низкой стабильности и высокому пенообразованию, что и является технической проблемой, решаемой заявленным техническим решением.
Техническим результатом заявленного технического решения является применение соединений на основе амидов аминокислот и нитрилотриуксусной кислоты формулы (I) в качестве промоторов гидратообразования, что, в конечном счете, обеспечивает расширение линейки реагентов указанного назначения.
Сущностью заявленного технического решения является применение соединений на основе амидов аминокислот и нитрилотриуксусной кислоты формулы (I) в качестве промоторов гидратообразования:

Заявленное техническое решение иллюстрируется Фиг. 1 - Фиг. 3:
На Фиг. 1 представлена блок-схема установки для тестирования гидратообразования, где:
1 - баллон с модельным газом;
2 - газовый бустер;
3 - датчик давления;
4 - источник постоянного тока;
5 - верхнеприводная мешалка;
6 - магнитная муфта;
7 - термопара;
8 - автоклав;
9 - термостат;
10 - коммутатор;
11 - система сбора данных (Теркон);
12 - компьютер.
На Фиг. 2 представлена Таблица, где приведены конверсия воды в гидрат и время достижения максимальной конверсии гидрата метана для чистой воды, раствора SDS, ЭДТА+Лей и амидов аминокислот и нитрилотриуксусной кислоты формулы I при концентрации 0,05 мас.%.
На Фиг. 3 представлены фотографии пены для SDS и соединения I-3 в концентрации 0,05 мас.%.
Далее заявителем приведено описание заявленного технического решения.
Заявленный технический результат достигается синтезом соединений формулы I, обладающих способностью промотировать образование газовых гидратов.
Заявленные соединения получены согласно нижеприведенной Схеме 1, где заявленные соединения обозначены номерами от I-1 до I-13.
Характеристики соединений представлены в примерах конкретного выполнения заявленного технического решения.
В работе использовались следующие реактивы: аспарагиновая кислота, аланин, цистеиновая кислота, глутаминовая кислота, лейцин, метионин, норвалин, норлейцин, фенилаланин, пролин, треонин, валин, 6-аминогексановая кислота, нитрилотриуксусная кислота (НТК) и додецилсульфат натрия (SDS) с массовой долей более 98 мас.% были получены из коммерческих источников и использовались без дополнительной очистки. Все газогидратные эксперименты проводились с использованием газа метана (чистота 99,9 % от ООО «НИИ КМ», Россия).
Спектры ЯМР 1H, 13C регистрировали с помощью ЯМР спектрометра Bruker AVANCE 400 (Bruker, Германия) при рабочей частоте 400 и 101 МГц, соответственно. Химические сдвиги определяли относительно остаточных протонов дейтерированного растворителя (D2O).
Далее заявителем приведена общая методика получения амидов аминокислот и нитрилотриуксусной кислоты формулы I (Схема 1).
На 1 стадии получают триметил-2,2',2"-нитрилотриацетат (ТМНТК) путем взаимодействия НТК с избытком метанола при барботировании газообразной соляной кислоты при 60°С. Через 4 часа оставшуюся соляную кислоту нейтрализуют, например, бикарбонатом натрия и раствор концентрируют, например, с использованием ротационного испарителя. Образовавшийся продукт ТМНТК экстрагируют из образовавшейся массы этилацетатом, затем органическую часть концентрируют, например, с использованием ротационного испарителя.
Затем каждую аминокислоту превращают в натриевую соль с использованием эквимольного количества гидроксида натрия на каждую карбоксильную группу аминокислоты путем растворения исходной аминокислоты и гидроксида натрия в воде с последующей отгонкой растворителя, например, с использованием ротационного испарителя.
На 2 стадии проводят процесс амидирования, для чего берут смесь 1 эквивалент соединения ТМНТК и 3 эквивалента соли соответствующей аминокислоты в водном метаноле (в объемном соотношении V метанола : V воды = 1:1), и перемешивают при 50°C в течение 7 дней. По завершении реакции растворитель выпаривают при пониженном давлении, например, в ротационном испарителе. Остаточную массу высушивают в вакууме.
Получают целевые продукты I-1 - I-13.

Далее заявителем приведены примеры осуществления заявленного технического решения.
Пример 1. Получение соединения 2,2',2"-((2,2',2"- нитрилотрис(ацетил))трис(азандиил))трис(4-метилпентаноат) натрия (I-1).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-1.
Получили массу вещества 12,21 гр. Выход: 95%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.56 (м, 3H), 3.44 (с, 6H), 1.62 (м, 9H), 0.93 (м, 18H).
Спектр ЯМР 13C (101 МГц, D2O) δ 178.97, 176.17, 58.37, 54.07, 41.60, 24.49, 22.43, 21.32.
Пример 2. Получение соединения 5-карбоксилато-9-(2-((1-карбоксилато-3-(метилтио)пропил)амино)-2-оксоэтил)-13-(2-(метилтио)этил)-7,11-диоксо-2-тиа-6,9,12-триазатетрадекан-14-оат натрия (I-2).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-2.
Масса вещества 16,82 гр. Выход: 99%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.32 (м, 3H), 3.14 (с, 6H), 2.54 (т, 6H), 2.10 (с, 9H), 1.80 (м, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 183.14, 179.80, 58.91, 55.51, 34.37, 29.95, 14.33.
Пример 3. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трис(3-фенилпропаноат) натрия (I-3).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-3.
Масса вещества 14,6 гр. Выход: 97%.
Спектр ЯМР 1H (400 МГц, D2O) δ 7.44 (м, 15H), 4.50 (т, 3H), 3.66 (с, 6H), 2.75 (м, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 178.39, 172.84, 138.83, 129.35, 128.94, 127.02, 57.80, 53.03, 42.69.
Пример 4. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))тригексаноат натрия (I-4).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-4.
Масса вещества 11,86 гр. Выход: 93%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.47 (т, 3H), 3.31 (с, 6H), 1.71 (м, 6H), 1.32 (м, 12H), 0.89 (т, 9H).
Спектр ЯМР 13C (101 МГц, D2O) δ 180.74, 177.07, 58.51, 55.46, 31.80, 26.93, 22.04, 13.35.
Пример 5. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трисукцинат натрия (I-5).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-5.
Масса вещества 13,45 гр. Выход: 94%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.72 (с, 3H), 3.37 (с, 6H), 2.60 (д, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 178.84, 177.63, 58.25, 53.13, 39.40.
Пример 6. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трис(3-метилбутаноат) натрия (I-6).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-6.
Масса вещества 11,54 гр. Выход: 97%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.69 (с, 3H), 3.52 (с, 6H), 2.22 (м, 3H), 1.00 (д, 18H).
Спектр ЯМР 13C (101 МГц, D2O) δ 175.76, 172.12, 60.79, 57.65, 29.67, 18.32.
Пример 7. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))триглутарат натрия (I-7).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-7.
Масса вещества 14,76 гр. Выход: 97%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.59 (м, 3H), 3.47 (с, 6H), 2.30 (м, 6H), 2.02 (м, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 182.03, 177.28, 58.32, 55.24, 33.90, 28.62.
Пример 8. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трипентаноат натрия (I-8).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-8.
Масса вещества 11,29 гр. Выход: 95%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.53 (м, 9H), 1.73 (м, 6H), 1.35 (м, 6H), 0.93 (м, 9H).
Спектр ЯМР 13C (101 МГц, D2O) δ 178.27, 175.41, 57.91, 55.25, 34.17, 18.23, 13.27.
Пример 9. Получение соединения (2,2',2''-нитрилотрис(ацетил))трипролинат натрия (I-9).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-9
Масса вещества 11,25 гр. Выход: 96%.
Спектр ЯМР 1H (400 МГц, D2O) δ 4.01 (м, 3H), 3.29 (м, 12H), 2.29 (м, 3H), 1.94 (м, 9H).
Спектр ЯМР 13C (101 МГц, D2O) δ 177.85, 175.87, 61.48, 58.57, 46.29, 29.44, 24.16.
Пример 10. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трис(3-гидроксибутаноат) натрия (I-10).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-10.
Масса вещества 10,96 гр. Выход: 91%.
Спектр ЯМР 1H (400 МГц, D2O) δ 4.16 (м, 3H), 3.71 (м, 3H), 3.45 (м, 6H), 1.28 (м, 9H).
Спектр ЯМР 13C (101 МГц, D2O) δ 177.61, 175.19, 68.24, 61.53, 58.34, 19.55.
Пример 11. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трипропионат натрия (I-11).
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-11.
Масса вещества 9,77 гр. Выход: 97%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.64 (q, 3H), 3.51 (с, 6H), 1.40 (д, 9H).
Спектр ЯМР 13C (101 МГц, D2O) δ 178.16, 174.67, 58.00, 50.94, 17.36.
Пример 12. Получение соединения 6,6',6''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))тригексаноат натрия (I-12)
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-12.
Масса вещества 12,48 гр. Выход: 98%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.38 (с, 6H), 2.94 (т, 6H), 2.18 (т, 6H), 1.59 (м, 12H), 1.35 (м, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 183.92, 178.05, 58.49, 39.65, 37.46, 27.18, 25.68, 25.45.
Пример 13. Получение соединения 2,2',2''-((2,2',2''-нитрилотрис(ацетил))трис(азандиил))трис(3-сульфонатопропаноат) натрия (I-13)
Получали в соответствии с общей методикой получения амидов аминокислот и нитрилотриуксусной кислоты по Схеме 1, где R - I-13.
Масса вещества 15,94 гр. Выход: 96%.
Спектр ЯМР 1H (400 МГц, D2O) δ 3.95 (с, 3H), 3.72 (с, 6H), 3.31 (м, 6H).
Спектр ЯМР 13C (101 МГц, D2O) δ 174.52, 171.70, 57.64, 52.42, 52.12.
Пример 14 . Исследование способности амидов аминокислот и нитрилотриуксусной кислоты (I) промотировать образование газовых гидратов.
Исследование образования гидратов метана в присутствии промоторов проводили с использованием автоклава высокого давления. Схема установки для проведения экспериментов по оценке промотирования гидратообразования представлена на Фиг. 1. Основным элементом установки является автоклавная ячейка высокого давления (8) (например, TOP INDUSTRIE, Франция), оборудованная верхнеприводной мешалкой (5) с магнитной муфтой (6). Измерение процесса гидратообразования проводится с помощью калиброванных датчиков давления (3) и термопары (7). Погрешности измерения температуры и давления составляют 0,1°С и 0,005 МПа соответственно. Для преобразования сети переменного тока в постоянный использовался источник постоянного тока (4)
Растворы промоторов концентрации 0,05 мас.% готовили с использованием деионизированной воды. В автоклавную ячейку высокого давления (8) общим объемом 284 мл добавляли 50 мл раствора промотора, и остаточный воздух из ячейки трижды продували метаном 0,5 МПа из баллона (1). После этого в автоклавной ячейке высокого давления (8) с помощью газового бустера (2) создавали давление до 9 МПа при 20°С, начинали перемешивание со скоростью 400 об/мин с помощью верхнеприводной мешалкой (5). Затем запускали запись данных с помощью системы сбора данных (11) и коммутатора (10), которые регистрировали на локальном компьютере (12), а затем с помощью термостата (9) осуществляли цикл охлаждения от +20°С до +1°С за 1 ч с последующим изотермическим режимом при +1°С в течение 8 часов.
Для исследования образования гидратов метана в присутствии промоторов взяли:
- заявленные соединения I-1 - I-13 концентрацией 0,05 мас.%,
- чистую воду (контроль),
- раствор додецилсульфата натрия (SDS) концентрацией 0,05 мас.% - самый известный и широко применяемый промотор гидратообразования (опыт сравнения),
- в качестве соединения сравнения использовали амид лейцина и этилендиаминтетрауксусной кислоты (далее - ЭДТА+Лей), который обладает лучшими промотирующими способностями среди соединений, которые представлены в патенте на изобретение RU 2798318 C1.
Результаты представлены в Таблице на Фиг.2.
При этом заявитель поясняет, что чем больше конверсия воды в гидрат и чем меньше время индукции по отношению к чистой воде, тем более эффективным считается промотор.
Как видно из Таблицы, для чистой воды конверсия воды в гидрат составляет 40 ± 2%, а время индукции 75 ± 26 мин. При этом конверсия воды в гидрат и время индукции 0,05 масс.% раствора SDS, как хорошо известного кинетического промотора, составляют 88 ± 2% и 54 ± 14 мин, соответственно.
В присутствии соединений общей формулы I (концентрация 0,05 масс.%) образование гидрата метана проходит с конверсией воды в гидрат от (83 ± 5)% до (98 ± 1)%, что более чем в 2 раза превышает таковой показатель для чистой воды. При этом 7 соединений формулы I из 13 увеличивают конверсию воды в гидрат лучше, чем SDS. Это соединения I-1, I-3 - I-7, I-11.
Все соединения формулы I, за исключением соединения I-1, значительно уменьшают время индукции в сравнении с чистой водой и раствором SDS. Соединения I-2 - I-6, I-8, I-9, I-11 - I-13 способствуют уменьшению времени индукции более чем в два раза по сравнению с чистой водой. А соединения I-6, I-8, I-11 и I-13 обладают вдвое меньшим временем индукции по сравнению с хорошо известным кинетическим промотором SDS.
Соединение ЭДТА+Лей в концентрации 0,05 масс.% способствует достижению конверсии воды в гидрат равной 94 ± 2%, что превосходит показатель для раствора SDS, и является показателем отличной промотирующей активности, однако еще большую промотирующую активность проявляет соединение I-3. Соединение I-3, которое является амидом фенилаланина и нитрилотриуксусной кислоты, способствует достижению 98 ± 1% конверсии воды в гидрат и уменьшает время индукции до 31 ± 3 минут.
Пример 15 . Исследование пенообразования амидов аминокислот и нитрилотриуксусной кислоты I.
Пенообразование амидов аминокислот и нитрилотриуксусной кислоты формулы I и SDS изучали с помощью лабораторной мешалки Heidolph Hei-Torque Value 100 (6000 об/мин, 1 мин). Концентрация исследуемых образцов - 0,05 мас.%. По результатам экспериментов показано, что для всех соединений I-1 - I-13, в отличие от SDS, пена не образуется. Для примера на Фиг.3 приведены фотографии пены для SDS и соединения I-3.
Таким образом, можно сделать вывод, что соединения формулы I не образуют пены по сравнению с известным коммерческим реагентом SDS, а значит обладают более лучшими эксплуатационными характеристиками в качестве промоторов гидратообразования.
Таким образом, можно сделать вывод, что по всем рассмотренным показателям соединения формулы I являются промоторами гидратообразования, при этом большинтство из которых превосходят один из самых известных промоторов - додецилсульфат натрия.
Таким образом, из описанного выше можно сделать вывод, что заявителем решена техническая проблема и достигнут заявленный технический результат, а именно - создана новая линейка нефтепромысловых реагентов - амидов аминокислот и нитрилотриуксусной кислоты формулы I, обладающих способностью промотировать образование газовых гидратов без образования пены при разгазировании, с целью расширения линейки нефтепромысловых реагентов указанного назначения.
Заявленное техническое решение соответствует условию патентоспособности «новизна», предъявляемому к изобретениям, так как из исследованного уровня техники не выявлены технические решения, обладающие заявленной совокупностью признаков, обеспечивающих достижение заявленных результатов.
Заявленное техническое решение соответствует условию патентоспособности «изобретательский уровень», предъявляемому к изобретениям, так как не является очевидным для специалиста в данной области науки и техники, так как заявленное техническое решение обеспечивает возможность реализации задачи промотирования гидратообразования с более высокими потребительскими свойствами - без образования пены при разгазировании.
Заявленное техническое решение соответствует условию патентоспособности «промышленная применимость», так как может быть реализовано на любом специализированном предприятии с использованием стандартного оборудования, известных отечественных материалов и технологий.
| название | год | авторы | номер документа |
|---|---|---|---|
| Промоторы гидратообразования на основе амидов аминокислот и этилендиаминтетрауксусной кислоты | 2022 |
|
RU2798318C1 |
| Промотор гидратообразования на основе сульфосукцинатов спиртов | 2022 |
|
RU2797598C1 |
| Промотор гидратообразования на основе трис-сульфосукцината касторового масла | 2023 |
|
RU2820709C1 |
| Промоторы гидратообразования углекислого газа на основе амидов аминокислот и лимонной кислоты | 2024 |
|
RU2836617C1 |
| Промоторы гидратообразования на основе производных касторового масла | 2023 |
|
RU2813108C1 |
| Промотор гидратообразования на основе касторового масла | 2020 |
|
RU2755790C1 |
| Промоторы гидратообразования углекислого газа на основе амидов аминокислот и этилендиаминтетрауксусной кислоты | 2024 |
|
RU2830051C1 |
| Ингибитор роста гидратов метана на основе сульфированного хитозана | 2020 |
|
RU2751893C1 |
| Ингибитор гидратообразования и коррозии на основе полиуретана, содержащего фрагменты триглицеридов подсолнечного масла | 2021 |
|
RU2770995C1 |
| Ингибитор гидратообразования и коррозии на основе сульфированного хитозана | 2020 |
|
RU2736036C1 |



Изобретение относится к применению соединений на основе амидов аминокислот и нитрилотриуксусной кислоты формулы (I)





в качестве промоторов гидратообразования. Соединения формулы (I) обладают способностью промотировать образование газовых гидратов без образования пены при разгазировании и могут найти применение в нефтегазовой отрасли в процессах добычи, транспортировки и хранения природного газа. 3 ил., 15 пр.
Применение соединений на основе амидов аминокислот и нитрилотриуксусной кислоты формулы (I)





в качестве промоторов гидратообразования.
| M | |||
| SCHULTZ et al., Synthesis of Dianionic and Trianionic Chiral, Chelating Ligands Based on Amino Acids, AUST | |||
| J | |||
| CHEM., 2008, Vol | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| АВТОМАТИЧЕСКОЕ УСТРОЙСТВО ДЛЯ ПОДАЧИ УГЛЯ К ТОПКАМ | 1920 |
|
SU297A1 |
| Промоторы гидратообразования на основе амидов аминокислот и этилендиаминтетрауксусной кислоты | 2022 |
|
RU2798318C1 |
| Промотор гидратообразования на основе касторового масла | 2020 |
|
RU2755790C1 |
| G | |||
| BHATTACHARJEE et al., Amino Acids as Kinetic Promoters for Gas Hydrate Applications: A Mini Review, ENERGY & FUELS, | |||
Авторы
Даты
2024-08-26—Публикация
2023-12-28—Подача