Изобретение относится к медицине, а именно к онкологии, и может быть использовано при лечении злокачественных новообразований.
Известно, что одним из факторов канцерогенеза является отсутствие или очень низкая концентрация внутриклеточного кислорода (Ed McCabe «O2xygen Therapies: A New Way of Approaching Disease», Morrisville, N.Y.: Energy Pubns, 1988, c. 81).
Гипоксия как общая особенность микроокружения солидных опухолей (МОО) в основном объясняется быстрой пролиферацией и чрезмерным гликолизом опухолевых клеток. Гипоксическое МОО может вызывать снижение терапевтического эффекта противоопухолевых стратегий, включая химиотерапию (XT), лучевую терапию (ЛТ), фотодинамическую терапию (ФДТ) и сонодинамическую терапию (СДТ). Например, индуцируемый гипоксией фактор-1α (HIF-1α), активируемый гипоксией в опухолях, может активировать регуляцию белка 1 (MDR1) с множественной лекарственной устойчивостью, приводящей к лекарственной устойчивости XT. ЛТ разрушает раковые клетки, ионизируя интерстициальную жидкость человеческого организма и образуя свободные радикалы, вызывающие разрушение молекул ДНК и перекрестное сшивание, что наиболее эффективно происходит в присутствии кислорода. При ФДТ и СДТ только в присутствии O2 фотосенсибилизаторы или соносенсибилизаторы могут генерировать синглетный кислород (1О2) посредством передачи энергии при возбуждении светом или ультразвуком для окислительного уничтожения опухолевых клеток. Аналогичным образом индуцированное с помощью гидропероксидных радикалов (*ООН) истощение глюкозы приводит к нарушению метаболизма глюкозы опухолевых клеток, запуская терапию голоданием, которая происходит только в аэробных условиях. Кроме того, H2O2 может действовать как сигнальная молекула как внутри, так и между клетками благодаря своему свойству свободной диффузии. Следовательно, высокие уровни экспрессии H2O2 связаны с различными клеточными сигнальными путями дифференцировки, роста и апоптоза опухолевых клеток, например, опухолевые клетки могут влиять на иммунный ответ МОО, запуская окислительно-восстановительные сигнальные каскады. Также в условиях кислого МОО и достаточного количества пероксида водорода возможно проведение химиодинамической терапии (ХДТ). ХДТ основана на фентон-опосредованных ионами железа или ионами других металлов (например, Cu+) фентоноподобных реакциях, катализирующих Н2О2, в результате чего образуется высокоцитотоксичный радикал •ОН, который приводит к более сильному окислительному повреждению онкологических клеток, чем непосредственно сам пероксид водорода. Однако количества эндогенного Н2О2 в опухолях (50-100 мкМ) недостаточно для поддержания выработки •ОН. В дополнение к этому МОО содержит большое количество глутатиона (GSH, 2-10 мМ), который может элиминировать •ОН и уменьшить окислительное повреждение онкологических клеток. (Yunxiu Zhang, Jianhong Zhang, Qingyan Jia, Jiechao Ge, Pengfei Wang «Innovative strategies of hydrogen peroxide-involving tumor therapeutics)), Materials Chemistry Frontiers, 2021, 5, p. 4474-4475. DOI: 10.1039/dlqm00134e).
Действительно, глутатион является известным антиоксидантом, в организме участвует в регуляции окислительно-восстановительного гомеостаза, метаболических процессах, обеспечивает защиту МОО от окислительного стресса и, соответственно, способствует прогрессированию опухоли, где его повышенные уровни коррелируют с увеличением метастазирования (Ankita Bansal, М. Celeste Simon «Glutathione metabolism in cancer progression and treatment resistance)), Journal of Cell Biology, 2018, 217(7), p.2291-2298. DOI: 10.1083/jcb.201804161).
Однако следует отметить, что повышенный уровень глутатиона характерен не только для солидных опухолей, но также отмечается и в лейкемических клетках (бластах), что коррелирует с устойчивостью к химиопрепаратам, используемым для лечения детей и взрослых с острым лимфобластным лейкозом (Z.T. Maung, L. Hogarth, М.М. Reid, S.J. Proctor, P.J. Hamilton, A.G. Hall «Raised intracellular glutathione levels correlate with in vitro resistance to cytotoxic drugs in leukaemic cells from patients with acute lymphoblastic leukemia», Leukemia, 1994 Sep.; 8(9):1487-91. PMID: 8090028). Более того, повышенный уровень бластного глутатиона связан с повышенным риском рецидива острого лимфолейкоза (Pamela R. Kearns, Rob Pieters, М.М. Antoinette Rottier, Andrew D.J. Pearson, Andrew G. Hall «Raised blast glutathione levels are associated with an increased risk of relapse in childhood acute lymphocytic leukemia)), Blood, 2001, 97 (2): 393-398. DOI: 10.1182/blood.V97.2.393), что возможно имеет схожие механизмы с ситуацией, когда повышенные уровни глутатиона в МОО коррелируют с увеличением метастазирования (смотри выше).
С Н2О2 глутатион (GSH) взаимодействует напрямую с образованием дисульфида:
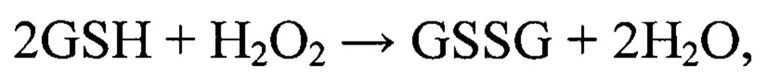
при этом в кислотной среде (например, кислом или слабокислом МОО) образуются радикалы GS• (К.М. Зинатуллина, О.Т. Касаикина, В.А. Кузьмин, Н.П. Храмеева «Взаимодействие глутатиона с пероксидом водорода. Кинетическая модель», Кинетика и катализ, 2019, том 60, №3, с. 281-288. DOI: 10.1134/s0453881119030183), а скорости расходования GSH и образования радикалов GS• в реакции GSH с 8,6 мМ Н2О2 (водный раствор, 37°С) возрастают соответственно в 2,2 и 2,4 раза при увеличении концентрации GSH от 2,6 до 10,1 мМ (К.М. Зинатуллина, О.Т. Касаикина, В.А. Кузьмин, Н.П. Храмеева «Про- и антиокислительные характеристики природных тиолов», Известия Академии наук. Серия химическая, 2018, №4, с. 728).
Следовательно, чем более выражен онкологический процесс, тем выше концентрация глутатиона (GSH), тем больше скорости расходования GSH и образования радикалов GS•, что имеет тройной онкопротекторный эффект: снижение уровня глутатиона способствует уменьшению элиминации •ОН, что в сочетании с образованием радикалов GS• повышает окислительный потенциал МОО и, следовательно, увеличивает окислительные повреждения онкологических клеток, что также препятствует метастазированию, так как имеет место прямая корреляция между уровнем глутатиона и развитием метастазов.
Кроме того, известно, что ацетилхолин, регулируя активность рецепторов к главному фактору роста эпителия и главному васкулогенному фактору роста, вовлекается в процесс превращений «аденома → карцинома». Слизистая оболочка толстого кишечника обладает ацетилхолинсинтезирующей функцией, которая регулируется уровнем содержания ацетилхолина нейронального происхождения. Совместное действие данных систем активирует процессы восстановления эпителиальных покровов толстого кишечника, играя важную роль в формировании очагов неоплазий. В случае формирования неоплазий ацетилхолин выступает в роли аутокринного и паракринного ростового фактора (А.В. Смирнова, И.Е. Трубицына «Ацетилхолин. Роль в канцерогенезе толстого кишечника. Обзор», Экспериментальная и клиническая гастроэнтерология, 2012, №9, с. 68). Клеточные линии рака легкого также синтезируют и секретируют ацетилхолин, который действует как аутокринный фактор роста (P. Song, H.S. Sekhon, В. Proskocil, J.K. Blusztajn, G.P. Mark, E.R. Spindel «Synthesis of acetylcholine by lung cancer», Life Sciences, 2003, Vol. 72, Issues 18-19, 28 March, p. 2159-2168. DOI: 10.1016/S0024-3205(03)00078-X). В свою очередь обнаружено, что под влиянием катионов ацетилхолина (Ach+) увеличивается скорость образования радикалов GS• в реакции GSH с H2O2 более чем в два раза (К.М. Зинатуллина «Кинетика и механизм радикальных реакций гидрофильных тиолов», автореферат диссертации на соискание ученой степени кандидата химических наук, Москва, 2021, с. 23), что еще больше повышает окислительный потенциал МОО.
В дополнение к вышесказанному показано, что ресвератрол, в молекуле которого содержится двойная связь, активированная сопряжением с двумя фенольными кольцами, взаимодействует с GSH в водных растворах при 37°С, при этом реакция протекает по цепному механизму и ускоряется в присутствии H2O2 (К.М. Зинатуллина, Н.П. Храмеева, О.Т. Касаикина, Б.И. Шапиро, В.А. Кузьмин «Кинетические характеристики взаимодействия ресвератрола с пероксильными радикалами и природными тиолами в водной среде», Известия Академии наук. Серия химическая, 2017, №11, с. 2145), что еще больше увеличивает скорость снижения повышенного уровня глутатиона, вызванного онкологическим процессом. Ресвератрол, являясь природным продуктом растительного происхождения, может поступать и организм с пищей (орехи, виноград, красное вино и др.) или в виде пищевой добавки.
Снижение концентрации глутатиона за счет взаимодействия с H2O2 дополнительно приводит к повышению эффективности XT за счет уменьшения потенциала для конъюгации GSH с ксенобиотиками, в частности, химиотерапевтическими препаратами (О.А. Борисенок, М.И. Бушма, О.Н. Басалай, А.Ю. Радковец «Биологическая роль глутатиона», Медицинские новости, 2019, №7, с. 6).
Необходимо отметить, что глутатион повышается не только в опухоли, но и в крови больных (И.А. Горошинская, Е.И. Сурикова, Е.М. Франциянц, Л.А. Немашкалова, П.С. Качесова, Д.Е. Медведева, А.А. Маслов. «Глутатион-зависимая система в крови больных раком желудка с разным гистотипом опухоли и распространенностью заболевания», Исследования и практика в медицине, 2021, том 8, №4, с. 12-22. DOI: 10.17709/2410-1893-2021-8-4-1).
Общеизвестно, что пероксид водорода является источником молекулярного кислорода:
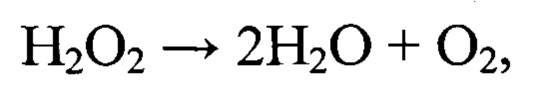
что может уменьшать гипоксию МОО и тем самым создавать условия для более эффективного применения таких противоопухолевых методов лечения, как XT, ЛТ, ФДТ, СДТ, ХДТ и др.
Например, известно, что у некоторых препаратов для XT, таких как паклитаксел и доксорубицин, терапевтический эффект сильно ослабляется при гипоксии, а эффект ЛТ может быть уменьшен на две трети в отсутствие молекул O2 (Yunxiu Zhang, Jianhong Zhang, Qingyan Jia, Jiechao Ge, Pengfei Wang «Innovative strategies of hydrogen peroxide-involving tumor therapeutics», Materials Chemistry Frontiers, 2021, 5, p. 4476. DOI: 10.1039/dlqm00134e).
Повышение оксигенации и окислительного потенциала МОО также может приводить к ускорению метаболизма эндо- и ксенобиотиков, в частности, химиотерапевтических препаратов, что в конечном итоге снижает токсическую нагрузку на организм как от самого заболевания, так и от XT и ЛТ.
Хорошо известно, что пероксид водорода эффективно распадается с образованием O2 при каталазе каталазой и каталазоподобными наноматериалами (например, ионами Mn, Fe3O4, CuS, CeO2, FeS2 и др.), которые широко использовались при создании многофункциональных нанореакторов для катализа распада эндогенного H2O2 с образованием O2 in situ в целях облегчения гипоксии опухоли и повышения противоопухолевой эффективности (Yunxiu Zhang, Jianhong Zhang, Qingyan Jia, Jiechao Ge, Pengfei Wang «Innovative strategies of hydrogen peroxide-involving tumor therapeutics)), Materials Chemistry Frontiers, 2021, 5, p. 4476. DOI: 10.1039/d1qm00134e). Принципиальными недостатками данного способа, принятого за прототип, являются:
- образование O2 только из эндогенного пероксида водорода, которого в опухолях недостаточно (50-100 мкМ);
- образование O2 in situ;
- задействование только одной противоопухолевой стратегии использования H2O2, а именно: облегчение гипоксии опухоли.
При этом известно, что увеличение концентрации вводимой внутривенно H2O2 более 0,18%, или более 0,05 М (справочно: плотность раствора H2O2 с концентрацией 1% имеет плотность 1,002 г/см при 18°С) приводит к выделению большого количества O2, в связи с чем возможна газовая эмболия пузырьками O2 мелких сосудов (патент РФ №2147889).
Задачей настоящего изобретения является разработка способа лечения онкологических заболеваний с помощью экзогенного экологически чистого водного раствора пероксида водорода (далее - экопероксид) как самостоятельного паллиативного средства, так и в сочетании с другими противоопухолевыми методами лечения для достижения улучшенных противоопухолевых эффектов, а также снижения токсической нагрузки на организм в ходе лечения.
Для решения поставленной задачи предлагается использовать введение в организм экопероксида как самостоятельного паллиативного, так и в сочетании с другими противоопухолевыми методами лечения.
Технический результат заключается в противоопухолевом эффекте от введения в организм экзогенного экологически чистого водного раствора пероксида водорода, улучшении противоопухолевых эффектов при его сочетании с другими противоопухолевыми методами лечения, а также снижении токсической нагрузки на организм в ходе лечения.
Технический результат достигается тем, что ежедневно вводят в организм как самостоятельное паллиативное средство, так и в сочетании с другими противоопухолевыми методами лечения экзогенный экологически чистый водный раствор пероксида водорода в диапазоне концентраций от 500 мкМ, что составляет 10-кратный избыток по отношению к концентрации минимального уровня эндогенного H2O2 в опухолях, до предельной безопасной его концентрации 0,05 М.
В варианте способа проводят внутривенное введение экопероксида в диапазоне концентраций от 500 мкМ до 0,05 М.
Способ лечения онкологических заболеваний с помощью экзогенного экологически чистого водного раствора пероксида водорода в диапазоне концентраций от 500 мкМ до 0,05 М реализуется следующим образом.
В настоящее время для получения пероксида (перекиси) водорода используют электрохимический метод через надсерную кислоту и органический метод жидкофазного окисления изопропилового спирта согласно ГОСТ 177-88 «Водорода перекись. Технические условия». При этом получаемый высококонцентрированный раствор H2O2 содержит токсические стабилизаторы (серную кислоту, мышьяк и др.), добавляемые для замедления разложения пероксида водорода, которые не позволяют использовать его для внутреннего применения в медицине.
Однако ряд клиник США и Мексики используют терапию пероксидом водорода, обычно основанную на введении препарата путем внутривенной инъекции, для широкого круга заболеваний (кроме онкологических). Для приготовления инъекционных (внутривенных) растворов используют 30% пероксид водорода пищевой или косметической марки фармакопеи США, являющийся сильным окислителем, что требует особой осторожности при обращении. Исходный 30% H2O2 разбавляют равным количеством стерильной дистиллированной воды, чтобы получить 15%-ный исходный раствор. Исходный раствор пропускают через фильтр Millipore для стерилизации и удаления твердых частиц. Затем готовят инфузионный раствор, используя стерильный водный 5%-ный раствор декстрозы, добавляя 0,25 мл стерильного 15%-ного исходного раствора H2O2 в 100 мл 5%-ного раствора декстрозы, в результате чего получают концентрацию 0,0375% H2O2, которую в конечном итоге используют для внутривенных инъекций (Moatasem Elshareif M.D. «Therapeutic use of Hydrogen Peroxide in ischemic heart disease», Research, June 2022, p. 1-6. https://www.researchgate.net/publication/361229121).
Принципиальным недостатком такого инфузионного раствора H2O2 является наличие стабилизатора, который удерживает пероксид водорода от распада и тем самым снижает его окислительный потенциал. Другим недостатком является то, что подготовка для внутривенного введения носит многостадийный характер, включая обращение с сильным окислителем (30% H2O2), при этом стабилизатор обладает токсичностью.
Известны способ и устройство получения экологически чистого раствора пероксида водорода из воды, в частности, из дистиллированной воды, с помощью воздействия на нее стримерами высоковольтного электрического разряда, что лишено вышеуказанных недостатков (международная заявка WO 2022/019795 А1).
Для реализации способа лечения онкологических заболеваний с помощью экзогенного экологически чистого водного раствора пероксида водорода последний получен по способу и на устройстве, описанными в вышеуказанной заявке на изобретение, и использован с концентрацией 500 мкМ, то есть на уровне минимально достаточном.
Экопероксид вводят как самостоятельное паллиативное средство, так и в сочетании с XT и ЛТ, максимально реализуя вышеописанные механизмы противоопухолевого действия H2O2, повышая оксигенацию и окислительный потенциал как организма, так и МОО, запуская окислительно-восстановительные противоопухолевые сигнальные каскады. Окислительный потенциал увеличивают за счет снижения концентрации глутатиона путем непосредственного взаимодействия его с H2O2, в том числе в присутствии ацетилхолина, а также взаимодействия глутатиона с ресвератролом в присутствии H2O2, при этом сохраняется высокоцитотоксичный радикал •ОН и дополнительно образуется радикал GS•. Ресвератрол в организм поступает с пищей, например, в виде орехов, винограда, красного вина и других продуктов растительного происхождения или в виде пищевой добавки.
Повышение оксигенации и окислительного потенциала как организма, так и МОО приводит к ускорению метаболизма эндо- и ксенобиотиков, в частности, химиотерапевтических препаратов, что в конечном итоге снижает токсическую нагрузку на организм как от самого заболевания, так и от XT и ЛТ.
Экологически чистый водный раствор пероксида водорода в организм вводят внутривенно или перорально.
Наиболее эффективно применение экологически чистого водного раствора пероксида водорода при сочетании его с другими противоопухолевыми методами лечения, в частности, при XT и ЛТ.
В случае прогрессирования онкологического заболевания и исчерпании общепринятых лечебных возможностей (оперативное лечение, XT, ЛТ и др.) - внутривенное, пероральное введение в организм экзогенного экологически чистого водного раствора пероксида водорода является важным паллиативным средством.
Дозу экопероксида, продолжительность курса лечения и путь (пути) введения H2O2 в организм определяет лечащий врач в зависимости от стадии (степени тяжести) онкологического заболевания, локализации опухоли и состояния больного, наследственной предрасположенности, перенесенного противоопухолевого лечения.
Заявленное изобретение иллюстрируется примерами 1-4, таблицами 1-6.
Пример 1. Экспериментальная оценка влияния экопероксида, доксорубицина и их комбинации на продолжительность жизни мышей после трансплантации лейкозных клеток Р388.
Доксорубицин - противоопухолевый препарат, показанный при лечении лейкозов.
Схема эксперимента (4 группы по 10 мышей в каждой):
- 1 группа (контрольная) - трансплантация только лейкозных клеток Р388;
- 2 группа (опытная) - трансплантация лейкозных клеток Р388 с введением экопероксида двукратно через 1 час и через 24 часа после трансплантации лейкозных клеток;
- 3 группа (опытная) - трансплантация лейкозных клеток Р388 с введением доксорубицина однократно через 24 часа после трансплантации лейкозных клеток;
- 4 группа (опытная) - трансплантация лейкозных клеток Р388 с введением экопероксида через 1 час после трансплантации лейкозных клеток Р388, затем через 24 часа вводили доксорубицин и через 5 минут после доксорубицина вводили еще раз экопероксид.
Лейкозные клетки Р388 вводили животным внутрибрюшинно.
Экопероксид и доксорубицин вводили внутрибрюшинно (аналог внутривенного введения у человека).
Экопероксид вводили с концентрацией 850 мкМ в объеме 0,5 мл при средней массе мыши 20 г в дозе 0,7 мг/кг.
Доксорубицин вводили в дозе 5 мг/кг массы мыши.
Лабораторных животных наблюдали 75 суток с последующей эвтаназией.
В ходе эксперимента определяли среднюю продолжительность жизни погибших мышей, а также выживаемость (В, %) лабораторных животных в целом по группе, которую оценивали по формуле:
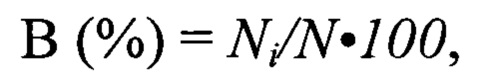
где, Ni - количество живых мышей на 75 сутки эксперимента, N - общее количество мышей, участвующих в эксперименте, в контрольной и опытных группах соответственно.
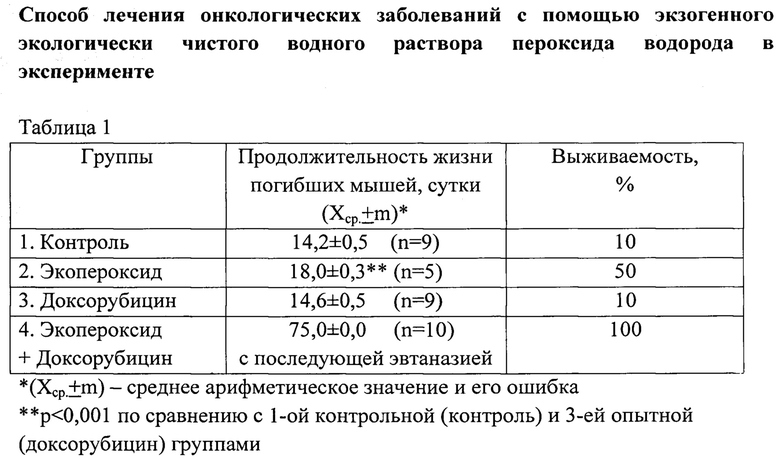
В таблице 1 представлена оценка влияния экопероксида, доксорубицина и их комбинации на продолжительность жизни мышей после трансплантации лейкозных клеток (Р388).
Как следует из таблицы 1, комбинированное применение экопероксида и противоопухолевого препарата доксорубицин обеспечило максимальную 100% выживаемость в течение 75 суток наблюдения после трансплантации лейкозных клеток Р388. При применении же только экопероксида выживаемость была на уровне 50%, что в 5 раз выше, а продолжительность жизни погибших мышей на 3-е суток дольше, чем в контроле и опытной группе с введением только доксорубицина, являющимся достаточно токсичным препаратом. Предварительное и последующее после доксорубицина введение экопероксида обеспечивало повышение оксигенации организма: в этих условиях наиболее эффективно проявлялось противоопухолевое действие доксорубицина, что согласуется с вышеприведенными известными данными о том, что терапевтический эффект доксорубицина сильно ослабляется при гипоксии.
Пример 2. Экспериментальная оценка противоопухолевой активности экопероксида, доцетаксела и их комбинации на модели рака предстательной железы DU145 у мышей.
Доцетаксел - противоопухолевый препарат, показанный при раке предстательной железы.
Схема эксперимента (4 группы по 7 мышей в каждой):
- 1 группа (контрольная) - трансплантация только опухолевых клеток DU145;
- 2 группа (опытная) - трансплантация опухолевых клеток DU145 с введением экопероксида;
- 3 группа (опытная) - трансплантация опухолевых клеток DU145 с введением доцетаксела;
- 4 группа (опытная) - трансплантация опухолевых клеток DU145 с введением с комбинированным введением экопероксида и доцетаксела.
Опухолевые клетки DU145 вводили животным подкожно билатерально, то есть в каждой группе имело место 14 опухолей.
Экопероксид и доцетаксел вводили внутрибрюшинно (аналог внутривенного введения у человека).
Лечение начинали на 17-е сутки после подкожной перевивки DU145, когда средний объем опухолевых узлов достиг 100 мм, далее лечение продолжали 19 суток и еще наблюдали в течение 20, 21 и 22 суток с последующей эвтаназией.
Экопероксид с концентрацией 500 мкМ в объеме 0,7 мл при средней массе мыши 24 г в дозе 0,5 мг/кг вводили ежедневно.
Доцетаксел вводили в дозе 10 мг/кг массы мыши один раз через двое суток на третьи после предыдущего введения, то есть последний раз доцетаксел вводили на 19 последние сутки лечения.
Объем опухоли определяли по формуле:
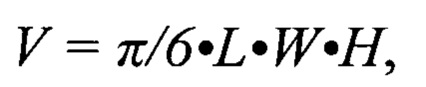
где L, W, Н - линейные размеры опухоли в миллиметрах (длина - L, ширина - W, высота - Н).
Торможение роста опухоли (ТРО, %) вычисляли по формуле:
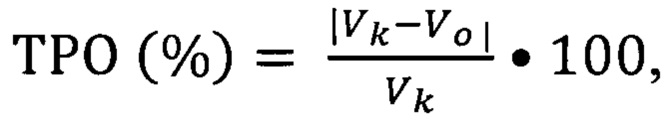
где Vk и Vo - средний объем опухоли (мм3) в контрольной и опытной группах соответственно.
Выживаемость (В, %) лабораторных животных оценивали по формуле:
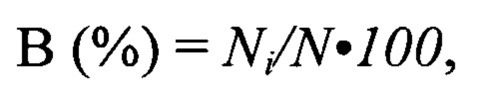
где, Ni - количество живых мышей на i день эксперимента, N - общее количество мышей, участвующих в эксперименте, в контрольной и опытной группах соответственно.
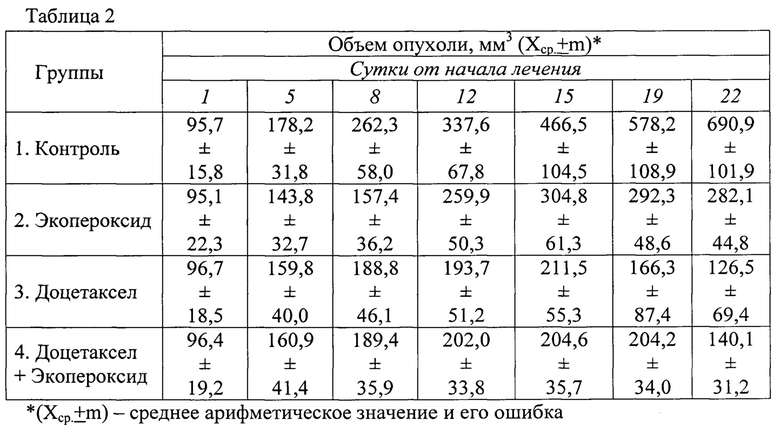
Динамика роста опухоли в экспериментальных группах представлена в таблице 2.
1 группа (контрольная). В первые сутки, то есть на момент начала лечения в опытных группах, объем опухоли составил Vcp=95,7±15,8 мм, который практически не отличался от аналогичных показателей в опытных группах. Без лечения размеры опухоли к 19 и 22-м суткам после трансплантации достигли соответственно Vcp=578,2±108,9 мм и Vcp=690,9±101,9 мм. Все мыши в группе живы.
2 группа (опытная, с введением экопероксида). На 19-е сутки после начала лечения наблюдали ТРО=49% (Vcp=292,3±48,6 мм против Vcp=578,2±108,9 мм в контроле, р=0,053). На третьи сутки после прекращения лечения (22 сутки эксперимента) торможение роста опухоли выросло на 10% и составило уже ТРО=59% (Vcp=282,l±44,8 мм против Vcp=690,9±101,9 мм3 в контроле, р=0,028). Все мыши в группе живы.
3 группа (опытная с введением доцетаксела). На 19-е сутки после начала лечения ТРО=71% (Vcp=166,3±87,4 мм3 против Vcp=578,2±108,9 мм3 в контроле, р=0,008). На третьи сутки после прекращения лечения (22 сутки эксперимента) наблюдали ТРО=82% (Vcp=126,5±69,4 мм3 против Vcp=690,9±101,9 мм3 в контроле, р=0,002). На 19 сутки (последний день лечения) и на 22 сутки (третьи сутки после прекращения лечения) выживаемость составила 29%.
4 группа (опытная с введением экопероксида и доцетаксела). На 19-е сутки после начала лечения наблюдали ТРО=65% (Vcp=204,2±34,0 мм3 против Vcp=578,2±108,9 мм3 в контроле, р=0,024). На третьи сутки после прекращения лечения наблюдали ТРО=78% (Vcp=140,1±31,3 мм3 против Vcp=690,9±101,9 мм3 в контроле, р=0,002). На 19 сутки (последний день лечения) выживаемость составила 71%, а на 22 сутки (третьи сутки после прекращения лечения) - 29%.
Снижение токсической нагрузки при лечении доцетакселом особенно ярко проявляется при анализе выживаемости мышей в контрольной и опытных группах в ходе всего эксперимента.
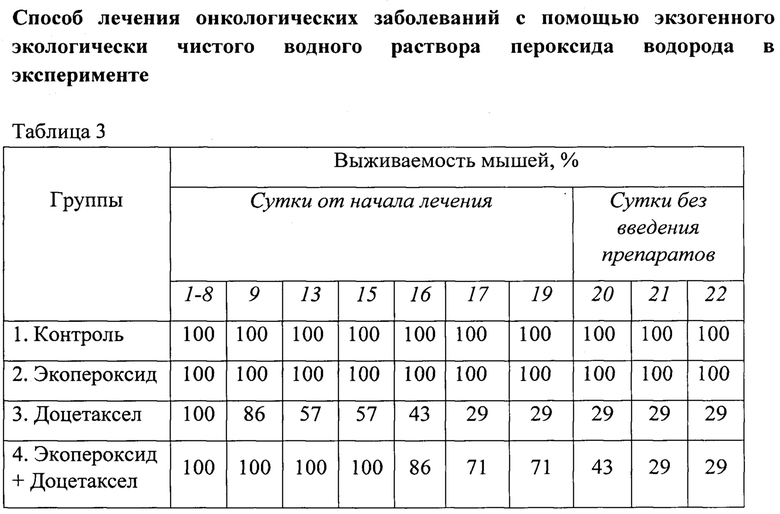
В таблице 3 представлена выживаемость мышей в контрольной и опытных группах в ходе эксперимента.
При лечении доцетакселом (3 группа) уже после 8-х суток появляются погибшие мыши и выживаемость мышей снижается по нарастающей вплоть до 29%, в то время как при лечении в комбинации «экопероксид+доцетаксел»
(4 группа) погибшие мыши появляются только после 15-х суток, при этом выживаемость в этой группе была от 2 до 2,4 раза выше, чем в группе, где применялся только доцетаксел. После завершения лечения на 19 сутки и прекращении защитного действия экопероксида уже на 21-ые и 22-ые сутки выживаемость сравнялась с 17 сутками в 3-ей группой, где вводился только доцетаксел, достигнув 29% при практически одинаковом ТРО. Но так как при экзогенном введении экопероксида реализуется несколько противоопухолевых стратегий, то несмотря на прекращение введения экопероксида и снижение выживаемости в 4-ой группе (экопероксид+доцетаксел) до уровня 3-ей группы (доцетаксел) еще сохраняется его следовое (остаточное) онкопротекторное действие, выражающееся в том, что ТРО во 2-ой группе, где вводился только экопероксид, за 20-22 сутки увеличилось на 10%, достигнув максимального результата в группе, а именно: ТРО=59% при 100% выживаемости.
Таким образом, комбинированное применение экопероксида и противоопухолевого препарата доцетаксел обеспечило более высокую выживаемость (в 2-2,4 раза) по сравнению с лечением только доцетакселом при практически одинаковом ТРО, тем самым экспериментально подтверждая защитную функцию экопероксида от токсического действия химиопрепарта. При применении только экопероксида выживаемость была на уровне 100%, что в 3,4 раз выше, чем в группах 3 и 4 на 22 сутки эксперимента при достаточно высоком ТРО=59%.
Пример 3. Экспериментальная оценка противоопухолевой активности экопероксида при его пероральном применении на модели эпидермоидной карциномы легкого Льюис (Lewis lung carcinoma (LLC)) у мышей.
Схема эксперимента:
- 1 группа (контрольная) - без лечения с трансплантацией только опухолевых клеток LLC, состоящая из 10 мышей;
- 2 группа (опытная) - трансплантация опухолевых клеток LLC с пероральным введением экопероксида через 48 часов с момента трансплантации опухолевых клеток LLC, состоящая из 6 мышей.
Опухолевые клетки карциномы легкого Льюис вводили животным подкожно.
Экопероксид с концентрацией 500 мкМ в объеме 0,5 мл при средней массе мыши 18 г в дозе 0,5 мг/кг вводили перорально ежедневно. Начинали поить через 48 часов с момента трансплантации опухолевых клеток по принятой для химиопрепаратов методике ежедневно в течение 5 суток с интервалом 24 часа с последующим наблюдением за животными до их гибели. Начало лечения экопероксидом через 48 часов соответствовало времени интенсивного размножения опухолевых клеток, что обеспечивало их нахождение в наиболее чувствительном состоянии (по опыту химиотерапии).
Объем опухолевого узла определяли по формуле:
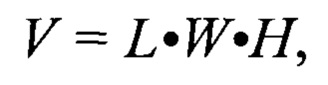
где L, W, H - три максимальных взаимно перпендикулярных линейных размера опухоли в миллиметрах (длина - L, ширина - W, высота - Н).
Торможение роста опухоли (ТРО, %) вычисляли по формуле:
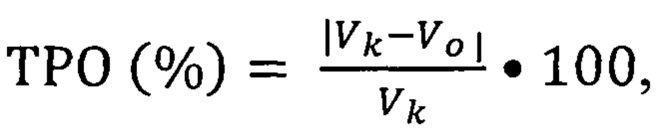
где Vk и Vo - средний объем опухоли (мм3) в контрольной и опытной группах соответственно.
Также определяли среднюю продолжительность жизни (СПЖ) в сутках в контрольной и опытной группах, на основании чего рассчитывали увеличение продолжительности жизни в процентах (УПЖ, %) в опытной группе по отношению к контрольной по формуле:
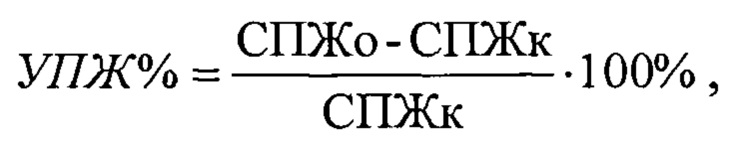
где СПЖо и СПЖк - средние продолжительности жизни животных в сутках в опытной и контрольной группах соответственно.
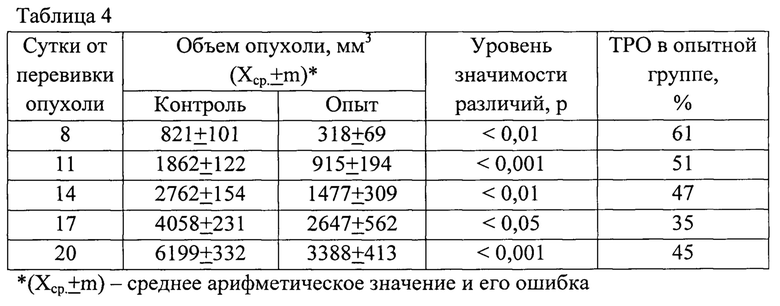
В таблице 4 представлен объем опухоли в контрольной и опытной группах со статистической оценкой значимости различий и процент торможения роста опухоли (ТРО%) в опытной группе на 8, 11, 14, 17 и 20 сутки с момента перевивки опухоли LLC.
Как следует из таблицы 4, пероральное введение экопероксида при LLC мышей, показало достоверную его противоопухолевую активность с ТРО=61% на 8-е сутки с момента перевивки опухоли (1-е сутки после прекращения лечения) в опытной группе, которое поддерживалось на достоверном уровне в опытной группе на 11, 14, 17 и 20 сутки с момента перевивки опухоли со средним значением ТРО=45%.
Существенное торможение роста опухоли в опытной группе по сравнению с контрольной группой закономерно приводит и к большей продолжительности жизни в опытной группе.
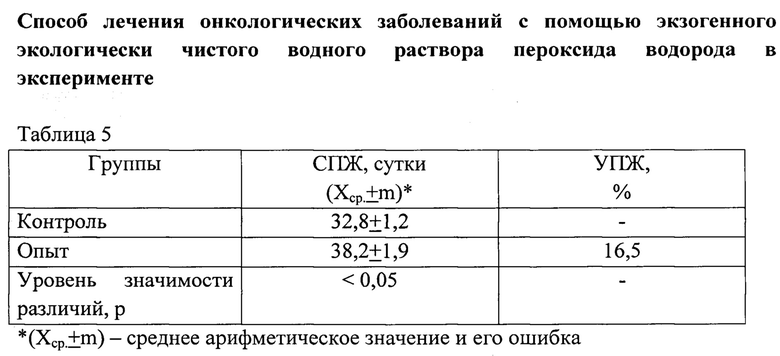
В таблице 5 представлено сравнение СПЖ в контрольной и опытной группах и увеличения продолжительности жизни в опытной группе по отношению к контрольной группе.
В опытной группе СПЖ оказалась на 5,4 суток больше по сравнению с контролем с уровнем значимости различий р<0,05, при этом процент увеличения продолжительности жизни в опытной группе по отношению к контролю составил УПЖ=16,5%.
Таким образом, пероральное применение экопероксида обеспечивает через 5 суток лечения торможение роста опухоли до 61%, которое сохраняется в дальнейшем уже без лечения на уровне ~45% как минимум в течение 20 суток за счет следового (остаточного) онкопротекторного действия экопероксида, что в конечном итоге обеспечивает увеличение средней продолжительности жизни на 5,4 суток, что составляет 16,5% по отношению к контрольной группе.
Пример 4. Экспериментальная оценка взаимодействия глутатиона с ресвератролом в присутствии и отсутствие пероксида водорода (Н2О2).
Ресвератрол - растительный полифенол, содержащийся в значительном количестве в ряде продуктов и напитков, в частности, красном вине. Он привлекает внимание медиков и биохимиков в связи с так называемым «французским парадоксом» - низким уровнем сердечно-сосудистых и онкологических заболеваний при высококалорийном питании с обилием жиров, что связывают с регулярным потреблением во Франции красного вина, содержащего ресвератрол (https://ru.wikipedia.org/wiki/Французский_парадокс). В ходе перекисного окисления жиров может образовываться в организме дополнительное количество пероксида водорода.
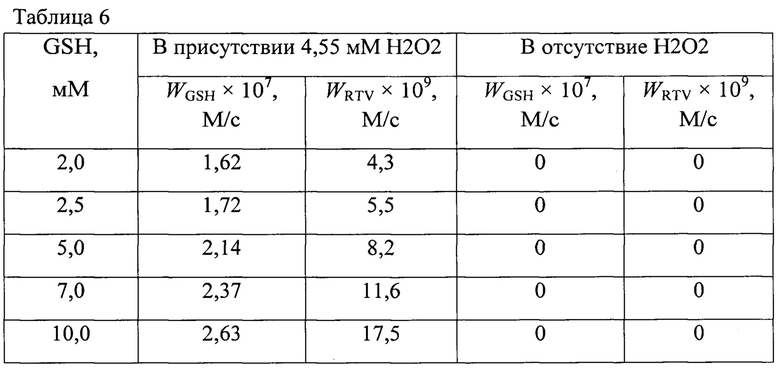
В связи с этим проведен эксперимент in vitro по оценке взаимодействия глутатиона с ресвератролом в присутствии и отсутствие пероксида водорода (Н2О2). Измеряли скорости (W) расходования глутатиона (GSH) в диапазоне его концентраций от 2,0 до 10,0 мМ и 0,03 мМ ресвератрола (RVT) в присутствии 4,55 мМ пероксида водорода (H2O2) и его отсутствии в водной среде при температуре 37°С.
Результаты эксперимента представлены в таблице 6.
В ходе эксперимента установлено, что имеет место активное взаимодействие глутатиона с ресвератролом в присутствии пероксида водорода. При этом чем больше концентрация глутатиона, тем выше скорость его расходования, что имеет существенное значение для профилактики и лечения онкологических заболеваний, при которых микроокружение солидных опухолей содержит большое количество глутатиона в диапазоне от 2 до 10 мМ (Yunxiu Zhang, Jianhong Zhang, Qingyan Jia, Jiechao Ge, Pengfei Wang «Innovative strategies of hydrogen peroxide-involving tumor therapeutics», Materials Chemistry Frontiers, 2021, 5, p. 4474-4475. DOI: 10.1039/d1qm00134e).
Таким образом, приведенные примеры подтверждают эффективность предлагаемого способа лечения онкологических заболеваний с помощью экзогенного экологически чистого водного раствора пероксида водорода. Его введение повышает оксигенацию и окислительный потенциал как организма, так и МОО, при этом Н2О2, являясь сигнальной молекулой, активно участвует как напрямую в биохимических реакциях с глутатионом, так и в качестве катализатора, ускоряя его реакцию с ресвератролом, что в совокупности обеспечивает противоопухолевый эффект и позволяет рассматривать экопероксид как эффективное универсальное неспецифическое действующее опосредованно средство для терапии злокачественных опухолей, которое может применяться как самостоятельно в рамках паллиативной помощи, так и в сочетании с другими противоопухолевыми методами лечения для достижения улучшенных противоопухолевых эффектов, снижая при этом токсическую нагрузку на организм как от самого заболевания, так и от противоопухолевой терапии. Основными путями введения в организм экзогенного экологически чистого водного раствора пероксида водорода являются внутривенное или пероральное.
| название | год | авторы | номер документа |
|---|---|---|---|
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| Титановый имплантат с функцией локальной иммунотерапии для остеореконструктивной хирургии и профилактики местного рецидива онкологического заболевания и способ его изготовления | 2021 |
|
RU2779367C1 |
| Биомедицинский клеточный продукт со специфической противоопухолевой активностью, представленный популяциями лимфокин-активированных киллеров и анти-HER2 CAR-γδΤ-ОИЛ и анти-HER2 CAR-T-NK | 2022 |
|
RU2786210C1 |
| Низкотоксичная фармацевтическая композиция с противоопухолевой активностью в отношении холангиокарциномы | 2023 |
|
RU2825942C1 |
| Биомедицинский клеточный продукт с анти-HER2 специфической противоопухолевой активностью | 2019 |
|
RU2728361C1 |
| Биодеградируемый имплантат для локальной иммунотерапии онкологических больных | 2021 |
|
RU2780932C1 |
| Биомедицинский клеточный продукт для терапии злокачественных новообразований | 2023 |
|
RU2813531C1 |
| Биодеградируемый металлический имплантат для локальной иммунотерапии пациентов с солидными опухолями | 2021 |
|
RU2780927C1 |
| Способ лечения рака толстой кишки человека SW620 в эксперименте | 2017 |
|
RU2665168C1 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО | 2014 |
|
RU2572691C1 |
Изобретение относится к медицине, а именно к онкологии, и может быть использовано при лечении онкологических заболеваний в эксперименте. Способ включает введение в организм экзогенного экологически чистого водного раствора пероксида водорода (далее - экопероксид) в диапазоне концентраций от 500 до 850 мкМ, который вводят внутрь организма как самостоятельное паллиативное средство, так и в сочетании с другими противоопухолевыми методами лечения. Введение экопероксида осуществляют внутривенно или перорально, а также в сочетании с ресвератролом, поступающим в организм с пищей или в виде пищевой добавки. Использование изобретения позволяет достичь противоопухолевого эффекта за счет повышения оксигенации и окислительного потенциала как организма, так и микроокружения опухоли под действием экопероксида, снижения токсической нагрузки на организм как от самого заболевания, так и от противоопухолевой терапии. 3 з.п. ф-лы, 6 табл., 4 пр.
1. Способ лечения онкологических заболеваний в эксперименте, отличающийся тем, что применяют экзогенный экологически чистый водный раствор пероксида водорода (далее экопероксид) в диапазоне концентраций от 500 до 850 мкМ, который вводят внутрь организма как самостоятельное паллиативное средство, так и в сочетании с другими противоопухолевыми методами лечения.
2. Способ по п. 1, отличающийся тем, что введение в организм экопероксида осуществляют внутривенно.
3. Способ по п. 1, отличающийся тем, что введение в организм экопероксида осуществляют перорально.
4. Способ по п. 1, отличающийся тем, что экопероксид вводят внутрь организма в сочетании с ресвератролом, поступающим в организм с пищей или в виде пищевой добавки.
| СПОСОБ ОЗДОРОВЛЕНИЯ ОРГАНИЗМА | 2002 |
|
RU2201229C1 |
| Устройство получения экологически чистого раствора пероксида водорода для стимуляции роста и развития растений | 2020 |
|
RU2773011C1 |
| СТИМУЛЯТОР ЭНДОГЕННОЙ ПРОДУКЦИИ ЦИТОКИНОВ И ГЕПОПОЭТИЧЕСКИХ ФАКТОРОВ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 1995 |
|
RU2089179C1 |
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| MURPHY E.C | |||
| et al | |||
| Hydrogen peroxide and cutaneous biology: Translational applications, benefits, and risks | |||
| J Am Acad Dermatol | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| PMID: 31103570, реферат. | |||
Авторы
Даты
2024-09-04—Публикация
2023-04-03—Подача