Изобретение относится к медицине, а именно, к онкологии и реконструктивно-пластической хирургии у больных раком молочной железы.
Одной из самых сложных анатомических структур для восстановления во время реконструкции молочной железы является инфрамаммарная складка (ИМС). ИМС является важной анатомической структурой, определяющей положение, форму и вид женской груди, а ее несостоятельность при аугментации и реконструкции часто приводит к птозу и/или вторичным деформациям. Поэтому сохранение, восстановление ИМС является важной составляющей успешной реконструкции молочной железы и позволяет добиться оптимального эстетического результата, близкого к естественному виду груди.
Несмотря на значительные успехи в области реконструкции молочной железы, реконструкция инфрамаммарной складки до сих пор представляет сложность для онкологов и пластических хирургов (Kraft С.Т. et al. Inframammary Fold Reconstruction in the Previously Reconstructed Breast: A Comprehensive Review // PlastReconstr Surg. 2019. Vol. 143, №4. P. 1019-1029). Возможные методы часто описываются в литературе на небольших выборках и, как правило, без сравнения с контрольными группами и объективной оценки эстетического результата. Кроме того, большинство исследований включают короткий период наблюдения, а в некоторых случаях о послеоперационном ведении пациентов не сообщается.
Современная онкопластическая хирургия имеет множество различных методик и позволяет выполнять органосохраняющее лечение без нарушения эстетики груди. Но некоторые клинические ситуации предполагают как вариант хирургического лечения только мастэктомию.
В современной хирургии мастэктомия выполняется при верифицированном онкологическом заболевании. Среди возможных вариантов выполнения мастэктомии при онкологических заболеваниях молочной железы можно выделить следующие: традиционная радикальная мастэктомия (РМЭ), кожесохраняющая радикальная мастэктомия (КРМЭ) и подкожная радикальная мастэктомия с сохранением сосково-ареолярного комплекса (ПРМЭ).
Каждый метод имеет свои показания и противопоказания, предпочтения и риски, но во всех хирургических техниках нарушаются анатомические связи, формирующие ИМС с одной или двух сторон. Поэтому до настоящего времени продолжается поиск способов ее воссоздания с использованием местных тканей, имплантатов или трансплантатов.
Одним из актуальных направлений в реконструкции инфрамаммарной складки является использование вспомогательных мембран для укрепления нижнего склона имплантата. За рубежом к таким методикам относится ацелюллярный дермальный матрикс (ADM).
Известно применение ADM для укрепления нео-инфрамаммарной складки путем создания мышечно-дермального кармана имплантата, фиксируя матрикс к нижнему и латеральному краям большой грудной мышцы, тканям грудной стенки и/или переднему краю передней зубчатой мышцы (Spear S.L. et al. Applications of acellular dermal matrix in revision breast reconstruction surgery//PlastReconstr Surg. 2014. Vol. 133, №1. P. 1-10).
В ранней литературе применение ADM связывали с повышенным риском развития инфекционных осложнений, сером, гематом (Kim Т., Cho Н. The suitability of absorbable mesh insertion for oncoplastic breast surgery in patients with breast cancer scheduled to be irradiated // J Breast Cancer. 2013. Vol. 16, №1. P. 84-89). Однако в последние годы исследователи обратили внимание на дополнительное применение антибиотиков как местного применения, так и в качестве дополнительной профилактики в раннем послеоперационном периоде, что снизило количество осложнений до таковых при классических реконструкциях (Kim J.H. et al. Inframammary Fold Incision Can Reduce Skin Flap Necrosis in Immediate Breast Reconstruction With Implant and Conjoined Fascial Flap // Ann Plast Surg. 2020. Vol. 85, №5. P. 488-494).
В России также зарегистрирован патент на одномоментную реконструкцию молочной железы при раке с использованием ацеллюлярногодермального матрикса и силиконового эндопротеза (RU 2584133 С2). Таким образом, применение ADM в реконструкции молочной железы обосновано, но недостатки данной методики включают кратное увеличение стоимости операции.
В связи с этим ведутся разработки отечественных аналогов ADM, схожих по характеристикам, но приемлемой цене.
Так в 2020 году был зарегистрирован патент на способ реконструктивно-пластической хирургии у больных раком молочной железы с использованием ксеноперикарда Био ЛАБ-ПП/ПА и силиконового эндопротеза (RU 2743199 С2). Метод фиксации данной матрицы в организме аналогичен ранее описанной методике с ADM.
Таким образом, разработка и применение различных способов, которые надлежащим образом восстанавливают ИМС, является актуальным и необходимым для достижения оптимального эстетического результата реконструктивной маммопластики.
Техническим решением данного изобретения является применением небиодеградируемого сетчатого имплантата из политетрафторэтилена для реконструкции ИМС и достижения стабильного результата.
Технический результат заявленного изобретения заключается в обеспечении сохранения и укрепления ИМС в процессе хирургического лечения рака молочной железы посредством подкожной радикальной мастэктомии с использованием силиконового имплантата, и, соответственно, получения, в последующем, длительно сохраняющегося удовлетворительного косметического эффекта при одновременном значительном снижении риска осложнений, за счет исключения возможности развития хирургической агрессии по отношению к тканям, окружающим молочную железу вследствие использования биоинертного материала ПТФЭ, которым отграничивают силиконовый имплантат.
Технический результат достигается за счет предлагаемого способа реконструкции инфрамаммарной складки после подкожной радикальной мастэктомии у больных раком молочной железы (РМЖ) 0-III стадий с использованием силиконового имплантата, отличающийся тем, что после проведения подкожной радикальной мастэктомии выделяют нижний край большой грудной мышцы и переднюю зубчатую мышцу, формируя таким образом субпекторальный карман, из перфорированной пористой мембраны (ПТФЭ) выкраивают полукруг, при этом его основание соответствует длине нео-инфрамаммарной складки, а высота соответствует длине половины окружности силиконового имплантата, затем основание мембраны подшивают в проекции нео-инфрамаммарной складки к грудной фасции непрерывным швом рассасывающейся атравматичной нитью викрил 3/0, устанавливают в субпекторальный карман силиконовый имплантат и покрывают нижний полюс установленного силиконового имплантата мембраной, закрывая при этом дно субпекторального кармана, свободный полукруглый край мембраны сопоставляют с нижним краем большой грудной мышцы и передней зубчатой мышцы и накладывают непрерывный шов рассасывающейся атравматичной нитью викрил 3/0.
Способ иллюстрирован следующими графическими материалами:
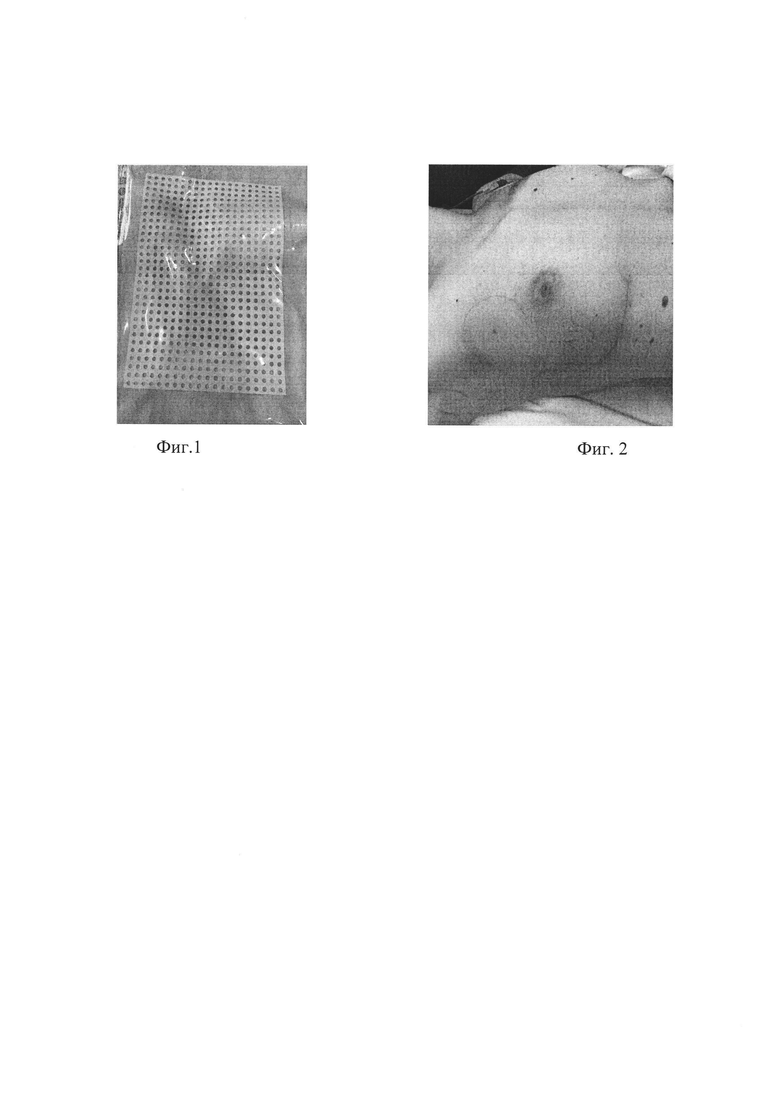
Фиг. 1 - Мембрана ПТФЭ 10,0×15,0 см.
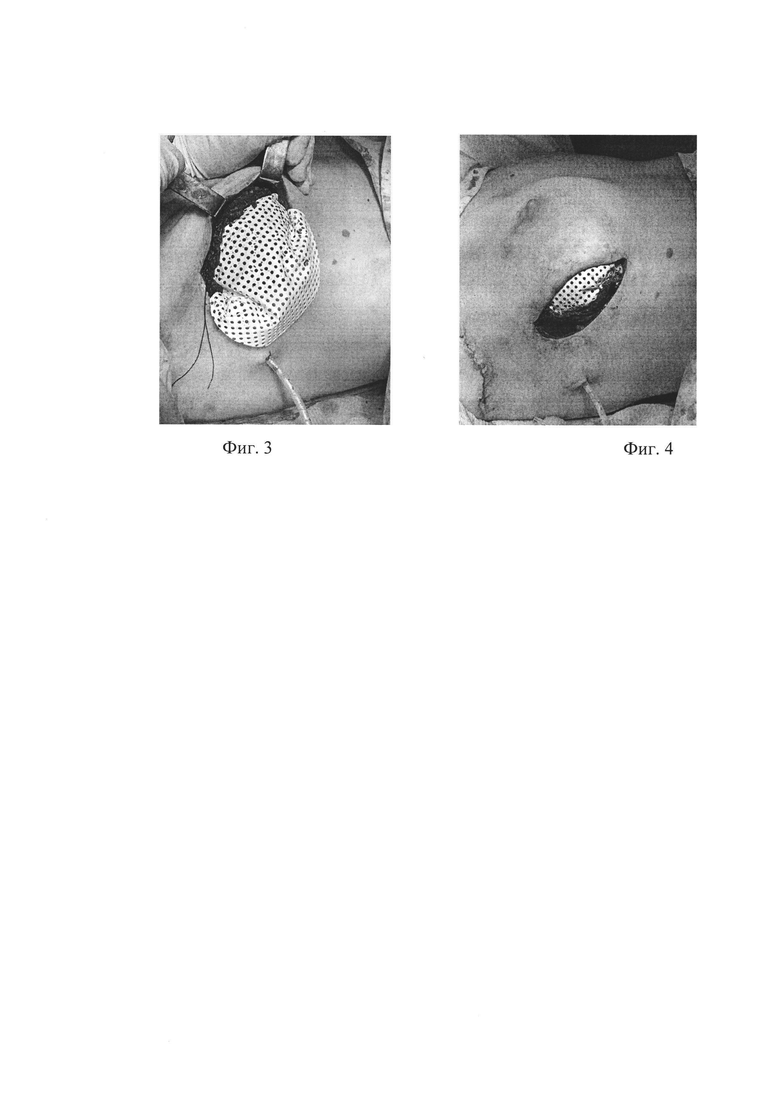
Фиг. 2 - Предоперационная разметка.
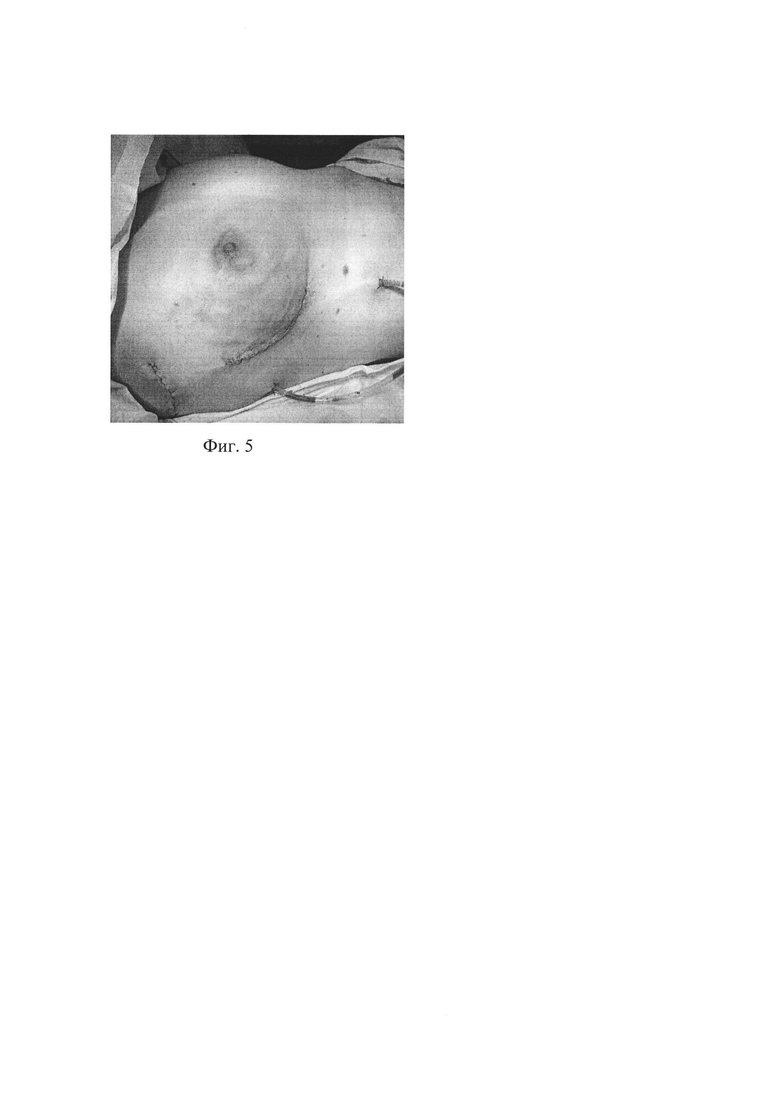
Фиг. 3 - Вид операционной раны после подшивания мембраны ПТФЭ к нижнему краю большой грудной мышцы.
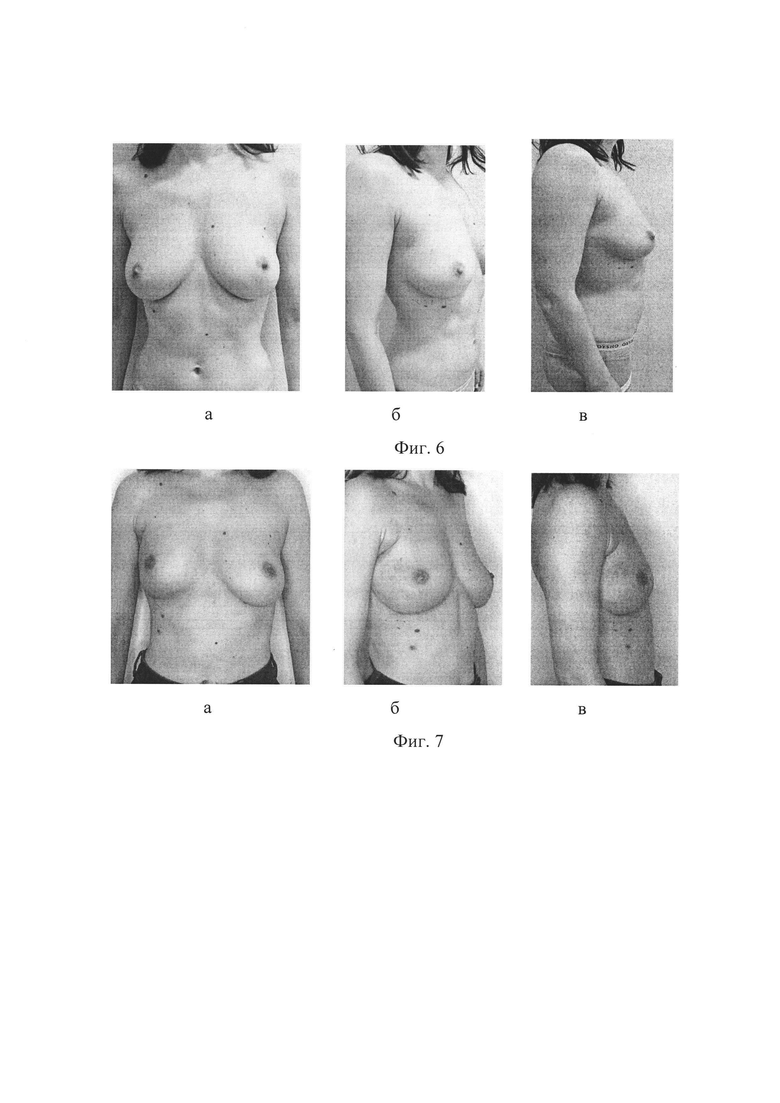
Фиг. 4 - Вид операционной раны после установки силиконового эндопротеза и закрытия мышечно-мембранного кармана.
Фиг. 5 - Вид ушитой операционной раны.
Фиг. 6 - Вид пациентки перед операцией: а) в прямой проекции; б) в полубоковой проекции, справа; в) в боковой проекции, справа.
Фиг. 7 - Вид пациентки через 3 недели после операции: в прямой проекции; б) в полубоковой проекции, справа; в) в боковой проекции, справа.
Ниже представлено более детальное описание заявленного способа, которое не ограничивает объем притязаний изобретения, а демонстрирует возможность его осуществления с достижением заявляемого технического результата.
Показаниями к осуществлению способа, согласно данному изобретению, является РМЖ 0-III стадий. Выполнять данное вмешательство возможно как на I этапе лечения, так и после проведенной неоадъювантной лекарственной терапии (в зависимости от характера местной распространенности опухолевого процесса).
Выполняют подкожную радикальную мастэктомию у больных раком молочной железы. Затем выделяют нижний край большой грудной мышцы и переднюю зубчатую мышцу, формируя таким образом субпекторальный карман.
Из перфорированной пористой мембраны (ПТФЭ) выкраивают полукруг, при этом его основание соответствует длине нео-инфрамаммарной складки, а высота соответствует длине половины окружности силиконового имплантата. Заявитель использовал новый материал отечественного производства - политетрафторэтилен (ПТФЭ).
ПТФЭ используется в таких областях, как кардио- и сердечнососудистая хирургия, травматология, герниология (Roina Y. et al. ePTFE-basedbiomedicaldevices: Anoverviewofsurgicalefficiency // J BiomedMater Res В ApplBiomater. 2022. Vol. 110, №2. P. 302-320). ПТФЭ - синтетический нерассасывающийся материал белого цвета, имеющий пористую структуру. Лабораторные исследования показали биосовместимость, инертность, апирогенность, достаточную прочность и эластичность мембран, легко моделируются. Таким образом, применение ПТФЭ в качестве эндопротеза обосновано с точки зрения механических и физических свойств. Принимая во внимание характеристики ПТФЭ, результаты его применения в ранее проведенных областях и российское производство, можно предположить, что данный материал может конкурировать с такими аналогами, как ацеллюлярный дермальный матрикс и сетчатые импланты, при использовании в качестве вспомогательного материала при реконструктивной маммопластике с использованием имплантов в качестве фиксатора и покрытия нижнего склона молочной железы при дефиците подкожно-жировой клетчатки.
Аналогов использования ПТФЭ в онкологии и реконструктивно-пластической хирургии у больных раком молочной железы в отечественной и зарубежной литературе нами не обнаружено.
В данном случае использована перфорированная пористая мембрана компании «Экофлон» (RU 2389449 С2), которую для укрепления послегрыжевого дефекта брюшной стенки. Наличие дополнительных перфораций в мембране улучшает циркуляцию жидкости (эксудата) вокруг имплантата и быстрое прорастание кровеносными сосудами. Мембрана не требует предварительной обработки, поставляется в стерильном крафт-пакете и готова к применению.
Однако возможно применение и других ПТФЭ мембран, которые соответствуют необходимым в данном случае характеристикам.
Основание мембраны подшивают в проекции нео-инфрамаммарной складки к грудной фасции непрерывным швом рассасывающейся атравматичной нитью викрил 3/0. Устанавливают в субпекторальный карман силиконовый имплантат и покрывают нижний полюс установленного силиконового имплантата мембраной, закрывая при этом дно субпекторального кармана. Свободный полукруглый край мембраны сопоставляют с нижним краем большой грудной мышцы и передней зубчатой мышцы и накладывают непрерывный шов рассасывающейся атравматичной нитью викрил 3/0. Устанавливают контрольный дренаж и накладывают асептическую повязку.
Далее приводим клинический пример для подтверждения полученных нами результатов.
Пример 1.
Пациентка Т., 1985 г. рождения. Диагноз заключительный клинический (основной): С50.9 Рак правой молочной железы IIA ст. T2N0M0, Люминальный "A" (HER-2 негативный).
Из анамнеза: Считает себя больной с февраля 2023 г, когда отметила уплотнение в правой молочной железе. Обследована. Выявлен рак правой молочной железы IIA ст. T2N2M0, Люминальный "А" (HER-2негативный).
Локально при поступлении: Молочные железы симметричные. Сосково-альвеолярные комплексы не изменены. Кожный покров молочных желез без патологических изменений. Пальпаторно в верхне-наружном квадранте правой молочной железы пальпируется узловое образование размерами до 6-7 см с четкими ровными контурами, безболезненное, плотно-эластической консистенции, кожа над ним не изменена. Периферические лимфоузлы не пальпируются.
После дополнительного обследования 24.03.2023 выполнено оперативное лечение: Кожносберегающая радикальная мастэктомия по Маддену справа с перевязкой лимфатических сосудов подмышечно-подключично-подлопаточной области с использованием микрохирургической техники и одномоментной маммопластикой имплантатом и композитным материалом из политетрафторэтилена (ПТФЭ).
По предварительной разметке (фиг. 2), произведен разрез в правой аксиллярной области. Посредством гамма-датчика выделена и удалена клетчатка со сторожевыми лимфоузлами, предварительно маркированными радиофармпрепаратом. Узлы направлены на срочное гистологическое исследование. По инфрамаммарной складке правой молочной железы произведен разрез до 7 см. Выполнена подкожная мастэктомия справа. Ретроареолярная клетчатка направлена на срочное гистологическое исследование.
Выделен нижний край большой грудной мышцы и передняя зубчатая мышца - сформирован субпекторальный карман, в который установлен имплантат объемом 285 СС (фиг. 3).
Из ПТФЭ (фиг. 1) выкроен полукруг, основание которого соответствует длине нео-инфрамаммарной складки, а высота - длине половины окружности силиконового имплантата. Основание мембраны подшивают в проекции нео-инфрамаммарной складки к грудной фасции непрерывным швом рассасывающейся атравматичной нитью викрил 3/0.
В субпекторальный карман установлен силиконовый имплантат, нижний полюс которого покрывают мембраной, закрывая при этом дно субпекторального кармана (фиг. 4). Свободный полукруглый край мембраны сопоставили с нижним краем большой грудной мышцы и передней зубчатой мышцы. Накладывают непрерывный шов рассасывающейся атравматичной нитью викрил 3/0 (фиг. 5).
По результатам срочного гистологического исследования выявлено метастатическое поражение одного сторожевого лимфоузла. Выполнена аксиллярная лимфодиссекция. Дренирование правой подмышечной области, полости импланта. Ушивание раны правой молочной железы, правой подмышечной области.
Хороший эстетический результат подтвержден наблюдением пациента в раннем послеоперационном периоде (фиг. 6) и в течение 6 месяцев после выполнения операции (фиг. 7) и обусловлен отсутствием деформации инфрамаммарной складки и красивой естественной формы молочной железы в целом.
Преимущества описанного способа:
- позволяет стабильно укрепить ИМС;
- снижает риск смещения ИМС;
- обеспечивает отток жидкости из кармана имплантата и прорастание собственными тканями, благодаря перфорациям мембраны;
- снижает болевой синдром в послеоперационном периоде за счет снижения хирургической агрессии и онкопластических маммологических операциях;
- снижает экономическую составляющую за счет низкой цены политетрафторэтиленовой мембраны, производимой на территории РФ.
Пример 2.
Пациентка М., 1975 г. рождения. Диагноз заключительный клинический (основной): С50.9 Рак правой молочной железы IIIA ст. T2N2M0, Люминальный "В", HER-2 негативный. Состояние после 8 курсов неоадъювантной ПХТ. Узловая мастопатия слева.
Из анамнеза: считает себя больной с февраля 2022 г, когда отметила боли в правой молочной железе. В марте отметила тянущие боли в правой подмышечной области. В апреле 2022 г. маммография - опухоль правой молочной железы. Обследована. Выявлен рак правой молочной железы III А ст. T2N2M0, Люминальный "В", HER-2 негативный. С мая по сентябрь 2022 г. проведено 8 курсов неоадъювантной полихимиотерапии. Получает гормонотерапию (согласно выписке из истории болезни).
Локально при поступлении: Молочные железы симметричные. Сосково-альвеолярные комплексы не изменены. Кожный покров молочных желез без патологических изменений. Пальпаторно узловые образования в железах не определяются. Периферические лимфоузлы не пальпируются.
После дополнительного обследования 20.10.2022 выполнено оперативное лечение: Двусторонняя подкожная мастэктомия. Биопсия сторожевого лимфоузла справа. Правосторонняя аксиллярная лимфодиссекция. Одномоментная маммопластика имплантатами и ПТФЭ.
Пример 3.
Пациентка И., 1974 г. рождения. Диагноз заключительный клинический (основной): С50.8 Рак левой молочной железы IA ст. cT1(m)N0M0, Люминальный "A" (HER-2 негативный).
Из анамнеза: в течении длительного времени наблюдалась по поводу фиброзно-кистозной мастопатии. В декабре 2021 г. на УЗИ было выявлено новообразование в левой молочной железе. По результатам трепан-биопсии верифицирован рак левой молочной железы IA ст. cT1(m)N0M0, Люминальный "A" (HER-2 негативный).
Локально при поступлении: Молочные железы симметричные. Сосково-альвеолярные комплексы не изменены. Кожный покров молочных желез без патологических изменений. Пальпаторнов левой молочной железе на границе верхних квадрантов пальпируются 4 плотных новообразования диаметром до 2 см с нечетким контуром ограничено подвижные относительно окружающих тканей. Периферические лимфоузлы не пальпируются.
После дополнительного обследования 11.01.2022 выполнено оперативное лечение: Подкожная мастэктомия слева. Биопсия сторожевого лимфоузла справа. Одномоментная маммопластика имплантатами и ПТФЭ.
| название | год | авторы | номер документа |
|---|---|---|---|
| Применение аллоимплантата на основе широкой фасции бедра человека при одномоментных реконструкциях с использованием силиконового эндопротеза у больных раком молочной железы | 2023 |
|
RU2809428C1 |
| СПОСОБ ОДНОМОМЕНТНОЙ РЕКОНСТРУКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ ПРИ РАКЕ С ИСПОЛЬЗОВАНИЕМ АЦЕЛЛЮЛЯРНОГО ДЕРМАЛЬНОГО МАТРИКСА И СИЛИКОНОВОГО ЭНДОПРОТЕЗА | 2015 |
|
RU2584133C2 |
| СПОСОБ ОДНОМОМЕНТНОЙ РЕКОНСТРУКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ ПРИ РАКЕ С ИСПОЛЬЗОВАНИЕМ АЛЛОИМПЛАНТАТА НА ОСНОВЕ ТВЕРДОЙ МОЗГОВОЙ ОБОЛОЧКИ И СИЛИКОНОВОГО ЭНДОПРОТЕЗА | 2019 |
|
RU2705265C2 |
| Способ реконструктивно-пластической хирургии у больных раком молочной железы с использованием ксеноперикарда БиоЛАБ-ПП/ПА и силиконового эндопротеза | 2020 |
|
RU2743199C2 |
| Способ стабилизации имплантата при реконструктивно-пластической хирургии у больных раком молочной железы | 2023 |
|
RU2811656C1 |
| Способ выполнения укрытия эндопротеза при реконструкции молочной железы | 2024 |
|
RU2826772C1 |
| Способ препекторальной реконструкции имплантатом с текстурированным покрытием при малом и среднем размерах молочных желез, "pinch test" более 1 см, птозе II-III степени | 2020 |
|
RU2756184C2 |
| Способ пластики молочной железы | 2020 |
|
RU2749478C1 |
| Способ отсроченной препекторальной реконструкции после мастэктомии при раке молочной железы с помощью перманентного имплантата | 2024 |
|
RU2831000C1 |
| СПОСОБ РЕКОНСТРУКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПОДКОЖНОЙ МАСТЭКТОМИИ | 2021 |
|
RU2779493C1 |
Изобретение относится к медицине, а именно к онкологии и реконструктивно-пластической хирургии. После проведения подкожной радикальной мастэктомии выделяют нижний край большой грудной мышцы и переднюю зубчатую мышцу, формируя таким образом субпекторальный карман. Из перфорированной пористой мембраны (ПТФЭ) выкраивают полукруг, при этом его основание соответствует длине нео-инфрамаммарной складки, а высота соответствует длине половины окружности силиконового имплантата. Основание мембраны подшивают в проекции нео-инфрамаммарной складки к грудной фасции непрерывным швом рассасывающейся атравматичной нитью викрил 3/0. Устанавливают в субпекторальный карман силиконовый имплантат и покрывают нижний полюс установленного силиконового имплантата мембраной, закрывая при этом дно субпекторального кармана. Свободный полукруглый край мембраны сопоставляют с нижним краем большой грудной мышцы и передней зубчатой мышцы и накладывают непрерывный шов рассасывающейся атравматичной нитью викрил 3/0. Способ обеспечивает сохранение и укрепление ИМС в процессе хирургического лечения рака молочной железы у данной категории пациенток и, соответственно, получение, в последующем, длительно сохраняющегося удовлетворительного косметического эффекта при одновременном значительном снижении риска осложнений, за счет исключения возможности развития хирургической агрессии по отношению к тканям, окружающим молочную железу вследствие использования биоинертного материала ПТФЭ, которым отграничивают силиконовый имплантат. 7 ил., 3 пр.
Способ реконструкции инфрамаммарной складки после подкожной радикальной мастэктомии у больных раком молочной железы - РМЖ 0-III стадий с использованием силиконового имплантата, отличающийся тем, что после проведения подкожной радикальной мастэктомии выделяют нижний край большой грудной мышцы и переднюю зубчатую мышцу, формируя таким образом субпекторальный карман, из перфорированной пористой мембраны - ПТФЭ выкраивают полукруг, при этом его основание соответствует длине нео-инфрамаммарной складки, а высота соответствует длине половины окружности силиконового имплантата, затем основание мембраны подшивают в проекции нео-инфрамаммарной складки к грудной фасции непрерывным швом рассасывающейся атравматичной нитью викрил 3/0, устанавливают в субпекторальный карман силиконовый имплантат и покрывают нижний полюс установленного силиконового имплантата мембраной, закрывая при этом дно субпекторального кармана, свободный полукруглый край мембраны сопоставляют с нижним краем большой грудной мышцы и передней зубчатой мышцы и накладывают непрерывный шов рассасывающейся атравматичной нитью викрил 3/0.
| SPEAR S.L | |||
| et al | |||
| Applications of acellular dermal matrix in revision breast reconstruction surgery | |||
| PlastReconstr Surg | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Vol | |||
| Топочная решетка для многозольного топлива | 1923 |
|
SU133A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ФОРМИРОВАНИЯ ИНФРАМАММАРНОЙ СКЛАДКИ ПРИ ДВУХЭТАПНОЙ РЕКОНСТРУКЦИИ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2567790C1 |
| Применение аллоимплантата на основе широкой фасции бедра человека при одномоментных реконструкциях с использованием силиконового эндопротеза у больных раком молочной железы | 2023 |
|
RU2809428C1 |
| СЕРГЕЕВ И.В., ФАЙЗУЛЛИН Т.Р., ЛАРИОНОВ Д.П | |||
| Методы реконструкции инфрамаммарной складки после маммопластики | |||
| Пластическая хирургия и | |||
Авторы
Даты
2024-09-09—Публикация
2023-12-08—Подача