Изобретение относится к области медицины, кардиологии.
Сахарный диабет (СД) и артериальная гипертензия (АГ) являются одними из наиболее распространенных хронических неинфекционных заболеваний и представляет собой серьезную проблему здравоохранения, так как их сочетание ассоциировано с двукратным увеличением риска сердечнососудистой смертности [Buse JB и соавт.2007]. В большинстве случаев смерть наступает от ишемических событий [Yusuf S и соавт, 2004].
АГ в два раза чаще встречается у больных СД по сравнению с теми, у кого диабета нет. Более того, у пациентов с АГ чаще выявляется резистентность к инсулину и они подвержены большему риску развития диабета, чем люди с нормальным артериальным давлением (АД).
Несмотря на большие успехи в профилактике, лечении и реабилитации пациентов с АГ, в клинической практике часто встречается резистентная АГ, при которой имеет место недостижение целевых значений АД при назначении комбинированной антигипертензивной терапии, включающей три препарата, один из которых диуретик. К более агрессивному и неконтролируемому течению АГ приводит сочетание у пациента АГ и СД.
Соответственно, диабет и гипертония тесно взаимосвязаны и имеют схожие анатомо-морфологические изменения, такие как эндотелиальная дисфункция, хроническое воспаление, ремоделирование артерий, атеросклероз, дислипидемия и ожирение. Гипергликемия, резистентность к инсулину и повышенное содержание конечных продуктов гликирования способствуют увеличению риска заболевания коронарных и периферических артерий при СД в 2-4 раза [Fishman SL и соавт, 2018; Shu J и совт, 2018]. В литературе имеются данные о том, что эти факторы отрицательно воздействуют на эндотелий сосудов и имеют тесную связь с макрососудистыми заболеваниями, включая диффузный атеросклероз [Aronson D и соавт, 2002]. В частности, наиболее частыми кардиальными осложнениями течения СД являются стеноз/тромбоз коронарных сосудов, реокклюзия шунтов и рестеноз в стенте. Уже доказано, что у больных СД наблюдается ускоренная поздняя потеря просвета сосуда, и риск внутристентового рестеноза гораздо выше [Paramasivam G и соавт, 2020]. Фактически СД является независимым предиктором рецидива рестеноза [Zhao L и соавт, 2017], что делает больных диабетом особенно сложной популяцией для лечения. Учитывая тот факт, что с каждым годом во всем мире растет количество чрескожных коронарных вмешательств (ЧКВ) и имплантируемых стентов, медицинскому сообществу неизбежно придется искать новые возможности для уменьшения количества повторных интервенций у данной когорты пациентов.
В основе тесной взаимосвязи АГ и СД лежит единство патогенетических звеньев, в частности инсулинорезистентности и гиперсимпатикотонии. Одним из патогенетических вариантов лечения этих заболеваний является недавно разработанная эндоваскулярная технология ренальной денервации (РДН) методом радиочастотной аблации. Ее эффективность обусловлена селективным деструктивным эффектом на симпатические нервные сплетения, расположенные в адвентициальном и периваскулярном пространстве почечных артерий. Именно в этой зоне выявлена высокая концентрация симпатических ганглиев, содержащих афферентные и эфферентные нервные волокна, вовлеченные в регуляцию артериального давления, углеводного обмена и экскреторную функцию почек посредством активации симпатической нервной системы и ренин-ангиотензин-альдостероновой системы [Miiller J и соавт, 1972]. В этой связи РДН имеет плейотропный эффект в виде снижения инсулинорезистентности, релаксации сосудистой стенки, выведению избытка воды и натрия из организма и замедления прогрессирования хронической почечной недостаточности [Mahfoud F и соавт, 2011; Chen W и соавт, 2016, Hering D; Kiuchi MG и соавт, 2016]. Появление гемодинамически значимых стенозов в коронарных артериях является осложнением течения СД, которое напрямую коррелирует с уровнем гликемии и степенью инсулинорезистентности. Достигнув с помощью РДН значимого снижения уровня артериального давления, уровня гликемии и степени инсулинорезистентности, возможно замедлить прогрессирование коронарного атеросклероза, улучшить результаты эндоваскулярного лечения ишемической болезни сердца (ИБС) и снизить частоту развития неблагоприятных сердечно-сосудистых событий.
На основании представленных результатов крупных международных многоцентровых рандомизированных исследований [SPYRAL HTN-OFF MED, SPYRAL HTN-ON MED] было доказана эффективность РДН в снижении уровня как среднесуточного, так и офисного АД у пациентов с неконтролируемой артериальной гипертонией [Townsend R и соавт, 2017; Kandzari D и соавт, 2018]. Эффект РДН носил стойкий характер, так даже через 36 снижение офисного систолического артериального давления составило -18,7 мм рт.ст. для группы почечной денервации и -8,6 мм рт.ст. для группы контроля (р<0,01). По данным суточного мониторирования артериального давления (СМАД): разница между группой денервации почечных артерий и контрольной группой среднего амбулаторного диастолического артериального давления составила -5,9 мм рт. ст. (95% ДИ от -10,1 до -1,8; р=0,0055), утреннего систолического артериального давления -11,0 мм рт.ст. (от -19,8 до -2,1; р=0,016) и ночного систолического артериального давления -11,8 мм рт.ст. (от -19,0 до -4,7; р=0,0017) [Mahfoud F и соавт, 2022].
В иностранных и отечественных исследованиях имеются сведения о положительном влиянии РДН на уровень гликемии. Согласно результатам исследований отмечается достоверно значимое снижение уровня гликемии натощак, уровня гликированного гемоглобина и степени инсулинорезистентности (индекс HOMA-IR) [Mahfoud F и соавт, 2011; Фальковская А.Ю и соавт, 2021; Zhang Z и соавт, 2021].
В последнее время в научной литературе все чаще стали появляться сведения о возможности проведения катетерной денервации чревного ствола в качестве метода лечения СД [Pan Т и соавт, 2021]. В отличии от РДН, при которой деструктивное воздействие оказывается на почечных афферентных и эфферентных нервы, денервация чревного ствола и верхней брыжеечной артерии нацелена на постганглионарные нервы, которые берут начало от чревного и верхних брыжеечных ганглиев, и это может стать основанием большей эффективности данного подхода в лечении СД и заболеваний, в патогенезе которых весомое значение имеет гиперсимпатикотония.
Экспериментальные данные показывают, что хирургическая или химическая симпатическая денервация общей печеночной артерии улучшает толерантность к глюкозе и усиливает постпрандиальный клиренс глюкозы у собак, а также уменьшает проявления стеатоза печени у мышей [Hurr С и соавт, 2019; Kraft G и соавт, 2021]. Катетерная денервация почечных и общей печеночной артерии ранее изучалась в экспериментальных условиях у свиней в качестве перспективного метода лечения СД [Kiuchi MG и соавт, 2021].
В тоже время опираясь на анатомические сведения, симпатические нервная система участвует в иннервации поджелудочной железы и печени посредством постсинаптических висцеральных нервов, которые берут начало от превертебральных чревных и верхних брыжеечных ганглиев, и контролирует секрецию гормонов, выработку глюкозы и ее метаболизм [McCuskey RS и соавт, 2004; Lin ЕЕ и соавт, 2021]. Принимая во внимания эти данные, комбинированная катетерная денервация чревного ствола и верхней брыжеечной артерии представляет собой перспективное научное и клиническое направление в лечении СД.
Универсальность патогенетического механизма (гиперактивация симпатической нервной системы) в развитии и прогрессировании сердечнососудистых заболевании, а также заболеваний обмена вещества (метаболический синдром, СД), обосновывает возможность использования методов, позволяющих снизить влияние это механизма и улучшить результаты лечения. Одним из таких методов является катетерная денервация почечных артерий, чревного ствола и верхней брыжеечной артерии. Синергизм двух методов эндоваскулярного лечения (ЧКВ и денервация висцеральных ветвей аорты) является научно обоснованным и рассматривается в качестве перспективного комплексного подхода в лечении коморбидных пациентов с достижение положительных плейотропных эффектов (снижении АД, уровня гликемии и инсулинорезистентности, снижение частоты рестенозирования и формирования стенозов de novo).
Техническая задача, на которую направлено заявляемое изобретение, заключается в улучшении результатов эндоваскулярного лечения ИБС у пациентов с СД 2 типа и АГ и снижении частоты развития неблагоприятных сердечно-сосудистых событий (ССС).
Технический результат достигается за счет того, что в способе комплексного эндоваскулярного лечения пациентов с доказанной ишемией миокарда, артериальной гипертензией и сахарным диабетом осуществляется полная функциональная реваскуляризация миокарда методом ЧКВ, при которой лечению подвергаются коронарные артерии диаметром более 2 мм и стенозом более 50% и для которой используют стенты, выделяющие лекарственный препарат 2 и 3 поколения, после ЧКВ проводят ангиографию правой и левой почечных артерий, чревного ствола и верхней брыжеечной артерии, затем приступают к выполнению катетерной денервации методом многополюсной радиочастотной аблации, под внутривенной седацией и через бедренный доступ, и при котором через установленный в общую бедренную артерию интродьюсер 6F с помощью проводникового катетера поочередно к устью чревного ствола, верхней брыжеечной, правой и левой почечных артерий доставляется катетер Symplicity Spyral™ (Medtronic, США), затем с его помощью осуществляется многофокусное аблационное воздействие проксимальных отделов чревного ствола и брыжеечной артерии (1 аппликация с эффективной работой всех четырех электродов катетера), всего основного ствола почечных артерий, а также всех дочерних ветвей почечных артерий с диаметром более 3 мм, после этого проводят финальную (окончательную) ангиографию.
В частном случае, если объем введенного во время ЧКВ рентгенконтрастного вещества (РКВ) не достиг предельно допустимого безопасного значения (расчет по формуле объем введенного РКВ/скорость клубочковой фильтрации (по формуле CKD-EPI) <3,7), проводится одномоментная катетерная денервация чревного ствола, верхней брыжеечной и почечных артерий.
В частном случае, если объем введенного во время ЧКВ РКВ достиг предельно допустимого безопасного значения или его превысил (объем введенного РКВ/скорость клубочковой фильтрации (по формуле CKD-EPI) >3,7), второй этап в виде катетерной денервации проводится не менее чем через 3 дня после 1 этапа (ЧКВ) и после исключения развития контраст-индуцированной нефропатии.
В частном случае если ЧКВ проводилось лучевым доступом или проведение катетерной денервации отсрочено по времени, то для его осуществления обеспечивается дополнительный бедренный доступ путем пункции общей бедренной артерии по методике Сельдингера и установки интродьюсера 6F.
В частном случае, если же ЧКВ проводилось через бедренный доступ, то проводят одномоментное проведение катетерной денервации чревного ствола, верхней брыжеечной и почечных артерий, и используют тот же доступ, что и доступ при ЧКВ. Изобретение поясняется следующими фигурами:
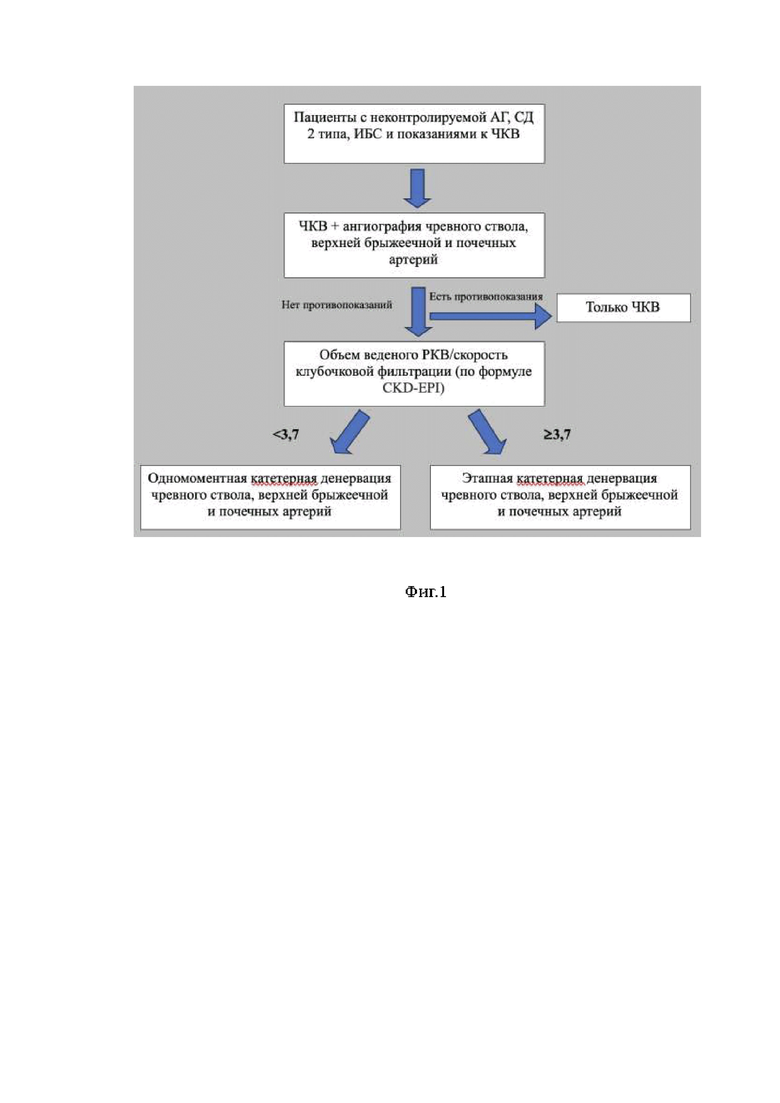
Фиг. 1 - схема выполнения хирургического лечения;
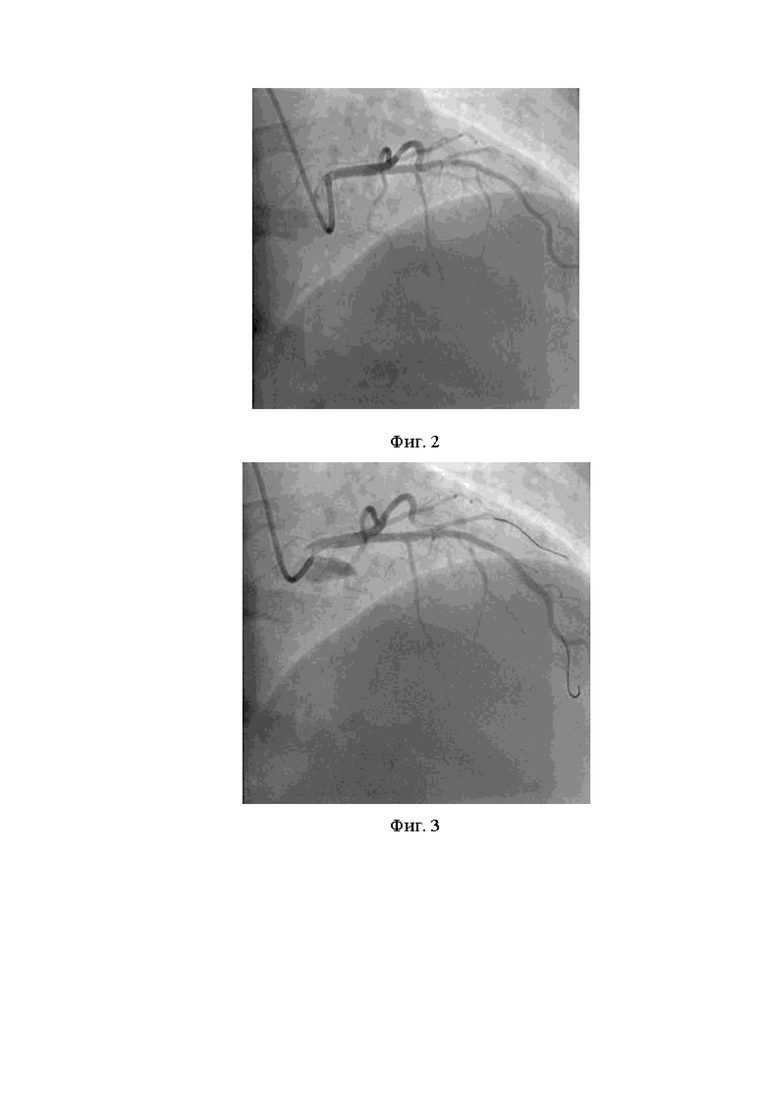
Фиг. 2 - 60% стеноз среднего сегмента передней нисходящей артерии
Фиг. 3 - результат стентирования передней нисходящей артерии
Фиг. 4 - катетерная денервация легочного ствола
Фиг. 5 - катетерная денервация верхней брыжеечной артерии
Фиг. 6 - катетерная денервация левой почечной артерии
Фиг. 7 - катетерная денервация правой почечной артерии
Фиг. 8 - контрольный результат стентирования передней нисходящей артерии через 12 месяцев наблюдения
Фиг. 9 - измерение остаточного просвета в ранее имплантированном стенте в передней нисходящей артерии
Способ осуществляется в два этапа следующим образом. Первым этапом проводится ЧКВ у пациентов с доказанной по результатам инструментальных методов диагностики (стресс-эхокардиография/сцинтиграфия миокарда с нагрузкой) ишемией миокарда. Ангиопластике и стентированию подвергаются коронарные артерии диаметром более 2 мм и стенозом более 50%. Используются стенты, выделяющие лекарственный препарат, 2 и 3 поколения.
После завершения этого этапа выполняется ангиография правой и левой почечных артерий, чревного ствола и верхней брыжеечной артерии для оценки их анатомии (наличие аномалий развития и/или атеросклеротических поражений артерий (стеноз >50%), стентированные артерии, отсутствие плотного контакта электродов катетера с сосудистой стенкой при большом диаметре последней - противопоказание) и технической возможности (невозможность выполнения в случае выраженного периферического атеросклероза подвздошно-бедренного сегмента с обеих сторон) проведения катетерной денервации методом многополюсной радиочастотной аблации.
В случае, если объем введенного во время ЧКВ рентгенконтрастного вещества (РКВ) не достиг предельно допустимого безопасного значения <3,7, который рассчитывают по формуле как отношение объема введенного РКВ к скорости клубочковой фильтрации (по формуле CKD-EPI), проводится одномоментная катетерная денервация (фиг. 1).
В случае если на момент окончания первого этапа ЧКВ объем введенного РКВ превысил предельно допустимое безопасное значение (>3,7), второй этап в виде катетерной денервации проводится не менее чем через 3 дня после первого этапа и после исключения развития контраст-индуцированной нефропатии (фиг. 1).
Операция катетерной денервации методом многополюсной радиочастотной аблации выполняется под внутривенной седацией и через бедренный доступ. Если ЧКВ проводилось лучевым доступом или второй этап комплексного лечения отсрочен по времени, то для осуществления катетерной денервации необходимо обеспечить бедренный доступ. Если же ЧКВ проводилось через бедренный доступ и возможно одномоментное проведение второго этапа, то этот же доступ используется для катетерной денервации. через установленный в общую бедренную артерию интродьюсер 6F с помощью проводникового катетера поочередно к устью правой и левой почечных артерий доставляется катетер Symplicity Spyral™ [Medtronic, USA]. Далее с его помощью осуществляется многофокусное аблационное воздействие проксимального отдела чревного ствола и верхней брыжеечной артерии (1 аппликация с эффективной работой всех четырех электродов катетера), основного ствола правой и левой почечных артерий, а также всех дочерних ветвей с диаметром более 3 мм.
Для улучшения контакта электродов катетера со стенкой чревного ствола и верхней брыжеечной артерии ручку катетера можно повернуть на 90° против часовой стрелки.
В обязательном порядке проводится финальная ангиография артерий для исключения развития интраоперационных осложнений.
Новизной изобретения является применение комплексного эндоваскулярного лечения пациентов с СД 2 типа, неконтролируемой АГ и ИБС, нуждающихся в ЧКВ, который заключается в сочетании полной функциональной эндоваскулярной реваскуляризации коронарных артерий и катетерной денервации чревного ствола, верхней брыжеечной артерии и почечных артерий методом радиочастотной аблации многополюсным электродом. Изобретение имеет изобретательский уровень, так как в доступных источниках информации России и за рубежом указаний на подобный способ улучшения результатов лечения коморбидных пациентов не обнаружено. Имеются сведения об изолированного применении РДН у пациентов с резистентной и неконтролируемой АГ, а также катетерной денервации чревного ствола у пациентов с онкологическими заболеваниями и СД 2 типа.
Изобретение является промышленно применимым, так как может быть многократно воспроизведено и применено в здравоохранении, в лечебных учреждениях специализированного профиля.
Для доказательства приводим выписки из историй болезни, подтверждающие клинический эффект лечения предлагаемым способом.
Пример клинического применения способа №1
Пациентка Б., 50 лет с жалобами на дискомфорт в грудной клетке при умеренной физической нагрузке поступила в кардиологический стационар. Из анамнеза известно, что длительное время страдает артериальная гипертония с максимальным повышение цифр артериального давления (АД) до 230/110 мм рт.ст., рабочее АД 120/70 мм рт.ст. На регулярной основе принимает гипотензивные препараты различных классов с сохранением нестабильности цифр АД. В настоящий момент постоянно принимает комбинированную терапию, включающую блокатор рецепторов ангиотензина, селективный блокатор «медленных» кальциевых каналов, бета-адреноблокатор и диуретик.
Нарушение мозгового кровообращения в анамнезе отрицает. Впервые СД 2 типа был диагностирован 7 лет назад, в течение последнего года на инсулинотерапии пролонгированным инсулином 34 ЕД 1 раз в сутки, инсулином короткого действия 8ЕД 3 раза в сутки. Дополнительно пациентка получает терапию селективным обратимым ингибитором натрий-глюкозного котранспортера 2-го типа.
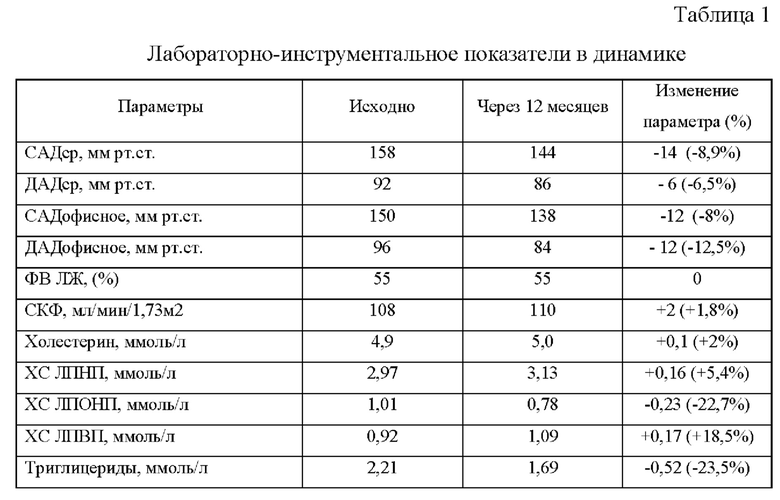
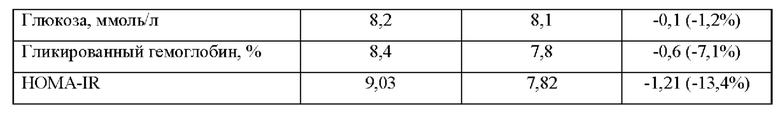
При обследовании офисное АД составило 150/96 мм рт.ст, по результатам СМАД среднее АД 158/92 мм рт.ст. Исходные результаты лабораторно-инструментальной диагностики представлены в таблице 1.
Учитывая клинику стенокардии напряжения с целью верификации ишемии проведена стресс-эхокардиография, по результатам которой проба с физической расценена как положительная. На пике нагрузке отмечалось появление зон гипокинеза в области апикального передне-перегородочного сегмента левого желудочка.
Проведена коронарография. При контрольной ангиографии выявлен 60% стеноз среднего сегмента передней нисходящей артерии (фиг. 2). Принято решение о стентировании передней нисходящей артерии ad hoc. Был имплантирован стент, выделяющий лекарственный препарат, 2 поколения. Как результат, просвет артерии восстановлен, признаков диссекции не обнаружено (фиг. 3). Проведена ангиография чревного ствола, верхней брыжеечной, правой и левой почечных артерий, противопоказаний к проведению катетерной денервации не выявлено.
Учитывая небольшой объем введенного рентгенконтрастного вещества (90 мл), допустимую безопасную дозу рентгеновского излучения (11,4 мЗв) и сохранную азотвыделительную функцию почек, принято решение о проведении одномоментной ренальной денервации через правый бедренный доступ. Общее количество эффективных аблационных воздействий составило 64: в чревном стволе - 8, в верхней брыжеечной артерии - 8, в дочерних ветвях почечных артерий - 25, в основном стволе почечных артерий- 21 (фиг. 6, фиг. 7). После завершения катетерной денервации пациента была переведена для наблюдения в блок интенсивной терапии и через 2 суток выписана из стационара. При выписке отметила отсутствие привычных приступов стенокардии напряжения при нагрузках.
В течение всего периода наблюдения (12 месяцев) рецидива стенокардии напряжения не отмечалось, развития острого нарушения мозгового кровообращения и инфаркт миокарда не зафиксировано, пациентка отметила стабилизацию цифр АД. Учитывая тенденцию к гипотонии, пациентке была снижена доза антигипертензивных препаратов. На контрольном обследовании отмечена положительная динамика лабораторных показателей уровня гликемии и липидов крови, которая представлена в таблице. При осмотре офисное АД составило 138/84 мм рт.ст. Проведена катетеризация лучевой артерии, установлен интродьюсер 6F в лучевую артерию. Проведена коронарография, по результатам которой ранее имплантированный стент без признаков тромбоза и рестеноза, в других коронарных артериях новых стенозов не обнаружено (фиг. 8). Оценка степени стенозирования проводилась с использованием количественного ангиографического анализа коронарных артерий (QCA) (фиг. 9).
Пример клинического применения способа №2
Пациентка Т., 69 лет с жалобами на одышку смешанного характера (эквивалентную подъему выше 3 этажа, ускорение темпа ходьбы), проходящую в покое поступила в кардиологический стационар. Из анамнеза известно, что длительное время страдает артериальная гипертония с максимальным повышение цифр АД до 230/120 мм рт.ст., рабочее АД 120/70 мм рт.ст. На регулярной основе принимает гипотензивные препараты различных классов с сохранением нестабильности цифр АД. В настоящий момент постоянно принимает комбинированную терапию, включающую блокатор рецепторов ангиотензина, селективный блокатор «медленных» кальциевых каналов, бета-адреноблокатор и диуретик.
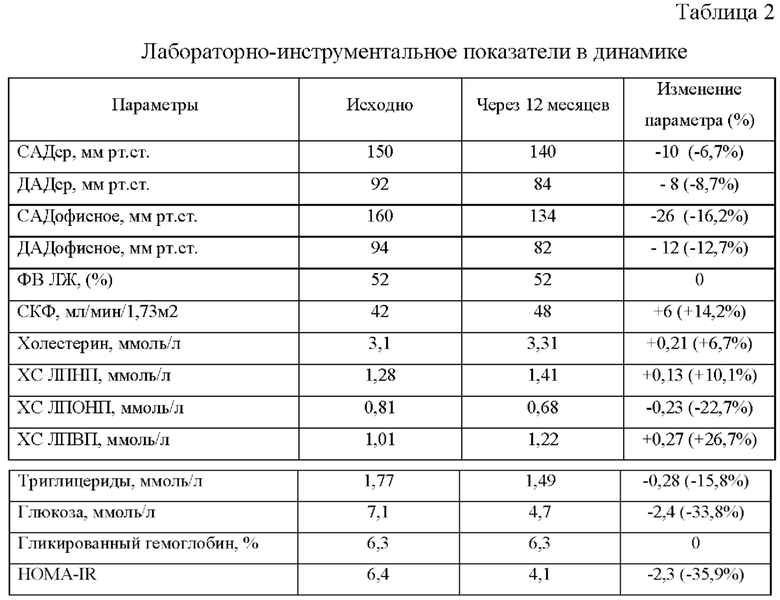
При обследовании офисное АД составило 160/94 мм рт.ст, по результатам СМАД среднее АД 150/92 мм рт.ст. Исходные результаты лабораторно-инструментальной диагностики представлены в таблице 2.
Нарушение мозгового кровообращения в анамнезе отрицает. Впервые СД 2 типа был диагностирован 10 лет назад, находится на терапии Метформином 850 мг.
Пациентка имеет отягощенный коронарный анамнез: в 2011 году перенесла острый инфаркт миокарда задней стенки левого желудочка. В 2012 году проведена коронарография, выявлено многососудистое поражение: стеноз передней нисходящей артерии 75%, ветви тупого края 10%, правой коронарной артерии 90%. Учитывая анатомо-морфологические характеристики поражения, пациентке была выполнена операция маммарокоронарного шунтирования передней нисходящей артерии, аортокоронарное шунтирование задней нисходящей артерии, правой коронарной артерии, ветви тупого края и диагональной ветви в условиях искусственного кровообращения и гипотермии.
Чувствовала себя удовлетворительно, однако спустя 7 лет в связи с возобновлением приступов стенокардии проведена коронарошунтография, выявили стеноз огибающей артерии 80%, ветви тупого края 80%), шунт к ветви тупого края окклюзирован. По результатам выполнено ЧКВ огибающей артерии с переходом в ветвь тупого края двумя стентами с лекарственным покрытием.
Через 2 года пациентка вновь отметила снижения толерантности к физической нагрузке, появление жалоб на колющие, простреливающие боли в груди, вне связи с физической нагрузкой, слабость, головокружение, общий дискомфорт, усиливающиеся при повышении АД до 190/100 мм рт ст. Проведена нагрузочная проба на выявление скрытой ишемии, проба положительная. По результатам коронарошунтографии через правый бедренный доступ выявлен стеноз аортокоронарного шунта к диагональной ветви. Принято решение о стентировании аортокоронарного шунта к диагональной ветви ad hoc. Был имплантирован стент, выделяющий лекарственный препарат, 3 поколения. Как результат, просвет артерии восстановлен, признаков диссекции не обнаружено. Проведена ангиография чревного ствола, верхней брыжеечной артерии, правой и левой почечной артерий, противопоказаний к проведению катетерной денервации не выявлено.
Учитывая достижение предельно допустимого безопасного объема введенного рентгенконтрастного вещества (160 мл) и компрометированную азотвыделительную функцию почек (наличие хронической болезни почек 3Б - СКФ=42 мл/мин/1,73 м2), что согласно предложенному алгоритму составляет более 3,7. Было принято решение о проведении этапной катетерной денервации. Через 3 суток через правый бедренный доступ было выполнена успешная операция катетерной денервации чревного ствола (фиг. 4), верхней брыжеечной (фиг. 5), правой и левой почечных артерий. Общее количество эффективных аблационных воздействий составило 54: в чревном стволе - 6, в верхней брыжеечной артерии - 8, в дочерних ветвях почечных артерий - 22, в основном стволе почечных артерий- 18. После завершения катетерной денервации пациента была переведена для наблюдения в блок интенсивной терапии и через 2 суток выписана из стационара. При выписке отметила отсутствие привычных приступов стенокардии напряжения при нагрузках.
В течение всего периода наблюдения (12 месяцев) рецидива стенокардии напряжения не отмечалось, развития острого нарушения мозгового кровообращения и инфаркт миокарда не зафиксировано, пациентка отметила стабилизацию цифр АД. Сохранялась прежняя терапия. На контрольном обследовании отмечена положительная динамика лабораторных показателей уровня гликемии и некоторых фракций липидов крови, которая представлена в таблице. При осмотре офисное АД составило 134/88 мм рт.ст. Проведена коронарошунтография, по результатам которой ранее имплантированный стент в аортокоронарный шунт к диагональной ветви без признаков тромбоза и рестеноза, в других коронарных артериях новых стенозов не обнаружено.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения тромбоза и стеноза артериального анастомоза после трансплантации печени | 2020 |
|
RU2736905C1 |
| Способ выполнения внутрисосудистой оптической когерентной томографии почечных артерий | 2022 |
|
RU2805645C1 |
| СПОСОБ ГЕМОДИНАМИЧЕСКОЙ ПОДДЕРЖКИ И ЗАЩИТЫ МИОКАРДА ПРИ ЭНДОВАСКУЛЯРНОЙ КОРОНАРНОЙ РЕВАСКУЛЯРИЗАЦИИ У ПАЦИЕНТОВ ВЫСОКОГО РИСКА | 2012 |
|
RU2479250C1 |
| Способ рентгенэндоваскулярной эмболизации висцеральных ветвей через артерии верхних конечностей при помощи катетера Headhunter при различных патологиях желудочно-кишечного тракта | 2016 |
|
RU2652743C1 |
| МАГНИТОНАВИГАЦИОННАЯ КАТЕТЕРНАЯ СИСТЕМА ДЛЯ СОЗДАНИЯ ЭНДОВАСКУЛЯРНЫХ МЕЖСОСУДИСТЫХ АНАСТОМОЗОВ | 2018 |
|
RU2662414C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЗИСТЕНТНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ | 2012 |
|
RU2487686C1 |
| СПОСОБ КОНТРАСТИРОВАНИЯ КОРОНАРНЫХ АРТЕРИЙ ВО ВРЕМЯ ПРОВЕДЕНИЯ АНТЕГРАДНОЙ РЕКАНАЛИЗАЦИИ ХРОНИЧЕСКИ ОККЛЮЗИРОВАННЫХ КОРОНАРНЫХ АРТЕРИЙ (ХОКА) | 2015 |
|
RU2599374C1 |
| СПОСОБ ВРЕМЕННОЙ ПОДДЕРЖКИ КРОВОСНАБЖЕНИЯ МИОКАРДА У ПАЦИЕНТОВ С ПОРАЖЕНИЕМ СТВОЛА ЛЕВОЙ КОРОНАРНОЙ АРТЕРИИ | 2014 |
|
RU2552023C1 |
| Способ эндопротезирования дуги аорты с направленной фенестрацией в устье левой подключичной артерии со сложной анатомией | 2024 |
|
RU2835724C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОГО ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОЙ ЗНАЧИМОСТИ СТЕНОЗИРУЮЩИХ ПОРАЖЕНИЙ ПОЧЕЧНЫХ АРТЕРИЙ У ПАЦИЕНТОВ С РЕНОВАСКУЛЯРНОЙ ГИПЕРТЕНЗИЕЙ | 2013 |
|
RU2531131C1 |



Изобретение относится к области медицины, кардиологии. На первом этапе осуществляют реваскуляризация миокарда методом чрескожных коронарных вмешательств, при которой лечению подвергаются коронарные артерии диаметром более 2 мм и стенозом более 50% и для которой используют стенты, выделяющие лекарственный препарат 2 и 3 поколения. На втором этапе осуществляют ангиографию правой и левой почечных артерий, чревного ствола и верхней брыжеечной артерии, затем приступают к выполнению катетерной денервации методом многополюсной радиочастотной абляции, под внутривенной седацией и через бедренный доступ. При этом через установленный в общую бедренную артерию интродьюсер 6F с помощью проводникового катетера поочередно к устью чревного ствола, верхней брыжеечной, правой и левой почечных артерий доставляют катетер Symplicity Spyral, затем с его помощью осуществляют многофокусное абляционное воздействие проксимальных отделов чревного ствола и брыжеечной артерии, всего основного ствола почечных артерий, а также всех дочерних ветвей почечных артерий с диаметром более 3 мм, после этого проводят окончательную ангиографию. Способ позволяет улучшить результаты эндоваскулярного лечения ИБС у пациентов с СД 2 типа и АГ при снижении частоты развития неблагоприятных сердечно-сосудистых событий. 4 з.п. ф-лы, 9 ил., 2 табл., 2 пр.
1. Способ комплексного эндоваскулярного лечения пациентов с сахарным диабетом и сердечно-сосудистой коморбидностью, характеризующийся тем, что осуществляют полную функциональную реваскуляризацию миокарда методом чрескожных коронарных вмешательств (ЧKB) коронарных артерий диаметром более 2 мм и стенозом более 50%, при которой используют стенты, выделяющие лекарственный препарат 2 или 3 поколения, после этого проводят ангиографию правой и левой почечных артерий, чревного ствола и верхней брыжеечной артерии, затем приступают к выполнению катетерной денервации методом многополюсной радиочастотной абляции, для этого под внутривенной седацией и через бедренный доступ, при котором через установленный в общую бедренную артерию интродьюсер 6F с помощью проводникового катетера поочередно к устью чревного ствола, верхней брыжеечной, правой и левой почечных артерий доставляют катетер Symplicity Spyral, затем с его помощью осуществляют многофокусное абляционное воздействие проксимальных отделов чревного ствола и брыжеечной артерии, всего основного ствола почечных артерий, а также всех дочерних ветвей почечных артерий с диаметром более 3 мм, после этого проводят окончательную ангиографию.
2. Способ по п. 1, отличающийся тем, что, при объеме введенного во время ЧKB рентгенконтрастного вещества (РКВ), не достигшего предельно допустимого безопасного значения и рассчитываемого по формуле как отношение объема введенного РКВ к скорости клубочковой фильтрации и определяемого как <3,7, проводится одномоментная катетерная денервация чревного ствола, верхней брыжеечной и почечных артерий.
3. Способ по п. 1, отличающийся тем, что, при объеме введенного во время ЧKB достигшего предельно допустимого безопасного значения и рассчитываемого по формуле как отношение объема введенного РКВ к скорости клубочковой фильтрации и определяемого как >3,7, катетерная денервация проводится не менее чем через 3 дня после ЧKB и после исключения развития контраст-индуцированной нефропатии.
4. Способ по п. 1, отличающийся тем, что, в случае проведения ЧKB или лучевым доступом или проведение катетерной денервации отсрочено по времени, то для осуществления катетерной денервации обеспечивают дополнительный бедренный доступ путем пункции общей бедренной артерии по методике Сельдингера и установки интродьюсера 6F.
5. Способ по п. 1, отличающийся тем, что при проведении ЧKB через бедренный доступ проводят одномоментное проведение катетерной денервации чревного ствола, верхней брыжеечной и почечных артерий, при этом используют тот же доступ, что и доступ при МKB.
| Араблинский Н | |||
| А | |||
| и др | |||
| Отдаленные результаты применения ренальной денервации в лечении коморбидных пациентов с артериальной гипертензией, сахарным диабетом и атеросклерозом коронарных артерий, Кардиоваскулярная терапия и профилактика, 2023, том | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Спускная труба при плотине | 0 |
|
SU77A1 |
| СПОСОБ ОТБОРА ПАЦИЕНТОВ С МЕДИКАМЕНТОЗНО-РЕЗИСТЕНТНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ ДЛЯ ВЫПОЛНЕНИЯ ПРОЦЕДУРЫ СИМПАТИЧЕСКОЙ ДЕНЕРВАЦИИ ПОЧЕЧНЫХ АРТЕРИЙ | 2014 |
|
RU2563449C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЗИСТЕНТНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ | 2012 |
|
RU2487686C1 |
| СПОСОБ ЛЕЧЕНИЯ РЕЗИСТИВНОЙ АРТЕРИАЛЬНОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2016 |
|
RU2694583C1 |
Авторы
Даты
2024-10-01—Публикация
2023-12-13—Подача