Изобретение относится к области медицины, а именно к сердечнососудистой хирургии, и может быть использовано в интервенционной кардиологии для лечения легочной артериальной гипертензии.
Известен способ хирургического лечения легочной гипертензии при помощи межпредсердной септостомии (Диагностика и лечение легочной гипертензии. Клинические рекомендации [Электронный ресурс]. - Электрон. текстовые дан. - Режим доступа к сайту, свободный: http://mzdrav.rk.gov.ru/file/mzdrav_18042014_Klinicheskie_rekomendacii_Legoc hnaja_gipertenzija.pdf). При этом формирование шунта справа-налево позволяет снизить среднее давление в правом предсердии и перегрузку правого желудочка, увеличить преднагрузку левого желудочка и образом сердечного выброса. В результате улучшается транспорт кислорода, уменьшается симпатическая гиперактивация, что приводит к снижению эпизодов синкопе и повышению толерантности к физической нагрузке. Однако, проведение предсердной септостомии рекомендовано только больным с III-IV ФК (ВОЗ) с частыми синкопе и/или рефрактерной правожелудочковой сердечной недостаточностью, а смертность при проведении процедуры составляет 5-15%.
Известна операция хирургической денервации легочных артерий, при которой торакотомическим доступом выделяют легочный ствол и проксимальные сегменты обеих легочных артерий, после чего в области бифуркации легочного ствола и проксимальных сегментов легочных артерий удаляют адвентицию и частично медию при помощи техники микродиссекции (Juratsch CE, Jengo JA, Castagna J, Laks MM. Experimental pulmonary hypertension produced by surgical and chemical denervation of the pulmonary vasculature. Chest. 1980; 77(4): 525-530. doi: 10.1378/chest.77.4.525). Данный способ не нашел применения в клинической практике ввиду его травматичности.
Наиболее близким к заявляемому является способ катетерной денервации легочных артерий у пациентов с идиопатической артериальной легочной гипертензией, устойчивой к медикаментозной терапии (Chen S-L, Zhang F-F, Xu J, Xie D-J, Zhou L, Nguyen T, Stone GW. Pulmonary Artery Denervation to Treat Pulmonary Arterial Hypertension. The Single-Center, Prospective, First-in-Man PADN-1 Study (First-in-Man Pulmonary Artery Denervation for Treatment of Pulmonary Artery Hypertension). JACC 2013; 62(12): 1092-100). Способ основан на транскатетерном нанесении циркулярных радиочастотных повреждений в трех областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии. Для выполнения манипуляций используют аблационный катетер с кольцевым наконечником, по периметру которого на расстоянии 2 мм друг от друга монтированы десять электродов. Перед процедурой радиочастотной аблации (РЧА) выполняют ангиографию для визуализации легочных сосудов и правых отделов сердца, а также определяют место локализации аблационного катетера.
Недостатком способа является то, что аблационные точки располагают линейно в один ряд, что в дальнейшем может приводить к стенозу легочных артерий вследствие склерозирования в зоне аблационных повреждений. Кроме того, ангиографический контроль позиционирования аблационного катетера не позволяет точно определить место перехода миокарда выводного тракта правого желудочка на легочный ствол, которое у разных субъектов вариабельно. Поэтому аблации может ошибочно подвергаться область, анатомически соответствующая легочному стволу, но являющаяся на самом деле миокардом выводного тракта правого желудочка, переходящим на легочный ствол. Это приведет к повреждению миокарда, активно участвующего в сокращении правого желудочка, и к недостаточной глубине воздействия, не позволяющей достигнуть полноценной денервации легочных артерий.
Техническим результатом изобретения является повышение эффективности и безопасности катетерной денервации легочных артерий, за счет построения амплитудной биполярной карты выводного тракта правого желудочка, легочного ствола и обеих легочных артерий, а также изменения дизайна аблационного воздействия, при котором аблационные повреждения наносят зигзагообразно, исключая область проксимальнее места перехода миокарда выводного тракта правого желудочка на легочный ствол.
Предложенный способ катетерной денервации легочных артерий включает построение амплитудной биполярной карты выводного тракта правого желудочка, легочного ствола и обеих легочных артерий (ЛА), после чего осуществляют выполнение радиочастотной аблации в трех циркулярных областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии. При этом, аблационные повреждения наносят в виде замкнутой зигзагообразной прерывистой линии по внутренней окружности сосудов, исключая область проксимальнее места перехода миокарда выводного тракта правого желудочка на легочный ствол.
Предложенный способ позволяет, не уменьшая плотности радиочастотных повреждений, оставлять между ними участки неповрежденной ткани и исключить вероятность развития стеноза легочных артерий на фоне их последующего склерозирования, а также исключить радиочастотное повреждение области, анатомически соответствующей легочному стволу, но являющейся на самом деле миокардом выводного тракта правого желудочка, переходящим в легочный ствол.
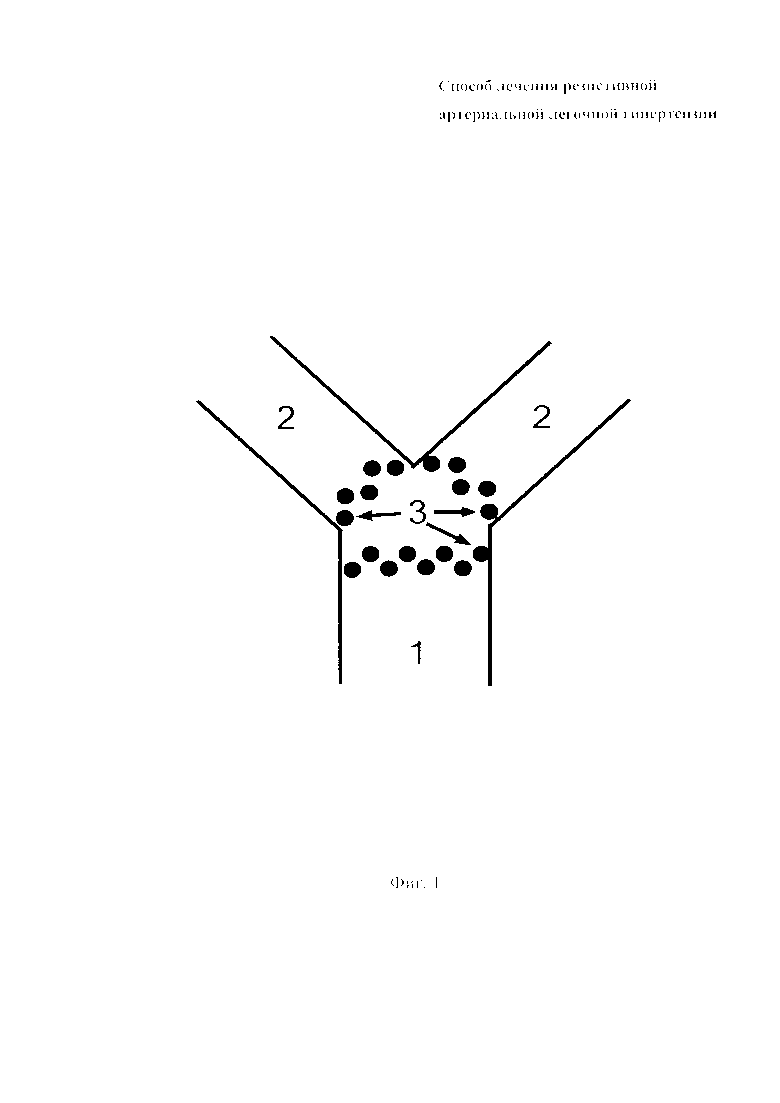
Изобретение поясняется чертежами, где на фиг. 1 показан дизайн катетерной денервации легочных артерий, включающий в себя выполнение радиочастотной аблации в трех циркулярных областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии, где 1 - легочный ствол; 2 - легочные артерии; 3 - радиочастотные повреждения, выполненные зигзагообразной прерывистой линией.
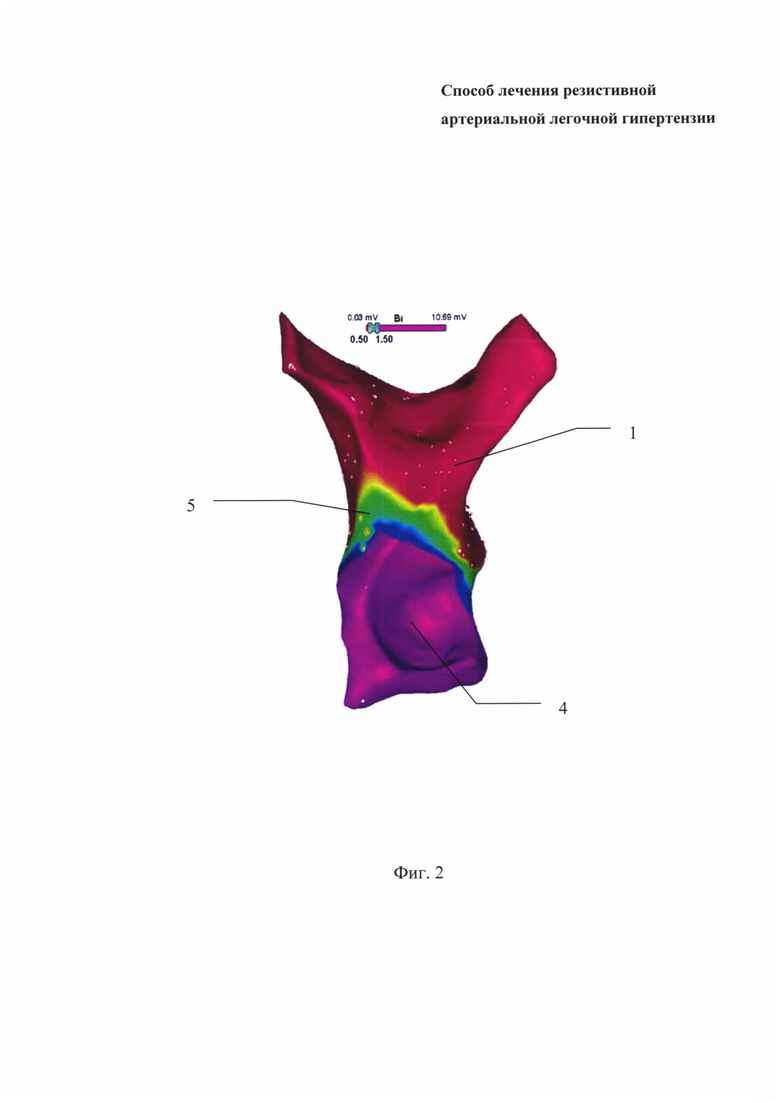
На фиг. 2 изображена амплитудная биполярная карта в задней проекции выводного тракта правого желудочка, легочного ствола и обеих легочных артерий в режиме Fast Anatomical Mapping с наложением данных об амплитуде биполярного электрографического сигнала с дистального полюса аблационного электрода, где 4 - выводной тракт правого желудочка, а 5 - зона мышечной муфты легочного ствола.
На фиг. 3 - амплитудная биполярная карта (в сеточном режиме) в передней проекции выводного тракта правого желудочка, легочного ствола и обеих легочных артерий в режиме Fast Anatomical Mapping с наложением данных об амплитуде биполярного электрографического сигнала с дистального полюса аблационного электрода.
Способ осуществляют следующим образом. Исходное положение пациента при выполнении предлагаемого способа лечения резистивной артериальной легочной гипертензии - лежа на спине. Процедуру осуществляют под внутривенной анестезией пропофолом, фентанилом и мидазоламом. Интраоперационная гипокоагуляция поддерживается непрерывной инфузией нефракционированного гепарина до достижения активированного времени свертывания 250-300 секунд.
Сосудистый доступ к правым отделам сердца выполняют путем катетеризации бедренной вены по S.-I. Seldinger с установкой интродьюсера диаметром 8 Fr. Через него в правый желудочек вводят ангиографический катетер Pigtail 6 Fr с изгибом 135°. Проводят измерение систолического, диастолического и среднего давления в правом желудочке, после чего катетер продвигают в легочный ствол, где выполняют аналогичные измерения.
После этого ангиографический катетер заменяют на аблационный с открытым контуром орошения (например, Navistar Thermocool F или EZ Steer Thermocool D/F NAV или Smarttouch F или Smarttouch Bidirectional D/F (Biosense Webster, США-Израиль). Далее проводят электроанатомическую реконструкцию на системе электромагнитной нефлюороскопической навигации (например, Carto 3 (Biosense Webster, США-Израиль) выводного тракта 4 правого желудочка, легочного ствола 1 и обеих главных легочных артерий 2 в режиме Fast Anatomical Mapping с наложением данных об амплитуде биполярного электрографического сигнала с дистального полюса аблационного электрода. Таким образом, получают данные об анатомии правых отделов, включая зону перехода выводного тракта 4 правого желудочка (амплитуда биполярного сигнала ≥ 1,5 мВ, фиолетовые оттенки) в легочный ствол 1 (амплитуда биполярного сигнала ≤ 0,5 мВ, красные оттенки). Переходная амплитуда сигнала (зеленые оттенки) соответствует мышечной муфте 5 легочного ствола 1.
Далее выполняют аблацию point-by-point с мощностью 30 Вт, температурой 43°C и скоростью орошения 17 мл/мин в режиме контроля по температуре продолжительностью по 30 с на точку. Радиочастотному воздействию подвергаются три циркулярные области: на 2 мм дистальнее устья левой легочной артерии 2, на 2 мм проксимальнее бифуркации легочного ствола 1 и на 2 мм дистальнее устья правой легочной артерии 2, исключая область проксимальнее места перехода миокарда выводного тракта 4 правого желудочка на легочной ствол 1.
По окончании воздействия аблационный катетер заменяют на ангиографический (Pigtail), при помощи которого выполняют те же измерения, что и до процедуры аблации.
Предложенный способ может быть использован у всех пациентов, позволяя повысить эффективность и безопасность катетерной денервации легочных артерий путем выполнения радиочастотных повреждений достаточной плотности с оставлением между ними участков неповрежденной ткани и исключая вероятность развития стеноза легочных артерий на фоне их последующего склерозирования, а также исключая радиочастотное повреждение области, анатомически соответствующей легочному стволу, но являющейся на самом деле миокардом выводного тракта правого желудочка, переходящим в легочный ствол.
Пример 1. Пациент Ж, 52 года, находился в отделении рентгенохирургических методов диагностики и лечения с 12.09.2016 по 15.09.2016 с диагнозом длительно персистирующей фибрилляции предсердий, вторичной легочной гипертензии.
Предъявлял жалобы на ускоренное неритмичное сердцебиение, сопровождающиеся одышкой и слабостью при минимальной физической нагрузке. «Аритмический» анамнез - в течение шести лет. Последний эпизод длится более трех лет, что позволяет форму фибрилляции предсердий классифицировать как длительно персистирующую.
По объективным данным: учащенный нерегулярный пульс, умеренное тахипноэ, укороченное дыхание по всем полям.
Расстояние шестиминутной ходьбы составило 220 м, по модифицированной шкале Борга пациент набрал 4 балла.
На поверхностной электрокардиограмме в покое регистрировалась фибрилляция предсердий со средней частотой сердечных сокращений 110 ударов в минуту, горизонтальное положение электрической оси сердца, признаки перегрузки миокарда левого желудочка.
По данным эхокардиографии имелась дилатация левого предсердия (переднезадний размер 5,2 см), расширение правого желудочка до 3,2 см, трикуспидальная регургитация 1 степени. Систолическая функция на фоне тахисистолии незначительно снижена (фракция выброса ЛЖ по Simpson - 43%). Систолическое давление в правом желудочке - 45 мм рт. ст.
Пациенту 13.09.2015 проведена процедура катетерной аблации фибрилляции предсердий, дополненная катетерной пульмональной денервацией. Исходно на фоне фибрилляции давление в правом желудочке составило 48/9 мм рт. ст. (среднее - 27 мм рт. ст.), в легочном стволе - 46/18 мм рт. ст. (среднее - 29 мм рт. ст.), давление заклинивания легочной артерии - 18 мм рт. ст. Выполнено восстановление синусового ритма кардиоверсией мощностью 300 Дж, после чего давление в правых отделах не изменилось. Выполнена радиочастотная антральная изоляция легочных вен с мощностью 30-40 Вт и температурой 43°C в орошаемом режиме. После изоляции легочных вен давление в правых отделах также не изменилось.
Согласно способу прототипу проведена пульмональная денервация в трех циркулярных областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии, при котором аблационные повреждения выполнялись сплошной линией.
По окончании воздействия давление в правом желудочке составило 37/7 мм рт. ст.(среднее - 22 мм рт. ст.), в легочном стволе - 32/12 мм рт. ст. (среднее - 21 мм рт. ст.), давление заклинивания легочной артерии - 16 мм рт. ст. Учитывая высокий транспульмональный градиент, заподозрен острый стеноз легочных артерий. Выполнена ангиопульмонография, на которой выявлен умеренный (около 50% просвета) стеноз левой легочной артерии. После пробы с нитроглицерином степень стенозирования не изменилась. Выполнена баллонная ангиопластика левой легочной артерии с остаточным стенозом менее 10% просвета.
После этого построена электроанатомическая амплитудная карта легочных артерий, легочного ствола и выводного тракта правого желудочка и выяснено, что часть радиочастотных воздействий были выполнены в зоне перехода миокарда выводного отдела правого желудочка на легочный ствол. Дополнительно были нанесены воздействия дистальнее этой области, что привело к дополнительному уменьшению среднего давления в правом желудочке на 4 мм рт. ст., в легочной артерии - на 6 мм рт. ст. Транспульмональный градиент уменьшился на 6 мм рт. ст.
В данном клиническом случае выполнение аблационного повреждения непрерывной линией привело к развитию острого стенозирования левой легочной артерии, которое пришлось устранять путем баллонной ангиопластики. Также продемонстрировано, что аблация в области перехода миокарда выводного отдела правого желудочка на легочный ствол приводит к недостаточно полному эффекту процедуры.
Пример 2. Пациентка Н., 63 года, находился в отделении рентгенохирургических методов диагностики и лечения с 26.09.2016 по 28.09.2016 с диагнозом длительно персистирующей фибрилляции предсердий, вторичной легочной гипертензии.
Предъявляла жалобы на ускоренное неритмичное сердцебиение, сопровождающиеся одышкой и слабостью при минимальной нагрузке. «Аритмический» анамнез - в течение пяти лет.
По объективным данным: учащенный нерегулярный пульс, умеренное тахипноэ.
На поверхностной электрокардиограмме в покое регистрировалась фибрилляция предсердий со средней частотой сердечных сокращений 106 ударов в минуту, горизонтальное положение электрической оси сердца.
По данным эхокардиографии имелась умеренная дилатация левого предсердия (5,4 см), правого желудочка (3,2 см), трикуспидальная регургитация 1 степени. Систолическая функция на фоне тахисистолии незначительно снижена (фракция выброса ЛЖ по Simpson - 44%). Систолическое давление в правом желудочке - 47 мм рт. ст.
Пациенту 27.09.2016 проведена процедура катетерной аблации фибрилляци предсердий, дополненная катетерной пульмональной денервацией. Исходно на фоне фибрилляции давление в правом желудочке составило 48/10 мм рт. ст. (среднее - 30 мм рт. ст.), в легочном стволе - 48/21 мм рт. ст. (среднее - 32 мм рт. ст.), давление заклинивания легочной артерии - 13 мм рт. ст. Выполнено восстановление синусового ритма кардиоверсией мощностью 360 Дж, после чего давление в правых отделах не изменилось. Выполнена радиочастотная антральная изоляция легочных вен с мощностью 30-40 Вт и температурой 43°C в орошаемом режиме. После изоляции легочных вен давление в правых отделах также не изменилось.
Далее выполнено построение амплитудной биполярной карты выводного отдела правого желудочка, легочного ствола и легочных артерий, после чего проведена пульмональная денервация по предложенному способу.
По окончании воздействия давление в правом желудочке составило 33/7 мм рт. ст. (среднее - 20 мм рт. ст.), в легочном стволе - 30/13 мм рт. ст. (среднее - 21 мм рт. ст.), давление заклинивания легочной артерии - 15 мм рт. ст. Небольшое повышение давления в левом предсердии и, вследствие этого, давления заклинивания легочной артерии - частое явление после изоляции легочных вен. Транспульмональный градиент составил менее 15 мм рт. ст., что исключало резистивный компонент легочного сопротивления. При контрольной ангиопульмонографии признаков стенозирования легочных артерий не выявлено.
В данном клиническом случае выполнение предложенного способа позволило эффективно устранить резистивную легочную гипертенизю, предотвратив при этом стенозирование легочных артерий.
Предложенный способ катетерной денервации легочных артерий использован на 6 пациентах, в результате чего получены данные о его высокой эффективности и безопасности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВТОРИЧНОЙ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ У ПАЦИЕНТОВ С ПОРОКАМИ МИТРАЛЬНОГО КЛАПАНА | 2016 |
|
RU2661710C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2024 |
|
RU2833935C1 |
| Способ хирургического лечения острой тромбоэмболии легочной артерии высокого и промежуточно высокого риска | 2021 |
|
RU2789686C1 |
| Способ двусторонней криоденервации легочных артерий и устройство для его осуществления | 2020 |
|
RU2749632C1 |
| СПОСОБ ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ | 2010 |
|
RU2477158C2 |
| СПОСОБ АМПУТАЦИИ УШКА ЛЕВОГО ПРЕДСЕРДИЯ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАЦИЕНТОВ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ | 2024 |
|
RU2833936C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ ПРИ ПРОТЕЗИРОВАНИИ МИТРАЛЬНОГО КЛАПАНА В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2020 |
|
RU2758133C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2015 |
|
RU2613445C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНАТОМИИ СЕРДЦА И КРУПНЫХ СОСУДОВ | 2013 |
|
RU2539993C2 |
| Способ комплексного эндоваскулярного лечения пациентов с сахарным диабетом и сердечно-сосудистой коморбидностью | 2023 |
|
RU2827665C1 |

Изобретение относится к области медицины, а именно к сердечно-сосудистой хирургии. Выполняют построение амплитудной биполярной карты выводного тракта правого желудочка, легочного ствола и обеих легочных артерий (ЛА). После чего наносят радиочастотные повреждения в трех циркулярных областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии. Аблационные повреждения наносят в виде незамкнутой зигзагообразной линии по внутренней окружности сосудов, исключая область проксимальнее места перехода миокарда выводного тракта правого желудочка на легочный ствол. Способ позволяет повысить эффективность и безопасность катетерной денервации легочных артерий, предотвращает стеноз и некроз легочных артерий. 3 ил., 2 пр.
Способ лечения резистивной легочной артериальной гипертензии, включающий визуализацию правой и левой легочных артерий, а также легочного ствола с последующим нанесением радиочастотных повреждений в трех циркулярных областях: на 2 мм дистальнее устья левой легочной артерии, на 2 мм проксимальнее бифуркации легочного ствола и на 2 мм дистальнее устья правой легочной артерии, отличающийся тем, что визуализацию осуществляют путем построения амплитудной биполярной карты и дополнительно оценивают локализацию перехода миокарда выводного тракта правого желудочка на легочный ствол, при этом аблационные повреждения в трех циркулярных областях наносят в виде незамкнутой зигзагообразной линии, исключая область проксимальнее места перехода миокарда выводного тракта правого желудочка на легочный ствол.
| Chen S-L, Zhang F-F, Xu J, Xie D-J, Zhou L, Nguyen T, Stone GW | |||
| Pulmonary Artery Denervation to Treat Pulmonary Arterial Hypertension | |||
| The Single-Center, Prospective, First-in-Man PADN-1 Study (First-in-Man Pulmonary Artery Denervation for Treatment of Pulmonary Artery Hypertension) | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ЛЕГОЧНОЙ ГИПЕРТЕНЗИЕЙ | 1996 |
|
RU2111748C1 |
| WO 2016007851 A1, 14.01.16 | |||
| Christopher F | |||
| Liu, MD., Ubiquitous Myocardial Extensions into the Pulmonary Artery Demonstrated by Integrated Intracardiac Echocardiography and Electroanatomic Mapping: Changing the Paradigm of Idiopathic Right Ventricular Outflow Tract Arrhythmias, Circ Arrhythm Electrophysiol | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2019-07-16—Публикация
2016-12-13—Подача