Перекрестная ссылка на родственные заявки
Данная заявка представляет собой национальную фазу международной заявки США № PCT/RS2020/000016, поданной 16 октября 2020 г., содержание которой включено в настоящий документ посредством ссылки во всей своей полноте во всех отношениях.
Область техники, к которой относится изобретение
Данное изобретение относится к терапевтическому применению растительного препарата с особым химическим составом, получаемого путем смешивания двух или более эфирных масел из родов Satureja L., Origanum L. и Thymus L., для приготовления пищевой добавки или лекарственного средства для успешного уничтожения болезнетворных бактерий. В частности, изобретение относится к применению такого растительного препарата для приготовления пищевой добавки или лекарственного средства для успешного уничтожения Helicobacter pylori (H. pylori) у людей.
Уровень техники
H. pylori обитает в желудке человека, где может вызывать многие тяжелые желудочно-кишечные расстройства, такие как гастрит, язва желудка и двенадцатиперстной кишки, карцинома желудка. По данным Всемирной организации здравоохранения (ВОЗ), примерно 50% населения земного шара инфицировано H. pylori, с разным уровнем распространения в развитых (от 25 до 50%) и развивающихся странах (от 70 до 90%). Хотя большинство пациентов не испытывают симптомов заболевания, у значительного процента инфицированных субъектов будет развиваться язвенная болезнь (примерно от 10 до 20%), у четверти этих пациентов (примерно 4,25%) будут серьезные осложнения язвенной болезни, а у 1-2% болезнь будет прогрессировать вплоть до рака желудка. Рак желудка является второй наиболее распространенной причиной смерти от рака в мире (Кустерс и др. (2006) Патогенез инфекции H. pylori. Клиническая микробиология. Обзор. 19:449-490). Соответственно, в 1994 году, ВОЗ объявила H. pylori канцерогеном для человека. Более того, из-за инфекции H. pylori примерно 500 миллионов человек во всем мире рано или поздно будут страдать от тяжелой патологии желудка, то есть пептической язвы, и примерно у 30 миллионов может развиться рак желудка.
Существует острая необходимость добиться уничтожения H. pylori в слизистой оболочке желудка. Для этого были использованы многочисленные методы антибиотикотерапии: амоксициллин, тетрациклин, метронидазол, фуразолидон, левофлоксацин и кларитромицин (Ванмахер (2011) Обзор схем лечения H. pylori, 18-е совещание Комитета экспертов по отбору и использованию основных лекарственных средств). В настоящее время, терапия инфекции H. pylori состоит из высоких доз трех-четырех различных антибиотиков в дополнение к вспомогательным средствам. Однако эта терапия демонстрирует весьма ограниченную эффективность, в основном из-за чрезвычайно частого появления штаммов H. pylori, устойчивых к действию антибиотиков. Например: трёхкомпонентная терапия с использованием кларитромицина и амоксициллина/метронидазола с ингибитором протонной помпы (ИПП) показала эффективность в 84% и 76% случаев, в то время как четырехкомпонентная терапия, состоящая из ИПП, висмута, метронидазола и тетрациклина, показала эффективность в 87% случаев. Поскольку даже 20% пациентов с инфекцией H. pylori не излечиваются после завершения первого курса лечения антибиотиками, требуется дополнительный цикл лечения. Так, ВОЗ включила H. pylori в «Список приоритетных устойчивых к действию антибиотиков бактерий для руководства исследованиями, открытием и разработкой новых антибиотиков», который был разработан группой из 70 ведущих мировых экспертов в 2017 году. Более того, все упомянутые способы лечения часто связаны с тяжелыми желудочно-кишечными побочными эффектами, такими как диарея, тошнота, рвота, вздутие живота и боль в животе, которые пациенты тяжело переносят.
Кроме того, было предложено несколько альтернативных способов лечения инфекции H. pylori у людей на основе микроорганизмов, пептидов, полисахаридов и внутрижелудочного облучения фиолетовым светом, но они не были эффективны в уничтожении бактерий (Айала и др. (2014) Изучение альтернативного лечения инфекции Helicobacter pylori, Гастроэнтерология 20(6): 1450-1469). Кроме того, недавнее исследование вакцин подтвердило, что перспективные вакцинные препараты еще не найдены (Sutton & Boag (2019) Статус исследований и разработок вакцин против Helicobacter pylori, Вакцина 37:7295-7299).
Пробиотики и некоторые пищевые добавки на растительной основе используются для предотвращения или уменьшения некоторых побочных эффектов антибиотикотерапии. Однако не существует имеющихся в продаже пищевых добавок или иных растительных препаратов, которые были бы протестированы на людях на предмет наличия антихеликобактерной активности, улучшения терапевтического ответа на антибиотики или предотвращения повторного появления инфекции H. pylori у людей.
Эфирные масла, полученные из ароматических растений, являются хорошо известными противомикробными препаратами в отношении многих штаммов бактерий. Эфирные масла представляют собой сложные смеси летучих органических соединений (преимущественно терпенов и фенилпропанов), получаемых гидродистилляцией или перегонкой с водяным паром из ароматических растений. Эфирное масло из одного ароматического растения может содержать несколько сотен различных компонентов. Химический состав эфирного масла из отдельных видов растений сильно варьируется, как в качественном, так и в количественном отношении. За эту изменчивость отвечают различные факторы, в том числе: внутренние факторы, связанные с растением, взаимодействие растения с окружающей средой (тип почвы, климат и т.д.), зрелость растения, орган растения, выбранный для выделения эфирного масла, время суток, когда проводится сбор, и внешние факторы, связанные со способом извлечения. Противомикробный потенциал эфирного масла в значительной степени зависит от его химического состава. Следовательно, нельзя заявлять о степени противомикробной активности эфирного масла из конкретного растения без определения его химического профиля. Поэтому, при исследовании возможного применения конкретных эфирных масел, следует определить химический состав каждого образца эфирного масла.
Некоторые эфирные масла проявляют противомикробную активность in vitro в биопробах даже в отношении полирезистентных штаммов H. pylori (Martin & Ernst (2003) Лекарственные препараты растительного происхождения для лечения бактериальных инфекций: обзор контролируемых клинических испытаний. Противомикробная химиотерапия 51:241-246; Оно и др. (2003) Противомикробная активность эфирных масел в отношении Helicobacter pylori, Хеликобактер 8:207-215, Такеучи и др. (2014) Лекарственные средства природного происхождения и пищевые компоненты, имеющие антихеликобактерную активность, Гастроэнтерология 20:8971-8978).
Существуют многочисленные доказательства противомикробной активности эфирных масел в отношении H. pylori in vitro, с получением из видов из родов Satureja L., Origanum L. и Thymus L.
Например, эфирные масла Satureja bachtiarica, Satureja montana и Satureja hortensis проявляют высокую антихеликобактерную активность in vitro (Бергонцелли и др. (2003) Эфирные масла как компоненты основанного на диете подхода к лечению инфекции Helicobacter. Противомикробные агенты и химиотерапия 47:3240-324; Фальсафи и др. (2015) Химический состав и действие эфирного масла Satureja bachtiarica Bunge против Helicobacter pylori. Фитомед 22:173-177; Лесяк и др. (2016): Бинарные и третичные смеси эфирных масел Satureja hortensis и Origanum vulgare в качестве сильнодействующих противомикробных агентов против Helicobacter pylori. Фитотерапия Исследования 30:476-484).
Эфирное масло, полученное из Origanum vulgare, показало антихеликобактерную активность in vitro в биопробах (Бергонцелли и др. (2003) Эфирные масла как компоненты основанного на диете подхода к лечению инфекции Helicobacter. Противомикробные агенты и химиотерапия 47:3240-324). Также доказано, что карвакрол, основной компонент эфирного масла орегано, проявляет бактерицидную активность в отношении штаммов H. pylori in vitro (Маринелли и др. (2018) Карвакрол и его производные в качестве антибактериальных средств. Фитохимия Обзор 17:903-921; Руис-Рико и др. (2020) Противомикробная активность иммобилизованных компонентов эфирного масла в отношении Helicobacter pylori in vitro. Биотехнология и Микробиология 36:3-9).
Было показано, что эфирное масло тимьяна обыкновенного Thymus vulgaris обладает антибактериальным действием против H. pylori (Эсмаэлли и др. (2012): Антихеликобактерная активность соевого порошка и эфирных масел Thymus vulgaris и Eucalyptus globulus. Микробиология 6:65-69). Кроме того, некоторые другие виды тимьяна проявляют антихеликобактерную активность (Дандлен и др. (2011): Противомикробная активность эфирных масел португальского тимьяна, цитотоксичность и ингибирование внутриклеточного роста. Обзор. Bras. Farmacogn 21:1012-1024). Кроме того, основной компонент эфирного масла тимьяна - тимол - показал высокую бактерицидную активность против штаммов H. pylori in vitro (Корона-Гловняк и др. (2020) Активность эфирных масел in vitro против роста Helicobacter pylori и активности уреазы. Молекулы 25:1-15).
Кроме того, было показано, что циклические углеводороды - цимен, который в больших количествах присутствует в эфирном масле тимьяна, и γ-терпинен, в изобилии присутствующий в эфирном масле Satureja hortensis, не обладают антибактериальной активностью в отношении грамотрицательных бактерий (Корона-Гловняк и др. (2020) Активность эфирных масел in vitro против роста Helicobacter pylori и активности уреазы. Молекулы 25:1-15). Однако сообщалось, что некоторые соединения, не обладающие антибактериальной активностью, в присутствии других противомикробных агентов проявляют синергический эффект. Например, присутствие п-цимена в эфирном масле наряду с карвакролом может усиливать противомикробную активность масла (Ульти и др. (2002) Фенольная гидроксильная группа карвакрола необходима для действия против патогена пищевого происхождения Bacillus cereus. Микробиология окружающей среды 68:1561-1568).
Кроме того, смеси эфирных масел, в частности бинарные и третичные смеси эфирных масел Satureja hortensis, Origanum vulgare подвид vulgare и Origanum vulgare подвид hirtum были более эффективными по сравнению с активностью каждого масла из смеси в отдельности (Лесяк и др. (2016): Бинарные и третичные смеси эфирных масел Satureja hortensis и Origanum vulgare в качестве сильнодействующих противомикробных агентов против Helicobacter pylori. Фитотерапия Исследования 30:476-484).
Что касается результатов in vivo на экспериментальных животных, то было доказано, что смесь эфирных масел Satureja hortensis и Origanum vulgare подвид hirtum успешно уничтожили H. pylori у 70% мышей без применения антибиотиков, при этом, не проявляя токсичности и не изменяя баланс цитокинов и хемокинов (Хармати и др. (2017): Бинарная смесь эфирных масел Satureja hortensis и Origanum vulgare подвид hirtum: терапевтическая эффективность in vivo против инфекции Helicobacter pylori. Helicobacter el 2350).
Однако, в известном уровне техники отсутствуют исследования, проведенные на людях, в которых оценивают терапевтическую эффективность эфирных масел, полученных из Satureja sp., Origanum sp. и Thymus sp., их смесей или чистых соединений, выделенных из этих масел, для уничтожения H. pylori.
Приведенный выше краткий обзор ясно указывает на острую необходимость поиска новых способов лечения для уничтожения инфекции H. pylori у людей и различных подходов, предлагаемых для борьбы с этой бактерией.
Техническая проблема
Задачей настоящего изобретения является получение растительного препарата, имеющего особый химический профиль, с содержанием смеси эфирных масел и являющегося высокоэффективным для уничтожения инфекции H. pylori у людей.
Второй задачей настоящего изобретения является предоставление способа приготовления описанного растительного препарата.
Третьей задачей настоящего изобретения является предоставление режима дозирования для лечения растительным препаратом пациентов с подтвержденной инфекцией H. pylori, что приводит к успешному уничтожению H. pylori в слизистой оболочке желудка.
Четвертой задачей настоящего изобретения является предоставление способа лечения растительным препаратом для уничтожения H. pylori в слизистой оболочке желудка без использования каких-либо известных лекарственных средств или антибиотиков.
Пятой задачей настоящего изобретения является предоставление способа лечения растительным препаратом для уничтожения H. pylori в слизистой оболочке желудка, который не вызывает каких-либо нежелательных побочных эффектов, таких как диарея, тошнота, рвота, вздутие живота и боль в животе, которые очень распространены при стандартной антибиотикотерапии.
Раскрытие изобретения
Изобретение заключается в применении растительного препарата - особой смеси эфирных масел - в качестве пищевой добавки или лекарственного средства для профилактики и лечения инфекции Helicobacter pylori у людей. Такая смесь характеризуется присутствием 4 доминирующих соединений в следующих количествах: карвакрол примерно от 35% до примерно 50%, γ-терпинен примерно от 10% до примерно 30%, тимол примерно от 10% до примерно 25%, п-цимен примерно от 8% до примерно 20%, выражено в % от общей площади пиков на ГХ/МС хроматограмме. Смесь может быть получена путем смешивания двух или более эфирных масел видов из родов Satureja L., Origanum L. и Thymus L. Смесь может быть помещена на жидкий или твердый носитель и заключена в не гастрорезистентные капсулы. Препарат, раскрытый в настоящей заявке, пригоден для применения в качестве пищевой добавки или растительного лекарственного средства для лечения инфекции H. pylori. В настоящей заявке также раскрыт режим дозирования для успешного уничтожения H. pylori в слизистой оболочке желудка у людей.
Способ получения препарата (смеси эфирных масел):
Растительный препарат по настоящему изобретению должен иметь особый химический профиль для достижения высокой антихеликобактерной активности. Он характеризуется присутствием четырех доминирующих соединений: карвакрола примерно от 35% до примерно 50%, γ-терпинена примерно от 10% до примерно 30%, тимола примерно от 10% до примерно 25%, п-цимена примерно от 8% до примерно 20%. Количества выражены в % от общей площади всех пиков на хроматограмме, полученной методом газовой хроматографии с масс-спектрометрическим детектированием (ГХ-МС). Дополнительно, препарат может содержать минорные соединения, такие как α-терпинен, транс-β-кариофиллен, α-пинен, β-пинен, β-мирцен, линалоол, 1,8-цинеол, лимонен, с присутствием каждого в количестве от 0,1 до 3% (выражено в % от общей площади всех пиков на ГХ-МС хроматограмме). Любые другие компоненты препарата могут присутствовать в количестве до 0,4% каждого. Предпочтительно, состав препарата (выражается в % от общей площади всех пиков на хроматограмме) должен включать: карвакрол примерно от 38% до примерно 48%, γ-терпинен примерно от 18% до примерно 28%, тимол примерно от 10% до примерно 12%, п-цимен примерно от 9% до примерно 14% и α-терпинен, транс-β-кариофиллен, α-пинен, β-пинен, β-мирцен, линалоол, 1,8-цинеол, лимонен, с присутствием каждого в количестве от 0,4 до 2,9%. Наибольший эффект в отношении H. pylori показал препарат со следующим точным составом (выражается в % от общей площади всех пиков на хроматограмме): карвакрол 47,5%, γ-терпинен 18,5%, тимол 11,9%, п-цимен 13,6%, α-терпинен 1,55%, транс-β-кариофиллен 1,49%, линалоол 1,24%, α-пинен 0,99%, β-мирцен 0,97%, 1,8-цинеол 0,55%, лимонен 0,46% и β-пинен 0,40%.
Препарат по настоящему изобретению может быть получен путем смешивания двух или более эфирных масел, предпочтительно полученных гидродистилляцией, из следующих растений: Satureja sp., Origanum sp. и Thymus sp. Эти растения обычно используются в качестве специй или чая. Что особенно важно, эти эфирные масла в целом признаны безопасными (GRAS) веществами Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и одобрены Европейской комиссией для их предполагаемого использования в качестве ароматизаторов в пищевых продуктах.
Предпочтительно, растительный препарат по настоящему изобретению может быть получен путем смешивания эфирных масел Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. в следующем соотношении: 2:1:1 соответственно. Поскольку химический профиль эфирных масел сильно варьируется, в основном из-за различных экологических факторов, способов выращивания ароматических растений и способов выделения, предпочтительный химический состав отдельных эфирных масел, используемых для получения растительного препарата по настоящему изобретению, приведен в таблице ниже:
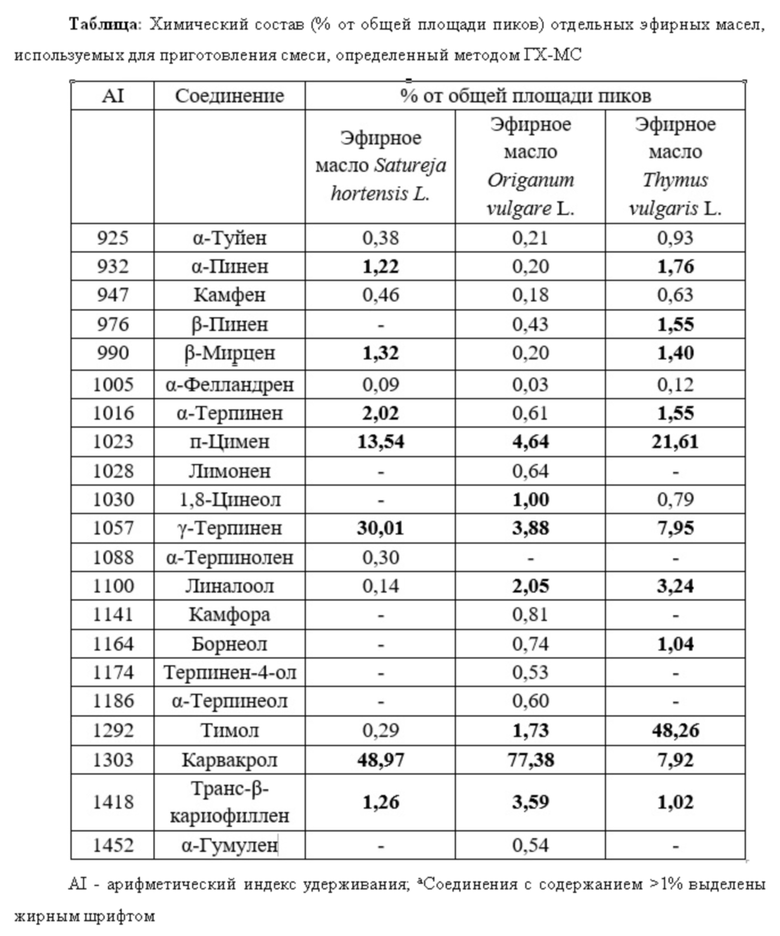
Эфирные масла, раскрытые в настоящем изобретении, получены из растений вида Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. Растительный материал собирали в фазе цветения и после сушки на воздухе при температуре 25-30°С измельчали в блендере. Эфирные масла выделяли гидродистилляцией в соответствии с процедурой Ph. EUR. IV (Европейская фармакопея, 2002 г.) в аппарате Клевенджера. Вкратце, 100 г растительного материала заливали водой, и дистилляция продолжалась в течение 3 часов. После охлаждения, чистое эфирное масло отбирали из аппарата Клевенджера и высушивали безводным сульфатом натрия. После удаления сульфата фильтрованием через воронку Бюхнера, эфирное масло собирали и хранили при температуре -20°C до использования. Полученные эфирные масла Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. смешивали в следующем соотношении: 2:1:1, соответственно, для получения растительного препарата по настоящему изобретению, который в дальнейшем использовали для лечения инфицированных H. pylori добровольцев.
Возможное применение настоящего изобретения:
Растительный препарат по настоящему изобретению можно использовать для лечения или профилактики инфекции H. pylori в качестве пищевой добавки или растительного лекарственного средства. Если он используется в качестве лекарственного средства, его можно применять отдельно или в сочетании со стандартной антибиотикотерапией. Препарат (особая смесь эфирных масел) может быть помещен на жидкий или твердый носитель и заключен в желатиновые капсулы. Каждая капсула должна содержать не менее 50 мг препарата, предпочтительно 65 мг препарата.
Эффективность растительного препарата по настоящему изобретению против H. pylori подтверждена исследованиями как in vitro, так и in vivo.
Растительный препарат по настоящему изобретению был протестирован против 20 клинических штаммов H. pylori, отнесенных к 4 различным популяциям, включающим HpEurope (европейскую), HpEAsia (восточноазиатскую), HpAsia2 (индийскую) и HpAfrical (африканскую). Большинство штаммов были устойчивы к нескольким антибиотикам. Испытания проводили с использованием метода разведений в агаре. Минимальную ингибирующую концентрацию (МИК) определяли как наименьшую концентрацию композиции, необходимую для полного подавления роста H. pylori. Минимальную бактерицидную концентрацию (МБК) определяли по количеству жизнеспособных колоний, а бактерицидная эффективность продукта выражалась в процентном снижении количества колоний бактерий по сравнению с необработанным участком. Результаты подтвердили, что препарат активен на одинаковом уровне активности против различных штаммов H. pylori, устойчивых к антибиотикам. Это означает, что препарат по настоящему изобретению не является селективным в отношении конкретного типа H. pylori и не имеет специфических клеток-мишеней. А именно, эфирные масла представляют собой сложные смеси большого количества липофильных соединений, которые проникают через клеточную стенку, разрушают бактериальную мембрану и взаимодействуют с интегральными мембранными белками. Такая сложность смеси полностью лишает микроорганизм способности к развитию резистентности. Это означает, что препарат подходит для уничтожения всех типов H. pylori, следовательно, он может применяться для лечения пациентов во всем мире, независимо от того, какой штамм H. pylori (устойчивый или неустойчивый к антибиотикам) вызвал инфекцию.
В рамках настоящей патентной заявки раскрыты результаты лечения 28 добровольцев (разделенных на три группы) растительным препаратом по настоящему изобретению.
В первую группу вошли 10 добровольцев с подтвержденной острой инфекцией H. pylori со слабо выраженными симптомами инфекции (вздутие живота, боль в животе, повышенный уровень желудочной кислоты, кашель, потеря аппетита). Добровольцы принимали желатиновые капсулы, содержащие 65 мг препарата, с растворением в 435 мг подсолнечного масла (5 добровольцев) или помещением на твердый носитель (5 добровольцев). Каждый доброволец принимал по 2 капсулы в сутки (65 мг препарата в капсуле), 1 утром и 1 вечером натощак за 30 минут до еды, в течение 30 дней подряд, то есть 130 мг растительного препарата ежедневно, по 65 мг дважды в сутки в течение 30 дней подряд.
В течение этих 30 дней они не получали никакого другого лечения инфекции H. pylori и соблюдали обычный режим питания, без употребления алкоголя. Через четыре и восемь недель после окончания лечения, добровольцев тестировали на определение антигена H. pylori в кале. Инфекция была уничтожена в 50% случаев. Вот почему был сделан вывод, что дозировка должна быть выше, по меньшей мере в начале лечения, и продолжительнее.
Во вторую группу вошли 15 добровольцев с подтвержденной острой инфекцией H. pylori со слабо выраженными симптомами инфекции (вздутие живота, боль в животе, повышенный уровень желудочной кислоты, кашель, потеря аппетита). По сравнению с режимом дозирования, применявшимся в первой группе, режим дозирования, применявшийся во второй группе, был выше в начале лечения и продолжительнее. Добровольцы принимали желатиновые капсулы, содержащие 65 мг препарата, с растворением в 435 мг подсолнечного масла (7 добровольцев) или помещением на твердый носитель (8 добровольцев). Каждый доброволец принимал по 4 капсулы в сутки, 2 утром и 2 вечером натощак за 30 минут до еды, в течение 15 дней подряд, затем по 2 капсулы в сутки, 1 утром и 1 вечером натощак за 30 минут до еды, в течение еще 30 дней, то есть 260 мг растительного препарата ежедневно, по 130 мг дважды в сутки в течение 15 дней подряд, затем 130 мг растительного препарата ежедневно, по 65 мг дважды в сутки в течение еще 30 дней. В течение этих 45 дней они не получали никакого другого лечения инфекции H. pylori и соблюдали обычный режим питания, без употребления алкоголя. Через четыре и восемь недель после окончания лечения, добровольцев тестировали на определение антигена H. pylori в кале. У 14 добровольцев из 15 подтверждено полное уничтожение инфекции H. pylori (инфекция была уничтожена в 93% случаев). Десять добровольцев сообщили о полном исчезновении симптомов заболевания (боль в желудке, повышенный уровень желудочной кислоты, вздутие живота) через 10 дней после начала лечения, в то время как у остальных четырех симптомы исчезли до конца терапии. Это означает, что растительный препарат по настоящему изобретению, помимо антибактериального действия в отношении H. pylori, оказывает противовоспалительное действие. Во время лечения, ни один из добровольцев не сообщил о каких-либо желудочно-кишечных побочных эффектах, таких как диарея, тошнота, рвота или боль в животе, которые очень часто встречаются при антибиотикотерапии. Такие результаты убедительно подтверждают, что препарат по настоящему изобретению эффективно уничтожает инфекцию H. pylori в слизистой оболочке желудка, предпочтительно без применения антибиотиков, и не вызывает каких-либо нежелательных побочных эффектов.
В третьей группе 3 других добровольца с хронической инфекцией (симптомы присутствуют более года) получали стандартную терапию (ИПП дважды в сутки + кларитромицин (2)×(500 мг) + амоксициллин (2×1000 мг)) в течение двух недель вместе с желатиновыми капсулами, содержащими 65 мг препарата по настоящему изобретению, с растворением в 435 мг подсолнечного масла. Через четыре и восемь недель после окончания лечения, добровольцев тестировали на определение антигена H. pylori в кале, и было подтверждено отсутствие инфекции. Это подтверждает, что препарат по настоящему изобретению не снижает эффект от стандартной терапии, а наоборот, улучшает его.
Кроме того, в отличие от всех известных в настоящее время и используемых терапевтических средств при лечении инфекции, вызванной H. pylori, раскрытый здесь препарат является полностью натуральным по составу и не содержит никаких синтетических соединений, что делает данную композицию предпочтительной для людей с аллергией или повышенной чувствительностью к антибиотикам.
Также данный препарат может быть использован для профилактики инфекции H. pylori у тех, кто склонен к гастриту и инфекции H. pylori. В целях профилактики, препарат можно принимать один или два раза в течение года в течение 60 дней подряд по одной капсуле в сутки натощак за 30 минут до еды, то есть 65 мг растительного препарата ежедневно в течение 60 дней подряд. Предпочтительно, такую терапию проводить в конце летнего или в конце зимнего периода. Препарат по настоящему изобретению особенно подходит для пациентов с доказанной инфекцией H. pylori, в частности для пациентов, которые предпочитают фитотерапию вместо использования антибиотиков, и еще более предпочтительно для пациентов, которые ранее лечились антибиотиками, но не вылечились после завершения лечения антибиотиками.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОРАЛЬНАЯ ПРОТИВОПАРАЗИТАРНАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2712765C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ ЭФИРНЫХ МАСЕЛ, ПОЛУЧЕННЫХ ИЗ РАСТЕНИЙ, ДЛЯ ИСПОЛЬЗОВАНИЯ В ОБЛАСТИ МЕДИЦИНЫ И ВЕТЕРИНАРИИ | 1996 |
|
RU2157697C2 |
| КОМПОЗИЦИИ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА, СОДЕРЖАЩИЕ РАСТИТЕЛЬНЫЕ ЭКСТРАКТЫ | 2008 |
|
RU2440821C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО САЛАТНОГО АРОМАТИЗИРОВАННОГО МАСЛА | 2019 |
|
RU2725709C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА С УСИЛЕННОЙ АКТИВНОСТЬЮ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1999 |
|
RU2155062C1 |
| АРОМАТИЗИРОВАННОЕ САЛАТНОЕ МАСЛО | 2021 |
|
RU2779146C1 |
| Способ получения композиции соли и обогащающего ингредиента | 2019 |
|
RU2710159C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ТИМОЛА И КАРВАКРОЛА В ЛЕКАРСТВЕННОМ РАСТИТЕЛЬНОМ СЫРЬЕ | 2007 |
|
RU2329499C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЖЕНСКОЙ ПОЛОВОЙ СФЕРЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2217157C1 |
| Способ получения тимохинона из семян черного тмина | 2023 |
|
RU2821514C1 |
Группа изобретений относится к фармацевтической промышленности, а именно к препарату лечения Helicobacter pylori инфекции у людей. Растительный препарат для лечения Helicobacter pylori инфекции у людей, полученный путем смешивания эфирных масел из растений Satureja hortensis L., Origanum vulgare L. подвид hirtum и Thymus vulgaris L. в соотношении 2:1:1, а также содержащий следующие компоненты, выраженные в процентах от общей площади пиков на ГХ/МС хроматограмме: карвакрол от 35% до 50%, γ-терпинен от 10% до 25%, тимол от 10% до 25%, п-цимен от 10% до 20%, причем растительный препарат предназначен для применения перорально. Способ лечения желудочной инфекции Helicobacter pylori у субъекта, включающий пероральное введение субъекту терапевтически эффективного количества растительного препарата по п. 1, содержащего эфирные масла Satureja hortensis L., Origanum vulgare L. подвид hirtum и Thymus vulgaris L. в соотношении: 2:1:1. Способ приготовления вышеописанного растительного препарата, содержащий следующие этапы: сбор надземных частей растений Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. в фазе цветения для получения собранного растительного материала; сушка собранного растительного материала на воздухе при температуре 25-30°C с получением высушенного растительного материала; измельчение высушенного растительного материала с получением измельченного материала; получение эфирных масел из измельченного материала; сушка эфирных масел безводным сульфатом натрия; удаление сульфата из эфирных масел фильтрованием и смешивание эфирных масел с получением вышеописанного растительного препарата, причем смешивают эфирные масла Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. в соотношении 2:1:1 соответственно. Вышеописанный препарат имеет особый химический профиль, является высокоэффективным для уничтожения инфекции Helicobacter pylori у людей. 3 н. и 10 з.п. ф-лы, 1 табл.
1. Растительный препарат для лечения Helicobacter pylori инфекции у людей, полученный путем смешивания эфирных масел из растений Satureja hortensis L., Origanum vulgare L. подвид hirtum и Thymus vulgaris L. в соотношении 2:1:1, а также содержащий следующие компоненты, выраженные в процентах от общей площади пиков на ГХ/МС хроматограмме:
карвакрол от 35% до 50%,
γ-терпинен от 10% до 25%,
тимол от 10% до 25%,
п-цимен от 10% до 20%,
причем растительный препарат предназначен для применения перорально.
2. Растительный препарат по п. 1, дополнительно содержащий:
α-терпинен, транс-β-кариофиллен, α-пинен, β-пинен, β-мирцен, линалоол, 1,8-цинеол и лимонен, с присутствием каждого в растительном препарате в количестве от 0,4% до 2,9%,
выражено в % от общей площади пиков на ГХ/МС хроматограмме.
3. Растительный препарат по п. 2, отличающийся тем, что растительный препарат содержит:
карвакрол от 38% до 48%,
γ-терпинен от 15% до 25%,
тимол от 10% до 16%,
п-цимен от 10% до 15%, и
α-терпинен, транс-β-кариофиллен, α-пинен, β-пинен, β-мирцен, линалоол, 1,8-цинеол и лимонен, с присутствием каждого в растительном препарате в количестве от 0,4% до 2,9%, выражено в % от общей площади пиков на ГХ/МС хроматограмме.
4. Растительный препарат по п. 2, отличающийся тем, что растительный препарат содержит:
47,5% карвакрола,
18,5% γ-терпинена,
11,9% тимола,
13,6% п-цимена,
1,55% α-терпинена,
1,49% транс-β-кариофиллена,
1,24% линалоола,
0,99% α-пинена,
0,97% β-мирцена,
0,55% 1,8-цинеола,
0,46% лимонена и
0,40% β-пинена, выражено в % от общей площади пиков на ГХ/МС хроматограмме.
5. Растительный препарат по п. 1, дополнительно содержащий жидкий носитель или твердый носитель.
6. Растительный препарат по п. 5, отличающийся тем, что жидким носителем является подсолнечное масло.
7. Растительный препарат по п. 5, отличающийся тем, что твердый носитель содержит диоксид кремния.
8. Способ лечения желудочной инфекции Helicobacter pylori у субъекта, включающий пероральное введение субъекту терапевтически эффективного количества растительного препарата по п. 1, содержащего эфирные масла Satureja hortensis L., Origanum vulgare L. подвид hirtum и Thymus vulgaris L. в соотношении: 2:1:1.
9. Способ по п. 8, отличающийся тем, что растительный препарат вводят в сочетании с одним или несколькими антибиотиками.
10. Способ по п. 8, отличающийся тем, что растительный препарат готовят для приема дважды в сутки в дозированной форме по 65 мг в течение 30 дней подряд.
11. Способ по п. 8, отличающийся тем, что растительный препарат готовят для приема дважды в сутки в дозированной форме по 130 мг в течение 15 дней подряд с последующим приемом дважды в сутки в дозированной форме по 65 мг в течение 30 дней подряд.
12. Способ приготовления растительного препарата по п. 1, содержащий следующие этапы:
- сбор надземных частей растений Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. в фазе цветения для получения собранного растительного материала,
- сушку собранного растительного материала на воздухе при температуре 25-30°C с получением высушенного растительного материала,
- измельчение высушенного растительного материала с получением измельченного материала,
- получение эфирных масел из измельченного материала,
- сушку эфирных масел безводным сульфатом натрия,
- удаление сульфата из эфирных масел фильтрованием и
- смешивание эфирных масел с получением растительного препарата по п. 1, причем смешивают эфирные масла Satureja hortensis L., Origanum vulgare подвид hirtum L. и Thymus vulgaris L. в соотношении 2:1:1 соответственно.
13. Способ по п. 12, отличающийся тем, что получение эфирных масел включает гидродистилляцию измельченного материала.
| WO 2015032922 A1, 12.03.2015 | |||
| LESJAK M | |||
| et al | |||
| Binary and tertiary mixtures of Satureja hortensis and Origanum vulgare essential oils as potent antimicrobial agents against Helicobacter pylori //Phytother Res | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| SAIKA TARIQA et al | |||
| A comprehensivere view of the antibacterial, | |||
Авторы
Даты
2024-10-03—Публикация
2020-10-16—Подача