Изобретение относится к аналитической и коллоидной химии. Данное техническое решение может быть использовано для определения критической концентрации мицеллообразования (ККМ) полиоксиэтилированных алкилфенолов в водных растворах.
В настоящее время методы определения ККМ принято делить на прямые и косвенные. К прямым методам, основанным на регистрации изменения какого-либо физико-химического свойства при увеличении концентрации поверхностно-активных веществ (ПАВ) в растворе, чаще относят технологии определения мутности растворов, поверхностного натяжения, электрической проводимости, коэффициента преломления света, вязкости [Ланге К.Р. Поверхностно-активные вещества: синтез, свойства, анализ, применение / под научн. ред. Л.П. Зайченко. СПб.: Профессия, 2004. 240 с.]. Измерение электропроводности и поверхностного натяжения являются наиболее распространенными методами, но они имеют ряд существенных ограничений: продолжительны по времени, применяются только для измерения высоких значений ККМ ионогенных ПАВ. В косвенных методах регистрируют изменения физико-химических характеристик, например, светопоглощение или люминесценцию, происходящие с веществами - «зондами» в присутствии мицелл ПАВ различной природы.
Среди большого разнообразия методов, применяющихся для определения ККМ, спектроскопические методы привлекают внимание исследователей простотой выполнения эксперимента, достаточно высокой точностью, аппаратурной оснащенностью. Возможности и ограничения прямых и косвенных спектроскопических определений ККМ показаны в обзоре [Mabrouk M.M., Hamed N.A., Mansour F.R. Spectroscopic methods for determination of critical micelle concentrations of surfactants; a comprehensive review //Applied Spectroscopy Reviews. 2023. Vol. 58, №.3. P.206-234]. Большинство методов являются косвенными, основанными на различии в светопоглощении или испускании «зондов» в присутствии свободных молекул и мицелл ПАВ. Изменение формы спектральных кривых происходит за счет различного влияния мицелл ПАВ на физико-химические процессы: растворимость красителей; кислотно-основные и таутомерные равновесия; каталитическую активность органических соединений; образование ионных ассоциатов и др. При увеличении концентрации ПАВ также происходит изменение испускания различных «зондов», что приводит к выраженным изменениям форм спектров флуоресценции и их интенсивности.
Однако применение для одного и того же ПАВ различных «зондов», изменяющих их физико-химические свойства, может привести к получению различных значений ККМ поскольку мицеллообразование зависит от микроокружения отдельных молекул ПАВ.
Известно также прямое определение ККМ для растворов ПАВ серии Тритон спектрофотометрическим методом [Mabrouk M.M., Hamed N.A., Mansour F.R. Spectroscopic methods for determination of critical micelle concentrations of surfactants; a comprehensive review //Applied Spectroscopy Reviews. 2023. Vol. 58, №3. P.206-234] путем построения зависимости поглощения при заданной длине волны от концентрации ПАВ в растворе и нахождения точки, соответствующей концентрации, при которой происходит отклонение от закона Бугера-Ламберта-Бера.
Однако данный способ требует применение спектрофотометров, обладающих возможностью измерения оптической плотности выше двух и для высоконцентрированных растворов ПАВ, что ограничивает его применение, не позволяя определить ККМ образования сферических мицелл.
Известен также способ определения критической концентрации мицеллообразования ПАВ, применяемых при электроосаждении [авторское свидетельство SU 1719970]. Он характеризуется тем, что регистрируют зависимость оптической плотности водных растворов ПАВ от концентрации относительно раствора, исследуемого ПАВ, концентрации которого составляет 50-65% от его концентрации, используемой в электроосаждении, и ККМ определяют по точке перегиба на этой зависимости.
Однако, данный способ адаптирован только к ПАВ ионной природы, применяемых при электроосаждении, используемые для спектрофотометрии растворы которых мутные. В связи со специфичностью способа он может быть применен для решения конкретных задач и не может быть перенесен в другую отрасль для определения ККМ ПАВ других видов.
Наиболее близким аналогом к заявляемому способу является способ спектрофотометрического определения ККМ Тритонов [Investigating the micellization of the triton-X surfactants: A non-invasive fluorometric and calorimetric approach / S. Jaiswal, R. Mondal, D. Paul et al. // Chemical Physics Letters. 2016. Vol. 646. P. 18-24; Anand U., Jash C., Mukherjee S. Spectroscopic determination of Critical Micelle Concentration in aqueous and non-aqueous media using a non-invasive method // Journal of colloid and interface science. 2011. Vol. 364, №2. P.400-406], включающий подготовку серии водных растворов неионогенных поверхностно-активных веществ (НПАВ) (Tритон X-114, Tритон X-100 и Tритон X-165), регистрацию их спектров поглощения, построение графика концентрационной зависимости спектральной характеристики в виде оптической плотности растворов, определение значения критической концентрации мицеллообразования путем нахождения на графике точки перегиба.
Однако описанные в разных источниках результаты практического применения данного способа определения ККМ были противоречивы. Так, при изучении светопоглощения водных растворов Tритона Х-100 в диапазоне концентраций 0,0428-0,6838 мМ было установлено, что поглощение увеличивается немонотонно и характеризуется максимумом (λmax) при 277±1нм. Изучение спектров поглощения водных растворов Тритонов с различной степенью оксиэтилирования (Tритон X-114, Tритон X-100 и Tритон X-165) [Anand U., Jash C., Mukherjee S. Spectroscopic determination of Critical Micelle Concentration in aqueous and non-aqueous media using a non-invasive method // Journal of colloid and interface science. 2011. Vol. 364, №2. P. 400-406] показало, что поглощение монотонно увеличивается с концентрацией ПАВ и максимально при 274±1 нм для всех растворов. В обоих случаях не были зафиксированы изменения положения максимумов и форм спектров даже при высоких концентрациях ПАВ, что не позволило определить точку перегиба, а, следовательно, и ККМ.
Задачей заявляемого изобретения является разработка воспроизводимого и точного способа, позволяющего спектрофотометрически определять критическую концентрацию мицеллообразования полиоксиэтилированных алкилфенолов на начальном этапе формирования сферических мицелл.
Сущность заявляемого изобретения заключается в том, что в способе спектрофотометрического определения критической концентрации мицеллообразования полиоксиэтилированных алкилфенолов, включающем подготовку серии водных растворов НПАВ, регистрацию их спектров поглощения в диапазоне 230-300 нм, построение концентрационной зависимости спектральной характеристики кривых поглощения в виде графика, определение значения критической концентрации мицеллообразования путем нахождения на графике точки перегиба, серию водных растворов НПАВ подготавливают с шагом концентраций 0,02 мМ, обеспечивая выполнение закона Бугера-Ламберта-Бера в диапазоне их оптической плотности 0,1-1,2; регистрацию спектров поглощения водных растворов осуществляют с шагом сканирования 0,1 нм, после чего определяют положение максимума поглощения λmax, нм, которое использует для построения концентрационной зависимости, для определения точки перегиба на графике находят точки с постоянным значением λmax, нм, соединяя их прямой линией параллельный оси абсцисс, затем определяют точки с постоянно возрастающим значением λmax, нм, соединяя их прямой линией с тангенсом угла наклона больше нуля и коэффициентом детерминации R2 не менее 0,98, точку перегиба определяют как точку пересечения двух построенных прямых линий.
Технический результат заявляемого изобретения.
Такой технический прием как использование серии водных растворов НПАВ с шагом концентраций 0,02 мМ и регистрацией спектров поглощения через 0,1 нм позволяет получить воспроизводимые результаты для построения концентрационной зависимости в виде характерной формы кривой при определении ККМ у разных НПАВ по точке перегиба.
Специфика отбора точек для построения наклонной прямой, заключающаяся в определении положения λmax, нм и учете коэффициента детерминации R2, позволяет с высокой точностью определить точку перегиба, соответствующую ККМ.
Заявляемое изобретение поясняется с помощью примеров, которые визуализируются фиг.1-4. На фиг.1-4 изображено:
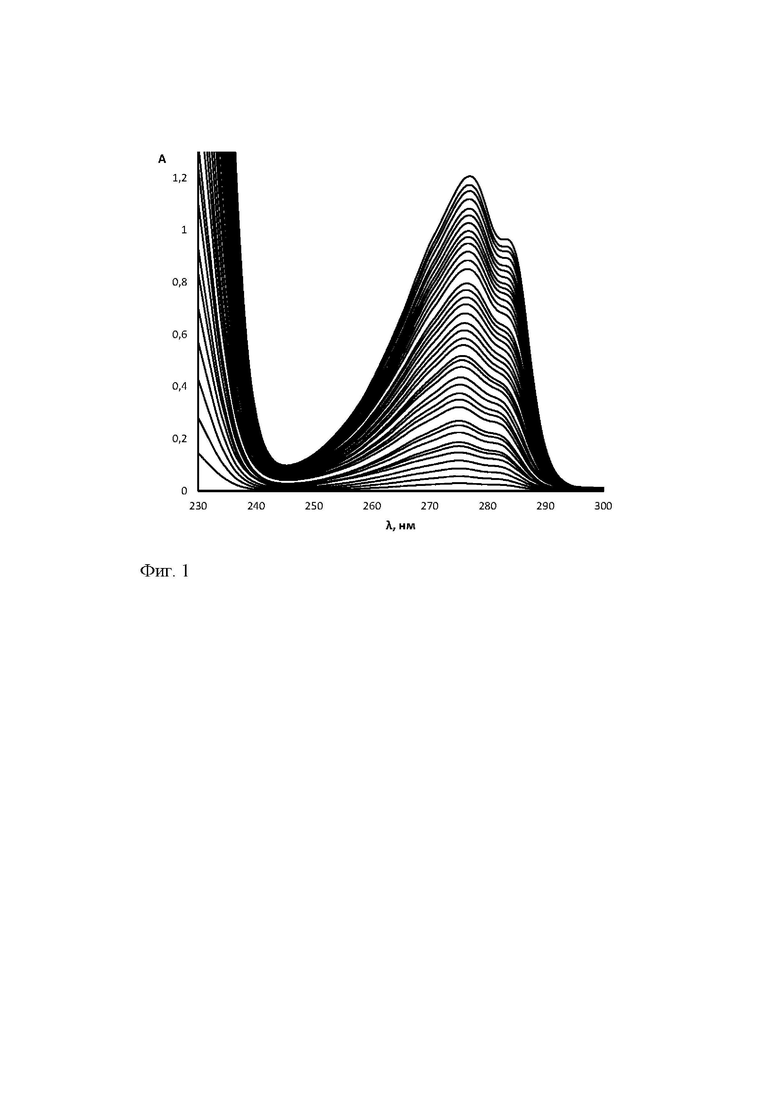
фиг.1 - спектры поглощения водных растворов ТХ-100 при концентрациях (0.02 - 0.80 мМ);
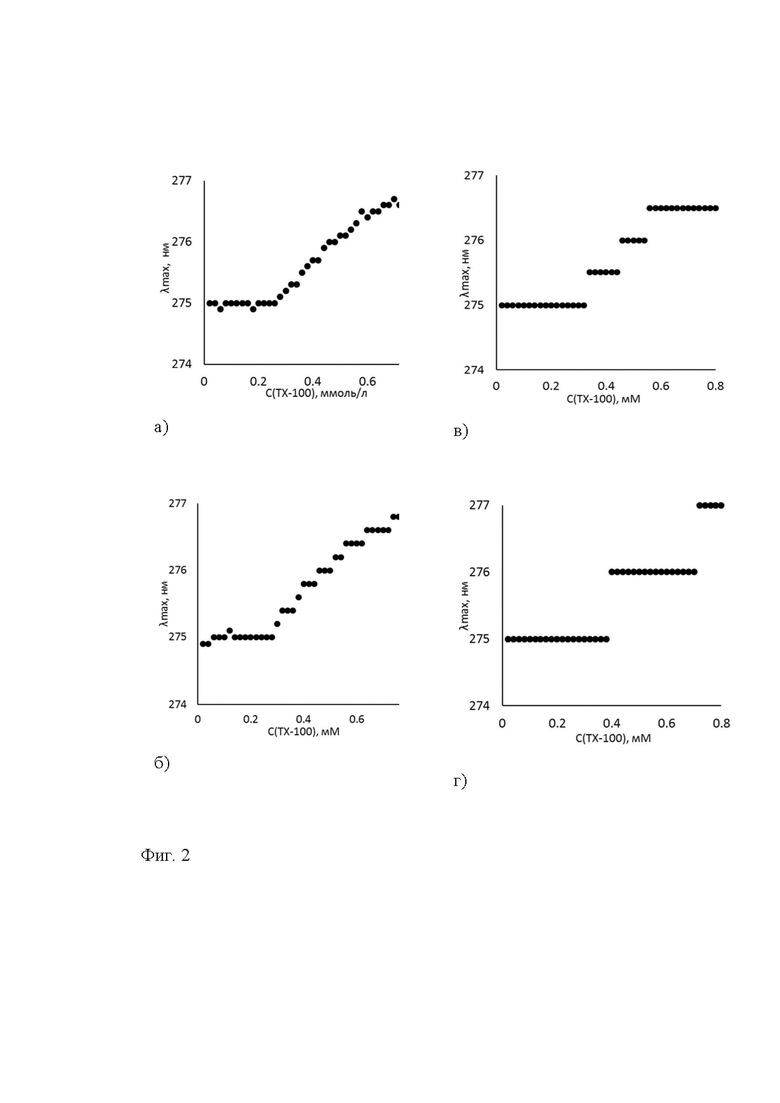
фиг.2 - положение максимума поглощения при различных шагах сканирования: а) 0,1 нм; б) 0,2 нм; в) 0.5 нм г) 1,0 нм;
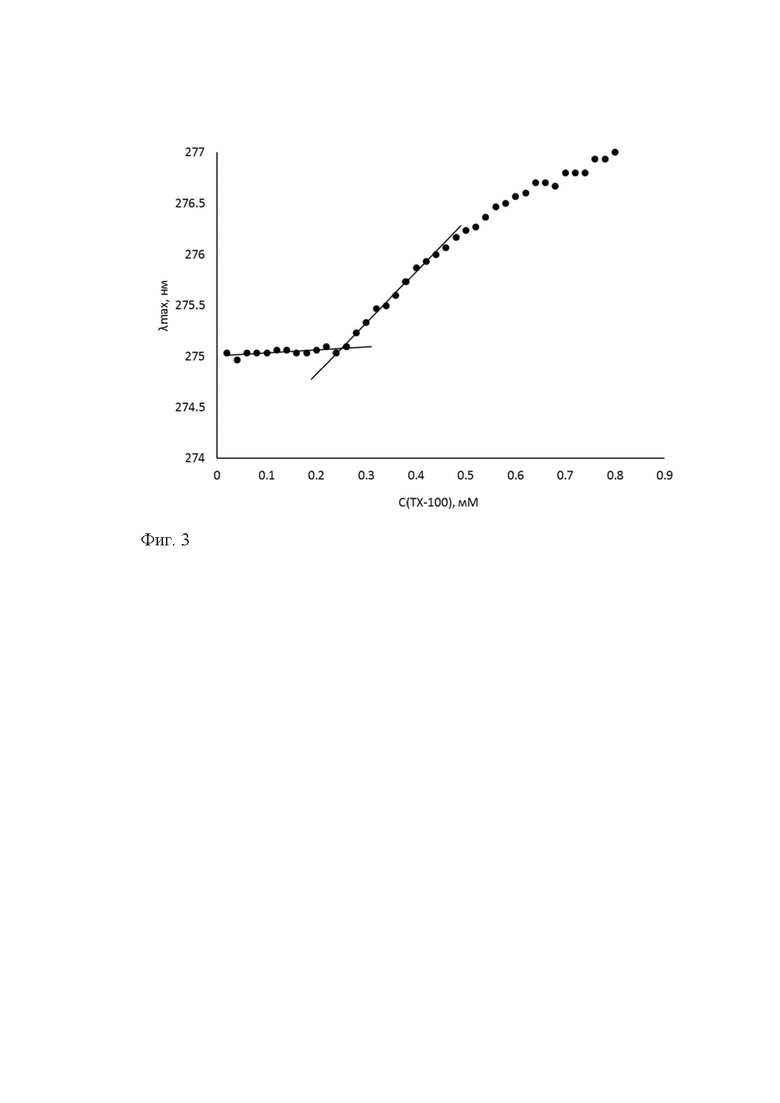
фиг.3 - зависимость положения максимума поглощения от концентрации ТХ-100 с шагом сканирования 0,1 нм;
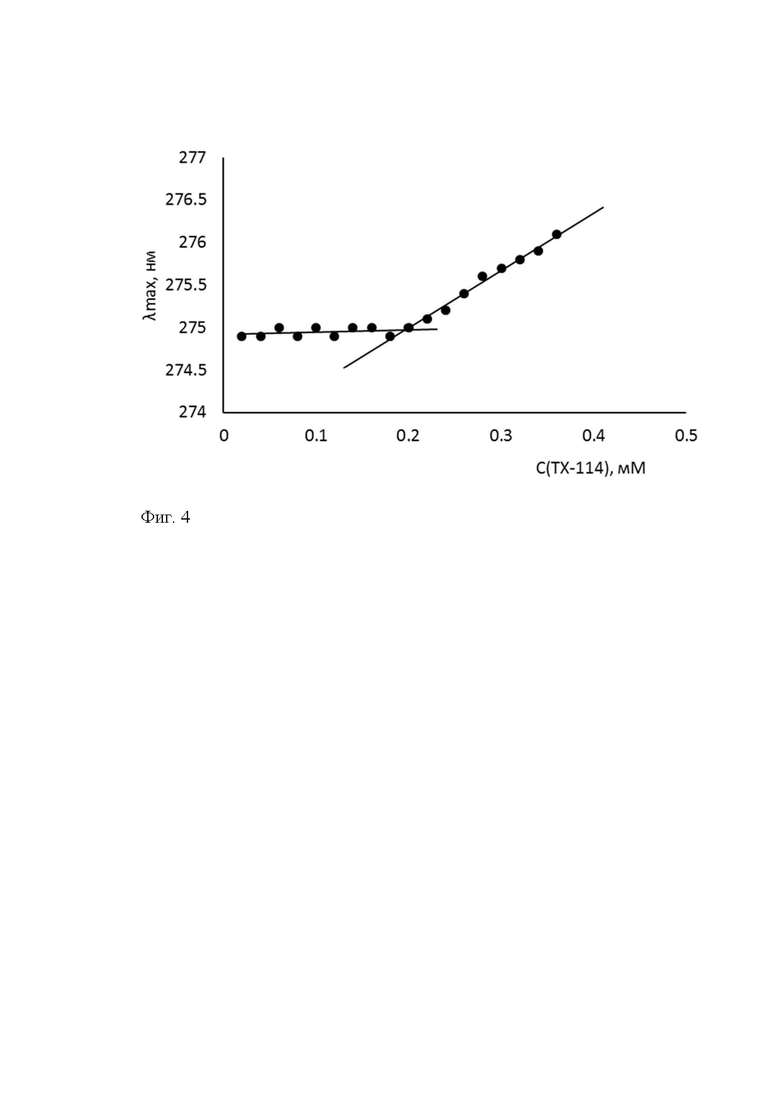
фиг.4 - зависимость положения максимума поглощения от концентрации ТХ-114 с шагом сканирования 0,1 нм.
Способ спектрофотометрического определения критической концентрации мицеллообразования полиоксиэтилированных алкилфенолов осуществляют следующим образом.
Предварительно готовят серию растворов НПАВ таким образом, чтобы интервал между концентрациями составлял не менее 0,02 мМ, обеспечивая выполнение закона Бугера-Ламберта-Бера в диапазоне их оптической плотности 0,1-1,2. Регистрируют спектры поглощения в диапазоне 230-300 нм на спектрофотометре, позволяющем проводить сканирование по длине волны с шагом сканирования 0,1 нм. Затем определяют положение максимума поглощения λmax, нм.
Для определения ККМ строят в виде графика концентрационную зависимость положения максимума поглощения λmax, нм от концентрации НПАВ в растворе. На графике в области низких концентраций определяют точки, параллельные оси абсцисс, соединяют их прямой линией, поскольку в этой области концентраций положение максимума λmax, нм не изменяется. Далее определяют точки с постоянно возрастающим значением λmax, нм, которые лежат на прямой линии с наклоном, причем тангенс угла наклона прямой должен быть больше нуля. Находят уравнение зависимости положения максимума поглощения λmax, нм от концентрации, которое должно иметь вид y=kx+b, где y- положение максимума поглощения λmax, нм, Х -концентрация НПАВ, выраженная в мМ, К- тангенс угла наклона прямой, b - свободный член. Коэффициент детерминации R2 должен быть не менее 0,98. Определяют значения критической концентрации мицеллообразования путем нахождения на графике точки пересечения двух построенных прямых линий, соответствующей точке перегиба.
Примеры.
Для подтверждения работоспособности заявляемого способа нами была определена ККМ водных растворов оксиэтилированных алкилфенолов Тритон Х-100 (ТХ-100) («Carl Roth», Германия) и Тритон Х-114 (ТХ-114) («PanReac AppliChem», Германия) квалификации «extra pure». Исходные растворы с концентрацией 1,0 10-3 моль/л готовили растворением точной навески НПАВ в бидистилированной воде («УПВА-5», Россия; электропроводность 2,33 мкСм/см, «АНИОН 4152», Россия). Взвешивание проводили на аналитических весах «HR-200» («A&D», Япония, ± 0,0001г). Концентрация растворов подбиралась таким образом, чтобы оптическая плотность не превышала 1,2. Линейный характер зависимости оптической плотности растворов (А) от концентрации ПАВ (С, мМ) свидетельствовало о соблюдении основного закона светопоглощения. Достоверность линейной связи А = a + bС подтверждали методом корреляционного анализа [Smagunova A.N., Karpukova O.M. Methods of mathematical statistics in analytical chemistry: Uchebnoe posobie. Rostov-na -Donu: Feniks, 2012. 346 p]. Для исследований готовили 40 рабочих растворов ТХ-100 в диапазоне концентраций 0,02 мМ - 0,80 мМ и 20 рабочих растворов ТХ-114 с концентрациями от 0,02 мМ до 0,40 мМ разбавлением исходных растворов бидистиллированной водой, интервал между концентрациями 0,02 мМ. Использовали дозаторы («Ленпипет», Россия) и предварительно откалиброванные мерные колбы вместимостью 10,0 мл. Перед спектрофотометрированием рабочие растворы термостатировали при 25°С в течении 30 минут (термостат суховоздушный ТСО-1/80 СПУ, Россия). Электронные спектры поглощения регистрировали на двухлучевом сканирующем спектрофотометре SHIMADZU UV - 1800 (Япония) в режиме «спектральный». Для измерения использовали кварцевые кюветы с l=1 см. Воспроизводимость по шкале длин волн ±0,1 нм.
Как видно из представленных на фиг.1 спектральных кривых в диапазоне длин волн 230-300 нм оптическая плотность растворов ТХ-100 с концентрациями от 0,02 до 0,80 мМ не превышала 1,2, а возрастание концентрации сопровождалось монотонным увеличением поглощения. Было установлено, что растворы с концентрациями от 0,02 до 0,20 мМ имели максимум поглощения λmax 275 нм и плечо 278-280 нм. При увеличении концентрации до 0,80 мМ происходил батохромный сдвиг λmax до 2 нм.
Оптическая плотность растворов ТХ-114 с концентрациями от 0,02 до 0,30 мМ в диапазоне длин волн 230-300 нм не превышала 0,5, возрастание концентрации также сопровождалось монотонным увеличением поглощения. Более концентрированные растворы становились мутными вследствие более низкой растворимости НПАВ. Формы электронных спектров поглощения растворов ТХ-100 и ТХ-114 идентичны. Было установлено, что растворы с концентрациями от 0,02 до 0,18 мМ имеют максимум поглощения λmax 275 нм и плечо 278-280 нм. Увеличение концентрации до 0,30 мМ сопровождалось батохромным сдвигом λmax, не превышающим 1,5 нм.
Проверку выполнимости закона поглощения проводили при 275 и 277 нм для растворов ТХ-100 с концентрациями 0,02-0,80 мМ, при 275 и 276 нм для растворов ТХ-114 с концентрациями 0,02-0,30 мМ. Уравнения зависимостей оптической плотности растворов от концентрации НПАВ в растворе прямолинейны, значения коэффициента детерминации R2 больше 0,98. Уравнения зависимостей для ТХ-100: А(275) = 1,4796С (R2 = 0, 9995), А(277) = 1,5438С (R2 = 0, 9995). Уравнения зависимостей для ТХ-114: А(275) = 1,6382С (R2 = 0, 9961), А(276) = 1,6457С (R2 = 0, 9952). Полученные зависимости подтвердили выполнение основного закона светопоглощения.
Поскольку батохромные сдвиги в спектрах поглощения свидетельствовали о снижении энергии электронного перехода [Сильверстейн Р., Басслер Г., Морил Т. Спектрометрическая идентификация органических соединений - М.: Мир, 1977. 590 с.], то смещение λmax можно было объяснить образованием более энергетически выгодных агрегатов - мицелл. Для 40 растворов с концентрациями от 0,02 до 0,80 мМ были зарегистрированы спектры поглощения в диапазоне 230-300 нм при шагах сканирования 0,1; 0,2; 0,5 и 1,0 нм и определены λmax. Установлено, что в области низких концентраций (до 0,20 мМ) при всех шагах сканирования λmax оставалась неизменной и соответствовала 275 нм, а концентрация, при которой наблюдали изменение положения λmax зависела от шага сканирования. Построены зависимости λmax (у) от концентрации ТХ-100 (С, мМ) при всех шагах сканирования (фиг.2).
Как видно из фиг. 2, на концентрационных зависимостях спектральной характеристики λmax наблюдался излом при различных концентрациях, соответствующих началу батохромного сдвига λmax, которые соответственно равны: 0,20 мМ при 0,1 нм, 0,22 мМ при 0,2 нм, 0,35 мМ при 0,5 нм и 0,38 мМ при 1,0 нм. Установленные различия приводили к искажению результата определения ККМ. Это подтвердило, что определение ККМ необходимо проводить при шаге сканирования 0,1 нм.
Для определения ККМ водных растворов ТХ-100 приготовлена серия растворов в диапазоне концентраций 0,02-0,80 мМ, зарегистрированы спектры поглощения с шагом сканирования 0,1 нм, определено положение λmax для всех концентраций. Была построена зависимость λmax (у) от концентрации ТХ-100 (С, мМ) (фиг.3). На полученном графике выделяли три участка, причем в области концентрации 0,22 - 0,24 мМ кривая имела излом. Первый участок в диапазоне концентраций 0,02 - 0,22 мМ представлял собой прямую линию, параллельную оси абсцисс. Длина волны максимума поглощения водных растворов практически постоянна и равна 275,0±0,1 нм. В этой области оптическая плотность растворов прямо пропорциональна концентрации и не превышает 0,4. Второй участок, соответствующий диапазону концентраций 0,24 - 0,44 мМ, характеризовался монотонным сдвигом максимума до 276 нм, причем увеличение концентрации на каждые 0,02 мМ приводило к сдвигу полосы на 0,1 нм. Оптическая плотность растворов монотонно увеличивалась и не превышала 0,65. Участок также был прямолинеен, но имел определенный наклон. В результате оценки зависимости λmax от С(ТХ-100) было получено уравнение этого участка: y=5,00С+273,83 (R2 = 0,994). Третий участок кривой, соответствующий растворам с концентрацией 0,46 - 0,80 мМ, характеризовался более пологим наклоном, «скорость» батохромного сдвига уменьшалась: сдвиг на 1,0 нм происходил при увеличении концентрации на 0,34 мМ. Оптическая плотность наиболее концентрированного раствора не превышала 1,2. На этом участке прямолинейная зависимость отсутствовала, коэффициент детерминации (R2) меньше 0,98. Уравнение полученной зависимости имело вид y=2,57С+274,96 (R2 = 0,970).
Аналогичная зависимость была построена для растворов ТХ-114 с концентрациями 0,02-0,30 мМ. Также были установлены два прямолинейных участка и наблюдали характерный излом в области концентраций 0,16-0,20 мМ (фиг.4). В области низких концентраций - прямая, параллельная оси абсцисс, соответствующая значению λmax 274,95±0,04 нм, при повышении концентрации - батохромные сдвиги полосы поглощения до 276,40±0,25 нм, которые описываются прямой линией, соответствующей уравнению y=7,33С+273,41 (R2 = 0,994).
В обоих случаях на графике были построены прямые линии, соответствующие первому и второму участку. Искомую величину ККМ определяли по точке перегиба, которая соответствовала точке пересечения двух ранее построенных прямых линий. Рассчитанное значение ККМ составило для ТХ-100 - (0,24±0,02) мМ, а для ТХ-114 - (0,20±0,01) мМ.
Результаты согласуются со значениями ККМ ТХ-100 и ТХ-114, полученными другими методами. Таким образом работоспособность способа спектрофотометрического определения критической концентрации мицеллообразования полиоксиэтилированных алкилфенолов была доказана.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения критической концентрации мицеллообразования поверхностно-активных веществ, применяемых при электроосаждении | 1990 |
|
SU1719970A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КРИТИЧЕСКОЙ КОНЦЕНТРАЦИИ МИЦЕЛЛООБРАЗОВАНИЯ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ | 2020 |
|
RU2743736C1 |
| Способ измерения параметров фазового перехода жидкость-жидкость и мицеллообразования | 2020 |
|
RU2730433C1 |
| СПОСОБ ОБНАРУЖЕНИЯ ЛИЗИНА В СМЕСИ α-АМИНОКИСЛОТ | 2011 |
|
RU2484460C2 |
| Способ разработки нефтяной залежи заводнением | 1989 |
|
SU1645473A1 |
| Устройство для бесконтактного измерения критической концентрации мицеллообразования поверхностно-активных веществ | 2024 |
|
RU2837802C1 |
| Способ количественного определения суммы флавоноидов в траве аврана лекарственного | 2023 |
|
RU2829551C1 |
| Способ измерения параметров фазового перехода жидкость-жидкость в водных растворах амфифилов | 2017 |
|
RU2674556C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ НОВОКАИНА | 2019 |
|
RU2715997C1 |
| Способ измерения параметров фазового перехода жидкость-жидкость | 2019 |
|
RU2720399C1 |
Изобретение относится к области измерительной техники и касается способа спектрофотометрического определения критической концентрации мицеллообразования полиоксиэтилированных алкилфенолов. Способ включает подготовку серии водных растворов НПАВ, регистрацию их спектров поглощения в диапазоне 230-300 нм, построение концентрационной зависимости спектральной характеристики кривых поглощения в виде графика, определение значения критической концентрации мицеллообразования путем нахождения на графике точки перегиба. Серию водных растворов подготавливают с шагом концентраций 0,02 мМ. Регистрацию спектров поглощения осуществляют с шагом сканирования 0,1 нм. Далее определяют положение максимума поглощения λmax, которое используют для построения концентрационной зависимости. Для определения точки перегиба на графике находят точки с постоянным значением λmax, соединяя их прямой линией, параллельной оси абсцисс, затем определяют точки с постоянно возрастающим значением λmax, нм, соединяя их прямой линией. Точку перегиба определяют как точку пересечения двух построенных прямых линий. Технический результат заключается в повышении точности измерения критической концентрации мицеллообразования. 4 ил.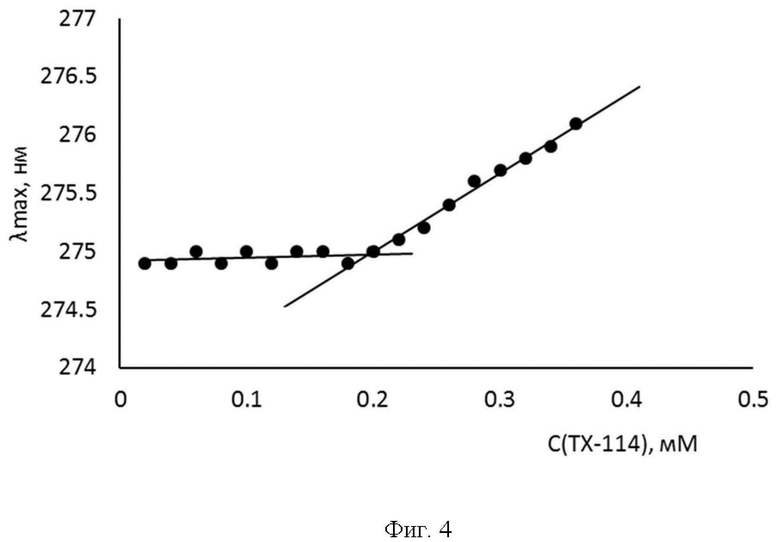
Способ спектрофотометрического определения критической концентрации мицеллообразования полиоксиэтилированных алкилфенолов, включающий подготовку серии водных растворов НПАВ, регистрацию их спектров поглощения в диапазоне 230-300 нм, построение концентрационной зависимости спектральной характеристики кривых поглощения в виде графика, определение значения критической концентрации мицеллообразования путем нахождения на графике точки перегиба, отличающийся тем, что серию водных растворов НПАВ подготавливают с шагом концентраций 0,02 мМ, обеспечивая выполнение закона Бугера-Ламберта-Бера в диапазоне их оптической плотности 0,1-1,2; регистрацию спектров поглощения водных растворов осуществляют с шагом сканирования 0,1 нм, после чего определяют положение максимума поглощения λmax, нм, которое использует для построения концентрационной зависимости, для определения точки перегиба на графике находят точки с постоянным значением λmax, нм, соединяя их прямой линией, параллельной оси абсцисс, затем определяют точки с постоянно возрастающим значением λmax, нм, соединяя их прямой линией с тангенсом угла наклона больше нуля и коэффициентом корреляции R2 не менее 0,98, точку перегиба определяют как точку пересечения двух построенных прямых линий.
| Anand U., Jash C., Mukherjee S | |||
| "Spectroscopic determination of Critical Micelle Concentration in aqueous and non-aqueous media using a non-invasive method", JOURNAL OF COLLOID AND INTERFACE SCIENCE, т | |||
| Способ получения мыла | 1920 |
|
SU364A1 |
| Способ фотографической записи звуковых колебаний | 1922 |
|
SU400A1 |
| Способ определения критической концентрации мицеллообразования поверхностно-активных веществ, применяемых при электроосаждении | 1990 |
|
SU1719970A1 |
| CN 105115929 B, 03.10.2017 | |||
| WO 2019080076 A1, 02.05.2019. | |||
Авторы
Даты
2024-10-07—Публикация
2024-05-17—Подача