Изобретение относится к медицине, в частности к доставке гемостатического средства, а именно к способу для доставки гемостатического средства в организм при продолжающемся внутриполостном кровотечении.
На сегодняшний день существует большое количество методики и приспособлений для доставки гемостатических средств, но не известны быстрые, эффективные и надежные устройства и способы для доставки гемостатического средства в организм при продолжающемся внутриполостном кровотечении.
Известен безыгольный шприц с инжектором из составных элементов (Безыгольный шприц с инжектором из составных элементов: патент RU 2221596, Российская Федерация, заявка RU 2002103864, заявл. 2000.06.30, опубл. 2004.01.20). Шприц содержит инжектор, имеющий по меньшей мере одно сопло впрыскивания, а с другой стороны - перегородку, перемещаемую под воздействием толкающей системы, создающей давление и обеспечивающей выталкивание лекарственного препарата через инжектор, расположенный со стороны нижнего торца указанного шприца. Чтобы изготовить сопла в толстостенном материале инжектора и иметь возможность контролировать расстояние (дальность), на котором поддерживается непрерывность струи, инжектор содержит по меньшей мере два элемента, на соприкасающихся поверхностях которых выполнена по меньшей мере одна канавка, образующая сопло впрыскивания в сборке упомянутых выше элементов.
Использование данного шприца для доставки гемостатического средства средства в организм при продолжающемся внутриполостном кровотечении представляется затруднительным из-за отсутствия возможности использования сменного картриджа и стыковки с катетером.
Известен способ остановки кровотечения при травмах печени (Способ остановки кровотечения при травмах печени: патент RU 2421159, Российская Федерация, заявка RU 2009123811, заявл. 22.06.2009, опубл. 20.06.2011), в ходе осуществления которого криоаппликатор наполняли жидким азотом, контактную поверхность его устанавливали на рану паренхимы печени, для предупреждения примораживания криоаппликатора к ткани печени проводили 2-3 круговых движения криоаппликатором. Для достижения окончательного гемо- и желчестаза проводили 3 цикла воздействия криоапликатором, продолжительность одного цикла составляла 1 минуту.
К недостаткам такого способа можно отнести необходимость использования жидкого азота и высокий риск повреждения тканей вследствие переохлаждения внутренних органом.
Наиболее близким к заявляемому способу является способ лечения массивных диффузных внутриполостных кровотечений (Способ лечения массивных диффузных внутриполостных кровотечений: патент RU 2246272, Российская Федерация, заявка RU 2009123811, заявл. 22.06.2009, опубл. 20.06.2011). Способ включает использование тампона, между слоями которого, вблизи очага кровотечения, расположены инжекторные дренажи и салфетка, обладающая повышенными сорбирующими свойствами. Тампон окружен биологически интактной полиэтиленовой оболочкой.
Недостатком данного способа является относительно низкая эффективность, обусловленная использованием сорбирующего тампона и расположением инжекторных дренажей для доставки гемостатического средства, которые при такой конструкции не могут обеспечить качественную и быструю доставку гемостатического средства.
Наиболее близким к заявляемому устройству является инжектор для доставки гемостатического порошка (Инжектор для доставки гемостатического порошка: патент CN 104958829, Китайская Народная Республика, заявка CN 201510437229, заявл. - 22.07.2015, опубл. 07.10.2015), состоящий из основного и вспомогательного корпуса (картридж). В основном корпусе эжектора расположен газовый баллон, нижняя часть основного корпуса эжектора снабжена торцевой крышкой, а отверстие газового баллона снабжено воздушным клапаном. Гильза для смешивания газа и порошка расположена в дополнительном эжектора, полость для смешивания газа и порошка расположена в гильзе для смешивания газа и порошка, на верхнем конце рукава для смешивания газа и порошка находится флакон с лекарством, лекарство выходное отверстие флакона с лекарством сообщается с полостью для смешивания газа и порошка, нижний конец рукава для смешивания газа и порошка выходит из вспомогательном корпусе, а нижний конец снабжен соплом. В соединительном корпусе расположена газовая трубка, один конец газовой трубки соединен с воздушным клапаном, а другой конец газовой трубки сообщается с полостью смешивания газа и порошка.
Недостатком данного устройство является отсутствие возможности использования для доставки геля и относительно низкая эффективность из-за отсутствия элементов для стыковки с катетером. Кроме того, данное устройство является достаточно сложным технически и предусматривает использования газового баллона. Такое устройство является ненадежным и требует регулярного технического обслуживания.
Технической проблемой является необходимость разработки эффективных способа и устройства доставки гемостатического средства в виде геля, лишенных вышеприведенных недостатков.
Технический результат состоит в обеспечении эффективной и быстрой доставки местного биоразлагаемого гемостатического средства (далее - «МБГС») через прокол брюшной стенки. Дополнительный технический результат заключается в упрощении устройства и способа доставки гемостатического средства, а также в повышении надежности.
Технический результат достигается тем, что в устройстве доставки гемостатического средства, включающем инжектор и соединенный с ним сменный картридж, предназначенный для заполнения гемостатическим средством, причем основной корпус включает рукоятку и спусковой механизм, согласно изобретению инжектор содержит шток, а также пружину и стопор прямого хода, пружину и стопор обратного хода и рукоятку отвода поршня, причем шток инжектора выполнен с возможностью соединения к катетером.
Технический результат также достигается тем, что в способе доставки гемостатического средства, в ходе которого в полость очага кровотечения устанавливают инжектор для подведения гемостатического средства в области кровотечения, накладывают асептическую повязку, согласно изобретению используют вышеописанное устройство, при этом выполняют продольный разрез кожи и подкожной клетчатки с помощью стилета, после чего стилет извлекают и устанавливают катетер, который соединяют с устройством для доставки и вводят гемостатический гель, после чего катетер отсоединяют от устройства для доставки, а затем последовательно извлекают устройство для доставки с инжектором и катетер, после чего рану ушивают.
В наиболее предпочтительном варианте реализации устройства шток выполнен из алюминия, стопоры и пружины прямого и обратного хода выполнены из стали, а рукоятка отвода поршня выполнена из ABS-пластика или полиэтилентерефталата. Такая конструкция является наиболее надежной и из-за своей простоты и удобной формы она позволяет быстро и просто ввести гемостатический гель во внутрибрюшное пространство.
В наиболее предпочтительном варианте реализации способа в качестве геля используют композицию со следующим составом, мас. %:
Такая методика обеспечивает наиболее простую и эффективную доставку гемостатического средства при продолжающемся внутриполостном кровотечении.
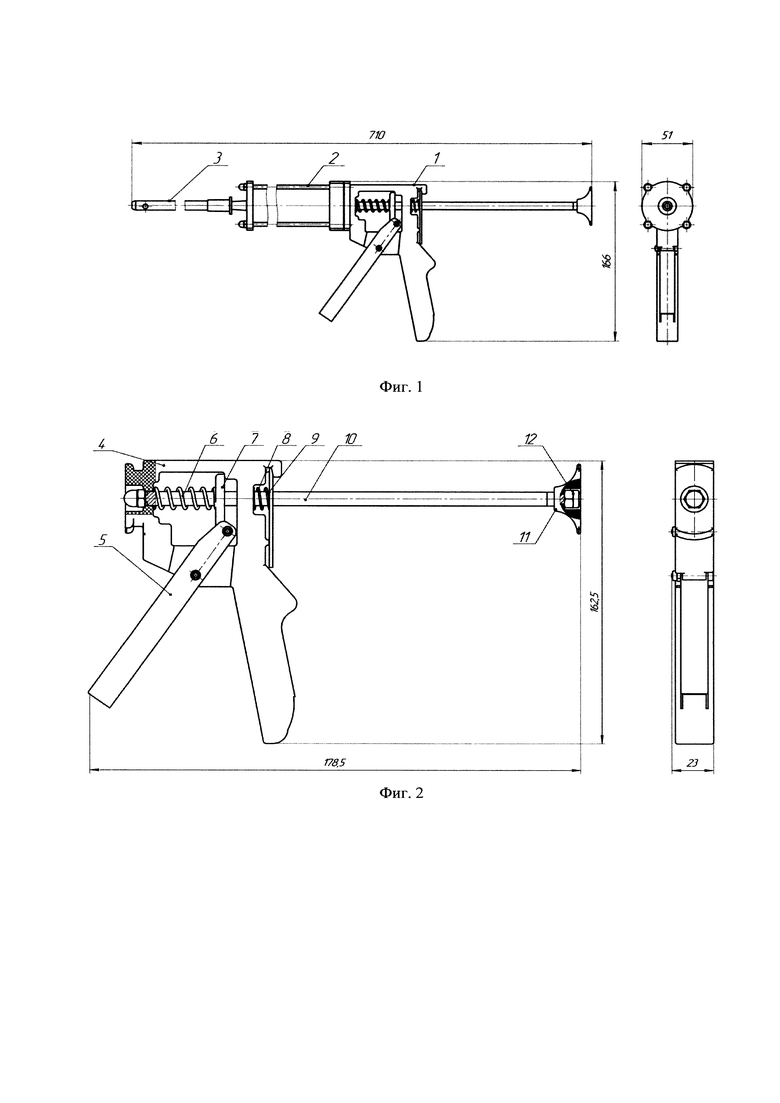
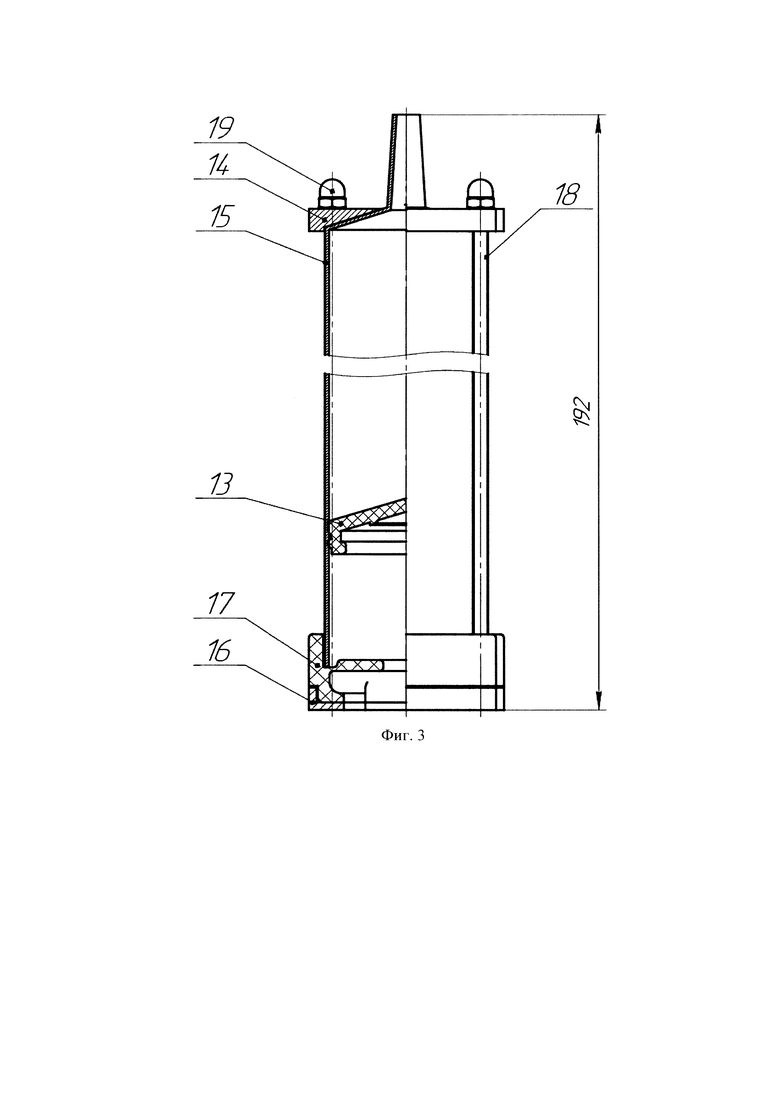
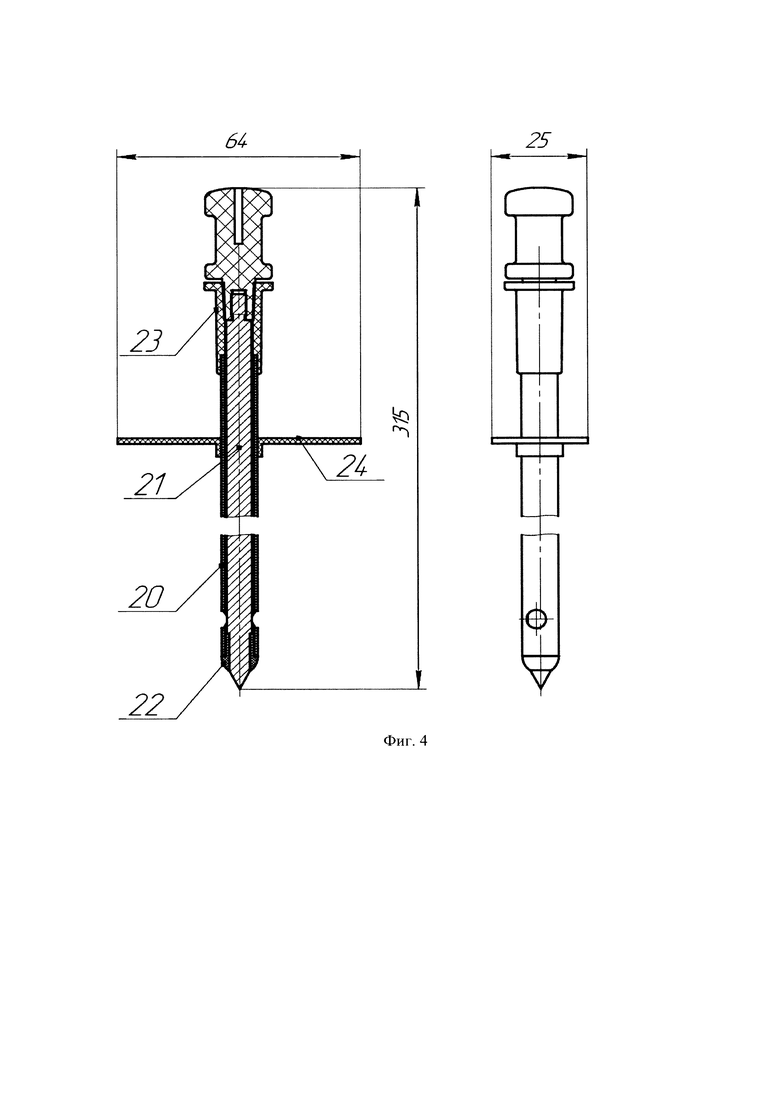
Заявляемое изобретение поясняется чертежами, где на фиг. 1 представлено устройство для доставки гемостатического средства в общем виде, на фиг. 2 представлен инжектор, на фиг. 3 картридж, а на фиг. 4 троакар со стилетом.
Устройство для доставки гемостатического средства содержит инжектор 1, картридж 2 и троакар со стилетом 3 (троакар-катетер).
Инжектор 1 содержит корпус 4, рукоятку подачи 5 (спусковой механизм), пружину 6 прямого хода, стопор 7 прямого хода, пружину 8 обратного хода, стопор 9 обратного хода, шток 10, рукоятку 11 отвода поршня и гайку 12.
Картридж 2 содержит поршень 13, вкладыш 14 контейнера передний, колбу 15 контейнера, крышку 16 контейнера заднюю, вкладыш 17 контейнера задний, шпильку 18 контейнера МБГС и гайку 19.
Троакар 3 содержит гильзу троакара 20, стилет 21, а также наконечник 22 стилета, коннектор 23 и планку 24 крепежную.
Сборку данных частей (1, 2, 3) осуществляют после введения троакара 3 во внутрибрюшную полость. Причем для этого от троакара отсоединяют стилет 21 и оставляют только коннектор 23 и гильзу 20 троакара. Картридж 2 с помощью вкладыша 17 подсоединяют к штоку 10 инжектора. После чего к передней части картриджа 2 подсоединяют троакар 3 через коннектор 23. Далее путем нажатия на рукоятку подачи 5 шток давит на поршень 13, который перемещает гель, находящийся внутри картриджа 2 в сторону троакара 3.
Заявляемый способ осуществляют следующим образом.
При оказании помощи пострадавшему с продолжающимся внутрибрюшным кровотечением ниже пупка, в случае переломов костей - выше пупка, по средней линии живота выполняют местную инфильтрационную анестезию на всю толщину передней брюшной стенки. Затем делают продольный разрез кожи и подкожной клетчатки длиной до (1,5-2) см. Для исключения ложноположительного результата на кровоточащие сосуды накладывают зажимы. Апоневроз белой линии живота захватывают однозубым крючком или бельевыми цапками. Передняя брюшная стенка левой рукой оперирующего оттягивается краниально и вверх. Затем перпендикулярно приподнятой и натянутой брюшной стенке (примерно 45 градусов к поверхности стола) сразу под крючком осторожными вращательными движениями троакара 3 последовательно прокалывают апоневроз и париетальная брюшина. Затем стилет 21 извлекают, в брюшную полость через гильзу 20 троакара вводят прозрачный катетер (не показана на чертежах. Появление в катетере крови является признаком продолжающегося внутрибрюшного кровотечения. Затем катетер проводят по гильзе 20 троакара в правое подреберье.
В корпус специального средства доставки МБГС устанавливают емкость с гемостатическим гелем (сменный картридж 2 с внутренним поршнем 13). Катетер, введенный в брюшную полость, соединяют со сменным картриджем 2 через коннектор 23. Десятью нажатиями на рукоятку 5 средства доставки в брюшную полость вводят МБГС. Катетер, введенный в брюшную полость, отсоединяют устройства для доставки.
После введения гемостатического средства катетер удаляют, операционная рана послойно ушивается отдельными узловыми швами. На область зашитой раны накладывают асептическую повязку (наклейка).
Рекомендовано наложение бандажа брюшной полости для улучшения эффективности гемостаза. Для этого необходимо вскрыть упаковку с компрессионной повязкой и придерживая свободный край повязки наложить циркулярную повязку на уровне мезо- и гипогастральной области живота.
В случае наличия индикатора компрессии на бандажной повязке, растянуть эластическое полотно повязки таким образом, чтобы индикатор компрессии приобрел форму в соответствии с инструкцией по применению данной повязки.
При необходимости смены картриджа 2 с МБГС (для большей дозировки) вместо удаления катетера его оставляют введенным в брюшную полость и отсоединяют от устройства для доставки. Производят смену картриджа 2 с МБГС и снова катетер соединяют устройством для доставки. После завершают процедуру аналогично вышеприведенной методике.
Заявляемое изобретение поясняется примерами.
Пример 1. Проверка скорости введения МБГС.
Проверку скорости введения средств доставки МБГС осуществляли с использованием мерного цилиндра ГОСТ 1770-74. Для этого заполнили картридж МБГС при температуре (20±2)°С, вставили его в инжектор и присоединили к нему катетер. Включили секундомер и нажать несколько раз на рукоять инжектора. Измерили количество МБГС, вытесненного в мерный цилиндр. Процедуру повторили несколько раз. Заполнить протокол измерений и вычислили среднюю скорость введения МБГС в мл/сек.
Средняя скорость у заявляемого устройства составила 13 мл/сек.
Пример 2. Проверка надежности соединения катетера с картриджем.
Проверку прочности соединения катетера с картриджем проводили на разрывных машинах следующим образом: картридж крепили в верхнем зажиме машины, в нижнем - катетер дренажный. Скорость перемещения зажимов составила 50 мм/мин. В начале эксперимента включили привод машины и следили за плавным увеличением нагрузки по шкале прибора.
Соединения не были разрушены в течение 15 с при нагрузке 20 Н и, соответственно, их посчитали выдержавшими испытания.
Пример 3. Оценка эффективности заявляемых способа и устройства на модели кровотечения из раны печени крупного лабораторного животного.
Исследования проводились в сериях острых и под острых экспериментов:
остром - моделирование внутрибрюшного кровотечения из раны печени у свиней;
подостром - оценка биосовместимости и биоразлагаемой способности МБГС при их внутрибрюшном использовании у кроликов.
Распределение крупных лабораторных животных по группам:
Группа №1 (Контроль 1), n=3. «Группа с внутриполостным кровотечением (3 степень интенсивности по шкале VIBe Scale) с тампонадой печени салфетками без использования МБГС»
Группа №2 (Контроль 2), n=3. «Группа с внутриполостным кровотечением (3 степень интенсивности по шкале VIBe Scale) без использования МБГС»
Группа №3 (Опыт 1), n=3. «Группа с внутриполостным кровотечением и использованием МБГС (3 степень интенсивности по шкале VIBe Scale) при тампонаде раны печени»
Группа №4 (Опыт 2), n=3. «Группа с внутриполостным кровотечением и использованием МБГС (3 степень интенсивности по шкале VIBe Scale), введенного в брюшную полость при помощи образца средства доставки».
Распределение крупных кроликов по группам представлено в таблице 1.
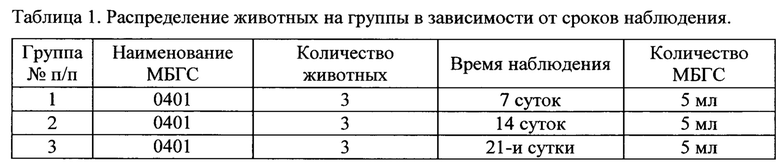
Избранный дизайн исследования позволил оценить гемостатическую эффективность представленных вариантов МБГС. В 3-х наблюдениях при использовании средства доставки МБГС в брюшную полость и в 3-х случаях при использовании МБГС с тампонадой брюшной полости перевязочным материалом.
В день операции перед транспортировкой из вивария в экспериментальную операционную для индукции анестезии, а также в ходе эксперимента для поддержания состояния наркоза внутримышечно вводилось 5 мг/кг массы тела тилетамина и золазепама (Zoletil® 100). Животное фиксировали на операционном столе в положении на спине с разведенными в стороны конечностями, после чего выполняли интубацию трахеи интубационной трубкой №7. В течение всего эксперимента проводилась искусственная вентиляция легких аппаратом «Villa» (Япония), в режиме перемежающейся вентиляции с положительным давлением, частотой от 12 до 15 вдохов в минуту с ингаляцией 100% кислорода. На вводном наркозе используется 5% от объема, а для поддержания анестезии - от 2 до 3% от объема изофлурана.
В правой паховой области под УЗИ навигацией выполняли катетеризацию бедренной артерии и бедренной вены по Сельдингеру с установкой интродьюсеров 6Fr для инвазивного мониторинга артериального давления и для проведения инфузионной терапии. В левой паховой области под УЗИ навигацией выполняли катетеризацию левой бедренной артерии по Сельдингеру с установкой интродьюсера 6Fr для выполнения дозированной кровопотери.
В условиях операционной после фиксации исходных показателей состояния животного выполнялась дозированная кровопотеря из левой бедренной артерии через установленный артериальный катетер. Объем кровопотери составлял 30% от ОЦК (1 и 3 группы) или 15% от ОЦК (2 и 4 группы) с учетом того, что весь объем крови составляет 7% от массы тела животного. Кровопотерю осуществляли аппаратом «Гемма» (ЗАО «ПЛАЗМОФИЛЬТР, Россия) в течение 30 минут. Затем производили инфузию в правую бедренную вену 1000 мл раствора Рингера лактата. После чего выполняли верхнесрединную лапаротомию, операционное поле отграничивали стерильным материалом, левая доля печени выводилась в рану. Затем на диафрагмальную поверхность печени накладывали пластмассовый ограничитель с квадратным отверстием в центре (размером 3×3 см) После регистрации исходных показателей состояния животного, согласного карте эксперимента, наносили рану печени. Выступающая часть печени в ограничителе отсекали скальпелем, в результате чего получалась рана печени (размер раны: 3×3 см., глубина раны: 5 мм) с интенсивностью кровотечения 3 степени по шкале VIBe Scale, по классификации AAST травма печени 2 степени.
Период наблюдения за животным с неконтролируемым внутрибрюшным кровотечением составлял не менее 10 минут. За это время лапаротомная рана послойно ушивалась. Выполняли УЗИ брюшной полости, подтверждалось наличие свободной жидкости (крови) в животе.
Затем производилось введение МБГС в брюшную полость. Выполняли лапароцентез в мезогастральной области по белой линии живота. Через полученный доступ вводился троакар-катетер средства доставки МБГС. Перед введением МБГС выполнялась рентгенография живота для оценки рентгеноконтрастности троакара-катетера. После чего 150 мл МБГС вводилось сначала в область печеночно-почечного пространства, затем 150 мл МБГС вводилось в область почечно-селезеночного пространства
Затем с целью уменьшения объема брюшной полости производили бинтование живота компрессионной повязкой.
В группе животных №2 введение МБГС не выполнялось, производили только бинтование брюшной полости. Период наблюдения составлял не менее 3 часов, в течение которого показатели жизнедеятельности животного записывали соответственно карте эксперимента. При снижении систолического артериального давления ниже 60 мм рт.ст. производилась инфузионная терапия раствором Рингера до достижения уровня систолического АД не ниже 90 мм рт.ст. По окончании периода наблюдения выполнялась лапаротомия, оценивалась интенсивность кровотечения, объем свободной крови и крови в свертках в брюшной полости, интенсивность кровотечения из раны печени, локализация геля, его адгезия к органам брюшной полости и ране печени. Оценивали макроскопическую реакцию брюшины, состояние кишечника, печени. Результаты заносились в индивидуальные карты наблюдения.
У животных групп №№1, 3 спустя 10 минут наблюдения после нанесения раны печени производилась ее тампонада стерильными марлевыми тампонами с использованием (группа №3) или без использования (группа №1) МБГС. Лапаротомная рана ушивалась. Период наблюдения в условиях наркоза составлял не менее 3 часов, в течение которых показатели жизнедеятельности животного регистрировали соответственно карте эксперимента. При снижении систолического артериального давления ниже 60 мм рт.ст. производили инфузионную терапию раствором Рингера лактата до достижения уровня систолического АД не ниже 90 мм рт.ст. По окончании периода наблюдения (3 часа) животное выводили из наркоза и помещали в виварий для дальнейшего наблюдения. Спустя сутки выполнялась лапаротомия, оценивали интенсивность кровотечения, объем свободной крови и крови в свертках в брюшной полости, осматривали и взвешивали тампоны, оставленные в брюшной полости. Определяли локализацию МБГС, его адгезию к органам брюшной полости и ране печени. Оценивали макроскопическую реакцию брюшины, состояние кишечника, печени. Результаты заносились в индивидуальные карты наблюдения. Затем путем передозировки наркоза животное выводилось из эксперимента.
В результате проведенного экспериментального исследования установлено, что представленные образцы МБГС обладают достаточной кровоостанавливающей способностью, которая позволяет остановить кровотечение из раны печени 3 степени по шкале Vibe Scale из раны печени. Средство доставки МБГС позволяет безопасно и быстро ввести необходимое количество МБГС в брюшную полость. Рентгеноконтрастная метка на троакаре катетере при необходимости позволяет позиционировать и доставить МБГС к предполагаемому источнику кровотечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гемостатическая композиция (варианты) | 2022 |
|
RU2826621C2 |
| Способ остановки внутреннего полостного кровотечения, саморасширяющаяся полиуретановая пена и устройство для осуществления способа | 2015 |
|
RU2607321C2 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОЙ НЕФРОСКОПИИ У СОБАК И КОШЕК | 2017 |
|
RU2668477C1 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОЙ РЕЗЕКЦИИ ПРЯМОЙ КИШКИ, ВКЛЮЧАЮЩИЙ ИЗВЛЕЧЕНИЕ РЕЗЕЦИРОВАННОГО УЧАСТКА ТОЛСТОЙ КИШКИ С ОПУХОЛЬЮ ПУТЕМ ВЫВОРОТА ПРЯМОЙ КИШКИ И ЭКСТРААБДОМИНАЛЬНУЮ РЕЗЕКЦИЮ | 2023 |
|
RU2824006C1 |
| СПОСОБ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ У ПАЦИЕНТОВ, ПОЛУЧАЮЩИХ ЛЕЧЕНИЕ ПЕРИТОНЕАЛЬНЫМ ДИАЛИЗОМ | 2015 |
|
RU2582456C1 |
| УСТРОЙСТВО ДЛЯ МОНИТОРИНГА БРЮШНОЙ ПОЛОСТИ | 2012 |
|
RU2542370C2 |
| СПОСОБ ОВАРИОГИСТЕРЭКТОМИИ У КОШЕК | 2015 |
|
RU2597991C1 |
| СПОСОБ БЕЗОПАСНОГО ДОСТУПА В БРЮШНУЮ ПОЛОСТЬ У ПАЦИЕНТОВ С ПОСЛЕОПЕРАЦИОННЫМИ ВНУТРИБРЮШНЫМИ ОСЛОЖНЕНИЯМИ | 2011 |
|
RU2472463C1 |
| СПОСОБ САНАЦИОННОЙ ВИДЕОАБСЦЕССОСКОПИИ В КОМПЛЕКСНОМ ЛЕЧЕНИИ ВНУТРИБРЮШНЫХ АБСЦЕССОВ И УСТРОЙСТВО ДЛЯ САНАЦИОННОЙ ВИДЕОАБСЦЕССОСКОПИИ | 2023 |
|
RU2824423C1 |
| СПОСОБ ЛОКАЛЬНОЙ ДЕСТРУКЦИИ ПЕРВИЧНЫХ И МЕТАСТАТИЧЕСКИХ НОВООБРАЗОВАНИЙ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ И ЗАБРЮШИННОГО ПРОСТРАНСТВА С ЛАПАРОСКОПИЧЕСКИМ ДОСТУПОМ | 2021 |
|
RU2770279C1 |
Изобретение относится к медицине, в частности к доставке гемостатического средства, а именно к способу доставки гемостатического средства в организм при продолжающемся внутриполостном кровотечении. Способ доставки гемостатического средства, в ходе которого в полость очага кровотечения устанавливают инжектор для подведения гемостатического средства в области кровотечения, накладывают асептическую повязку. При этом выполняют продольный разрез кожи и подкожной клетчатки с помощью стилета, после чего стилет извлекают и устанавливают катетер, который соединяют с устройством для доставки и вводят гемостатический гель, после чего катетер отсоединяют от устройства для доставки, а затем последовательно извлекают устройство для доставки с инжектором и катетер, после чего рану ушивают. Технический результат состоит в обеспечении эффективной и быстрой доставки местного биоразлагаемого гемостатического средства через прокол брюшной стенки. Дополнительный технический результат заключается в упрощении устройства и способа доставки гемостатического средства, а также в повышении надежности. 1 з.п. ф-лы, 4 ил., 1 табл.
1. Способ доставки гемостатического средства, в ходе которого в полость очага кровотечения устанавливают инжектор для подведения гемостатического средства в области кровотечения, накладывают асептическую повязку, отличающийся тем, что для его реализации используют устройство доставки гемостатического средства, включающее инжектор и соединенный с ним сменный картридж, предназначенный для заполнения гемостатическим средством, причем основной корпус включает рукоятку и спусковой механизм, отличающийся тем, что инжектор содержит шток, а также пружину и стопор прямого хода, пружину и стопор обратного хода и рукоятку отвода поршня, при этом выполняют продольный разрез кожи и подкожной клетчатки с помощью стилета, после чего стилет извлекают и устанавливают катетер, который соединяют с устройством для доставки и вводят гемостатический гель, после чего катетер отсоединяют от устройства для доставки, а затем последовательно извлекают устройство для доставки с инжектором и катетер, после чего рану ушивают.
2. Способ по п. 1, отличающийся тем, что в качестве геля используют композицию со следующим составом, мас.%:
| WO2018047157 A1, 15.03.2018 | |||
| US4338925 A, 13.07 | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| УСТРОЙСТВО для ОБСЛУЖИВАНИЯ ФУТЛЯРА ЧУГУННОЙ ЛЕТКИ ДОМЕННОЙ НЕЧИ | 0 |
|
SU190383A1 |
| СИСТЕМА И СПОСОБ ДЛЯ ХРАНЕНИЯ, ДОЗИРОВАНИЯ И ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2015 |
|
RU2673577C2 |
| Способ изготовления индивидуальных эргономических рукояток лапароскопических хирургических инструментов с использованием трехмерной печати | 2018 |
|
RU2706996C1 |
Авторы
Даты
2024-10-09—Публикация
2022-06-27—Подача