Область техники, к которой относится изобретение
Изобретение относится к медицине, фармацевтической промышленности, а именно к фармацевтической композиции на основе фабомотизола дигидрохлорида, обладающей анксиолитической активностью, и может быть использовано для производства лекарственного средства в виде таблеток.
Уровень техники
МНН Фабомотизол (5-этокси-2-[2-(морфолино)-этилтио] бензимидазола дигидрохлорид) 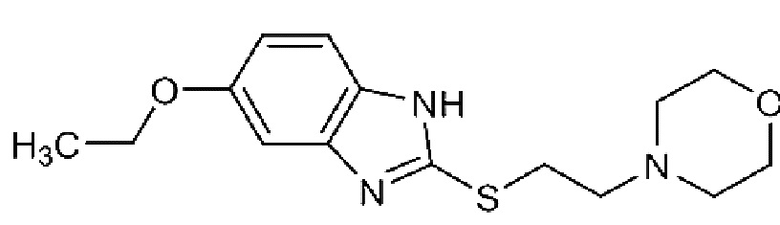 относится к группе транквилизаторов, действует на сигма-1-рецепторы в нервных клетках головного мозга, стабилизируя ГАМК/бензодиазепиновые рецепторы и восстанавливая их чувствительность к эндогенным медиаторам торможения. Кроме того, Фабомотизол повышает биоэнергетический потенциал нейронов и оказывает нейропротекторное действие (восстанавливает и защищает нервные клетки).
относится к группе транквилизаторов, действует на сигма-1-рецепторы в нервных клетках головного мозга, стабилизируя ГАМК/бензодиазепиновые рецепторы и восстанавливая их чувствительность к эндогенным медиаторам торможения. Кроме того, Фабомотизол повышает биоэнергетический потенциал нейронов и оказывает нейропротекторное действие (восстанавливает и защищает нервные клетки).
Из уровня техники известны несколько композиций на основе фабомотизола дигидрохлорида.
Патент RU2289403 (дата приоритета: 30.07.2004 г.) «Фармацевтическая композиция на основе Афобазола» раскрывает состав фармацевтической композиции для получения твердой лекарственной формы афобазола, включающая в качестве действующего вещества терапевтически эффективное количество афобазола, а в качестве вспомогательных веществ - лактозу, микрокристаллическую целлюлозу, крахмал, поливинилпирролидон, стеариновую кислоту или ее соль при следующем соотношении компонентов, г:
Частный вариант такой композиции был разрешен Минздравом России к медицинскому применению в качестве анксиолитического средства под названием Афобазол® (ЛП-000861, АО «Отисифарм»). Состав препарата Афобазол® на 1 таблетку следующий:
фабомотизола дигидрохлорида 10 мг;
крахмал картофельный 48 мг;
лактозы моногидрат 48,5 мг;
повидон среднемолекулярный (поливинилпирролидон среднемолекулярный, коллидон 25) 7 мг;
магния стеарат 1,5 мг.
Состав препарата Афобазол®, 10 мг, таблетки, является наиболее близким аналогом заявляемого технического решения.
Из патента RU2694837 (дата приоритета: 06.07.2017 г.) «Фармацевтическая композиция пролонгированного действия на основе 5-этокси-2-[2-(морфолино)-этилтио] бензимидазола дигидрохлорида и/или основания (Афобазола)» известна фармацевтическая композиция анксиолитического действия, содержащая 5-этокси-2-[2-(морфолино)-этилтио] бензимидазола дигидрохлорид в терапевтически эффективном количестве с замедленным высвобождением действующего вещества, отличающаяся тем, что включает комбинацию модификаторов высвобождения, состоящую из по меньшей мере одного гидрофильного модификатора высвобождения и по меньшей мере одного замедлителя высвобождения при определенном их количественном соотношении, и включающая другие обычно применяемые фармацевтически приемлемые вспомогательные вещества при следующем соотношении компонентов, мас. %:
5-этокси-2-[2-(морфолино)-этилтио] бензимидазола дигидрохлорид 7,00-30,00
Частным вариантом такой композиции является выпущенный на рынок препарат Афобазол® ретард (ЛП-006555, АО «Отисифарм»), имеющий состав на 1 таблетку:
Фабомотизола дигидрохлорид 30,0 мг;
коллидон® SR [поливинилцетат – 80 %, повидон – 19 %, натрия лаурилсульфат – 0,8 %, кремния диоксид – 0,2 %] 120 мг;
гипромеллоза – 25,0 мг;
лактоза 23,0 мг;
магния стеарат 2,0 мг;
пленочная оболочка:
опадрай II 85 F18422 белый [поливиниловый спирт, частично гидролизованный – 40,0 %, титана диоксид – 25,0 %, макрогол 4000 – 20,2 %, тальк – 14,8 %] 6,0 мг.
Известные из уровня техники композиции в лекарственной форме «таблетки» подобраны с учетом физико-химических характеристик активной фармацевтической субстанции фабомотизола для получения по технологии влажной грануляции. Данная технология позволяет получать лекарственные препараты, удовлетворяющие требованиям Фармакопей ЕАЭС и РФ, но влажная грануляция имеет существенный недостаток, а именно, длительность производства, вследствие необходимости предварительного приготовления раствора увлажнителя, получение увлажненных гранул с последующей их калибровкой, сушкой и отбраковкой некачественного полупродукта с целью получения массы для таблетирования. Кроме того, применение при влажной грануляции увлажнителя с последующей сушкой смеси в сушилке-грануляторе может приводить к деструкции действующего вещества из-за влияния влаги и температуры, что соответственно сказывается на качестве препарата.
Кроме того, таблетки композиции-прототипа имеют сравнительно низкие значения по прочности, что может вызывать сколы в процессе производства готовой таблетированной формы.
Таким образом, технической проблемой, решение которой обеспечивается при осуществлении или использовании заявляемого изобретения, и которая не могла быть решена при осуществлении или использовании аналогов изобретения, заключается в необходимости разработки фармацевтической композиции на основе фабомотизола дигидрохлорида с дополнительными компонентами, которая позволяет получать твердую лекарственную форму с высокой биодоступностью и оптимизировать технологический процесс получения лекарственного препарата с целью получения качественного продукта.
Обозначенная проблема решается оптимальным подбором дополнительных и вспомогательных компонентов и их содержания в фармацевтической композиции.
Раскрытие сущности изобретения
Фармацевтическая композиция в форме таблетки, обладающая анксиолитическим действием, содержащая фабомотизола дигидрохлорид, 2-меркапто-5-этоксибензимидазол, 4-(2-хлорэтил)морфолин гидрохлорид и вспомогательные вещества при следующем соотношении компонентов, мас. %:
В качестве наполнителей можно использовать микрокристаллическую целлюлозу, микрокристаллическую целлюлозу силикатированную, лактозы моногидрат, лактозу безводную, сорбитол, маннитол, кальция гидрофосфат, мальтодекстрин или смесь данных веществ.
В качестве веществ, влияющих на кинетику растворения препарата, применяют кроскармеллозу натрия или карбоксиметилкрахмал натрия, или крахмал прежелатизированный, или кросповидон, или повидон, или коповидон, или гипролоза низкозамещенная, или гипролоза, или гидроксипропилметицеллюлоза, или этилцеллюлоза, или смесь данных веществ.
В качестве скользящих и/или смазывающих агентов выбирают стеариновую кислоту или магния стеарат, или кальция стеарат, или натрия стеарилфумарат, или гидрогенизированное касторовое масло, или кремния диоксид, или тальк, или смесь данных веществ.
Частным вариантом выполнения фармацевтической композиции является композиция следующего состава, мас. %:
Другим частным вариантом выполнения фармацевтической композиции является композиция следующего состава, мас. %:
Заявляемое соотношение ингредиентов является оптимальным и найдено экспериментально.
Предложенная фармацевтическая композиция отличается от предшествующего уровня техники тем, что из состава полностью исключен крахмал картофельный или крахмал кукурузный и добавлены компоненты 2-меркапто-5-этоксибензимидазол и 4-(2-хлорэтил)морфолин гидрохлорид. Роль веществ, влияющих на кинетику растворения препарата (дезинтегрантов) в предложенной композиции исполняет крахмал прежелатизированный. Данные изменения позволяют оптимизировать технологический процесс производства фармацевтической композиции за счет перехода от технологии влажной грануляции к технологии прямого прессования при получении таблеток, исключив стадии получения влажных гранул с последующей их сушкой и калибровкой для получения таблеточной массы, или получение капсул, наполненных смесью порошков указанных дозированных компонентов, что было затруднительно ранее из-за плохой сыпучести и аморфности субстанции фабомотизола гидрохлорида. Данные изменения позволяют получать качественный продукт, стабильный на протяжении всего срока годности.
Технический результат заявляемого технического решения заключается в повышении производительности технологического процесса получения твердой фармацевтической композиции в единицу времени, с одновременным повышением качества производимых таблетированных форм, стабильных на протяжении всего срока годности препарата.
Указанный технический результат достигается оптимизацией технологии производства, путем сокращения времени производства в 2 раза, за счет совершенствования состава вспомогательных веществ и добавлением дополнительных компонентов, позволяющего исключить стадии получения увлажненных гранул с последующей сушкой; увеличении качества производимых твердых лекарственных форм, путем устранения дефектов при производстве с увеличением производительности; повышении биодоступности твердого лекарственного препарата, за счет получения более быстрого профиля высвобождения фабомотизола в сравнении с прототипом.
Таблица 1. Сравнение длительности и производительности технологических процессов
*в зависимости от использованного оборудования при сушке влажных гранул
Таким образом, на процесс получения технологией влажной грануляции 100 кг таблеток необходимо 15-25,5 часов, т.е. производительность составляет 100 кг за 15ч (100 : 15 = 6,67 кг/ч) или 100 кг за 25,5 ч (100 : 25,5 = 3,92 кг/ч). Производительность состава-прототипа составляет 3,92-6,67 кг/ч.
Наработка 100 кг предлагаемого состава технологией прямого прессования необходимо 7-7,5 часов, т.е. производительность составляет 100 кг за 7 ч (100 : 7 = 14,29 кг/ч) или 100 кг за 7,5 час (100 : 7,5 = 13,33 кг/ч).
Отсюда следует, что предлагаемый состав позволяет сократить время производства больше чем в 2 раза относительно состава-прототипа, производительность увеличивается в 2-3 раза относительно состава-прототипа.
Повышение качества получаемых таблеток заключается в уменьшении количества таблеток со сколами и дефектами при производстве. Заявленное изобретение в процессе производства позволяет минимизировать количество брака. Истираемость таблеток по заявляемой композиции составила менее 0,2 %, тогда как для состава-прототипа этот показатель мог достигать до 0,8 %. Снижение процента истираемости в процессе производства способствовало уменьшению количества брака: менее 1,0 % таблеток со сколами для заявляемого состава в сравнении с 5 % брака на таблетках состава-прототипа.
Технический результат предлагаемой фармацевтической композиции достигается подбором активных и вспомогательных компонентов. Вспомогательные вещества играют важную роль в обеспечении биодоступности, эффективности, стабильности и безопасности лекарственного препарата и влияют на скорость, полноту высвобождения и всасывания активных ингредиентов, а, следовательно, регулируют время наступления и силу фармакологического эффекта. Вспомогательные вещества в предлагаемой таблетированной лекарственной форме по своему назначению выполняют разные функции и подразделяются на наполнители (разбавители), связующие (склеивающие), дезинтегранты (разрыхляющие), скользящие и смазывающие (антифрикционные).
Наполнитель используется для обеспечения необходимой массы таблеток при малых дозировках активных компонентов. В случае прямого прессования он проявляет также связующие и дезинтегрирующие свойства, а также улучшается сыпучесть и насыпной объем готовой таблеточной массы.
Вещества, влияющие на кинетику растворения препарата (дезинтегранты) добавляются в состав таблеток для улучшения их распадаемости в среде желудочно-кишечного тракта и высвобождения лекарственных веществ с оказанием необходимого терапевтического эффекта, повышения биодоступности.
Для улучшения антифрикционных свойств массы для таблетирования, уменьшения ее налипания на таблет-пресс и производственное оборудование добавляются скользящие и/или смазывающие агенты. Скользящие агенты увеличивают текучесть массы для таблетирования. Смазывающие агенты способствуют снижению трения частиц между собой и частиц с контактными частями оборудования на производстве.
Изменение качественного и количественного состава в заявляемой фармацевтической композиции для получения лекарственного препарата фабомотизола в твердой лекарственной форме не сказалось на биодоступности препарата, так как данные проведенных сравнительных тестов кинетики растворения (СТКР) согласно Примеру 3 показывает сопоставимо быстрое высвобождение действующего вещества из заявляемой фармацевтической композиции и состава-прототипа – более 80 % от номинального значения за 15 минут.
Таблица 2. Состав для исследований
200 мг, мг
Были подготовлены серии препарата с массой таблеток 200 мг с 10 мг активного компонента.
Ввиду отсутствия воздействия стресс-факторов на фабомотизол в процессе получения таблеточной массы (влага и температура), заявляемая композиция имеет высокую стабильность – после 3-х лет хранения содержание посторонних примесей не превышает 0,1-0,5 % (от массы активного вещества), остальные показатели качества, предъявляемые к твердой лекарственной форме, соответствуют требованиям нормативной документации.
Также было отмечено повышение общей динамики элиминации (ОДЕ) для таблеток заявляемой композиции (AV = 4,7-6,4) по сравнению с таблетками состава-прототипа (AV = 11-12,5), что свидетельствует о повышении биодоступности предлагаемого состава композиции.
Анксиолитическое действие предлагаемой композиции определяется наличием транквизизатора - фабомотизола - в составе композиции, а также 2-меркапто-5-этоксибензимидазол и 4-(2-хлорэтил)морфолин гидрохлорида, фабомотизол дигидрохлорид, 2-меркапто-5-этоксибензимидазол и 4-(2-хлорэтил)морфолин гидрохлорид являются активными агентами фармацевтической композиции. Действие фармацевтической композиции реализуется преимущественно в виде сочетания анксиолитического (противотревожного) и легкого стимулирующего (активирующего) эффектов. Фабомотизол уменьшает или устраняет чувство тревоги (озабоченность, плохие предчувствия, опасения), раздражительность, напряженность (пугливость, плаксивость, чувство беспокойства, неспособность расслабиться, бессонница, страх), депрессивное настроение, соматические проявления тревоги (мышечные, сенсорные, сердечно-сосудистые, дыхательные, желудочно-кишечные симптомы), вегетативные нарушения (сухость во рту, потливость, головокружение), когнитивные расстройства (трудности при концентрации внимания, ослабленная память), в т.ч. возникающие при стрессорных расстройствах (расстройства адаптации). Особенно показано применение Фабомотизола у лиц с преимущественно астеническими личностными чертами в виде тревожной мнительности, неуверенности, повышенной ранимости и эмоциональной лабильности, склонности к эмоционально-стрессовым реакциям.
Эффект от применения развивается на 5-7 день лечения, максимальный эффект – к концу 4 недели лечения и сохраняется после окончания лечения в среднем 1-2 недели. Фабомотизол не вызывает мышечную слабость, сонливость и не обладает негативным влиянием на концентрацию внимания и память. При его применении не формируется привыкание, лекарственная зависимость и не развивается синдром «отмены».
Предлагаемая композиция может применяться у взрослых при тревожных состояниях, а именно в случае генерализованных тревожных расстройствах; неврастении; расстройствах адаптации; у больных с различными соматическими заболеваниями, такими как бронхиальная астма, синдром раздраженного кишечника, системная красная волчанка, ИБС, гипертоническая болезнь, аритмии; при дерматологических, онкологических и других заболеваниях.
Предлагаемая композиция может быть использована для лечения нарушений сна, связанных с тревогой; нейроциркуляторной дистонии; предменструального синдрома; алкогольного абстинентного синдрома; для облегчения синдрома «отмены» при отказе от курения.
Краткое описание чертежей
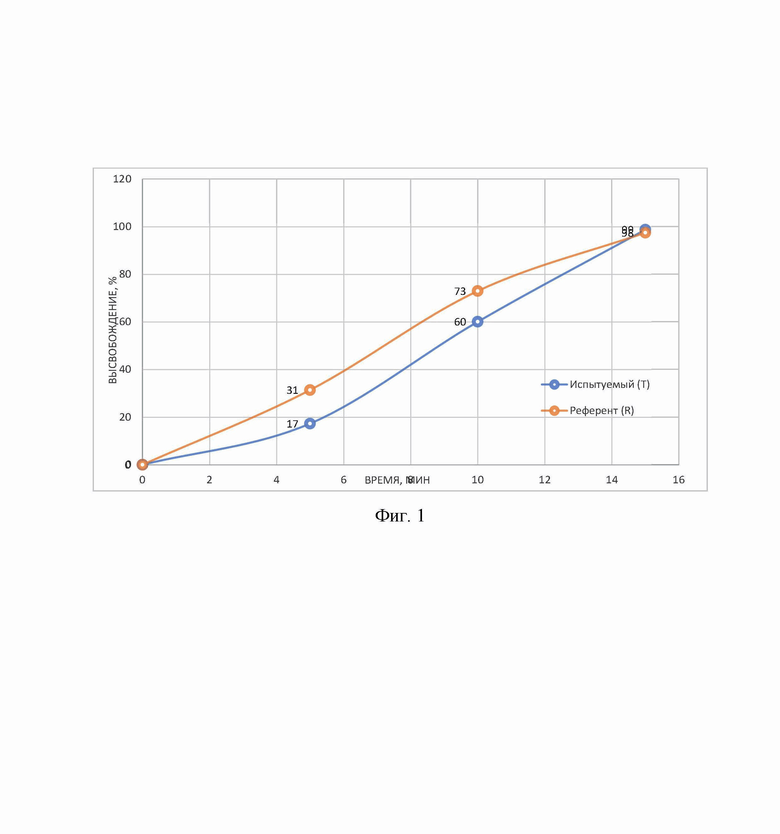
На Фиг. 1 представлены усредненные профили растворения лекарственного средства в форме таблеток заявляемого состава и состава-прототипа – Афобазол®, 10 мг, таблетки (зарегистрированный состав ЛС-000861) в среде 0,1 М раствор соляной кислоты, рН 1,2.
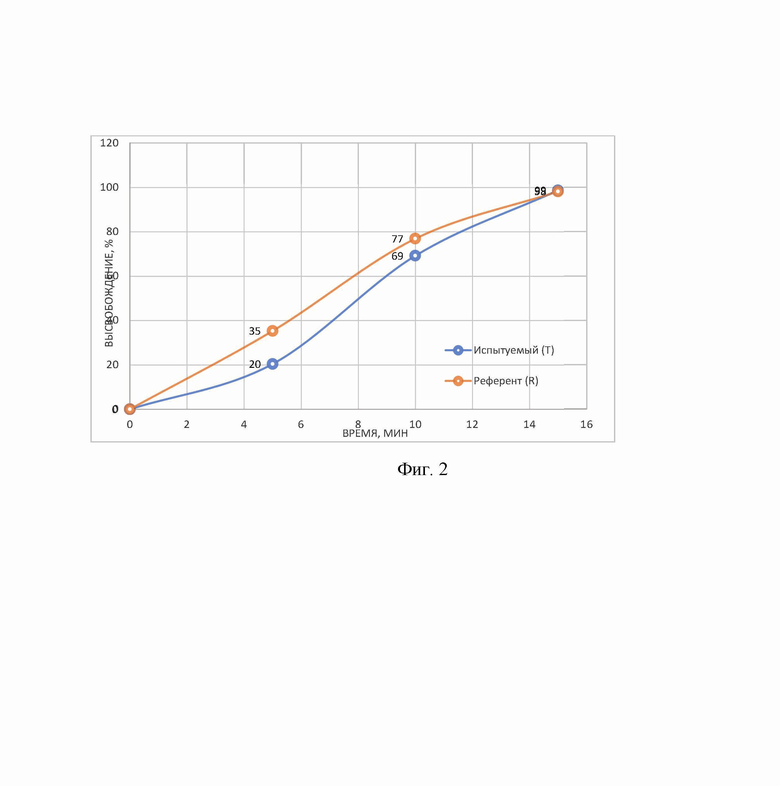
На Фиг. 2 представлены усредненные профили растворения лекарственного средства в форме таблеток заявляемого состава и состава-прототипа – Афобазол®, 10 мг, таблетки (зарегистрированный состав ЛС-000861) в среде ацетатный буферный раствор pH 4,5.
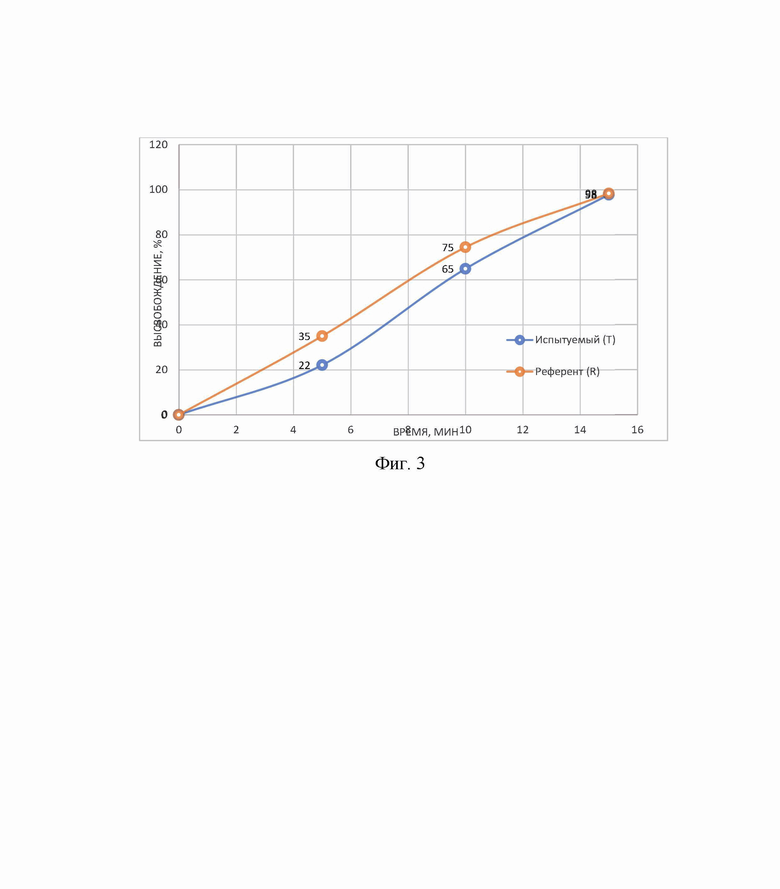
На Фиг. 3 представлены усредненные профили растворения лекарственного средства в форме таблеток заявляемого состава и состава-прототипа – Афобазол®, 10 мг, таблетки (зарегистрированный состав ЛС-000861) в среде фосфатный буферный раствор рН 6,8.
Осуществление изобретения
Далее приводятся примеры осуществления предлагаемого технического решения, которые его иллюстрируют, но не охватывают все возможные варианты его осуществления. Специалисту в данной области техники понятно, что возможны и другие частные варианты осуществления предлагаемого технического решения, включающие иные композиции таблеток фабомотизола в соответствии с предложенным составом, не описанные в настоящих примерах.
Для получения заявляемого технического решения используют следующие компоненты.
Фабомотизол (CAS 173352-39-1) - 4-[2-[(6-этокси-1H-бензимидазол-2-ил)сульфанил]этил]морфолин)
Эмпирическая формула: C15H21N3O2S ⋅ 2 HCl
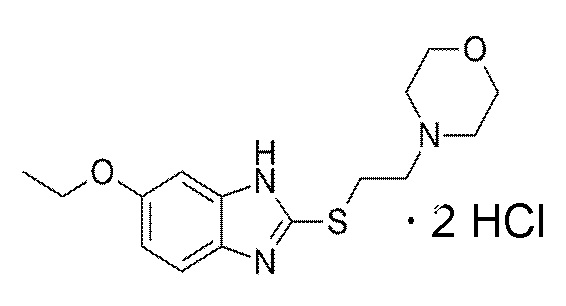
Молекулярная масса: 380,34
2-меркапто-5-этоксибензимидазол (CAS 55489-15-1) - эмпирическая формула: C9H10N2OS, молекулярная масса: 194,25
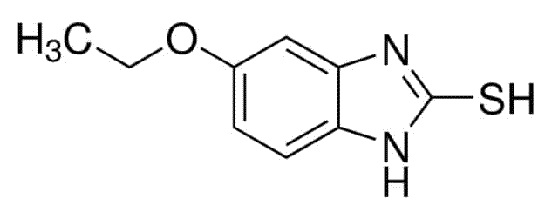
4-(2-Хлорэтил)морфолин гидрохлорид (CAS 3647-69-6)
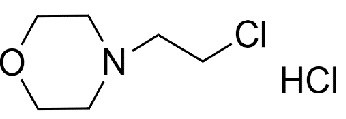
Эмпирическая формула: C6H13Cl2NO
Молекулярная масса:186,08
Для получения предлагаемой композиции могут быть использованы любые доступные в продаже наполнители, веществ, влияющих на кинетику растворения препарата (дезинтегранты за исключением крахмала картофельного или крахмала кукурузного), скользящие и/или смазывающие агенты.
Предлагаемую твердую фармацевтическую композицию получают следующим образом.
Пример 1
Просеивают необходимое количество фабомотизола дигидрохлорида, 2-меркапто-5-этоксибензимидазола, 4-(2-хлорэтил) морфолин гидрохлорида, один или нескольких наполнителей, вещества, влияющи на кинетику растворения препарата (дезинтегранты за исключением крахмала картофельного или крахмала кукурузного), скользящих и/или смазывающих агентов через сито с размером ячеек 0,5-1,0 мм.
После просеивания порошки собирают в производственные емкости и направляют на стадию получения массы для лекарственной формы.
В отдельной емкости готовят тритурат фабомотизола из отвешенного количества фабомотизола дигидрохлорида, 2-меркапто-5-этоксибензимидазола, 4-(2-хлорэтил)морфолин гидрохлорида и части просеянного наполнителя.
В смеситель загружают оставшееся количество наполнителя, тритурат фабомотизола, один или несколько веществ, влияющих на кинетику растворения препарата (дезинтегрантов) и перемешивают содержимое смесителя 15-25 минут.
Далее в смеситель добавляют отвешенное количество просеянного одного или нескольких скользящих и/или смазывающих агентов и опудривают в течение 3-10 минут.
Выгружают массу для таблетирования в емкости.
Таблетирование массы проводят на таблеточном прессе. Настраивают таблетпресс на получение плоскоцилиндрических таблеток с массой от 185 до 215 мг, диаметром 8 мм, высотой 3,1-3,6 мм.
Одновременно с таблетированием происходит обеспыливание таблеток и отбраковка по внешнему виду, средней массе и прочности.
Пример 2
Получение таблеток предлагаемого состава получают согласно способу по Примеру 1, используя в качестве вспомогательных веществ микрокристаллическую целлюлозу или микрокристаллическую целлюлозу силикатированную, или лактозы моногидрат, или лактозу безводную, или сорбитол, или маннитол, или кальция гидрофосфат, или мальтодекстрин или кроскармеллозу натрия или карбоксиметилкрахмал натрия, или крахмал прежелатизированный, или кросповидон, или повидон, или коповидон, или гипролозу низкозамещенную, или гипролозу, или гидроксипропилметицеллюлозу, или этилцеллюлозу или стеариновую кислоту или магния стеарат, или кальция стеарат, или натрия стеарилфумарат, или гидрогенизированное касторовое масло, или кремния диоксид, или тальк.
В качестве наполнителя применяют микрокристаллическую целлюлозу или микрокристаллическую целлюлозу силикатированную, или лактозы моногидрат, или лактозы безводной, или сорбитол, или маннитол, или кальция гидрофосфат, или мальтодекстрин или их смеси.
В качестве веществ, влияющих на кинетику растворения препарата, применяют кроскармеллозу натрия или карбоксиметилкрахмал натрия, или крахмал прежелатизированный, или кросповидон, или повидон, или коповидон, или гипролозу низкозамещенную, или гипролозу, или гидроксипропилметицеллюлозу, или этилцеллюлозу или их смеси.
В качестве скользящих и/или смазывающих агентов используют стеариновую кислоту или магния стеарат, или кальция стеарат, или натрия стеарилфумарат, или гидрогенизированное касторовое масло, или кремния диоксид, или тальк.
Пример 3
Исследование кинетики растворения состава (Таблица 2) проводили согласно ОФС.1.4.2.0014.15 «Растворение для твердых дозированных лекарственных форм» на аппарате «лопастная мешалка» (Erweka, Германия) при скорости вращения 75 об/мин.
По результатам изучения кинетики растворения лекарственных средств Фабомотизол, 10 мг, таблетки заявляемого состава и состава-прототипа Афобазол®, 10 мг, были признаны эквивалентными и во всех исследуемых средах высвобождение действующего вещества составило более 80 % за 15 минут.
Профили растворения лекарственных средств в форме таблеток заявляемого состава и состава-прототипа Афобазол®, 10 мг, таблетки приведены на Фиг 1-3.
Пример 4
Предлагаемую композицию выполняют в форме таблеток в дозировке 10 мг активных компонентов. Получаемые таблетки применяют внутрь, после еды. Оптимальной разовой дозой является 10 мг активного компонента, а суточная - 30 мг, суточную дозу делят на 3 приема в течение дня.
Длительность курсового применения препарата определяется врачом индивидуально, средний курс лечения составляет 2-4 недели.
В некоторых случаях под наблюдением врача суточная доза может быть увеличена до 60 мг активного компонента, а длительность лечения до 3 месяцев.
Побочными действиями от приема предлагаемой композиции могут быть аллергические реакции, в редких случаях может наблюдаться головная боль.
Противопоказаниями к применению предлагаемой композиции могут выступать повышенная чувствительность к компонентам; беременность; период лактации (грудного вскармливания); детский возраст до 18 лет.
Таким образом, предлагаемая фармацевтическая композиция для получения твердого лекарственного препарата фабомотизола, за счет точно подобранного состава обеспечивает уменьшение длительности технологии получения готовой лекарственной формы, с одновременным повышением их качества, вследствие чего является перспективной для получения анксиолитического лекарственного препарата.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармацевтическая композиция пролонгированного действия на основе 5-этокси-2-[2-(морфолино)-этилтио] бензимидазола дигидрохлорида и/или основания (Афобазола) | 2017 |
|
RU2694837C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ АФОБАЗОЛА | 2004 |
|
RU2289403C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ МОКСИФЛОКСАЦИНА И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 2014 |
|
RU2558932C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2453315C2 |
| ТВЕРДОФАЗНЫЙ ЛИНЕЗОЛИДСОДЕРЖАЩИЙ ПРЕПАРАТ | 2017 |
|
RU2690491C2 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА | 2007 |
|
RU2366421C2 |
| Лекарственная форма в виде капсулы, содержащая таблетки с диметилфурмаратом | 2019 |
|
RU2742745C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2013 |
|
RU2543322C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2012 |
|
RU2505286C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ МОНТЕЛУКАСТА И ЛЕВОЦЕТИРИЗИНА | 2013 |
|
RU2677649C2 |
Изобретение относится к медицине, фармацевтической промышленности, а именно к твердой фармацевтической композиции на основе фабомотизола дигидрохлорида, обладающей анксиолитической активностью, и может быть использовано для производства лекарственного средства в виде таблеток методом прямого прессования. Предлагаемая фармацевтическая композиция включает, мас.%: фабомотизола дигидрохлорид 0,5-30; 2-меркапто-5-этоксибензимидазол 0,001-1 и/или 4-(2-хлорэтил)морфолин гидрохлорид 0,0001-0,5; маннитол, и/или кальция гидрофосфат, и/или лактоза безводная, и/или сорбитол, и/или мальтодекстрин, и/или лактозы моногидрат, и/или микрокристаллическая целлюлоза, и/или микрокристаллическая целлюлоза силикатированная 68,8989-85; крахмал прежелатизированный, и/или кроскармеллоза натрия, и/или карбоксиметилкрахмал натрия, и/или кросповидон, и/или повидон, и/или коповидон, и/или гипролоза низкозамещенная, и/или гипролоза, и/или гидроксипропилметицеллюлоза, и/или этилцеллюлоза, за исключением крахмала картофельного или крахмала кукурузного, 1,0-10; кальция стеарат, и/или натрия стеарилфумарат, и/или стеариновая кислота, и/или магния стеарат, и/или гидрогенизированное касторовое масло, и/или кремния диоксид, и/или тальк 0,1-3. Технический результат: повышение производительности технологии получения твердой фармацевтической композиции в единицу времени с одновременным повышением качества производимых таблетированных форм, стабильных на протяжении всего срока годности препарата. 1 з.п. ф-лы, 2 табл., 3 ил., 4 пр.
1. Фармацевтическая композиция в лекарственной форме таблетки анксиолитического действия, полученная прямым прессованием, включающая фабомотизола дигидрохлорид и вспомогательные вещества, отличающаяся тем, что дополнительно содержит 2-меркапто-5-этоксибензимидазол и/или 4-(2-хлорэтил)морфолин гидрохлорид при следующем соотношении компонентов, мас.%:
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что соотношение компонентов выбрано следующим, мас.%:
| Афобазол (Afobazol) Инструкция по применению (Описание лекарственного препарата Афобазол (Afobazol) основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для электронного издания справочника Видаль 2018 года, дата обновления: 2018.12.26, [онлайн], [найдено 30.05.2023] | |||
| Найдено из Интернет: |
Авторы
Даты
2024-10-21—Публикация
2022-12-02—Подача