Изобретение относится к медицине, а именно к стоматологии, и предназначено для повышения эффективности эндодонтического лечения путем модификации гуттаперчевых штифтов биокерамическими наночастицами для трехмерной обтурации корневых каналов зубов.
Лечение болезней пульпы и периапикальных тканей остается одной из ведущих проблем в стоматологии, что определяется высокой распространенностью данной патологии среди населения (А.И., Цепов с соавт. 2018; Митронин А.В., 2020; Янушевич О.О., с соавт., 2021; Ricucci D., Siqueira J.F., Li Y., 2019; Cohen S., Hargreaves K.M., Berman L.H., 2020). Ведущим этиологическим фактором развития осложнений кариеса являются микроорганизмы и продукты их жизнедеятельности (Дмитриева Л.А., 2010; Царев В.Н., и соавт., 2016; Базикян Э.А., 2018). Доказано, что микрофлора корневых каналов организована в биопленки, что повышает ее устойчивость к антимикробным препаратам (Волков Д.П., Митронин А.В., 2015; Ипполитов Е.В., Подпорин М.С., 2017).
Одним из важных факторов, обеспечивающих хорошие отдаленные результаты эндодонтического лечения зубов, является герметичное пломбирование их корневых каналов (Максимовский Ю.М., Митронин А.В., 2015; Николаев А.И., Цепов Л.М., 2022). Целью эндодонтического лечения является устранение инфекционного патогена из системы корневых каналов и предотвращение ее повторного инфицирования путем гомогенной обтурации внутрикорневого пространства зуба.
Данные микробиологической диагностики свидетельствуют о значительном снижении интенсивности микробной обсемененности системы корневых каналов после хемо-механической обработки, однако, 40-60% корневых каналов остаются инфицированными, что может стать причиной развития осложнений в долгосрочной перспективе (Кречина Е.К., 2018; Ricucci D., 2019; De Deus G., 2021). Таким образом, качественная обтурация системы корневых каналов играет важную роль в борьбе с эндодонтической инфекцией, инактивируя оставшиеся бактерии и предотвращая повторное инфицирование корневого канала (Katge F.A., Patil D.P., 2017; Jardine А.Р. и соавт., 2019).
Выбор метода обтурации корневых каналов зависит от клинических показаний, навыков врача и оснащенности лечебного учреждения. Наиболее распространенными являются различные методики пломбирования системы корневых каналов гуттаперчей с использованием силера. В современных методиках пломбирования силеру отводится роль связующего агента между гуттаперчевыми штифтами и стенками корневых каналов; он также заполняет боковые канальцы, ответвления корневой системы (Чуев В.Н., 2018; Макеева И.М., 2021; Trope М., 2015; Yang D.K., и соавт., 2018; Roizenblit R.N., и соавт., 2020). Известно, что современные эндодонтические герметики противостоят микробному консорциуму системы корневых каналов.
Корневая пломба должна быть монолитным, герметичным, постоянным препятствием на пути инфекции. На сегодняшний день для пломбирования корневых каналов используют филлер и силеры. В качестве филлера применяют гуттаперчевые штифты различной конусности и размера.
Гуттаперчевые штифты на протяжении долгих лет применяются при пломбировании корневых каналов зуба (Елисеева М.В., и соавт., 2018; Torabinejad М, 2010 Ricucci D., 2017). Гуттаперча представляет собой твердый, но в то же время эластичный и гибкий продукт коагуляции латекса гуттаперченосных деревьев. Химический состав гуттаперчевых штифтов, которые применяются в стоматологии, несколько изменен за счет добавления оксида цинка или различных смол. К их преимуществам относят хорошую биосовместимость и низкую токсичность, способность к конденсации и пространственную стабильность. Тем не менее, гуттаперча имеет ряд недостатков: гуттаперчевые штифты не могут применяться при пломбировании корневых каналов без силера, так как не имеют адгезии к дентину; гуттаперчевые штифты не обладают антибактериальным или бактериостатическим эффектом; тонкие гуттаперчевые штифты имеют излишне высокую гибкость и мягкость, что зачастую затрудняет процедуру пломбирования, особенно при работе с узкими корневыми каналами, а также может приводить к деформации штифтов в процессе их припасовки; нагретая (жидкая) гуттаперча дает усадку при охлаждении (Хабадзе З.С., и соавт., 2019; Манак Т.С., Клюйко К.Г., 2020).
Для постоянной обтурации системы корневых каналов используют эндогерметики, или силеры, к которым также предъявляются определенные требования. Отечественные и зарубежные производители предлагают большое разнообразие силеров, которые различаются по физико-химическим свойствам и составу. В качестве материалов для пломбирования корневых каналов применяют цинк-фосфатные цементы, цинкоксид эвгеноловые пасты, стеклоиономерные цементы; материалы с содержанием резорцин-формальдегидной смолы; средства на основе фосфата кальция, силеры на основе эпоксидных смол, биокерамические силеры. Обтурация системы корневых каналов предполагает максимизацию количества гуттаперчи и уменьшение толщины силера. Эпоксидные силеры, цинкоксид эвгеноловые силеры и др. дают значительную усадку и рассасываются со временем, вследствие этого всегда рекомендуется использовать тонкий слой силера во избежание потери герметичности и разрушения корневой пломбы.
В связи с этим, в настоящее время научно-практический интерес представляют биокерамические силеры, которые с недавнего времени применяются при обтурации корневых каналов и имеют определенные преимущества по сравнению с широко используемыми эпоксидными герметиками. Биокерамические цементы становятся все более используемыми благодаря их щелочному рН, высокой биосовместимости, биологической активности, нетоксичности, стабильности цементной матрицы, хорошим герметизирующим свойствам и способности увеличивать прочность корня после гомогенной обтурации (Крихели Н.И., 2021; Kim R.J., и соавт., 2014; Silva E.J., 2018). Кроме того, благодаря своему высокощелочному уровню рН, в процессе полимеризации биокерамический силер оказывает антимикробное действие на эндодонтическую флору (Koutroulis А, и соавт., 2019; Atmeh A.R., и соавт., 2020).
Ключевой целью пломбирования корневых каналов является создание непроницаемой пломбы для предотвращения повторного инфицирования системы корневых каналов микробной биопленкой путем устранения любого свободного пространства, в котором могли бы развиваться бактерии (Мамедова Л.А., 2016; Debelian G., Trope М., 2016; Camilleri J., 2017). Следовательно, используемые пломбировочные материалы должны обеспечивать трехмерное пломбирование, не оставляя пустого пространства, которое могло бы поставить под сомнение непроницаемость корневой пломбы. В отличие от традиционных силеров, биокерамический силер использует естественную влажную среду дентинных канальцев корня для окончательного отверждения (Khalil I., и соавт., 2016; Zordan-Bronzel C.L., 2019). По мере отверждения, гидрофильный силер формирует гидроксиапатит и химически прикрепляется к дентину корня, а также не дает усадки. Однако, между гуттаперчевыми штифтами и цементом не возникает химической адгезии, гуттаперча в корневом канале удерживается лишь механическим способом, что может оказывать негативное влияние на герметичность корневой пломбы в долгосрочной перспективе (Gok Т., и соавт., 2017). Таким образом, несмотря на значительное количество исследований, проблема качества и эффективности постоянной обтурации в процессе эндодонтического лечения в настоящее время остается крайне актуальной.
Следовательно, необходим поиск альтернативных способов пломбирования корневых каналов зуба в концепции трехмерной герметичной обтурации и разработка оптимизированных рекомендаций по созданию монолитной корневой пломбы на основе биокерамических силеров и гуттаперчи в клинических условиях. Предполагается, что решить данную проблему позволит создание биоактивного слоя на поверхности гуттаперчи для облегчения сцепления между внутренней стенкой корневого дентина и пломбировочным материалом корневого канала. На сегодняшний день в стоматологической отрасли представлены следующие коммерчески доступные аналоги: EndoReZ™ - система для пломбирования, которая включает покрытые смолой гуттаперчевые штифты и полимерный силер, или модель Active GP Plus™, включающую покрытые частичками стеклоиономера гуттаперчевые штифты и стеклоиономерный силер.
Известен способ пломбирования системы корневого канала зуба - [Пат. 2280420 Российская Федерация, МПК А61С 5/04. Способ пломбирования системы корневого канала зуба / И.В. Маланьин, И.С. Бондаренко, М.П. Певзнер, А.П. Сумелиди, Ю.Н. Голуб; заявитель и патентообладатель И.В. Маланьин, И.С. Бондаренко, М.П. Певзнер, А.П. Сумелиди, Ю.Н. Голуб. - №2004132110/14; заявл. 03.11.2004; опубл. 20.04.2006, Бюл. №21]. Пломбирование корневых каналов начинают с предварительного получения слепков каналов, затем покрывают стенки канала и слепок инертным силером, причем после внесения слепка в канал в центр его вводят файл, разогретый до 300°С, на 40-50 секунд и одновременно подают к файлу ультразвуковые колебания, затем вводят в образовавшееся пространство после проникновения гуттаперчи в латеральные ответвления канала соразмерный с размером файла гуттаперчевый штифт. Основным недостатком данного способа пломбирования является то, что гуттаперчевые штифты после нагревания дают усадку, что способствует появлению пустых пространств в системе корневых каналов, что может привести к повторному инфицированию эндодонто-периодонтального комплекса зуба. Кроме того, между силером и гуттаперчей отсутствует адгезия, что также является причиной разгерметизации корневой пломбы с течением времени.
Известен способ пломбирования корневых каналов постоянных зубов с использованием адгезивной смолы и оптического волокна - [Пат. 2190981 Российская Федерация, МПК А61С 5/00, А61С 5/04. Способ пломбирования корневых каналов постоянных зубов (варианты) / Ю.А. Винниченко, А.В. Винниченко; заявитель и патентообладатель Ю.А. Винниченко, А.В. Винниченко. - №2001109056/14; заявл. 09,04.2001; опубл. 20.10.2002, Бюл. №29]. При пломбировании корневой канал заполняют адгезивной смолой, которую полимеризуют через одну минуту путем воздействия импульсным лазерным излучением синего спектра длиной волны 0,473 мкм в течение двух минут, при этом в корневой канал на глубину 7-10 мм от апикального отверстия вводят оптическое волокно, после удаления которого образовавшийся дефект вновь заполняют адгезивной смолой до устья канала, погружают в него оптическое волокно на глубину 1-2 мм и полимеризуют лазерным излучением в том же режиме. Также возможен второй вариант пломбирования системы корневых каналов. Перед введением пломбировочного материала стенки корневого канала обрабатывают адгезивной смолой, которую полимеризуют через одну минуту путем воздействия импульсным лазерным излучением синего спектра длиной волны 0,473 мкм в течение двух минут, при этом в корневой канал на глубину 7-10 мм от апикального отверстия вводят оптическое волокно, которое затем перемещают на уровень устья канала и вновь проводят полимеризацию лазерным излучением в том же режиме. Недостатками данного способа пломбирования является то, что используемая адгезивная смола оказывает токсическое действие на периапикальные ткани зуба, что впоследствии вызывает раздражение окружающих тканей, воспаление и развитие периапикальных абсцессов. Кроме того, оптическое волокно является жестким материалом, что ограничивает его использование в изогнутых корневых каналах, которые встречаются в 40-60% случаев (Чиликин В.Н., 2003; Собкина Н.А., 2015; Bergenholtz G., 2010).
Известен способ пломбирования корневых каналов коллаген-апатитовым имплантатом, принятый за прототип - [Пат. 2155023 Российская Федерация, МПК А61К 6/02, А61Р 1/02. Средство для пломбирования корневых каналов зуба / С.Е. Чигарина, А.И. Богатов, С.Д. Литвинов, С.И. Буланов, В.Н. Чигарин; заявитель и патентообладатель Чигарина Светлана Егоровна. - №99113699/14; заявл. 21.06.1999; опубл. 27.08.2000, Бюл. №24]. Пломбирование системы корневых каналов зуба осуществляется за счет использования композиции на основе фосфата кальция в виде гидроксиапатита, при этом дополнительно содержит коллаген в соотношении 60:40 соответственно. Для пломбирования корневых каналов зубов в качестве пломбировочного материала используют коллаген-апатитовый имплантат, полученный на основе биополимера (коллаген) с неорганическим компонентом. После традиционного эндодонтического лечения, не добиваясь полного гемостаза, корневые каналы заполняют с помощью корневого штопфера нужным количеством материала. В качестве материала берут коллаген-апатитовый имплантат, который представляет собой твердый материал, в котором достигнута высокая степень структурной интегрированности между коллагеном и гидроксиапатитом. Его смешивают с дистиллированной водой в соотношении 1:20 по весу до насыщения. После заполнения корневого канала накладывают изолирующую прокладку и производят наложение пломбы из любого постоянного пломбировочного материала. Вместе с тем, результаты применения данного способа пломбирования корневых каналов свидетельствуют о неблагоприятном исходе лечения в отдаленные периоды наблюдений, так как коллаген-апатитовый имплантат выполнен из биодеградируемого материала и не обеспечивает гомогенной обтурации каналов в долгосрочной перспективе.
Исходя из этого следует заключить, что требуется разработка наиболее совершенных методов пломбирования корневых каналов с использованием современных материалов в концепции 3D-обтурации.
Задачей, на решение которой направлено заявляемое изобретение, является повышение эффективности лечения болезней пульпы и периапикальных тканей и предотвращение реинфицирования корневых каналов зуба в долгосрочной перспективе посредством разработки гуттаперчевых штифтов с биоактивным керамическим покрытием для усиления герметичности корневой пломбы при их использовании с биокерамическими силерами.
Авторы предлагают способ, характеризующийся простотой, малыми временными затратами и высокой результативностью.
Технический результат заявленного изобретения заключается в улучшении качества пломбирования системы корневых каналов зубов за счет модификации гуттаперчевых штифтов биокерамическими наночастицами, а именно напылением тонкого и однородного слоя микрокристаллической кальцийфосфатной биокерамики на размягченный поверхностный слой гуттаперчи, что позволяет создавать герметичную монолитную корневую пломбу с использованием современных биокерамических силеров.
Технический результат достигается следующим образом. В процессе эндодонтического лечения по завершении механической и медикаментозной обработки системы корневых каналов приступают к постоянной обтурации внутрикорневого пространства биокерамическим силером и гуттаперчей. Корневой канал тщательно высушивают с помощью абсорбирующих штифтов. После подбора и припасовки мастер-штифта выполняется его предварительная обработка, которая обеспечивается за счет вертикального погружения гуттаперчевого штифта в раствор 0,1-10,0% канифоли в легколетучем органическом растворителе на 3-5 секунд с последующим напылением тонкого и однородного слоя микрокристаллической кальцийфосфатной биокерамики на размягченный поверхностный слой гуттаперчи. Внутрикорневое пространство заполняют биокерамическим силером с помощью шприца и интраканальной насадки с последующим введением биокерамического гуттаперчевого штифта на рабочую длину корневого канала. Затем срезают излишки гуттаперчи термоплаггером и проводят рентгенологический контроль пломбирования.
В современной стоматологии известно понятие «биомиметика», как синоним естественной интеграции биоматериалов, т.е. биологической, биомеханической, функциональной и косметической интеграции, максимально имитирующей физиологическое поведение естественных зубов [Gil Tirlet, 2015].
Представленный нами биомиметический способ модификации гуттаперчи обеспечивается за счет того, что поверхностный слой мастер-штифта растворяется, штифт размягчается без термической обработки, превращаясь в химически пластифицированную гуттаперчу. В дальнейшем штифт покрывается слоем биокерамических наночастиц и одномоментно отверждается. Такая технология не только увеличивает шероховатость штифта и, в дальнейшем, площадь фактического его контакта с силером, что способствует увеличению механической адгезии между штифтом и силером, но и обеспечивает химическое взаимодействие между ними. Это позволяет сформировать пространственно стабильное герметичное уплотнение, которое, в свою очередь, становится барьером для повторного инфицирования системы корневых каналов, а также предотвращает микроподтекание и разгерметизацию внутрикорневого пространства. Авторы рекомендуют использовать в качестве легколетучего растворителя гуттаперчи хлороформ.
В отечественной и зарубежной литературе описаны различные методы нанесения покрытий на поверхность медицинских объектов. К наиболее распространенным методам относятся плазменное напыление, включающее высокие температуры воздействия и плазму, создаваемую газообразным аргоном, для распыления расплавленных материалов на поверхность. В аспекте стоматологии, плазменное напыление является наиболее распространенным методом нанесения вещества гидроксиапатит в качестве поверхностной пленки, однако, данный метод не подходит для нанесения активных веществ на поверхность гуттаперчевых штифтов из-за чрезвычайно высоких температур обработки. Достоверно известно, что гуттаперча имеет низкую температуру плавления и, следовательно, низкую устойчивость к нагреванию. Согласно данным литературы, недостатком плазменного напыления пленки из гидроксиапатита является образование аморфной фазы (известной как аморфный фосфат кальция) и других неактивных фаз фосфата кальция.
Целью настоящего изобретения является повышение герметичности корневой пломбы за счет получения биоактивного покрытия, содержащего кальцийфосфатную керамику, на поверхности гуттаперчевых штифтов биомиметическим методом.
Для усиления корневой пломбы полезными свойствами биокерамики, в настоящей методике формирование покрытия происходит путем механической фиксации наночастиц в размягченном поверхностном слое гуттаперчи. Соответственно, при схватывании наночастиц биокерамики с биокерамическим силером образуется стабильный, плотный и однородный слой кристаллического гидроксиапатита на всем протяжении гуттаперчевого штифта и силера. В свою очередь, по мере отверждения, гидрофильный биокерамический силер формирует гидроксиапатит и химически прикрепляется к дентину корня зуба. Таким образом, при постоянной обтурации системы корневых каналов биокерамическим силером и гуттаперчевым штифтом, модифицированным биокерамическими наночастицами, формируется гомогенная корневая пломба, которая позволяет добиться герметичного заполнения системы корневого канала и создает благоприятные биологические условия для процесса заживления тканей, тем самым повышая эффективность лечения осложнений кариеса.
На подготовительном этапе исследования при разработке способа модификации гуттаперчевых штифтов биокерамическими наночастицами был проведен эксперимент для подбора наиболее эффективного средства для растворения поверхностного слоя гуттаперчи. В качестве растворителя были изучены различные легколетучие растворители гуттаперчи, в соответствии с которыми образцы гуттаперчевых штифтов были разделены на 4 группы: 1 группа - хлороформ; 2 группа - ксилол; 3 группа - скипидар; 4 группа -эукалиптол. Полученные образцы были изучены методом сканирующей электронной микроскопией (СЭМ) и энергодисперсионного анализа.
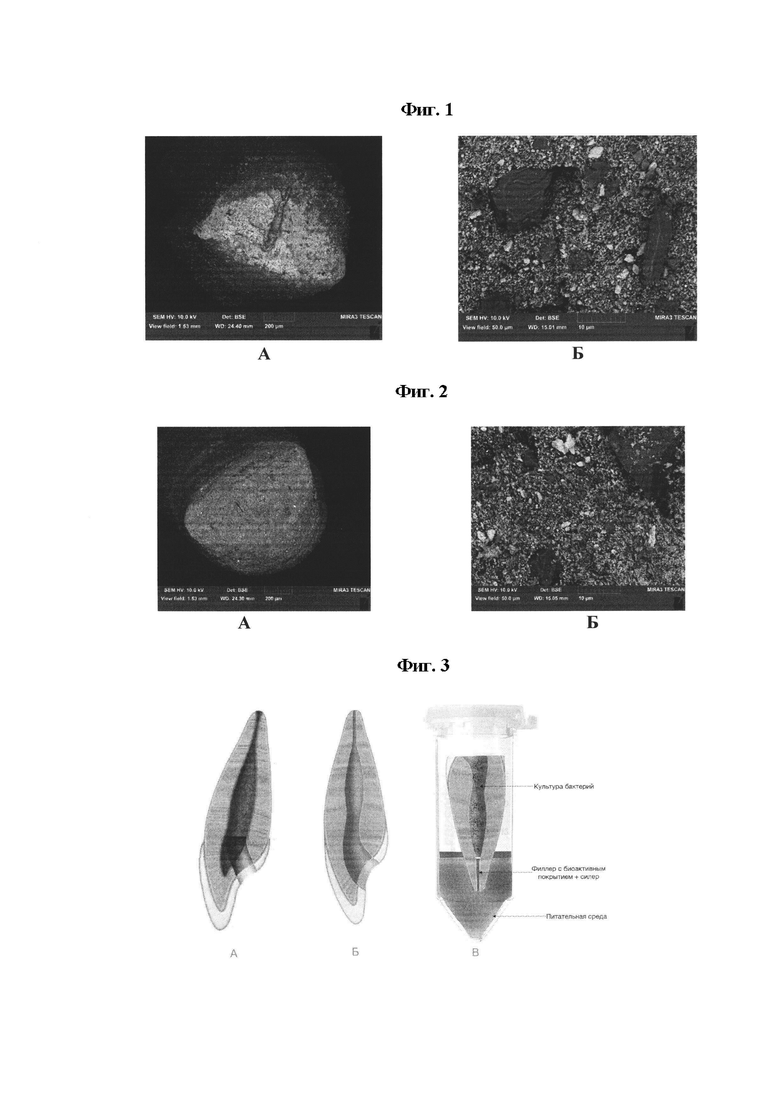
Согласно результатам проведенного исследования, наиболее равномерно напыляется порошок на гуттаперчу при использовании легколетучего растворителя - хлороформа (фиг. 1, А - поперечный срез гуттаперчевого штифта с биоактивным покрытием, который был создан с помощью хлороформа; Б - кальцийфосфатные частицы биокерамики на поверхности гуттаперчи). Вместе с тем, для усиления свойств адгезии наночастиц биокерамики к поверхностному слою гуттаперчевого штифта в хлороформ была добавлена канифоль в различной концентрации (от 0,1 до 30%) и повторно проведен анализ поверхности гуттаперчевых штифтом с помощью СЭМ-исследования.
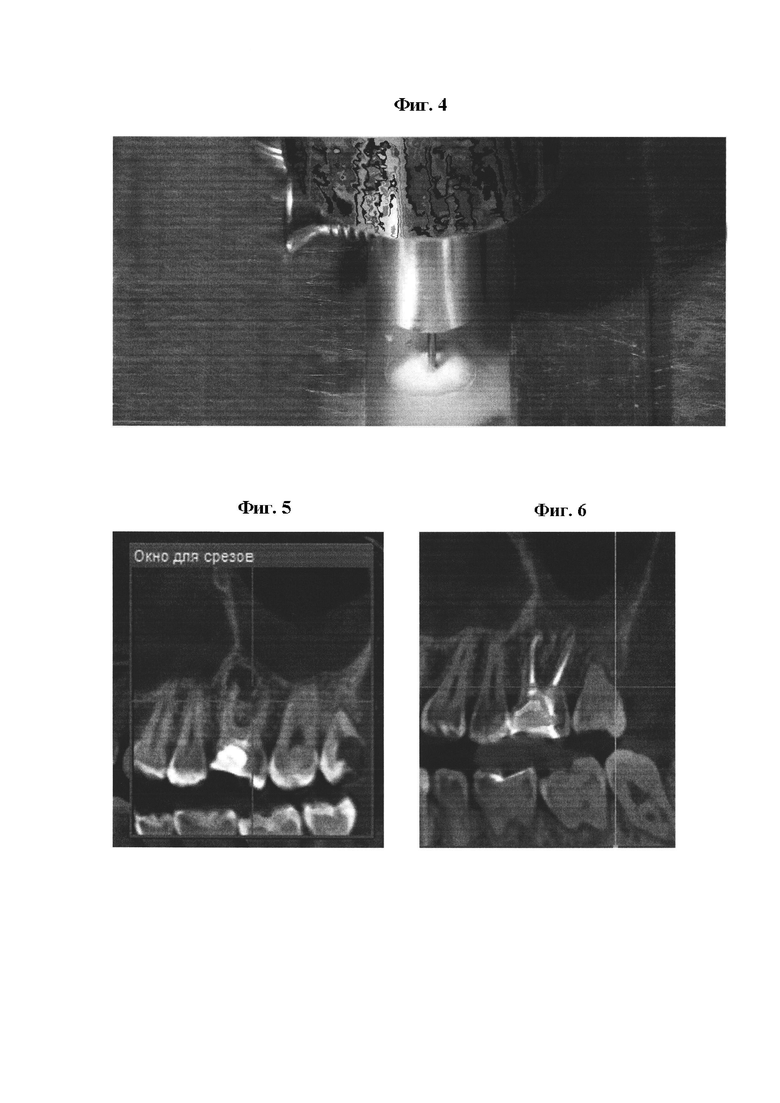
Было установлено, что при добавлении к хлороформу 10% канифоли и напылению наночастиц, гуттаперчевый штифт становится более прочным, но гибким, в отличие от других экспериментальных образцов (фиг. 2, А - поперечный срез гуттаперчевого штифта с биоактивным покрытием, который был создан и укреплен с помощью 10% канифоли в растворителе; Б -кальцийфосфатные частицы биокерамики на поверхности гуттаперчи). Таким образом, для дальнейших исследований была выбрана методика модификации гуттаперчевого штифта с помощью 10% раствора канифоли в хлороформе и микрокристаллической кальфийфосфатной биокерамики.
Для подтверждения подлинности наших рассуждений и предложенного способа биологической обтурации было проведено лабораторное исследование герметизирующей способности гуттаперчевых штифтов с биокерамическим покрытием и биокерамическим силером в условиях эксперимента in vitro. Дизайн лабораторного исследования состоял из трех последовательных этапов: 1 - микробиологический анализ короно-апикального микробного подтекания (КАМП); 2 - оценка силы сцепления гуттаперчевых штифтов с биокерамическим покрытием и биокерамическим силером с помощью «push-out» теста (тест на выталкивание).
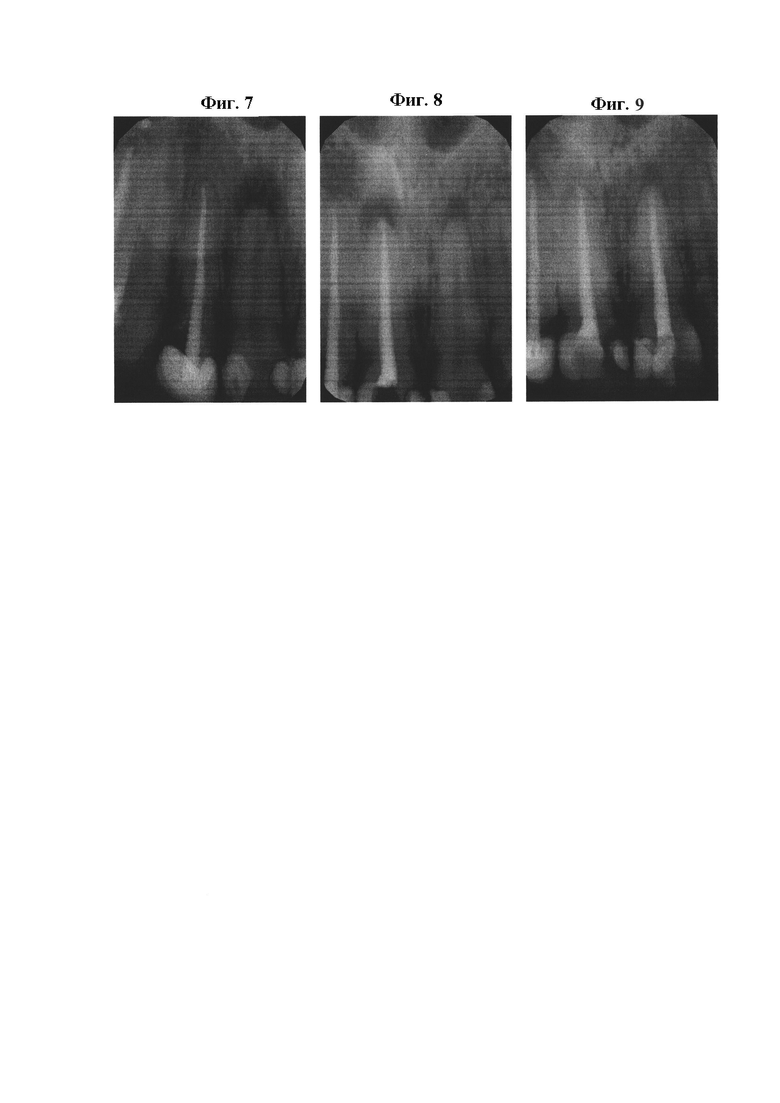
В лабораторное исследование было включено 40 удаленных центральных резцов верхней челюсти. Выполнена декоронация зубов для стандартизации исследования, длина корневого канала 16 мм. Проведена механическая и медикоментозная обработка корневых каналов, корневые каналы расширены до размера 35.04 по ISO. Все образцы в случайном порядке были распределены на 4 группы в соответствии с методикой дальнейшего пломбирования, в том числе группа без пломбирования: 1 группа (отрицательный контроль) - корневые каналы не запломбированы (n=10), 2 группа - традиционный способ пломбирования корневых каналов зубов эпоксидным силером и гуттаперчей в технике латеральной конденсации (n=10), 3 группа - пломбирование корневых каналов зубов биокерамическим силером и гуттаперчей методом одного штифта (n=10); 4 группа - предложенный способ пломбирования корневых каналов биокерамическим силером и гуттаперчей с биокерамическим нанопокрытием методом одного штифта (n=10). Затем образцы погружались в пробирку типа Эппендорф с 0,5 мл физиологического раствора, и помещались в термостат для окончательного отверждения корневой пломбы. Через 48 часов зубы промывали, высушивали, корональные 14 мм корня снаружи покрывали изоляционным лаком, в то время как апикальные 2 мм оставляли открытыми. Проводили удаление корневой пломбы в средней трети корней, запломбированной оставляли только апикальную треть корней (2-3 мм от верхушки корня). Выполняли рентгенологической контроль распломбирования. Образцы дезинфицировали в 5,25% растворе гипохлорита натрия в течение 30 минут, затем обильно промывали дистиллированной водой и высушивали. Затем образцы помещали в пробирку с питательной средой Hugh-Leifson. В свободное внутрикорневое пространство вносили культуру бактерий Staphylococcus aureus и инкубировали при Т=37° в течение 24 часов. Схема проведения эксперимента представлена на фиг. 3, где А - корневой канал после удаления зуба; Б - корневой канал после механической и медикаментозной обработки 3% раствором гипохлорита натрия; В - помещенный в пробирку типа Эппендорф с питательной средой образец зуба, апикальная часть которого запломбирована филлером и силером, согласно группе исследования, и в среднюю треть корневого канала введена взвесь микроорганизмов. Оценку микробного подтекания проводили через 1, 7, 30 суток с начала эксперимента, в качестве контроля использовали цветной показатель питательной среды. Далее микробные колонии пересевались на питательные среды для подтверждения и идентификации микроорганизмов.
Результаты микробиологического исследования имели статистически значимую разницу между группами исследования (р<0,01). Оценка герметичности обтурации апикальной части корневых каналов продемонстрировала отсутствие микроподтеканий в 3 и 4 экспериментальных группах через 30 дней эксперимента в 92% и 100% случаев, соответственно. Корневая пломба, выполненная из гуттаперчи и эпоксидного силера, оказалась негерметичной в 65% случаев уже через 7 дней наблюдения. При этом, в контрольной группе в 100% наблюдали изменение цвета через 24 часа с начала инкубации. Визуальное изменение цвета среды свидетельствует о проникновении культуры бактерий через корневую пломбу в питательную среду. Полученные результаты свидетельствуют о высокой герметичности корневой пломбы, выполненной по разработанной методике. Таким образом, пломбирование корневых каналов биокерамическим силером и гуттаперчей с биоактивным нанокерамическим покрытием методикой «силера и одного штифта» обеспечивают трехмерную высокопрочную обтурацию корневого канала в долгосрочной перспективе.
Для оценки силы адгезии корневой пломбы был проведен «push-out» тест. Исследование выполнялось на удаленных резцах верхней челюсти, которые предварительно были обработаны и запломбированы с помощью биокерамического силера и двух типов гуттаперчи - стандартной (группа А) и гуттаперчей, модифицированной биокерамическими наночастицами (группа Б). Образцы были зафиксированы в эпоксидной смоле, и получали поперечные срезы корня толщиной 1 мм с помощью алмазного диска с водяным охлаждением. Из каждого образца было получено 3-4 среза толщиной 1 мм. Для проведения «push-out» теста была использована универсальная испытательная машина. К центру корневой пломбы, а именно к гуттаперчевому штифту, прикладывалась возрастающая нагрузка со скоростью 0,5 мм/мин до тех пор, пока не происходило разрушение соединения «пломба-зуб» (фиг. 4). Согласно результатам, предложенный метод создает адгезию между гуттаперчевыми штифтами с биокерамическим покрытием и биокерамическим силером, измеренную в диапазоне критических нагрузок 7,35-9,23 МПа, что гораздо выше, чем адгезия между гуттаперчевыми штифтами и биокерамическим силером (3,25-4,55 МПа).
Авторы настоящего изобретения в ходе экспериментального исследования продемонстрировали, что оценка in vitro герметизирующей способности и силы сцепления гуттаперчевых штифтов с биокерамическим покрытием и подобным силером показала значительное улучшение обеих характеристик по сравнению с пломбированием зубов традиционным методом с использованием стандартных гуттаперчевых штифтов.
Модификация поверхностного слоя гуттаперчевых штифтов биоактивным покрытием позволяет создавать монолитную конструкцию между гуттаперчей и биокерамическим силером за счет образования первично химической связи между наночастицами биокерамики, внедренными в гуттаперчевый штифт, и собственно основным объемом силера. Это позволяет надежно и плотно обтурировать систему корневых каналов зубов, тем самым повышая эффективность лечения болезней пульпы и периапикальных тканей и предотвращая реинфицирование корневых каналов в долгосрочной перспективе. Монолитно-гомогенная биокерамическая корневая пломба длительно препятствует проникновению микрофлоры как через апикальное отверстие, так и через устье корневого канала, за счет пролонгированной антибактериальной активности и высокой герметичности обтурации. Кроме того, биокерамика внутри корневой системы способствует реминерализации дентина и очагов микробной деминерализации, что создает условие для восстановления механической прочности дентина корня зуба и препятствует его фрактурам при больших жевательных нагрузках.
Таким образом, при традиционной методике обтурации корневых каналов краевое прилегание к гуттаперче недостаточно плотное, что приводит к образованию щелей и множественных микрополостей. При эндодонтическом лечении это приводит к плохому герметизму корневой пломбы, что является предпосылкой для повторного инфицирования корневой системы. Вместе с тем, при нанесении биоактивного покрытия на поверхность гуттаперчевых штифтов филлер приобретает новые свойства, такие как биосовместимость и усиленная адгезия, что является ключевым фактором для дальнейшего применения в качестве пломбировочного материала при лечении болезней пульпы и периапикальных тканей. Это позволяет предотвратить микроподтекание и неблагоприятную миграцию бактерий не только в области «силер-дентин», но и прежде всего в области «гуттаперча-силер» в эндодонтических пролеченных зубах, которые, в противном случае, могут стать причиной повторного инфицирования. Более того, образующийся в процессе химического взаимодействия фосфат кальция является одной из многочисленных встречающихся в природе естественных композиций фосфата кальция, поэтому минерализованный гидроксиапатит на гуттаперчевых штифтах способен укреплять костную ткань, а также способствовать росту новой кости, окружающей корень зуба. В дополнение к биологическим функциям, представленным выше, для нанесения биоактивного покрытия на гуттаперчу не требуется термическая обработка (что впоследствии могло бы стать причиной усадки гуттаперчи), а также не требуется наличие сложного и дорогостоящего оборудования. Следовательно, применение системы «биокерамический силер + гуттаперчевые штифты (филлер) с биоактивным биокерамическим покрытием» представляет собой многообещающий способ пломбирования корневых каналов для дальнейшего применения в первичном и повторном эндодонтическом лечении зубов, что повысит качество терапии пациентов с болезнями пульпы и периапикальных тканей и будет способствовать оздоровлению полости рта.
Клинический пример №1
Пациент М., 1991 года рождения, обратился с жалобами на боль в области зуба 2.6, усиливающуюся при накусывании на зуб. По данным осмотра была выявлена несостоятельная реставрация в 2.6 зубе, нарушение краевого прилегания и рецидив кариеса. Холодовая проба была отрицательная, показатели ЭОД были снижены до 200 мкА. На компьютерной томограмме в области 2.6 зуба был выявлен очаг деструкции костной ткани в области верхушки передне-щечного и небного корней округлой формы, размером 0,3×0,3 см (фиг. 5). К04.5 Хронический апикальный периодонтит зуба 2.6. Пациентом было подписано информированное добровольное согласие на участие в данном исследовании и пломбировании корневых каналов зуба 2.6 биокерамическим силером и гуттаперчей с биоактивным покрытием.
Лечение: В процессе лечения после выполнения местной анестезии, изоляции рабочего поля с помощью системы коффердам и препарирования кариозных тканей зуба, была вскрыта полость зуба. Выполнена механическая обработка четырех корневых каналов до размера 30.04 по ISO с помощью системы вращающихся файлов Race EVO (FKG). Корневые каналы медикаментозно обрабатывали 3% раствором гипохлорита натрия и проводили ультразвуковую активацию ирригационного раствора с помощью насадки Irrisafe (Acteon). Корневые каналы высушивали с помощью бумажных адсорберов. На две недели корневой канал был временно запломбирован нетвердеющей пастой на основе гидроокиси кальция. В следующее посещение проводилась повторная медикаментозная обработка корневых каналов, корневые каналы высушивали с помощью бумажных адсорберов. Затем подбирали и припасовывали гуттаперчевый мастер-штифт размером 30.04 и выполняли рентгенологический контроль для оценки глубины проникновения штифта на полную рабочую длину корневого канала. Подобранный гуттаперчевый мастер-штифт предварительно подготавливали методом погружения в 10% раствор канифоли в хлороформе на 5 секунд с последующим напылением тонкого и однородного слоя микрокристаллической кальцийфосфатной биокерамики на размягченный поверхностный слой гуттаперчи. В корневые каналы вводили биокерамический силер с помощью интраканальной насадки, затем в заполненный силером корневой канал вводили гуттаперчевый штифт с биоактивным покрытием на рабочую длину корневого канала. Излишки гуттаперчи были срезаны термоплаггером, герметизацию устьев также выполняли с помощью термоплаггера и плаггера Машту. В завершении эндодонтического лечения проводили рентгенологический контроль пломбирования. Зуб 2.6 восстанавливали прямой композитной реставрацией с последующим изготовлением ортопедической конструкции.
На контрольном осмотре через 6 и 12 месяцев после лечения клиническая картина была благоприятной. На компьютерной томограмме не было выявлено патологических изменений в периапикальной области зуба 2.6 (фиг. 6).
Клинический пример №2
Пациентка П., 1995 года рождения, обратилась с жалобами на боль при накусывании на зуб 1.1. На прицельной внутриротовой рентгенограмме 1.1 зуба был выявлен очаг деструкции костной ткани в области верхушки корня округлой формы, размером 0,4×0,5 см (фиг. 7). Был поставлен диагноз по МКБ-10 К04.5 Хронический апикальный периодонтит зуба 1.1. Пациентом было подписано информированное добровольное согласие на участие в данном исследовании и пломбировании корневого канала зуба 1.1 биокерамическим силером и гуттаперчей с биоактивным покрытием.
Лечение: В процессе лечения после выполнения местной анестезии, изоляции рабочего поля с помощью системы коффердам и обеспечения доступа к пульпарной полости, было найдено устье корневого канала. Проведена механическая обработка корневого канала до размера 35.06 по ISO с помощью системы вращающихся файлов Race (FKG). Корневой канал медикаментозно обрабатывали 3% раствором гипохлорита натрия и проводили ультразвуковую активацию ирригационного раствора с помощью насадки Irrisafe (Acteon). На две недели корневой канал был временно запломбирован нетвердеющей пастой на основе гидроокиси кальция. В следующее посещение проводилась повторная медикаментозная обработка корневого канала, корневой канал высушивали с помощью бумажных адсорберов. Затем подбирали и припасовывали гуттаперчевый мастер-штифт размером 35.06, выполняли его калибровку. Затем осуществляли рентгенологический контроль для оценки глубины проникновения штифта на полную рабочую длину корневого канала. При пломбировании зуба 1.1 подобранный гуттаперчевый мастер-штифт предварительно подготавливали методом погружения в 10% раствор канифоли в хлороформе на 5 секунд с последующим напылением тонкого и однородного слоя микрокристаллической кальцийфосфатной биокерамики на размягченный поверхностный слой гуттаперчи. В корневой канал вводили биокерамический силер с помощью интраканальной насадки, затем в заполненный силером корневой канал вводили гуттаперчевый штифт с биоактивным покрытием на рабочую длину корневого канала. Излишки гуттаперчи были срезаны термоплаггером, герметизацию устья также выполняли с помощью термоплаггера и плаггера Машту. В завершении эндодонтического лечения проводили рентгенологический контроль пломбирования (фиг. 8). Зуб 1.1 восстанавливали прямой композитной реставрацией.
На контрольном осмотре через 6 и 12 месяцев после лечения клиническая картина была благоприятной. На контрольной рентгенограмме через 12 месяцев после проведенного лечения отмечается значительное уменьшение очага деструкции костной ткани в периапикальной области зуба 1.1 (фиг. 9). Продолжается динамическое наблюдение за состоянием периапикальных тканей зуба 1.1.
Предложенный способ постоянного пломбирования системы корневых каналов зубов отвечает требованиям, предъявляемым к герметичной биологической обтурации внутрикорневого пространства, что значительно повышает качество эндодонтического лечения осложнений кариеса и предотвращает возможные осложнения. Анализируя результаты исследования, можно сделать заключение о том, что предложенный способ удобен для использования, хорошо переносится пациентами, не имеет побочного действия и противопоказаний к применению.
Результаты проведенных лабораторных и клинических исследований позволяют рекомендовать предложенный способ модификации гуттаперчевых штифтов биокерамическими наночастицами для трехмерной обтурации корневых каналов зубов в практическое здравоохранение.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ противомикробной обработки дентина корня зуба при эндодонтическом лечении пульпита и периодонтита | 2019 |
|
RU2729726C1 |
| Способ обтурации анатомически сложной корневой системы жевательной группы зубов | 2024 |
|
RU2825105C1 |
| Способ обтурации корневых каналов зубов, отягощенных отсутствием апикальной констрикции, перирадикулярной деструкцией костной ткани и резорбцией | 2023 |
|
RU2829273C1 |
| Способ консервативного лечения апикального периодонтита | 2022 |
|
RU2798701C1 |
| СПОСОБ ГЕРМЕТИЗАЦИИ ЭНДОДОНТИЧЕСКОГО ДОСТУПА | 2012 |
|
RU2489986C1 |
| СПОСОБ ПЛОМБИРОВАНИЯ СИСТЕМЫ КОРНЕВОГО КАНАЛА ЗУБА | 2004 |
|
RU2280420C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО АПИКАЛЬНОГО ПЕРИОДОНТИТА | 2017 |
|
RU2665177C1 |
| СТЕКЛОИОНОМЕРНЫЙ СИЛЕР НА СИЛИКОНОВОЙ ОСНОВЕ ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ ЗУБА | 2006 |
|
RU2308259C1 |
| Способ хирургическо-консервативного лечения хронического апикального периодонтита | 2023 |
|
RU2823204C1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСЛОЖНЕНИЙ ПРИ ЛЕЧЕНИИ КОРНЕВЫХ КАНАЛОВ ЗУБОВ | 2021 |
|
RU2775197C1 |
Изобретение относится к медицине, а именно к стоматологии, и предназначено для использования при эндодонтическом лечении. В процессе эндодонтического лечения, по завершении механической и медикаментозной обработки системы корневых каналов приступают к постоянной обтурации внутрикорневого пространства биокерамическим силером и гуттаперчей. Корневой канал тщательно высушивают с помощью абсорбирующих штифтов. После подбора и припасовки мастер-штифта выполняется его предварительная обработка, которая обеспечивается за счет вертикального погружения гуттаперчевого штифта в 10% раствор канифоли в хлороформе на 3-5 секунд с последующим напылением на размягченный поверхностный слой гуттаперчи однородного слоя микрокристаллической кальцийфосфатной биокерамики. Внутрикорневое пространство заполняют биокерамическим силером с помощью шприца и интраканальной насадки с последующим введением биокерамического гуттаперчевого штифта (филлера) на рабочую длину корневого канала. Затем в полости зуба у устья канала излишки гуттаперчи срезают термоплаггером и проводят рентгенологический контроль пломбирования. Способ за счет модификации гуттаперчевых штифтов биокерамическими наночастицами улучшит качество пломбирования системы корневых каналов зубов и создаст герметичную монолитную корневую пломбу. 9 ил., 2 пр.
Способ трехмерной обтурации корневых каналов зубов посредством гуттаперчевых штифтов с биоактивным керамическим покрытием, отличающийся тем, что в процессе эндодонтического лечения после механической и медикаментозной обработки системы корневых каналов проводят постоянную обтурацию внутрикорневого пространства биокерамическим силером и гуттаперчей, при этом проводят предварительную обработку гуттаперчевого мастер-штифта путем его вертикального погружения в 10% раствор канифоли в хлороформе на 3-5 секунд с последующим напылением однородного слоя микрокристаллической кальцийфосфатной биокерамики на размягченный поверхностный слой гуттаперчи, а внутрикорневое пространство заполняют биокерамическим силером посредством шприца и интраканальной насадки с последующим введением биокерамического гуттаперчевого штифта на рабочую длину корневого канала.
| СРЕДСТВО ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ ЗУБА | 1999 |
|
RU2155023C1 |
| СПОСОБ ЛЕЧЕНИЯ КОРНЕВЫХ КАНАЛОВ ЗУБОВ | 2021 |
|
RU2771916C1 |
| СПОСОБ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ ПОСТОЯННЫХ ЗУБОВ (ВАРИАНТЫ) | 2001 |
|
RU2190981C1 |
| WO 2017162706 A1, 28.09.2017 | |||
| JP 2020006220 A, 16.01.2020 | |||
| US 0004480996 A1, 06.11.1984 | |||
| Македонова Ю.А | |||
| Биокерамические технологии в эндодонтии | |||
| Статья в сборнике трудов конференции "Современные технологии в мировом научном пространстве", Пермь, 2017, стр | |||
| Способ получения суррогата олифы | 1922 |
|
SU164A1 |
Авторы
Даты
2024-10-30—Публикация
2023-12-08—Подача