ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет относительно предварительной заявки на патент США №62/623682, поданной 30 января 2018 г., которая полностью включена в настоящее описание посредством ссылки.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0002] Клиницисты стремились использовать естественные клетки-киллеры (NK) для адоптивного переноса ввиду их способности распознавать и убивать опухолевые клетки без необходимости в каком-либо конкретном маркере опухолевых клеток. Alizadeh et al., Clin Cancer Res. 16(13): 3399-3408 (2010). Однако разработке процедур адоптивного переноса NK клеток препятствовало ограниченное количество жизнеспособных клеток. NK клетки представляют собой лишь небольшую долю клеток в крови, и выделение из типичного взятого образца крови не приводит к получению большого количества клеток. Кроме того, NK клетки должны быть очищены от загрязняющих РВМС, таких как Т и В клетки, посредством истощения популяции CD3 и CD 19, соответственно. Childs et al, American Society of Hematology (ASH) Education Book, vol. 2013 no. 1 234-246 (2013). Это необходимый шаг для аллогенной трансплантации, когда присутствие Т и В клеток увеличивает риск развития реакции трансплантат против хозяина (GVHD), но дополнительно снижает выход NK клеток.
[0003] NK клетки плохо размножаются in vitro по сравнению с другими видами клеток, главным образом, из-за раннего старения. Используя даже самые эффективные способы, NK клетки чувствительны к укорочению и старению теломеров только после нескольких пассажей. Denman et al., PLoS ONE 7(1): e30264 (2012). Наиболее эффективным способом повышения жизнеспособности и пролиферации NK клеток in vitro является совместное культивирование с питающими клетками. Обычно используемые питающие клетки для размножения NK клеток включают облученные мононуклеарные клетки периферической крови (РВМС), линии трансформированных вирусом Эпштейна-Барра лимфобластоидных клеток (EBV-LCL), генно-модифицированные клетки K562, конститутивно экспрессирующие IL-15 или 21, и другие облученные линии опухолевых клеток. Berg et al., Cytotherapy, 11(3): 341-55 (2009). Совместное культивирование с питающими клетками значительно повышает жизнеспособность NK клеток, а пролиферация с популяцией увеличивается в 1000-50000 раз.
[0004] Иммунная терапия имеет большие перспективы для улучшения исхода таких раковых заболеваний, как остеосаркома (ОС), при которой выживаемость не улучшалась в течение последних 30 лет. ОС, включая химиотерапевтическую резистентную ОС, легко убивается in vitro как аутологичными, так и аллогенными активированными NK клетками. Однако микроокружение опухоли при ОС и других солидных опухолях имеет повышенные уровни высокоиммуносупрессивного цитокина, трансформирующего ростового фактора бета (TGF-β). Lamora et al, Clin Cancer Res 20: 5097-5112 (2014); Xu et al, DNA Cell Biol, 33: 802-806 (2014). Добавление блокирующего антитела к TGF-β улучшило эффективность вакцины на дендритных клетках в ОС (Kawano et al, Clin Orthop Relat Res., 470: 2288-2294 (2012)), предоставив доказательство принципа, что TGF-β активно подавляет иммунную терапию при ОС.
[0005] Подавление TGF-β функции NK клеток многогранно. TGF-β модулирует развитие NK клеток и впоследствии отрицательно влияет на их функцию при достижении созревания. TGF-β развивает незрелую линию NK клеток, предотвращая прогрессирование NK клеток в CD16+NK клетки. TGF-β также может индуцировать прежние CD 16+ NK клетки, превращая их в CD16-. Keskin et al., Proc Natl Acad Sci USA, 104: 3378-3383 (2007). Кроме того, мыши, экспрессирующие доминантно-отрицательный TGFβR на NK клетках, имеют увеличенное количество зрелых NK клеток по сравнению с мышами дикого типа. Viel et al, Science signaling 9: ral9 (2016).
[0006] В зрелых NK клетках TGF-β ингибирует противоопухолевую активность посредством множества механизмов. TGF-β снижает IL-2 и IL-15-индуцированную пролиферацию NK-клеток (Wilson et al, PloS one 6: e22842 (2011)), a IL-15 индуцирует активацию mTOR. Viel et al, Sci Signal., 16; 9(415): ral9 (2016). TGF-β также ингибирует секрецию IFNγ, которая важна для стимуляции адаптивной иммунной системы и может подвергнуть чувствительные опухоли лизису NK клеток. TGF-β ингибирует IFNγ как прямо, так и опосредованно. SMAD3 напрямую связывается с промотором IFNγ и может также опосредованно ингибировать IFNγ путем снижения экспрессии стимулирующих IFNγ транскрипционных факторов, T-bet и Е4ВР4. Tang et al, Nat Commun, 8: 14677 (2017). Однако опосредованное TGF-β ингибирование секреции IFNγ может быть частично ослаблено путем предварительной инкубации NK-клеток с IL-12, TL-15 или TL-18. Yu et al, Immunity, 24: 575-590 (2006). Кроме того, TGF-β также ингибирует секрецию TNFα и GM-CSF и модулирует экспрессию хемокиновых рецепторов, чтобы способствовать удержанию NK клеток в костном мозге. Castriconi et al, J Immunol, 190: 5321-5328 (2013).
[0007] В частности, TGF-β опосредует ингибирование цитотоксичности NK клеток путем снижения секреции гранзима и перфорина и экспрессии следующих активирующих рецепторов: NKG2D, NKp30, KIRs, DNAM-1, NKp44, TRAIL и CD 16. Это ингибирует распознавание NK клеток злокачественных клеток, экспрессирующих их родственные лиганды.
[0008] Существует несколько подходов к созданию NK и Т-клеток, устойчивых к TGF-β. К ним относятся доминантно негативные клетки, экспрессирующие TGFβRII, и комбинированная терапия с использованием низкомолекулярных ингибиторов TGF-β с иммунной терапией. Важно отметить, что все эти способы продемонстрировали повышенную in vitro и in vivo эффективность терапии NK и Т-клетками. Wallace et al, Clin Cancer Res., 14(12): 3966-74 (2008); Bollard, C., Blood, 99: 3179-3187 (2002). Однако ингибирование TGF-β в широком спектре потенциально может привести к неблагоприятным побочным эффектам; поскольку передача сигналов TGF-(3 зависит от контекста и может оказывать как стимулирующее, так и подавляющее опухоль воздействие. Например, ингибирование TGF-β в мышиных моделях увеличивало количество циркулирующих опухолевых клеток (Wrzesinski et al., Clin Cancer Res., 13: 5262-5270 (2007)), а ингибирование TGF-β в широком спектре вызывает глубокое аутоиммунное заболевание. Li et al, Immunity 25: 455-471 (2006). Следовательно, ингибирование TGF-β следует проводить только с осторожностью и после определения чувствительности опухоли к TGF-β. Таким образом, несистемные способы генерирования врожденной устойчивости к TGF-β являются многообещающей альтернативой, позволяющей избежать неблагоприятных эффектов, которые может оказывать системное ингибирование TGF-β.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
[0009] Многие виды рака уменьшают уничтожение NK-клеток высвобождением TGF-β. Авторы изобретения разработали негенетический способ направления (импринтинга) NK клеток для образования устойчивости к TGF-β. TGF-β импринтированные NK клетки (TGFβi NK) были получены путем добавления TGF-β во время стимуляции NK клеток IL-12/15/18. TGFβi NK сохраняли свою цитотоксичность после стимуляции лучше, чем нормальные NK клетки. Дополнительно, TGFβi NK клетки, культивируемые с TGF-β, имеют повышенную секрецию IFN-γ, TNF-α и GM-CSF, что может увеличивать гибель опухоли и в целом стимулировать адаптивный иммунный ответ. Повышенная секреция цитокинов сохраняется более одного месяца. Устойчивость к TGF-β сохраняется в течение как минимум 1 недели in vitro и опосредуется снижением SMAD3.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0010] Настоящее изобретение может быть более понятно со ссылкой на следующие фигуры, где:
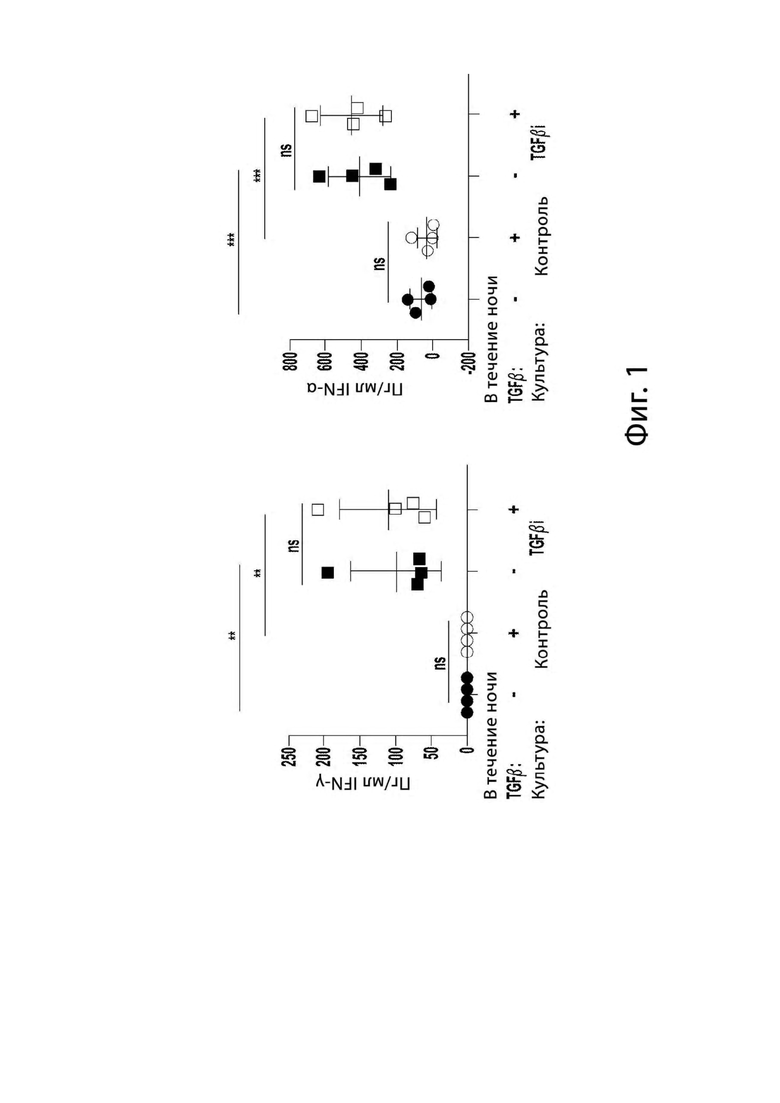
[0011] на Фигуре 1 представлены графики, показывающие, что активация NK клеток родительским (немодифицированным) К562 в присутствии TGFβ индуцирует TGFβi NK клетки с гиперсекрецией цитокинов в ответ на опухолевые мишени. NK клетки стимулировали еженедельно К562 и культивировали в среде, содержащей IL-2 (контроль) или IL-2 и 10 нг/мл TGFB (TGFβi) в течение 14 дней. После культивирования секрецию IFNγ и TNFα оценивали в супернатанте после совместного культивирования с опухолевыми мишенями MG63. Строки и столбцы представляют собой среднее значение ± стандартное отклонение. Статистические различия были определены при помощи двустороннего повторного измерения ANOVA при помощи критерия множественных сравнений Холма-Сидака для всех других графиков. * р≤0,05, ** р≤0,01, *** р≤0,001, **** р≤0,0001.
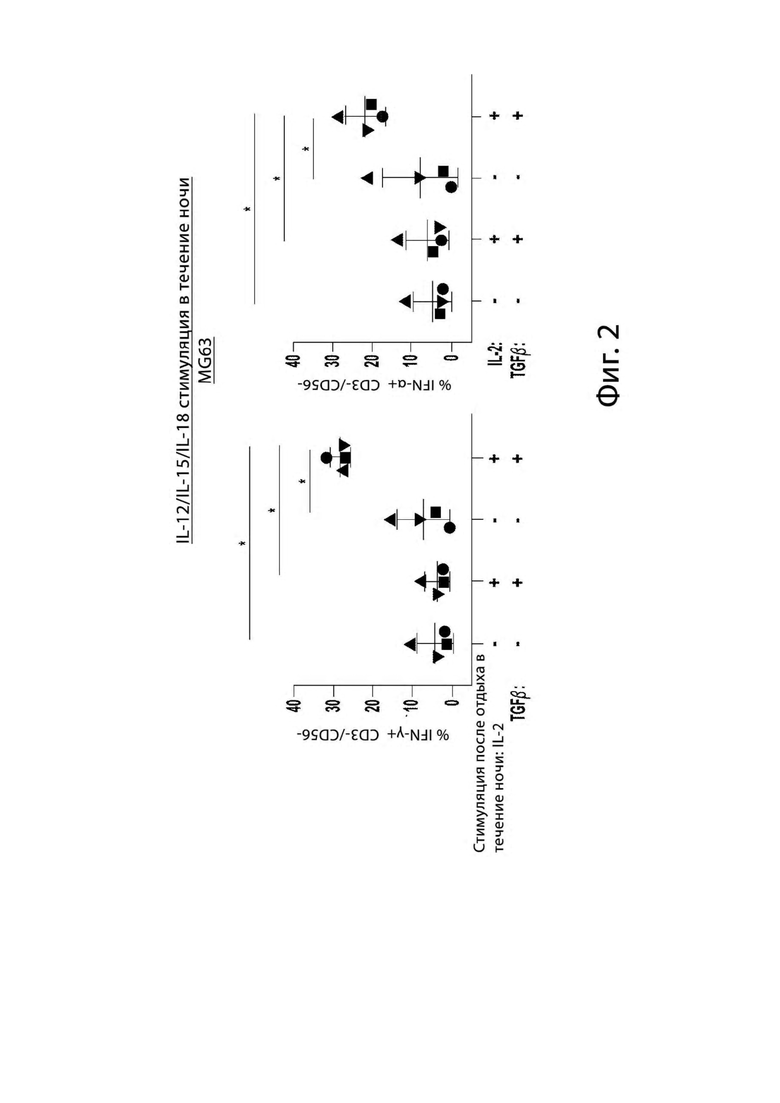
[0012] На Фигуре 2 представлены графики, показывающие, что активация NK клеток провоспалительными цитокинами в присутствии TGFβ индуцирует NK клетки TGFβi с гиперсекрецией цитокинов в ответ на опухолевые мишени. NK-клетки активировали в течение ночи при помощи IL-12, -15 и -18 (10 нг/мл, 50 нг/мл и 50 нг/мл, соответственно) с или без IL-2 и TGFβ, после чего культивировали в IL-15 (1 нг/мл) с или без IL-2 и TGFβ. Через 7-14 дней культивирования продуцирование противоопухолевых IFNγ и TNFα в ответ на MG63 измеряли при помощи внутриклеточной проточной цитометрии (n=4). Процент NK клеток IFNγ+ и TNFα+ нормализовали до отсутствия мишени. Индивидуальные данные точек изображены для всех измерений. Статистические различия были определены при помощи двусторонних повторных измерений ANOVA при помощи критерия множественных сравнений Холма-Сидака для всех других графиков. * р≤0,05, ** р≤0,01, *** р≤0,001, **** р≤0,0001.
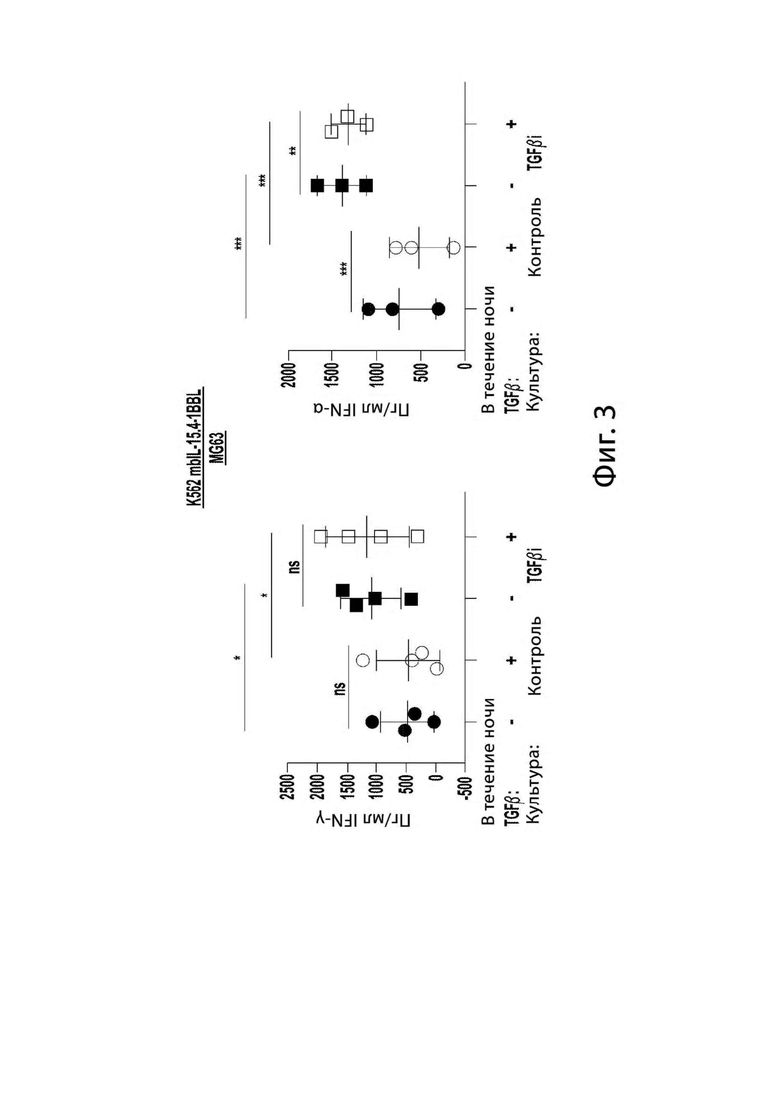
[0013] На Фигуре 3 представлены графики, показывающие, что экспансия NK клеток при помощи питающих клеток K562 mbIL-15 (клон 4) в присутствии TGFβ индуцирует TGFβi NK клетки с гиперсекрецией цитокинов в ответ на опухолевые мишени. После 14-дневного размножения питающими клетками с (TGFβi) или без (контроль), NK-клетки оставляли на ночь в 50 МЕ/мл IL-2 с или без 10 нг/мл TGFβ. Затем NK-клетки совместно культивировали с опухолевыми мишенями в той же среде, и супернатанты собирали для измерения секреции цитокинов. Контроль показан черным, TGFβi - красным. Статистические различия были определены при помощи двустороннего повторного измерения ANOVA при помощи критерия множественных сравнений Холма-Сидака для всех остальных. * р≤0,05, ** р≤0,01, *** р≤0,001, **** р≤0,0001.
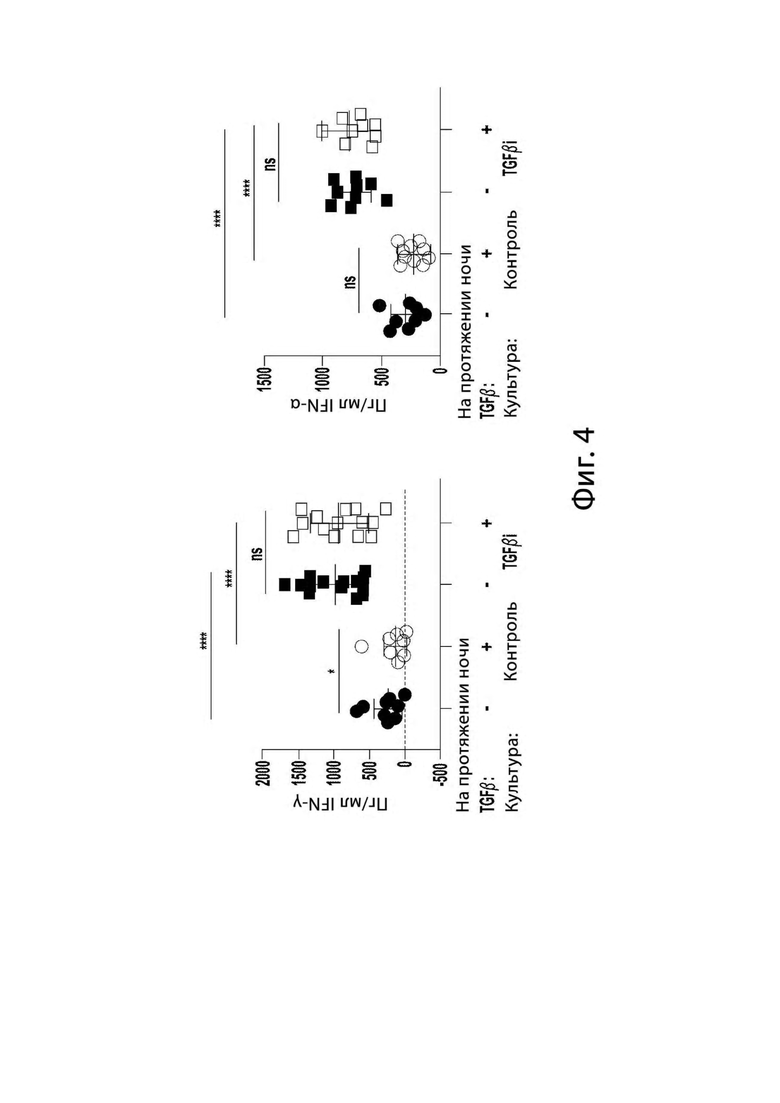
[0014] На Фигуре 4 представлены графики, показывающие, что экспансия NK клеток питающими клетками K562 mbIL-21 в присутствии TGFβ индуцирует TGFβi NK клетки с повышенной секрецией цитокинов в ответ на опухолевые мишени. После 14-дневного размножения при помощи питающих клеток с (TGFβi) или без (контроль) TGFβ, NK клетки оставляли в течение ночи в 50 МЕ/мл IL-2 с или без 10 нг/мл TGFβ. Затем NK-клетки совместно культивировали с опухолевыми мишенями в той же среде, и супернатанты собирали для измерения секреции цитокинов. Контроль показан черным, TGFβi - красным. Статистические различия были определены при помощи двустороннего повторного измерения ANOVA при помощи теста множественных сравнений Холма-Сидака для всех остальных. * р<0,05, ** р<0,01, *** р<0,001, **** р<0,0001.
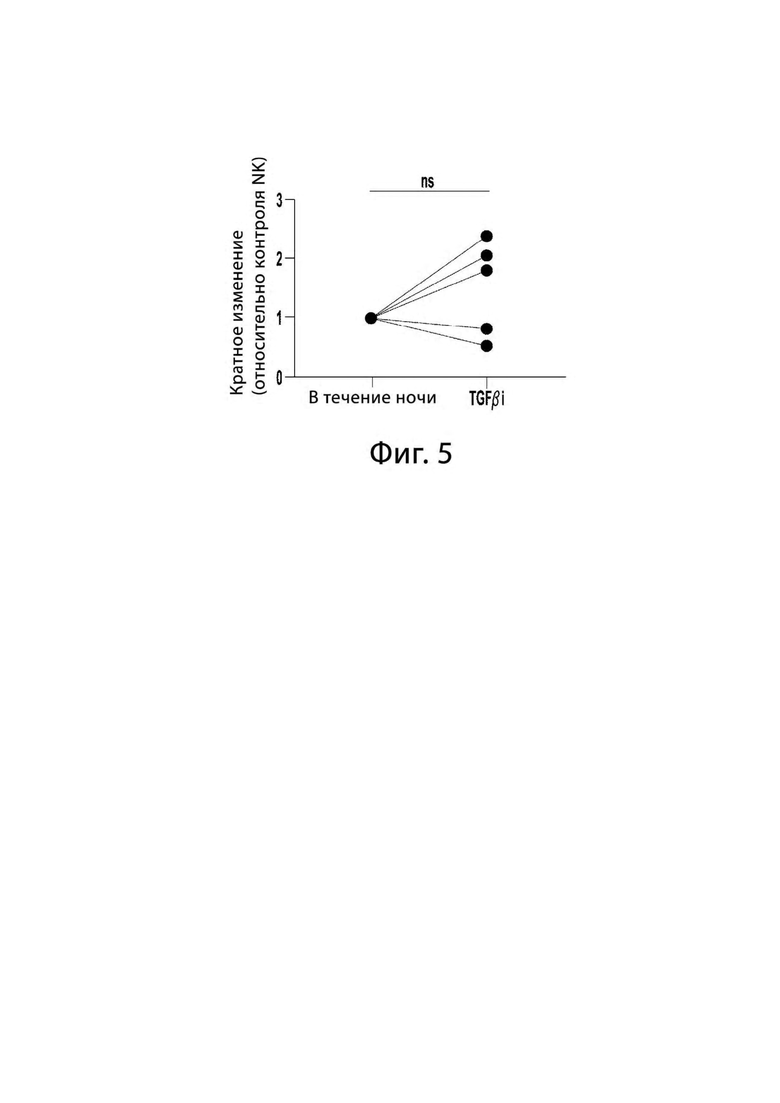
[0015] На Фигуре 5 представлен график, показывающий, что добавление TGFβ для генерации TGFβi NK клеток не снижает пролиферативный потенциал в культурах размножения с питающими клетками K562 mbIL-21 (CSTX002). NK клетки размножали в течение 14 дней на питающих клетках с (TGFβi) или без (контроль) TGFβ в парных культурах от 5 доноров, начиная с того же числа клеток в День 0. Показано общее количество жизнеспособных клеток через 14 дней, нормализованное для контроля NK клеток для каждого парного размножения. Незначительно согласно парному t-критерию Стьюдента.
[0016] На Фигуре 6 представлены графики, показывающие, что NK клетки TGFβi поддерживают гиперсекрецию цитокинов по отношению к опухолевым клеткам в течение нескольких недель. A) TGFβi и контрольные NK клетки, размноженные родительскими питающими клетками K562 в течение 14 дней (размножение), или размноженные и оставленные в течение дополнительных 7 дней (отдых), культивировали совместно с клетками-мишенями MG63 и супернатант оценивали на секрецию цитокинов. В) В аналогичном эксперименте секрецию цитокинов по отношению к MG63 с расширенным контролем K562mbIL-21 и NK клетками TGFβi оценивали на 7-й и 14-й день размножения и снова после отдыха на 21-й, 35-й и 47-й День. Среднее значение с изображением минимальных и максимальных усов. Контроль в черном, TGFβi в красном. Статистические различия были определены парным t-тестом * р≤0,05, ** р≤0,01, *** р≤0,001, **** р≤0,0001.
[0017] На Фигуре 7 представлены графики, показывающие, что NK клетки TGFβi проявляют повышенную секрецию цитокинов против различных типов рака. После 14-дневного размножения в контрольных условиях или в присутствии TGFβ для индукции TGFβi NK клеток NK клетки оставляли в течение ночи с IL-2 или TGFβ или без них. Затем NK клетки совместно культивировали с опухолевыми мишенями в той же свежей среде в течение 3 часов, и супернатанты собирали для измерения секреции цитокинов IFNγ и TNFα. Индивидуальные точки данных изображены для DAOY (медуллобластома, n=12) и CHLA-255 (нейробластома, n=5). Строки и столбцы представляют собой среднее значение ± стандартное отклонение.
[0018] На Фигуре 8 представлен график, показывающий, что NK клетки TGFβi демонстрируют резкое подавление TGFβi-сигнального белка SMAD3. После 14 дней размножения в контрольных условиях или при наличии TGFβ для индукции TGFβi NK клеток, NK клетки оценивали на экспрессию белка SMAD3 и Е4ВР4 (n=4) при помощи анализа вестерн-блоттинг.
[0019] На Фигуре 9 представлен график, показывающий, что TGFβi NK клетки гиперсекретируют GM-CSF, TNFα и IFNγ. Контрольные и TGFβi NK клетки стимулировали 10 мкг/мл РНА при 2×106 NK клеток/мл в течение 4 часов и измеряли секрецию цитокинов. Строки и столбцы представляют собой среднее значение ± стандартное отклонение. Статистические различия были определены при помощи парного t-теста.
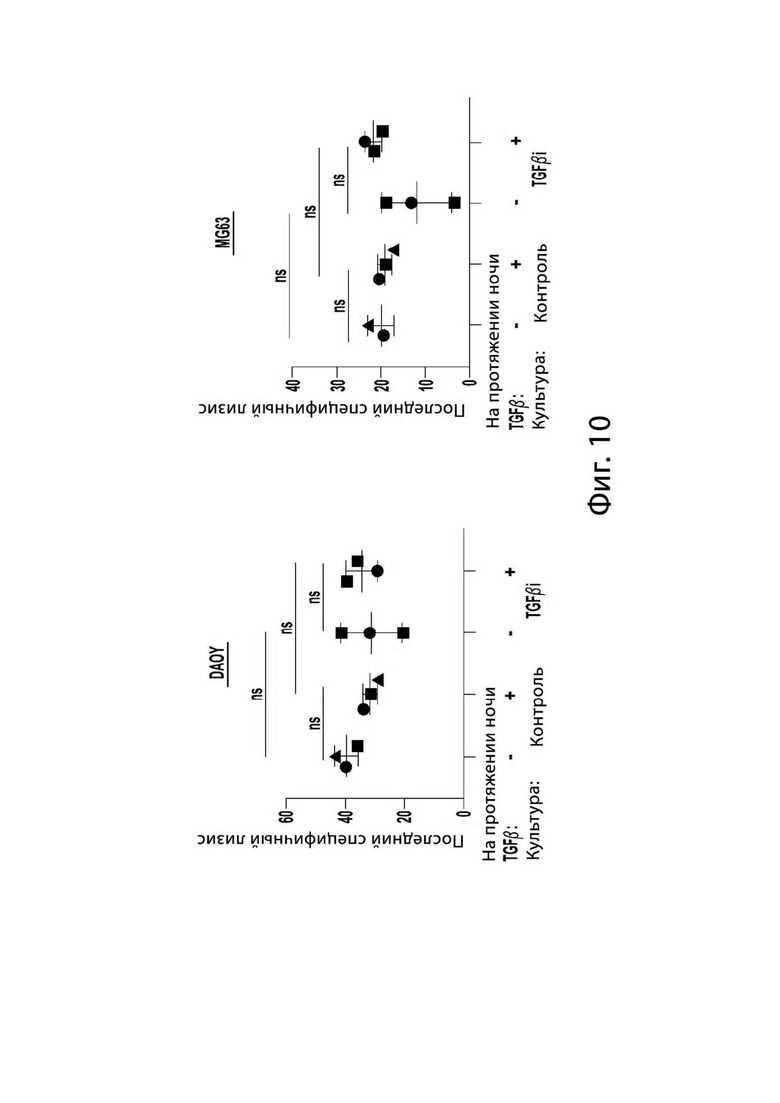
[0020] На Фигуре 10 представлены графики, показывающие, что TGFβi NK клетки, размноженные родительским K562, обладают сходной цитотоксичностью с контрольными NK клетками. Цитотоксичность контроля и TGFβi NK-клеток измеряли, используя 4-часовой анализ цитотоксичности с высвобождением кальцеина, после обработки в течение ночи только IL-2 или IL-2 и TGFβ. Строки и столбцы представляют собой среднее значение ± стандартное отклонение. Статистические различия были определены при помощи двусторонних повторных измерений ANOVA при помощи теста множественных сравнений Холма-Сидака. * р≤0,05, ** р≤0,01, *** р≤0,001, **** р≤0,0001.
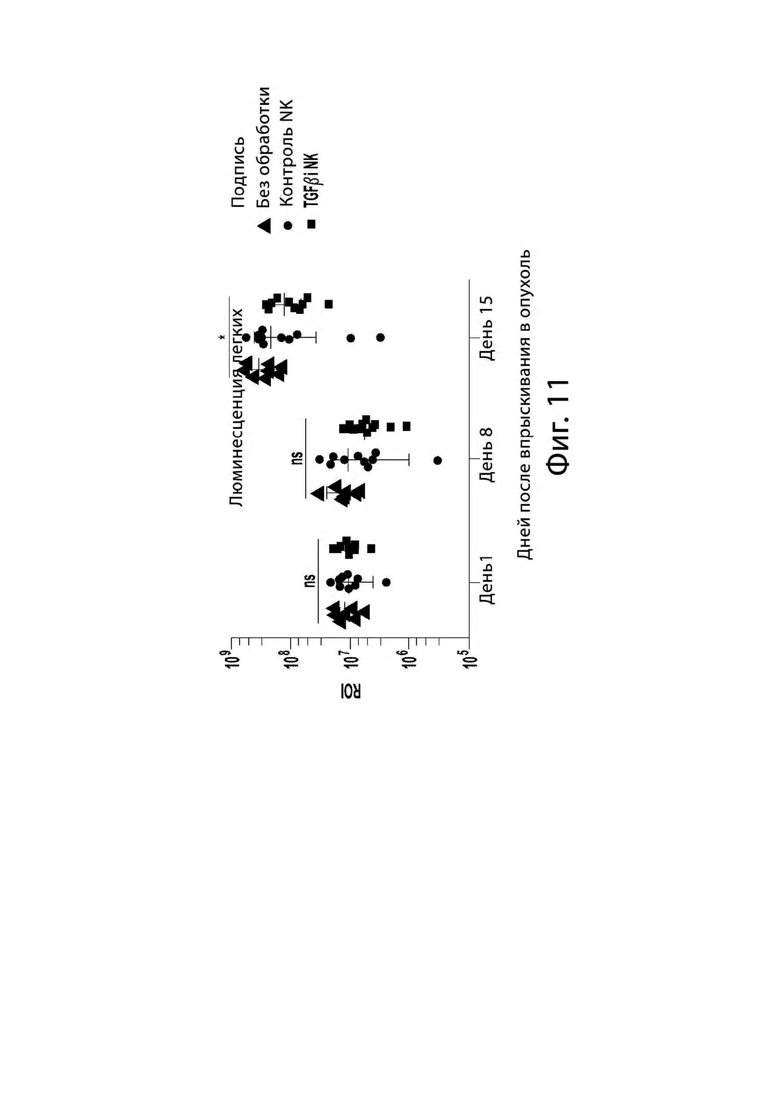
[0021] На Фигуре 11 представлен график, показывающий, что размноженные NK клетки TGFβi контролируют рост опухоли лучше, чем контрольные размноженные NK клетки на мышиной модели остеосаркомы. Обработка мышей NK клетками TGFβi, размноженными на питающих клетках K562mbIL-21, но не контролирующих NK-клетках, значительно снижает рост клеточной линии остеосаркомы 143b в легких мышей NSG.
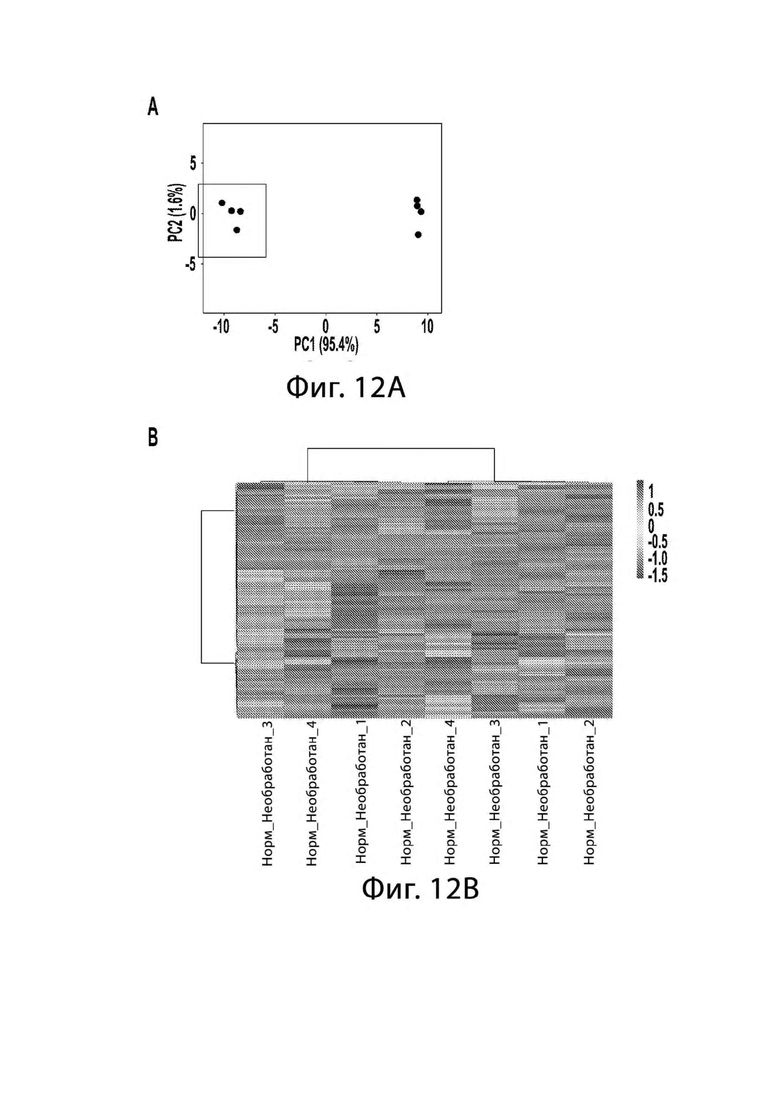
[0022] На Фигуре 12 представлены графики, показывающие, что NK клетки TGFβi имеют профиль экспрессии генов, который отличает их от стандартных размноженных NK клеток. Стандартные и TGFβi NK клетки размножали попарно на CSTX002 от 4 доноров. мРНК выделяли и подвергали секвенированию РНК. Были идентифицированы лучшие 100 дифференциально экспрессированных генов. А) Был проведен анализ основных компонентов, в котором исходные значения были преобразованы в ln (х+1). Единичное масштабирование вариации применяется к строкам; SVD с условной подстановкой используется для расчета основных компонентов. Оси X и Y показывают основной компонент 1 и основной компонент 2, которые объясняют 95,4% и 1,6% от общей вариации, соответственно. Клетки TGFβi NK обозначены в красной рамке. Более 95% дисперсии обусловлено импринтингом TGFβ, в то время как менее 2% является результатом вариации доноров. В) Кластерный анализ был выполнен на тех же лог-преобразованных данных. Ряды центрированы; единичное масштабирование вариации применяется к строкам. Как строки, так и столбцы сгруппированы с использованием расстояния корреляции и средней связи.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0023] Настоящее изобретение относится к клеткам TGF-β с импринтингом естественных киллеров (TGFβi NK), которые обладают высокой цитотоксичностью, продуцируют высокие уровни цитокинов и устойчивы к суперсемейству TGF-β иммуносупрессивных цитокинов. Эти клетки могут быть получены путем хронической активации in vitro естественных клеток-киллеров в присутствии цитокина суперсемейства TGF-β. Изобретение также относится к способу лечения рака или инфекции у субъекта, нуждающегося в таком лечении, путем введения субъекту терапевтически эффективного количества NK клеток TGFβi.
Определения
[0024] Для ясности понимания и для облегчения ссылок в данной заявке составлен список терминов, использованных в разделе краткого описания и в остальной части данной заявки. Некоторые термины хорошо известны в данной области техники и определены в данной заявке для ясности, тогда как некоторые термины являются уникальными для данной заявки и поэтому должны быть определены для правильного понимания данной заявки.
[0025] Формы единственного числа в данной заявке означают один или более чем один; по меньшей мере один. Если в данной заявке используется форма множественного числа, она обычно включает единственное число.
[0026] Также в данной заявке числовые диапазоны, приведенные по конечным точкам, включают все числа, включенные в этот диапазон (например, от 1 до 5 включает в себя 1, 1,5, 2, 2,75, 3, 3,80, 4, 5 и т.д.).
[0027] В контексте данного документа, «субъект» может относиться к любому теплокровному организму, включая, но не ограничиваясь приведенным, людей, крыс, мышей, собак, коз, овец, лошадей, обезьян, обезьян, свиней, кроликов, крупный рогатый скот и т.д. Если термин используется в контексте субъекта, нуждающегося или требующего композиций по настоящей заявке, этот термин может быть приведен как «субъект, нуждающийся в этом» и включать субъекты, которые были клинически диагностированы (например, медицинским работником, например, врачом), как нуждающиеся в композициях по настоящей заявке, субъекты, которые подозреваются в том, что им необходимы композиции по настоящей заявке, субъекты, подверженные риску заболевания или состояния, и которые могут извлечь пользу из композиций по настоящей заявке, и субъекты, которые уже страдают от заболевания или состояния и которые могут извлечь пользу из композиций по настоящей заявке.
[0028] Термин «фармацевтически приемлемый», в контексте данного документа, относится к тем соединениям, материалам, композициям и/или лекарственным формам, которые в рамках здравого медицинского обоснования пригодны для использования в контакте с тканями людей и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнений, соразмерных с разумным соотношением польза/риск.
[0029] Термин «терапевтически эффективный» предназначен для определения количества агента, который будет достигать цели снижения тяжести заболевания, избегая неблагоприятных побочных эффектов, таких как те, которые обычно связаны с альтернативной терапией. Терапевтически эффективное количество можно вводить в одной или более доз. Лечение, которое является терапевтически эффективным, включает лечение, которое улучшает качество жизни субъекта, даже если оно само по себе не улучшает исход заболевания.
[0030] «Эффективное количество» обычно означает количество, которое обеспечивает желаемый локальный или системный эффект, например, эффективное для стимуляции образования цитокинов, включая достижение конкретных желательных эффектов, описанных в настоящей заявке. Например, эффективное количество представляет собой количество, достаточное для достижения полезного или желаемого клинического результата.
[0031] «Лечить», или «лечение» широко используются в отношении изобретения, и каждый такой термин включает, среди прочего, предотвращение, улучшение, ингибирование или лечение дефицита, дисфункции, заболевания или другого вредного процесса, включая те, которые мешают и/или являются результатом терапии. В различных вариантах воплощения симптомы заболевания или расстройства ослабляются, по меньшей мере, на 5%, по меньшей мере, на 10%, по меньшей мере, на 20%, по меньшей мере, на 30%, по меньшей мере, на 40% или, по меньшей мере, на 50%.
[0032] В контексте данного документа, термин «вводить» относится к размещению композиции (например, клеточной композиции) в субъекте способом или путем, который приводит, по меньшей мере, к частичной локализации композиции в желательном месте, так что производится желаемый эффект. Устойчивые природные клетки-киллеры или композиции, описанныев данной заявке, могут вводиться любым подходящим маршрутом, известным в данной области техники, включая, но не ограничиваясь приведенным, пероральный или парентеральный маршруты, включая внутривенный, внутримышечный, подкожный, трансдермальный, дыхательный маршруты (аэрозоль), легочное, назальное, ректальное и местное (в том числе буккальное и подъязычное) введение.
[0033] В контексте данного документа, термин «цитокин» относится к небольшому белку (~ 5 ~ 20 кДа), который важен для передачи сигналов в клетке и, в частности, для иммуномодуляции. Примеры цитокинов включают хемокины, интерфероны, интерлейкины, лимфокины и факторы некроза опухолей.
Лечение с использованием TGFBi NK клеток
[0034] В одном аспекте, настоящее изобретение относится к способу лечения рака или инфекции у субъекта, нуждающегося в этом. Способ включает введение субъекту терапевтически эффективного количества клеток TGF-β с импринтингом естественных киллеров (TGFβi NK). Как описано в данной заявке, TGFβi NK клетки могут быть более эффективными и сохраняться дольше in vivo по сравнению с типичными размноженными естественными клетками киллерами, поскольку их устойчивость к цитокинам суперсемейства TGF-β защищает их от подавления иммунной системой.
[0035] В контексте данного документа, термин «естественные клетки-киллеры» («NK клетки») относится к типу цитотоксических лимфоцитов иммунной системы. NK клетки обеспечивают быстрый ответ на инфицированные вирусом клетки и отвечают на трансформированные клетки. Как правило, иммунные клетки обнаруживают пептиды от патогенов, представленных молекулами Большого комплекса гистосовместимости (МНС), на поверхности инфицированных клеток, вызывая высвобождение цитокинов, вызывая лизис или апоптоз. Однако NK клетки уникальны, так как обладают способностью распознавать стрессовые клетки независимо от того, присутствуют ли пептиды из патогенов на молекулах МНС. Их назвали «естественными киллерами» из-за первоначального представления о том, что они не требуют предварительной активации, чтобы убить цель. NK клетки представляют собой крупные гранулярные лимфоциты (LGL) и, как известно, дифференцируются и созревают в костном мозге, откуда они затем попадают в кровообращение.
[0036] Данное изобретение включает в себя NK клетки, которые устойчивы к цитокинам суперсемейства трансформирующего фактора роста-бета (TGF-β), и способы получения и использования таких устойчивых NK клеток. Суперсемейство TGF-β представляет собой большую группу структурно родственных регуляторных белков клеток. TGF-β является многофункциональным пептидом, который контролирует пролиферацию, дифференцировку и другие функции во многих типах клеток. TGF-β-1 представляет собой пептид из 112 аминокислотных остатков, полученный путем протеолитического отщепления от С-конца белка-предшественника. Эти белки взаимодействуют с консервативным семейством серин-треонин-специфических рецепторов протеинкиназы клеточной поверхности и генерируют внутриклеточные сигналы с использованием консервативного семейства белков, называемых SMAD. Основные подсемейства суперсемейства TGF-β включают подсемейство TGF-β (включая изоформы TGF-β 1-4), белки, связанные с декапентаплегическим Vg (DVR) (например, костный морфогенный белок), факторы роста и дифференцировки (например, GDF-1 - GDF-15) и подсемейство активина и ингибина. В некоторых вариантах воплощения изобретения TGFβi NK клетки устойчивы к TGF-β.
[0037] Клетки TGFβi NK можно использовать для лечения рака или инфекции у субъекта. Клетки TGFβ NK обычно вводят путем адоптивного переноса клеток. В некоторых вариантах воплощения изобретения у субъекта был диагностирован рак. Рак, как определено в данной заявке, представляет собой заболевание, основанное на развитии клеток, которые содержат генетическое повреждение, приводящее к относительно неограниченному росту клеток. Генетическое повреждение, присутствующее в раковой клетке, сохраняется в качестве наследуемого признака в последующих поколениях линии раковых клеток. Рак, леченный способом в соответствии с данным изобретением, может представлять собой любую из форм рака, известных специалистам в данной области техники или описанных в данной заявке. Можно лечить рак, который проявляется как солидные опухоли, а также рак, который вместо этого образует несолидные опухоли, как это обычно наблюдается при лейкемии. Настоящее изобретение предлагает способы лечения субъекта, который поражен различными различными типами рака, включая рак, саркому и лимфому.
[0038] В некоторых вариантах воплощения рак, подвергаемый лечению, представляет собой лейкоз (например, острый лимфобластный лейкоз; острый миелоидный лейкоз; хронический миелогенный лейкоз, хронический лимфоцитарный лейкоз), миелодиспластический синдром, лимфому (например, В-клеточную неходжкинскую лимфому, лимфому Ходжкина, Т-клеточную лимфобластную лимфому, анапластическую крупноклеточную лимфому), солидную опухоль (например, рак молочной железы, рак простаты, рак желудка, рак толстой кишки, гепатоцеллюлярную карциному, рак носоглотки, нейробластому, глиому высокой степени тяжести), саркому (например, саркому Юинга, рабдомиосаркому, не рабдомиосаркомную саркому мягких тканей, остеосаркому). В других вариантах воплощения изобретения рак выбран из группы, состоящей из лейкемии, лимфомы, рабдомиосаркомы, рака головного мозга и рака кости.
[0039] Эффективность лечения рака может быть определена путем оценки снижения опухолевой нагрузки или уменьшения роста опухоли у субъекта в ответ на введение TGFβi NK клеток. Снижение опухолевой нагрузки может представлять собой прямое уменьшение массы или может быть измерено с точки зрения задержки роста опухоли, которая рассчитывается путем вычитания среднего времени роста контрольных опухолей до определенного объема из времени, необходимого для достижения опухолями, которые лечат, такого же объема.
[0040] В других вариантах воплощения субъект, которого лечат, имеет инфекционное заболевание. TGFβi NK клетки оказывают системное действие широкого спектра и могут быть использованы для лечения инфекции различными микроорганизмами. В контексте данного документа, «инфекционные заболевания» означает, что они включают все заболевания, которые вызваны инфицированием вирусами, патогенными бактериями или грибками, при этом инфицирование может произойти через органы дыхания, кровь или кожу. Неограничивающие примеры таких инфекционных заболеваний включают, но не ограничиваются приведенным, гепатит В, гепатит С, инфекцию вирусом папилломы человека (HPV), вирус иммунодефицита человека (HIV), цитомегаловирусную инфекцию, вирусные респираторные заболевания, грипп и так далее.
TGF-β импринтинговые естественные клетки-киллеры
[0041] Другой аспект данного изобретения относится к естественной клетке-киллеру (NK) или клечной линии NK, культивируемых в присутствии суперсемейства цитокинов TGF-β, называемых в данной заявке TGFβi NK клетками. Это включает в себя NK клетки или клеточную линию, полученные способами, описанными в данной заявке, и композиции, содержащие NK клетки, представленные в данной заявке. В конкретном аспекте композиция представляет собой фармацевтическую композицию, содержащую одну или более NK клеток или клеточных линий, представленных в данной заявке. В некоторых вариантах TGFβi NK клетки проявляют повышенную устойчивость к TGF-β.
[0042] TGFβi NK клетки могут быть аллогенными или аутологичными клетками. В некоторых аспектах NK клетка представляет собой NK клетку млекопитающего. Примеры "млекопитающих" включают приматов (например, человека), собак, кошек, грызунов, свиней, жвачных животных и тому подобное. Конкретные примеры включают людей, собак, кошек, лошадей, коров, овец, коз, кроликов, морских свинок, крыс и мышей. В конкретном варианте воплощения изобретения NK клетка млекопитающего представляет собой NK клетку человека.
[0043] NK-клетки TGFβi проявляют ряд характеристик, которые отличают их от NK-клеток природного происхождения. В таких вариантах воплощения NK клетки или клеточные линии проявляют повышенную устойчивость к TGF-β. В других вариантах воплощения изобретения NK клетки продуцируют и увеличивают количество интерферона-γ (IFN-γ) и/или фактора некроза опухолей-α (TNF-α) и/или гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF). В других вариантах воплощения изобретения NK-клетки демонстрируют пониженные уровни белка члена семейства SMAD 3 (SMAD3) и/или белка бета-рецептора III трансформирующего фактора роста (TGFBR3). SMAD-белки получили свое название как сокращение названий С. elegans Sma и Drosophila Mad (Derynck et al., Cell, 95(6), p737~740, 1998) и являются активаторами транскрипции ответов TGF-β.
[0044] TGFβi NK клетки проявляют ряд характеристик, которые отличают их от NK-клеток природного происхождения. В некоторых вариантах воплощения NK-клетки имеют профиль экспрессии гена, по существу сходный с показанным на Фигуре 12. Профиль экспрессии гена, который по существу сходен, представляет собой профиль, в котором экспрессия гена находится в пределах 10% от показанного. В некоторых вариантах воплощения изобретения TGFβi NK клетки продуцируют повышенные количества одного или более белков IFN-γ, TNF-α и GM-CSF. В некоторых вариантах воплощения изобретения NK клетки или клеточные линии демонстрируют повышенную экспрессию SCUBE1, MYO7A, KLF3, WIPF3 и ЕРНА1.
[0045] TGFβi NK клетки проявляют ряд характеристик, которые отличают их от NK клеток природного происхождения. В некоторых вариантах воплощения изобретения TGFβi NK клетки демонстрируют пониженные уровни белка SMAD3 и/или белка TGFBR3. В некоторых вариантах воплощения изобретения NK клетки или клеточные линии демонстрируют пониженную экспрессию CD300A, SGSM1, SMAD3, ТВХ21 и GZMK, TGFBR3 и GZMA.
Получение клеточной линии естественных киллеров, импринтированной к TGF-β-суперсемейству (TGFβi NK)
[0046] В другом аспекте настоящего изобретения предложен способ получения клеточной линии естественных киллеров, импринтированной к TGF-β-суперсемейству (TGFβi NK), включающий активацию in vitro естественных клеток киллеров в присутствии цитокина TGF-β-суперсемейства. Способы могут дополнительно включать выделение или отделение одной или более TGFβi NK клеток, полученных способами, представленными в данной заявке. Кроме того, способы могут дополнительно включать культивирование одной или более TGFβi NK клеток. В некоторых вариантах воплощения изобретения получают клеточную линию TGFβi NK. В некоторых вариантах воплощения изобретения клеточная линия TGFβi NK размножается в присутствии TGF-β. Клеточная линия представляет собой множество клеток, которые могут поддерживаться в клеточной культуре.
[0047] Размножение (т.е. активация) относится к пролиферации NK клеток ex vivo, так что популяция NK клеток увеличивается. NK клетки могут быть размножены, например, из мононуклеарных клеток периферической крови. Однако NK клетки также могут быть размножены из других типов клеток, таких как гематопоэтические стволовые клетки или клетки-предшественники. Исходная кровь или стволовые клетки могут быть выделены из множества различных источников, таких как плацента, пуповинная кровь, плацентарная кровь, периферическая кровь, селезенка или печень. Размножение происходит в среде для культивирования клеток. Подходящие среды для культивирования клеток известны специалистам в данной области техники и включают в себя базальную среду Игла (ВМЕ), модифицированную по Дульбекко среду Игла (DMEM), минимальную основную среду Глазго (GMEM), модифицированную по Дульбекко среду Игла/питательную смесь F-12 Ham (DMEM/F-12), минимальную поддерживающую среду (MEM), среду Дульбекко в модификации Искова (IMDM), питательную смесь F-10 Ham (Ham's F-10), питательную смесь F-12 Ham (Ham's F-12), среду RPMI-1640, среду Вильямса Е, STEMSPAN® (Кат. № Stem Cell Technologies, Vancouver, Canada), основную питательную среду Glycostem (GBGM®), среду AIM-V® (Invitrogen), X-VIVO™ 10 (Lonza), X-VIVO.TM. 15 (Lonza), OPTMIZER (Invitrogen), STEMSPAN® H3000 (STEMCELL Technologies), CELLGRO COMPLETE™ (Mediatech) или любые их модифицированные варианты или комбинации.
[0048] В контексте данного документа, термин «питающие клетки» относится к клеткам, которые не обладают способностью делиться и пролиферировать, но обладают метаболической активностью и, таким образом, продуцируют различные метаболические продукты, способствующие пролиферации NK клеток-мишеней. Примеры питающих клеток, которые можно использовать в настоящем изобретении, включают, но не ограничиваются приведенным, линии клеток животных, введенные с генами, лейкоциты периферической крови (PBL), обработанные различными цитокинами или соединениями, аутологичные или аллогенные лейкоциты периферической крови (PBL), Т-клетки, В-клетки, моноциты и тому подобное. В некоторых вариантах воплощения изобретения питающими клетками являются питающие клетки K562. В дополнительных вариантах воплощения изобретения питающие клетки K562 выбраны из клеток клона 4, клеток клона 9 и клеток CSTX002.
[0049] В некоторых вариантах воплощения изобретения активация in vitro естественных клеток-киллеров осуществляется в присутствии NK-стимулирующей экзосомы или NK-стимулирующей наночастицы. Экзосомы представляют собой небольшие внеклеточные везикулы, полученные из эндосом, с диаметром 30-100 нм. Полученные из опухолей экзосомы переносят большое количество молекул и факторов из опухолевых клеток и могут быть использованы для стимуляции естественных клеток-киллеров. См. Li et al, Exp Cell Res., 363(2): 141-150 (2018). Наночастицы также можно использовать для стимуляции естественных клеток-киллеров. Наночастицы представляют собой частицы размером от 1 до 2500 нм с окружающим межфазным слоем. Они включают сверхмалые наночастицы размером от 1 до 100 нм и тонкие наночастицы размером от 100 до 2500 нм. Наночастицы могут быть получены с использованием полимера или минералов, таких как оксид графена. В некоторых вариантах воплощения изобретения наночастицы функционализированы для включения дополнительных групп, таких как антитела, которые помогают стимулировать естественные клетки-киллеры. См., например, Loftus et al., Nano Lett., 18(5): 3282-3289 (2018).
Дозировка и введение
[0050] TGFβi NK клетки следует вводить и дозировать в соответствии с надлежащей медицинской практикой, принимая во внимание место и способ введения, график введения, возраст пациента, пол, массу тела, природу и тяжесть расстройства, которое нужно лечить или предотвращать, и другие факторы, известные практикующим специалистам в области медицины. Клетки могут быть введены в виде одной дозы или в разделенных дозах. Таким образом, фармацевтически «эффективное количество» для целей настоящего изобретения определяется такими соображениями, которые известны в данной области техники. Количество должно быть эффективным для достижения улучшения, включая, но не ограничиваясь, улучшенную выживаемость или более быстрое выздоровление, или улучшение или устранение симптомов и других показателей, которые выбраны в качестве соответствующих мер специалистами в данной области техники.
[0051] Как правило, указанная доза составляет приблизительно 10×106 клеток/кг массы тела субъекта или менее, составляет приблизительно 9×106 клеток/кг или менее, составляет приблизительно 8×106 клеток/кг или менее, составляет приблизительно 7×106 клеток/кг или менее, составляет приблизительно 6×106 клеток/кг или менее, составляет приблизительно 5x106 клеток/кг или менее. В альтернативном варианте воплощения изобретения указанная доза может составлять от приблизительно 0,25×106 клеток/кг до приблизительно 5×106 клеток/кг; или более предпочтительно от приблизительно 1×106 клеток/кг до приблизительно 5x106 клеток/кг. Соответственно, в других альтернативных вариантах воплощения изобретения доза может составлять приблизительно 0,25x106 клеток/кг, 0,5×106 клеток/кг, 0,6×106 клеток/кг, 0,7×106 клеток/кг; 0,8×106 клеток/кг; 0,9×106 клеток/кг; 1,1×106 клеток/кг; 1,2×106 клеток/кг; 1,3×106 клеток/кг; 1,4×106 клеток/кг; 1,5×106 клеток/кг; 1,6×106 клеток/кг; 1,7×106 клеток/кг; 1,8×106 клеток/кг; 1,9×106 клеток/кг или 2×106 клеток/кг. В других вариантах воплощения доза может составлять от 0,1 до 1 миллиона клеток/кг; или от 1 до 2 миллионов клеток/кг; или от 2 до 3 миллионов клеток/кг; или от 3 до 4 миллионов клеток/кг; или от 4 до 5 миллионов клеток/кг; или от 5 до 6 миллионов клеток/кг; или от 6 до 7 миллионов клеток/кг; или от 7 до 8 миллионов клеток/кг; или от 8 до 9 миллионов клеток/кг; или от 9 до 10 миллионов клеток/кг.
[0052] Типичные способы введения включают, но не ограничиваются приведенным, инъекцию, инфузию, инсталляцию, ингаляцию или прием внутрь. Инъекция» включает, без ограничения, внутривенную, внутримышечную, внутриартериальную, интратекальную, интравентрикулярную, внутрикапсулярную, интраорбитальную, внутрисердечную, внутрикожную, внутрибрюшинную, транстрахеальную, подкожную, субкутикулярную, внутрисуставную, субкапсулярную, субарахноидальную, интраспинальную, интрацеребро-спинальную, а также внутрикожную инъекцию и инфузию. В предпочтительных вариантах воплощения изобретения композиции вводят при помощи внутривенной инфузии или инъекции.
[0053] TGFβi NK клетки могут доставляться в форме фармацевтической композиции, содержащей изотонический эксципиент, полученный в достаточно стерильных условиях для введения человеку. Композиция может быть стерильной. Состав должен соответствовать способу введения. Для общих принципов составления лекарственного средства, читатель отсылается к Cell Therapy: Stem Cell Transplantation, Gene Therapy, and Cellular Immunotherapy, G. Morstyn & W. Sheridan eds, Cambridge University Press, 1996; и Hematopoietic Stem Cell Therapy, E. D. Ball, J. Lister & P. Law, Churchill Livingstone, 2000. Выбор клеточного эксципиента и любых сопутствующих элементов композиции, включающей популяцию TGFβi NK клеток, будет адаптирован в соответствии с маршрутом и устройством, используемым для введения.
[0054] В некоторых вариантах воплощения изобретения TGFβi NK клетки вводят вместе с фармацевтически приемлемым носителем. Подходящие фармацевтически приемлемые носители включают, но не ограничиваются приведенным, воду, солевые растворы (например, NaCl), физиологический раствор, забуференный солевой раствор, спирты, глицерин, этанол, гуммиарабик, растительные масла, бензиловые спирты, полиэтиленгликоли, желатин, углеводы, такие как лактоза, амилоза или крахмал, декстроза, стеарат магния, тальк, кремниевая кислота, вязкий парафин, парфюмерное масло, сложные эфиры жирных кислот, гидроксиметилцеллюлоза, поливинилпирролидон и др., а также их комбинации. Фармацевтические препараты могут, если это желательно, смешиваться со вспомогательными агентами, например, смазывающими веществами, консервантами, стабилизаторами, смачивающими агентами, эмульгаторами, солями для воздействия на осмотическое давление, буферами, красителями, ароматизаторами и/или ароматическими веществами и т.д., которые не оказывают вредного воздействия при реакции с активными соединениями.
[0055] Следующий пример включен для демонстрации предпочтительных вариантов воплощения изобретения. Специалистам в данной области техники должно быть понятно, что методики, раскрытые в примере, который следует ниже, представляют собой методики, открытые изобретателем для эффективного функционирования при практическом применении изобретения, и, таким образом, могут рассматриваться как составляющие предпочтительные способы его применения. Однако специалистам в данной области техники в свете настоящего раскрытия должно быть понятно, что в конкретных вариантах воплощения изобретения, которые раскрыты, могут быть сделаны многие изменения, и все же будет получен аналогичный или похожий результат, не выходя за пределы сущности и объема данного изобретения.
ПРИМЕР
Пример 1: Импринтинг NK клеток TGF-β для устойчивости к TGF-β
[0056] Авторы изобретения сгенерировали человеческие NK клетки, размноженные культурой TGF-β (TGFβi NK), которые имеют пониженную чувствительность к TGF-β, наиболее вероятно, из-за потери одного из ключевых сигнальных белков TGF-β-SMAD3. Авторы изобретения демонстрируют: a) TGFβi NK клетки значительно повышают секрецию IFN-γ, TNF-α и GM-CSF против опухолевых мишеней и б) TGFβi NK клетки сохраняют гиперсекрецию цитокинов в течение по меньшей мере 1 месяца после активации.
Способы
[00571 Культура клеток: NK клетки культивировали в среде RPMI 1640, дополненной Glutamax, 10% FBS и антибиотиками. Все клетки регулярно тестировали на загрязнение микоплазмой с использованием Lonza MycoAlert (Lonza, LT027-58) и обнаружили, что тесты были негативными во все моменты времени. Питающие клетки K562 были приобретены у АТСС (CCL-243) и облучены при 100 Гр.
[0058] Размножение NK клеток: очищенные первичные NK клетки человека стимулировали в День 0 1:2 облученным K562 и 1: 1 в День 7. Используемые клеточные линии K562 указаны в подписях к Фигурам как немодифицированные (родительские), экспрессирующие 4-1BBL и мембраносвязанный IL-15 (клон 4), или экспрессирующие 4-1BBL и мембрансвязанный IL-21 (клон 9 или CSTX002). Стандартные размноженные NK клетки были дополнены 50 МЕ/мл рекомбинантного человеческого IL-2, а резистентные (TGFβi NK) размноженные NK клетки получили 50 МЕ/мл IL-2 и 10 нг/мл TGF-β (Biolegend, 580706). Свежая среда и цитокины добавлялись каждые 2-3 дня. Размножение NK клеток рассчитывали на основе процентного содержания CD3-/CD56+ клеток.
[00591 Проточная цитометрия: внутриклеточная проточная цитометрия была выполнена с использованием набора для фиксации/пермеабилизации BD Cytofix/Cytoperm с GolgiStop (BD Biosciences, 554715).
Антитела к следующим белкам были использованы для оценки фенотипа и функции NK: CD3 PeCy7/APC-H7,CD56 FITC/BV421, NKG2D Pe-CF594/BV510, TRAIL PE/APC/BV421, FasL РЕ, NKp30 PE/Alexa Fluor 647/PE-Vio615, Гранзим A APC, Гранзим В BV510, Перфорин BV421, DNAM-1 BV711, CD 107a BV510, IFN-γ APC, TNF-α BV42I, CD16 РЕ, и Tonbo Ghost Dye 510/780. Клеточные события были приобретены у LSR Fortessa. Диапазон отображения данных проточной цитометрии определяли, используя клетки, окрашенные только красителем для определения жизнеспособности, и контроли одного цвета анализировали с использованием потока Flow Jo 7.6.5/10. SMAD3.
[0060] Анализ на цитотоксичность: NK клетки готовили для анализов на цитотоксичность, оставляя на ночь либо в человеческом IL-2, либо в IL-2 (50 МЕ/мл) с 10 нг/мл растворимого TGF-β (Biolegend). Анализ цитотоксичности проводили способом на основе кальцеина-АМ, по меньшей мере, в двух экземплярах, используя 3 пг кальцеина АМ/мл/1000000 клеток-мишеней в полной среде. Анализы кальцеина проводились в тех же цитокинах, в которых NK-клетки оставляли на ночь. Somachi et al, Journal of visualized experiments: JoVE 48, 2540 (2011).
[0061] Проточная цитометрия внутриклеточной функции: для определения дегрануляции по экспрессии CD107a и продукции внутриклеточных цитокинов в ответ на опухоли 300000 NK клеток совместно культивировали в 96-луночном круглодонном планшете с 60000 опухолевых клеток (соотношение 5:1 Е:Т) или при отсутствии мишени для контроля в 200 мкл среды, как описано для анализов цитотоксичности. Один мкл монензина добавляли в каждый образец вместе с CD 107а в начале анализа. Планшеты центрифугировали при 100 g × 2 минуты, чтобы способствовать междуклеточному контакту, и помещали в инкубатор при 37°С на 3 часа. Через 3 часа среду удаляли и начинали окрашивать клеточную поверхность и внутриклеточные белки, как подробно описано.
[0062] Питометрическая матрица гранул (СВА): Чтобы определить высвобождение NK клеток IFNγ и TNFα, NK клетки культивировали, как описано для внутриклеточной функциональной проточной цитометрии, за исключением монензина и антитела CD107a. После 3-часового совместного культивирования с опухолевыми мишенями или 4-часовой стимуляции 10 мкг/мл РНА супернатанты собирали и замораживали при минус 75°С до использования. В день анализа супернатанты размораживали и использовали 50 мкл неразбавленного супернатанта в соответствии с инструкциями производителя для основного набора растворимого белка BD СВА (BD Biosciences, кат. №:558265) и IFNγ and TNFα Flex Set (BD Biosciences, кат: 558269, 560112) или MACSPlex Cytokine 12 Kit (Miltenyi, кат: 130-099-169). Аналиты приобретали от BD LSR II или MACSQuant. Среднее геометрическое для каждого аналита было определено в Flow Jo v.10.1 и неизвестные образцы были интерполированы с использованием стандартной кривой с R2 более 0,9 от известных стандартов для BD LSR II приобретенных образцов. Анализ полученных аналитов MACSQuant проводился с использованием программного обеспечения MACSQuantiiy (версия 2.8, Bergisch Gladbach, Германия). Это программное обеспечение использует средние значения АРС по стандартам MACSPlex и рассчитывает концентрацию цитокинов в каждом образце.
[0063] Активация NK клеток цитокинами. Для стимуляции NK клеток IL-12, IL-15 и IL-18 первичные NK клетки стимулировали в течение ночи 10 нг/мл IL-12 (Biolegend, 573002), 50 нг/мл IL-15 (Biolegend, 570302) и 50 нг/мл IL-18 (Biolegend, 592102), как описано, и оставляли в 1 нг/мл IL-15 в течение 7-14 дней после стимуляции IL-12, IL-15 и IL-18 в течение ночи. Для определения влияния IL-2 и TGFβi на продукцию цитокинов NK клетки обрабатывали, как описано, но с добавлением IL-2 и/или TGF-β, как указано, при ночной стимуляции IL-12, IL-15, и IL-18, а также 1 нг/мл IL-15 в течение 7-14 дней. Для измерения выработки цитокинов, NK клетки оставляли в 1 нг/мл IL-15 только в течение ночи и на протяжении всего анализа и совместно культивировали с MG63 в соотношении 5:1 или равным количеством NK клеток только в отсутствие контроля мишени, и окрашивание внутриклеточного потока проводили, как описано ниже.
[0064] ОТ-ПЦР/qПЦР: РНК из свежих, никогда не замороженных, размноженных на 14-й день человеческих NK клеток выделяли с использованием набора RNAeasy, колонок QiaShredder и набора не содержащей РНКазу ДНКазы (все Qiagen, 74104, 79654, 79254) и кДНК синтезировали при помощи высокоэффективного набора для обратной транскрипции кДНК (Thermo Fisher, 4368814). ПЦР для маршрута TGF-β была проведена с использованием Taqman Fast PCR Mastermix и 96-луночного Pathway Array TGF-β Human Fast (ThermoFisher, 4418742) на Applied Biosystems 7900HT.
[0065] Статистический анализ: Статистический анализ проводили, как описано в каждой подписи к Фигурам, с использованием GraphPad Prism 6.0 или 7.0 (La Jolla, СА, USA), р значения менее 0,05 считали значимыми.
Результаты и обсуждение
[0066] IFNγ и TNFα являются двумя провоспалительными цитокинами, важными для противоопухолевого ответа, и было сообщено, что их продукция ингибируется TGF-β. Для определения продукции провоспалительных цитокинов NK клетками NK клетки культивировали в течение 2 недель с родительским (немодифицированным K562) плюс или минус TGFβ. По истечении 2 недель контрольные и TGFβi NK клетки инкубировали с опухолевыми мишенями, как описано, и супернатанты собирали для измерения секреции IFN-γ и TNF-α при помощи цитометрической матрицы гранул. Наблюдалось значительное увеличение секреции IFN-γ и TNFα как в присутствии, так и в отсутствие TGF-β по сравнению с контрольными размноженными NK клетками (Фигура 1).
[0067] Затем мы определили, необходима ли стимуляция при помощи K562 или других опухолевых клеток для гиперпродукции цитокинов TGFβi. С этой целью мы использовали IL-12, IL-15 и IL-18, которые хорошо известны для активации NK клеток в отсутствие стимуляции опухоли. Когда TGFβ добавляли в культуру, NK клетки продуцировали повышенные IFNγ и TNFα в ответ на опухолевые стимулы (Фигура 2).
[0068] Для того, чтобы определить, могут ли другие питающие клетки K562 генерировать TGFβi NK клетки с повышенной продукцией цитокинов, K562, экспрессирующие mbIL-15 (Фигура 3) или mbIL-21 (Фигура 4), совместно культивировали с NK клетками в течение 2 недель плюс или минус TGFβ. Обе питающие клетки индуцировали TGFβi NK-клетки с повышенной продукцией цитокинов.
[0069] Поскольку сообщалось, что TGFβ ингибирует пролиферацию NK клеток, мы измерили пролиферацию через 2 недели в ответ на стимуляцию K562mbIL-21. С этой целью TGFβ не оказывал значительного влияния на пролиферацию (Фигура 5).
[0070] Затем определяли персистенцию фенотипа и функции TGFβi NK-клеток. TGFβi NK клетки и донорские стандартные NK клетки оставляли на отдых только при низкой дозе IL-2 (например, TGFβi NK удаляли из TGF-β) после завершения 2 недель активации. TGFβi NK клетки оценивали на секрецию IFN-γ и TNF-α в конце размножения и через 7-33 дней после активации. После активации TGFβi NK клетки сохраняли увеличение секреции IFN-γ и TNF-α как на исходном уровне, так и при обработке TGF-β (Фигура 6).
[0071] Кроме того, мы хотели определить, поддерживают ли TGFβi NK клетки гиперпродукцию цитокинов в ответ на различные стимулы. С этой целью мы обнаружили, что TGFβi NK клетки продуцируют повышенные IFNγ и TNFα в ответ на клеточные линии медуллобластомы и нейробластомы и что это повышенное производство цитокинов может быть индуцировано стимуляцией РНА, что указывает на врожденную способность продуцировать повышенные противоопухолевые цитокины (Фигура 7 и 9).
[0072] Функция SMAD3 как супрессора противоопухолевой функции NK клеток уже была ясна. SMAD3 связывается непосредственно с промотором IFNγ для ингибирования экспрессии IFNγ, и SMAD3-/- мыши имеют усиленную функцию NK клеток и сниженный рост опухоли. Таким образом, авторы изобретения определяли, был ли SMAD3 уменьшен на уровне белка при помощи вестерн-блоттинга, и обнаружили, что TGFβi NK значительно уменьшал белок SMAD3 (Фигура 8).
[0073] Дополнительно, мы проверили цитотоксичность NK TGFβi клеток in vitro с родительскими K562 культивируемыми NK клетками и in vivo с mbIL-21 размноженными NK клетками. Цитотоксичность не изменилась (Фигура 10). Фактически, in vivo TGFβi NK клетки значительно снижали рост остеосаркомы в легких у мышей NSG (Фигура11).
[0074] Кроме того, используя анализ РНК-seq, мы обнаружили, что TGFβi NK клетки транскрипционно отличались от контрольных NK клеток, что свидетельствует о широком изменении фенотипа клеток (Фигура 12) в дополнение к функции.
[0075] Таким образом, человеческие NK клетки, расширенные культурой TGF-β (TGFβi NK), имеют пониженную чувствительность к TGF-β, скорее всего, из-за потери одного из ключевых сигнальных белков TGF-β - SMAD3. TGFβi NK клетки заметно повышают секрецию IFN-γ, TNF-α и GM-CSF. Удивительно, но в отличие от предыдущих статей, TGF-β не ингибировал общую 2-недельную пролиферацию TGFβi NK клеток. Bellone et al, J Immunol 155: 1066-1073 (1995). Условия стимуляции, использованные в предыдущих статьях для индукции пролиферации (IL-2 и IL-15), и временные точки могут быть ключевыми для различий, наблюдаемых при пролиферации. Предыдущие измерения влияния TGF-β на пролиферацию NK клеток изучали кратковременную пролиферацию, а не пролиферацию в течение 2 недель. Viel et al, Science signaling 9: ra19 (2016). Авторы изобретения предполагают, что хроническая стимуляция TGF-β с активацией опухоли стимулирует активацию определенной группы NK клеток, потенциально тех, которые являются SMAD3neg для выживания. Эти SMAD3neg NK клетки будут устойчивы к фосфорилированию SMAD3 при помощи TGF-β в среде для культивирования клеток, что позволяет увеличить пролиферацию. Oida et al, Journal of immunological method 362: 195-198 (2010).
[0076] Способность TGFβi NK клеток продуцировать IFN-γ и TNF-α оценивали, поскольку эти цитокины могут как ингибировать TGF-β, так и наоборот, TGF-β может ингибировать продукцию IFN-γ и TNF-α. Неожиданно было обнаружено значительное увеличение противоопухолевой секреции IFN-γ и TNF-α в TGFβi NK клетках по сравнению со стандартными NK клетками как с обработкой TGF-β, так и без нее. Предыдущие исследования показали, что делеция SMAD3 увеличивает исходную продукцию IFN-γ, поэтому, вероятно, аналогичный механизм имеет место в клетках TGFβi NK, которые не экспрессируют SMAD3. Tang et al, Nat Commun 8: 14677 (2017). Сообщается, что TGF-β ингибирует продукцию TNFα в первичных NK клетках (Bellone et al., J Immunol 155: 1066-1073 (1995)). Неожиданно, TGFβi NK клетки имели значительно повышенную секрецию TNF-α с TGF-β или без него в среде для анализа по сравнению со стандартными NK клетками. Регуляция продуцирования TNF-α менее понятна, но также известно, что она ингибируется TGFβ, поэтому было неожиданно обнаружить повышенную секрецию TNF-α в TGFβi NK клетках.
[0077] Хотя данное изобретение было конкретно проиллюстрировано и описано со ссылками на его предпочтительные варианты воплощения, специалистам в данной области техники должно быть понятно, что в него могут быть внесены различные изменения в форме и деталях, не выходящие за пределы объема изобретения, охватываемого прилагаемой формулой изобретения. Все патенты, публикации и ссылки, процитированные в приведенном выше описании, полностью включены в данную заявку посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки чувствительности опухоли к иммуноонкологическим препаратам | 2021 |
|
RU2771760C1 |
| ПРИМЕНЕНИЕ ЧАСТИЦ НА ОСНОВЕ ЦИТОПЛАЗМАТИЧЕСКОЙ МЕМБРАНЫ, ЛИПОСОМ И ЭКЗОСОМ ДЛЯ АНАЛИЗА АКТИВНОСТИ ИММУННЫХ КЛЕТОК | 2020 |
|
RU2829443C2 |
| ПРИМЕНЕНИЕ СТИМУЛИРУЮЩЕГО СРЕДСТВА ДЛЯ АНАЛИЗА АКТИВНОСТИ ИММУННЫХ КЛЕТОК | 2020 |
|
RU2822517C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ С МУТИРОВАННЫМИ КОСТИМУЛЯТОРНЫМИ ДОМЕНАМИ CD28 | 2018 |
|
RU2800922C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРИРОДНЫХ КЛЕТОК-КИЛЛЕРОВ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2019 |
|
RU2780848C2 |
| ОПРЕДЕЛЕНИЕ ДОЗЫ ДЛЯ ИММУНОТЕРАПЕВТИЧЕСКИХ СРЕДСТВ | 2017 |
|
RU2771717C2 |
| УНИВЕРСАЛЬНЫЕ АНТИГЕНПРЕЗЕНТИРУЮЩИЕ КЛЕТКИ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2809113C2 |
| СПОСОБ И КОМПОЗИЦИИ ДЛЯ КЛЕТОЧНОЙ ИММУНОТЕРАПИИ | 2012 |
|
RU2688185C2 |
| Способ прогнозирования продолжительности жизни больных с метастатическими формами опухолей | 2023 |
|
RU2821659C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ Т-КЛЕТОК ПРОТИВ АНТИГЕНА ПАПИЛЛОМАВИРУСА ЧЕЛОВЕКА | 2014 |
|
RU2713333C2 |



Группа изобретений относится к биотехнологии. Представлен способ лечения рака у субъекта, нуждающегося в таком лечении, включающий введение субъекту терапевтически эффективного количества популяции размноженных естественных клеток-киллеров, проявляющих повышенную устойчивость к трансформирующему ростовому фактору бета, по сравнению с NK-клетками природного происхождения, где популяцию NK-клеток активируют и размножают in vitro в присутствии TGF-β и питающих клеток лейкемии. Также раскрыты способы получения популяции in vitro размноженных естественных клеток-киллеров для применения в лечении рака, где популяцию NK-клеток активирируют и размножают in vitro в присутствии трансформирующего ростового фактора бета и питающих клеток лейкемии, где популяция размноженных NK-клеток проявляет повышенную устойчивость к TGF-β. Изобретение может применяться в лечении рака у пациентов. 3 н. и 19 з.п. ф-лы, 12 ил., 1 пр.
1. Способ лечения рака у субъекта, нуждающегося в таком лечении, включающий введение субъекту терапевтически эффективного количества популяции размноженных естественных клеток-киллеров (NK), проявляющих повышенную устойчивость к трансформирующему ростовому фактору бета (TGF-β), по сравнению с NK-клетками природного происхождения, где популяцию NK-клеток активируют и размножают in vitro в присутствии TGF-β и питающих клеток лейкемии.
2. Способ по п. 1, отличающийся тем, что после размножения NK-клетки оставляют на ночь в присутствии IL-2.
3. Способ по п. 2, отличающийся тем, что питающими клетками являются питающие клетки К562.
4. Способ по п. 3, отличающийся тем, что питающие клетки К562 генетически модифицированы для экспрессии 4-1BBL и мембраносвязанного IL-21.
5. Способ по п. 1, отличающийся тем, что рак представляет собой солидную опухоль.
6. Способ по п. 5, отличающийся тем, что рак выбирают из группы, состоящей из лейкемии, лимфомы, рабдомиосаркомы, рака головного мозга и рака кости.
7. Способ по п. 1, отличающийся тем, что популяция размноженных NK-клеток продуцирует повышенные количества одного или более из IFN-γ, TNF-α и GM-CSF.
8. Способ по п. 1, отличающийся тем, что популяция размноженных NK-клеток демонстрирует пониженные уровни белка SMAD3 и/или белка TGFΒR3.
9. Способ по п. 1, в котором популяция размноженных NK-клеток имеет повышенную экспрессию SCUBE1, MY07A, KLF3, WIPF3 и EPHA1; или в котором популяция размноженных NK-клеток имеет пониженную экспрессию CD300A, SGSM1, SMAD3, TBX21, GZMK, TGFBR3 и GZMA.
10. Способ по п. 1, отличающийся тем, что популяцию размноженных NK-клеток вводят вместе с фармацевтически приемлемым носителем.
11. Способ получения популяции in vitro размноженных естественных клеток-киллеров (NK) для применения в лечении рака, где популяцию NK-клеток активирируют и размножают in vitro в присутствии трансформирующего ростового фактора бета (TGF-β) и питающих клеток лейкемии, где популяция размноженных NK-клеток проявляет повышенную устойчивость к TGF-β и питающим клеткам лейкемии по сравнению с NK-клетками природного происхождения.
12. Способ по п. 11, причем указанная популяция размноженных NK-клеток продуцирует повышенные количества одного или более из IFN-γ, TNF-α и GM-CSF.
13. Способ по п. 11, причем указанная популяция размноженных NK-клеток демонстрирует пониженные уровни белка SMAD3 и/или белка TGFΒR3.
14. Способ по п. 11, причем указанная популяция размноженных NK-клеток имеет повышенную экспрессию SCUBE1, MY07A, KLF3, WIPF3 и EPHA1; или популяция размноженных NK-клеток имеет пониженную экспрессию CD300A, SGSM1, SMAD3, TBX21, GZMK, TGFBR3 и GZMA.
15. Способ по п. 11, причем указанная популяция размноженных NK-клеток содержит человеческие NK-клетки.
16. Способ по п. 11, причем указанная популяция размноженных NK-клеток содержит собачьи NK-клетки.
17. Способ получения популяции размноженных естественных клеток-киллеров (NK), проявляющих повышенную устойчивость к TGF-β, по сравнению с NK-клетками природного происхождения, включающий in vitro активацию и размножение популяции естественных клеток-киллеров в присутствии питающих клеток лейкемии вместе с IL-2 и TGF-β, NK-стимулирующих экзосом вместе с IL-2 и TGF-β или NK-стимулирующих наночастиц вместе с IL-2 и TGF-β.
18. Способ по п. 17, отличающийся тем, что питающими клетками лейкемии являются питающие клетки К562.
19. Способ по п. 18, отличающийся тем, что питающие клетки K562 генетически модифицированы для экспрессии костимулирующих белков и/или цитокинов.
20. Способ по п. 18, где питающие клетки К562 генетически модицифированы для экспрессии 4-1BBL и мембраносвязанного IL-21.
21. Способ по п. 11, где питающие клетки лейкемии являются питающими клетками К562.
22. Способ по п. 21, где питающие клетки К562 генетически модицифированы для экспрессии 4-1BBL и мембраносвязанного IL-21.
| US 2017056448 A1, 02.03.2017 | |||
| HAYASHI et al., TGFbeta down-regulates IFN-gamma production in IL-18 treated NK cell line LNK5E6, Biochem Biophys Res Commun., 2003, 24, 300 (4), pp | |||
| Устройство для избирательного управления с одного конца линии несколькими реле | 1918 |
|
SU980A1 |
| YU J | |||
| et al., Pro- and antiinflammatory cytokine signaling: reciprocal antagonism regulates interferon-gamma production by human natural killer cells, | |||
Авторы
Даты
2024-11-14—Публикация
2019-01-29—Подача