ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Для этой заявки испрашивается приоритет по предварительной заявке на патент США № 62/675110, зарегистрированной 22 мая 2018 года, предварительной заявке на патент США № 62/810290, зарегистрированной 25 февраля 2019 года, предварительной заявке на патент США № 62/820838, зарегистрированной 19 марта 2019 года, и предварительной заявке на патент США № 62/820842, зарегистрированной 19 марта 2019 года. Полное содержание этих заявок включено в настоящее изобретение во всех отношениях путем ссылок на них.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0002] Это изобретение относится к способам и композициям для лечения, стабилизации, предотвращения и/или отсрочки возникновения легочной гипертензии с использованием наночастиц, которые включают ингибитор mTOR (например, рапамицин или его производное) и белковый носитель.
УРОВЕНЬ ТЕХНИКИ
[0003] Легочная гипертензия (PH) представляет собой синдром, характеризующийся повышенным давлением в легочной артерии. Гемодинамически легочную гипертензию определяют по величине систолического давления в легочной артерии выше 30 мм рт. ст. или по оценке среднего давления в легочной артерии выше 25 мм рт. ст. (см. публикацию Zaiman et al., Am. J. Respir. Cell Mol. Biol. 33:425-31 (2005)). По прошествии некоторого времени, повышенное давление при легочной гипертензии приводит к повреждению как крупных, так и мелких легочных артерий. Стенки мельчайших кровеносных сосудов утолщаются и больше не способны нормально переносить кислород и углекислый газ между кровью и легкими. Со временем легочная гипертензия приводит к утолщению легочных артерий и сужению проходов, по которым течет кровь. По мере развития легочной гипертензии, правая сторона сердца вынуждена работать с большим напряжением, для того чтобы компенсировать отрицательное воздействие этого заболевания, однако повышенное усилие приводит к увеличению и утолщению сердца. Разрастание гладких мышц и эндотелиальных клеток, которые в нормальных условиях находятся в состоянии покоя, приводит к ремоделированию сосудов с облитерацией просвета легочной сосудистой системы. Это вызывает прогрессирующее повышение легочного давления, поскольку кровь перекачивается через меньшую площадь просвета. Увеличение правого желудочка повышает риск развития у человека тромбоэмболии легочной артерии, так как кровь имеет тенденцию скапливаться в желудочке и в ногах. В случае образования в скапливающейся крови сгустков, они могут в конечном итоге перемещаться и отлагаться в легких, приводя к катастрофическим последствиям. Постепенное повышение давления также создает дополнительную нагрузку на правый желудочек, который в конечном итоге перестает функционировать, что приводит к преждевременной смерти этих пациентов.
[0004] В результате легочной гипертензии, в легочных артериях возникают различные патологические изменения. Стойкая вазоконстрикция и структурное ремоделирование легочных сосудов являются основными признаками легочной гипертензии. Клетки гладких мышц легочных сосудов претерпевают смену фенотипа с сократительного нормального фенотипа на синтетический фенотип, что приводит к росту клеток и отложению матрикса. Гистологическое исследование образцов тканей пациентов с легочной гипертензией показывает утолщение интимы, а также гипертрофию клеток гладких мышц, особенно для сосудов диаметром менее 100 мкм. Кроме того, аномальные клетки гладких мышц часто сверхэкспрессируют эндотелин и транспортеры серотонина, которые, по-видимому, играют определенную роль в развитии легочной гипертензии.
[0005] На начальном этапе, наиболее частым симптомом легочной гипертензии является одышка при физической нагрузке. Некоторые люди чувствуют головокружение или утомляемость при физической нагрузке, и обычным явлением является боль в груди, напоминающая стенокардию. Поскольку ткани организма не получают достаточного количества кислорода, еще одной проблемой является общая слабость. Другие симптомы, такие как кашель и хрипы, могут быть вызваны первопричинным заболеванием легких. Отек, в частности, ног, может возникать в результате того, что жидкость из вен может просачиваться в ткани, что свидетельствует о развитии легочного сердца. У некоторых людей с легочной гипертензией наблюдаются нарушения соединительной ткани, в частности склеродермия. В случаях, когда у людей наблюдаются оба состояния, легочная гипертензия и заболевания соединительной ткани, до появления симптомов легочной гипертензии, а иногда и на несколько лет раньше, часто развивается феномен Рейно.
[0006] Лечение некоторых видов легочной гипертензии часто направлено на первопричинное заболевание легких. В настоящее время, варианты лечения доступны для тех пациентов, которые страдают от дисфункции клеток-мишеней при легочной гипертензии, которая приводит к сужению сосудистой сети. Такие лекарственные средства, как простаноиды, ингибиторы фосфодиэстеразы-5 и антагонисты рецепторов эндотелина, в основном вызывают дилатацию легочных сосудов. Вазодилататоры, такие как блокаторы кальциевых каналов, оксид азота и простациклин, часто помогают при легочной гипертензии, ассоциированной со склеродермией, хроническим заболеванием печени и ВИЧ-инфекцией. В отличие от этого, эффективность этих препаратов для людей с легочной гипертензией, обусловленной первопричинным заболеванием легких, не доказана. У большинства людей с легочной гипертензией, возникшей по неизвестной причине, вазодилататоры, такие как простациклин, резко снижают артериальное давление в легочных артериях. Простациклин, вводимый внутривенно через катетер, хирургически имплантированный в кожу, улучшает качество жизни, увеличивает выживаемость и снижает срочность проведения трансплантации легких. К сожалению, многие пациенты плохо отвечают на эти лекарственные средства или перестают отвечать на них со временем. Единственным оставшимся вариантом для лечения легочной гипертензией в этом случае является одинарная или двойная трансплантация легкого. Несмотря на то, что имеются некоторые свидетельства того, что доступные методы лечения оказывают вторичное влияние на ремоделирование сосудов, тем не менее, в настоящее время не существует методов лечения, направленных на патологическую пролиферацию клеток при легочной артериальной гипертензии.
[0007] Многие антипролиферативные средства растворяют в растворителе/поверхностно-активном веществе, которые вызывают реакции гиперчувствительности. Большие усилия были направлены на разработку водорастворимых пролекарств и производных антипролиферативных средств, содержащих группы, обладающие более высокими гидрофильными свойствами, с целью повышения растворимости в воде и, таким образом, устранения необходимости в потенциально токсичных растворителях/поверхностно-активных веществах. Другой подход к решению проблемы, связанной с плохой растворимостью в воде антипролиферативных средств, заключается в разработке различных лекарственных форм, таких как наночастицы, эмульсии масло в воде и липосомы. Композиции наночастиц практически не растворимых в воде лекарственных средств и их применение описаны, например, в патентных документах PCT Application Pub. No. WO07/027941 и WO 2008/109163
[0008] Полное содержание всех публикаций, патентов, заявок на патенты и опубликованных заявок на патенты, упоминаемых в изобретении, включено в настоящее изобретение путем ссылок на них.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0009] В настоящем изобретении предлагаются способы лечения легочной гипертензии у индивидуума, включающие введение индивидууму композиции, содержащей наночастицы, включающие ингибитор mTOR и белковый носитель, где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не менее чем приблизительно 0,1 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не менее чем приблизительно 5 мг/м2.
[0010] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 5 мг/м2.
[0011] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл через пять дней после введения композиции наночастиц.
[0012] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл через семь дней после введения композиции наночастиц.
[0013] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, композицию наночастиц вводят, по меньшей мере, один раз в неделю.
[0014] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, композицию наночастиц вводят не чаще чем один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят один раз каждые две недели, два раза в три недели или три раза в четыре недели.
[0015] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель.
[0016] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, легочная гипертензия представляет собой легочную артериальную гипертензию.
[0017] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, легочную гипертензию выбирают из группы, состоящей из идиопатической легочной артериальной гипертензии (IPAH), наследственной легочной артериальной гипертензии (HPAH), индуцированной лекарственным препаратом или токсином легочной артериальной гипертензии, ассоциированной с заболеванием соединительной ткани легочной артериальной гипертензии и ассоциированной с врожденными пороками сердца легочной артериальной гипертензии.
[0018] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, индивидуум имеет функциональный класс III или IV легочной артериальной гипертензии по классификации ВОЗ.
[0019] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму.
[0020] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц.
[0021] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно.
[0022] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, ингибитор mTOR представляет собой рапамицин.
[0023] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, индивидуум подвергался, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает введение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелин-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект.
[0024] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, белковый носитель представляет собой альбумин. В некоторых вариантах осуществления, альбумин представляет собой человеческий сывороточный альбумин.
[0025] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм.
[0026] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1.
[0027] В некоторых вариантах осуществления в соответствии с любым одним из описанных в изобретении способов, индивидуумом является человек.
[0028] В настоящем изобретении также предлагаются лекарственные формы с разовой дозой для лечения легочной гипертензии, включающие (a) наночастицы, которые содержат ингибитор mTOR и белковый носитель, где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и (b) фармацевтически приемлемый носитель.
[0029] В настоящем изобретении также предлагаются наборы, включающие (a) наночастицы, которые содержат ингибитор mTOR и белковый носитель, где доза ингибитора mTOR в наборе составляет не более чем приблизительно 10 мг/м2, и (b) инструкции по применению набора при лечении легочной гипертензии.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0030] На фигурах 1A и 1B представлены остаточные концентрации рапамицина (нг/мл) в цельной крови, измеряемые один раз в неделю на протяжении 16-недельного периода введения ABI-009 (фигура 1A), и вводимые каждую неделю дозы рапамицина в ABI-009 для каждого субъекта (фигура 1B).
[0031] На фигуре 2 представлены величины сопротивления легочных сосудов (PVR, дин⋅сек/см5), сердечного выброса (CO, л/мин) и сердечного индекса (CI, л/мин/м2) после периода 16-недельного введения ABI-009 при сравнении с величинами на момент начала исследования.
[0032] На фигуре 3 приведены обобщенные результаты по улучшению функциональных и гемодинамических параметров у пациентов, страдающих легочной артериальной гипертензией, после лечения с помощью ABI-009.
[0033] На фигуре 4 приведена схема исследования в фазе 1 клинического испытания.
[0034] На фигуре 5 в графическом виде представлены результаты определения параметров эффективности лечения, в том числе дистанции, преодолеваемой пациентом пешком за 6 минут (6MWD), сопротивления легочных сосудов (PVR), сердечного выброса и NT proBNP (N-терминального фрагмента мозгового натрийуретического пептида), после 16-недельного периода лечения. Усики отображают минимальную и максимальную величину, прямоугольники характеризуют межквартильный размах.
[0035] На фигуре 6 в графическом виде представлены уровни рапамицина (нг/г) в крови, в легком и печени крыс через 24 часа после введения nab-рапамицина (nab-R) и перорального рапамицина (пероральный-R). Были указаны фактические величины (N=5 в каждой группе).
[0036] На фигуре 7 в графическом виде представлены концентрации рапамицина в образцах цельной крови, взятых у крыс после подкожного (SC) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009) в период времени от 0 до 24 часов после введения.
[0037] На фигуре 8 в графическом виде представлены концентрации рапамицина в образцах цельной крови, взятых у крыс после подкожного (SC) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009) в период времени от 0 до 168 часов после введения.
[0038] На фигуре 9 в графическом виде представлены концентрации рапамицина в образцах цельной крови, взятых у крыс после подкожного (SC) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009) в период времени от 0 до 24 часов после введения.
[0039] На фигуре 10 в графическом виде представлены данные по биодоступности nab-рапамицина (ABI-009) после подкожного (subQ) или внутривенного (IV) введения разовой дозы у крыс, указанные в форме рассчитанной площади под фармакокинетической кривой (AUC).
[0040] На фигуре 11 в графическом виде представлены концентрации рапамицина в костном мозге крысы (верхний график) или в головном мозге крысы (нижний график) через 24 или 168 часов после подкожного (subQ) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009).
[0041] На фигуре 12 в графическом виде представлены концентрации рапамицина в сердце крысы (верхний график) или в печени крысы (нижний график) через 24 или 168 часов после подкожного (subQ) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009).
[0042] На фигуре 13 в графическом виде представлены концентрации рапамицина в легком крысы (верхний график) или поджелудочной железе крысы (нижний график) через 24 или 168 часов после подкожного (subQ) или внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009).
[0043] На фигуре 14 графически представлено сравнение гистопатологии, оцененной в баллах на коже, взятой у крыс в различных группах, подвергаемых лечению.
[0044] На фигуре 15 приведено изображение гистологического среза кожи крысы в группе 1 (0,9% физиологический раствор). Гистологические поражения в подкожных тканях (SC) ограничены агрегатами смеси воспалительных клеток (черная стрелка). Указаны дерма (D) и эпидермис (E).
[0045] На фигуре 16 приведено изображение гистологического среза кожи крысы в группе 2 (HSA (человеческий сывороточный альбумин) в 0,9% физиологическом растворе). В подкожном слое (SC) видны множественные агрегаты смеси воспалительных клеток (черные стрелки). Эпидермис (E) и дерма (D) не имеют особенностей.
[0046] На фигуре 17 приведено изображение гистологического среза кожи крысы в группе 3 (ABI-009, 1,7 мг/кг). В подкожных тканях (SC) видна минимальная инфильтрация смеси воспалительных клеток (черная стрелка). Указаны эпидермис (E) и дерма (D).
[0047] На фигуре 18 приведено изображение гистологического среза кожи крысы в группе 4 (ABI-009, 5 мг/кг). В подкожном слое (SC) присутствуют рассеянная инфильтрация смеси воспалительных клеток (черная стрелка) и место незначительного некроза (голубая стрелка). Эпидермис (E) и дерма (D) не имеют особенностей.
[0048] На фигуре 19 приведено изображение гистологического среза кожи крысы в группе 4 (ABI-009, 10 мг/кг). Обнаруживаются подкожная (SC) инфильтрация смеси воспалительных клеток (черная стрелка) и область некроза (синяя стрелка). Эпидермис (E) и дерма (D) не имеют особенностей.
[0049] На фигуре 20 в графическом виде представлены средние уровни остаточного сиролимуса в крови крыс, которым вводили ABI-009 в дозе 1,7 мг/кг, 5 мг/кг или 10 мг/кг.
[0050] На фигуре 21 в графическом виде представлены концентрации рапамицина в головном мозге (A), сердце (B), печени (C), легком (D), поджелудочной железе (E) и крови (F) крыс через 2, 8, 24, 72 или 120 часов после внутривенного (IV) введения разовой дозы nab-рапамицина (ABI-009).
[0051] На фигуре 22 в графическом виде представлены изменения (%) суммарной оценки в баллах каждого пункта опроса EmPHasis 10 (число пациентов n=5 для каждого пункта) с момента начала исследования до недели 17.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0052] В настоящем изобретении предлагаются способы лечения легочной гипертензии (например, тяжелой формы легочной артериальной гипертензии, например, легочной артериальной гипертензии функционального класса III или IV по классификации ВОЗ) у индивидуума, включающие введение индивидууму эффективного количества композиции, содержащей ингибитор mTOR (например, лекарственное средство семейства лимус, например, рапамицин или его производное) и белковый носитель (например, альбумин). Одобренные в настоящее время терапевтические средства для лечения легочной артериальной гипертензии (PAH) действуют, в основном, как вазодилататоры и не позволяют решать проблему заболевания, связанную с гиперпролиферацией эндотелиальных клеток и клеток гладких мышц. Иматиниб, ингибитор тирозинкиназы, является только антипролиферативным средством, которое было исследовано при лечении легочной артериальной гипертензии на последних стадиях клинических испытаний, но при его применении возникали значительные проблемы безопасности. Это изобретение частично основано на неожиданно обнаруженном авторами изобретения факте, что введение композиции, включающей ингибитор mTOR (например, композиции наночастиц, содержащей рапамицин и альбумин) индивидууму с тяжелой формой легочной гипертензии (например, легочной артериальной гипертензии функционального класса III по классификации ВОЗ) не только снижает сопротивление легочных сосудов (PVR), но также существенно улучшает состояние при недостаточности кровообращения, например, существенно улучшает сердечный выброс, и/или улучшает результаты теста на преодоление пациентом пешком дистанции за 6 минут. Такой положительный эффект достигался при использовании дозы, составляющей не более чем одну десятую или одну двадцатую часть от максимально переносимой дозы (MTD). Например, композиция наночастиц, включающая рапамицин и альбумин, продуцировала такой эффект при дозе не более чем приблизительно 1, 5 или 10 мг/м2 (например, недельной дозе 1-10 мг/м2), в то время как MTD композиции наночастиц составляет приблизительно 100 мг/м2. Такие дозы композиции рапамицина позволяют также достигать благоприятного профиля безопасности.
[0053] Соответственно, в некоторых аспектах, в настоящем изобретении предлагаются способы лечения легочной гипертензии, включающие введение индивидууму эффективного количества композиции, содержащей ингибитор mTOR (например, лекарственное средство семейства лимус, например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR является такой, что она позволяет соблюдать баланс между продуцируемым благоприятным профилем безопасности и достижением положительного эффекта при лечении легочной гипертензии. В некоторых аспектах, в изобретении предлагаются способы улучшения состояние при недостаточности кровообращения (например, улучшения сердечного выброса) у индивидуума с легочной гипертензией. В некоторых аспектах, в изобретении предлагаются способы снижения сопротивления легочных сосудов (PVR) у индивидуума с легочной гипертензией. В некоторых аспектах, в изобретении предлагается способ улучшения результатов теста на преодоление пациентом пешком дистанции за 6 минут (6MWD) у индивидуума с легочной гипертензией. В некоторых вариантах осуществления, доза ингибитора mTOR (например, рапамицина или его производного) в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, композицию вводят внутривенно или подкожно.
Определения
[0054] Если конкретно не указано иное, то все используемые в изобретении технические и научные термины имеют такое же значение, которое является общепринятым для обычных специалистов в той области, к которой относится изобретение. Кроме того, любой способ или материал, аналогичный или эквивалентный описанному в изобретении способу или материалу, может быть использован при реализации настоящего изобретения. Применительно к настоящему изобретению, далее приведены определения следующим терминам.
[0055] Следует иметь в виду, что описанные варианты осуществления изобретения включают в себя варианты осуществления, "состоящие" и/или "по существу состоящие" из других вариантов осуществления.
[0056] Используемый в изобретении термин "композиция" или "композиции" включает композиции и применим к композициям по изобретению. В изобретении также предлагаются фармацевтические композиции, содержащие описанные в изобретении компоненты.
[0057] Ссылка в изобретении на "рапамицин" относится к рапамицину или его производным, и, соответственно, изобретение рассматривает и включает в себя все эти варианты осуществления. В этом изобретении, названия "рапамицин" и "сиролимус" используются взаимозаменяемо. Рапамицин иногда называют в других местах описания изобретения рапамицином или рапамуном. Ссылка на "рапамицин" используется для упрощения описания и носит иллюстративный характер. Производные рапамицина включают, но этим не ограничивая, соединения, которые являются структурно аналогичными рапамицину, или которые относятся к тому же общему химическому классу, что и рапамицин, аналоги рапамицина или фармацевтически приемлемые соли рапамицина или его производных или аналогов. В некоторых вариантах осуществления, ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) повышает базальную активность AKT, повышает фосфорилирование AKT, повышает активность PI3-киназы, увеличивает продолжительность активации AKT (например, активации, индуцированной экзогенным IGF-1), ингибирует фосфорилирование серина в IRS-1, ингибирует деградацию IRS-1, ингибирует или изменяет подклеточную локализацию CXCR4, ингибирует секрецию VEGF, снижает экспрессию циклина D2, снижает экспрессию сурвивина, ингибирует IL-6-индуцированный рост клеток множественной миеломы, ингибирует клеточную пролиферацию при легочной гипертензии, повышает апоптоз, увеличивает блокирование клеточного цикла, увеличивает расщепление поли(ADPрибоза)полимеразы, увеличивает расщепление каспазы-8/каспазы-9, изменяет или ингибирует активацию сигнальных путей фосфатидилинозитол-3-киназа/AKT/mTOR и/или циклин D1/ретинобластома, ингибирует ангиогенез и/или ингибирует образование остеокластов. В некоторых вариантах осуществления, производное рапамицина сохраняет одно или более аналогичных рапамицину биологических, фармакологических, химических и/или физических свойств (в том числе, например, функциональность). Примеры производного рапамицина включают бензоилрапамицин, такой как описанный в параграфе [0022] патентного документа WO 2006/089207, полное содержание которого включено в настоящее изобретение путем ссылки на него. Другие примеры производных рапамицина включают WY-090217, AY-22989, NSC-226080, SiiA-9268A, оксаазациклогентриаконтин, темрапамицин (CCI 779 (Wyeth)), эверолимус (RAD 001 (Novartis)), пимекролимус (ASM981), SDZ-RAD, SAR943, ABT-578, AP23573 и биолимус A9.
[0058] Если однозначно не указано иное, то используемый в изобретении термин "индивидуум" подразумевает млекопитающего, включая, но этим не ограничивая, примата, человека, жвачное животное, лошадь, представителя семейства кошачьих, представителя семейства псовых или представителя отряда грызунов.
[0059] Используемый в изобретении термин "лечение" означает метод достижения положительных или требуемых результатов, в том числе клинических результатов. Применительно к этому изобретению, положительные или требуемые клинические результаты включают, но этим не ограничивая, один или более из следующих: облегчение одного или более симптомов, возникающих вследствие заболевания, уменьшение степени распространения заболевания, стабилизация заболевания (например, предотвращение или отсрочка усугубления заболевания), предотвращение или отсрочка возникновения заболевания, отсрочка или замедление прогрессирования заболевания, облегчение болезненного состояния, снижение дозы одного или более других лекарственных препаратов, требуемых для лечения заболевания, повышение качества жизни и/или пролонгирование времени выживания. В некоторых вариантах осуществления, композиция позволяет снижать тяжесть одного или более симптомов, ассоциированных с легочной гипертензией, по меньшей мере, приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 100% по сравнению с соответствующим симптомом у того же самого субъекта до лечения или по сравнению с соответствующим симптомом у других субъектов, не получающих эту композицию. Термин "лечение" также включает в себя уменьшение патологических последствий легочной гипертензии. Способы по изобретению предполагают любой один или более из этих аспектов лечения.
[0060] Используемое в изобретении выражение "отсрочка" развития легочной гипертензии означает задержку, торможение, замедление, запаздывание, стабилизацию и/или перенос на более поздний срок развития заболевания. Эта отсрочка может иметь различную продолжительность по времени, зависящую от анамнеза заболевания и/или индивидуума, подвергаемого лечению. Для любого специалиста в данной области является очевидным, что достаточная или значительная отсрочка может, по сути, включать в себя предотвращение, в результате которого у индивидуума не развивается заболевание. Способ, который позволяет достигать "отсрочки" развития легочной гипертензии, представляет собой способ, который позволяет уменьшать вероятность развития заболевания в данный интервал времени и/или уменьшать степень распространения заболевания в данный интервал времени по сравнению со случаем, когда этот способ не используют. Такие сравнения обычно основаны на клинических исследованиях с использованием статистически значимого числа субъектов. Развитие легочной гипертензии может быть обнаружено с помощью стандартных методов, таких как обычные медицинские осмотры, рентген, электрокардиограмма и эхокардиограмма. Развитие может также обозначать прогрессию заболевания, которая может быть вначале не обнаруживаемой и включать возникновение и проявление заболевания.
[0061] Используемое в изобретении выражение "подверженный риску" индивидуум представляет собой индивидуума, который подвержен риску развития легочной гипертензии. У "подверженного риску" индивидуума может быть диагностировано или может не быть диагностировано заболевание, и у него может проявляться или может не проявляться диагностированное заболевание до применения описанных в изобретении способов лечения. Выражение "подвергнутый риску" обозначает, что индивидуум подвергается одному или более так называемым факторам риска, которые представляют собой измеряемые параметры, коррелирующие с развитием легочной гипертензии, и которые описаны в изобретении. Индивидуум, подвергающийся одному или более из этих факторов риска, имеет более высокую вероятность развития легочной гипертензии, чем индивидуум, не имеющий этих факторов риска (фактора риска).
[0062] Под используемым в изобретении термином "фармацевтически активное соединение" подразумевается химическое соединение, которое индуцирует требуемый эффект, например, лечение, стабилизацию, предотвращение и/или отсрочку возникновения легочной гипертензии.
[0063] Под используемым в изобретении термином "комбинированная терапия" подразумевается первая терапия, которая включает использование наночастиц, содержащих ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель, в сочетании со второй терапией (например, хирургическим вмешательством или использованием терапевтического средства), применяемые для лечения, стабилизации, предотвращения и/или отсрочки возникновения легочной гипертензии. Введение "в сочетании с" другим соединением включает введение в одной и той же композиции или в различных композициях, либо последовательно, одновременно, либо в течение длительного времени. В некоторых вариантах осуществления, комбинированная терапия необязательно включает один или более фармацевтически приемлемых носителя вспомогательных веществ, фармацевтически неактивных соединений и/или инертных веществ.
[0064] В данной области техники считается, что "эффективное количество" может находиться в одной или более дозах, то есть, для достижения требуемых результатов лечения может потребоваться разовая доза или многократные дозы. Эффективное количество может рассматриваться применительно к введению одного или более терапевтических средств, и можно считать, что композиция наночастиц (например, композиция, включающая рапамицин и белковый носитель) вводится в эффективном количестве, если, в сочетании с одним или более другими средствами, может быть достигнут требуемый или положительный результат. Компоненты (например, первое и второе лекарственные средства) при комбинированной терапии по изобретению могут быть введены последовательно, одновременно или в течение длительного времени, используя одни и те же или различные способы введения для каждого компонента. Из этого следует, что эффективное количество при комбинированной терапии включает количество первого лекарственного средства и количество второго лекарственного средства, которые при введении последовательно, одновременно или в течение длительного времени продуцируют требуемый результат.
[0065] Термин "терапевтически эффективное количество" относится к количеству композиции (например, наночастиц, которые включают ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель), терапевтического средства или комбинированное терапевтического препарата, достаточному для продуцирования требуемого терапевтического результата (например, снижение тяжести или продолжительности, стабилизация тяжести или ликвидация одного или более симптомов легочной гипертензии). При терапевтическом применении, положительные или требуемые результаты включают, например, облегчение одного или более симптомов, возникающих вследствие заболевания (биохимических, гистологических и/или поведенческих), в том числе их осложнений и промежуточных патологических фенотипов, проявляющихся в процессе развития заболевания, повышение качества жизни пациентов, страдающих от заболевания, снижение дозы других лекарственных препаратов, требующихся для лечения заболевания, усиление действия другого лекарственного препарата, отсрочка прогрессирования заболевания и/или пролонгирование времени выживания пациентов.
[0066] Термин "профилактически эффективное количество" относится к количеству композиции (например, наночастиц, которые включают ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель), терапевтического средства или комбинированное терапевтического препарата, достаточному для предотвращения или снижения тяжести одного или более последующих симптомов легочной гипертензии при введении индивидууму, который предрасположен и/или у которого может развиться легочная гипертензия. При профилактическом применении, положительные или требуемые результаты включают, например, такие результаты, как исключение или снижение риска, снижение тяжести последующего заболевания или отсрочка начала заболевания (например, отсрочка биохимических, гистологических и/или поведенческих симптомов заболевания, их осложнений и промежуточных патологических фенотипов, проявляющихся в процессе последующего развития заболевания).
[0067] Используемые в изобретении термины "фармацевтически приемлемый" или "фармакологически совместимый" обозначают материал, который не является неприемлемым с биологической или же с другой точки зрения, например, материал может быть введен в фармацевтическую композицию, вводимую пациенту, не вызывая каких-либо существенных нежелательных биологических эффектов или не оказывая вредного воздействия при взаимодействии с любым из других компонентов композиции, в которой он содержится. Фармацевтически приемлемые носители или вспомогательные вещества преимущественно соответствуют требуемым стандартам токсикологических и промышленных испытаний и/или включены в "Руководство по ингредиентам, не являющимся активными веществами", подготовленное Управлением по надзору за качеством продуктов питания и лекарственных средств США.
[0068] Ссылка в изобретении на "приблизительную" величину или параметр включает (и описывает) варианты осуществления, которые относятся к этой величине или параметру как таковым. Например, описание, относящееся к "приблизительно X", включает описание "X".
[0069] Используемый в изобретении термин "приблизительно X-Y" имеет такое же значение, как "от приблизительно X до приблизительно Y". Используемое в изобретении выражение "приблизительно X, Y или Z" имеет такое же значение, как "приблизительно X, приблизительно Y или приблизительно Z".
[0070] Используемая в изобретении ссылка "не" применительно к величине или параметру обычно означает и описывает "за исключением" величины или параметра. Например, способ не используют для лечения рака типа X означает, что способ используют для лечения типов рака за исключением рака типа X.
[0071] Используемая в изобретении форма единственного числа включает не только аспекты с одним элементом, но также включают аспекты с более чем одним элементом. Например, формы единственного числа включают ссылки на множественное число, если из контекста в явном виде не явствует иное. Из этого следует, например, что ссылка на "клетку" включает множество таких клеток, и ссылка на "средство" включает ссылку на одно или более средств, известных специалистам в данной области, и на другие подобные средства.
Способы лечения легочной гипертензии
[0072] В настоящем изобретении предлагается ряд способов применения композиций наночастиц с ингибитором mTOR (например, рапамицином или его производным, например, рапамицином) и белковым носителем (например, альбумином, например, человеческим альбумином, например, человеческим сывороточным альбумином) для лечения легочной гипертензии (например, тяжелой формы легочной артериальной гипертензии). В некоторых вариантах осуществления, доза ингибитора mTOR (например, рапамицина) составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR (например, рапамицина) составляет не менее чем приблизительно 0,1 мг/м2. В некоторых вариантах осуществления, композицию наночастиц вводят по меньшей мере, один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят не чаще чем один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально (например, внутривенно или подкожно).
[0073] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (такого как сиролимус) в легкое индивидуума, где способ включает подкожное введение композиции, такой как фармацевтическая композиция, включающей наночастицы, содержащие рапамицин и альбумин, где доза рапамицина в наночастицах для доставки эффективного количества рапамицина в легкое составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2 (например, от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2), и величины и множество величин внутри указанных диапазонов. В некоторых вариантах осуществления, индивидуум страдает легочной гипертензией (например, тяжелой формой легочной артериальной гипертензии).
[0074] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл через пять дней после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл через семь дней после введения композиции наночастиц. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса II, III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0075] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0076] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2, например, приблизительно 1 мг/м2, приблизительно 2,5 мг/м2, приблизительно 5 мг/м2 или приблизительно 10 мг/м2), и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0077] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, индивидуум подвергается, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает применение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0078] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, индивидуум подвергается, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает применение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0079] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению, по меньшей мере, к одной, двум или трем предшествующим терапиям, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению, по меньшей мере, к двух предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, по меньшей мере, одна, две или три предшествующие терапии включают применение средства, выбранного из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, композицию наночастиц вводят парентерально. В некоторых вариантах осуществления, композицию наночастиц вводят внутривенно. В некоторых вариантах осуществления, композицию наночастиц вводят подкожно. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0080] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0081] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий подкожное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий подкожное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0082] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, индивидуум подвергается, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает применение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0083] В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий подкожное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ лечения легочной гипертензии у индивидуума, включающий подкожное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, индивидуум подвергается, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает применение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. В некоторых вариантах осуществления, композицию наночастиц вводят приблизительно один раз в неделю. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR в крови составляет не более чем приблизительно 20 нг/мл в течение 7 дней или на 7-ой день после введения композиции наночастиц. В некоторых вариантах осуществления, композиция включает более чем приблизительно 50% ингибитора mTOR в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму. В некоторых вариантах осуществления, белковый носитель представляет собой человеческий сывороточный альбумин. В некоторых вариантах осуществления, средний диаметр наночастиц в композиции составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем приблизительно 18:1. В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0084] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0085] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0086] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0087] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0088] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0089] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0090] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0091] В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения состояния при недостаточности кровообращения (например, при недостаточности сердечного выброса) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) на более чем приблизительно 10%, 15%, 20%, 25 или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0092] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0093] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0094] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0095] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0096] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0097] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0098] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0099] В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ снижения сопротивления легочных сосудов (PVR) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25% или 30% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0100] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0101] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0102] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0103] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0104] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0105] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0106] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0107] В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения результатов теста на преодоление пешком дистанции за шесть минут у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за шесть минут на более чем приблизительно 10%, 15%, 20%, 25%, 30% или 35% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0108] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0109] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0110] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0111] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0112] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0113] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0114] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0115] В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ улучшения сердечного выброса (CO) или сердечного притока (CI) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 2,5%, 5%, 7,5% или 10% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0116] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легки индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0117] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0118] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, и где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0119] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет менее чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 5 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 5 мг/м2, или от приблизительно 2,5 мг/м2 до приблизительно 5 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0120] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0121] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0122] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму внутривенно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0123] В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, предлагается способ доставки эффективного количества ингибитора mTOR (например, рапамицина или его производного) в легкие индивидуума, страдающего легочной гипертензией, включающий внутривенное введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2, где композицию наночастиц вводят индивидууму подкожно, где индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии, и где легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, индивидуум имеет концентрацию ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 250, 500, 750, 1000, 1100 или 1200 нг/г через 24 часа после введения. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для продуцирования концентрации ингибитора mTOR в легких, по меньшей мере, приблизительно 50, 100, 150, 200, 250, 300 или 320 нг/г через 120 часов после введения. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель).
[0124] В некоторых вариантах осуществления, предлагается способ повышения качества жизни у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин или его производное) и белковый носитель (например, альбумин), где доза ингибитора mTOR в композиции составляет не более чем приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2(например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 2,5 мг/м2 до приблизительно 10 мг/м2, или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, доза ингибитора mTOR в композиции составляет не более чем приблизительно 5 мг/м2. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III или IV по классификации Всемирной организации здравоохранения (ВОЗ). В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких. В некоторых вариантах осуществления, композицию наночастиц вводят в течение, по меньшей мере, приблизительно четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель). В некоторых вариантах осуществления, повышенное качество жизни характеризуется улучшенной оценкой в баллах качества жизни после проведения лечения в сравнении с соответствующей оценкой в баллах перед введением наночастиц ингибитора mTOR. В некоторых вариантах осуществления, оценка качества жизни в балах основывается на самооценке при проведении опроса (например, emPHasis-10). Смотрите публикацию Yorke et al., Eur Respir J. 2014 Apr; 43(4): 1106-1113. В некоторых вариантах осуществления, суммарная оценка в баллах качества жизни снижается, по меньшей мере, приблизительно на 10%, 20%, 30%, 40% или 50% после введения ингибитора mTOR по сравнению с соответствующей начальной оценкой в баллах, проведенной до введения ингибитора mTOR.
Дозирование и способ введения
[0125] Доза композиции по изобретению, вводимая индивидууму (такому как человек), может изменяться в зависимости от конкретно применяемой композиции, способа введения и конкретной стадии легочной гипертензии, повергаемой лечению. Количество должно быть достаточным для продуцирования требуемого ответа, такого как терапевтический или профилактический ответ против легочной гипертензии. В некоторых вариантах осуществления, количество композиции представляет собой терапевтически эффективное количество. В некоторых вариантах осуществления, количество композиции представляет собой профилактически эффективное количество. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции находится ниже уровня, который вызывает токсикологическое воздействие (то есть, воздействие выше клинически допустимого уровня токсичности), или находится на уровне, при котором потенциальный побочный эффект можно контролировать или он допустим при введении композиции индивидууму.
[0126] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для повышения базальной активности AKT, повышения фосфорилирования AKT, повышения активности PI3-киназы, увеличения продолжительности активации AKT (например, активации, индуцированной экзогенным IGF-1), ингибирования фосфорилирования серина в IRS-1, ингибирования деградации IRS-1, ингибирования или изменения подклеточной локализации CXCR4, ингибирования секреции VEGF, снижения экспрессии циклина D2, снижения экспрессии сурвивина, ингибирования IL-6-индуцированного роста клеток множественной миеломы, ингибирования клеточной пролиферации при легочной гипертензии, повышения апоптоза, увеличения блокирования клеточного цикла, увеличения расщепления поли(ADPрибоза)полимеразы, увеличения расщепления каспазы-8/каспазы-9, изменения или ингибирования активации сигнальных путей фосфатидилинозитол-3-киназа/AKT/mTOR и/или циклин D1/ретинобластома, ингибирования ангиогенеза и/или ингибирования образования остеокластов.
[0127] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения увеличения сердечного выброса (CO) или сердечного притока (CI) на более чем приблизительно 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода не более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается увеличение величины CO или CI приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается увеличение величины CO или CI приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев, вследствие чего обнаруживается увеличение величины CO или CI приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6 или 7 лет, вследствие чего обнаруживается увеличение величины CO или CI приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%.
[0128] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для снижения сопротивления легочных сосудов (PVR) приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода не более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается снижение величины PVR приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается снижение величины PVR приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев, вследствие чего обнаруживается снижение величины PVR приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6 или 7 лет, вследствие чего обнаруживается снижение величины PVR приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%.
[0129] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения улучшения результатов теста на преодоление пешком дистанции за 6 минут (6MWD) более чем приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода не более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается улучшение результатов выполнения теста 6MWD приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается улучшение результатов выполнения теста 6MWD приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев, вследствие чего обнаруживается улучшение результатов выполнения теста 6MWD приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6 или 7 лет, вследствие чего обнаруживается улучшение результатов выполнения теста 6MWD приблизительно на 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50%.
[0130] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, достаточное для достижения положительного результата у индивидуума или у совокупности индивидуумов, подвергнутых лечению с помощью композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин), при проведении любой одной или более следующих оценок: 1) оценка методом доплеровской эхокардиографии структуры и функции правого желудочка, 2) исследование функции легких (такой как форсированная жизненная емкость (FVC)); 3) NT Pro-BNP; 4) CRP; 5) тропонин; 6) липиды натощак; 7) функциональный класс по классификации ВОЗ; 8) давление в легочной артерии (PAP); 9) давление окклюзии легочной артерии (PAOP); 10) давление заклинивания в легочных капиллярах (PCWP) или 11) центральное венозное давление (CVP). В некоторых вариантах осуществления, положительный результат включает улучшение функционального класса по классификации ВОЗ. В некоторых вариантах осуществления, улучшение включает изменение от III функционального класса по классификации легочной артериальной гипертензии ВОЗ до II функционального класса по классификации легочной артериальной гипертензии ВОЗ. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода не более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается положительный результат. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель, вследствие чего обнаруживается положительный результат. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 месяцев, вследствие чего обнаруживается положительный результат. В некоторых вариантах осуществления, индивидууму вводят композицию ингибитора mTOR в течение периода более чем приблизительно 1, 2, 3, 4, 5, 6 или 7 лет, вследствие чего обнаруживается положительный результат. В некоторых вариантах осуществления, у индивидуума обнаруживается изменение, по меньшей мере, приблизительно на 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% любой из описанных выше оценок после того, как его подвергают лечению с помощью композиции наночастиц ингибитора mTOR, по сравнению с исходным уровнем (то есть, до проведения лечения). В некоторых вариантах осуществления, у индивидуума обнаруживается изменение, по меньшей мере, приблизительно на 2%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45% или 50% любого из описанных выше симптомов после того, как его подвергают лечению с помощью композиции наночастиц ингибитора mTOR в течение периода не более чем приблизительно 4, 6, 8, 10, 12, 14 или 16 недель.
[0131] В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции представляет собой количество, которое обеспечивает благоприятный профиль безопасности у индивидуума, страдающего легочной гипертензией. В некоторых вариантах осуществления, благоприятный профиль безопасности сохраняется в течение, по меньшей мере, приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 недель. В некоторых вариантах осуществления, благоприятный профиль безопасности не включает в себя серьезное нежелательное явление (SAE). В некоторых вариантах осуществления, серьезное нежелательное явление включает состояние смерти, состояние, угрожающее жизни, состояние, требующее госпитализации больного или пролонгирования существующей госпитализации, состояние, приводящее к постоянной и значительное потери трудоспособности или дееспособности, состояние, вызывающее врожденную аномалию или порок развития, и/или другое важное с медицинской точки зрения серьезное осложнение. В некоторых вариантах осуществления, благоприятный профиль безопасности не включает более чем приблизительно 0, 1, 2, 3, 4, 5, 6, 7 или 8 нежелательных явлений в период в течение приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 недель после начала введения композиции mTOR. В некоторых вариантах осуществления, нежелательное явления включает несколько из нежелательных явлений, описанных в Общей терминологии критериев нежелательных явлений (Common Terminology Criteria for Adverse Events (CTCAE)) версии 4.0 или более высокой версии. Например, в некоторых вариантах осуществления, нежелательное явление включает все нежелательные явления степени 2 или выше, описанные в Общей терминологии критериев нежелательных явлений (CTCAE) версии 4.0 или более высокой версии. В некоторых вариантах осуществления, нежелательное явления включает все нежелательные явления степени 3 или выше, описанные в Общей терминологии критериев нежелательных явлений (CTCAE) версии 4.0 или более высокой версии. В некоторых вариантах осуществления, нежелательное явления включает все нежелательные явления (то есть, все нежелательные явления от степени 1 или выше), описанные в Общей терминологии критериев нежелательных явлений (CTCAE) версии 4.0 или более высокой версии. В некоторых вариантах осуществления, нежелательное явления включает тромбоцитопению степени 1 или выше, высыпание степени 2 или выше, парестезию степени 1 или выше, гипертриглицеридемию или гиперхолестеринемию степени 1 или выше, диарею степени 1 или выше, воспаление подкожной клетчатки/инфекцию, требующие внутривенного введения антител степени 3 или выше.
[0132] В некоторых вариантах осуществления, в изобретении предлагается способ лечения легочной гипертензии у индивидуума путем введения индивидууму (например, человеку) эффективного количества композиции, включающей наночастицы, которые содержат ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель (например, альбумин, такой как человеческий сывороточный альбумин). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции находится в любом из следующих диапазонов: от приблизительно 0,1 до приблизительно 1 мг, от приблизительно 1 до приблизительно 3 мг, от приблизительно 3 до приблизительно 6 мг, от приблизительно 6 до приблизительно 9 мг, от приблизительно 9 до приблизительно 12 мг, от приблизительно 12 до приблизительно 15 мг, или от приблизительно 15 до приблизительно 18 мг. В некоторых вариантах осуществления, количество рапамицина или его производного в эффективном количестве композиции (например, в лекарственной форме с разовой дозой) находится в диапазоне от приблизительно 0,1 мг до приблизительно 18 мг, например, от приблизительно 1 мг до приблизительно 18 мг. В некоторых вариантах осуществления, концентрация рапамицина в композиции является разбавленной (приблизительно 0,1 мг/мл) или концентрированной (приблизительно 100 мг/мл), в том числе, например, любая из концентраций от приблизительно 0,1 до приблизительно 50 мг/мл, от приблизительно 0,1 до приблизительно 20 мг/мл, от приблизительно 1 до приблизительно 10 мг/мл, от приблизительно 2 мг/мл до приблизительно 8 мг/мл, от приблизительно 4 до приблизительно 6 мг/мл, приблизительно 5 мг/мл. В некоторых вариантах осуществления, концентрация рапамицина составляет, по меньшей мере, приблизительно 0,5 мг/мл, 1,3 мг/мл, 1,5 мг/мл, 2 мг/мл, 3 мг/мл, 4 мг/мл, 5 мг/мл, 6 мг/мл, 7 мг/мл, 8 мг/мл, 9 мг/мл, 10 мг/мл, 15 мг/мл, 20 мг/мл, 25 мг/мл, 30 мг/мл, 40 мг/мл или 50 мг/мл.
[0133] Примеры эффективных количеств ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции наночастиц включают, но этим не ограничивая, приблизительно 0,1 мг/м2, 0,5 мг/м2, 1 мг/м2, 1,5 мг/м2, 2 мг/м2, 2,5 мг/м2, 3 мг/м2, 3,5 мг/м2, 4 мг/м2, 4,5 мг/м2, 5 мг/м2, 5,5 мг/м2, 6 мг/м2, 6,5 мг/м2, 7 мг/м2, 7,5 мг/м2, 8 мг/м2, 8,5 мг/м2, 9 мг/м2, 9,5 мг/м2 или 10 мг/м2. В различных вариантах осуществления, композиция включает не более чем приблизительно 10 мг/м2, 9,5 мг/м2, 9 мг/м2, 8,5 мг/м2, 8 мг/м2, 7,5 мг/м2, 7 мг/м2, 6,5 мг/м2, 6 мг/м2, 5,5 мг/м2, 5 мг/м2, 4,5 мг/м2, 4 мг/м2, 3,5 мг/м2, 3 мг/м2, 2,5 мг/м2, 2 мг/м2, 1,5 мг/м2 или 1 мг/м2 ингибитора mTOR (например, рапамицина или его производного, например, рапамицина). В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицин или его производного, например, рапамицина) при одном введении составляет менее чем приблизительно 10 мг/м2, 9,5 мг/м2, 9 мг/м2, 8,5 мг/м2, 8 мг/м2, 7,5 мг/м2, 7 мг/м2, 6,5 мг/м2, 6 мг/м2, 5,5 мг/м2, 5 мг/м2, 4,5 мг/м2, 4 мг/м2, 3,5 мг/м2, 3 мг/м2, 2,5 мг/м2, 2 мг/м2, 1,5 мг/м2 или 1 мг/м2. В некоторых вариантах осуществления, эффективное количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции находится в любом из следующих диапазонов: от приблизительно 0,1 до приблизительно 1 мг/м2, от приблизительно 1 до приблизительно 10 мг/м2 (например, приблизительно 1-2, 2-3, 3-4, 4-5, 5-6, 6-7, 7-8, 8-9, 9-10 мг/м2), от приблизительно 1 до приблизительно 2,5 мг/м2, от приблизительно 2,5 до приблизительно 5 мг/м2, от приблизительно 5 до приблизительно 7,5 мг/м2, или от приблизительно 7,5 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, эффективное количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции составляет от приблизительно 0,1 до приблизительно 10 мг/м2, например, от приблизительно 1 до приблизительно 5 мг/м2, или приблизительно 5 мг/м2, приблизительно 10 мг/м2. В некоторых вариантах осуществления, эффективное количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции составляет приблизительно 5 мг/м2.
[0134] В некоторых вариантах осуществления любого из приведенных выше аспектов, эффективное количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции включает, по меньшей мере, приблизительно 0,001 мг/кг, 0,005 мг/кг, 0,01 мг/кг, 0,02 мг/кг, 0,05 мг/кг, 0,1 мг/кг, 0,12 мг/кг, 0,14 мг/кг, 0,16 мг/кг, 0,18 мг/кг, 0,20 мг/кг, 0,22 мг/кг или 0,24 мг/кг. В различных вариантах осуществления, эффективное количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции включает не более чем приблизительно или менее чем приблизительно 0,24 мг/кг, 0,22 мг/кг, 0,2 мг/кг, 0,18 мг/кг, 0,16 мг/кг, 0,14 мг/кг, 0,12 мг/кг, 0,10 мг/кг, 0,05 мг/кг, 0,02 мг/кг или 0,01 мг/кг ингибитора mTOR (например, рапамицина или его производного, например, рапамицина).
[0135] В некоторых вариантах осуществления, доза ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в композиции составляет не более чем приблизительно 50%, 40%, 30%, 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от максимально переносимой дозы (MTD) ингибитора mTOR в композиции.
[0136] В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет, по меньшей мере, приблизительно 2, 3, 4, 5, 6, 7 или 8 нг/мл сразу после или в течение 1, 2, 3, 4, 5, 6 или 7 дней после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет, по меньшей мере, приблизительно 2 нг/мл на 5-ый день после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет, по меньшей мере, приблизительно 2, 3, 4, 5, 6, 7 или 8 нг/мл на 1, 2, 3 или 4 день перед введением следующей дозы композиции наночастиц.
[0137] В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет не более чем приблизительно 30, 28, 26, 24, 22, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9 или 8 нг/мл сразу после или в течение 3, 4, 5, 6 или 7 дней после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет не более чем приблизительно 20 нг/мл после или в течение 7 дней после введения композиции наночастиц. В некоторых вариантах осуществления, концентрация ингибитора mTOR (например, рапамицина) в крови составляет не более чем приблизительно 30, 28, 26, 24, 22, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9 или 8 нг/мл на 1, 2, 3 или 4 день до введения следующей дозы композиции наночастиц.
[0138] В некоторых вариантах осуществления, индивидуум имеет или у него поддерживается остаточный уровень (например, средний остаточный уровень) ингибитора mTOR, по меньшей мере, приблизительно 0,1 нг/мл (такой как, по меньшей мере, приблизительно 0,5 нг/мл или 1 нг/мл) в течение периода лечения. В некоторых вариантах осуществления, индивидуум имеет или у него поддерживается остаточный уровень (например, средний остаточный уровень) ингибитора mTOR не более чем приблизительно 300 нг/мл (такой как не более чем приблизительно 100 нг/мл, 50 нг/мл или 20 нг/мл) в течение периода лечения. В некоторых вариантах осуществления, индивидуум имеет или у него поддерживается остаточный уровень (например, средний остаточный уровень) ингибитора mTOR приблизительно 0,1-300 нг/мл (такой как приблизительно 0,5-50 нг/мл или 1-20 нг/мл) в течение периода лечения. В некоторых вариантах осуществления, индивидууму вводят композицию наночастиц ингибитора mTOR (например, рапамицина) с частотой приблизительно от одного раза в неделю до одного раза каждые две недели (например, с частотой приблизительно один раз в неделю) в течение периода лечения.
[0139] В некоторых вариантах осуществления, остаточная концентрация ингибитора mTOR (например, рапамицина) в крови составляет, по меньшей мере, приблизительно 2, 3, 4, 5, 6, 7 или 8 нг/мл. В некоторых вариантах осуществления, остаточная концентрация ингибитора mTOR (например, рапамицина) в крови составляет, по меньшей мере, приблизительно 2 нг/мл. В некоторых вариантах осуществления, остаточная концентрация ингибитора mTOR (например, рапамицина) в крови составляет не более чем приблизительно 30, 28, 26, 24, 22, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9 или 8 нг/мл. В некоторых вариантах осуществления, остаточная концентрация ингибитора mTOR (например, рапамицина) в крови составляет не более чем приблизительно 20 нг/мл.
[0140] В некоторых вариантах осуществления, композицию наночастиц вводят в течение не чаще чем один раз в неделю, например, один раз в неделю без перерыва; один раз в неделю, в три недели из четырех недель; один раз каждые три недели; один раз каждые две недели; или один раз в неделю, в две недели из трех недель. В некоторых вариантах осуществления, композицию вводят приблизительно один раз каждые 2 недели, один раз каждые 3 недели, один раз каждые 4 недели, один раз каждые 6 недель или один раз каждые 8 недель. В некоторых вариантах осуществления, композицию наночастиц вводят не чаще чем два раза в неделю, три раза в неделю, четыре раза в неделю, пять раз в неделю, шесть раз в неделю. В некоторых вариантах осуществления, композицию вводят, по меньшей мере, один раз в неделю. В некоторых вариантах осуществления, композицию вводят, по меньшей мере, приблизительно 1 раз, 2 раза, 3 раза, 4 раза, 5 раз, 6 раз или 7 раз (то есть, ежедневно) в неделю. В некоторых вариантах осуществления, интервалы между каждым введением составляют менее чем приблизительно 3 месяца, 1 месяц, 20 дней, 15 дней, 12 дней, 10 дней, 9 дней, 8 дней, 7 дней, 6 дней, 5 дней, 4 дня, 3 дня, 2 дня или 1 день. В некоторых вариантах осуществления, интервалы между каждым введением составляют более чем приблизительно 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 8 месяцев или 12 месяцев. В некоторых вариантах осуществления, не предусмотрен перерыв в режиме дозирования. В некоторых вариантах осуществления, интервал между каждым введением составляет не более чем приблизительно неделю.
[0141] Введение композиции может быть продлено в течение длительного периода времени, например, от приблизительно четырех недель до приблизительно семи лет. В некоторых вариантах осуществления, композицию вводят в течение периода, по меньшей мере, приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 14, 16, 20, 24, 28, 32, 36, 40, 44 или 48 недель. В некоторых вариантах осуществления, композицию вводят в течение периода, по меньшей мере, приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 18, 24, 30, 36, 48, 60, 72 или 84 месяцев. В некоторых вариантах осуществления, рапамицин или его производное вводят в течение периода, по меньшей мере, четырех недель, где интервал между каждым введением составляет не более чем приблизительно неделю, и где доза ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) при каждом введении составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2. В некоторых вариантах осуществления, композицию вводят в течение не более чем приблизительно 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 14, 16, 20, 24, 28 или 32 недель. В некоторых вариантах осуществления, композицию вводят в течение не более чем приблизительно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 18, 24, 30, 36, 48, 60, 72 или 84 месяцев.
[0142] В некоторых вариантах осуществления, рапамицин или его производное вводят в течение периода, по меньшей мере, четырех недель (например, в течение, по меньшей мере, приблизительно восьми, двенадцати, шестнадцати, двадцати четырех, тридцати двух, сорока или сорока восьми недель), где интервал между каждым введением составляет не более чем приблизительно неделю, и где доза ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) при каждом введении составляет от приблизительно 0,1 мг/м2 до приблизительно 10 мг/м2, например, от приблизительно 1 мг/м2 до приблизительно 10 мг/м2 или от приблизительно 5 мг/м2 до приблизительно 10 мг/м2.
[0143] С целью контролирования побочных действий лекарственного препарата, дозирование композиции наночастиц может быть отменено или прервано с уменьшением или без уменьшения дозы.
[0144] В некоторых вариантах осуществления, способ включает фазу индукции и фазу поддержания. В некоторых вариантах осуществления, фаза индукции включает введение композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин) и белковый носитель (например, альбумин), один раз в неделю. В некоторых вариантах осуществления, фаза поддержания включает введение композиции, включающей наночастицы, содержащие ингибитор mTOR (например, рапамицин) и белковый носитель (например, альбумин), реже чем один раз в неделю (например, один раз каждые две недели, например, один раз каждые три недели). В некоторых вариантах осуществления, фаза поддержания включает в себя, по меньшей мере, 1, 2, 4, 6, 8, 10, 12, 14, 16, 18 или 20 недель.
[0145] В некоторых вариантах осуществления, в изобретении предлагается способ лечения легочной гипертензии у индивидуума путем парентерального введения индивидууму (например, человеку) эффективного количества композиции, включающей наночастицы, которые содержат ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель (например, альбумин, такой как человеческий сывороточный альбумин). В изобретении также предлагается способ лечения легочной гипертензии у индивидуума путем внутривенного, внутриартериального, внутримышечного, подкожного, ингаляционного, интраперитонеального, назального или интратрахеального введения индивидууму (например, человеку) эффективного количества композиции, включающей наночастицы, которые содержат ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и белковый носитель (например, альбумин, такой как человеческий сывороточный альбумин). В некоторых вариантах осуществления, способ введения представляет собой внутривенный, внутриартериальный, внутримышечный или подкожный способ введения. В некоторых вариантах осуществления, композицию наночастиц вводят субъекту системно (например, внутривенно или подкожно). В некоторых вариантах осуществления, способ введения представляет собой внутривенный способ введения. В некоторых вариантах осуществления, способ введения представляет собой подкожный способ введения. В некоторых вариантах осуществления, эффективное количество композиции вводят системно (например, внутривенно) в течение периода времени менее 30 минут. В некоторых вариантах осуществления, эффективное количество композиции вводят системно (например, внутривенно) в течение периода времени приблизительно 30 минут, 20 минут, 15 минут, 10 минут, 5 минут или 1 минуты.
[0146] В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR обеспечивает возможность инфузионного введения композиции наночастиц ингибитора mTOR индивидууму в течение времени инфузии, которое короче чем приблизительно 24 часа. Например, в некоторых вариантах осуществления, композицию наночастиц ингибитора mTOR (такую как композиция наночастиц рапамицин/альбумин) вводят в течение периода времени инфузии менее чем приблизительно 24 часов, 12 часов, 8 часов, 5 часов, 3 часов, 2 часов, 1 часа, 30 минут, 20 минут или 10 минут. В некоторых вариантах осуществления, композицию наночастиц ингибитора mTOR (такую как композиция наночастиц рапамицин/альбумин) вводят в течение периода времени инфузии приблизительно 30 минут.
[0147] В некоторых вариантах осуществления, в композиции не содержится таксан. В некоторых вариантах осуществления, рапамицин или его производное является единственным фармацевтически активным средством для лечения легочной гипертензии, которое содержится в композиции.
[0148] Любая из описанных в изобретении композиций может быть введена индивидууму (такому как человек) различными способами, включающими, например, внутривенный, внутриартериальный, интраперитонеальный, внутрилегочный, пероральный, ингаляционный, интравезикулярный, внутримышечный, интратрахеальный, подкожный, интраокулярный, интратекальный, трансмукозальный, и трансдермальный способы введения. В некоторых вариантах осуществления, может быть использована лекарственная форма замедленным непрерывным высвобождением композиции. В одном варианте изобретения, наночастицы (такие как наночастицы альбумина) соединений по изобретению могут быть введены любым приемлемым способом, включая, но этим не ограничивая, пероральный, внутримышечный, трансдермальный, внутривенный способы, с помощью ингалятора или других систем доставки взвешенных в воздухе частиц и других подобных приспособлений. В некоторых вариантах осуществления, рапамицин или его производное наносят в виде слоя на стент или вводят с использованием стента. В некоторых вариантах осуществления, рапамицин или его производное не наносят в виде слоя на стент или не вводят с использованием стента.
[0149] В некоторых вариантах осуществления, композиция наночастиц может быть введена путем ингаляции для лечения легочной гипертензии. В некоторых вариантах осуществления, композиция наночастиц может быть введена путем ингаляции с использованием аэрозоля для лечения легочной гипертензии. Составы, применяемые для аэрозольного введения включают композицию, содержащую водные и неводные изотонические стерильные растворы, которые могут включать антиоксиданты, буферы, бактериостатические средства и растворенные вещества, а также водные и неводные стерильные суспензии, которые могут включать суспендирующие средства, солюбилизаторы, загустители, стабилизаторы и консерванты, по отдельности или в комбинации с другими подходящими компонентами, из которых могут быть приготовлены аэрозольные составы для ингаляционного введения. В некоторых вариантах осуществления, аэрозольный носитель может включать, но этим не ограничивая, лактозу, трегалозу, фарматозу 325 M, сахарозу, маннит и другие подобные вещества. Размер частиц порошка аэрозольного носителя значительно больше чем размер сформированных частиц лекарственного средства (~63-90 мкм для лактозы, 40-100 мкм для фарматозы). Эти аэрозольные составы могут быть помещены в находящиеся под давлением подходящие пропелленты, такие как дифтордихлорметан, пропан, азот, и другие подобные пропелленты. Эти составы могут быть также приготовлены в форме фармацевтических препаратов для применения без использования повышенного давления, например, для применения в небулайзере или аэрозольном ингаляторе.
Композиции наночастиц
[0150] Описанная в изобретении композиция наночастиц ингибитора mTORs включает наночастицы, состоящие (в различных вариантах осуществления, состоящие в основном из или состоящие из) из ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумина (такого как человеческий сывороточный альбумин). Наночастицы плохо растворимых в воде лекарственных средств (таких как макролиды) раскрыты, например, в патентных документах U.S. Pat. Nos. 5916596; 6,506,405; 6749868, 6537579, 7820788 и 8911786, а также в патентных документах U.S. Pat. Pub. Nos. 2006/0263434 и 2007/0082838; PCT Patent Application W008/137148, полное содержание каждого из которых включено в настоящее изобретение путем ссылки на них.
[0151] В некоторых вариантах осуществления, фармацевтические композиции дополнительно включают средство или средства для повышения растворения сухих форм композиций и/или повышения стабильности композиции. В некоторых вариантах осуществления, дополнительное средство или средства включают сахарид. Сахарид может представлять собой, но этим не ограничивая, моносахариды, дисахариды, полисахариды и их производные или модификации. Сахарид может представлять собой, например, маннит, сахарозу, фруктозу, лактозу, мальтозу, декстрозу или трегалозу. В некоторых вариантах осуществления, дополнительное средство или средства включают глицин. Поэтому, в настоящем изобретении, в одном аспекте предлагается фармацевтическая композиция, применяемая для подкожного введения индивидууму, включающая a) наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин, и b) сахарид.
[0152] В некоторых вариантах осуществления, сахарид присутствует в количестве, которое является эффективным для повышения стабильности наночастиц в композиции по сравнению с композицией наночастиц без сахарида. В некоторых вариантах осуществления, сахарид находится в количестве, которое является эффективным для улучшения фильтруемости композиции наночастиц по сравнению с композицией наночастиц без сахарида.
[0153] В некоторых вариантах осуществления, сахарид присутствует в количестве, эффективном для улучшения растворимости фармацевтической композиции. В некоторых вариантах осуществления, улучшение растворимости включает повышение скорости растворимости сухой формы композиции наночастиц после добавления раствора для восстановления из нее препарата.
[0154] В некоторых вариантах осуществления, сахарид присутствует в количестве, которое снижает частоту возникновения или тяжесть побочных эффектов после введения при введении композиции наночастиц подкожно. Например, в некоторых вариантах осуществления, побочный эффект представляет собой высыпание, и композиция включает наночастицы, содержащие ингибитор mTOR и альбумин, и сахарид присутствует в количестве, которое снижает частоту возникновения высыпания после подкожного введения композиции наночастиц.
[0155] В некоторых вариантах осуществления, композиция включает наночастицы со средним размером или средним диаметром не более чем приблизительно 1000 нанометров (нм), например, не более чем приблизительно 900, 800, 700, 600, 500, 400, 300, 200 и 100 нм. В некоторых вариантах осуществления, средние размеры или средние диаметры наночастиц составляют не более чем приблизительно 200 нм. В некоторых вариантах осуществления, средние размеры или средние диаметры наночастиц составляют не более чем приблизительно 150 нм. В некоторых вариантах осуществления, средние размеры или средние диаметры наночастиц составляют не более чем приблизительно 100 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 до приблизительно 400 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет не менее чем приблизительно 50 нм. В некоторых вариантах осуществления, наночастицы являются подвергнутыми стерилизующему фильтрованию.
[0156] В некоторых вариантах осуществления, описанные в изобретении частицы (такие как наночастицы) имеют средний размер или средний диаметр не более чем приблизительно 1000, 900, 800, 700, 600, 500, 400, 300, 200, 150, 120 и 100 нм. В некоторых вариантах осуществления, средний размер или средний диаметр частиц составляет не более чем приблизительно 200 нм. В некоторых вариантах осуществления, средний размер или средний диаметр частиц находится в диапазоне от приблизительно 20 нм до приблизительно 400 нм. В некоторых вариантах осуществления, средний размер или средний диаметр частиц находится в диапазоне от приблизительно 40 нм до приблизительно 200 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм. В некоторых вариантах осуществления, средняя величина диаметра частиц составляет менее чем или равен 120 нм. В некоторых вариантах осуществления, средняя величина диаметра частиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм. В некоторых вариантах осуществления, частицы являются подвергнутыми стерилизующему фильтрованию.
[0157] В некоторых вариантах осуществления, описанные в изобретении наночастицы в композиции имеют средний диаметр не более чем приблизительно 200 нм, в том числе, например, не более чем приблизительно 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 90, 80, 70 или 60 нм. В некоторых вариантах осуществления, по меньшей мере, приблизительно 50% (например, по меньшей мере, приблизительно 60%, 70%, 80%, 90%, 95% или 99%) наночастиц в композиции имеют диаметр не более чем приблизительно 200 нм, в том числе, например, не более чем приблизительно 190, 180, 170, 160, 150, 140, 130, 120, 110, 100, 90, 80, 70 или 60 нм. В некоторых вариантах осуществления, по меньшей мере, приблизительно 50% (например, по меньшей мере, 60%, 70%, 80%, 90%, 95% или 99%) наночастиц в композиции находятся в диапазоне от приблизительно 10 нм до приблизительно 400 нм, в том числе, например, от приблизительно 10 нм до приблизительно 200 нм, от приблизительно 20 нм до приблизительно 200 нм, от приблизительно 30 нм до приблизительно 180 нм, от приблизительно 40 нм до приблизительно 150 нм, от приблизительно 40 нм до приблизительно 120 нм и от приблизительно 60 нм до приблизительно 100 нм.
[0158] Методы определения среднего размера частиц являются хорошо известными, например, метод динамического рассеяния света (DLS) традиционно используют при определении размера частиц в субмикронном диапазоне. Смотрите Международный стандарт ISO22412 "Анализ размера частиц - Метод динамического рассеяния света", Международная организация по стандартизации (ISO) 2008 и Определения общепринятых терминов по динамическому рассеянию света, Malvern Instruments Limited, 2011. В некоторых вариантах осуществления, размер частиц измеряют как средневзвешенный средний размер наночастиц (Dv50) в композиции.
[0159] В некоторых вариантах осуществления, наночастицы включают ингибитор mTOR, ассоциированный с альбумином. В некоторых вариантах осуществления, наночастицы включают ингибитор mTOR, с нанесенным на него альбумином.
[0160] В некоторых вариантах осуществления, альбумин имеет сульфгидрильные группы, которые могут образовывать дисульфидные связи. В некоторых вариантах осуществления, по меньшей мере, приблизительно 5% (в том числе, например, по меньшей мере, приблизительно 10%, 15%, 20%, 25%, 30%, 40%, 50%, 60%, 70%, 80%, или 90%) альбумина у части наночастиц композиции являются поперечно сшитым (например, поперечно сшитым с помощью одной или более дисульфидных связей).
[0161] В некоторых вариантах осуществления, наночастицы, включающие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированы (например, покрыты) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин). В некоторых вариантах осуществления, композиция включает ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) как в форме наночастиц, так и в не форме наночастиц (например, в форме растворов или в форме растворимых комплексов альбумин/наночастица), где, по меньшей мере, приблизительно 50%, 60%, 70%, 80%, 90%, 95% или 99% ингибитора mTOR в композиции находится в форме наночастиц. В некоторых вариантах осуществления, ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) в наночастицах составляет более чем приблизительно 50%, 60%, 70%, 80%, 90%, 95% или 99% наночастиц по массе. В некоторых вариантах осуществления, наночастицы не имеют полимерный связующий материал. В некоторых вариантах осуществления, наночастицы включают сердцевину из ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное), которая практически не содержит полимерные материалы (такие как полимерный связующий материал).
[0162] В некоторых вариантах осуществления, композиция включает альбумин в частях композиции как в форме наночастиц, так и не в форме наночастиц, где, по меньшей мере, приблизительно 50%, 60%, 70%, 80%, 90%, 95% или 99% альбумина в композиции находится в части композиции не в форме наночастиц.
[0163] В некоторых вариантах осуществления, массовое отношение альбумина (такого как человеческий альбумин или человеческий сывороточный альбумин) к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции наночастиц ингибитора mTOR составляет приблизительно 18:1 или менее, например, приблизительно 15:1 или менее, например, приблизительно 10:1 или менее. В некоторых вариантах осуществления, массовое отношение альбумина (такого как человеческий альбумин или человеческий сывороточный альбумин) к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции находится в диапазоне от приблизительно 1:1 до приблизительно 18:1, от приблизительно 2:1 до приблизительно 15:1, от приблизительно 3:1 до приблизительно 13:1, от приблизительно 4:1 до приблизительно 12:1, от приблизительно 5:1 до приблизительно 10:1. В некоторых вариантах осуществления, массовое отношение альбумина к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в части наночастиц композиции составляет приблизительно 1:2, 1:3, 1:4, 1:5, 1:9, 1:10, 1:15 или менее. В некоторых вариантах осуществления, массовое отношение альбумина (такого как человеческий альбумин или человеческий сывороточный альбумин) к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции составляют следующие отношения: от приблизительно 1:1 до приблизительно 18:1, от приблизительно 1:1 до приблизительно 15:1, от приблизительно 1:1 до приблизительно 12:1, от приблизительно 1:1 до приблизительно 10:1, от приблизительно 1:1 до приблизительно 9:1, от приблизительно 1:1 до приблизительно 8:1, от приблизительно 1:1 до приблизительно 7:1, от приблизительно 1:1 до приблизительно 6:1, от приблизительно 1:1 до приблизительно 5:1, от приблизительно 1:1 до приблизительно 4:1, от приблизительно 1:1 до приблизительно 3:1, от приблизительно 1:1 до приблизительно 2:1, от приблизительно 1:1 до приблизительно 1:1.
[0164] В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR (такая как композиция наночастиц рапамицин/альбумин) включает одну или более из указанных выше характеристик.
[0165] Описанные в изобретении наночастицы могут присутствовать в сухом составе (таком как лиофилизированная композиция) или могут быть суспендированы в биологически совместимой среде. Подходящие биологически совместимые среды включают, но этим не ограничивая, воду, забуференную водную среду, физиологический раствор, забуференный физиологический раствор, необязательно забуференные растворы аминокислот, необязательно забуференные растворы белков, необязательно забуференные растворы сахаров, необязательно забуференные растворы витаминов, необязательно забуференные растворы синтетических полимеров, липидсодержащие эмульсии и другие подобные среды.
[0166] В некоторых вариантах осуществления, фармацевтически приемлемый носитель включает альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин). Альбумин может быть либо природного происхождения, или получен синтетически. В некоторых вариантах осуществления, альбумин представляет собой человеческий альбумин или человеческий сывороточный альбумин. В некоторых вариантах осуществления, альбумин представляет собой рекомбинантный альбумин.
[0167] Человеческий сывороточный альбумин (HSA) представляет собой хорошо растворимый глобулярный белок с молекулярной массой Mr 65000 и состоит из 585 аминокислот. HSA является самым распространенным белком в плазме и обеспечивает 70-80% коллоидно-осмотического давления человеческой плазмы. Аминокислотная последовательность человеческого сывороточного альбумина (HSA) содержит суммарно 17 дисульфидных мостиков, один свободный тиол (Cys 34) и один триптофан (Trp 214). Внутривенное введение раствора HSA назначали для предотвращения и лечения гиповолемического шока (смотрите, например, публикации Tullis, JAMA, 237: 355-360, 460-463, (1977) и Houser et al., Surgery, Gynecology and Obstetrics, 150: 811-816 (1980)) и совместно с обменным переливанием крови при лечении гипербилирубинемии новорожденных (смотрите, например, публикацию Finlayson, Seminars in Thrombosis and Hemostasis, 6, 85-120, (1980)). Предполагается применение и других альбуминов, таких как бычий сывороточный альбумин. Использование таких нечеловеческих альбуминов могло быть целесообразным, например, в случае использования этих композиций у не принадлежащих к человеческому роду млекопитающих, например в ветеринарии (в том числе при лечении домашних и сельскохозяйственных животных). Человеческий сывороточный альбумин (HSA) имеет множество гидрофобных участков связывания (суммарно восемь для жирных кислот, эндогенный лиганд HSA) и связывается с целым рядом лекарственных средств, в частности, с нейтральными и отрицательно заряженными гидрофобными соединениями (Goodman et al., The Pharmacological Basis of Therapeutics, 9th ed, McGraw-Hill New York (1996)). Было сделано предположение, что два участка связывания с высокой аффинностью находятся в субдоменах IIA и IIIA молекулы HSA, которые представляют собой сильно удлиненные гидрофобные щелевидные углубления с заряженными остатками лизина и аргинина близко к поверхности, которые выполняют функцию точек присоединения для характерных элементов полярных лигандов (смотрите, например, публикации Fehske et al., Biochem. Pharmcol., 30, 687-92 (198a), Vorum, Dan. Med. Bull., 46, 379-99 (1999), Kragh-Hansen, Dan. Med. Bull., 1441, 131-40 (1990), Curry et al., Nat. Struct. Biol., 5, 827-35 (1998), Sugio et al., Protein. Eng., 12, 439-46 (1999), He et al., Nature, 358, 209-15 (199b) и Carter et al., Adv. Protein. Chem., 45, 153-203 (1994)). Было показано, что рапамицин и пропофол связываются с HSA (смотрите, например, публикации Paal et al., Eur. J. Biochem., 268(7), 2187-91 (200a), Purcell et al., Biochem. Biophys. Acta, 1478(a), 61-8 (2000), Altmayer et al., Arzneimittelforschung, 45, 1053-6 (1995) и Garrido et al., Rev. Esp. Anestestiol. Reanim., 41, 308-12 (1994)). Кроме того, было показано, что доцетаксел связывается с белками плазмы крови человека (смотрите, например, публикацию Urien et al., Invest. New Drugs, 14(b), 147-51 (1996)).
[0168] В некоторых вариантах осуществления, описанная в изобретении композиция практически не содержит (например, не содержит) поверхностно-активные вещества, такие как кремофор (или полиоксиэтилированное касторовое масло, в том числе Cremophor EL® (BASF) или Tween 80). В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR (такая как композиция наночастиц рапамицин/альбумин) практически не содержит (например, не содержит) поверхностно-активные вещества. Композиция "практически не содержит кремофор" или "практически не содержит поверхностно-активное вещество", если количество кремофора или поверхностно-активного вещества в композиции является недостаточным для того чтобы вызывать один или более побочных эффектов у индивидуума при введении индивидууму композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин). В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR (такая как композиция наночастиц рапамицин/альбумин) содержит менее чем приблизительно 20%, 15%, 10%, 7,5%, 5%, 2,5% или 1% органического растворителя или поверхностно-активного вещества. В некоторых вариантах осуществления, альбумин представляет собой человеческий альбумин или человеческий сывороточный альбумин. В некоторых вариантах осуществления, альбумин представляет собой рекомбинантный альбумин.
[0169] Количество альбумина в описанной в изобретении композиции будет изменяться в зависимости от других компонентов в композиции. В некоторых вариантах осуществления, композиция включает альбумин в количестве, которое является достаточным для стабилизации ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) в водной суспензии, например, в форме стабильной коллоидной суспензии (такой как стабильная суспензия наночастиц). В некоторых вариантах осуществления, альбумин находится в количестве, которое снижает скорость седиментации ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) в водной среде. Для содержащих частицы композиций, количество альбумина также зависит от размера и плотности наночастиц ингибитора mTOR.
[0170] Ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) является "стабилизированным" в водной суспензии, если он остается суспендированным в водной среде (например, без видимого осаждения или седиментации) в течение продолжительного периода времени, например, в течение, по меньшей мере, приблизительно 0,1, 0,2, 0,25, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36, 48, 60 или 72 часов. Для введения индивидууму (такому как человек) обычно, но не обязательно, применяют суспензию. Стабильность суспензии обычно, но не обязательно, оценивают при температуре хранения (такой как комнатная температура (такая как 20-25ºC) или в условиях охлаждения (например, при 4ºC)). Например, суспензия является стабильной при температуре хранения, если она не обнаруживает признаков флокуляции или агломерации частиц, видимых невооруженным глазом или при рассмотрении через оптический микроскоп при увеличении в 1000 раз, приблизительно через пятнадцать минут после приготовления суспензии. Стабильность может быть оценена в условиях проведения ускоренных испытаний, например, при температуре, которая составляет приблизительно 40ºC или выше.
[0171] Описанные в изобретении композиции могут представлять собой стабильную водную суспензию ингибитора mTOR, например, стабильную водную суспензию ингибитора mTOR при концентрации от приблизительно 0,1 до приблизительно 200 мг/мл, от приблизительно 0,1 до приблизительно 150 мг/мл, от приблизительно 0,1 до приблизительно 100 мг/мл, от приблизительно 0,1 до приблизительно 50 мг/мл, от приблизительно 0,1 до приблизительно 20 мг/мл, от приблизительно 1 до приблизительно 10 мг/мл, от приблизительно 2 мг/мл до приблизительно 8 мг/мл, от приблизительно 4 до приблизительно 6 мг/мл, и приблизительно 5 мг/мл. В некоторых вариантах осуществления, концентрация ингибитора mTOR составляет, по меньшей мере, приблизительно 0,2 мг/мл, 1,3 мг/мл, 1,5 мг/мл, 2 мг/мл, 3 мг/мл, 4 мг/мл, 5 мг/мл, 6 мг/мл, 7 мг/мл, 8 мг/мл, 9 мг/мл, 10 мг/мл, 15 мг/мл, 20 мг/мл, 25 мг/мл, 30 мг/мл, 40 мг/мл, 50 мг/мл, 100 мг/мл, 150 мг/мл или 200 мг/мл.
[0172] В некоторых вариантах осуществления, альбумин присутствует в количестве, которое является достаточным для стабилизации ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) в водной суспензии при определенной концентрации. Например, концентрация ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции составляет от приблизительно 0,1 до приблизительно 100 мг/мл, в том числе, например, от приблизительно 0,1 до приблизительно 50 мг/мл, от приблизительно 0,1 до приблизительно 20 мг/мл, от приблизительно 1 до приблизительно 10 мг/мл, от приблизительно 2 мг/мл до приблизительно 8 мг/мл, от приблизительно 4 до приблизительно 6 мг/мл, или приблизительно 5 мг/мл. В некоторых вариантах осуществления, концентрация ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) составляет, по меньшей мере, приблизительно 1,3 мг/мл, 1,5 мг/мл, 2 мг/мл, 3 мг/мл, 4 мг/мл, 5 мг/мл, 6 мг/мл, 7 мг/мл, 8 мг/мл, 9 мг/мл, 10 мг/мл, 15 мг/мл, 20 мг/мл, 25 мг/мл, 30 мг/мл, 40 мг/мл и 50 мг/мл. В некоторых вариантах осуществления, альбумин присутствует в количестве, которое позволяет не применять поверхностно-активные вещества (такие как кремофор), поэтому композиция не содержит или практически не содержит поверхностно-активное вещество (такое как кремофор).
[0173] В некоторых вариантах осуществления, композиция в жидкой форме включает от приблизительно 0,1% до приблизительно 50% (масса/объем) (например, приблизительно 0,5% (масса/объем), приблизительно 5% (масса/объем), приблизительно 10% (масса/объем), приблизительно 15% (масса/объем), приблизительно 20% (масса/объем), приблизительно 30% (масса/объем), приблизительно 40% (масса/объем) или приблизительно 50% (масса/объем)) альбумина. В некоторых вариантах осуществления, композиция в жидкой форме включает от приблизительно 0,5% до приблизительно 5% (масса/объем) альбумина.
[0174] В некоторых вариантах осуществления, массовое отношение альбумина к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции наночастиц ингибитора mTOR является таким, что достаточное количество ингибитора mTOR связывается с клеткой или транспортируется в клетку. Не смотря на то, что массовое отношение альбумина к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) следует оптимизировать для различных комбинаций альбумина и ингибитора mTOR, тем не менее, как правило, массовое отношение альбумина к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) (по массе) составляет от приблизительно 0,01:1 до приблизительно 100:1, от приблизительно 0,02:1 до приблизительно 50:1, от приблизительно 0,05:1 до приблизительно 20:1, от приблизительно 0,1:1 до приблизительно 20:1, от приблизительно 1:1 до приблизительно 18:1, от приблизительно 2:1 до приблизительно 15:1, от приблизительно 3:1 до приблизительно 12:1, от приблизительно 4:1 до приблизительно 10:1, от приблизительно 5:1 до приблизительно 9:1, или приблизительно 9:1. В некоторых вариантах осуществления, массовое отношение альбумина к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) составляет приблизительно 18:1 или менее, 15:1 или менее, 14:1 или менее, 13:1 или менее, 12:1 или менее, 11:1 или менее, 10:1 или менее, 9:1 или менее, 8:1 или менее, 7:1 или менее, 6:1 или менее, 5:1 или менее, 4:1 или менее, и 3:1 или менее. В некоторых вариантах осуществления, массовое отношение альбумина (такого как человеческий альбумин или человеческий сывороточный альбумин) к ингибитору mTOR (такому как лекарственное средство семейства лимус, например, рапамицин или его производное) в композиции составляет любое одно из следующих значений: от приблизительно 1:1 до приблизительно 18:1, от приблизительно 1:1 до приблизительно 15:1, от приблизительно 1:1 до приблизительно 12:1, от приблизительно 1:1 до приблизительно 10:1, от приблизительно 1:1 до приблизительно 9:1, от приблизительно 1:1 до приблизительно 8:1, от приблизительно 1:1 до приблизительно 7:1, от приблизительно 1:1 до приблизительно 6:1, от приблизительно 1:1 до приблизительно 5:1, от приблизительно 1:1 до приблизительно 4:1, от приблизительно 1:1 до приблизительно 3:1, от приблизительно 1:1 до приблизительно 2:1, приблизительно 1:1.
[0175] В некоторых вариантах осуществления, фармацевтическая композиция включает наночастицы, содержащие ингибитор mTOR и альбумин, где массовое отношение альбумина к ингибитору mTOR в композиции составляет от приблизительно 0,01:1 до приблизительно 100:1. В некоторых вариантах осуществления, композиция включает наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин, где массовое отношение альбумина к ингибитору mTOR (такому как рапамицин) в композиции составляет приблизительно 18:1 или менее (в том числе, например, от приблизительно 1:1 до приблизительно 18:1, от приблизительно 2:1 до приблизительно 15:1, от приблизительно 3:1 до приблизительно 12:1, от приблизительно 4:1 до приблизительно 10:1, от приблизительно 5:1 до приблизительно 9:1, и приблизительно 9:1). В некоторых вариантах осуществления, композиция включает наночастицы, содержащие рапамицин или его производное и альбумин, где массовое отношение альбумина к рапамицину или его производному в композиции составляет приблизительно 18:1 или менее (в том числе, например, от приблизительно 1:1 до приблизительно 18:1, от приблизительно 2:1 до приблизительно 15:1, от приблизительно 3:1 до приблизительно 12:1, от приблизительно 4:1 до приблизительно 10:1, от приблизительно 5:1 до приблизительно 9:1, и приблизительно 9:1). В некоторых вариантах осуществления, на ингибитор mTOR (такой как рапамицин) нанесен слой альбумина.
[0176] В некоторых вариантах осуществления, альбумин позволяет вводить композицию индивидууму (такому как человек) без значительных побочных эффектов. В некоторых вариантах осуществления, альбумин (такой как человеческий сывороточный альбумин или человеческий альбумин) находится в количестве, которое является эффективным для снижения одного или более побочных эффектов введения ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) человека. Термин "снижение одного или более побочных эффектов" введения ингибитора mTOR (такого как лекарственное средство семейства лимус, например, рапамицин или его производное) относится к снижению, облегчению, исключению или устранению одного или более нежелательных эффектов, вызываемых ингибитором mTOR, а также побочных эффектов, вызываемых средствами доставки (такими как растворители, которые делают возможным применение лекарственного средства семейства лимус для инъекции), используемыми для доставки ингибитора mTOR. Такие побочные эффекты включают, например, миелосупрессию, нейротоксичность, гиперчувствительность, воспаление, венозное раздражение, флебит, боль, раздражение кожи, периферическую нейропатию, нейтропеническую лихорадку, анафилактическую реакцию, венозный тромбоз, экстравазацию и их комбинации. Однако, эти побочные эффекты приводятся только в качестве примеров, и могут быть снижены другие побочные эффекты или комбинации побочных эффектов, связанных с лекарственными средствами семейства лимус (такими как лекарственное средство семейства лимус, например, рапамицин или его производное).
[0177] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где средний размер или средний диаметр наночастиц составляет от приблизительно 10 до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где средний размер или средний диаметр наночастиц составляет от приблизительно 40 до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0178] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, от приблизительно 3:1 до приблизительно 9:1, например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм), где массовое отношение альбумина and ингибитор mTOR в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0179] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0180] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, от приблизительно 3:1 до приблизительно 9:1, например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм), где массовое отношение альбумина к рапамицину в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0181] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, стабилизированный альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм). В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0182] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, от приблизительно 3:1 до приблизительно 9:1, например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, стабилизированный альбумином (таким как человеческий сывороточный альбумин), где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100-120 нм, например, приблизительно 100 нм), где массовое отношение альбумина к рапамицину в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0183] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм). В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм). В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где средний размер или средний диаметр наночастиц составляет от приблизительно 10 до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где средний размер или средний диаметр наночастиц составляет от приблизительно 40 до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0184] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин) и альбумин (такой как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин и человеческий альбумин (такой как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм), где массовое отношение альбумина к ингибитору mTOR в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0185] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, стабилизированный альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм), где массовое отношение альбумина к рапамицину в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0186] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0187] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), ассоциированный (например, покрытый слоем) с альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр приблизительно 150 нм, где массовое отношение альбумина к ингибитору mTOR в композиции составляет не более чем приблизительно 9:1 (например, приблизительно 9:1 или приблизительно 8:1). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, ассоциированный (например, покрытый слоем) с человеческим альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм), где массовое отношение альбумина к рапамицину в композиции составляет приблизительно 9:1 или приблизительно 8:1. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0188] В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 200 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм. В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие ингибитор mTOR (такой как рапамицин), стабилизированный альбумином (таким как человеческий альбумин или человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм). В некоторых вариантах осуществления, описанные в изобретении композиции наночастиц ингибитора mTOR включают наночастицы, содержащие рапамицин, стабилизированный альбумином (таким как человеческий сывороточный альбумин), где композиция дополнительно включает сахарид, где наночастицы имеют средний диаметр не более чем приблизительно 150 нм (например, приблизительно 100 нм). В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 10 нм до приблизительно 150 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет от приблизительно 40 нм до приблизительно 120 нм. В некоторых вариантах осуществления, средний размер или средний диаметр наночастиц составляет приблизительно 100-120 нм, например, приблизительно 100 нм.
[0189] В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR включает nab-рапамицин. В некоторых вариантах осуществления, композиция наночастиц ингибитора mTOR представляет собой nab-рапамицин. Nab-рапамицин представляет собой композицию рапамицина, стабилизированного человеческим альбумином USP, который может быть диспергирован в непосредственно инъецируемом физиологическом растворе. Массовое отношение человеческого альбумина к рапамицину составляет от приблизительно 3:1 до приблизительно 9:1, например, от приблизительно 8:1 до приблизительно 9:1. При диспергировании в подходящей водной среде, такой как 0,9% раствор хлорида натрия для инъекции или 5% раствор декстрозы для инъекции, nab-рапамицин образует стабильную коллоидную суспензию рапамицина. Средний размер наночастиц в коллоидной суспензии составляет приблизительно 100 нанометров. Так как HSA легко растворим в воде, то nab-рапамицин может быть ресуспендирован в широком диапазоне концентраций от разбавленной суспензии (0,1 мг/мл рапамицина или его производного) до концентрированной (например, 50 мг/мл рапамицина или его производного), в том числе, например, от приблизительно 2 мг/мл до приблизительно 8 мг/мл, или приблизительно 5 мг/мл.
[0190] Методы приготовления композиций наночастиц являются хорошо известными. Например, наночастицы, содержащие ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) и альбумин (такой как человеческий сывороточный альбумин или человеческий альбумин) могут быть приготовлены в условиях больших сдвиговых усилий (например, при ультразвуковом воздействии, путем гомогенизации под высоким давлением или другими подобными методами). Эти методы раскрыты, например, в патентных документах U.S. Pat. Nos.5916596; 6506405; 6749868, 6537579, 7820788 и 8911786, а также в патентных документах U.S. Pat. Pub. Nos. 2007/0082838, 2006/0263434 и PCT Application WO08/137148.
[0191] Вкратце, ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) растворяют в органическом растворителе, и раствор может быть добавлен к раствору альбумина. Смесь подвергают гомогенизации под высоким давлением. Органический растворитель может быть затем удален путем испарения. Полученная дисперсия может быть затем подвергнута лиофилизированию. Подходящий органический растворитель включает, например, кетоны, сложные эфиры, простые эфиры, хлорированные растворители и другие хорошо известные растворители. Например, органический растворитель может представлять собой метиленхлорид или смесь хлороформ/этанол (например, при соотношении 1:9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1 или 9:1).
[0192] В некоторых вариантах осуществления, композиция представляет собой сухую (например, лиофилизированную) композицию, которая может быть восстановлена, ресуспендирована или регидратирована с образованием, как правило, стабильной водной суспензии наночастиц, содержащих ингибитор mTOR и альбумин. В некоторых вариантах осуществления, композиция представляет собой жидкую (например, водную) композицию, полученную путем восстановления или ресуспендирования сухой композиции. В некоторых вариантах осуществления, композиция представляет собой промежуточную жидкую (например, водную) композицию, которая может быть высушена (например, лиофилизирована).
A. Ингибитор mTOR
[0193] Описанные в некоторых вариантах осуществления изобретения способы включают введение композиций наночастиц ингибитора mTOR. Используемый в изобретении термин "ингибитор mTOR" относится к ингибитору mTOR. mTOR представляет собой серин/треонин-специфическую протеинкиназу, следующую за сигнальным путем фосфатидилинозитола-3-киназа (PI3K)/Akt (протеинкиназа B), и является ключевым регулятором выживаемости, пролиферации, стресса и метаболизма клеток. Дисрегуляция пути mTOR была обнаружена в случае многих карцином у человека, и ингибирование mTOR продуцировало существенные ингибирующие воздействия на прогрессирование опухоли.
[0194] Мишень рапамицина (mTOR) у млекопитающих (также известная как механистическая мишень рапамицина или FK506-связывающий белок 12-рапамицин-ассоциированный белок 1 (FRAP1)) представляет собой атипичную серин/треониновую протеинкиназу, которая присутствует в двух различных комплексах, mTOR комплекс 1 (mTORC1) и mTOR комплекс 2 (mTORC2). mTORC1 состоит из mTOR, регуляторно-ассоциированного белка mTOR (raptor), летального для млекопитающих с белком SEC13 8 (MLST8), PRAS40 и DEPTOR (Kim et al. (2002). Cell 110: 163-75; Fang et al. (2001). Science 294 (5548): 1942-5). mTORC1 объединяет четыре основных входных сигнала: питательные вещества (такие как аминокислоты и фосфатидная кислота), факторы роста (инсулин), энергия и стресс (такие как гипоксия и повреждение ДНК). Доступность аминокислот передается в mTORC1 через путь, включающий Rag и Ragulator (LAMTOR1-3), Факторы роста и гормоны (например, инсулин) передают сигнал в mTORC1 через Akt, который инактивирует TSC2 для предотвращения ингибирования mTORC1. С другой стороны, низкие уровни АТФ приводят к AMPK-зависимой активации TSC2 и фосфорилированию raptor для снижения сигнальных белков mTORC1.
[0195] Активный mTORC1 имеет ряд последующих биологических воздействий, включающих трансляцию мРНК через фосфорилирование нижестоящих мишеней (4E-BP1 и p70 S6 киназа), подавление аутофагии (Atg13, ULK1), биогенез рибосом и активацию транскрипции, приводящую к метаболизму митохондрий или адипогенезу. Соответственно, активность mTORC1 способствует либо росту клеток при благоприятных условиях, либо протеканию катаболических процессов во время стресса при неблагоприятных условиях.
[0196] mTORC2 состоит из mTOR, из нечувствительного к рапамицину компаньона mTOR (RICTOR), GβL и белка 1, взаимодействующего с активируемой стрессом протеинкиназой млекопитающих (mSIN1). В отличие от mTORC1, для которого были определены многие восходящие сигналы и клеточные функции (смотрите выше), о биологии mTORC2 известно относительно мало. mTORC2 регулирует организацию цитоскелета посредством стимуляции стрессовых волокон F-актина, паксиллина, RhoA, Rac1, Cdc42 и протеинкиназы Cα (PKCα). Было обнаружено, что нокдаун компонентов mTORC2 влияет на полимеризацию актина и нарушает морфологию клеток (Jacinto et al. (2004). Nat. Cell Biol. 6, 1122-1128; Sarbassov et al. (2004). Curr. Biol. 14, 1296-1302). Это позволяет предположить, что mTORC2 контролирует актиновый цитоскелет путем промотирования фосфорилирования с помощью протеинкиназы Cα (PKCα), фосфорилирования паксиллина и его перемещению в фокальные адгезии, а также загрузки GTP RhoA и Rac1. Молекулярный механизм, с помощью которого mTORC2 регулирует эти процессы пока не изучен.
[0197] В некоторых вариантах осуществления, ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) представляет собой ингибитор mTORC1. В некоторых вариантах осуществления, ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) представляет собой ингибитор mTORC2. В некоторых вариантах осуществления, ингибитор mTOR (такой как лекарственное средство семейства лимус, например, рапамицин или его производное) представляет собой ингибитор как mTORC1, так и mTORC2.
[0198] В некоторых вариантах осуществления, ингибитор mTOR представляет собой лекарственное средство семейства лимус, которое включает рапамицин и его аналоги. Примеры лекарственных средств семейства лимус включают, но этим не ограничивая, темрапамицин (CCI-779), эверолимус (RAD001), ридафоролимус (AP-23573), дефоролимус (MK-8669), зотаролимус (ABT-578), пимекролимус и такролимус (FK-506). В некоторых вариантах осуществления, лекарственное средство семейства лимус выбирают из группы, состоящей из темрапамицина (CCI-779), эверолимуса (RAD001), ридафоролимуса (AP-23573), дефоролимуса (MK-8669), зотаролимуса (ABT-578), пимекролимуса и такролимуса (FK-506). В некоторых вариантах осуществления, ингибитор mTOR представляет собой ингибитор mTOR-киназы, такой как CC-115 или CC-223.
[0199] В некоторых вариантах осуществления, ингибитор mTOR представляет собой рапамицин. Рапамицин представляет собой макролидный антибиотик, который образует комплекс с FKBP-12 и ингибирует путь mTOR путем связывания mTORC1.
[0200] В некоторых вариантах осуществления, ингибитор mTOR выбирают из группы, состоящей из рапамицина, BEZ235 (NVP-BEZ235), эверолимуса (также известного как RAD001, зортресса, сертикана и афинитора), AZD8055, темрапамицина (также известного как CCI-779 и торизел), CC-115, CC-223, PI-103, Ku-0063794, INK 128, AZD2014, NVP-BGT226, PF-04691502, CH5132799, GDC-0980 (RG7422), Torin 1, WAY-600, WYE-125132, WYE-687, GSK2126458, PF-05212384 (PKI-587), PP-121, OSI-027, Palomid 529, PP242, XL765, GSK1059615, WYE-354 и ридафоролимуса (также известного как дефоролимус).
[0201] BEZ235 (NVP-BEZ235) представляет собой производное имидазохилонина, которое является каталитическим ингибитором mTORC1 (Roper J, et al. PLoS One, 2011, 6(9), e25132). Эверолимус представляет собой 40-O-(2-гидроксиэтильное) производное рапамицина и связывает циклофилин FKBP-12, и он также образует комплекс с mTORC1. AZD8055 является синтетическим препаратом, который ингибирует фосфорилирование mTORC1 (p70S6K и 4E-BP1). Темрапамицин является синтетическим препаратом, который образует комплекс с FK506-связывающим белком и препятствует активации mTOR, когда он входит в состав комплекса mTORC1. PI-103 является синтетическим препаратом, который ингибирует активацию рапамицин-чувствительного (mTORC1) комплекса (Knight et al. (2006) Cell. 125: 733-47). KU-0063794 является синтетическим препаратом, который ингибирует фосфорилирование mTORC1 в Ser2448 в зависимости от величины дозы и длительности терапии. INK 128, AZD2014, NVP-BGT226, CH5132799, WYE-687 являются каждый синтетическим ингибитором mTORC1. PF-04691502 ингибирует активность mTORC1. GDC-0980 является синтетическим перорально биологически доступным препаратом, который ингибирует PI3 киназу класса I и TORC1. Торин 1 представляет собой мощный синтетический ингибитор mTOR. WAY-600 представляет собой мощный АТФ-конкурирующий и селективный ингибитор mTOR. WYE-125132 представляет собой АТФ-конкурирующий синтетический ингибитор mTORC1. GSK2126458 представляет собой ингибитор mTORC1. PKI-587 представляет собой сильнодействующий ингибитор двойного действия PI3Kα, PI3Kγ и mTOR. PP-121 является многоцелевым ингибитором PDGFR, Hck, mTOR, VEGFR2, Src и Abl. OSI-027 является селективным и мощным ингибитором двойного действия mTORC1 и mTORC2 с величиной IC50 22 нМ и 65 нМ, соответственно. Palomid 529 представляет собой синтетический ингибитор mTORC1, который не обладает аффинность в отношении ABCB1/ABCG2 и характеризуется высокой степенью проникновения в головной мозг (Lin et al. (2013) Int J Cancer DOI: 10,1002/ijc. 28126 (электронная публикация перед выходом печатной публикации). PP242 является селективным ингибитором mTOR. XL765 является ингибитором двойного действия mTOR/PI3k для mTOR, p110α, p110β, p110γ и p110δ. GSK1059615 представляет собой новый ингибитор двойного действия PI3Kα, PI3Kβ, PI3Kδ, PI3Kγ и mTOR. WYE-354 ингибирует mTORC1 в клетках линии HEK293 (0,2 мкM-5 мкM) и в клетках линии HUVEC (10 нM-1 мкM). WYE-354 является мощным специфическим АТФ-конкурирующим ингибитором mTOR. Дефоролимус (ридафоролимус, AP23573, MK-8669) является селективным ингибитором mTOR.
B. Белковый носитель
[0202] В некоторых вариантах осуществления, композиция включает ингибитор mTOR и белковый носитель. Термин "белки" относится к полипептидам или полимерам аминокислот любой длины (в том числе к полноразмерным или фрагментам), которые могут быть линейными или разветвленными, включать модифицированные аминокислоты и/или могут прерываться с помощью не аминокислот. Термин также включает в себя полимер аминокислоты, который был модифицирован естественным путем или путем вмешательства, например, путем образования дисульфидной связи, гликозилирования, липидизации, ацетилирования, фосфорилирования или любой другой манипуляции или модификации. Этот термин также включает в себя, например, полипептиды, содержащие один или более аналогов амитнокислоты (в том числе, например, не встречающиеся в природе аминокислоты, и так далее), а также другие известные в данной области модификации. Описанные в изобретении белки могут быть природными, то есть, полученными или произведенными из природного источника (такого как кровь), или синтезированными (например, синтезированными химическими методами или синтезированными технологией рекомбинантных ДНК). Примеры подходящих белковых носителей включают белки, в норме обнаруживаемые в крови или плазме, которые включают, но этим не ограничивая, альбумин, иммуноглобулин, в том числе IgA, липопротеины, аполипопротеин B, альфа-кислый гликопротеин, бета-2-макроглобулин, тиреоглобулин, трансферин, фибронектин, фактор VII, фактор VIII, фактор IX, фактор X и другие подобные белки. В некоторых вариантах осуществления, белковый носитель является не белком крови, например, казеином, α-лактальбумином и β-лактоглобулином. Белковые носители могут быть либо природного происхождения, либо полученными синтетически.
[0203] В некоторых вариантах осуществления, белковый носитель представляет собой альбумин. В некоторых вариантах осуществления, альбумин представляет собой сывороточный альбумин. В некоторых вариантах осуществления, альбумин представляет собой человеческий сывороточный альбумин.
C. Другие компоненты в композиции наночастиц ингибитора mTOR
[0204] Описанные в изобретении наночастицы могут присутствовать в композиции, которая включает другие средства, вспомогательные вещества или стабилизаторы. Например, для повышения стабильности путем повышения отрицательного дзета-потенциала наночастиц, могут быть добавлены конкретные отрицательно заряженные компоненты. Такие отрицательно заряженные компоненты включают, но этим не ограничивая, соли желчных кислот, состоящих из гликохолевой кислоты, холевой кислоты, хенодезоксихолевой кислоты, таурохолевой кислоты, гликохенодезоксихолевой кислоты, таурохенодезоксихолевой кислоты, литохолевой кислоты, урсодеоксихолевой кислоты, дегидрохолевой кислоты и других; фосфолипиды, в том числе фосфолипиды на основе лецитина (яичного желтка), которые включают следующие фосфатидилхолины: пальмитоилолеоилфосфатидилхолин, пальмитоил-линолеоилфосфатидилхолин, стеароиллинолеоилфосфатидилхолин, стеароилолеоилфосфатидилхолин, стеароиларахидоилфосфатидилхолин и дипальмитоилфосфатидилхолин. Другие фосфолипиды включают L-α-димиристоилфосфатидилхолин (DMPC), диолеоилфосфатидилхолин (DOPC), дистеариолфосфатидилхолин (DSPC), гидрированный фосфатидилхолин сои (HSPC) и другие родственные соединения. В качестве добавок могут также использоваться отрицательно заряженные поверхностно-активные вещества или эмульгаторы, например, холестерилсульфат натрия и другие подобные соединения.
[0205] В некоторых вариантах осуществления, композицию применяют для введения человеку. В некоторых вариантах осуществления, композицию применяют для введения млекопитающему например, в ветеринарии, для введения домашним и сельскохозяйственным животным. Имеется большое разнообразие подходящих форм композиции наночастиц ингибитора mTOR (такой как композиция наночастиц рапамицин/альбумин) (смотрите, например, патентные документы U.S. Pat. Nos. 5916596 и 6096331). Приводимые далее формы и способы являются только примерами и никоим образом не ограничивают изобретение. Формы, подходящие для перорального введения могут состоять из (a) жидких растворов, например, эффективного количества соединения, растворенного в разбавителях, таких как вода, физиологический раствор или апельсиновый сок, (b) капсул, пакетиков или таблеток, содержащих заданное количество активного ингредиента в виде твердых частиц или гранул, (c) суспензий в соответствующей жидкости и (d) подходящих эмульсий. Таблетки могут включать одно или более таких веществ как лактоза, маннит, кукурузный крахмал, картофельный крахмал, микрокристаллическая целлюлоза, аравийская камедь, желатин, коллоидный диоксид кремния, кроскармеллоза натрия, тальк, стеарат магния, стеариновая кислота и другие вспомогательные вещества, окрашивающие вещества, разбавители, буферные вещества, увлажняющие средства, консерванты, ароматизаторы и фармакологически совместимые субстанции. Пастилки могут включать активный ингредиент в веществе, корригирующим вкус и запах, обычно, сахарозе и аравийской камеди или трагакантовой камеди, также как ароматизированные таблетки, содержащие активный ингредиент в инертной основе, такой желатин и глицерин, или сахароза и аравийская камедь, эмульсии, гели, и другие подобные вещества, содержащие, помимо активного ингредиента, такие вспомогательные вещества, известные в фармацевтике.
[0206] Примеры подходящих носителей, вспомогательных веществ и разбавителей включают, но этим не ограничивая, лактозу, декстрозу, сахарозу, сорбит, маннит, крахмалы, аравийскую камедь, фосфат калия, альгинаты, трагакантовую камедь, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, физиологический раствор, сироп, метилцеллюлозу, метил- и пропилгидроксибензоаты, тальк, стеарат магния и минеральное масло. В некоторых вариантах осуществления, обсуждаемая в изобретении композиция наночастиц с носителем присутствует в сухой форме (такой как лиофилизированная композиция). Лекарственные формы могут дополнительно включать смазывающие вещества, смачивающие средства, эмульгаторы и суспендирующие средства, консерванты, подсластители или ароматизаторы.
[0207] Формы, подходящие для парентерального введения включают водные и неводные изотонические стерильные инъецируемые растворы, которые могут содержать антиоксиданты, буферы, бактериостатики и растворенные вещества, которые делают лекарственную форму совместимой с кровью предполагаемого реципиента, и водные и неводные стерильные суспензии, которые могут включать суспендирующие средства, солюбилизаторы, загустители, стабилизаторы, и консерванты. Лекарственные формы могут быть представлены в герметизированных контейнерах с разовой дозой или в многодозовых герметизированных контейнерах, таких как ампулы и флаконы, и могут храниться в сублимированном (лиофилизированном) состоянии, требующем только добавления стерильного жидкого вспомогательного средства, например, воды для инъекции, непосредственно перед использованием. Растворы и суспензии для немедленной инъекции могут быть приготовлены из стерильных порошков, гранул и таблеток, которые были описаны ранее. Предпочтительными формами являются инъецируемые формы.
[0208] В некоторых вариантах осуществления, композицию готовят с величиной pH в диапазоне от приблизительно 4,5 до приблизительно 9,0, в том числе, например с величиной pH в диапазоне от приблизительно 5,0 до приблизительно 8,0, от приблизительно 6,5 до приблизительно 7,5, и от приблизительно 6,5 до приблизительно 7,0. В некоторых вариантах осуществления, композицию готовят с величиной pH не менее чем приблизительно 6, в том числе, например, не менее чем приблизительно 6,5, 7 или 8 (например, приблизительно 8). Композиция может быть также приготовлена с добавлением подходящего модификатора тоничности, такого как глицерин, для того чтобы композиция была изотонична с кровью.
Легочная гипертензия
[0209] В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию. В некоторых вариантах осуществления, легочную гипертензию выбирают из группы, состоящей из идиопатической легочной артериальной гипертензии (IPAH), наследственной легочной артериальной гипертензии (HPAH), индуцированной лекарственным препаратом или токсином легочной артериальной гипертензии, ассоциированной с заболеванием соединительной ткани легочной артериальной гипертензии и ассоциированной с врожденными пороками сердца легочной артериальной гипертензии.
[0210] В некоторых вариантах осуществления, легочная гипертензия представляет собой тяжелую форму легочной артериальной гипертензии. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса II, III или IV по классификации Всемирной организации здравоохранения [ВОЗ]. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса II по классификации ВОЗ. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса III по классификации ВОЗ. В некоторых вариантах осуществления, легочная гипертензия легочная гипертензия представляет собой легочную артериальную гипертензию функционального класса IV по классификации ВОЗ.
Индивидуум
[0211] В некоторых вариантах осуществления, индивидуумом является человек. В некоторых вариантах осуществления, индивидуумом является взрослый человек.
[0212] В некоторых вариантах осуществления, индивидуум подвергался, по меньшей мере, одной предшествующей терапии для легочной гипертензии. В некоторых вариантах осуществления, индивидуум подвергался, по меньшей мере, двум предшествующим терапиям для легочной гипертензии. В некоторых вариантах осуществления, индивидуум подвергался одной или двум предшествующим терапиям для легочной гипертензии.
[0213] В некоторых вариантах осуществления, предшествующая терапия включает стандартную или общепринятую терапию для легочной гипертензии. В некоторых вариантах осуществления, предшествующая терапия включает применение вазодилататор. В некоторых вариантах осуществления, предшествующая терапия регулирует вазодилатацию и/или вазоконстрикцию. В некоторых вариантах осуществления, применяемое при предшествующей терапии лекарственное средство выбирают из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, применяемое при предшествующей терапии лекарственное средство выбирают из группы, состоящей из эпопростенола, илопроста, трепростинила, бозентана, мацитентана, амбрисентана, силденафила, тадалафила и риоцигуата. В некоторых вариантах осуществления, вторая терапия включает применение ингибитора тирозинкиназы (например, иматиниба).
[0214] В некоторых вариантах осуществления, в результате проведения предшествующей терапии у индивидуума достигался положительный эффект. В некоторых вариантах осуществления, индивидуум не отвечал на предшествующую терапию. В некоторых вариантах осуществления, индивидуум имел рецидив после предшествующей терапии.
[0215] В некоторых вариантах осуществления, индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению, по меньшей мере, к одной, двум или трем предшествующим терапиям.
[0216] В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития фиброза в легких. В некоторых вариантах осуществления, индивидуум характеризуется высоким уровнем развития ангиогенеза в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным фиброзом в легких. В некоторых вариантах осуществления, индивидуум характеризуется повышенным ангиогенезом в легких.
[0217] В некоторых вариантах осуществления, индивидуум имеет исходный результат теста на преодоление пешком дистанции за 6 минут (6MWD) (измеренный сразу перед началом введения) приблизительно 150-450 метров. В некоторых вариантах осуществления, индивидуум имеет исходную величину отношения форсированной жизненной емкости не менее чем 0,60. В некоторых вариантах осуществления, индивидуум имеет величину объема воздуха при форсированном выдохе в одну секунду (FEV1) не менее чем приблизительно 55% от референсного уровня (например, расчетного нормального уровня). В некоторых вариантах осуществления, индивидуум имеет среднюю величину давления в легочной артерии (PAP) не менее чем приблизительно 25 мм рт.ст. В некоторых вариантах осуществления, индивидуум имеет величину давления заклинивания в легочных капиллярах (PCWP) или величину конечного диастолического давление в левом желудочке (LVEDP) не более чем приблизительно 15 мм рт.ст. В некоторых вариантах осуществления, индивидуум имеет величину сопротивления легочных сосудов (PVR) более чем приблизительно 5 мм рт.ст/л/мин (единиц Вуда).
Комбинированная терапия
[0218] В этом изобретении также предлагаются способы введения ингибитора mTOR (например, рапамицина или его производного) субъекту, имеющему легочную гипертензию, где способ дополнительно включает введение второго терапевтического средства. В некоторых вариантах осуществления, второе терапевтическое средство является стандартным или общепринятым средством, применяемым при легочной гипертензии. В некоторых вариантах осуществления, второе терапевтическое средство включает вазодилататор. В некоторых вариантах осуществления, второе терапевтическое средство регулирует вазодилатацию и/или вазоконстрикцию. В некоторых вариантах осуществления, второе терапевтическое средство выбирают из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC). В некоторых вариантах осуществления, второе терапевтическое средство выбирают из группы, состоящей из эпопростенола, илопроста, трепростинила, бозентана, мацитентана, амбрисентана, силденафила, тадалафила и риоцигуата. В некоторых вариантах осуществления, второе терапевтическое средство включает ингибитор тирозинкиназы (например, иматиниб).
[0219] В некоторых вариантах осуществления, композицию наночастиц вводят одновременно со вторым терапевтическим средством. В некоторых вариантах осуществления, композицию наночастиц вводят параллельно со вторым терапевтическим средством. В некоторых вариантах осуществления, композицию наночастиц вводят последовательно со вторым терапевтическим средством.
Наборы
[0220] В изобретении также предлагаются наборы, включающие описанные в изобретении композиции, составы, лекарственные формы с разовой дозой и готовые препараты, для применения в описанных в изобретении способах лечения, способах введения и режимах дозирования. В некоторых вариантах осуществления любого из этих наборов, наборы могут применяться для лечения легочной гипертензии. В некоторых вариантах осуществления, легочная гипертензия представляет собой идиопатическую легочную артериальную гипертензию (IPAH), наследственную легочную артериальную гипертензию (FPAH) или ассоциированную легочную артериальную гипертензию (APAH). Наборы по изобретению включают один или более контейнеров, содержащих композиции наночастиц рапамицина или его производного (составы или лекарственные формы с разовой дозой и/или готовые препараты), и, в некоторых вариантах осуществления, дополнительно включают инструкции для применения в соответствии с любым из описанных в изобретении способов лечения. В некоторых вариантах осуществления, набор включает i) композицию, содержащую наночастицы, включающие рапамицин и белковый носитель (такой как альбумин), и ii) инструкции по введению наночастиц и химиотерапевтических средств одновременно и/или последовательно для лечения легочной гипертензии. В некоторых вариантах осуществления, легочная гипертензия представляет собой легочную артериальную гипертензию. В некоторых вариантах осуществления, легочная гипертензия представляет собой тяжелую форму легочной артериальной гипертензии. В некоторых вариантах осуществления, легочная артериальная гипертензия представляет собой идиопатическую легочную артериальную гипертензию. В различных вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в наборе находится в любом из следующих диапазонов: от приблизительно 0,1 мг до приблизительно 1 мг, от приблизительно 1 до приблизительно 3 мг, от приблизительно 3 до приблизительно 6 мг, от приблизительно 6 до приблизительно 9 мг, от приблизительно 9 до приблизительно 12 мг, от приблизительно 12 до приблизительно 15 мг, или от приблизительно 15 до приблизительно 18 мг. В некоторых вариантах осуществления, количество ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) в наборе находится в диапазоне от приблизительно 0,1 мг до приблизительно 10 мг, например, от приблизительно 1 мг до приблизительно 5 мг или от приблизительно 5 мг до приблизительно 10 мг.
[0221] Инструкции, входящие в наборы по изобретению, обычно представляют собой письменные инструкции на этикетке или на вкладыше в упаковке (например, на листе бумаги, входящим в набор), но также допустимы инструкции, которые могут быть прочитаны с помощью компьютера (например, инструкции, хранящиеся на магнитном или оптическом диске). Инструкции по применению композиций наночастиц обычно включают информацию о дозе, режиме дозирования и способе введения для предполагаемого лечения. Набор может дополнительно содержать описание выбора подходящего индивидуума или лечения.
[0222] В настоящем изобретении также предлагаются наборы, включающие описанные в изобретении композиции (или лекарственные формы с разовой дозой и/или готовые препараты), которые могут дополнительно включать инструкцию (инструкции) по способам применения композиции, например, по применениям, дополнительно описанным в изобретении. В некоторых вариантах осуществления, набор по изобретению включает описанную выше упаковку. В других вариантах осуществления, набор по изобретению включает описанную выше упаковку и вторую упаковку, содержащую буфер. Набор может дополнительно включать другие материалы, необходимые с коммерческой и пользовательской точек зрения, в том числе другие буферы, разбавители, фильтры, иглы, шприцы и вкладыши с инструкциями по осуществлению описанных в изобретении способов.
[0223] Для проведения комбинированных терапий по изобретению, набор может содержать инструкции по одновременному и/или последовательному введению первого и второго терапевтического средства для эффективного лечения легочной гипертензии. Первое и второе терапевтические средства могут присутствовать в раздельных контейнерах или в одном единственном контейнере. Следует иметь в виду, что набор может включать всего одну композицию или две или более композиций, где одна композиция содержит первое терапевтическое средство, а другая композиция содержит второе терапевтическое средство.
[0224] Могут быть также предложены наборы, которые содержат дозы раскрытого в изобретении ингибитора mTOR (например, рапамицина или его производного, например, рапамицина), достаточные для проведения эффективного лечения индивидуум в течение длительного периода времени, например, в течение недели, 2 недель, 3 недель, 4 недель, 6 недель, 8 недель, 3 месяцев, 4 месяцев, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев или более more. Наборы могут также включать множество разовых доз описанных в изобретении композиций, фармацевтических композиций и составов ингибитора mTOR (например, рапамицина или его производного, например, рапамицина) и инструкции по применению и по фасовке в количествах, достаточных для хранения и применения в аптечных учреждениях, например, в больничных аптеках и в составляющих препараты аптеках. В некоторых вариантах осуществления, набор включает сухую (например, лиофилизированную) композицию, которая может быть восстановлена, ресуспендирована или регидратирована с образованием, как правило, стабильной водной суспензии наночастиц, содержащих ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и альбумин (например, сывороточный альбумин, например, человеческий сывороточный альбумин). В некоторых вариантах осуществления, набор включает сухую (например, лиофилизированную) композицию, которая может быть восстановлена, ресуспендирована или регидратирована с образованием, как правило, стабильной водной суспензии наночастиц, содержащих ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) и альбумин.
[0225] Наборы по изобретению находятся в подходящей упаковке. Подходящая упаковка включает, но этим не ограничивая, флаконы, бутылочки, сосуды, гибкие упаковки (например, герметические полиэтилентерефталатные или полиэтиленовые пакеты), и другие подобные упаковки. Наборы могут содержать дополнительные компоненты, такие как буферы, и пояснительную информацию.
[0226] Наборы по изобретению включают один или более контейнеров, содержащих композицию наночастиц ингибитора mTOR (такую как композиция наночастиц рапамицин/альбумин) (или лекарственную форму с разовой дозой и/или готовый препарат), применяемую для подкожного введения. В некоторых вариантах осуществления, набор дополнительно включает инструкции по применению в соответствии с любым из описанных в изобретении способов. Набор может дополнительно включать описание выбора индивидуумов, подходящих для лечения. Инструкции, вложенные в наборы по изобретению, обычно представляют собой письменные инструкции на этикетке или на вкладыше в упаковке (например, на листе бумаги, входящим в набор), но также допустимы инструкции, которые могут быть прочитаны с помощью компьютера (например, инструкции, хранящиеся на магнитном или оптическом диске).
Методы приготовления композиций
[0227] Методы приготовления композиций, содержащих белковые носители и плохо растворимые в воде лекарственные средства, являются хорошо известными. Например, наночастицы, содержащие плохо растворимые в воде лекарственные средства и белковые носители (например, альбумин), могут быть приготовлены в условиях больших сдвиговых усилий (например, при ультразвуковом воздействии, путем гомогенизации под высоким давлением или другими подобными методами). Эти методы раскрыты, например, в патентных документах U.S. Pat. Nos. 5916596, 6506405 и 6537579, а также в патентном документе U.S. Pat. Pub. No. 2005/0004002A1, полное содержание которых включено в настоящее изобретение путем ссылок на них.
[0228] Вкратце, ингибитор mTOR (например, рапамицин или его производное, например, рапамицин) растворяют в органическом растворителе. Подходящие органические растворители включает, например, кетоны, сложные эфиры, простые эфиры, хлорированные растворители и другие хорошо известные растворители. Например, органический растворитель может представлять собой метиленхлорид, смесь хлороформ/этанол или хлороформ/третбутанол (например, при соотношении приблизительно 1:9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1 или 9:1, или при соотношении приблизительно 3:7, 5:7, 4:6, 5:5, 6:5, 8:5, 9:5, 9,5:5, 5:3, 7:3, 6:4 или 9,5:0,5). Раствор добавляют к белковому носителю (например, к человеческому сывороточному альбумину). Смесь подвергают гомогенизации под высоким давлением (например, используя гомогенизатор Avestin, APV Gaulin, Microfluidizer™, такой как Microfluidizer™ Processor M-110EH from Microfluidics, Stansted или Ultra Turrax). Эмульсия может быть подвергнута циклическому пропусканию через гомогенизатор высокого давления в течение от приблизительно 2 до приблизительно 100 циклов, например, от приблизительно 5 до приблизительно 50 циклов, или от приблизительно 8 до приблизительно 20 циклов (например, в течение приблизительно 8, 10, 12, 14, 16, 18 или 20 циклов). Органический растворитель затем может быть удален путем испарения с использованием соответствующего известного оборудования, включающего, но этим не ограничивая, роторные испарители, испарители с падающей пленкой, пленочные испарители, распылительные сушилки, и другое подобное оборудование, которое может эксплуатироваться в периодическом или непрерывном режиме. Растворитель может быть удален при пониженном давлении (например, при приблизительно 25 мм рт.ст., 30 мм рт.ст., 40 мм рт.ст., 50 мм рт.ст., 100 мм рт.ст., 200 мм рт.ст. или 300 мм рт.ст.). Количество времени, затрачиваемое на удаление растворителя при пониженном давлении, может корректироваться, исходя из объема композиции. Например, для композиции, получаемой в объеме 300 мл, растворитель может быть удален при давлении от приблизительно 1 до приблизительно 300 мм рт.ст. (например, при приблизительно 5-100 мм рт.ст., 10-50 мм рт.ст., 20-40 мм рт.ст. или 25 мм рт.ст.) в течение от приблизительно 5 до приблизительно 60 минут (например, в течение приблизительно 7, 8, 9, 10, 11, 12, 13, 14, 15 16, 18, 20, 25 или 30 минут).
[0229] При необходимости корректировки отношения человеческого сывороточного альбумина к рапамицину или для корректировки концентрации рапамицина в дисперсии, к дисперсии быть добавлен раствор человеческого альбумина. Например, для корректировки отношения человеческого сывороточного альбумина к рапамицину до приблизительно 18:1, 15,:1 14:1, 13:1, 12:1, 11:1, 10:1, 9:1, 8:1, 7,5:1, 7:1, 6:1, 5:1, 4:1 или 3:1 может быть добавлен раствор человеческого сывороточного альбумина (например, 25% масса/объем). Например, для корректировки отношения человеческого сывороточного альбумина к ингибитору mTOR (например, рапамицину) до приблизительно 18:1, 15,:1 14:1, 13:1, 12:1, 11:1, 10:1, 9:1, 8:1, 7,5:1, 7:1, 6:1, 5:1, 4:1 или 3:1 может быть добавлен раствор человеческого сывороточного альбумина (например, 25% масса/объем). Например, для корректировки концентрации рапамицина в дисперсии до приблизительно 0,5 мг/мл, 1,3 мг/мл, 1,5 мг/мл, 2 мг/мл, 3 мг/мл, 4 мг/мл, 5 мг/мл, 6 мг/мл, 7 мг/мл, 8 мг/мл, 9 мг/мл, 10 мг/мл, 15 мг/мл, 20 мг/мл, 25 мг/мл, 30 мг/мл, 40 мг/мл или 50 мг/мл добавляют раствор человеческого сывороточного альбумина (например, 25% масса/объем) или другой раствор. Дисперсия может быть подвергнута последовательному фильтрованию через многосекционные фильтры, например, комбинацию фильтров с размером пор 1,2 мкм и 0,8/0,2 мкм; комбинацию фильтров с размером пор 1,2 мкм, 0,8 мкм, 0,45 мкм и 0,22 мкм; или комбинацию любых других известных фильтров. Полученная дисперсия может быть затем лиофилизирована. Композиции наночастиц могут быть получены с использованием периодического процесса или непрерывного процесса (например, при получении композиции в крупных масштабах).
[0230] Если не указано иное, то значения всех используемых в изобретении технических и научных терминов являются общепринятыми для любого специалиста в той области, к которой относится это изобретение. Для любого специалиста в данной области является очевидным, что любые методы и материалы, аналогичные или эквивалентные методам и материалам, описанным в изобретении, могут быть использованы для применения на практике или для испытания изобретения.
[0231] Следующие далее примеры приведены только с целью иллюстрации, и они не ограничивают настоящее изобретение.
ПРИМЕРЫ
Пример 1. Клиническое применение Nab-рапамицина для лечения тяжелой формы легочной артериальной гипертензии
[0232] Это исследование представляло собой проспективное многоцентровое открытое несравнительное исследование фазы 1 по подбору дозы для определения максимально переносимой дозы (MTD), ограничивающей дозу токсичности (DLT), безопасности и предварительной эффективности 16-недельного курса лечения с помощью ABI-009 (nab-рапамицина) пациентов с тяжелой формой легочной артериальной гипертензии (PAH), относящихся к функциональному классу III по классификации ВОЗ, независимо от наилучшей доступной фоновой терапии.
Лечение и результаты
1. Часть A.
[0233] ABI-009 вводили внутривенно (IV) один раз в неделю четырем субъектам в течение до 16 недель. Использовали два уровня доз ABI-009 (5 мг/м2 и 10 мг/м2).
[0234] Все четыре субъекта имели до начала лечения легочную артериальную гипертензию функционального класса III в соответствии с классификацией ВОЗ, принятой на совещании по классификации в городе Дана Пойнт в штате Калифорния США в 2008 году, и отрицательные результаты при проведении, по меньшей мере, двух предшествующих терапий для легочной артериальной гипертензии. Конкретные дозы ABI-009 для каждого субъекта приведены на фигуре 1B. Для всех четырех субъектов начальные дозы ABI-009 составляли 10 мг/м2, при этом трем субъектам дозы были снижены во время лечения из-за побочных эффектов. В частности, субъекту № 1 вводили 10 мг/м2 ABI-009 еженедельно в течение 16 недель. Субъекту № 2 вводили 10 мг/м2 ABI-009 на 1, 2 и 4 неделях и 5 мг/м2 ABI-009 на 5, 7-9 и 11-16 неделях. Субъекту № 2 не вводил дозу ABI-009 на 3, 6 и 10 неделях. Субъекту № 3 вводили 10 мг/м2 ABI-009 на 1-6 неделях и 5 мг/м2 ABI-009 на 7-16 неделях. Субъекту № 4 вводили 10 мг/м2 ABI-009 на 1 и 2 неделях и 5 мг/м2 ABI-009 на 5 и 6 неделях. Дозу ABI-009 не вводили на 3, 4, 7 и 8 неделях, и лечение закончили на 9 неделе. Минимальная концентрация рапамицина в цельной крови для каждой недели приведена на фигуре 1А.
[0235] Среди четырех субъектов, которым вводили 10 мг/м2 ABI-009, у двоих из них развилась тромбоцитопения 1 степени, что привело к временному прекращению введения ABI-009 одному субъекту. Сыпь 2 степени появилась у двух субъектов. В результате, для одного субъекта уменьшили дозу ABI-009, а для одного субъекта введение ABI-009 было прервано. Другие зарегистрированные нежелательные явления включают парестезию 1 степени, гипертриглицеридемию или гиперхолестеринемию 1 и 2 степени, диарею 1 степени, целлюлит 3 степени/инфекцию, требующую внутривенного введения антибиотиков.
[0236] Как показано в таблице 1, у субъекта № 3 неожиданно улучшились результаты теста на преодоление пешком дистанции за 6 минут (6MWD) (в метрах). Основное улучшение наблюдалось только после четырех недель лечения. Результаты теста 6MWD увеличивались от 290 м до 397,5 м. Через 16 недель лечения, результаты теста 6MWD повышались до 425 м. Функциональный класс по классификации ВОЗ для обоих субъекта #2 и субъекта #3 снижался от класса III до класса II после 8 недель лечения или 12 недель лечения.
[0237] Уровни легочного артериального давления (PVR), сердечного выброса (CO), и сердечного притока (CI) в конце лечения с помощью ABI-009 сравнивали с уровнями на момент времени неделя 0. У всех трех субъектов, которые закончили лечение с помощью ABI-009 на протяжении шестнадцати недель, величина PVR значимо снижалась. Неожиданно, у всех трех субъектов также обнаруживалось существенное увеличение величины сердечного выброса (CO). Смотрите фигуру 2.
Таблица 1.
NT proBNP (пг/мл)
(диапазон нормальных значений < 300 пг/мл)
SCR: при скрининге; WK: неделя; EOT: конец лечения.
1) Субъект #2 повредил лодыжку в автомобильной катастрофе после визита с целью проведения скрининга, поэтому, отсутствуют данные для теста 6MWD в течение периода лечения.
2. Часть B.
[0238] В модифицированной части исследования по подбору дозы, испытывали 3 уровня дозы ABI-009 в группах по 3 пациента в каждой (1 мг/м2, 2,5 мг/м2 и 5 мг/м2), используя дизайн исследования 3+3 увеличение+уменьшение дозы.
3. Часть C.
[0239] Установленным критериям соответствовали пациенты с легочной артериальной гипертензией функционального класса III по классификации ВОЗ, независимо от ранее проведенных ≥ 2 специфических терапий для легочной артериальной гипертензии. ABI-009 вводили внутривенно еженедельно в течение 16 недель в дозах 1 мг/м2, 2,5 мг/м2, 5 мг/м2 и 10 мг/м2 с использованием дизайна исследования для подбора дозы 3+3. Первичные критерии оценки включают ограничивающую дозу токсичность и побочные эффекты. Вторичные критерии оценки включают изменения функционального класса по классификации ВОЗ, результатов теста 6MWD и гемодинамики.
[0240] Шести пациентам вводили ABI-009, и отбор пациентов для исследования продолжается. Пять пациентов завершили 16-недельный курс терапии. Четырем пациентам вводили ABI-009 в исходной начальной дозе 10 мг/м2, по поводу одного пациента не возникало опасений, связанных с безопасностью, в случае двух пациентов потребовалось снижения дозы до 5 мг/м2 из-за появления сыпи (5-я неделя) или парестезии (7-я неделя), и в случае 1 пациента пришлось прекратить лечение на 8 неделе из-за целлюлита. Впоследствии схема увеличения дозы была изменена, и исследование начинали с более низкой дозы 1 мг/м2. На данный момент, 2 пациента завершили прием ABI-009 в дозе 1 мг/м2 в течение 16 недель без возникновения существенных проблем с безопасностью.
[0241] Функциональные и гемодинамические параметры приведены в обобщенном виде на фигуре 3 для 5 пациентов, которые закончили лечение с помощью ABI-009 в течение 16 недель. У каждого из 5 пациентов было обнаружено улучшение некоторых из параметров даже при самой низкой дозе.
4. Часть D.
[0242] По состоянию на 22 февраля 2019 года, 9 пациентов прошли курс лечения путем внутривенного введения ABI-009. Четырем пациентам вводили ABI-009 в дозе 5-10 мг/м2, трем пациентам - 1 мг/м2 и двум пациентам - 2,5 мг/м2. Из девяти пациентов пять завершили 16-недельный курс лечения с помощью ABI-009, у одного пациента (получавшего ABI-009 в дозе 10 мг/м2) лечение было прервано досрочно на 8 неделе. Три пациента (включая одного пациента, получающего ABI-009 в дозе 1 мг/м2, и 2 пациентов, получающих ABI-009 в дозе 2,5 мг/м2) в настоящее время проходят активное лечение и не завершили 16-недельной терапии. Смотрите фигуру 4, на которой представлен дизайн исследования.
[0243] Первичные критерии оценки включают a) MTD, DLT и профиль безопасности 16-недельного внутривенного введения ABI-0009 и b) профиль безопасности после 48-недельного лечения. Вторичные критерии оценки включают a) изменение гемодинамики от начального момента до конца лечения ("EOT") (начальное значение и значение через 17 недель): сопротивления легочных сосудов (PVR) (например, путем катетеризация правых отделов сердца (RHC)), давления в легочной артерии (PAP), давления заклинивания в легочных капиллярах (PCWP), центрального венозного давления (CVP) и давления в правом предсердии; b) изменения проводимых каждые 4 недели оценок (начальное значение и значение на неделе 5, 9, 13 и 17): результатов исследования с помощью доплеровской эхокардиографии структуры/функции правого желудочка, результатов теста на преодоление пешком дистанции за 6 минут (6MWD), функционального класса по классификации ВОЗ, результатов испытания функции легких; и c) изменения результатов теста 6MWD, функционального класса по классификации ВОЗ и результатов испытания функции легких каждые восемь недель фазы продолжения клинического исследования (то есть, на в недели E9, E17, E23 и E23). Поисковые критерии оценки включают: a) фармакокинетику и остаточные уровни рапамицина в течение еженедельного лечения у пациентов с легочной артериальной гипертензией; b) изменения биомаркеров легочной артериальной гипертензии: N-терминального натрийуретического пептида головного мозга (NTproBNP), C-реактивного белка, тропонина; c) изменения качества жизни (оценки в баллах при проведении опроса emPHasis-10); и d) необязательных биомаркеров для mTOR в крови, оценки, коррелятивной с биомаркерами легочной артериальной гипертензии, клинической эффективности/безопасности.
[0244] Параметры безопасности оценивали среди девяти пациентов, подвергавшихся лечению. Среди четырех пациентов, получавших ABI-009 в дозе 10 мг/м2 (в первой начальной дозе), у одного пациента не было связанных с безопасностью проблем; двум пациентам снижали дозу до 5 мг/м2 из-за возникновения высыпаний (неделя 5) или парестезии (неделя 7) и завершали лечение при дозе 5 мг/м2 без возникновения последующих проблем безопасности; оставшемуся одному пациенту прекращали лечение на недели 8 из-за возникновения целлюлита.
[0245] Впоследствии, схему дозирования изменяли, увеличивая дозирование от 1 мг/м2 до 2,5 мг/м2 и 5 мг/м2, при условии, что на каждом этапе не возникало проблем с безопасностью. Двое пациентов завершили 16-недельный лечение с помощью ABI-009 при дозе 1 мг/м2 без возникновения значительных проблем с безопасностью. Один пациент, получавший такую же дозу (то есть, 1 мг/м2), продолжает лечение на 15 неделе, и никаких проблем с безопасностью отмечено не было. Группа с дозой 2,5 мг/м2 в настоящее время содержит 2 пациентов, подвергнутых к этому моменту лечению.
[0246] Наиболее частыми нежелательными явлениями (все степени 1 и 2) на сегодняшний день были диарея (4 пациента), тромбоцитопения, сыпь и утомляемость (по 2 пациента для каждого из них). Они все возникали при уровне дозы 10 мг/м2, и эти проблемы решали путем изменений доз и стандартов лечения.
[0247] Параметры эффективности лечения оценивали среди пяти пациентов, прошедших курс терапии в течение шестнадцати недель. Как показано на фигуре 5, у трех из пяти пациентов улучшился функциональный класс по классификации ВОЗ от функционального класса III до функционального класса II. У трех из пяти пациентов результат теста 6MWD увеличился на 16-47%. Среди них, двое пациентов улучшили результат теста 6MWD более чем на 130 метров. У четырех из пяти пациентов наблюдалось снижение легочного сосудистого сопротивления (PVR). Средняя величина PVR снизилась на 19% после шестнадцати недель лечения с 616 дин·сек/см5 до 498 дин·сек/см5. У двух пациентов после лечения наблюдалось снижение PVR более чем на 30%. У трех пациентов при уровне дозы 10 мг/м2 наблюдалось увеличение сердечного выброса на 38-62% наряду с улучшением сердечного индекса. При проведении исследования функции легких также измеряли форсированную жизненную емкость (FVC). Средняя величина FVC увеличилась на 10% после 16 недель лечения. Среднее значение NT-proBNP снижалось на 53% с 1041 пг/мл до 492 пг/мл после 16 недель лечения. У четырех из пяти пациентов наблюдалось снижение уровня NT-proBNP, что свидетельствует об улучшении функции левого желудочка. Следует отметить, что один пациент, которому вводили дозу 10 мг/м2, во время проведения курса терапии попал в автокатастрофу, в результате которой у него произошел перелом стопы. В случае этого конкретного пациента, на фоне улучшения большинства параметров результат теста 6MWD не мог быть улучшен.
[0248] Изменения качества жизни оценивали путем проведения опроса EmPHasis10. Сумма баллов для пяти пациентов улучшалась от 146 на момент начала проведения лечения до 99 к неделе 17. Медиана для одного пациента (амплитуда) улучшалась 30%.
[0249] В совокупности, у всех пациентов после окончания проведения в течение 16 недель терапии с использованием ABI-009 в комбинации со стандартной терапией легочной артериальной гипертензии обнаруживалось некоторое улучшение функциональной емкости легких и/или гемодинамики.
[0250] Исследование выбора оптимального режима дозирования все еще продолжается, однако, промежуточные результаты по безопасности и эффективности, в том числе функциональные и гемодинамические измерения, обосновывают продолжение исследования применения ABI-009 у пациентов с тяжелой формой легочной артериальной гипертензии.
[0251] В процессе исследования, оценивали остаточные уровни сиролимуса (в цельной крови) у пациентов, подвергавшихся лечению различными дозами ABI-009. Результаты представлены в таблице 2.
[0252] Таблица 2. Данные клинических исследований по остаточному уровню сиролимуса (в цельной крови)
Исследуемая популяция
[0253] Критерии включения в исследование содержат следующие признаки. 1. Мужчина или женщина в возрасте старше 18 с текущим диагнозом легочной артериальной гипертензии (PAH) группы 1 по классификации ВОЗ, включающей идиопатическую легочную артериальную гипертензии (IPAH), наследственную легочную артериальную гипертензии (HPAH), индуцированную лекарственным препаратом или токсином легочную артериальную гипертензии или ассоциированную с заболеванием соединительной ткани легочную артериальную гипертензии, или врожденных пороков сердца (восстановленных более чем за 1 год до проведения скрининга). 2. Должны соответствовать следующим гемодинамическим определениям перед началом исследования препарата a. средняя величина давления в легочной артерии (PAP) ≥25 мм рт.ст.; b. давление заклинивания в легочных капиллярах (PCWP) или конечное диастолическое давление в левом желудочке (LVEDP) ≤15 мм; c. величина сопротивления легочных сосудов (PVR) >5 мм рт.ст./л/мин (единиц Вуда). 3. Функциональный класс III в соответствии с классификацией ВОЗ, принятой на совещании по классификации в городе Дана Пойнт в штате Калифорния США в 2008 году. 4. Проведение 2 или более специфических стандартных терапий для легочной артериальной гипертензии (PAH) (в течение ≥12 последующих недель и при стабильной дозе в течение ≥8 последующих недель), за исключением тех случаев, когда документально подтверждена неспособность перенесения 2 стандартных терапий. 5. Соответствие следующим критериям, определяемым путем проведения тестов на функцию легких, завершенных при скрининге: a. объем воздуха при форсированном выдохе в одну секунду (FEV1) ≥55% от расчетной нормальной величины; b. отношение объем воздуха при форсированном выдохе в одну секунду (FEV1) : форсированная жизненная емкость (FVC) ≥0,60. 6. Результаты теста 6MWD ≥150 метров и ≤450 метров.
[0254] Пациент не соответствовал критериям для включения в это исследование, если к нему мог быть применен любой из следующих критериев. 1. В анамнезе присутствует заболевание сердца, включающее фракцию выброса левого желудочка (LVEF) ≤40% или клинически значимое сужение клапана или атеросклеротическое заболевание сердца (инфаркт миокарда, стенокардию, нарушение мозгового кровообращения). 2. В анамнезе присутствует злокачественная опухоль за 2 года до момента включения в исследование. 3. Легочная гипертензия (PH), относящаяся к группам 2-5 по классификации легочной гипертензии, принятой в г. Ницца, Франция, в 2013 году. 4. Текущее или недавнее (<3 месяцев) применение внутривенных инотропных или вазопрессорных средств для лечения легочной артериальной гипертензии (PAH). 5. Недавняя (<3 месяцев) госпитализация по поводу легочной артериальной гипертензии (PAH). 6. В анамнезе присутствуют аллергические реакции, связанные с соединениями аналогичного химического или биологического состава, включая макролиды (например, азитромицин, кларитромицин, диритромицин и эритромицин) и кетолидные антибиотики. 7. Неконтролируемый сахарный диабет, определяемый по HbA1c > 8%, несмотря на адекватную терапию. 8. Неконтролируемая гиперлипидемия (уровень триглицеридов в сыворотке ≥300 мг/дл). 9. Холестерин в сыворотке ≥350 мг/дл. 10. Хирургическое вмешательство в течение 3 месяцев до даты начала исследования препарата. 11. Фоновые цитопении: а. абсолютное количество нейтрофилов ≤1,5 x 109/л; b. гемоглобин ≤9 г/дл; c. количество тромбоцитов ≤100000/мм3. 12. Фоновое заболевание печени: ALT/AST, общий билирубин, щелочная фосфатаза ≥1,5 x верхняя граница нормы. 13. Клиренс креатинина (формула Кокрофта) ≤30 мл/мин. 14. Предшествующее применение ингибитора mTOR в течение предыдущих 6 месяцев до момента включения в исследование. 15. Предшествующая пересадка легкого. 16. Применение сильных ингибиторов и индукторов CYP3A4 в течение 14 дней до приема первой дозы ABI-009. Кроме того, применение любых известных субстратов CYP3A4 с узким терапевтическим окном (таких как фентанил, альфентанил, астемизол, цизаприд, дигидроэрготамин, пимозид, хинидин, терфанид) в течение 14 дней до приема первой дозы ABI-009.
Оценка ключевых показателей безопасности
[0255] Применяемая шкала оценок токсичности нежелательного явления представляла собой Общую терминологию критериев нежелательных явлений (NCI CTCAE Version 4.1). Серьезное нежелательное явление (SAE) определяли как нежелательное явление, которое соответствует, по меньшей мере, одному из следующих вызывающих опасения критериев: 1) несовместимое с жизнью; 2) опасное для жизни (ставит пациента перед лицом непосредственного риска смерти); 3) требует госпитализации пациента или продление существующей госпитализации; 4) приводит в результате к устойчивой или существенной нетрудоспособности/недееспособности; 5) врожденная аномалия/ врожденный порок развития; и 6) другое важное с медицинской точки зрения серьезное событие.
Оценка ключевых показателей эффективности
[0256] Следующие характеристики измеряли каждую неделю, каждые четыре недели на исходном уровне и на 5, 9, 13 и 17 недели, или на исходном уровне и на 17 неделе: 1) оценки методом доплеровской эхокардиографии структуры и функции правого желудочка; 2) результаты теста на преодоление пешком дистанции за 6 минут (6MWD); 3) исследование легочной функции; 4) NT Pro-BNP; 5) С-реактивный белок (CRP); 6) тропонин; 7) липиды натощак; 8) функциональный класс по классификации ВОЗ; 9) фармакокинетика рапамицин; 10) сопротивление легочных сосудов (PVR) путем катетеризации правых отделов сердца; 11) давление в легочной артерии (PAP); 12) давление окклюзии легочной артерии (PAOP); 13) давление заклинивания в легочных капиллярах (PCWP); 14) центральное венозное давление (CVP); 15) сердечный выброс; 16) сердечный приток.
Пример 2. Доклиническое исследование nab-рапамицина для лечения легочной артериальной гипертензии (PAH)
[0257] Проводили доклинические исследования для оценки биораспределения ABI-009.
1. Часть A.
[0258] Разовую дозу 1,7мг/кг (10 мг/м2) ABI-009 внутривенно вводили крысам (3 крысы/группа). Собирали кровь и органы через 2, 8, 24, 72 и 120 часов для измерения концентраций сиролимуса.
[0259] Суммарное воздействие на ткани (AUC) было значимо выше в легких по сравнению с другими тканями на протяжении 120 часов (P<0,0001, ANOVA). Концентрации сиролимуса в легких составляли 3358, 2436, 1190, 322 и 171 нг/г через 2, 8, 24, 72 и 120 часов, и отношения легкие/кровь составляли 57, 98, 125, 121 и 140, соответственно. Смотрите фигуру 21.
2. Часть B.
[0260] Проводили сравнение фармакокинетики в цельной крови и распределение в ткани через 24 часа после внутривенного введения nab-рапамицина (доза 1 мг/кг) крысам (N=5) с пероральным введением рапамицина (доза 1,6 мг/кг) крысам (N=5) (смотрите публикацию Napoli KL, Wang ME, Stepkowski SM, et al: Distribution of sirolimus in rat tissue. Clin Biochem 30:135-42, 1997) для определения относительного накопления в легких (орган-мишень для легочной артериальной гипертензии (PAH)) и печени (основной способ выведения рапамицина). Уровни в крови и в тканях измеряли методом жидкостной хроматографии с тандемной масс-спектрометрией (LC/MS/MS) или методом высокоэффективной жидкостной хроматографии (HPLC).
[0261] Как показано на фигуре 6, уровни в крови через 24 часа были сопоставимы. Уровни nab-R (наб-рапамицина) в легких были значимо выше, чем в печени (p <0,05), уровни nab-R в легких были значимо выше, чем предполагаемый уровень oral-R (перорального рапамицина) в легких (p <0,05), уровни nab-R в печени были значимо ниже, чем предполагаемый уровень oral-R в печени (p <0,05)(парный t-критерий Стьюдента, используемый для всех сравнений). Рассчитанные экстракционные индексы тканей (концентрация рапамицина в ткани/концентрация рапамицина в крови) для легких составляли 72 и 24, соответственно, для наб-рапамицина и перорального рапамицина, что указывает на то, что нацеливание наб-рапамицина на легкие в 3 раза выше (P <0,05, t-критерий Стьюдента). В отличие от этого, экстракционные индексы для печени составляли 27 и 43, соответственно, для наб-рапамицина и перорального рапамицина, и снижение в 1,6 раза экстракционного индекса в случае наб-рапамицина позволяет предположить, что он поглощается печенью с более низкой скоростью, которая обусловлена связанным с альбумином составом, и это поддерживает более длительное нахождение наб-рапамицина в кровотоке. Ожидается, что уровни перорального рапамицина в печени должны быть примерно в 2 раза выше, чем в легких, поскольку метаболизм в печени является основным путем выведения перорального рапамицина, и это подтверждает отсутствие конкретных механизмов повышения поглощения перорального рапамицина в легких. Уровни наб-рапамицина в легких в 2,6 раза выше, чем в печени, и это в значительной степени доказывает наличие специфических механизмов транспорта наб-рапамицина в легочную ткань, что приводит к увеличению поглощения наб-рапамицина в легких.
[0262] Эти результаты демонстрируют высокую степень проникновения nab-рапамицина в легочную ткань.
Пример 3. Исследование фармакокинетики после подкожного и внутривенного дозирования ABI-009 на крысах линии Sprague Dawley (SD)
[0263] Самкам крыс линии SD вводили разовую дозу nab-рапамицина (ABI-009) подкожно (то есть, "SC" или "subQ") или внутривенно (IV). Дизайн исследования представлен ниже в таблице 3. В местах подкожной инъекции в любой момент времени после введения не обнаруживалось никаких признаков воспаления или токсичности при сравнении с физиологическим раствором в качестве контроля (плацебо).
Таблица 3. Дизайн исследования разовой дозы ABI-009 на крысах
[0264] После подкожной или внутривенной инъекции ABI-009, измеряли концентрации рапамицина в цельной крови в различные моменты времени. Результаты анализов собранных образцов цельной крови представлены на фигурах 7-9 и в таблицах 4 и 5 ниже.
Таблица 4. Концентрация рапамицина после введения ABI-009
(нг/мл)
(нг/мл)
(нг/мл)
Таблица 5. Концентрация рапамицина после введения ABI-009
(нг/мл)
(нг/мл)
[0265] Неожиданно, как это представлено на фигуре 10 и в таблице 6 ниже, подкожное введение повышало биологическую доступность по сравнению с внутривенным введением, на что указывала суммарная площадь под кривой (AUC). Подкожное введение только 0,56 мг/кг ABI-009 продуцировало аналогичное время воздействия при 1/3 от внутривенной дозы ABI-009 (1,7 мг/кг). Кроме того, подкожное введение снижало максимально достижимую концентрацию (Cmax) и замедляло время достижения максимальной концентрации (время достижения Cmax). Пиковые уровни рапамицина и AUC в крови повышались при более высоких дозах подкожного введения ABI-009.
Таблица 6. Фармакокинетика введения ABI-009 крысам
Пример 4. Биораспределение ABI-009 после введения крысам
[0266] Собирали ткани у крыс, описанных выше в примере 3, либо через 24 часа, либо через 168 часов (смотрите таблицу 3, в которой представлен дизайн исследования) после подкожного (subQ) или внутривенного (IV) введения ABI-009. Концентрация рапамицина в конкретных тканях крыс через 24 или 168 часов после введения указана на фигуре 11 (в костном мозге и головном мозге), на фигуре 12 (в сердце и печени) и на фигуре 13 (в легких и в поджелудочной железе).
[0267] Подкожное введение приводило к значительному распределению ABI-009 во все тестируемые органы, включающие костный мозг, головной мозг, сердце, печень, легкие и поджелудочную железу. Образец распределения по органам был аналогичным при подкожном и внутривенном введении, но подкожное введение при дозе 0,56 мг/кг позволяло достигать аналогичных концентраций в ткани, которые достигались в случае внутривенного введения при дозе 1,7 мг/кг. Наблюдалось значимое падение концентрации рапамицина в период между 24 и 168 часами после введения в хорошо перфузируемых органах, включающих сердце, печень, легкие и поджелудочную железу. Однако, концентрация в головном мозге была относительно стабильной в период между 24 и 168 часами после введения.
Пример 5. Исследование токсикологии после повторяющегося подкожного дозирования ABI-009 крысам линии SD
[0268] Целью исследования являлась общая оценка безопасности и локальной токсичности в местах инъекций после повторяющихся подкожных инъекций ABI-009 крысам линии SD. Для определения токсичности проводили наблюдения за проявлением признаков болезненного расстройства. Образцы кожи из мест инъекции анализировали на наличие признаков воспаления и некроза с использованием методов гистопатологии.
[0269] В исследовании использовали пятнадцать самок крыс линии Sprague Dawley (SD) с массой 160-180 грамм. Для получения исходного раствора (10 мг/мл), ABI-009 растворяли в физиологическом растворе, затем дополнительно разбавляли в растворе человеческого сывороточного альбумина (HSA) в 0,9% физиологическом растворе с получением раствора для подкожной инъекции (объем: 1,0 мл/кг).
A. Дизайн исследования
[0270] Крыс разделяли на 5 групп по 3 животных в каждой. Крыс взвешивали и вводили подкожно дозу, указанную в таблице 7, каждые 4 дня в течение 4 недель (7 инъекций).
Таблица 7. Группы, подвергавшиеся лечению
мг/кг
SC=подкожная инъекция
[0271] Ежедневно проводили осмотр животных на наличие клинических признаков общей токсичности и осматривали места инъекций на коже на возникновения реакций на подкожную инъекцию.
[0272] Перед каждой инъекцией у животных, получавших ABI-009 (группы 3, 4 и 5), собирали образцы цельной крови и анализировали их на остаточные уровни сиролимуса.
[0273] Через 4 недели всех животных умерщвляли, и образцы кожи из мест инъекции исследовали гистопатологическим методом на наличие признаков местной токсичности.
B. Методики эксперимента
1. Приготовление дозирующего раствора
[0274] Растворы плацебо для контроля состоят из 0,9% физиологического раствора и HSA в 0,9% физиологическом растворе. Конечная концентрация раствора составляет 90 мг/мл, считая на отношение альбумин:сиролимус 9:1 в испытуемом препарата ABI-009 (номер произведенной партии C345-001, номер партии Fisher 51394.2). Каждый флакон ABI-009 (C345-001) содержит 97,4 мг сиролимуса и 874 мг человеческого альбумина. Раствор HSA в физиологическом растворе разбавляют из 20% исходного раствора альбумина (200 мг/мл) фирмы Grifols.
[0275] Для дозирующих растворов ABI-009, сначала готовят исходный раствор ABI-009 с концентрацией 10 мг/мл, затем его разбавляют до требуемых концентраций для дозирующего раствора, используя HSA-физиологический раствор. Флакон со 100 мг ABI-009 растворяли в 10 мл 0,9% физиологического раствора с получением раствора с концентрацией 10 мг/мл.
[0276] Раствор ABI-009 с концентрацией 5 мг/мл получали путем разбавления 0,6 мл исходного раствора (10 мг/мл) с помощью 0,6 мл HSA-0,9% физиологический раствор с получением раствора 5,0 мг/мл для группы 4. Раствор ABI-009 с концентрацией 1,7 мг/мл готовили путем разбавления 0,3 мл раствора ABI-009 из группы 4 (5,0 мг/мл) с помощью 0,6 мл HSA-0,9% физиологический раствор с получением раствора 1,7 мг/мл для группы 3.
2. Дозирование
[0277] Крыс подвергали анестезии, взвешивали и вводили им растворы ABI-009, HSA раствор и физиологический раствор в соответствии с таблицей 8 путем подкожной (SC) инъекции каждые 4 дня в течение 4 недель (7 инъекций).
[0278] Таблица 8. Дозирующий объем
(мл/кг)
(90 мг HSA)
(90 мг HSA)
[0279] Ежедневно проводили осмотр крыс на наличие клинических признаков общей токсичности и осматривали места инъекций на коже на возникновения реакций на подкожную инъекцию. Для определения токсичности проводили наблюдения за проявлением признаков болезненного расстройства. Аномальными для поведения животного считали пилоэрекцию, потерю массы тела, сонливость, выделения, неврологические симптомы, клинические проявления, покраснение и воспаление места инъекции и любые другие признаки. Для всех крыс получали изображения места инъекции до и после подкожной инъекции.
3. Сбор и анализ образцов
[0280] В случае крыс, подвергавшихся лечению с помощью ABI-009 (группы 3, 4 и 5), крыс подвергали анестезии и отбирали образцы крови в предварительно охлажденные пробирки с K2EDTA перед каждым введение (за исключением 1-ой дозы). Цельную кровь собирали, хранили в маркированных пробирках Эппендорфа при -80°C и анализировали на остаточные уровни сиролимуса.
[0281] Всех животные умерщвляли в конечные моменты времени эвтаназии на 29-й день (после введения ABI-009 через 96 часов после недели 4 дня 25). В конечный момент времени эвтаназии, собирали образцы цельной крови для анализа остаточного уровня сиролимуса. Собирали мозг, легкие, печень, сердце, поджелудочную железу и костный мозг, промывали физиологическим раствором для удаления крови, делили на 2 порции и быстро замораживали в индивидуально маркированных пробирках, и хранили при -80°C. Замороженные образцы крови из групп, подвергавшихся лечению с помощью ABI-009 (группы 3, 4 и 5), отправляют на сухом льду в прибор фирмы BASi. Остаточные уровни сиролимуса в крови анализировали на приборе фирмы BASi методом жидкостной хроматографии с тандемной масс-спектрометрией.
[0282] В конечный момент времени эвтаназии, вырезали кожу и нижний слой дермы в области подкожного введения для гистологического анализа с окрашиванием гематоксилином и эозином на выявление признаков воспаления методом гистопатологии. Пятнадцать фиксированных формалином образцов кожи крыс подвергали гистопатологическим измерениям и обрабатывали в обычном порядке. Для приготовления по одному микроскопическому препарату из каждого блока, делали срезы и окрашивали их гематоксилином и эозином. Микроскопические препараты оценивал сертифицированный ветеринарный патолог методом световой микроскопии. Гистологические поражения оценивались по степени тяжести от 0 до 5 (0=отсутствие/нормальное состояние, 1=минимальная, 2=легкая, 3=умеренная, 4=выраженная, 5=тяжелая). Средние баллы разных групп анализировали с использованием t-критерия.
C. Результаты
4. Системная токсичность
[0283] Для определения токсичности, ежедневно проводили осмотр крыс на наличие признаков болезненного расстройства. Аномальными для поведения животного считали пилоэрекцию, потерю массы тела, сонливость, выделения, неврологические симптомы, клинические проявления, покраснение и воспаление места инъекции и любые другие признаки. Крысы чувствовали себя нормально после дозирования физиологического раствора, HSA и ABI-009 при существующем режиме дозирования (1,7-10 мг/кг, 7 доз), без обнаружения в процессе исследования признаков клинического стресса.
[0284] Не наблюдалось потери массы тела (< 20%), и во всех группах, подвергаемых лечению, у животных увеличивалась масса тела во время проведения исследования (таблица 9). Результаты показали, что крысы переносили подкожную инъекцию ABI-009 в диапазоне доз 1,7-10,0 мг/кг.
[0285] Таблица 9. Влияние лечения на массу тела крыс
1
5
9
SD - среднеквадратическое отклонение
5. Локальная токсичность
[0286] Гистопатологическим измерениям подвергали пятнадцать фиксированных формалином образцов кожи крыс из области подкожного введения. Гистопатологические обнаружения в образцах кожи включали некроз и смешанные инфильтраты воспалительных клеток в периваскулярных зонах, оба поражения наблюдались в подкожных тканях/подкожной клетчатке.
[0287] Некроз представлял собой очаговый некроз и характеризовался областью потери нормальных клеток, инфильтрацией нейтрофилов, кровотечением и экссудацией фибрина с различной прилегающей фиброплазией. Некроз наблюдался только в образцах от животных, которым вводили ABI-009 в дозах 5 мг/кг (группа 4, 1 животное с минимальным некрозом) и 10 мг/кг (группа 5, все 3 животных с легким или выраженным некрозом), тогда как введение физиологического раствора (группа 1), HSA (группа 2) и ABI-009 в концентрации 1,7 мг/кг (группа 3) не вызывало некроза (смотрите таблицу 10 и фигуру 14). Только введение ABI-009 при наивысшей дозе 10 мг/кг обнаруживало значительное увеличение бальной оценки некроза по сравнению с группой HSA (P=0,02, t-тест).
Таблица 10. Влияние лечения на проявление локальной токсичности
подкожный слой
SEM - стандартная ошибка среднего значения
Смешанная воспалительная клеточная инфильтрация в подкожных периваскулярных зонах характеризовалась инфильтрацией и агрегацией лимфоцитов, плазматических клеток, макрофагов, редко встречающихся многоядерных гигантских клеток и вариабельного количества нейтрофилов. Смешанную воспалительную клеточную инфильтрацию обнаруживали во всех группах лечения, при этом средние показатели в баллах были самыми высокими у животных, которым вводили HSA (группа 2) и ABI-009 в дозе 10 мг/кг (группа 5). В случае инъекции низкой дозы ABI-009 1,7 мг/кг (группа 3), средний показатель в баллах был аналогичен показателю в контрольной группе, в которой вводили физиологический раствор (группа 1). Смотрите таблицу 10 и фигуру 14. Высокая смешанная воспалительная клеточная инфильтрация, наблюдаемая в группе HSA (группа 2), по сравнению с контрольной группой, в которой вводили физиологический раствор (P=0,01, t-тест), позволяет предположить, что местное воспаление в значительной степени было вызвано инъекцией гетеропротеина человеческого сывороточного альбумина.
[0289] Типичные гистологические изображения для крыс в каждой группе приведены на фигурах 15-19.
[0290] В группах лечения с помощью ABI-009 наблюдалось дозозависимое увеличение локальной токсичности с увеличением дозы ABI-009. При самой низкой дозе ABI-009 1,7 мг/кг, гистология мест локальных инъекций была аналогична контрольной группе, в которой вводили физиологический раствор, тогда как некроз и инфильтрация воспалительных клеток подкожной ткани имели наиболее тяжелую форму у животных, которым вводили ABI-009 в дозе 10 мг/кг.
6. Остаточные уровни сиролимуса в крови
[0291] Образцы крови для анализа на остаточный сиролимус собирали перед каждой инъекцией (на 5, 9, 13, 17, 21, 25, 29 день) в группах, получавших ABI-009 (кроме перед введением 1-й дозы на 1 день), и анализировали на приборе фирмы BASi методом жидкостной хроматографии с тандемной масс-спектрометрией. Индивидуальные остаточные уровни показаны в таблице 11. Большинство значений остаточных уровней сиролимуса в крови через 4 дня после подкожной инъекции постоянно находились в диапазоне 2-20 нг/мл. Явно выделялись результаты для двух образцов в группе, в которой вводили ABI-009 10 мг/кг (группа 5). Причина отклонения этих результатов наблюдения не может быть установлена. Однако аномально высокие остаточные уровни наблюдались только в группе с наивысшей дозой ABI-009, в которой также обнаруживался некроз подкожной ткани, от легкого до выраженного, что свидетельствует о том, что поражения кожи могут препятствовать нормальному всасыванию ABI-009 и приводить к более длительному удержанию лекарственного средства.
Таблица 11. Остаточные уровни сиролимуса в крови
идентификационный номер
SEM - стандартная ошибка среднего значения
[0292] Для каждой группы лечения с помощью ABI-009, не обнаруживалось значимого накопления лекарственного средства на протяжении всего времени проведения исследования, так как остаточные уровни сиролимуса в крови оставались, как правило, стабильными. Наблюдалось зависимое от дозы повышение средних остаточных уровней сиролимуса при повышении дозы ABI-009. По сравнению с группой, в которой вводили ABI-009 в дозе 1,7 мг/кг, наблюдались более высокие остаточные уровни сиролимуса в группе, в которой вводили ABI-009 в дозе 5 мг/кг (P=0,06) и в группе с дозированием 10 мг/кг (P=0,01) (фигура 20).
[0293] Таким образом, крысы находились в нормальном состоянии после введения ABI-009 при применяемом режиме дозирования (1,7-10 мг/кг, 7 доз), без потери массы тела во время проведения исследования. Результаты гистопатологии продемонстрировали дозозависимые признаки локальной токсичности, от слабого до выраженного некроза при максимальной дозе ABI-009 (10 мг/кг). Смешанная воспалительная клеточная инфильтрация может, по-видимому, быть вызвана гетеропротеином человеческого сывороточного альбумина (HSA). Введение ABI-009 в дозе 1,7 мг/кг (концентрация раствора 1,7 мг/мл) характеризовалось локальными ответными реакциями реакции на инъекции, которые были аналогичными ответным реакциям при введении физиологического раствора в качестве контроля. После повторных подкожных инъекций не наблюдалось значительного накопления препарата. Остаточные уровни сиролимуса в крови повышались с увеличением дозы ABI-009.
[0294] Результаты исследования показали, что крысы системно переносят многократные дозы ABI-009 в диапазоне 1,7-10,0 мг/кг при подкожных инъекциях. Раствор ABI-009 в концентрации 1,7 мг/мл хорошо переносился местно. При этом уровне дозирования не наблюдалось неблагоприятных эффектов.
| название | год | авторы | номер документа |
|---|---|---|---|
| НАНОЧАСТИЦА, СОДЕРЖАЩАЯ РАПАМИЦИН И АЛЬБУМИН, В КАЧЕСТВЕ ПРОТИВОРАКОВОГО АГЕНТА | 2008 |
|
RU2483714C2 |
| НАНОЧАСТИЦА, СОДЕРЖАЩАЯ РАПАМИЦИН И АЛЬБУМИН, В КАЧЕСТВЕ ПРОТИВОРАКОВОГО АГЕНТА | 2013 |
|
RU2678448C2 |
| КОМБИНАЦИЯ И СПОСОБЫ ВВЕДЕНИЯ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ И КОМБИНИРОВАННОЙ ТЕРАПИИ | 2006 |
|
RU2452482C2 |
| КОМБИНАЦИИ И СПОСОБЫ ВВЕДЕНИЯ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ И КОМБИНИРОВАННОЙ ТЕРАПИИ | 2012 |
|
RU2632103C2 |
| КОМБИНАЦИИ И СПОСОБЫ ВВЕДЕНИЯ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ И КОМБИНИРОВАННАЯ ТЕРАПИЯ | 2013 |
|
RU2673805C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ КОМПОЗИЦИЯМИ НАНОЧАСТИЦ ТАКСАНА И ИНГИБИТОРАМИ ХЭДЖХОГ | 2010 |
|
RU2561055C2 |
| БИОМАРКЕРЫ | 2005 |
|
RU2429297C2 |
| БИОМАРКЕР | 2005 |
|
RU2385944C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА МОЧЕВОГО ПУЗЫРЯ | 2011 |
|
RU2621640C2 |
| ИНГАЛЯЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА РАПАМИЦИНА ДЛЯ ЛЕЧЕНИЯ ЛЕГОЧНОЙ ГИПЕРТЕНЗИИ | 2015 |
|
RU2732908C2 |
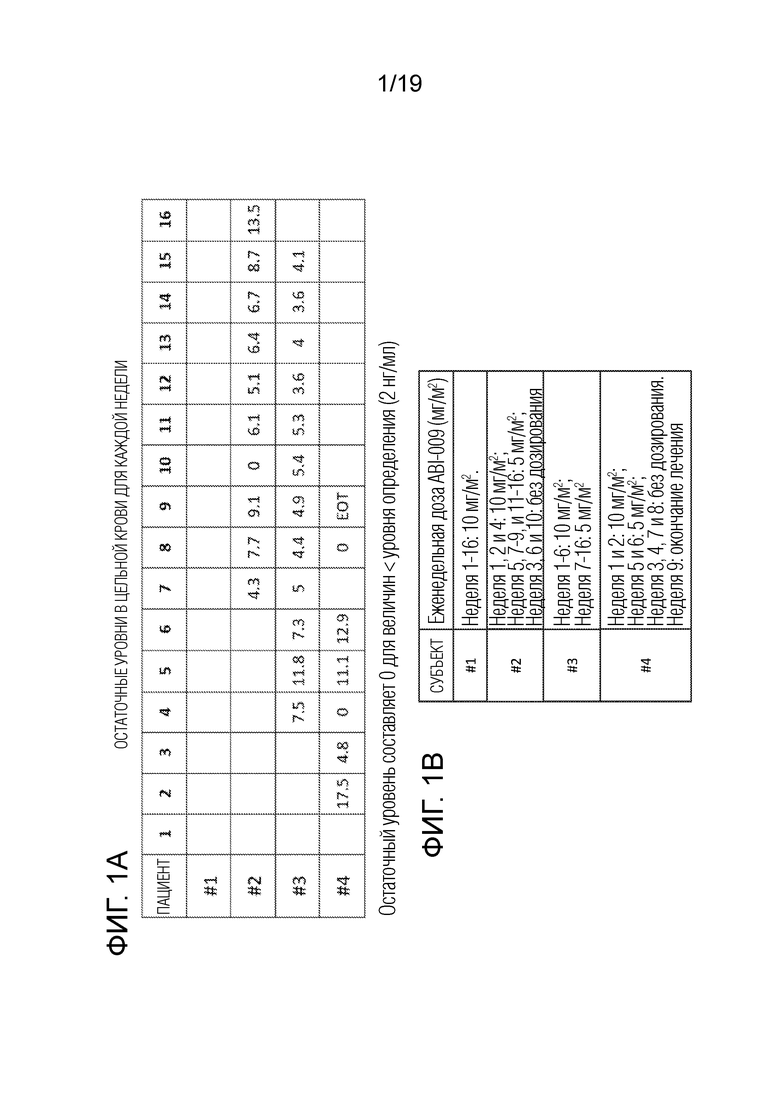
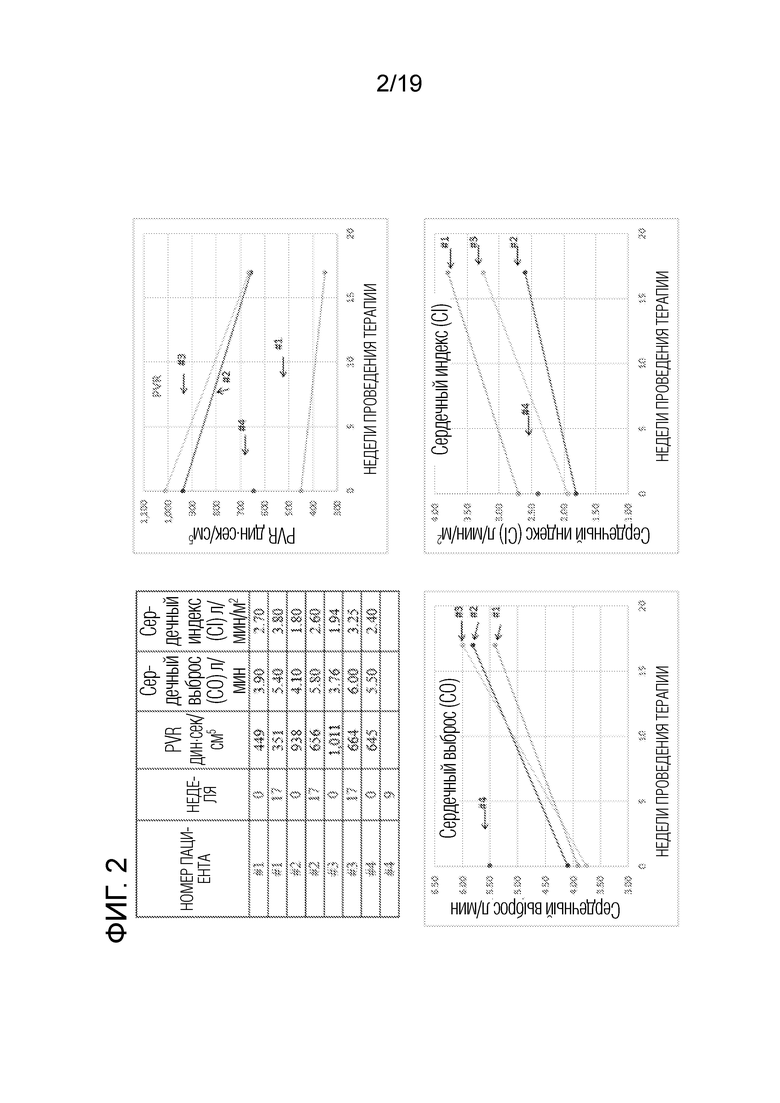
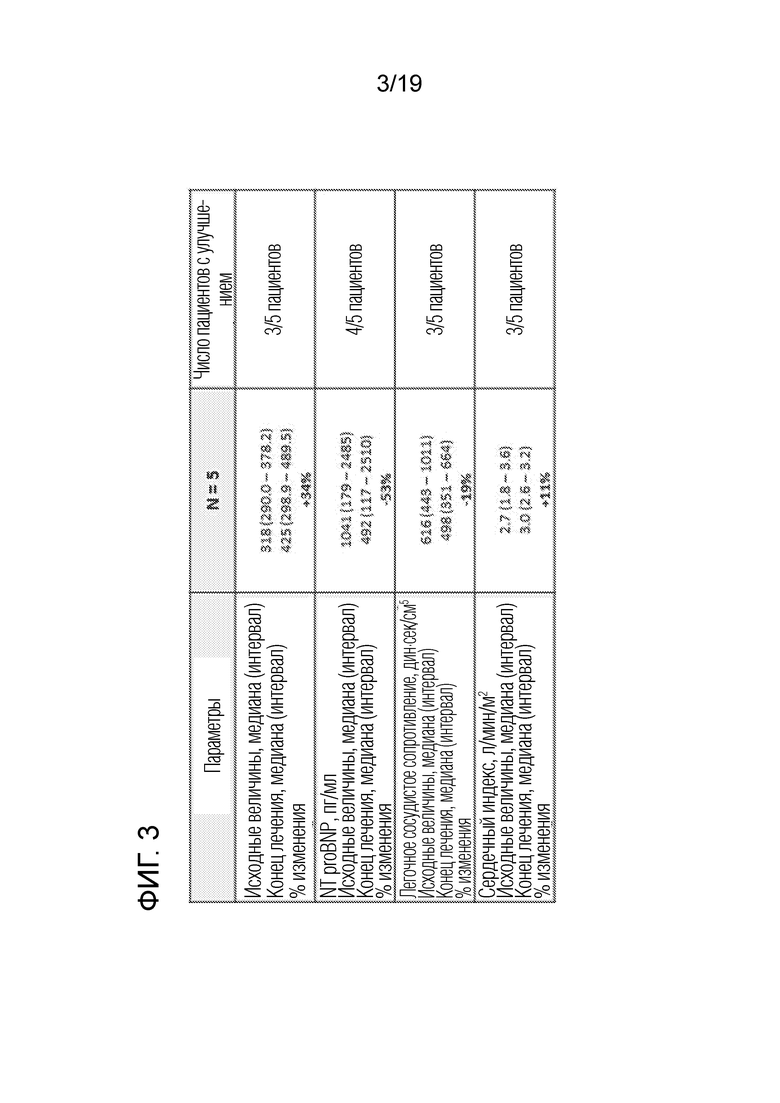
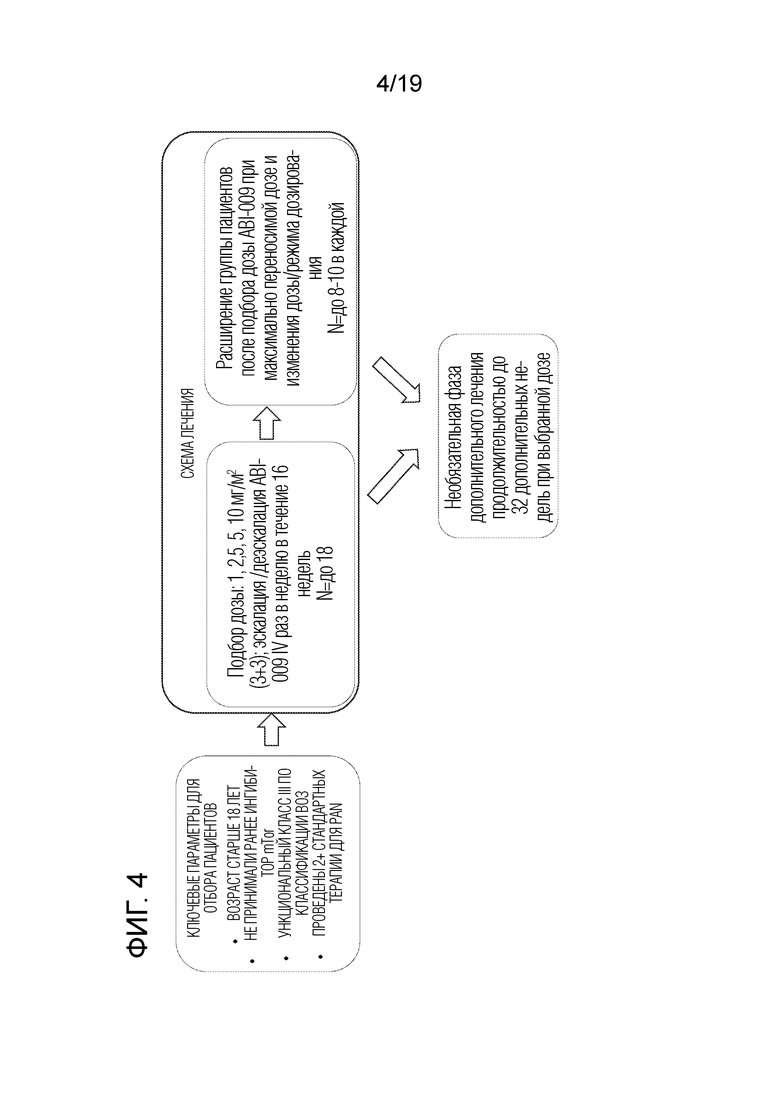
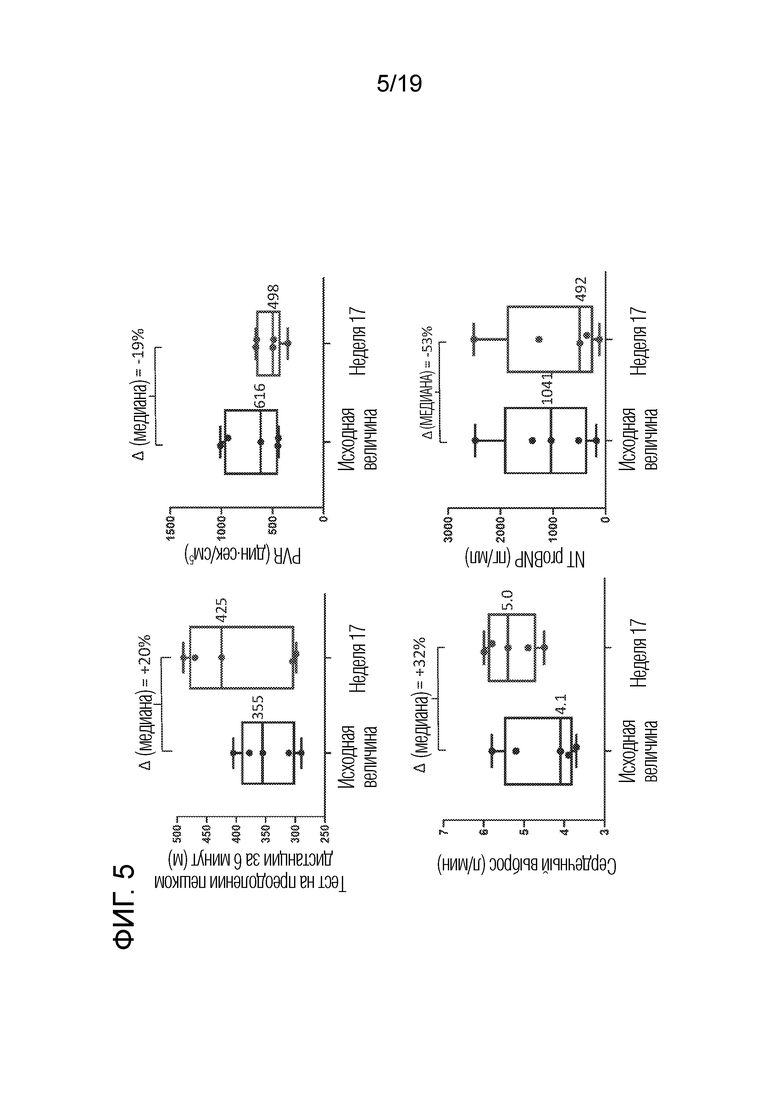
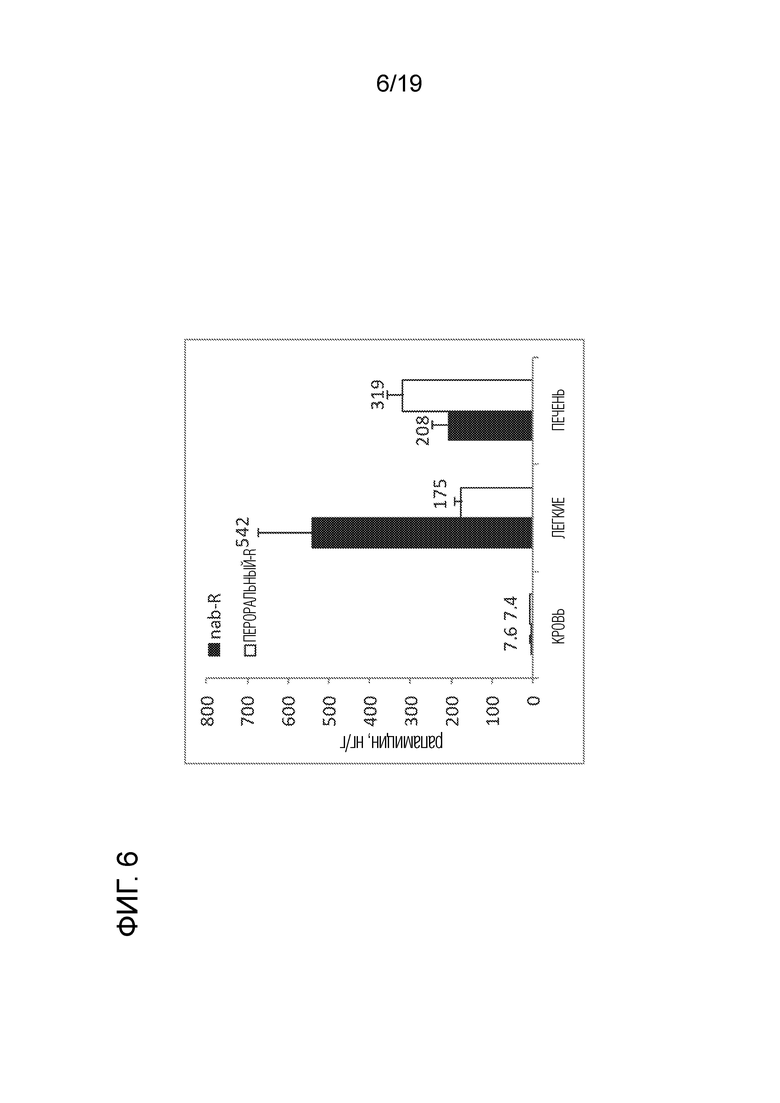
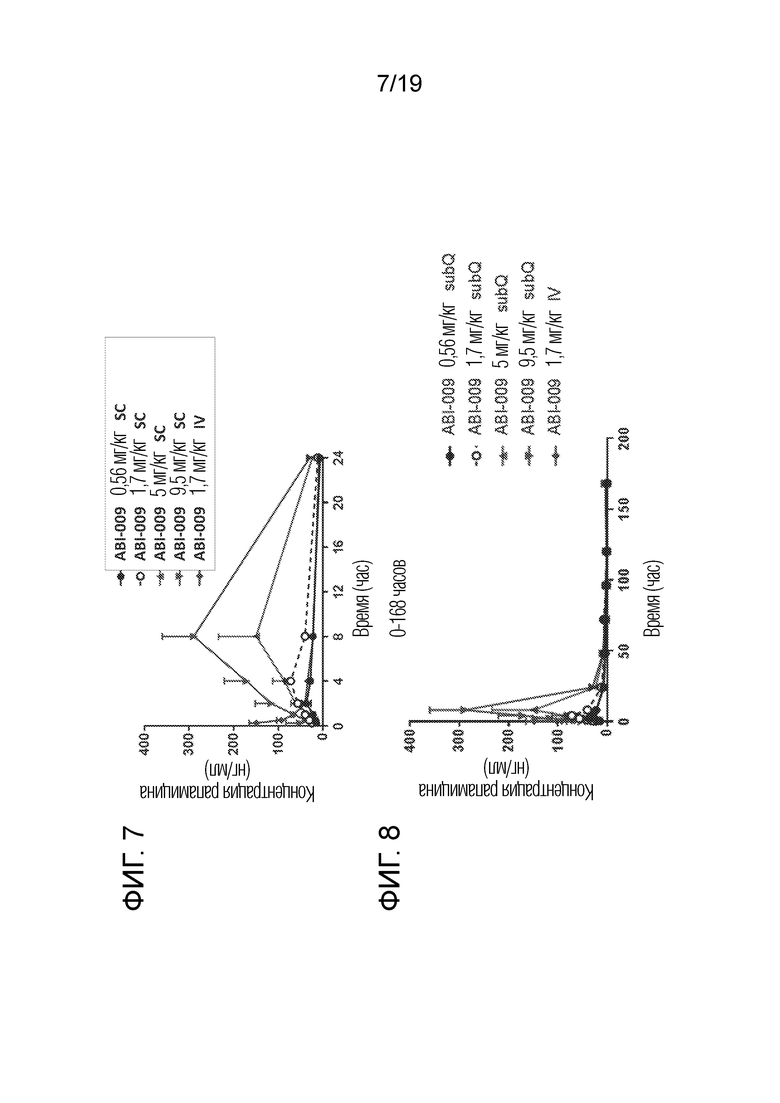
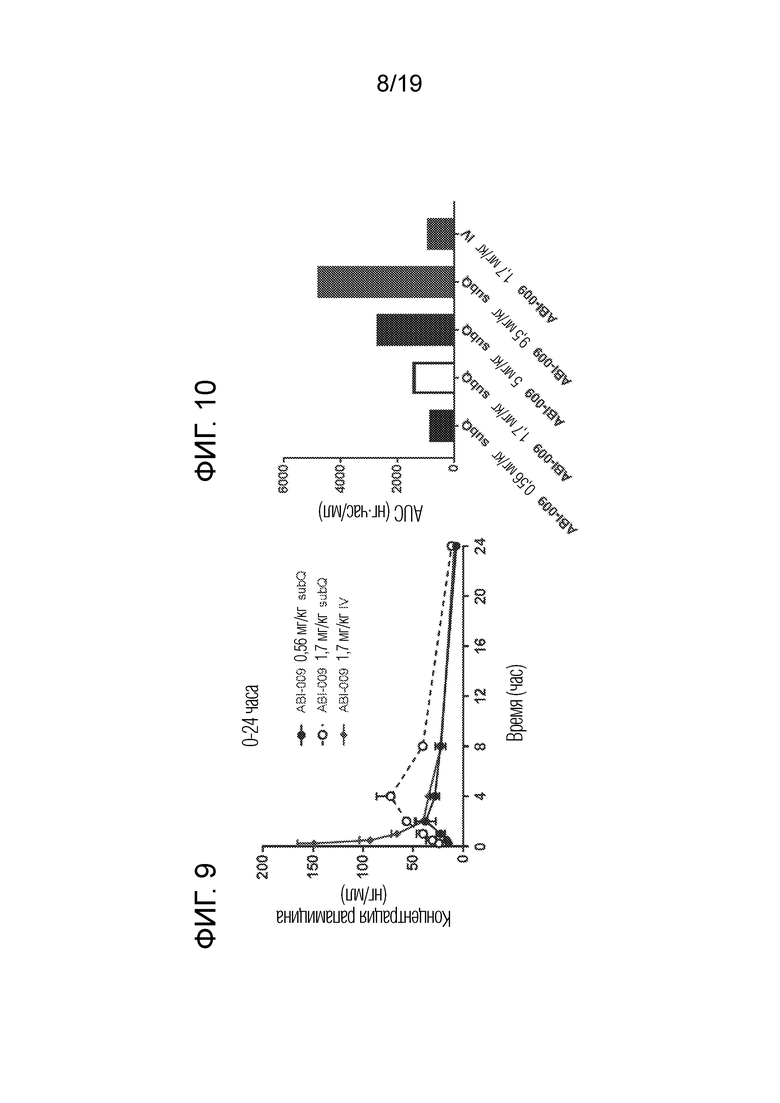
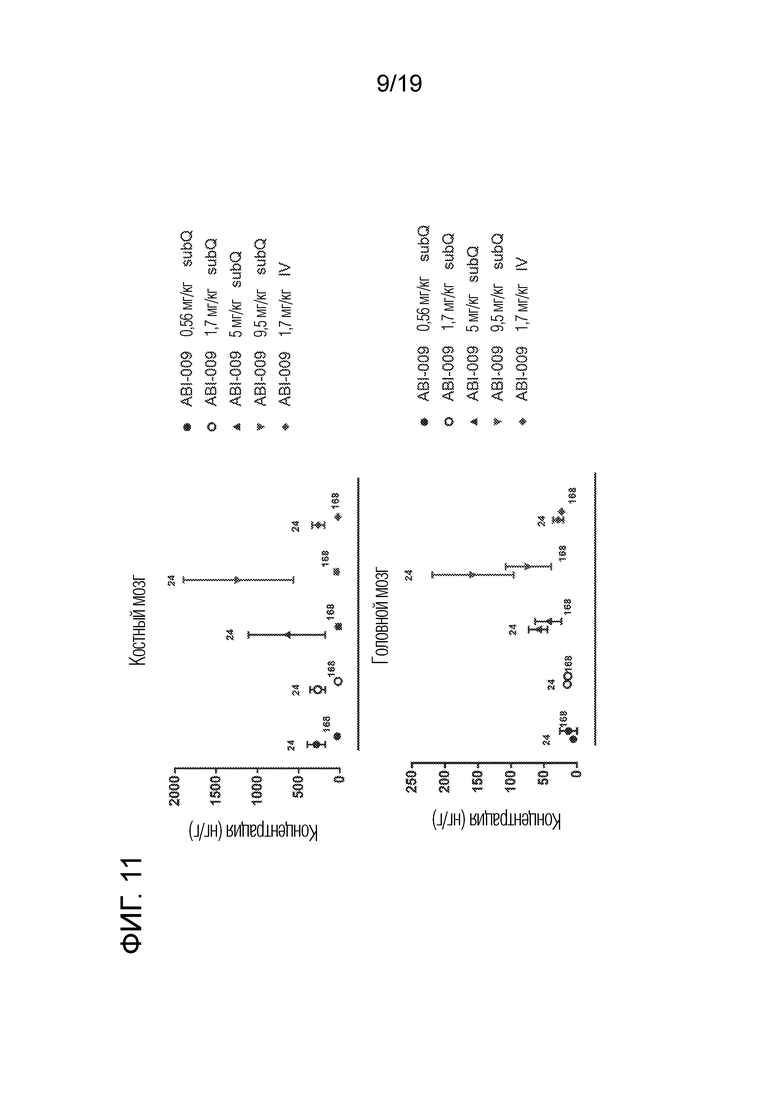
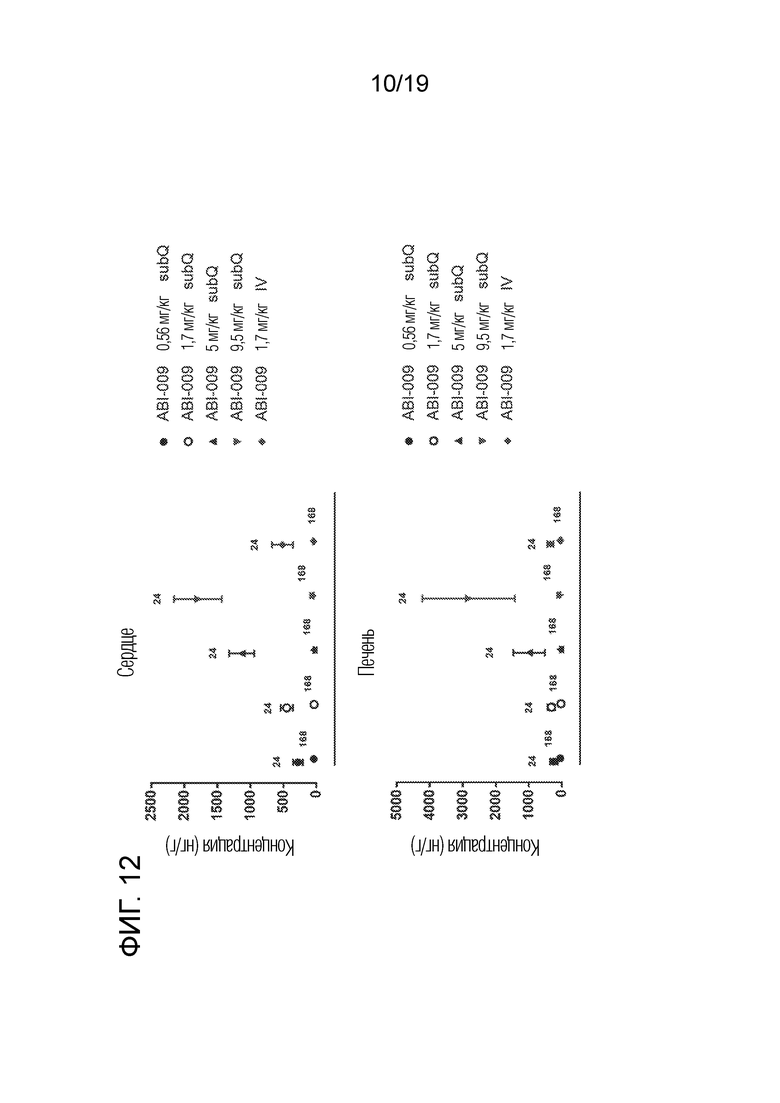
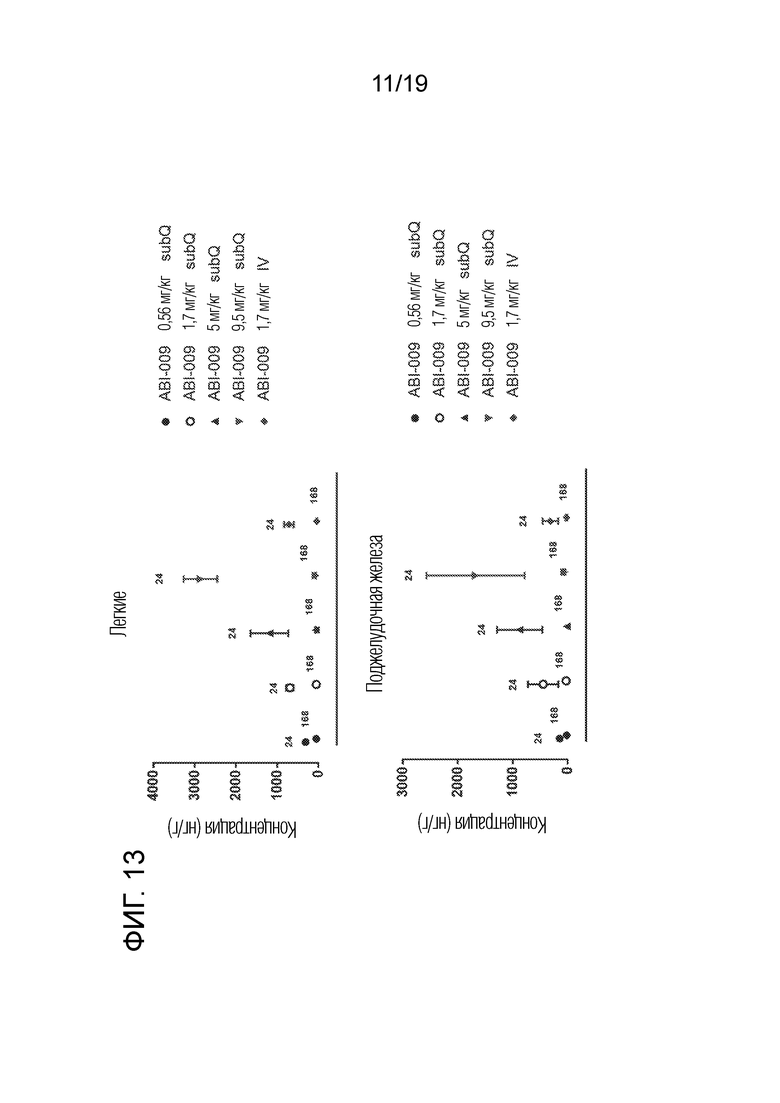
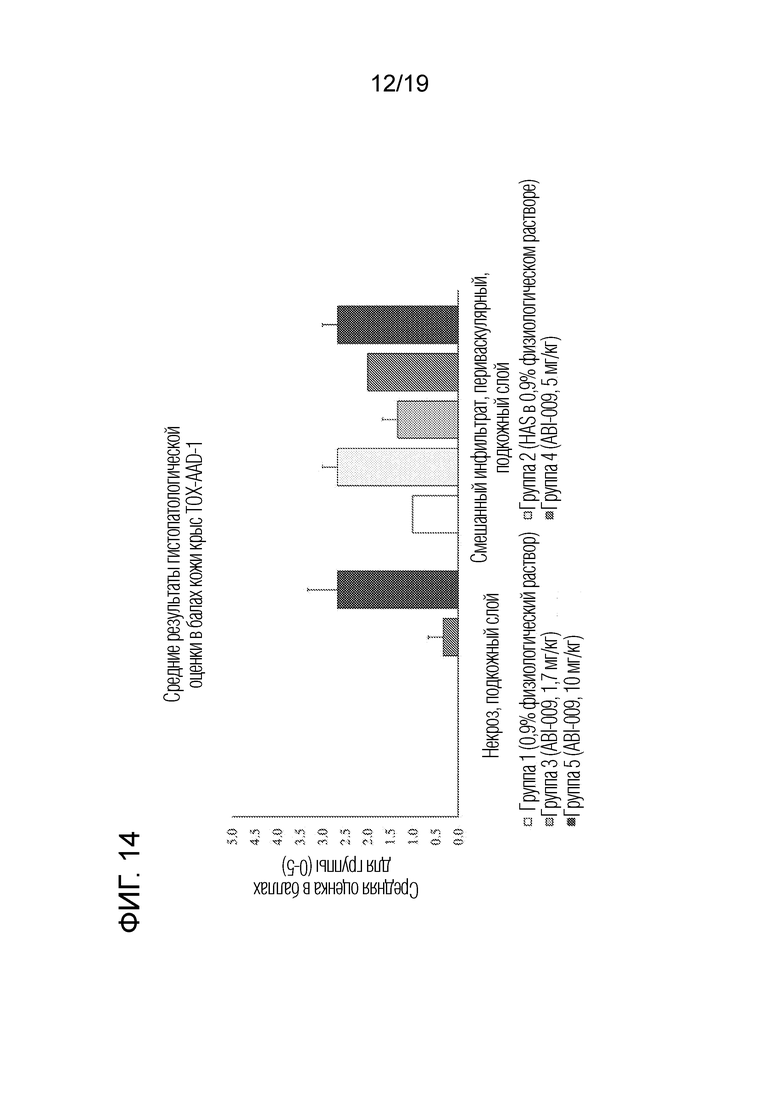
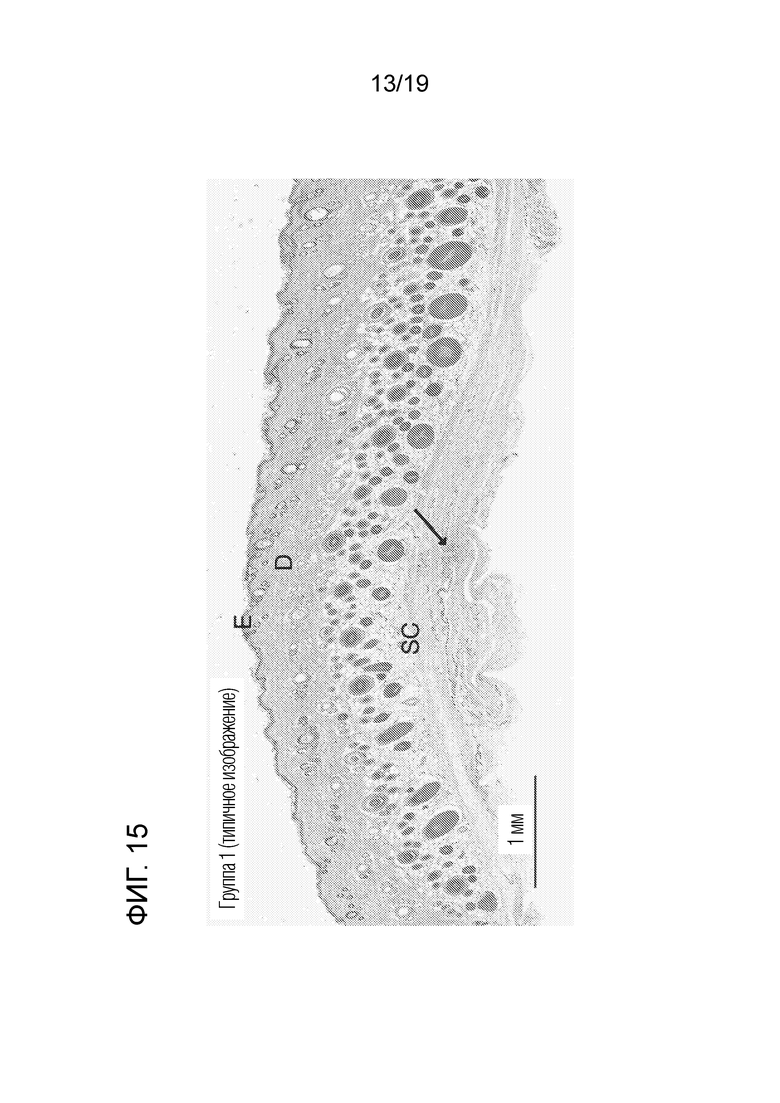
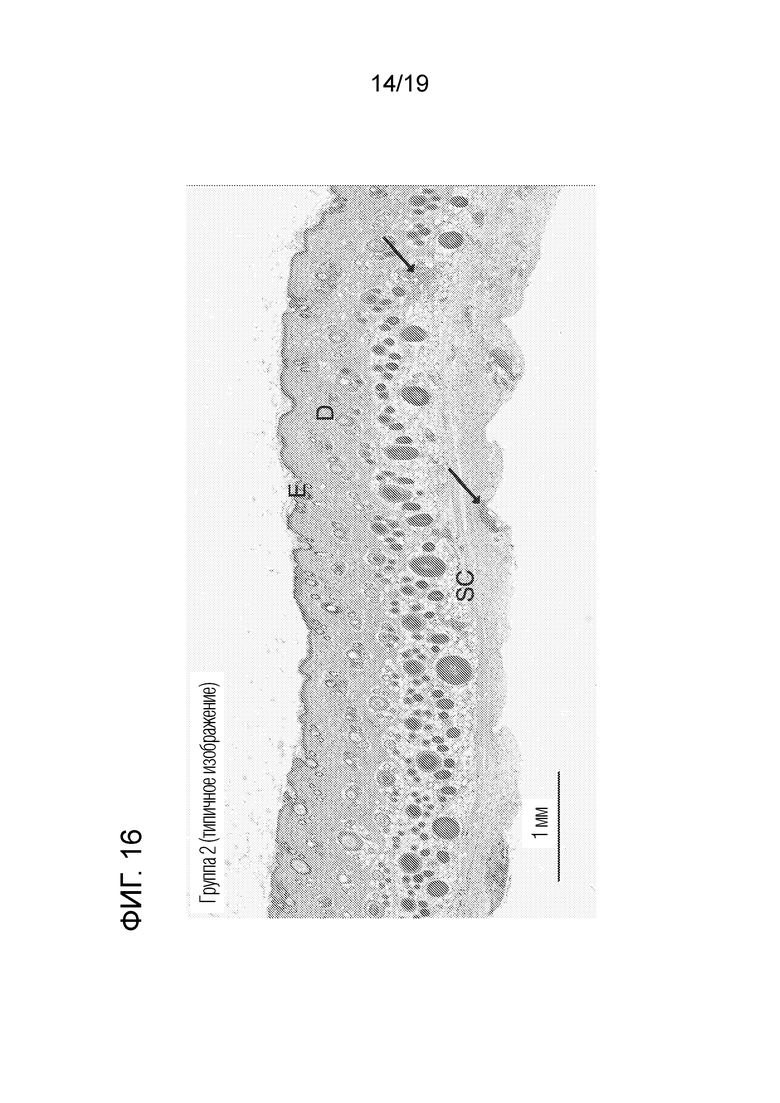



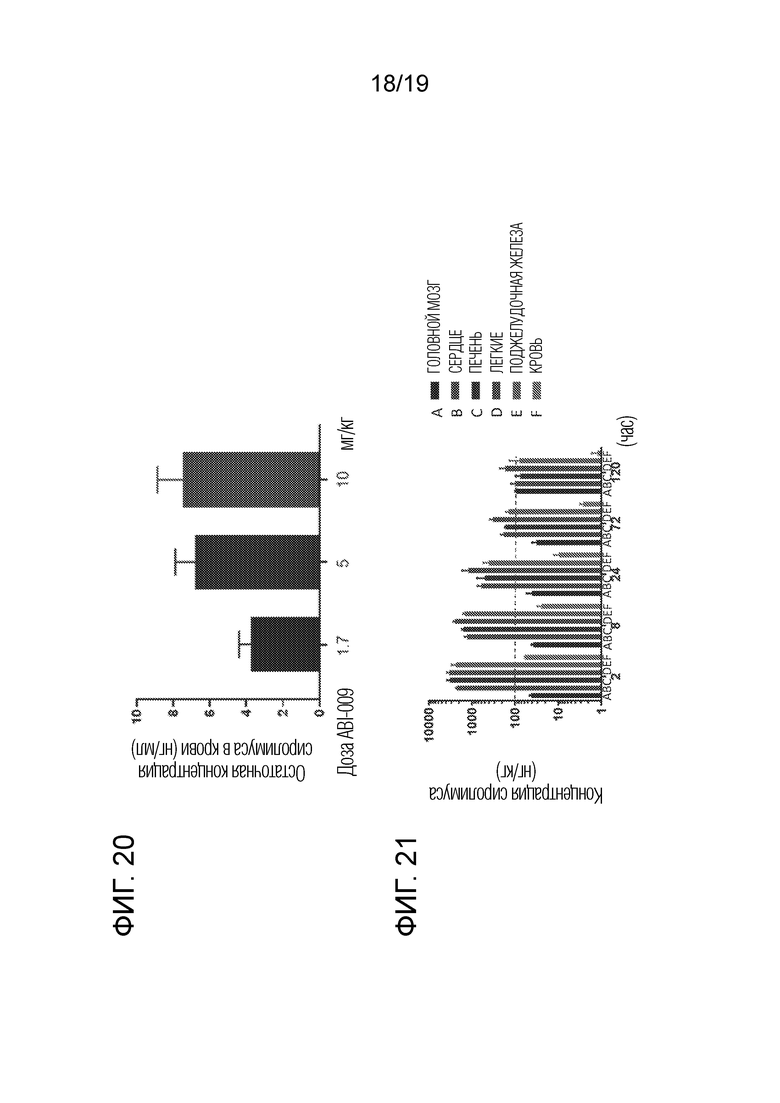

Группа изобретений относится к области медицины и фармацевтики. 1 и 3 объекты представляют собой варианты способа лечения легочной гипертензии у индивидуума, имеющего легочную гипертензию, включающего введение индивидууму композиции, содержащей наночастицы, включающие рапамицин и белковый носитель альбумин, где доза рапамицина в композиции составляет от 1 до 10 мг/м2, где композицию наночастиц вводят не чаще чем один раз в неделю, где индивидуумом является человек, резистентный, невосприимчивый или рецидивирующий по отношению по меньшей мере к двум предшествующим терапиям легочной гипертензии. 2 объект – способ улучшения результатов теста на преодоление пешком дистанции за шесть минут (6MWD) у индивидуума, страдающего легочной гипертензией, где индивидуумом является человек, резистентный, невосприимчивый или рецидивирующий по отношению по меньшей мере к двум предшествующим терапиям легочной гипертензии. Технический результат заключается в снижении давления в легочных сосудах (PVR), увеличении сердечного выброса (СО), улучшении при 6-минутной ходьбе (6MWD) и понижении функционального класса по классификации ВОЗ. 3 н. и 19 з.п. ф-лы, 22 ил., 11 табл., 5 пр.
1. Способ лечения легочной гипертензии у индивидуума, включающий введение индивидууму композиции, содержащей наночастицы, включающие ингибитор mTOR и белковый носитель, где ингибитор mTOR представляет собой рапамицин, где белковый носитель представляет собой альбумин, где доза ингибитора mTOR в композиции составляет от 1 до 10 мг/м2, где композицию наночастиц вводят не чаще чем один раз в неделю, где индивидуумом является человек, при этом введение композиции приводит к улучшению результатов теста на преодоление пешком дистанции за шесть минут (6MWD) приблизительно на 15% или более у индивидуума, и при этом индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению по меньшей мере к двум предшествующим терапиям легочной гипертензии.
2. Способ улучшения результатов теста на преодоление пешком дистанции за шесть минут (6MWD) у индивидуума, страдающего легочной гипертензией, включающий введение индивидууму композиции, содержащей наночастицы, включающие ингибитор mTOR и белковый носитель, где ингибитор mTOR представляет собой рапамицин, где белковый носитель представляет собой альбумин, где доза ингибитора mTOR в композиции составляет от 1 до 10 мг/м2, где композицию наночастиц вводят не чаще чем один раз в неделю, где индивидуумом является человек, при этом введение композиции приводит к улучшению результатов теста на преодоление пешком дистанции за шесть минут (6MWD) приблизительно на 15% или более у индивидуума, и при этом индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению по меньшей мере к двум предшествующим терапиям легочной гипертензии.
3. Способ лечения легочной гипертензии у индивидуума, имеющего легочную гипертензию, включающий введение индивидууму композиции, содержащей наночастицы, включающие ингибитор mTOR и белковый носитель, где ингибитор mTOR представляет собой рапамицин, где белковый носитель представляет собой альбумин, где доза ингибитора mTOR в композиции составляет от 1 до 10 мг/м2, где композицию наночастиц вводят не чаще чем один раз в неделю, где индивидуумом является человек, при этом индивидуум является резистентным, невосприимчивым или рецидивирующим по отношению по меньшей мере к двум предшествующим терапиям легочной гипертензии.
4. Способ по любому из пп. 1-3, где доза ингибитора mTOR в композиции составляет от 1 до 7,5 мг/м2.
5. Способ по любому из пп. 1-4, где доза ингибитора mTOR в композиции составляет не более чем 5 мг/м2.
6. Способ по п. 5, где доза ингибитора mTOR в композиции составляет 5 мг/м2.
7. Способ по любому из пп. 1-6, где композицию наночастиц вводят один раз в неделю.
8. Способ по любому из пп. 1-6, где композицию наночастиц вводят один раз каждые две недели, два раза в три недели или три раза в четыре недели.
9. Способ по любому из пп. 1-8, где композицию наночастиц вводят в течение по меньшей мере четырех недель.
10. Способ по любому из пп. 1-9, где легочная гипертензия представляет собой легочную артериальную гипертензию.
11. Способ по любому из пп. 1-10, где легочную гипертензию выбирают из группы, состоящей из идиопатической легочной артериальной гипертензии (IPAH), наследственной легочной артериальной гипертензии (HPAH), индуцированной лекарственным препаратом или токсином легочной артериальной гипертензии, ассоциированной с заболеванием соединительной ткани легочной артериальной гипертензии и ассоциированной с врожденными пороками сердца легочной артериальной гипертензии.
12. Способ по п. 10 или 11, где индивидуум имеет артериальную легочную гипертензию функционального класса III или IV по классификации ВОЗ.
13. Способ по любому из пп. 1-12, где ингибитор mTOR является только одним фармацевтически активным средством, применяемым для лечения легочной гипертензии, которое вводят индивидууму.
14. Способ по любому из пп. 1-13, где композиция включает более чем 50% ингибитора mTOR в форме наночастиц.
15. Способ по любому из пп. 1-14, где композицию наночастиц вводят парентерально.
16. Способ по п. 15, где композицию наночастиц вводят внутривенно.
17. Способ по п. 15, где композицию наночастиц вводят подкожно.
18. Способ по любому из пп. 1-17, где предшествующая терапия включает введение лекарственного средства, выбранного из группы, состоящей из аналога простациклина, антагониста рецептора эндотелина-1, ингибитора фосфодиэстеразы 5 (PDE-5) и стимулятора растворимой гуанилатциклазы (sGC).
19. Способ по любому из пп. 1-18, где в результате проведения предшествующей терапии у индивидуума достигался положительный эффект.
20. Способ по любому из пп. 1-19, где альбумин представляет собой человеческий сывороточный альбумин.
21. Способ по любому из пп. 1-20, где средний диаметр наночастиц в композиции составляет не более чем 200 нм.
22. Способ по любому из пп. 1-21, где массовое отношение белкового носителя к ингибитору mTOR в наночастицах составляет менее чем 18:1.
| US 20180133157 A1, 17.05.2018 | |||
| WO 2017004264 A1, 05.01.2017 | |||
| WO 2018064405 A1, 05.04.2018 | |||
| US 20170304276 A1, 26.10.2017. |
Авторы
Даты
2024-11-22—Публикация
2019-05-21—Подача