Настоящее изобретение относится к биомаркерам для определения чувствительности пролиферативных заболеваний, таких как рак, к терапевтическим агентам, прежде всего к ингибиторам mTOR, применяемым в сочетании с цитотоксическим агентом.
Многие ингибиторы mTOR обладают сильным антипролиферативным действием, что позволяет применять их для химиотерапии рака, прежде всего плотных опухолей, прежде всего развитых плотных опухолей. Ингибиторы mTOR объединяют также с определенными цитотоксическими агентами для дополнительного повышения эффективности лечения или для уменьшения побочных действий, например как описано в WO 02/66019. Однако все еще сохраняется необходимость в разработке направленной комбинированной терапии, основанной на использовании ингибиторов mTOR, что требует выявления пациентов, которые вероятно могут реагировать на лечение с использованием таких комбинаций агентов. Следовательно, существует необходимость в разработке биомаркеров, которые можно применять, например, в клинических опытах, позволяющих предсказывать чувствительность доброкачественного или злокачественного пролиферативного заболевания, например опухоли, у пациента к лечению ингибитором mTOR в сочетании с цитотоксическим агентом.
При создании изобретения неожиданно было установлено, что ген-супрессор опухоли р53 дикого типа (имеющий также название ген ТР53) можно использовать в качестве биомаркера для предсказания чувствительности пролиферативных заболеваний к лечению комбинацией ингибитора mTOR и цитотоксического агента. В частности, было установлено, что присутствие гена р53 дикого типа в линиях раковых клеток человека коррелирует с повышенной гибелью клеток/запрограммированной гибелью клеток/апоптозом, что происходит при обработке ингибитором mTOR в сочетании с цитотоксическим агентом, который нарушает или оказывает отрицательное воздействие на целостность ДНК. Таким образом, ингибиторы mTOR в комбинации с цитотоксическим агентом, по-видимому, обладают более выраженным антипролиферативным/приводящим к гибели клеток действием при обработке раковых клеток, сохраняющих р53 дикого типа. Белок р53 (кодируемый геном ТР53) представляет собой супрессор опухоли, который играет основную роль в регуляции прекращения клеточного цикла, физиологического старения, дифференцировке и запрограммированной гибели клеток/апоптозе клеток млекопитающих. В частности, опосредуемый р53 путь индуцирует прекращение клеточного цикла и/или апоптоз клеток млекопитающего, подвергнутых стрессу (например, повреждению ДНК, онкогенному стрессу, гипоксии, отсутствию сигналов выживания). Мутации в ТР53 встречаются примерно в половине всех случаев рака у человека, и во многих раковых клетках нарушена способность индуцировать р53-ответ (Vousden и Lu, Nature Reviews, 2, 2002, с.594-604). Последовательность человеческого р53 (мРНК [кодирующая последовательность; 1182 нуклеотидов] и белка [393 аминокислот]) можно получить в GenBank под регистрационными номерами NM 000546 или Р04637. Полная последовательность человеческого гена ТР53 депонирована в GenBank под регистрационным номером U94788.
Таким образом, в основу настоящего изобретения положена задача определения наличия гена р53 (ТР53) дикого типа в клетках, которые имеют тенденцию к аномальной пролиферации.
Одним из объектов настоящего изобретения является применение факта наличия гена р53 (ТР53) дикого типа (в отличие от отсутствия, дефицита или делеции гена р53 [ТР53], или присутствия имеющего мутацию гена р53 [ТР53]) в качестве биомаркера для оценки чувствительности пролиферативного заболевания к лечению ингибитором mTOR в сочетании с цитотоксическим агентом.
В контексте настоящего описания понятие ген р53 (ТР53) дикого типа относится не только к интронам и экзонам, но также и к связанными с ними и физически близкими к ним регуляторным областям, прежде всего областям, наиболее близким к 5' экзону. Оно включает, например, полноразмерную последовательность ДНК встречающегося в естественных условиях гена и необязательно замены нуклеотидов (включая инверсии), инсерции и делеции кодонов, при условии, что она обеспечивает экспрессию белка р53 дикого типа или его функционального эквивалента, например функционального белка р53, сохраняющего свою способность индуцировать апопотоз. Наоборот, отсутствие, дефицит, делеция или мутация гена р53 (ТР53) означает генетические или эпигенетические изменения, например амплификацию, метилирование, полиморфизмы, нуклеотидные мутации, делеции, инверсии или транслокации и утрату гетерозиготности (LOH), приводящие к нарушению экспрессии гена р53 (ТР53) или экспрессии мутантного гена, например, которые приводят к экспрессии мутантного белка р53, не обладающего более способностью индуцировать апоптоз клеток.
Следующим объектом изобретения является способ определения чувствительности пролиферативного заболевания у индивидуума к лечению ингибитором mTOR в сочетании с цитотоксическим агентом, заключающийся в том, что определяют статус р53 (ТР53) (дикий тип, либо мутант, либо с дефицитом/отсутствием статуса) в образце, взятом у индивидуума.
Еще одним объектом изобретения является способ отбора индивидуумов, страдающих пролиферативным заболеванием, для лечения ингибитором mTOR в сочетании с цитотоксическим агентом, заключающийся в том, что для каждого индивидуума определяют чувствительность пролиферативного заболевания к комбинированному лечению, согласно описанному выше способу, и отбирают для указанного комбинированного лечения индивидуумов, имеющих ген р53 (ТР53) дикого типа.
В контексте настоящего описания понятие «ингибитор mTOR» относится (но, не ограничиваясь ими) к рапамицину (сиролимус) или его производным. Рапамицин представляет собой известный макролидный антибиотик, продуцируемый Streptomyces hygroscopicus. Пригодными производными рапамицина являются, например, соединения формулы А
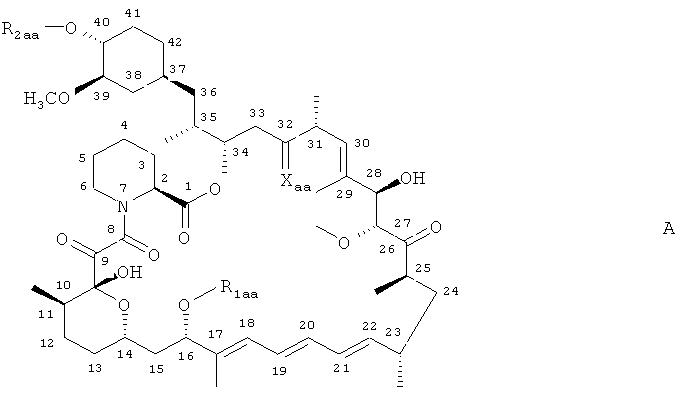
в которых
R1aa обозначает СН3 или С3-С6алкинил,
R2аа обозначает Н или -СН2-СН2-ОН, 3-гидрокси-(2-гидроксиметил)-2-метилпропаноил или тетразолил и
Хаа обозначает =O, (Н,Н) или (Н,ОН)
при условии, что R2aa не обозначат Н, если Хаа обозначает =O и R1aa обозначает СН3,
или пролекарство, когда R2аа обозначает -CH2-CH2-OH, например его гидролизуемый в физиологических условиях простой эфир.
Соединения формулы А описаны, например, в WO 94/09010, WO 95/16691, WO 96/41807, USP 5362718 или WO 99/15530, которые включены в настоящее описание в качестве ссылки. Их можно получать согласно изложенным методам или аналогично методам, описанным в указанных ссылках.
Репрезентативными производными рапамицина формулы I являются, например, 32-дезоксорапамицин, 16-пент-2-инилокси-32-дезоксорапамицин, 16-пент-2-инилокси-32(S- или R-)-дигидрорапамицин, 16-пент-2-инилокси-32(S- или R-)-дигидро-40-O-(2-гидроксиэтил)рапамицин, 40-[3-гидрокси-2-(гидроксиметил)-2-метилпропаноат]рапамицин (также имеющий название CCI779) или 40-эпи(тетразолил)рапамицин (также имеющий название АВТ578). Предпочтительным соединением является, например, 40-O-(2-гидроксиэтил)рапамицин, описанный в примере 8 WO 94/09010, или 32-дезоксорапамицин или 16-пент-2-инилокси-32(S)-дигидрорапамицин, описанный в WO 96/41807. Производные рапамицина могут включать также так называемые рапалоги, например описанные в WO 98/02441 и WO 01/14387, например АР23573, АР23464, АР23675 или АР23841. Другими примерами производного рапамицина являются соединения, описанные под названиями TAFA-93 (пролекарство рапамицина), биолимус-7 или биолимус-9.
В каждом случае, когда в описании указаны заявки на патент или научные публикации, подразумевается, что их сущность, касательно соединений, включена в настоящее описание в качестве ссылки. Это относится равным образом к их фармацевтически приемлемым солям, соответствующим рацематам, диастереоизомерам, энантиомерам, таутомерам, а также соответствующим кристаллическим модификациям вышеуказанных соединений, если они существуют, например сольватам, гидратам и полиморфам, указанным в настоящем описании. Соединения, применяемые в качестве действующих веществ в комбинациях, предлагаемых в изобретении, можно получать и вводить согласно методам, описанным соответственно в цитируемых документах.
В контексте настоящего описания понятие «цитотоксический агент» обозначает агент, который оказывает вредное действие на клеточную структуру и функцию, например нарушает или повреждает целостность ДНК и в конечном итоге может приводить к гибели клетки, например противоопухолевое лекарственное средство, например агент, обладающий активностью в отношении микротрубок или, прежде всего, лекарственное средство, повреждающее ДНК, например антинеопластический антиметаболит, содержащее платину соединение, алкилирующий агент или ингибитор топоизомеразы I или II. Понятие «цитотоксический агент» относится также к лучевой терапии, вызывающей повреждение ДНК, например ионизирующему облучению, например, с использованием радиоактивного йода. Такую лучевую терапию можно применять также совместно с терапией с использованием цитотоксического агента. Понятие «цитотоксический агент» включает также один, два или большее количество цитотоксических агентов, которые можно применять в форме комбинированной («коктейль») терапии.
В контексте настоящего описания понятие «ингибитор топоизомеразы I» включает (но, не ограничиваясь ими) топотекан, иринотекан, гиматекан, 9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148 (соединение А1 в WO 99/17804). Иринотекан можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком CAMPTOSAR™. Топотекан можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком HYCAMTIN™.
В контексте настоящего описания понятие "ингибитор топоизомеразы II" обозначает (но, не ограничиваясь ими) антрациклины, такие как доксорубицин (включая препараты на основе липосом, например CAELYX™), даунорубицин, эпирубицин, идарубицин и неморубицин, антрахиноны митоксантрон и лосоксантрон, и подофиллотоксины этопозид и тенипозид. Этопозид можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком ETOPOPHOS™. Тенипозид можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком VM 26-BRISTOL™. Доксорубицин можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком ADRIBLASTIN™. Эпирубицин можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком FARMORUBICIN™. Идарубицин можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком ZAVEDOS™. Митоксантрон можно вводить, например, в форме, в которой он поступает в продажу, например под товарным знаком NOVANTRON™.
Понятие «агент, обладающий активностью в отношении микротрубок» относится к стабилизирующим микротрубки и дестабилизирующим микротрубки агентам, включающим (но не ограничиваясь ими) таксаны, например паклитаксел и доцетаксел, алкалоиды винка, например винбластин, прежде всего винбластина сульфат, винкристин, прежде всего винкристина сульфат, и винорелбин, дискодермолиды и эпотилоны и их производные, например эпотилон Б или его производные. Паклитаксел можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком TAXOL. Доцетаксел можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком TAXOTERE™. Винбластина сульфат можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком VINBLASTIN R.P.™. Винкристина сульфат можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком FARMISTIN™. Дискодермолид можно получать, например, согласно методу, описанному в патенте США 5010099.
В контексте настоящего описания понятие «алкилирующий агент» включает (но, не ограничиваясь ими) циклофосфамид, ифосфамид, мелфалан или нитрозомочевину (BCNU или Gliadel™). Циклофосфамид можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком CYCLOSTIN™. Ифосфамид можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком HOLOXAN™.
Понятие «антинеопластический антиметаболит» включает (но, не ограничиваясь ими) 5-флуорацил, тегафур, капецитабин, кладрибин, цитарибин, флударабинфосфат, флуоридин, гемцитабин, 6-меркаптопурин, гидроксимочевину, метотрексат и эдатрексат и соли указанных соединений и, кроме того, ZD1694 (RALTITREXED™), LY231514 (ALIMTA™), LY264618 (LOMOTREXOL™) и OGT719. Капецитабин можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком XELODA™. Гемцитабин можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком GEMZAR™.
В контексте настоящего изобретения понятие «содержащее платину соединение» включает (но, не ограничиваясь ими) карбоплатин, цисплатин и оксалиплатин. Карбоплатин можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком CARBOPLAT™. Оксалиплатин можно применять, например, в форме, в которой он поступает в продажу, например под товарным знаком ELOXATIN™.
Пролиферативное заболевание может представлять собой доброкачественное или злокачественное пролиферативное заболевание, например доброкачественную гиперплазию предстательной железы, или неопластическое заболевание, предпочтительно злокачественное пролиферативное заболевание, например рак, например опухоли и/или метастазы (независимо от их локализации), опухоли головного мозга или другие опухоли центральной нервной системы (например, оболочки головного мозга, головного мозга, спинного мозга, черепных нервов и других частей центральной нервной системы, например глиобластомы или бластомы продолговатого мозга); рак головы или шеи; опухоли молочной железы; опухоли системы кровообращения (например, сердца, медиастения и плевры, и других внутригрудных органов, опухоли сосудов и ассоциированной с опухолью сосудистой ткани); опухоли выделительной системы (например, почек, почечной лоханки, мочеточника, мочевого пузыря, других и неспецифических органов мочевой системы); опухоли желудочно-кишечного тракта (например, пищевода, желудка, тонкой кишки, ободочной кишки, колоректального тракта, ректосигмовидного соединения, прямой кишки, заднего прохода и анального канала), опухоли, поражающие печень и внутрипеченочные желчные протоки, желчного пузыря, другие и неспецифические отделы желчного тракта, поджелудочной железы, других органов и органов пищеварительной системы); головы и шеи; ротовой полости (губы, язык, десны, дно полости рта, небо и другие области рта, околоушная железа и другие части слюнных желез, миндалина, ротоглотка, носоглотка, грушевидный карман, гипофаринкс и другие участки губ, ротовой полости и глотки); опухоли репродуктивной системы (например, вульвы, влагалища, шейки матки, тела матки, яичника и других областей женских половых органов, плаценты, пениса, предстательной железы, яичек и других областей, связанных с мужскими половыми органами); опухолей дыхательного тракта (например, носовой полости и среднего уха, вторичного синуса, гортани, трахеи, бронхов и легкого, например мелкоклеточный рак легкого или немелкоклеточный рак легкого); опухоли скелетной системы (например, костного и суставного хряща конечностей, костного суставного хряща и других областей); кожные опухоли (например, злокачественная меланома кожи, рак кожи, не связанный с меланомой, базально-клеточная карцинома кожи, плоскоклеточная карцинома кожи, мезотелиома, саркома Капоши); и опухоли, поражающие другие ткани, включая периферические нервы и вегетативную нервную систему, соединительную и мягкую ткань, забрюшинное пространство и брюшину, глаз и прилежащие органы, щитовидную железу, надпочечник и другие эндокринные железы и связанные с ними структуры, злокачественную опухолевую неоплазию и неспецифическую злокачественную опухоль лимфатических узлов, злокачественную опухолевую неоплазию дыхательной и пищеварительной систем и злокачественную неоплазию в других областях, опухоли кровеносной и лимфатической систем (например, болезнь Ходжкина, не-ходжкинскую лимфому, лимфому Беркитта, лимфомы, связанные со СПИДом, злокачественные иммунопролиферативные заболевания, множественную миелому и злокачественные неоплазии плазматических клеток, лимфоидный лейкоз, миелоидный лейкоз, острый или хронический лимфоцитарный лейкоз, моноцитарный лейкоз, другие виды лейкозов определенных типов клеток, лейкоз клеток неопределенного типа, другие и неопределенные злокачественные неоплазмы лимфоидной, гематопоэтической и родственных им тканей, например диффузную крупноклеточную лимфому, Т-клеточную лимфому или Т-клеточную лимфому кожных клеток). Миелоидный рак включает, например, острый или хронический миелоидный лейкоз.
Если выше или ниже в настоящем описании упоминаются опухоль, заболевание, связанное с опухолью, карцинома или рак, то при этом подразумеваются альтернативно или дополнительно также метастазы в указанном органе или ткани и/или в других областях, в которых имеются опухоль и/или метастазы.
Понятие «цитотоксический агент» может также обозначать в случае лимфатического или миелоидного рака, например, бусульфан, цитарабин, 6-тиогуанин, флударабин, гидроксимочевину, прокарбазин, блеомицин или метотрексат. В случае лимфатического или миелоидного рака в качестве цитотоксического агента предпочтительными являются ингибиторы топоизомеразы II, например даунорубицин или идарубицин, или предпочтительно соединения, которые воздействуют, снижают или ингибируют активность PDGFR (тромбоцитарный фактор роста) или представители семейства с-АbI и их слитые генные продукты, например иматиниб, ингибиторы фарнесилтрансферазы, Ara-C, VP-16, тенипосид, митоксантрон, карбоплатин или мидостаурин.
В соответствии со способом, предлагаемым в настоящем изобретении, можно отбирать индивидуумов, страдающих таким пролиферативным заболеванием, для предсказания их чувствительности к комбинированному лечению с использованием ингибитора mTOR и цитотоксического агента. Способ можно осуществлять in vitro, например, с использованием биологического образца ткани, взятого из организма индивидуума. Образец может представлять собой любой биологический материал, выделенный из организма млекопитающего, такой, например, как ткань, линии клеток, плазма или сыворотка, клеточный или тканевый лизат, предпочтительно опухолевая ткань.
Статус гена р53 (ТР53) анализируют в биологическом образце с помощью любых технических методов, основанных, например, на ДНК-анализе генетических и эпигенетических изменений, например ДНК-сканирования для определения амплификации, метилирования, полиморфизмов, нуклеотидных мутаций (например, мутаций кодонов 175Arg, 245Gly, 248Arg, 249Arg, 273Arg, 282Arg и других), нуклеотидных делеций, инверсий и/или трансляций и утраты гетерозиготности (LOH). Статус р53 (ТР53) анализируют в биологических образцах с помощью любых технических методов на основе, например экспрессии РНК с использованием, например, методов Нозерн-блоттинга или ОТ-ПЦР, или на основе анализа экспрессии/модификаций белка с использованием, например, методов Вестерн-блоттинга, иммуногистохимии или твердофазного иммуноферментного анализа (ELISA), в том числе с помощью иммуноанализа, иммунопреципитации и электрофоретического анализа.
Например, для измерения уровней белка р53/фосфорилирования/убикитинирования/ацетилирования можно использовать в стандартном формате иммуноанализа антитела, специфические для белка р53, или посттрансляционных модификаций, таких как фосфорилирование (например, фосфорилирование Ser46), убикитинирование или ацетилирование. Для определения уровней белка р53/посттрансляционных модификаций в качестве биомаркера применяют также анализ типа ELISA (твердофазный иммуноферментный анализ), анализ на основе иммунопреципитации, стандартные анализы методом Вестерн-блоттинга и иммуногистохимические анализы с использованием, например, моноклональных или поликлональных антител.
Поликлональные и моноклональные антитела, специфические в отношении белка р53/посттрансляционных модификаций, получают согласно известным методам иммунизации или используют поступающие в продажу антитела (например, от фирмы Santa Cruz Biotechnology Inc. каталожный номер sc6253).
Статус р53 можно оценивать также с помощью двумерного (2-D) гель-электрофореза. Метод 2-D-гель-электрофореза известен в данной области и, как правило, заключается в изоэлектрическом фокусировании (ИЭФ) в первом направлении и последующем ДСН-ПААГ (гель-электрофорез в полиакриламидном геле с додецилсульфатом натрия) во втором направлении. Полученные электрофореграммы анализируют, например, методом иммуноблоттинга с использованием антител.
В настоящем изобретении предложен также способ отбора индивидуумов, страдающих пролиферативным заболеванием, с целью предсказания их чувствительности к комбинированному лечению с использованием ингибитора mTOR и цитотоксического агента, заключающийся в том, что определяют статус р53 (ТР53) описанным выше способом.
Еще одним объектом изобретения является способ лечения пролиферативного заболевания у индивидуума, нуждающегося в этом, заключающийся в том, что определяют статус гена р53 (ТР53) или уровень экспрессии р53 и/или посттрансляционные модификации в образце, полученном из организма индивидуума с помощью описанного выше способа, и соответственно обрабатывают индивидуума ингибитором mTOR в сочетании с цитотоксическим агентом.
Еще один вариант осуществления изобретения касается способа повышения активности цитотоксического агента или преодоления устойчивости к цитотоксическому агенту у индивидуума, нуждающегося в этом, заключающийся в том, что определяют статус гена/экспрессии р53 (ТР53) в образце, полученном из организма индивидуума, с помощью описанного выше способа и вводят индивидууму ингибитор mTOR в терапевтически эффективном количестве либо одновременно, либо последовательно с указанным цитотоксическим агентом.
Статус р53 (ТР53) в конкретной ткани, взятой у конкретного пациента, например в образце опухолевой ткани, можно сравнивать с контрольным образцом, например с образцом здоровой ткани индивидуума, не страдающего заболеванием, или образцом здоровой (т.е. не пораженной опухолью) ткани того же индивидуума. Уровень статуса р53 (ТР53) дикого типа, при котором показано применение ингибитора mTOR в сочетании с цитотоксическим агентом, является критерием для предсказания благоприятного терапевтического действия (т.е. антипролиферативного и/или приводящего к повышенной гибели клеток) комбинированного лечения с использованием ингибитора mTOR и цитотоксического агента.
Кроме того, способ можно применять для выбора соответствующей дозы цитотоксического агента и/или ингибитора mTOR с целью индивидуальной оптимизации терапии для каждого конкретного пациента. В зависимости от статуса р53 дикого типа у пациента можно применять в комбинации более низкие дозы действующих веществ, например, часто можно применять не только меньшие дозы, но и вводить их с меньшей частотой или для уменьшения побочных действий при лечении нежелательной пролиферации. В контексте настоящего описания рассматриваемые факторы включают, прежде всего, конкретное состояние, подлежащее лечению, конкретное млекопитающее, подлежащее лечению, клиническое состояние конкретного пациента, область введения действующих веществ, конкретный тип действующих веществ, метод введения, график введения, степень серьезности состояния и другие факторы, известные практикующим врачам.
В контексте настоящего описания понятия «совместное введение» или «комбинированное введение», или т.п. включают введение выбранного ингибитора mTOR и цитотоксического агента конкретному пациенту, и подразумевается, что они относятся к режимам введения, при которых агенты не обязательно вводят одинаковым путем или в одно и то же время. Например, ингибитор mTOR и цитотоксический агент можно вводить пациенту в виде раздельных единиц одновременно, совместно или последовательно без фиксированных промежутков времени при условии, что такое введение обеспечивает терапевтически эффективные уровни обоих соединений в организме.
Терапевтически эффективное количество каждого действующего компонента композиции следует определять с учетом вышеизложенного, и оно представляет собой минимальное количество, необходимое для предупреждения, облегчения или лечения заболевания. Такое количество предпочтительно меньше количества, являющегося токсичным для хозяина, или количества, которое делает хозяина более чувствительным к инфекциям.
Приемлемые дозы ингибитора mTOR указаны, например, в WO 02/66019, например суточные дозы, которые составляют примерно от 0,1 до 30 мг, например от примерно 0,05 до 20 мг действующего вещества при введении р.о. в виде однократной дозы или в виде разделенных доз, или при периодическом введении, например один раз в неделю. Рапамицин или его производное, например соединение формулы А, можно вводить любым общепринятым путем, в частности энтерально, например орально в форме таблеток, капсул, растворов для питья или парентерально, например в форме растворов или суспензий для инъекции, содержащих, например от примерно 0,1 до примерно 99,9%, предпочтительно от примерно 1 до примерно 60%, действующего(их) веществ(а).
Топотекан можно вводить человеку в диапазоне доз от примерно 1 до 5 1 мг/м2/день. Иринотекан можно вводить человеку в диапазоне доз от примерно 50 до 350 мг/м2/день.
Паклитаксел можно вводить человеку в диапазоне доз от примерно 50 до 300 мг/м2/день. Доцетаксел можно вводить человеку в диапазоне доз от примерно 25 до 100 мг/м2/день.
Циклофосфамид можно вводить человеку в диапазоне доз от примерно 50 до 1500 мг/м2/день. Мелфалан можно вводить человеку в диапазоне доз от примерно 0,5 до 10 мг/м2/день.
5-Флуорацил можно вводить человеку в дозе приблизительно от 50 до 1000 мг/м2/день, например 500 мг/м2/день. Капецитабин можно вводить человеку в дозе приблизительно от 10 до 1000 мг/м2/день. Гемцитабина гидрохлорид можно вводить человеку в дозе, составляющей приблизительно 1000 мг/м2/неделю.
Карбоплатин можно вводить человеку в дозе приблизительно от 200 до 400 мг/м2 приблизительно каждые четыре недели. Цисплатин можно вводить человеку в дозе приблизительно от 25 до 75 мг/м2 приблизительно каждые три недели. Оксалиплатин можно вводить человеку в дозе приблизительно от 50 до 85 мг/м2 каждые две недели.
Иматиниб можно вводить человеку в дозе приблизительно от 2,5 до 850 мг/день, более предпочтительно от 5 до 600 мг/день и наиболее предпочтительно от 20 до 300 мг/день.
Предпочтительной комбинацией, которую применяют в способе, предлагаемом в изобретении, является, например комбинация рапамицина, 40-[3-гидрокси-2-(гидроксиметил)-2-метилпропаноат]рапамицинаили 40-O-(2-гидроксиэтил)рапамицина и цитотоксического агента, такого как гемцитабин или цисплатин. Другой комбинацией, которую используют в способе, предлагаемом в изобретении, является комбинация ингибитора mTOR и цитотоксического агента, например описанных выше гемцитабина или цисплатина, взятых в количествах, обладающих синергетическим действием.
Предпочтительно ТР53 представляет собой человеческий ген.
Предпочтительно способы, предлагаемые в изобретении, осуществляют на опухолевых клетках, презентирующих статус р53 (ТР53) дикого типа.
При разработке еще одного варианта осуществления изобретения неожиданно было установлено, что повышенная гибель клеток/запрограммированная гибель клеток/апоптоз, обусловленная обработкой ингибитором mTOR в сочетании с цитотоксическим агентом, для клеток, несущих р53 (ТР53) дикого типа, связана с выраженным ослаблением индуцированной цитотоксическим действием повышающей регуляции экспрессии белка р21Waf1/Cip1 (имеющего также названия CDKN1A, WAF1, CIP1, SDI1, САР20, MDA-6, р21), ниже в настоящем описании обозначен как р21.
р21 является представителем cip/kip-семейства "ингибиторов" циклинкиназ, который играет роль в прохождении клеточного цикла, а также в предупреждении апоптоза. В контексте настоящего описания четко установлена функция р21 в отношении прекращения клеточного роста в ответ на стрессовые сигналы, например повреждение ДНК, в ответ на активацию р53. Действительно установлено, что повышенная экспрессия белка р21 позволяет выживать таким подвергнутым стрессу клеткам, например позволяет завершать клетке процесс репарации ДНК. Таким образом, ослабление повышенной экспрессии р21 в результате обработки цитотоксическим агентом может стимулировать гибель клеток/запрограммированную гибель клеток/апоптоз (Weiss, Cancer Cell,4, 2003, c.425-429). Последовательность человеческого р21 (мРНК [кодирующая последовательность: 495 нуклеотидов] и белкового продукта [164 аминокислоты]) находится в GenBank под регистрационным номером NM 000389, NM 078467 или ААН01935. Полная последовательность человеческого гена р21 находится в GenBank под регистрационным номером NM 078467.
Кроме того, для некоторых страдающих раком пациентов характерна повышенная общая или цитозольная экспрессия р21 в клетках опухоли, что связано с невысокой достоверностью прогноза и слабой реакцией на химиотерапию (Weiss, supra). Оценка основного уровня экспрессии р21 в организме страдающего раком пациента может позволить отобрать пациентов для специфического химиотерапевтического лечения, например на основе терапии с использованием mTOR в сочетании с одним или несколькими цитотоксическими агентами и необязательно лучевой терапией.
Таким образом, в настоящем изобретении предложено также:
I. применение р21 в качестве биомаркера для определения чувствительности или ответа пролиферативного заболевания у индивидуума на лечение ингибитором mTOR в сочетании с цитотоксическим агентом;
II. способ отбора индивидуумов, страдающих пролиферативным заболеванием, с целью лечения ингибитором mTOR в сочетании с цитотоксическим агентом, заключающийся в том, что определяют чувствительность пролиферативного заболевания к лечению ингибитором mTOR в комбинации с цитотоксическим агентом у каждого индивидуума с помощью описанного выше способа и отбирают индивидуумов, у которых обнаружен повышенный уровень экспрессии р21, для комбинированного лечения;
III. способ определения чувствительности или ответа пролиферативного заболевания у индивидуума на лечение ингибитором mTOR в сочетании с цитотоксическим агентом, заключающийся в том, что определяют в образце, взятом у индивидуума, уровень экспрессии р21 до и/или после обработки цитотоксическим агентом индивидуально или в сочетании с ингибитором mTOR;
IV. способ повышения активности цитотоксического агента или преодоления устойчивости к цитотоксическому агенту у индивидуума, подвергающегося лечению цитотоксическим агентом, который заключается в том, что
определяют уровень экспрессии р21 в образце, взятом из организма индивидуума, с помощью описанного выше способа,
если экспрессия р21 подвергается повышающей регуляции после введения цитотоксического агента, то индивидууму вводят ингибитор mTOR в терапевтически эффективном количестве в сочетании с цитотоксическим агентом,
снова определяют уровень экспрессии р21 в новом образце, взятом из организма индивидуума после лечения комбинацией ингибитора mTOR и цитотоксического агента, и
если экспрессия р21 подвергается понижающей регуляции, индивидуума продолжают лечить ингибитором mTOR, вводя его либо одновременно, либо последовательно с цитотоксическим агентом.
Как уже отмечалось выше, уровни белка р21 можно определять согласно методу, описанному выше для р53; однако подразумевается, что вместо использования антител, специфических для р53, следует применять антитело, специфическое для р21, например моноклональное или поликлональное антитело, например поступающее в продажу (например, поставляемое фирмой Oncogene Research products, клон ЕА10, каталожный номер ОР64).
Уровень, обнаруженный в конкретной ткани, взятой из организма индивидуума, например в образце опухолевой ткани, можно сравнивать с контрольным образцом, например образцом здоровой ткани, взятым у индивидуума, не страдающего заболеванием, или в образце здоровой (т.е. неопухолевой) ткани, взятым у того же самого индивидуума. Отсутствие уменьшения индукции экспрессии р21 (при обработке ингибитором mTOR в сочетании с цитотоксическим агентом по сравнению с индукцией, происходящей при обработке только одним цитотоксическим агентом) позволяет прогнозировать благоприятное терапевтическое действие (т.е. антипролиферативное/вызывающее гибель клеток действие) ингибитора mTOR в сочетании с цитотоксическим агентом. Оценка индукции экспрессии р21 цитотоксическим агентом и/или обратное действие ингибитора mTOR на уровень экспрессии р21 может оказаться полезным также для адаптации доз цитотоксического агента, например для снижения цитотоксической дозы.
Ниже настоящее изобретение проиллюстрировано на примерах, не ограничивающих его объем.
Пример 1
Несущие р53 (ТР53) дикого типа опухолевые клетки человеческой аденокарциномы линии А549 (CCL-185) (Американская коллекция типовых культур, Роквилл, шт. Мэриленд, США) высевают с плотностью 2×103 клеток/100 мкл на лунку в 96-луночные планшеты и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки инкубируют в присутствии субоптимальных концентраций гемцитабина (например, от 5 до 17,5нМ) либо в сочетании с 20 нМ 40-O-(2-гидроксиэтил)рапамицином, либо с носителем, представляющим собой ДМСО, который используют в качестве контроля, еще в течение 72 ч. К клеткам добавляют краситель YО-РRО (йодид YO-PROR-1 [491/509], каталожный номер Y3603, фирма Molecular Probes) и используют планшет-ридер типа Cytofluor II Fluorescence для оценки гибели клеток или цитотоксичности, и после лизиса клеток для оценки относительной пролиферации клеток. В этом анализе ингибитор mTOR, например 40-O-(2-гидроксиэтил)рапамицин, вызывает статистически достоверное усиление приводящего к гибели клеток действия субоптимальных концентраций гемцитабина (р<0,05; дисперсионный регрессионный анализ (ANOVA) в сочетании с критерием Tukey). Результаты, аналогичные описанным выше, получают с использованием несущих р53 (ТР53) клеточных линий дикого типа, отличных от человеческой легочной аденокарциномы А549, например человеческой линии клеток молочной железы MCF7 (НТВ-22; Американская коллекция типовых культур).
Указанную процедуру повторяют с использованием линий опухолевых клеток, несущих мутантный/дефектный р53 (ТР53), например клеток рака предстательной железы человека линии РС3М (которые высевают с плотностью 0,8×103 клеток/100 мкл) или клеток рака молочной железы человека линии MDA-MB231 (которые высевают с плотностью 2×103 клеток/100 мкл; НТВ-26; Американская коллекция типовых культур). В несущих мутантный/дефектный р53 (ТР53) линиях клеток не обнаружено выраженного или закономерного усиления клеточной гибели.
Клетки линии А549 высевают с плотностью 0,1×106 клеток/10 мл на планшеты размером 10 см и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки инкубируют в присутствии субоптимальных концентраций гемцитабина (например, от 5 до 12,5 нМ) либо в сочетании с 20 нМ 40-O-(2-гидроксиэтил)рапамицином, либо с носителем ДМСО, используемым в качестве контроля, еще в течение 72 ч. Клеточные экстракты, содержащие 50 мкг общего белка, анализируют с помощью электрофореза в 8% ДСН-ПААГ и осуществляют анализ с помощью иммуноблоттинга с использованием кроличьих поликлональных антител к поли-АДФ-рибозополимеразе (Poly (ADP-Ribose) Polymerase (PARP)) (фирма Cell Signalling Technology, каталожный номер 9542). В этом анализе присутствие ингибитора mTOR, например 40-0-(2-гидроксиэтил)рапамицина, приводит к повышенному расщеплению PARP (маркер апоптоза) при субоптимальных концентрациях гемцитабина (по сравнению с использованием гемцитабина или ингибитора mTOR индивидуально в таких же концентрациях). Это подтверждает приведенные выше результаты, касающиеся того, что в несущих р53 (ТР53) дикого типа клетках линии А549 присутствие ингибитора mTOR приводит к более высоким уровням гибели клеток при субоптимальных концентрациях гемцитабина.
Пример 2
Несущие р53 (ТР53) дикого типа опухолевые клетки человеческой аденокарциномы линии А549 высевают с плотностью 5×103 клеток/100 мкл на лунку в 96-луночные планшеты и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки инкубируют в присутствии субоптимальных концентраций цисплатина (например, от 3 до 10 мкг/мл) либо в сочетании с 20 нМ 40-O-(2-гидроксиэтил)рапамицином, либо с носителем ДМСО, используемым в качестве контроля, еще в течение 24 ч. Осуществляют с использованием YO-PRO® анализ оценки гибели клеток или цитотоксичности и после лизиса клеток оценку относительной клеточной пролиферации. В этом анализе ингибитор mTOR, например 40-O-(2-гидроксиэтил)рапамицин, вызывает статистически достоверное усиление приводящего к гибели клеток действия субоптимальных концентраций цисплатина (р<0,05; ANOVA в сочетании с критерием Tukey). Последующий анализ с помощью двунаправленного ANOVA свидетельствует о наличии высокой степени достоверности совместного действия RAD001 и цисплатина (р<0,001). Результаты, аналогичные описанным выше, получают с использованием несущих р53 (ТР53) дикого типа клеток, клеточной линии, отличной от человеческой легочной аденокарциномы А549, например человеческой линии клеток молочной железы MCF7. В последнем случае инкубацию в присутствии соединений проводят в течение 30 ч.
Указанную процедуру повторяют с использованием линий опухолевых клеток, несущих мутантный/дефектный р53 (ТР53), например клеток рака предстательной железы человека линии РС3М (которые высевают с плотностью 3×103 клеток/100 мкл) или DU145 (которые высевают с плотностью 5×103 клеток/100 мкл:НТВ-81; Американская коллекция типовых культур). Инкубацию с соединениями осуществляют в этом случае в течение 22 ч для DU145 или 30 ч для РС3М. В несущих мутантный/дефектный р53 (ТР53) линиях клеток не обнаружено выраженного или закономерного усиления клеточной гибели.
Клетки линии А549 высевают с плотностью 0,1×106 клеток/10 мл на чашки диаметром 10 см и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки инкубируют в присутствии субоптимальных концентраций цисплатина (например, от 0,5 до 4 мкг/мл) либо в комбинации с 20 нМ 40-O-(2-гидроксиэтил)рапамицином, либо с носителем ДМСО, используемым в качестве контроля, еще в течение 24 ч. Клеточные экстракты, содержащие 50 мкг общего белка, анализируют с помощью электрофореза в 8% ДСН-ПААГ и осуществляют анализ с помощью иммуноблоттинга с использованием кроличьих поликлональных антител к Poly (ADP-Ribose) Polymerase (PARP) и р53. В этом анализе присутствие ингибитора mTOR, например 40-O-(2-гидроксиэтил)рапамицина, приводит к повышенному расщеплению PARP (маркер апоптоза) при субоптимальных концентрациях цисплатина (по сравнению с использованием цисплатина или ингибитора mTOR индивидуально в таких же концентрациях). Это подтверждает приведенные выше результаты, касающиеся того, что в несущих р53 (ТР53) дикого типа клетках линии А549, присутствие ингибитора mTOR приводит к более высоким уровням гибели клеток при субоптимальных концентрациях цисплатина.
Статус р53 (ТР53) является критерием предсказания чувствительности, например, опухоли у индивидуума к действию комбинации ингибитора mTOR и цитотоксического агента. Статус р53 можно оценивать использованием ДНК, РНК или белка, полученного из опухолевой ткани согласно описанному способу для предсказания чувствительности к действию комбинации ингибитора mTOR и цитотоксического агента.
Пример 3
Несущие р53 (ТР53) дикого типа клетки линии А549 и MCF7 высевают с плотностью 0,3×103 и 0,4×103 клеток/4 мл соответственно в чашки диаметром 6 см и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки инкубируют в присутствии субоптимальных концентраций цисплатина (например, от 0,5 до 4 мкг/мл) либо в сочетании с 20 нМ 40-O-(2-гидроксиэтил)рапамицином, либо с носителем ДМСО, используемым в качестве контроля, еще в течение 24 ч и 30 ч соответственно. Клеточные экстракты, содержащие 30 мкг общего белка, анализируют с помощью электрофореза в 15% ДСН-ПААГ и осуществляют анализ с помощью иммуноблоттинга с использованием мышиных моноклональных антител к р21 (фирма Oncogene Research Products, клон ЕА10, каталожный номер ОР64). В обеих линиях клеток цисплатин индивидуально вызывает повышенную экспрессию белка р21 в зависимости от концентрации. Неожиданно было установлено, что присутствие ингибитора mTOR, например 40-O-(2-гидроксиэтил)рапамицина, ослабляет индуцируемую цисплатином повышающую регуляцию экспрессии белка р21. В отличие от этого на экспрессию белка Вах, проапоптозного белка, регулируемого р53, не оказывает влияние агент ни при индивидуальном применении, ни в составе комбинации. В этом анализе вызывающая цитотоксическое действие экспрессия белка р21 ингибируется в присутствии ингибитора mTOR. Это позволяет объяснить повышенное приводящее к гибели клеток/апоптозу действие, вызываемое комбинациями цисплатина и ингибитора mTOR.
Пример 4
Несущие р53 (ТР53) дикого типа опухолевые клетки человеческой аденокарциномы линии А549 высевают с плотностью 0,1×106 клеток/5 мкл на лунку в чашки диаметром 6 см и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки оставляют нетрансфектированными или осуществляют кратковременную трансфекцию с использованием 100 нМ siPHK, мишенью которой является либо человеческий р53 (регистрационный номер: NM000546; последовательность мишени: 5'-GCATCTTATCCGAGTGGAА-3'), либо контрольной siPHK LacZ (регистрационный номер: М55068; последовательность мишени: 5'-GCGGCTGCCGGAАТТТАССТТ-3') с использованием олигофектамина (фирма Invitrogen, каталожный номер 12252-011). После инкубации в течение 30 ч клетки инкубируют с возрастающими концентрациями цисплатина (например, от 0,5 до 6 мкг/мл) еще в течение 24 ч. Клеточные экстракты, соответствующие 30 мкг (р21) и 50 мкг (р53 и PARP) общего белка, подвергают электрофорезу в 15% ДСН-ПААГ (р21) и 10% ДСН-ПААГ (р53 и PARP) и осуществляют анализ методом иммуноблоттинга с использованием мышиных моноклональных и кроличьих поликлональных антител к р21 и р53/PARP соответственно. Обработка цисплатином нетрансфектированных или контрольных трансфектированных siPHK LacZ клеток индуцирует зависимую от концентрации экспрессию белка р53 и р21, причем при более высоких концентрациях цисплатина (от 2 до 6 мкг/мл) происходит расщепление PARP (маркера апоптоза). Неожиданно было установлено, что в клетках, трансфектированных siPHK р53 происходит снижение индуцированной цисплатином экспрессии белка р53, что коррелирует с резким снижением экспрессии р21, расщеплением PARP и потерей жизнеспособности клеток. Такое же воздействие на экспрессию р53, экспрессию р21 и расщепление PARP обнаружено также при использовании двух других siPHK, мишенью которых является человеческий р53 (последовательности-мишени: 5'-GGAAGACTCCAGTGGТААТ-3' и 5'-GATАТТGAAСААTGGТТСА-3'). Эти данные однозначно подтверждают тот факт, что действие, приводящее к повышенной гибели клеток/апоптозу, вызываемое комбинациями цисплатина и ингибитора mTOR, обусловлено зависящими от р53 механизмами.
Пример 5
Несущие р53 (ТР53) дикого типа клетки линии А549 высевают с плотностью 0,1×106 клеток/5 мкл в чашки диаметром 6 см и инкубируют в течение 24 ч при 37°С и 5% СО2. Клетки оставляют нетрансфектированными или осуществляют кратковременную трансфекцию с использованием 100 нМ siPHK, мишенью которой является либо р21 (регистрационный номер: NM000389; последовательность-мишень: 5'-GTGGACAGCGAGCAGCTGA-3'), либо, как описано выше, контрольной siPHK LacZ с использованием олигофектамина (фирма Invitrogen, каталожный номер 12252-011). После инкубации в течение 30 ч клетки инкубируют с субоптимальными концентрациями цисплатина (например, от 1 до 2 мкг/мл) еще в течение 24 ч. Клеточные экстракты, соответствующие 30 мкг (р21) и 50 мкг (PARP) общего белка, подвергают электрофорезу в 15 и 10% ДСН-ПААГ соответственно и осуществляют анализ методом иммуноблоттинга с использованием мышиных моноклональных и кроличьих поликлональных антител к р21 и PARP соответственно. Обработка цисплатином нетрансфектированных или контрольных трансфектированных siPHK LacZ клеток индуцирует зависящую от концентрации экспрессию белка р53 и р21, причем расщепление PARP (маркер апоптоза) является слабо выраженным. Неожиданно было установлено, что в трансфектированных siPHK р21 клетках происходит ослабление индуцированной цисплатином экспрессии белка р21, что коррелирует с выраженной индукцией расщепления PARP. Эти данные однозначно подтверждают тот факт, что ослабление обусловленной цитотоксичностью экспрессии белка р21 приводит к действию, приводящему к повышенной гибели клеток/апоптозу, вызываемому комбинациями цисплатина и ингибитора mTOR.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОМАРКЕР | 2005 |
|
RU2385944C2 |
| ЛЕЧЕНИЕ НЕЙРОЭНДОКРИННЫХ ОПУХОЛЕЙ | 2006 |
|
RU2487711C2 |
| КОМБИНАЦИИ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2447891C2 |
| ПЕРЕНОС ГЕНОВ, ОПОСРЕДОВАННЫЙ ЛЕНТИВИРУСНЫМ ВЕКТОРОМ, И ИХ ИСПОЛЬЗОВАНИЕ | 2001 |
|
RU2288742C2 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА, АССОЦИИРОВАННОГО С ИНФЕКЦИЕЙ HPV | 2013 |
|
RU2636003C2 |
| ТЕРАПЕВТИЧЕСКИЕ, ДИАГНОСТИЧЕСКИЕ И ПРОГНОСТИЧЕСКИЕ СПОСОБЫ ДЛЯ РАКА МОЧЕВОГО ПУЗЫРЯ | 2015 |
|
RU2739942C2 |
| БИОМАРКЕРЫ, ПРОГНОЗИРУЮЩИЕ СПОСОБНОСТЬ К ТЕРАПЕВТИЧЕСКОМУ ОТВЕТУ НА ТЕРАПИЮ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2743657C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ МИОСТАТИНА, СОДЕРЖАЩИЕ ИХ КОМБИНАЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2781401C2 |
| ЛЕЧЕНИЕ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО РЕЦЕПТОРА АНТИГЕНА ПРОТИВ CD19 | 2015 |
|
RU2718542C2 |
| КОМБИНАЦИЯ ПИРИМИДИЛАМИНОБЕНЗАМИДА И ИНГИБИТОРА КИНАЗ mTOR | 2006 |
|
RU2443418C2 |


Настоящее изобретение относится к области молекулярной генетики и может быть использовано в медицине. Предлагается применение анализа статуса гена р53(ТР53) и/или уровня его экспрессии в качестве биомаркера при определении чувствительности индивидуума, страдающего пролиферативным заболеванием, к лечению ингибитором mTOR в сочетании с цитотоксическим агентом или при отборе чувствительных к указанной комбинированной терапии индивидуумов для последующего лечения заболевания этим методом. При этом чувствительность к лечению пролиферативного заболевания комбинацией ингибитора mTOR с цитотоксическим средством предсказывается при установлении наличия в образце, взятом у пациента, функционально активного гена р53 дикого типа. 3 н. и 11 з.п. ф-лы.
1. Применение определения статуса р53 (ТР53) у индивидуума, страдающего пролиферативным заболеванием, в качестве биомаркера для оценки чувствительности индивидуума к лечению ингибитором mTOR в сочетании с цитотоксическим агентом, при котором присутствие р53 дикого типа предсказывает чувствительность к лечению ингибитором mTOR в сочетании с цитотоксическим агентом.
2. Применение по п.1, которое заключается в использовании анализа гена р53 (ТР53) и уровня экспрессии/посттрансляционной модификации р53.
3. Применение по п.1, где пролиферативное заболевание представляет собой рак.
4. Применение по п.1, в котором ингибитор mTOR представляет собой рапамицин или производное рапамицина.
5. Применение по п.1, в котором производное рапамицина представляет собой 40-О-(2-гидроксиэтил)рапамицин, 40-[3-гидрокси-2-(гидроксиметил)-2-метилпропаноат]рапамицин или 40-эпи(тетразолил)рапамицин.
6. Применение по п.1, в котором цитотоксический агент выбирают из антинеопластического антиметаболита, содержащего платину соединения, алкилирующего агента, ингибитора топоизомеразы I или II, обладающего активностью в отношении микротрубок агента и радиационного облучения.
7. Способ определения чувствительности пролиферативного заболевания у индивидуума к комбинированной терапии с использованием ингибитора mTOR и цитотоксического агента, заключающийся в том, что определяют статус гена р53 (ТР53) и/или уровня экспрессии/посттрансляционной модификации р53 в образце, взятом из организма индивидуума, в котором присутствие р53 дикого типа предсказывает чувствительность к лечению ингибитором mTOR в сочетании с цитотоксическим агентом.
8. Способ по п.7, где пролиферативное заболевание представляет собой рак.
9. Способ по п.7, заключающийся в том, что определяют генетический статус р53 (ТР53) и/или уровень экспрессии р53.
10. Способ по п.7, в котором образец берут у индивидуума из опухоли.
11. Способ отбора индивидуумов, страдающих пролиферативным заболеванием, для комбинированной терапии с использованием ингибитора mTOR и цитотоксического агента, заключающийся в том, что определяют чувствительность пролиферативного заболевания к комбинированной терапии у каждого индивидуума с помощью способа, описанного в п.7, и отбирают для комбинированной терапии индивидуумов, имеющих статус р53 (ТР53) дикого типа.
12. Способ по п.7, в котором ингибитор mTOR представляет собой рапамицин или производное рапамицина.
13. Способ по п.7, в котором производное рапамицина представляет собой 40-О-(2-гидроксиэтил)рапамицин, 40-[3-гидрокси-2-(гидроксиметил)-2-метилпропаноат]рапамицин или 40-эпи(тетразолил)рапамицин.
14. Способ по п.7, в котором цитотоксический агент выбирают из антинеопластического антиметаболита, содержащего платину соединения, алкилирующего агента, ингибитора топоизомеразы I или II, обладающего активностью в отношении микротрубок агента и радиационного облучения.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| HUANG S | |||
| ET AL., Drug | |||
| Resist | |||
| Updat, 2001, 4(6), 378-391 PAGLIARO L | |||
| ET AL., Urol | |||
| Oncol., 2003, 21(6), 456-462 | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ РАКА | 1996 |
|
RU2174409C2 |
Авторы
Даты
2011-09-20—Публикация
2005-02-22—Подача