Родственные заявки
Настоящая заявка испрашивает приоритет в соответствии с 35 U.S.C. § 119(e) согласно предварительной заявке на патент США No. 62/856844, поданной 4 июня, 2019; предварительной заявке на патент США No. 62/932728, поданной 8 ноября, 2019; содержание которых полностью включено в настоящую заявку посредством ссылки.
Область техники, к которой относится изобретение
В настоящем документе представлены способы, композиции и наборы, относящиеся к композициям уриказы и/или композициям, содержащим синтетические наноносители, содержащие иммуносупрессант. В настоящем документе также представлены способы, композиции и наборы для лечения субъектов, включая субъектов с гиперурикемией, подагрой или состоянием, связанным с подагрой, и для предотвращения обострения подагры. Также в настоящем документе представлены способы идентификации субъекта для лечения, представленные в настоящем документе, а также способы мониторинга эффективности лечения. В некоторых вариантах осуществления, способы включают стадию (стадии) получения или определения титра антитела к уриказе у субъекта и/или сравнения титра антитела к уриказе с пороговым значением. В некоторых вариантах осуществления таких вариантов осуществления способы могут дополнительно включать любую из стадий или способов, представленных в настоящем документе, для лечения любого из субъектов, представленных в настоящем документе.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Выработка антител к лекарственным средствам (ADA) является частой причиной неэффективности биотерапевтического лечения и побочных аллергических реакций. Было продемонстрировано, что синтетические наноносители, содержащие иммуносупрессант, способны индуцировать иммунологическую толерантность к композиции, содержащей уриказу, что приводит к повышению эффективности композиции, содержащей уриказу. Повышенная эффективность была продемонстрирована, по меньшей мере, со значительно более высокой скоростью снижения уровня мочевой кислоты в сыворотке с течением времени по сравнению с другими видами лечения. Также было продемонстрировано, что синтетические наноносители, содержащие иммуносупрессант, при одновременном введении с композицией, содержащей уриказу, способны значительно снизить частоту обострения подагры по сравнению с другими видами лечения. Композиции, содержащие синтетические наноносители, содержащие иммуносупрессант, и композиции, содержащие уриказу, как представлено в настоящем документе, могут использоваться для эффективного и длительного (например, в течение по меньшей мере 30 дней) снижения уровней мочевой кислоты в сыворотке и/или уменьшения частоты обострений подагры.
Также было обнаружено, что использование уровня антител к уриказе у субъекта может быть полезным при лечении субъекта. Показателем антител к уриказе может быть титр антител к уриказе у субъекта. Показатель можно сравнить с пороговым значением. Таким образом, в настоящем документе представлены способы, включающие определение или получение уровня антител к уриказе у любого из субъектов, представленных в настоящем документе, например, в образце от субъекта, и/или сравнение уровня антител к уриказе у субъекта с пороговым значением. В любом из способов, представленных в настоящем документе, уровень антител к уриказе может быть выражен в виде титра. В любом из способов, представленных в настоящем документе, пороговым значением является титр менее примерно 1080. В любом из способов, представленных в настоящем документе, пороговое значение составляет примерно 1080. Любой из вышеперечисленных способов может также включать любую из нескольких стадий или любой из способов лечения, как представлено в настоящем документе.
Также в настоящем документе представлены способы, включающие введение субъекту, имеющему титр антител к уриказе ниже порогового значения, как представлено в настоящем документе, любой из композиций, содержащих уриказу, предоставленных в настоящем документе, отдельно или в комбинации с любой из композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, представленный в настоящем документе. Также в настоящем документе представлены способы предотвращения обострения подагры, включающие одновременное введение субъекту, имеющему титр антител к уриказе ниже порогового значения, композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и композиции, содержащей уриказу, такую как та, которую не вводят в качестве дополнительного терапевтического средства для предотвращения обострения подагры одновременно с совместным введением. В некоторых вариантах осуществления идентифицируют субъекта, как уже имевшего или у которого ожидается обострение подагры в результате лечения с помощью терапии подагры без сопутствующего введения дополнительного терапевтического средства для предотвращения обострения подагры. Субъект может нуждаться в этом. Субъект может быть любым из субъектов, описанных в настоящем документе.
В настоящем документе также представлены способы лечения субъекта, имеющего титр антител к уриказе ниже порогового значения, с подагрой или состоянием, связанным с подагрой, включающие введение любой из композиций, содержащих уриказу, представленных в настоящем документе, отдельно или в комбинации с любой из композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, представленных в настоящем документе. В одном варианте осуществления любого из способов, представленных в настоящем документе, композиции, содержащие уриказу, представленные в настоящем документе, отдельно или в комбинации с любой из композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, могут быть неоднократно введены субъекту. Субъект может нуждаться в этом. Субъект может быть любым из субъектов, описанных в настоящем документе.
В одном аспекте предлагается способ лечения человека-субъекта, страдающего подагрой или состоянием, связанным с подагрой, и имеющего титр антител к уриказе ниже порогового значения, включающий введение субъекту композиции, содержащей уриказу и фармацевтически приемлемый носитель. В одном варианте осуществления изобретения введение осуществляют не внутримышечным способом. В одном варианте осуществления композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят субъекту более одного раза. В одном варианте осуществления композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят субъекту более двух, более трех или более четырех раз. В одном варианте осуществления, композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят каждые две-четыре недели. В одном варианте осуществления композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят ежемесячно. В одном варианте осуществления композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят одновременно с композицией, содержащей иммуносупрессант.
В одном аспекте предлагается способ лечения субъекта с подагрой или состоянием, связанным с подагрой, и имеющего титр антител к уриказе ниже порогового значения, включающий одновременное введение субъекту композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и композиции, содержащей уриказу.
В настоящем документе также представлены способы лечения субъекта, имеющего титр антител к уриказе ниже порогового значения, у которого может возникнуть обострение подагры, включающие введение любой из композиций, содержащих уриказу, представленных в настоящем документе, в сочетании с любой из композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, представленных в настоящем документе. В одном аспекте способ предотвращения обострения подагры у субъекта, имеющего титр против уриказы ниже порогового значения, включающий одновременное введение субъекту композиции, содержащей синтетические наноносители, включающие иммуносупрессант, и композицию, содержащую уриказу. В одном варианте осуществления субъекту не вводят дополнительное терапевтическое средство для предотвращения обострения подагры, такое как лекарственное средство против обострения подагры, одновременно с совместным введением. В некоторых вариантах осуществления субъекту не вводят колхицин или НПВП одновременно с сопутствующим введением. В одном варианте осуществления идентифицируют субъекта, как уже имевшего или у которого ожидается обострение подагры в результате лечения с помощью терапии подагры, такой как терапевтическое средство, снижающее уровень мочевой кислоты. В одном варианте осуществления идентифицируют субъекта, как уже имевшего или у которого ожидается обострение подагры без сопутствующего введения дополнительного терапевтического средства для предотвращения обострения подагры.
В одном варианте осуществления любого из способов, представленных в настоящем документе, осуществляют идентификацию или мониторинг у субъекта наличия или поддержания уровня антител к уриказе (например, титра антител) ниже порогового значения. В одном варианте осуществления любого из способов, представленных в настоящем документе, лечебные дозы и/или частоту корректируют на основании идентификации или мониторинга. В одном варианте осуществления любого из способов, представленных в настоящем документе, способ дополнительно включает одну или несколько стадий для идентификации или мониторинга субъекта для определения уровня антител к уриказе (например, титра антител).
В одном варианте осуществления любого из способов, представленных в настоящем документе, сопутствующее введение у субъекта осуществляют более одного раза. В одном варианте осуществления любого из способов, представленных в настоящем документе, сопутствующее введение осуществляют по меньшей мере два раза (например, по меньшей мере три, четыре, пять, шесть, семь, восемь, девять или десять раз) у субъекта. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, и композицию, содержащую уриказу, вводят совместно каждые две-четыре недели. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, и композицию, содержащую уриказу, вводят ежемесячно одновременно. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, и композицию, содержащую уриказу, вводят ежемесячно в течение по меньшей мере трех месяцев (например, 4, 5, 6, 7, 7, 8, 9, 10 или более месяцев) одновременно.
В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую уриказу, вводят в указанной дозе 0,1 мг/кг - 1,2 мг/кг уриказы при каждом введении, например, при каждом сопутствующем введении. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую уриказу, вводят в указанной дозе 0,1 мг/кг, 0,2 мг/кг, 0,3 мг/кг, 0,4 мг/кг, 0,5 мг/кг, 0,6 мг/кг, 0,7 мг/кг, 0,8 мг/кг, 0,9 мг/кг, 1,0 мг/кг, 1,1 мг/кг или 1,2 мг/кг уриказы при каждом введении, например, при каждом сопутствующем введении. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую уриказу, вводят в указанной дозе 0,2-0,4 мг/кг уриказы при каждом введении, например, при каждом сопутствующем введении.
В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,05 мг/кг - 0,5 мг/кг иммуносупрессанта при каждом сопутствующем введении. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,05 мг/кг, 0,07 мг/кг, 0,075 мг/кг, 0,08 мг/кг, 0,1 мг/кг, 0,125 мг/кг, 0,15 мг/кг, 0,2 мг/кг, 0,25 мг/кг, 0,3 мг/кг, 0,35 мг/кг, 0,4 мг/кг, 0,45 мг/кг или 0,5 мг/кг иммуносупрессанта при каждом сопутствующем введении. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,075-0,2 мг/кг или 0,08-0,125 мг/кг иммуносупрессанта при каждом сопутствующем введении.
В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,5 мг/кг - 6,5 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,55 мг/кг, 0,6 мг/кг, 0,65 мг/кг, 0,7 мг/кг, 0,75 мг/кг, 0,8 мг/кг, 0,85 мг/кг, 0,9 мг/кг, 0,95 мг/кг, 1,0 мг/кг, 1,10 мг/кг 1,125 мг/кг, 1,5 мг/кг, 1,75 мг/кг, 2,0 мг/кг, 2,5 мг/кг, 3,0 мг/кг, 3,5 мг/кг, 4,0 мг/кг, 4,5 мг/кг, 5 мг/кг, 5,5 мг/кг, 6,0 мг/кг или 6,5 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,6-2,5 мг/кг, 0,7-2,5 мг/кг, 0,8-2,5 мг/кг, 0,9-2,5 мг/кг, 1,0-2,5 мг/кг, 1,5-2,5 мг/кг или 2,0-2,5 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,65-2,5 мг/кг, 0,65-2,0 мг/кг, 0,65-1,5 мг/кг или 0,65-1,0 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,75-2,0 мг/кг, 0,8-1,5 мг/кг, 0,9-1,5 мг/кг или 1-2 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в указанной дозе 0,9-2 мг/кг или 1-1,5 мг/кг при каждом сопутствующем введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант.
В одном варианте осуществления любого из способов, представленных в настоящем документе, способ дополнительно включает введение композиции, содержащей уриказу, субъекту по меньшей мере один раз (например, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более раз) после сопутствующего введения (введений) без сопутствующего введения дополнительного терапевтического средства, такого как композиция, содержащая иммуносупрессант, например, композиция, содержащая синтетические наноносители, содержащие иммуносупрессант. В одном варианте осуществления любого из способов, представленных в настоящем документе, способ дополнительно включает введение композиции, содержащей уриказу, по меньшей мере, дважды после сопутствующего введения (введений). В одном варианте осуществления любого из способов, представленных в настоящем документе, способ дополнительно включает введение композиции, содержащей уриказу, ежемесячно в течение двух месяцев после сопутствующего введения (введений) каждого введения без сопутствующего введения дополнительного терапевтического средства, такого как композиция, содержащая иммуносупрессант, такая как композиция, содержащая синтетические наноносители, содержащие иммуносупрессант. В некоторых вариантах осуществления, композицию, содержащую уриказу, вводят в указанной дозе 0,1-1,2 мг/кг уриказы при каждом введении после одного или нескольких одновременных введений без иммуносупрессанта. В некоторых вариантах осуществления, композицию, содержащую уриказу, вводят в указанной дозе 0,1 мг/кг, 0,2 мг/кг, 0,3 мг/кг, 0,4 мг/кг, 0,5 мг/кг, 0,6 мг/кг, 0,7 мг/кг, 0,8 мг/кг, 0,9 мг/кг, 1,0 мг/кг, 1,1 мг/кг, 1,2 мг/кг уриказы при каждом введении после одного или нескольких сопутствующих введений без иммуносупрессанта.
В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят до композиции, содержащей уриказу, например, при каждом сопутствующем введении. В одном варианте осуществления любого из способов, представленных в настоящем документе, композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, и композицию, содержащую уриказу, вводят с интервалом в один час друг от друга.
В одном варианте осуществления любого из способов, представленных в настоящем документе, субъекту не вводят дополнительное терапевтическое средство, такое как дополнительное лекарство от подагры, такое как средство для предотвращения обострения подагры
субъекту не вводят дополнительное терапевтическое средство, такое как дополнительное лекарство от подагры, такое как средство для предотвращения обострения подагры. В одном из вариантов осуществления этих вариантов осуществления дополнительное терапевтическое средство, такое как дополнительное терапевтическое средство для лечения подагры, такое как средство для предотвращения обострения подагры, не вводится одновременно при каждом сопутствующем введении.
Любой из способов, композиций или наборов, представленных в настоящем документе, может быть использован для лечения любого из субъектов, представленных в настоящем документе.
В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, субъект имеет повышенный уровень мочевой кислоты в сыворотке. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, у субъекта уровень мочевой кислоты в сыворотке составляет ≥5 мг/дл. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, у субъекта уровень мочевой кислоты в сыворотке составляет ≥6 мг/дл. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, у субъекта уровень мочевой кислоты в сыворотке составляет ≥7 мг/дл. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, субъект имеет или подвержен риску возникновения гиперурикемии; острой подагры; хронической подагры с тофусами или без них; идиопатической подагры; рефрактерной подагры; вторичной подагры; неуточненной подагры; подагры, связанной с сердечно-сосудистым заболеванием, заболеванием почек, заболеванием легких, неврологическим заболеванием, заболеванием глаз, дерматологическим заболеванием или заболеванием печени; или у него был приступ подагры или обострение подагры. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, ожидается, что у субъекта возникнет обострение подагры в результате лечения с помощью терапии подагры, такой как терапевтическое средство, снижающее уровень мочевой кислоты, такое как композиция, содержащая уриказу. В одном варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, у субъекта подагра, имеющая по меньшей мере одно из а) тофусы, b) обострение подагры в течение последних 6 месяцев и c) хроническая подагрическая артропатия.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, уриказа представляет собой пегилированную уриказу. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, пегилированная уриказа представляет собой пегситиказу или пеглотиказу. В одном варианте осуществления любого из способов, представленных в настоящем документе, пегилированная уриказа представляет собой пегситиказу.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, иммуносупрессант инкапсулирован в синтетических наноносителях.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, иммуносупрессант представляет собой ингибитор mTOR. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, ингибитор mTOR представляет собой рапалог. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, рапалог представляет собой рапамицин.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, синтетические наноносители представляют собой полимерные синтетические наноносители. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, полимерные синтетические наноносители содержат гидрофобный полиэфир. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, гидрофобный полиэфир включает PLA, PLG, PLGA или поликапролактон. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, полимерные синтетические наноносители дополнительно включают PEG. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, PEG конъюгирован с PLA, PLG, PLGA или поликапролактоном. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, полимерные синтетические наноносители включают PLA, PLG, PLGA или поликапролактон и PEG, конъюгированный с PLA, PLG, PLGA или поликапролактоном. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, полимерные синтетические наноносители включают PLA и PLA-PEG. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, синтетические наноносители представляют собой такие, которые описаны или могут быть получены любым из приведенных в качестве примеров способов, представленных в настоящем документе.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, среднее значение распределения частиц по размерам, полученное с использованием динамического рассеяния света синтетических наноносителей, составляет диаметр более 120 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет более 150 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет более 200 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет более 250 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет менее 300 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет менее 250 нм. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, диаметр составляет менее 200 нм.
В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта синтетических наноносителей составляет 7-12% или 8-12% масс. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта синтетических наноносителей составляет 7-10% или 8-10% масс. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта синтетических наноносителей составляет 9-11% масс. В одном варианте осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта синтетических наноносителей составляет 7%, 8%, 9%, 10%, 11% или 12% масс.
В одном варианте осуществления любого из способов, представленных в настоящем документе, каждое введение представляет собой внутривенное введение. В одном варианте осуществления любого из способов, представленных в настоящем документе, внутривенное введение представляет собой внутривенную инфузию.
В одном варианте осуществления любого из способов, представленных в настоящем документе, способ дополнительно включает введение субъекту дополнительного терапевтического средства. В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительное терапевтическое средство представляет собой противовоспалительное средство, такое как кортикостероид. В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительное терапевтическое средство представляет собой терапевтическое средство для лечения подагры, такое как пероральное терапевтическое средство для лечения подагры. В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительное терапевтическое средство вводится впоследствии. В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительное терапевтическое средство вводят после завершения лечения с совместным введением композиции (композиций) уриказы и композиции (композиций) синтетических наноносителей, например, в соответствии с любой из схем, представленных в настоящем документе.
В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительная терапия представляет собой терапию против обострения подагры. В одном варианте осуществления любого из способов, представленных в настоящем документе, терапию против обострения подагры представляет собой профилактическое лечение, проводимое одновременно, но до введения каждой вводимой композиции уриказы, например, в соответствии с любой из схем, представленных в настоящем документе. В одном варианте осуществления любого из способов, представленных в настоящем документе, терапия против обострения подагры представляет собой колхицин или НПВП.
В одном варианте осуществления любого из способов, представленных в настоящем документе, дополнительное терапевтическое средство представляет собой кортикостероид, и кортикостероид вводят одновременно, например, одновременно перед введением каждой вводимой композиции уриказы, например, в соответствии с любой из схем, представленных в настоящем документе.
В другом аспекте способ включает введение любому из субъектов, описанных в настоящем документе, композиции, содержащей уриказу в любой из доз, включая указанные дозы, и фармацевтически приемлемый носитель один или несколько раз (например, 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более раз). В некоторых вариантах осуществления, по меньшей мере одно введение или каждое введение осуществляется не внутримышечным способом введения. В некоторых примерах по меньшей мере одно введение или каждое введение представляет собой внутривенное введение, такое как внутривенная инфузия. В некоторых вариантах осуществления, композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят каждые две или четыре недели. В некоторых вариантах осуществления, композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят ежемесячно. В некоторых вариантах осуществления композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят одновременно с любой из композиций, содержащих иммуносупрессант, описанный в настоящем документе.
В одном аспекте представлена композиция или набор, включающий одну или несколько композиций, содержащих только уриказу или в комбинации с одной или несколькими композициями, содержащими синтетические наноносители, содержащие иммуносупрессант. Каждая композиция, содержащая уриказу, может быть любой из композиций, содержащих уриказу, как указано в настоящем документе, в любой из композиций или наборов. Каждая композиция, содержащая уриказу, может находиться в количестве, таком, чтобы она обеспечивала любую одну или несколько доз, включая указанные дозы, уриказы, как указано в настоящем документе, в любой из композиций или наборов. Каждая композиция, содержащая уриказу, может быть в лиофилизированной форме в любой из композиций или наборов. Каждая композиция, содержащая синтетические наноносители, содержащие иммуносупрессант, может быть любой из композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, как указано в настоящем документе, в любой из композиций или наборов. Каждая композиция, содержащая синтетические наноносители, содержащие иммуносупрессант, может находиться в таком количестве, чтобы обеспечивать любую одну или несколько доз, включая указанные дозы синтетических наноносителей, содержащих иммуносупрессант, или иммуносупрессанта, как представлено в настоящем документе в любой из композиций или наборов. Каждая композиция, содержащая синтетические наноносители, содержащие иммуносупрессант, может быть в лиофилизированной форме в любой из композиций или наборов. Каждая композиция, содержащая синтетические наноносители, содержащие иммуносупрессант, может находиться в замороженной суспензии в любой из композиций или наборов. В одном варианте осуществления любой из композиций или наборов замороженная суспензия дополнительно содержит фосфатно-солевой буферный раствор (PBS). В одном варианте осуществления любой из композиций или наборов лиофилизированная форма дополнительно содержит PBS и/или маннит. В одном варианте осуществления любой из композиций или наборов, композиция или набор дополнительно содержит 0,9% хлорид натрия, USP.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 представлено изображение, показывающее тофусы/отложения мочевой кислоты, визуализированные с помощью DECT.
На фиг. 2 представлено изображение в виде рисунка компонентов SEL-212.
На фиг. 3 представлен график уровней ADA у нечеловеческих приматов после лечения пустыми наноносителями+пегситиказа или пегситиказа+0,1Х или 1Х синтетические наноносители, содержащие рапамицин (SVP-рапамицин).
На фиг. 4 представлен график средних уровней мочевой кислоты в сыворотке (sUA) в 5 когортах фазы 1а клинического исследования после однократного внутривенной инфузии пегситиказы.
На фиг. 5 представлена графическая иллюстрация, показывающая уровни мочевой кислоты в сыворотке и уровни уриказа-специфических ADA для каждого субъекта в когорте #3 фазы 1a клинического исследования и когорте #9, когорте #4 и когорте #6 в фазы 1b клинического исследования.
На фиг. 6 представлен график, показывающий уровни мочевой кислоты в сыворотке когорты #3 из клинической фазы 1а и когорты #9, когорты #1, когорты #2, когорты #3, когорты #4, когорты #5 и когорты #6 из фазы 1b клинического исследования.
На фиг. 7 слева направо показаны данные двух повторных испытаний Kystexxa®, в середине представлены данные только SVP-рапамицин vs. только пегситиказа (когорта #9) и затем только рапамицин vs. когорта #6 (когорта SEL-212).
На фиг. 8 представлена графическая иллюстрация, показывающая уровни мочевой кислоты в сыворотке у субъектов, получавших только пегститиказу или в сочетании с синтетическими наноносителями, содержащими рапамицин (SVP-рапамицин) (0,1 или 0,3 мг/кг).
На фиг. 9 показаны дозы для фазы 2 клинического исследования.
На фиг. 10 представлен график, иллюстрирующий титры антител к уриказе. В этом случае периоды лечения без ответа имели титры 1080 или более.
На фиг. 11 представлен график, иллюстрирующий титры антител к уриказе. Те, что меньше 1:1080, имели повышенную устойчивую активность уриказы.
На фиг. 12A-12B показаны результаты с пятью ежемесячными дозами рапамицин-содержащих наноносителей, вводимых совместно с 0,2 мг/кг пегадриказы. На фиг. 12A показаны различные дозы рапамицин-содержащих наноносителей и на фиг. 12B показаны различные комбинации введений концентраций рапамицин-содержащих наноносителей.
На фиг. 13A-13D показано, что увеличение титра антител к уриказе приводит к более низкой активности уриказы (фиг. 13A-13B), в то время как увеличение концентрации рапамицин-содержащего наноносителя приводит к более высокой устойчивой активности уриказы (фиг. 13C-13D). На фиг. 13A и 13C, использовали дозы 0,2 мг/кг пегадриказы; на фиг. 13B и 13D, использовали дозы 0,4 мг/кг пегадриказы.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
A. Общие сведения
Подагра может быть болезненной и приводить к инвалидности, и считается, что она возникает из-за избытка мочевой кислоты. Кроме того, высокие концентрации мочевой кислоты, такие как мочевая кислота в сыворотке крови, могут увеличить риск сопутствующих заболеваний, включая сердечно-сосудистые, кардиометаболические, заболевания суставов и почек. В США и Европейском Союзе насчитывается примерно 8,3 миллиона и 10 миллионов людей, страдающих подагрой, соответственно.
На основании исследований и данных, примеры которых представлены выше и в других местах в настоящем документе, было продемонстрировано, что представленные композиции и способы являются существенно более эффективными, чем доступные в настоящее время методы лечения, могут снижать нежелательные иммунные реакции, связанные с доставкой уриказы, такой как пегилированная уриказа, могут обеспечивать значительный и длительный контроль уровней мочевой кислоты в сыворотке крови у пациентов, могут обеспечивать удаление болезненных и повреждающих отложений мочевой кислоты у пациентов, например, с хронической тофусной подагрой, и/или могут существенно снизить или устранить риск обострения подагры, которое может возникнуть при терапии, снижающей уровень мочевой кислоты, такой как уриказа.
Также было продемонстрировано, что использование показателя антител к уриказе у субъекта может быть полезным при идентификации субъекта для лечения или для оценки лечения субъекта. Показателем антител к уриказе может быть титр анти-уриказы у субъекта. Этот показатель можно сравнить с пороговым значением и принять решение о лечении.
B. ОПРЕДЕЛЕНИЯ
«Дополнительное терапевтическое средство», как используется в настоящем описании, относится к любому терапевтическому средству, которое используется в дополнение к другому лечению. Например, когда способ направлен на лечение синтетическими наноносителями, содержащими иммуносупрессант, и способ включает использование дополнительного терапевтического средства, дополнительное терапевтическое средство является дополнением к синтетическим наноносителям, содержащим иммуносупрессант. В качестве другого примера, когда способ направлен на лечение комбинацией композиции, содержащей уриказу, и композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и способ включает использование дополнительного терапевтического средства, дополнительное терапевтическое средство является дополнением к комбинации композиции уриказы и синтетических наноносителей. Как правило, дополнительное терапевтическое средство будет другим терапевтическим средством. Дополнительное терапевтическое средство можно вводить в то же время или в другое время и/или с помощью того же способа введения или с помощью другого способа введения, что и другое терапевтическое средство. В предпочтительных вариантах осуществления дополнительное терапевтическое средство будет вводиться одновременно и таким образом, чтобы обеспечить пользу субъекту во время окна эффективного лечения другим терапевтическим средством. Когда две композиции вводят с определенным периодом времени, обычно период времени измеряется от начала первой композиции до начала второй композиции. Как используется в настоящем документе, когда две композиции вводятся в течение часа, например, время до начала введения первой композиции составляет примерно час до начала введения второй композиции.
В некоторых вариантах осуществления дополнительное терапевтическое средство представляет собой другое терапевтическое средство для лечения подагры или состояния, связанного с подагрой. Как используется в настоящем документе, «терапевтическое средство для лечения подагры» означает любое терапевтическое средство, которое можно вводить и от которого субъект с подагрой может извлечь пользу при его введении. В некоторых вариантах осуществления, терапевтическое средство для лечения подагры представляет собой пероральное терапевтическое средство для лечения подагры (т.е. терапевтическое средство для лечения подагры, которое можно принимать или вводить перорально).
Дополнительным терапевтическим средством может быть любое из ранее одобренных терапевтических средств, описанных в настоящем документе или иным образом известных в данной области. В некоторых вариантах осуществления, дополнительное терапевтическое средство представляет собой терапевтическое средство, снижающее уровень мочевой кислоты. Таким терапевтическим средством является любое, которое приводит к более низкому уровню мочевой кислоты в сыворотке у субъекта по сравнению с уровнем мочевой кислоты в сыворотке без введения терапевтического средства. Такие терапевтические средства, снижающие уровень мочевой кислоты, включают, уриказы.
В некоторых вариантах осуществления дополнительное терапевтическое средство представляет собой терапевтическое средство для предотвращения обострения подагры или также называемое в настоящем документе лекарственным средством против обострения подагры. Любое терапевтическое средство, которое можно использовать для предотвращения обострения подагры, включено в этот класс терапевтических средств. В некоторых из этих вариантов осуществления терапевтическое средство для предотвращения обострения подагры вводится до введения другого терапевтического средства. В некоторых вариантах осуществления, терапевтическим средством для предотвращения обострения подагры является колхицин. В других вариантах осуществления терапевтическим средством для предотвращения обострения подагры является НПВП.
В варианте осуществления любой из способов лечения любого из субъектов или любой из композиций или наборов, как представлено в настоящем документе, может включать введение дополнительного терапевтического или дополнительного терапевтического средства, соответственно. В другом варианте осуществления, любой из способов лечения любого из субъектов или любой из композиций или наборов, как представлено в настоящем документе, не включает введение дополнительного терапевтического средства, например, в пределах окна эффективного лечения другого терапевтического средства, или дополнительного терапевтического средства, соответственно.
«Введение», или «применение», или «вводить» означает предоставление материала субъекту таким образом, чтобы у субъекта был фармакологический результат. Это может быть прямое или непрямое введение, такое как побуждение или указание другому субъекту, включая другого врача или самого субъекта, выполнить введение.
«Эффективное количество» в контексте композиции или дозы для введения субъекту относится к количеству композиции или дозы, которое вызывает один или несколько желаемых ответов у субъекта. В некоторых вариантах осуществления, эффективное количество является фармакодинамически эффективным количеством. Следовательно, в некоторых вариантах осуществления, эффективным количеством является любое количество композиции или дозы, представленной в настоящем документе, которое вызывает один или несколько желаемых терапевтических эффектов и/или иммунных ответов, как представлено в настоящем документе. Это количество может быть использовано для целей in vitro или in vivo. Для целей in vivo количество может быть таким, которое, по мнению врача, может принести клиническую пользу нуждающемуся в этом субъекту. Любая из композиций или доз, включая указанные дозы, как представлено в настоящем документе, может быть в эффективном количестве.
Эффективные количества могут включать снижение уровня нежелательной реакции, хотя в некоторых вариантах осуществления это включает полное предотвращение нежелательной реакции. Эффективные количества могут также включать задержку возникновения нежелательной реакции. Количество, которое является эффективным, также может быть количеством, которое обеспечивает желаемую терапевтическую конечную точку или желаемый терапевтический результат. В других вариантах осуществления, эффективные количества могут включать повышение уровня желаемого ответа, такого как терапевтическая конечная точка или результат. Эффективные количества, предпочтительно, приводят к терапевтическому результату или конечной точке и/или уменьшают или устраняют ADA по отношению к лечению и/или приводят к предотвращению обострения подагры у любого из субъектов, представленных в настоящем документе. Достижение любого из вышеперечисленных можно контролировать обычными способами.
Эффективные количества, конечно, будут зависеть от конкретного субъекта, подвергаемого лечению; тяжести состояния, заболевания или расстройства; индивидуальных параметров пациента, включая возраст, физическое состояние, размер и массу; продолжительность лечения; характер сопутствующей терапии (при ее наличии); конкретный способ введения и подобные факторы в пределах знаний и опыта практикующего врача. Эти факторы хорошо известны специалистам в данной области, и они могут быть учтены с помощью обычных экспериментов. Как правило, предпочтительно использовать максимальную дозу, то есть самую высокую безопасную дозу в соответствии со здравым медицинским заключением. Однако специалистам в данной области будет понятно, что пациент может настаивать на более низкой дозе или переносимой дозе по медицинским причинам, психологическим причинам или практически по любой другой причине.
Дозы компонентов в любой из композиций по настоящему изобретению или используемые в любом из способов по настоящему изобретению могут относиться к количеству компонентов в композиции, фактическим количествам соответствующих компонентов, полученных субъектом для введения, или количеству, которое указано на этикетке (также называемое в настоящем документе указанной дозой). Дозу можно вводить в зависимости от количества синтетических наноносителей, которые обеспечивают желаемое количество компонента(ов).
«Присоединять», или «присоединенный», или «соединять», или «связанный» (и тому подобное) означает химическое связывание одной структурной единицы (например, фрагмент) с другой. В некоторых вариантах осуществления, присоединение является ковалентным, что означает, что присоединение происходит в смысле наличия ковалентной связи между двумя структурными единицами. В нековалентных вариантах осуществления нековалентное присоединение опосредуется нековалентными взаимодействиями, включая, но не ограничиваясь этим, взаимодействия зарядов, аффинные взаимодействия, координацию металлов, физическую адсорбцию, взаимодействия гость-хозяин, гидрофобные взаимодействия, TT стэкинг-взаимодействия, водород-связывающие взаимодействия, ван-дер-ваальсовы взаимодействия, магнитные взаимодействия, электростатические взаимодействия, диполь-дипольные взаимодействия и/или их комбинации. В вариантах осуществления инкапсуляция является формой присоединения.
«Среднее», как используется в настоящем документе, относится к среднему арифметическому, если не указано иное.
«Совместно» означает введение субъекту двух или более веществ/средств способом, который коррелирован во времени, предпочтительно достаточно коррелирован во времени, чтобы обеспечить модуляцию физиологического или иммунологического ответа, и еще более предпочтительно два или несколько веществ/средств вводят в комбинации. В вариантах осуществления сопутствующее введение может включать введение двух или более веществ/средств в пределах определенного периода времени, предпочтительно в пределах 1 месяца, более предпочтительно в пределах 1 недели, еще более предпочтительно в пределах 1 дня и даже более предпочтительно в пределах 1 часа. В вариантах осуществления два или несколько веществ/средств вводят последовательно. В вариантах осуществления вещества/средства можно многократно вводить совместно; то есть сопутствующее введение более одного раза.
«Доза» относится к определенному количеству фармакологически активного вещества для введения субъекту в течение определенного времени. Если не указано иное, дозы, указанные для композиций, содержащих пегилированную уриказу, относятся к массе уриказы (т.е. белка без массы PEG или любых других компонентов композиции, содержащей пегилированную уриказу). Кроме того, если не указано иное, дозы, указанные для композиций, содержащих синтетические наноносители, содержащие иммуносупрессант, относятся к массе иммуносупрессанта (т.е. без учета массы вещества синтетического наноносителя или любого из других компонентов композиции синтетического наноносителя). Что касается дозы для введения, в варианте осуществления любого из способов, композиций или наборов, представленных в настоящем документе, любая из представленных в настоящем документе доз представляет собой дозу, указанную на этикетке/указанную дозу.
«Инкапсулировать» означает заключать по меньшей мере часть вещества внутрь синтетического наноносителя. В некоторых вариантах осуществления, вещество полностью заключено внутрь синтетического наноносителя. В других вариантах осуществления, большая часть или все инкапсулированное вещество не подвергается воздействию окружающей среды, внешней по отношению к синтетическому наноносителю. В других вариантах осуществления, не более 50%, 40%, 30%, 20%, 10% или 5% (масс./масс.) подвергается воздействию окружающей среды. Инкапсуляция отличается от абсорбции, при которой большая часть или все вещество помещается на поверхность синтетического наноносителя, и вещество остается доступным для местной окружающей среды, внешней по отношению к синтетическому наноносителю. В вариантах осуществления любого из способов или композиций, представленных в настоящем документе, иммуносупрессанты инкапсулируют внутри синтетических наноносителей.
«Повышенный уровень мочевой кислоты в сыворотке» относится к любому уровню мочевой кислоты в сыворотке субъекта, который может привести к нежелательному результату или будет считаться врачом повышенным. В одном варианте осуществления субъект любого из способов, представленных в настоящем документе, может иметь уровень мочевой кислоты в сыворотке ≥5 мг/дл, ≥6 мг/дл или ≥7 мг/дл. Такой субъект может быть субъектом с гиперуремией. Имеет ли субъект повышенный уровень мочевой кислоты в крови или нет, может определить врач-клиницист, и в некоторых вариантах осуществления, субъект является субъектом, у которого врач идентифицировал или думает, что идентифицирует повышенные уровни мочевой кислоты в сыворотке.
«Подагра» обычно относится к расстройству или состоянию, связанному с накоплением мочевой кислоты, такому как отложение кристаллов мочевой кислоты в тканях и суставах, и/или клинически значимому повышенному уровню мочевой кислоты в сыворотке. Накопление мочевой кислоты может быть связано с повышенной выработкой мочевой кислоты или снижением выведения мочевой кислоты. Подагра может изменяться от бессимптомных до тяжелых и болезненных воспалительных состояний. «Состояние, связанное с подагрой» относится к любому состоянию у субъекта, при котором субъект испытывает местные и/или системные эффекты подагры, включая воспаление и иммунные ответы, и при котором состояние вызвано или усугубляется, или состояние может привести к или усугубить, подагру. Обострение подагры представляет собой «приступ» или обострение симптомов подагры, которое может произойти в любой момент. Обострения подагры могут включать обострения подагры, которые возникают после назначения терапии, снижающей уровень мочевой кислоты.
«Гидрофобный полиэфир» относится к любому полимеру, который содержит один или несколько полиэфирных полимеров или их звеньев и который имеет гидрофобные характеристики. Полимеры на основе сложного полиэфира включают, но не ограничиваются ими, PLA, PLGA, PLG и поликапролактон. «Гидрофобный» относится к веществу, который по существу не участвует в водородной связи с водой. Такие вещества обычно неполярны, в основном неполярны или имеют нейтральный заряд. Синтетические наноносители могут полностью состоять из гидрофобных сложных полиэфиров или их звеньев. В некоторых вариантах осуществления, однако синтетические наноносители включают гидрофобные полиэфиры или их звенья в сочетании с другими полимерами или их звеньями. Эти другие полимеры или их звенья могут быть гидрофобными, но не обязательно таковыми. В некоторых предпочтительных вариантах осуществления, когда синтетические наноносители включают один или несколько других полимеров или их звеньев в дополнение к гидрофобному полиэфиру, матрица других полимеров или их звеньев с гидрофобным полиэфиром в целом является гидрофобной. Примеры синтетических наноносителей, которые могут быть использованы в изобретении и которые содержат гидрофобные полиэфиры, можно найти в публикациях США No. US 2016/0128986 и US 2016/0128987, и такие синтетические наноносители и описание таких синтетических наноносителей включены в настоящий документ посредством ссылки.
«Иммуносупрессант», как используется в настоящем документе, означает соединение, которое может вызывать толерогенный иммунный ответ, специфичный к антигену, также называемый в настоящем документе «иммуносупрессивным эффектом». Иммуносупрессивный эффект обычно относится к продукции или экспрессии цитокинов или других факторов антигенпрезентирующей клеткой (APC), которая снижает, ингибирует или предотвращает нежелательный иммунный ответ или которая способствует желаемому иммунному ответу, например регуляторному иммунному ответу, против специфического антигена. Когда APC приобретает иммуносупрессивную функцию (при иммуносупрессивном воздействии) на иммунные клетки, которые распознают антиген, представленный этим APC, говорят, что иммуносупрессивный эффект специфичен для представленного антигена. Примеры иммуносупрессантов включают «ингибиторы mTOR», класс лекарственных средств, которые ингибируют mTOR, серин/треонин-специфическую протеинкиназу, которая относится к семейству фосфатидилинозитол-3 киназ (PI3K), связанных с киназами (PIKK). Примеры иммуносупрессантов включают «ингибиторы mTOR», класс лекарств, которые ингибируют mTOR, серин/треонин-специфическую протеинкиназу, которая принадлежит к семейству фосфатидилинозитол-3-киназ (PI3K), родственных киназам (PIKK). Ингибиторы mTOR включают, но не ограничиваются ими, рапалоги, такие как рапамицин, а также АТФ-конкурентные ингибиторы киназы mTOR, такие как двойные ингибиторы mTORC1/mTORC2.
В вариантах осуществления любого из способов, композиций или наборов, представленных в настоящем документе, иммуносупрессанты, представленные в настоящем документе, прикреплены к синтетическим наноносителям. В предпочтительных вариантах осуществления иммуносупрессант представляет собой элемент, который является дополнением к веществу, составляющему структуру синтетического наноносителя. Например, в одном варианте осуществления, где синтетический наноноситель состоит из одного или нескольких полимеров, иммуносупрессант представляет собой соединение, которое дополнительно и присоединено к одному или нескольким полимерам. В вариантах осуществления, например, когда вещество синтетического наноносителя также приводит к иммуносупрессивному эффекту, иммуносупрессант представляет собой элемент, присутствующий в дополнение к веществу синтетического наноносителя, который приводит к иммуносупрессивному эффекту.
«Нагрузка», когда она содержится в композиции, содержащей синтетический наноноситель, например, связанный с ним, представляет собой количество иммуносупрессанта в композиции, основанное на общей сухой рецептурной массе веществ во всем синтетическом наноносителе (масс./масс.). Обычно такая нагрузка рассчитывается как среднее значение по популяции синтетических наноносителей. В одном варианте осуществления средняя нагрузка на синтетические наноносители составляет от 0,1% до 15%. В другом варианте осуществления нагрузка составляет от 0,1% до 10%. В другом варианте осуществления нагрузка составляет от 1% до 15%. В еще другом варианте осуществления нагрузка составляет от 5% до 15%. В еще одном варианте осуществления нагрузка составляет от 7% до 12%. В еще одном варианте осуществления нагрузка составляет от 8% до 12%. В еще одном варианте осуществления нагрузка составляет от 7% до 10%. В еще одном варианте осуществления нагрузка составляет от 8% до 10%. В еще одном варианте осуществления нагрузка составляет 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14% или 15% в среднем по популяции синтетических наноносителей. В любом из способов, композиций или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта, такого как рапамицин, может быть любой из нагрузок, представленных в настоящем документе.
Нагрузка рапамицина наноносителя в суспензии рассчитывается путем деления содержания рапамицина в наноносителе, определенного с помощью анализа ВЭЖХ исследуемого образца, на массу наноносителя. Общее содержание полимера измеряется либо путем гравиметрического выхода массы сухого наноносителя, либо путем определения общего содержания органических веществ в растворе наноносителя в соответствии с методами фармакопии и с поправкой на содержание PVA.
«Максимальный размер синтетического наноносителя» означает наибольший размер синтетического наноносителя, измеренный вдоль любой оси синтетического наноносителя. Например, для сфероидального синтетического наноносителя максимальный и минимальный размер синтетического наноносителя будет практически одинаковым и будет размером его диаметра. Аналогично, для кубоидального синтетического наноносителя минимальный размер синтетического наноносителя будет наименьшим из его высоты, ширины или длины, в то время как максимальный размер синтетического наноносителя будет наибольшим из его высоты, ширины или длины. В одном варианте осуществления минимальный размер по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% синтетических наноносителей в образце, исходя из общего количества синтетических наноносителей в образце, равен или более 100 нм. В варианте осуществления максимальный размер по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% синтетических наноносителей в образце, основанный на общем количестве синтетических наноносителей в образце, равен или менее 5 мкм. Предпочтительно, минимальный размер по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% синтетических наноносителей в образце, основанный на общем количестве синтетических наноносителей в образце, превышает 110 нм, более предпочтительно превышает 120 нм, более предпочтительно превышает 130 нм и еще более предпочтительно превышает 150 нм. Аспектные соотношения максимальных и минимальных размеров синтетических наноносителей могут варьироваться в зависимости от варианта осуществления. Например, соотношение сторон максимальных и минимальных размеров синтетических наноносителей может варьироваться от 1:1 до 1000000:1, предпочтительно от 1:1 до 100000:1, более предпочтительно от 1:1 до 10000:1, более предпочтительно от 1:1 до 1000:1, еще более предпочтительно от 1:1 до 100:1 и еще наиболее предпочтительно от 1:1 до 10:1.
Предпочтительно, максимальный размер по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% синтетических наноносителей в образце, основанный на общем количестве синтетических наноносителей в образце, равен или меньше 3 мкм, более предпочтительно равен или меньше 2 мкм, более предпочтительно равен или меньше 1 мкм, более предпочтительно равен или меньше 800 нм, более предпочтительно равен или меньше 600 нм, и более предпочтительно еще равен или меньше 500 нм. В предпочтительных вариантах осуществления минимальный размер по меньшей мере 75%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90% синтетических наноносителей в образце, исходя из общего количества синтетических наноносителей в образце, равен или более 100 нм, более предпочтительно равно или более 120 нм, более предпочтительно равно или более 130 нм, более предпочтительно равен или более 140 нм и еще более предпочтительно равен или более 150 нм. Измерение размеров синтетических наноносителей (например, эффективного диаметра) может быть получено, в некоторых вариантах осуществления, путем суспендирования синтетических наноносителей в жидкой (обычно водной) среде и с использованием динамического рассеяния света (DLS) (например, с помощью оборудования Brookhaven ZetaPALS). Например, суспензия синтетических наноносителей может быть разбавлена из водного буфера очищенной водой для достижения конечной концентрации суспензии синтетических наноносителей приблизительно от 0,01 до 0,5 мг/мл. Разбавленная суспензия может быть приготовлена непосредственно внутри или перенесена в подходящую кювету для анализа DLS. Затем кювету можно поместить в DLS, дать ей уравновеситься до контролируемой температуры, а затем сканировать в течение достаточного времени для получения стабильного и воспроизводимого распределения на основе соответствующих входных данных для вязкости среды и лучепреломляющих показателей образца. Затем регистрируется эффективный диаметр или среднее значение распределения. Определение эффективных размеров синтетических наноносителей с высоким соотношением сторон или несфероидальной формы может потребовать дополнительных методов, таких как электронная микроскопия, для получения более точных измерений. «Величина», или «размер», или «диаметр» синтетических наноносителей означает среднее значение распределения частиц по размерам, например, полученное с помощью динамического рассеяния света.
«Получение», как используется в настоящем документе, относится к любому способу, с помощью которого можно получить соответствующую информацию или вещества. Таким образом, соответствующая информация может быть получена экспериментальными методами. Соответствующие вещества могут быть созданы, спроектированы и т.п. с помощью различных экспериментальных или лабораторных способов, в некоторых вариантах осуществления. Соответствующая информация или вещества также могут быть получены путем предоставления или обеспечения информации, например, в отчете или материалов.
«Пегилированная уриказа» относится к любой уриказе, которая присоединена к одной или нескольким молекулам PEG (поли (этиленгликоль), поли (этиленоксид) или поли (оксиэтилен)) (например, поли (этиленгликоль), поли(этиленоксид) или поли (оксиэтилен) полимер или его звено). Предпочтительно, в некоторых вариантах осуществления, одна или несколько молекул PEG представляют собой молекулы поли(этиленгликоля). Термины «пегилированный» или «пегилирование» относятся к конъюгированной форме или процессу конъюгирования с уриказой, соответственно. Такая модифицированная уриказа называется пегилированной уриказой. Пегилированные уриказы включают, но не ограничиваются ими, пегситиказу и пеглотиказу (KRYSTEXXA®).
«Фармацевтически приемлемый эксципиент» или «фармацевтически приемлемый носитель» означает фармакологически неактивное вещество, используемое вместе с фармакологически активным веществом для формулирования композиций. Фармацевтически приемлемые эксципиенты включают различные вещества, известные в данной области, включая, но не ограничиваясь ими, сахариды (такие как глюкоза, лактоза и т.п.), консерванты, такие как противомикробные агенты, вспомогательные вещества для восстановления, красители, физиологический раствор (такой как фосфатный забуференный физиологический раствор) и буферы. Любая из композиций, представленных в настоящем документе, может включать фармацевтически приемлемый эксципиент или носитель.
«Рапалог» относится к рапамицину и молекулам, которые структурно родственны (аналог) рапамицину (сиролимус) и предпочтительно являются гидрофобными. Примеры рапалогов включают, без ограничения, темсиролимус (CCI-779), дефоролимус, эверолимус (RAD001), ридафоролимус (AP-23573), зотаролимус (ABT-578). Дополнительные примеры рапалогов можно найти, например, в публикации WO WO 1998/002441 и патенте США No. 8455510, описание таких рапалогов включено в настоящий документ посредством ссылки в полном объеме. В любом из способов, или композиций, или наборов, представленных в настоящем документе, иммуносупрессант может представлять собой рапалог.
«Субъект» означает животных, включая теплокровных млекопитающих, таких как люди и приматы; птиц; домашних или сельскохозяйственных животных, таких как кошки, собаки, овцы, козы, крупный рогатый скот, лошади и свиньи; лабораторных животных, таких как мыши, крысы и морские свинки; рыб; рептилий; животных зоопарка и диких животных; и тому подобное. В любом из способов, композиций и наборов, представленных в настоящем документе, субъектом является человек. В любом из способов, композиций и наборов, представленных в настоящем документе, субъектом является любой из субъектов, представленных в настоящем документе, например субъект, у которого имеется одно из состояний, указанных в настоящем документе, например подагра или другое состояние, связанное с подагрой.
«Синтетический наноноситель(наноносители)» означает дискретный объект, не встречающийся в природе, и имеющий по меньшей мере один размер, который меньше или равен 5 микронам. Синтетические наноносители могут иметь множество различных форм, включая, но не ограничиваясь ими, сфероидальную, кубоидальную, пирамидальную, продолговатую, цилиндрическую, тороидальную и тому подобное. Синтетические наноносители содержат одну или несколько поверхностей.
Синтетическим наноносителем может быть, но не ограничивается этим, одна или несколько наночастиц на основе липидов (также называемых здесь липидными наночастицами, т.е. наночастицами, в которых большая часть материала, составляющего их структуру, является липидами), полимерных наночастиц, металлических наночастиц, эмульсий на основе поверхностно-активных веществ, дендримеров, бакиболов, нанопроволок, вирусоподобных частиц (т.е. частиц, которые в основном состоят из вирусных структурных белков, но которые не являются инфекционными или обладают низкой инфекционностью), частиц на основе пептидов или белков (также называемых в настоящем документе частицами белка, т.е. частицы, где большая часть вещества, составляющего их структуру, представляет собой пептиды или белки) (такие как наночастицы альбумина) и/или наночастиц, которые разработаны с использованием комбинации наноматериалов, таких как липид-полимерные наночастицы. Синтетические наноносители могут иметь множество различных форм, включая, помимо прочего, сфероидальную, кубоидальную, пирамидальную, продолговатую, цилиндрическую, тороидальную и т.п. Примеры синтетических наноносителей включают (1) биоразлагаемые наночастицы, описанные в патенте США 5543158 на Gref et al., (2) полимерные наночастицы из опубликованной заявки на патент США 20060002852 на Saltzman et al., (3) литографически сконструированные наночастицы из опубликованной заявки на патент США 20090028910 на DeSimone et al., (4) раскрытие WO 2009/051837 на von Andrian et al., (5) наночастицы, раскрытые в опубликованной заявке на патент США 2008/0145441 на Penades et al., (6) нанопреципитированные наночастицы, раскрытые в P. Paolicelli et al., «Surface-modified PLGA-based Nanoparticles that can Efficiently Associate and Deliver Virus-like Particles» Nanomedicine. 5(6):843-853 (2010), и (7) таковые из Look et al., «Nanogel-based delivery of mycophenolic acid ameliorates systemic lupus erythematosus in mice» J. Clinical Investigation 123(4):1741-1749(2013).
Синтетические наноносители могут иметь минимальный размер, равный или менее примерно 100 нм, предпочтительно равный или менее 100 нм, не содержат поверхности с гидроксильными группами, которые активируют комплемент, или, альтернативно, содержат поверхность, которая состоит в основном из фрагментов, которые не являются гидроксильными группами, активирующими комплемент. В одном варианте осуществления синтетические наноносители, которые имеют минимальный размер, равный или менее примерно 100 нм, предпочтительно равный или менее 100 нм, не содержат поверхности, которая существенно активирует комплемент, или, альтернативно, содержат поверхность, которая состоит по существу из фрагментов, которые существенно не активируют комплемент. В более предпочтительном варианте осуществления синтетические наноносители в соответствии с изобретением, которые имеют минимальный размер, равный или менее примерно 100 нм, предпочтительно равный или менее 100 нм, не содержат поверхность, которая активирует комплемент, или, альтернативно, содержат поверхность, которая состоит в основном из фрагментов, которые не активируют комплемент. В вариантах осуществления синтетические наноносители не включают вирусоподобные частицы. В вариантах осуществления синтетические наноносители могут иметь аспектное соотношение более 1:1, 1:1,2, 1:1,5, 1:2, 1:3, 1:5, 1:7, или более 1:10.
«Лечение» относится к введению одного или нескольких терапевтических средств с ожиданием, что субъект может получить положительный эффект в результате введения. Лечение может также привести к профилактике состояния, как представлено в настоящем документе, и, следовательно, лечение включает профилактическое лечение. При профилактическом использовании субъектом является субъект, у которого врач ожидает, что существует вероятность развития состояния или другого нежелательного ответа, как предусмотрено в настоящем документе. В некоторых вариантах осуществления, субъект, у которого ожидается обострение подагры, является субъектом, у которого врач считает, что существует вероятность возникновения обострения подагры. Лечение может быть прямым или косвенным, например, путем побуждения или направления другого субъекта, включая другого врача или самого субъекта, для лечения субъекта.
«Масс.%» или «% масс.» относится к соотношению одной массы к другой массе, умноженному на 100. Например, %масс. могут быть отношением массы одного компонента к другому, умноженным на 100, или отношение массы одного компонента к общей массе более одного компонента, умноженной на 100. Как правило, %масс. измеряется как среднее значение по популяции синтетических наноносителей или как среднее значение по синтетическим наноносителям в композиции или суспензии.
C. СПОСОБЫ И РОДСТВЕННЫЕ КОМПОЗИЦИИ
Уриказа и пегилированная уриказа
Способы, композиции и наборы, описанные в настоящем документе, включают композиции, содержащие уриказу. Обычно считается, что уриказа катализирует превращение мочевой кислоты в аллантоин, который растворим и может выводиться из организма. Уриказа представляет собой фермент, эндогенный для всех млекопитающих, за исключением человека и некоторых приматов. Ген, кодирующий фермент уриказу, может быть получен из любого источника, известного в данной области, включая источники из млекопитающих и микробов, а также с помощью рекомбинантных и синтетических технологий. Как очевидно специалисту в данной области, ген может быть получен из источника и рекомбинантно (или трансгенно) экспрессирован и продуцирован в другом организме с использованием стандартных методов. См. Erlich, H A, (Ed.) (1989) PCR Technology. Principles and Applications for DNA Amplification. New York: Stockton Press; Sambrook, J, et al., (1989) Molecular Cloning. A Laboratory Manual, Second Edition. Cold Spring Harbor, N.Y.: Cold Spring Harbor Laboratory Press. Например, в патенте США No. 5700674 описано рекомбинантное получение уриказы в клетках E. coli. В некоторых вариантах осуществления, фермент продуцируется ферментацией в E. coli.
В некоторых вариантах осуществления, ген, кодирующий уриказу, или ее часть, получают от млекопитающего, например, свиньи, крупного рогатого скота, овцы, козы, павиана, обезьяны мыши, кролика или домашнего животного. В некоторых вариантах осуществления, ген, кодирующий уриказу, или ее часть, получают из микроорганизма, такого как бактерии или грибы (включая дрожжи). В некоторых вариантах осуществления, ген, кодирующий уриказу, получают из бактериального источника, такого как бактерия, принадлежащая к Streptomyces spp., Bacillus spp. или E. coli. В некоторых вариантах осуществления, ген, кодирующий уриказу, получают из грибкового (включая дрожжи) источника, такого как Candida (например, Candida utilis), Anthrobacter (например, Anthrobacter globiformis), Saccharomyces, Schizosaccaromyces, Emericella, Aspergillus (например, Aspergillus flavus), и Neurospora spp. В некоторых вариантах осуществления, уриказа получена из Candida utilis. В некоторых вариантах осуществления, уриказа представляет собой пегситиказу (3SBio как описано в патенте США No. 6913915, и такая уриказа и ее описание включены в настоящий документ посредством ссылки). В некоторых вариантах осуществления, уриказа получена из Aspergillus flavus. В некоторых вариантах осуществления, уриказа представляет собой расбуриказу (ELITEK®; FASTURTEC®, от Sanofi Genzyme).
В некоторых вариантах осуществления, уриказа представляет собой химерную уриказу, в которой части гена, кодирующего уриказу, получены из разных источников. Например, часть гена, кодирующего химерную уриказу, может быть получена из одного организма, и одна или несколько других частей гена, кодирующего химерную уриказу, могут быть получены из другого организма. В некоторых вариантах осуществления, часть гена, кодирующего химерную уриказу, получена от свиньи, а другая часть гена, кодирующего химерную уриказу, получена от бабуина. В некоторых вариантах осуществления, химерная уриказа представляет собой пеглотиказа/KRYSTEXXA®.
Также в рамках настоящего изобретения возможны варианты уриказ, которые могут включать одну или несколько мутаций (замены, вставки, делеции). В нуклеотидной последовательности, кодирующей белок уриказы, могут быть внесены мутации, которые могут приводить или не приводить к аминокислотной мутации. В общем, могут быть сделаны мутации, например, для увеличения продукции белка, оборота/периода полужизни белка или мРНК, кодирующей белок, модуляции (усиления или снижения) ферментативной активности уриказы.
В других вариантах осуществления, ген, кодирующий уриказу, получают из растений или беспозвоночных, таких как Drosophila или C. elegans.
Любой из белков уриказы, описанных в настоящем документе, может быть пегилирован. Уриказа может быть ковалентно связана с PEG через биосовместимую связывающую группу с использованием способов, известных в данной области, как описано, например, Park et al., Anticancer Res., 1:373-376 (1981); и Zaplipsky and Lee, Polyethylene Glycol Chemistry: Biotechnical and Biomedical Applications, J. M. Harris, ed., Plenum Press, New York, Chapter 21 (1992). Связывающая группа, используемая для ковалентного присоединения PEG к уриказе, может быть любой биосовместимой связывающей группой, что означает, что связывающая группа нетоксична и может быть использована in vitro или in vivo, не вызывая побочных эффектов. Альтернативно, PEG может быть непосредственно конъюгирован с уриказой, например, непосредственно с остатком лизина уриказы.
Уриказа может быть пегилирована во многих различных аминокислотных остатках белка уриказы. Количество молекул PEG и/или остатков, с которыми конъюгирован PEG, может влиять на активность уриказы. В некоторых вариантах осуществления пегилированная уриказа включает по меньшей мере одну молекулу PEG. В некоторых вариантах осуществления пегилированная уриказа включает в среднем по меньшей мере 2, 3, 4, 5, 6, 7,8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33,34, 35, 36, 37, 38, 39, 40, 45, 50, или более молекул PEG в расчете на белок уриказы. В некоторых вариантах осуществления, пегилированная уриказа включает примерно 20-25 молекул PEG на белок уриказы.
В среднем PEG имеет молекулярную массу от 5 кДа до 100 кДа. Как молекулярная масса (размер) используемого PEG, так и количество молекул PEG, используемых для пегилирования уриказы, могут варьироваться. В некоторых вариантах осуществления средняя молекулярная масса PEG составляет от 5 кДа до 100 кДа, 5 кДа - 75 кДа, 5 кДа - 50 кДа, 5 кДа to 30 кДа, 5 кДа - 20 кДа, 5 кДа - 10 кДа, 10 кДа - 75 кДа, 10 кДа - 50 кДа, 10 кДа - 30 кДа, 5 кДа - 30 кДа, 15 кДа - 50 кДа, 15 кДа - 30 кДа, 15 кДа - 25 кДа, 20 кДа - 75 кДа, 30 кДа - 80 кДа, 30 кДа - 70 кДа или 30 кДа - 50 кДа. В некоторых вариантах осуществления молекулярная масса PEG составляет примерно 5 кДа, 6 кДа, 7 кДа, 8 кДа, 9 кДа, 10 кДа, 11 кДа, 12 кДа, 13 кДа, 14 кДа, 15 кДа, 16 кДа, 17 кДа, 18 кДа, 19 кДа, 20 кДа, 21 кДа, 22 кДа, 23 кДа, 24 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа, 55 кДа, 60 кДа, 65 кДа, 70 кДа, 75 кДа, 80 кДа, 85 кДа, 90 кДа, 95 кДа или 100 кДа. В общем, PEG называют на основе молекулярной массы PEG. Например, PEG-20 относится к молекулам PEG с молекулярной массой 20 кДа, и PEG-5 относится к молекулам PEG с молекулярной массой 5 кДа. В некоторых вариантах осуществления, уриказа пегилирована молекулами PEG с молекулярной массой 20 кДа (PEG-20).
Пегилированные уриказы включают, без ограничения, пегситиказу (доступную от 3Sbio, и как описано в патенте США No. 6913915, и такая пегилированная уриказа и ее описание включены в настоящий документ посредством ссылки) и пеглотиказа/KRYSTEXXA® (Horizon Pharmaceuticals).
Предпочтительно, в некоторых вариантах осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, пегилированная уриказа представляет собой пегситиказу, рекомбинантную уриказу, конъюгированную с множеством молекул поли(этиленгликоля) с молекулярной массой 20 кДа. Уриказный компонент пегситиказы может быть клонирован из дрожжей Candida utilis и экспрессирован в E. coli для продуцирования.
Активность уриказы в катализе мочевой кислоты, включая пегилированную уриказу, может быть оценена с использованием способов, известных в данной области техники, или иным образом, представленным в настоящем документе.
Синтетические наноносители
Могут быть использованы различные синтетические наноносители. В некоторых вариантах осуществления синтетические наноносители представляют собой сферы или сфероиды. В некоторых вариантах осуществления синтетические наноносители имеют плоскую или пластинчатую форму. В некоторых вариантах осуществления синтетические наноносители являются кубами или кубическими. В некоторых вариантах осуществления, синтетические наноносители представляют собой овалы или эллипсы. В некоторых вариантах осуществления синтетические наноносители представляют собой цилиндры, конусы или пирамиды.
В некоторых вариантах осуществления желательно использовать популяцию синтетических наноносителей, которая относительно однородна с точки зрения размера или формы, чтобы каждый синтетический наноноситель обладал аналогичными свойствами. Например, по меньшей мере 80%, по меньшей мере 90% или по меньшей мере 95% синтетических наноносителей, исходя из общего числа синтетических наноносителей, могут иметь минимальный размер или максимальный размер, который находится в пределах 5%, 10% или 20% от среднего диаметра или среднего размера синтетических наноносителей.
Синтетические наноносители могут быть сплошными или полыми и могут включать один или несколько слоев. В некоторых вариантах осуществления, каждый слой имеет уникальную композицию и уникальные свойства по сравнению с другими слоями. Для примера, синтетические наноносители могут иметь структуру ядро/оболочка, в которой ядро представляет собой один слой (например, полимерное ядро), а оболочка представляет собой второй слой (например, липидный бислой или монослой). Синтетические наноносители могут включать множество различных слоев.
В предпочтительных вариантах осуществления синтетические наноносители включают полимер, как представлено в настоящем документе. Полимеры могут быть природными полимерами или полимерами не природного происхождения (синтетическими). Полимеры могут быть гомополимерами или сополимерами, включающими два или несколько мономеров. С точки зрения последовательности сополимеры могут быть случайными, блочными или содержать комбинацию случайных и блочных последовательностей. Как правило, полимеры в соответствии с настоящим изобретением представляют собой органические полимеры.
Синтетические наноносители, как представлено в настоящем документе, предпочтительно включают гидрофобные полиэфиры. Такие сложные полиэфиры могут включать сополимеры, содержащие звенья молочной кислоты и гликолевой кислоты, такие как поли(молочная кислота-со-гликолевая кислота) и поли(лактид-со-гликолид), совместно называемые в настоящем документе «PLGA»; и гомополимеры, содержащие звенья гликолевой кислоты, называемые в настоящем документе «PGA», и звенья молочной кислоты, такие как поли-L-молочная кислота, поли-D-молочная кислота, поли-D, L-молочная кислота, поли-L-лактид, поли-D-лактид и поли-D, L-лактид, совместно называемые в настоящем документе «PLA». В некоторых вариантах осуществления, полиэфиры, приводимые в качестве примера, включают, например, полигидроксикислоты; PEG сополимеры и сополимеры лактида и гликолида (например, сополимеры PLA-PEG, сополимеры PGA-PEG, сополимеры PLGA-PEG и их производные. В некоторых вариантах осуществления, полиэфиры включают, например, поли(капролактон), поли(капролактон)-PEG сополимеры, поли(L-лактид-co-L-лизин), поли(сериновый эфир), поли(сложный эфир 4-гидрокси-L-пролина), поли[α-(4-аминобутил)-L-гликолевую кислоту] и их производные.
В некоторых вариантах осуществления, полиэфир может представлять собой PLGA. PLGA представляет собой биосовместимый и биоразлагаемый сополимер молочной кислоты и гликолевой кислоты, и различные формы PLGA характеризуются соотношением молочная кислота:гликолевая кислота. Молочная кислота может быть L-молочной кислотой, D-молочной кислотой или D, L-молочной кислотой. Скорость разрушения PLGA можно устанавливать путем изменения соотношения молочная кислота:гликолевая кислота. В некоторых вариантах осуществления, PLGA, используемый в соответствии с настоящим изобретением, может быть охарактеризован соотношением молочная кислота:гликолевая кислота приблизительно 85:15, приблизительно 75:25, приблизительно 60:40, приблизительно 50:50, приблизительно 40:60, приблизительно 25:75 или приблизительно 15:85.
Синтетические наноносители могут включать один или несколько неполиэфирных полимеров или их блоков, которые также являются гидрофобными, и/или полимеров или их блоков, которые не являются гидрофобными. В некоторых вариантах осуществления, предпочтительно, чтобы синтетический наноноситель в целом содержал гидрофобный полиэфир и, в некоторых вариантах осуществления, сам был гидрофобным.
Синтетические наноносители могут включать один или несколько полимеров, которые являются плюроновым полимером без концевых метоксигрупп или его звеном. «Полимер без концевых метоксигрупп» означает полимер, который имеет по меньшей мере один конец, который заканчивается остатком, отличным от метокси. В некоторых вариантах осуществления полимер имеет по меньшей мере два конца, которые заканчиваются фрагментом, отличным от метокси. В других вариантах осуществления полимер не имеет концов, которые заканчиваются метокси. «Плюроновый полимер без концевой метоксигруппы» означает полимер, отличный от линейного плюронового полимера с метоксигруппой на обоих концах.
Синтетические наноносители могут включать, в некоторых вариантах осуществления, полигидроксиалканоаты, полиамиды, простые полиэфиры, полиолефины, полиакрилаты, поликарбонаты, полистирол, силиконы, фторполимеры или их звенья. Дополнительные примеры полимеров, которые могут содержаться в синтетических наноносителях, представленных в настоящем документе, включают поликарбонат, полиамид или полиэфир, или их звено. В других вариантах осуществления полимеры синтетических наноносителей могут включать поли(этиленгликоль) (PEG), полипропиленгликоль или их звено.
В некоторых вариантах осуществления, предпочтительно, чтобы синтетические наноносители включали полимер, который является биоразлагаемым. Следовательно, в таких вариантах осуществления полимеры синтетических наноносителей могут включать простой полиэфир, такой как поли(этиленгликоль) или полипропиленгликоль, или их звено. Кроме того, полимер может включать блок-сополимер простого полиэфира и биоразлагаемого полимера, так что полимер является биоразлагаемым. В других вариантах осуществления полимер не содержит исключительно простой полиэфир или его звено, такой как поли(этиленгликоль) или полипропиленгликоль, или его звено.
В некоторых вариантах осуществления, полимеры в соответствии с настоящим изобретением включают полимеры, одобренные для использования на людях Управлением по контролю за продуктами и лекарствами США (FDA) в соответствии с 21 C.F.R. § 177.2600.
Другие примеры полимеров, подходящих для использования в синтетических наноносителях, включают, но не ограничиваются ими, полиэтилены, поликарбонаты (например, поли(1,3-диоксан-2он)), полиангидриды (например, поли(себациновый ангидрид)), полипропилфумераты, полиамиды (например, поликапролактам), полиацетали, простые полиэфиры, сложные полиэфиры (например, полилактид, полигликолид, полиактид-со-гликолид, поликапролактон, полигидроксикислоту (например, поли(β-гидроксиалканоат))), поли(ортоэфиры), полицианоакрилаты, поливиниловые спирты, полиуретаны, полифосфазены, полиакрилаты, полиметакрилаты, полимочевины, полистиролы и полиамины, полилизин, сополимеры полилизин-PEG, и поли(этиленимин), поли(этиленимин)-PEG сополимеры.
Еще другие примеры полимеров, которые могут быть включены в синтетические наноносители, включают акриловые полимеры, например сополимеры акриловой кислоты и метакриловой кислоты, сополимеры метилметакрилата, этоксиэтилметакрилаты, цианоэтилметакрилат, сополимер аминоалкилметакрилата, поли(акриловая кислота), поли(метакриловая кислота), сополимер алкиламида и метакриловой кислоты, поли(метилметакрилат), поли(ангидрид метакриловой кислоты), метилметакрилат, полиметакрилат, сополимер поли(метилметакрилата), полиакриламид, аминоалкилметакрилатный сополимер, сополимеры глицидилметакрилата, полицианоакрилаты и комбинации, содержащие один или несколько из вышеперечисленных полимеров.
В некоторых вариантах осуществления полимеры синтетического наноносителя объединяются с образованием полимерной матрицы. Традиционно известно большое разнообразие полимеров и способов формирования из них полимерных матриц. В некоторых вариантах осуществления синтетический наноноситель, содержащий гидрофобный полиэфир, имеет гидрофобную среду внутри синтетического наноносителя.
В некоторых вариантах осуществления, полимеры можно модифицировать одним или несколькими фрагментами и/или функциональными группами. В соответствии с настоящим изобретением можно использовать различные фрагменты или функциональные группы. В некоторых вариантах осуществления, полимеры могут быть модифицированы полиэтиленгликолем (PEG), углеводом и/или ациклическими полиацеталами, полученными из полисахаридов (Papisov, 2001, ACS Symposium Series, 786:301). Определенные варианты осуществления могут быть осуществлены с использованием основных идей патента США No. 5543158, Gref et al., или публикации WO WO2009/051837, Von Andrian et al.
В некоторых вариантах осуществления, полимеры могут быть модифицированы группой липидов или жирных кислот. В некоторых вариантах осуществления, группа жирных кислот может быть одной или несколькими из масляной, капроновой, каприловой, каприновой, лауриновой, миристиновой, пальмитиновой, стеариновой, арахидовой, бегеновой или лигноцериновой кислоты. В некоторых вариантах осуществления группа жирных кислот может представлять собой одну или несколько из пальмитолеиновой, олеиновой, вакценовой, линолевой, альфа-линолевой, гамма-линолевой, арахидоновой, гадолеиновой, арахидоновой, эйкозапентаеновой, докозагексаеновой или эруковой кислоты.
В некоторых вариантах осуществления, полимеры могут быть линейными или разветвленными полимерами. В некоторых вариантах осуществления полимеры могут быть дендримерами. В некоторых вариантах осуществления полимеры могут быть существенно сшиты друг с другом. В некоторых вариантах осуществления полимеры могут практически не содержать поперечных связей. В некоторых вариантах осуществления полимеры можно использовать в соответствии с настоящим изобретением без прохождения стадии сшивания. Кроме того, следует понимать, что синтетические наноносители могут включать блок-сополимеры, привитые сополимеры, комплексы, смеси и/или аддукты любого из вышеперечисленных и других полимеров. Специалистам в данной области понятно, что полимеры, перечисленные в настоящем документе, представляют собой примерный, а не полный список полимеров, которые могут быть использованы в соответствии с настоящим изобретением, при условии, что они соответствуют желаемым критериям.
Свойства этих и других полимеров и способы их получения хорошо известны в данной области техники (см., например, патенты США 6123727; 5804178; 5770417; 5736372; 5716404; 6095148; 5837752; 5902599; 5696175; 5514378; 5512600; 5399665; 5019379; 5010167; 4806621; 4638045; и 4946929; Wang et al., 2001, J. Am. Chem. Soc., 123:9480; Lim et al., 2001, J. Am. Chem. Soc., 123:2460; Langer, 2000, Acc. Chem. Res., 33:94; Langer, 1999, J. Control. Release, 62:7; b Uhrich et al., 1999, Chem. Rev., 99:3181). В более общем плане различные способы синтеза определенных подходящих полимеров описаны в Concise Encyclopedia of Polymer Science and Polymeric Amines and Ammonium Salts, Ed. by Goethals, Pergamon Press, 1980; Principles of Polymerization by Odian, John Wiley & Sons, Fourth Edition, 2004; Contemporary Polymer Chemistry by Allcock et al., Prentice-Hall, 1981; Deming et al., 1997, Nature, 390:386; и в патентах США 6506577, 6632922, 6686446 и 6818732.
Синтетические наноносители могут быть получены с использованием широкого спектра способов, известных в данной области. Например, синтетические наноносители могут быть получены такими способами, как нанопреципитация, фокусировка потока с использованием жидкостных каналов, распылительная сушка, испарение растворителя в одинарной и двойной эмульсии, экстракция растворителем, разделение фаз, измельчение (включая криоизмельчение), обработка с помощью сверхкритической жидкости (например, жидкий диоксид углерода), процедуры с микроэмульсией, микрообработка, нанообработка, защитные слои, простая и сложная коацервация и другими способами, хорошо известными специалистам в данной области. Альтернативно или дополнительно, описаны синтезы водных и органических растворителей для монодисперсных полупроводниковых, проводящих, магнитных, органических и других наноматериалов (Pellegrino et al., 2005, Small, 1:48; Murray et al., 2000, Ann. Rev. Mat. Sci., 30:545; and Trindade et al., 2001, Chem. Mat., 13:3843). Дополнительные способы описаны в литературе (см., например, Doubrow, Ed., «Microcapsules and Nanoparticles in Medicine and Pharmacy» CRC Press, Boca Raton, 1992; Mathiowitz et al., 1987, J. Control. Release, 5:13; Mathiowitz et al., 1987, Reactive Polymers, 6:275; и Mathiowitz et al., 1988, J. Appl. Polymer Sci., 35:755; патенты США 5578325 и 6007845; P. Paolicelli et al., «Surface-modified PLGA-based Nanoparticles that can Efficiently Associate and Deliver Virus-like Particles» Nanomedicine. 5(6):843-853 (2010)).
При желании иммуносупрессанты могут быть инкапсулированы в синтетические наноносители с использованием различных способов, включая, но не ограничиваясь ими, C. Astete et al., «Synthesis and characterization of PLGA nanoparticles» J. Biomater. Sci. Polymer Edn, Vol. 17, No. 3, pp. 247-289 (2006); K. Avgoustakis «Pegylated Poly(Lactide) and Poly(Lactide-Co-Glycolide) Nanoparticles: Preparation, Properties and Possible Applications in Drug Delivery» Current Drug Delivery 1:321-333 (2004); C. Reis et al., «Nanoencapsulation I. Methods for preparation of drug-loaded polymeric nanoparticles» Nanomedicine 2:8-21 (2006); P. Paolicelli et al., №Surface-modified PLGA-based Nanoparticles that can Efficiently Associate and Deliver Virus-like Particles» Nanomedicine. 5(6):843-853 (2010). Могут быть использованы другие способы, подходящие для инкапсуляции веществ в синтетические наноносители, включая, без ограничения, способы, раскрытые в патенте США 6632671, Unger issued October 14, 2003.
В определенных вариантах осуществления синтетические наноносители получают с помощью процесса нанопреципитации или распылительной сушки. Условия, используемые при получении синтетических наноносителей, могут быть изменены для получения частиц желаемого размера или свойств (например, гидрофобности, гидрофильности, внешней морфологии, «вязкости», формы и т.п.). Способ получения синтетических наноносителей и используемые условия (например, растворитель, температура, концентрация, скорость воздушного потока и т.п.) могут зависеть от веществ, которые должны быть включены в синтетические наноносители, и/или композиции матрицы носителя.
Если синтетические наноносители, полученные любым из вышеперечисленных способов, имеют диапазон размеров за пределами желаемого диапазона, такие синтетические наноносители можно калибровать, например, с помощью сита.
Предпочтительно, в некоторых вариантах осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, синтетические наноносители представляют собой синтетические наноносители, состоящие из PLA и PLA-PEG. PLA является частью более широкого семейства поли(молочная со гликолевая кислота), или PLGA, биоразлагаемых полимеров, которые имеют коммерческое использование более 30 лет и входят в состав ряда одобренных продуктов. Полиэтиленгликоль, или PEG, широко изучался в клинических исследованиях и также является компонентом рецептуры многих одобренных биологических продуктов.
В качестве примеров синтетические наноносители, содержащие рапамицин, являются теми, которые получены или могут быть получены одним из следующих способов:
1) PLA с характеристической вязкостью 0,41 дл/г приобретали в Evonik Industries (Rellinghauser Straße 1-11 45128 Essen, Germany), код продукта Resomer Select 100 DL 4A. Блок-сополимер PLA-PEG-OMe с блоком PEG с концевыми группами метилового эфира приблизительно 5000 Да и общей характеристической вязкостью 0,50 дл/г приобретали у Evonik Industries (Rellinghauser Straße 1-11 45128 Essen, Germany), код продукта Resomer Select 100 DL mPEG 5000 (15% масс. PEG). Рапамицин приобретали у Concord Biotech Limited (1482-1486 Trasad Road, Dholka 382225, Ahmedabad India), код продукта SIROLIMUS. EMPROVE® Поливиниловый спирт 4-88, USP (85-89% гидролизованный, вязкость 3,4-4,6 мПа·с) приобретали у MilliporeSigma (EMD Millipore, 290 Concord Road Billerica, Massachusetts 01821), код продукта 1.41350. Физиологический раствор, забуференный фосфатом Дульбекко 1X (DPBS) приобретали у Lonza (Muenchensteinerstrasse 38, CH-4002 Basel, Switzerland), код продукта 17-512Q. Сорбитан монопальмитат приобретали у Croda International (300-A Columbus Circle, Edison, NJ 08837), код продукта SPAN 40. Растворы получали следующим образом. Раствор 1 получали растворением PLA при 150 мг/мл и PLA-PEG-Ome при 50 мг/мл в дихлорметане. Раствор 2 получали растворением рапамицина при 100 мг/мл в дихлорметане. Раствор 3 получали растворением SPAN 40 при 50 мг/мл в дихлорметане. Раствор 4 получали растворением PVA при 75 мг/мл в 100 мМ фосфатном буфере pH 8. Эмульсии типа «масло в воде» получали путем добавления раствора 1 (0,50 мл), раствора 2 (0,12 мл), раствора 3 (0,10 мл) и дихлорметана (0,28 мл) в толстостенную стеклянную пробирку под давлением. Затем объединенные растворы органической фазы смешивали повторным пипетированием. К этой смеси добавляли раствор 4 (3 мл). Затем пробирку высокого давления перемешивали на вортексе в течение 10 секунд. Затем сырую эмульсию гомогенизировали обработкой ультразвуком с амплитудой 30% в течение 1 минуты с использованием ультразвукового устройства Branson Digital Sonifier 250 с коническим наконечником 1/8 дюйма и напорной трубки, погруженной в ванну с ледяной водой. Затем эмульсию добавляли в стакан 50 мл, содержащий DPBS (30 мл). Это перемешивают при комнатной температуре в течение 2 часов, чтобы дихлорметан испарился и образовались наноносители. Часть наноносителей промывали путем переноса суспензии наноносителя в центрифужную пробирку и центрифугирования при 75,600×g при 4°C в течение 50 минут, удаления супернатанта и ресуспендирования осадка в DPBS, содержащем 0,25% масс./об. PVA. Процедуру промывки повторяли, и осадок повторно суспендирвали в DPBS, содержащем 0,25% мас./об. PVA, для получения суспензии наноносителя, имеющей номинальную концентрацию 10 мг/мл в расчете на полимер. Затем суспензию наноносителя фильтровали с использованием шприцевого фильтра с мембраной PES 0,22 мкм от MilliporeSigma (EMD Millipore, 290 Concord Rd. Billerica MA, код продукта SLGP033RB). Отфильтрованную суспензию наноносителя хранили при -20°C.
2) PLA с характеристической вязкостью 0,41 дл/г приобретали в Evonik Industries (Rellinghauser Straße 1-11 45128 Essen, Germany), код продукта Resomer Select 100 DL 4A. Блок-сополимер PLA-PEG-OMe с блоком PEG с концевыми группами метилового эфира приблизительно 5000 Да и общей характеристической вязкостью 0,50 дл/г приобретали у Evonik Industries (Rellinghauser Straße 1-11 45128 Essen, Germany), код продукта Resomer Select 100 DL mPEG 5000 (15% масс. PEG). Рапамицин приобретали у Concord Biotech Limited (1482-1486 Trasad Road, Dholka 382225, Ahmedabad India), код продукта SIROLIMUS. Сорбитан монопальмитат приобретали у Sigma-Aldrich (3050 Spruce St., St. Louis, MO 63103), код продукта 388920. EMPROVE® Поливиниловый спирт (PVA) 4-88, USP (85-89% гидролизованный, вязкость 3,4-4,6 мПа⋅с) приобретали у MilliporeSigma (EMD Millipore, 290 Concord Road Billerica, Massachusetts 01821), код продукта 1.41350. Физиологический раствор, забуференный фосфатом Дульбекко 1X (DPBS) приобретали у Lonza (Muenchensteinerstrasse 38, CH-4002 Basel, Switzerland), код продукта 17-512Q. Растворы получали следующим образом: Раствор 1: Смесь полимера, рапамицина и сорбитан монопальмитата получали растворением PLA при 37,5 мг/мл, PLA-PEG-Ome при 12,5 мг/мл, рапамицина при 8 мг/мл, и сорбитан монопальмитат при 2,5 в дихлорметане. Раствор 2: Поливиниловый спирт получали при 50 мг/мл в 100 мМ фосфатном буфере с pH 8. Эмульсию масло-в-воде получали путем объединения раствора 1 (1,0 мл) и раствора 2 (3 мл) в небольшой стеклянной пробирке под давлением, и перемешивали на вортексе в течение 10 секунд. Затем композицию гомогенизировали обработкой ультразвуком с амплитудой 30% в течение 1 минуты с использованием ультразвукового устройства Branson Digital Sonifier 250 с коническим наконечником 1/8 дюйма, напорной трубки, погруженной в ванну с ледяной водой. Затем эмульсию добавляли в стакан 50 мл, содержащий DPBS (15 мл), и накрывали алюминиевой фольгой. Вторую эмульсию типа «масло-в-воде» получали с использованием тех же веществ и того же способа, что и выше, и затем добавляли в тот же химический стакан с использованием свежей аликвоты DPBS (15 мл). Затем объединенную эмульсию оставляют открытой и перемешивали при комнатной температуре в течение 2 часов, чтобы дихлорметан испарился и образовались наноносители. Часть наноносителей промывали путем переноса суспензии наноносителя в центрифужную пробирку и центрифугирования при 75,600×g и 4°C в течение 50 минут, удаления супернатанта и ресуспендирования осадка в DPBS, содержащем 0,25% масс./об. PVA. Процедуру промывки повторяли, и затем осадок повторно суспендирвали в DPBS, содержащем 0,25% мас./об. PVA, для получения суспензии наноносителя, имеющей номинальную концентрацию 10 мг/мл в расчете на полимер. Затем суспензию наноносителя фильтровали с использованием шприцевого фильтра с мембраной PES 0,22 мкм от MilliporeSigma (EMD Millipore, 290 Concord Rd. Billerica MA, код продукта SLGP033RB). Отфильтрованную суспензию наноносителя затем хранили при -20°C.
Иммуносупрессанты
Любой иммуносупрессант, представленный в настоящем документе, можно использовать в любом из представленных способов или композиций и, в некоторых вариантах осуществления, может быть присоединен к синтетическим наноносителям. Иммуносупрессанты включают, но не ограничиваются ими, ингибиторы mTOR. Примеры ингибиторов mTOR включают рапамицин и рапалоги (например, CCL-779, RAD001, AP23573, C20-металлилрапамицин (C20-Marap), C16-(S)-бутилсульфонамидорапамицин (C16-BSrap), C16-(S)-3-метилиндолерапамицин (C16-iRap) (Bayle et al. Chemistry & Biology 2006, 13:99-107)), AZD8055, BEZ235 (NVP-BEZ235), хризофановая кислота (хризофанол), дефоролимус (MK-8669), эверолимус (RAD0001), KU-0063794, PI-103, PP242, темсиролимус, и WYE-354 (продается у Selleck, Houston, TX, USA).
Предпочтительно, в некоторых вариантах осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, иммуносупрессант представляет собой рапамицин. В некоторых из таких вариантов осуществления, рапамицин предпочтительно инкапсулирован в синтетические наноносители. Рапамицин является активным ингредиентом рапамуна, иммуносупрессанта, который ранее широко использовался у людей и в настоящее время одобрен FDA для профилактики отторжения органов у пациентов с трансплантацией почки в возрасте 13 лет и старше.
При соединении с синтетическим наноносителем количество иммуносупрессанта, связанного с синтетическим наноносителем, в расчете на общую сухую массу состава веществ во всем синтетическом наноносителе (масс./масс.), является таким, как описано в другом месте настоящего документа. Предпочтительно, в некоторых вариантах осуществления любого из способов, или композиций, или наборов, представленных в настоящем документе, нагрузка иммуносупрессанта, такого как рапамицин или рапалог, составляет от 7% до 12% или от 8% до 12% масс.
Дозирование
Если в настоящем документе не указано иное, количество (по массе) дозы композиции, содержащей пегилированную уриказу, а также концентрации на флакон, представленные в настоящем документе, относятся к количеству или концентрации белка уриказы, соответственно, не включая конъюгированные с ним молекулы PEG или любые добавленные эксципиенты в композиции. Фактическое количество пегилированной уриказы в таких случаях будет выше, чем описанная доза, из-за более высокой массы формы пегилированного белка. В одном примере доза 0,4 мг/кг композиции, содержащей пегилированную уриказу, относится к дозе 0,4 мг/кг белка уриказы.
Таким образом, доза композиции, содержащей пегилированную уриказу для введения субъекту, может быть рассчитана на основе дозы, указанной в настоящем документе, и массы субъекта в соответствии со следующим уравнением:
(доза в мг/кг (это белок уриказы)) × (масса субъекта (кг))/(концентрация на мл во флаконе (опять же это белок уриказы))=объем, подлежащий введению
Например, пегилированная уриказа может быть восстановлена в стерильной воде до концентрации 6 мг/мл. Таким образом, для этого примера, для введения дозы 0,4 мг/кг субъекту массой 90,7 кг, субъекту следует ввести 6,048 мл восстановленной композиции пегилированной уриказы:
(0,4 мг/кг) × (90,7 кг) / (6 мг/мл)=6,048 мл
В некоторых вариантах осуществления соответствующий объем композиции, содержащей пегилированную уриказу, разбавляют фармацевтически приемлемым эксципиентом (например, стерильным физиологическим раствором), например, для внутривенной инфузии субъекту в течение желаемого периода времени (например, 60 минут).
Аналогично, если в настоящем документе не указано иное, количество (по массе) дозы композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, а также концентрации на флакон, как указано в настоящем документе, относится к количеству или концентрации иммуносупрессанта, соответственно, и не включает синтетический материал наноносителя или любые добавленные эксципиенты или другие компоненты в композиции. Фактическое количество композиции синтетических наноносителей, включающей иммуносупрессант, будет выше, чем описанная доза, из-за добавленной массы вещества синтетического наноносителя и любых добавленных эксципиентов или других компонентов в композиции. В одном примере доза 0,08 мг/кг композиции, содержащей синтетические наноносители, включающие иммуносупрессант, относится к дозе 0,08 мг/кг иммуносупрессанта.
Таким образом, доза композиции, содержащей синтетические наноносители, включающие иммуносупрессант, для введения субъекту может быть рассчитана на основе массы субъекта в соответствии со следующим уравнением:
(доза в мг/кг (это иммуносупрессант)) × (масса субъекта (кг))/(концентрация на мл во флаконе (опять же это иммуносупрессант)=объем, подлежащий введению
Например, композиция, содержащая синтетические наноносители, содержащие иммуносупрессант, имеет концентрацию 2 мг/мл (опять же это концентрация иммуносупрессанта). Таким образом, для этого примера для введения дозы 0,08 мг/кг субъекту массой 90,7 кг субъекту следует ввести 3,6 мл композиции:
(0,08 мг/кг) × (90,7 кг) / (2 мг/мл)=3,6 мл
Нагрузка иммуносупрессанта (например, рапамицина) синтетических наноносителей, содержащих иммуносупрессант, может быть определена путем экстракции иммуносупрессанта из синтетических наноносителей с использованием жидкость-жидкостной экстракции, совместимой как с иммуносупрессантом, так и с синтетическими наноносителями (например, полимеры, содержащие синтетические наноносители) и анализа экстракта с помощью обращенно-фазовой жидкостной хроматографии с УФ-детектированием, специфичного для анализируемого вещества. Нагрузка иммуносупрессанта (содержание синтетических наноносителей) может быть точно и достоверно рассчитана по калибровочной стандартной кривой квалификационного эталонного стандарта, полученной в условиях, совместимых с хроматографией и процедурой экстракции наночастиц, и проанализирована одновременно.
Количество (по массе) дозы композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, может быть рассчитано на основе количества (по массе) дозы иммуносупрессанта в соответствии со следующим уравнением:
(1/нагрузка иммуносупрессанта) × (доза, указанная в зависимости от количества иммуносупрессанта)=доза иммуносупрессанта, указанная как количество синтетических наноносителей, содержащих иммуносупрессант
В качестве примера, нагрузка иммуносупрессанта в синтетических наноносителях может составлять примерно 10%, и если требуется доза 0,08 мг/кг иммуносупрессанта, доза, указанная как количество синтетических наноносителей, содержащих иммуносупрессант, составляет 8 мг/кг.
Количество белка уриказы, присутствующего в пегилированной уриказе, может быть определено с использованием способов, известных в данной области, например колориметрии, УФ-поглощения или аминокислотного анализа. Колориметрический подход основан на стандартном наборе, имеющемся в продаже, использующем типичные реакции на основе красителей, такие как описанные для анализов Брэдфорда или на основе бицинхониновой кислоты (BCA). Количество белка уриказы точно и достоверно рассчитывается по калибровочной стандартной кривой квалификационного эталонного стандарта белка, предпочтительно приобретенного из компендиальных источников, и одновременно анализируется с использованием того же спектрофотометра. Калибровка по одной или нескольким точкам известного белка с аналогичными или разными химическими свойствами может осуществляться в рамках одного и того же анализа, чтобы гарантировать согласованность считывания при выбранном УФ-поглощении. Смесь аминокислот, полученная в результате кислотного гидролиза лекарственного препарата, также может быть проанализирована и, как правило, обеспечивает точную и достоверную количественную оценку. Смесь аминокислот анализируют с помощью ВЭЖХ с УФ-детектированием или флуоресцентным детектированием и с использованием прехроматографической или постхроматографической дериватизации первичных и вторичных аминов. Имеющиеся в продаже смеси обычных аминокислот анализируют в рамках одного и того же анализа для построения калибровочных кривых отдельных аминокислот, по которым производится количественная оценка каждой аминокислоты.. В некоторых вариантах осуществления определение количества белка уриказы дополняется измерением активности фермента, которое может быть осуществлено путем измерения уменьшения избытка мочевой кислоты, контролируемого по поглощению УФ-излучения при 595 нм. Альтернативно или в дополнение, активность уриказы может быть определена с использованием коммерчески доступного набора, который может включать, например, маркировку продукта ферментативной реакции и измерение реакции уриказы по калибровочной кривой, построенной путем анализа известного количества фермента.
Подобно приведенной выше формуле, количество (по массе) дозы композиции, содержащей пегилированную уриказу, может быть рассчитано на основе количества (по массе) дозы уриказы в соответствии со следующим уравнением:
(1/(масса уриказы пегилированной уриказы/массу пегилированной уриказы)) × (доза, указанная на основе количества уриказы)=доза пегилированной уриказы, выраженная как количество пегилированной уриказы
Следует понимать, что количество, указанное в настоящем документе, может быть средним количеством, основанным на популяции соответствующих молекул в композиции.
Типичные дозы уриказы для композиций, содержащих уриказу, такую как пегситиказа, как представлено в настоящем документе, могут составлять 0,10 мг/кг, 0,11 мг/кг, 0,12 мг/кг, 0,13 мг/кг, 0,14 мг/кг, 0,15 мг/кг, 0,16 мг/кг, 0,17 мг/кг, 0,18 мг/кг, 0,19 мг/кг, 0,20 мг/кг, 0,21 мг/кг, 0,22 мг/кг, 0,23 мг/кг, 0,24 мг/кг, 0,25 мг/кг, 0,26 мг/кг, 0,27 мг/кг, 0,28 мг/кг, 0,29 мг/кг, 0,30 мг/кг, 0,31 мг/кг, 0,32 мг/кг, 0,34 мг/кг, 0,35 мг/кг, 0,36 мг/кг, 0,37 мг/кг, 0,38 мг/кг, 0,39 мг/кг, 0,40 мг/кг, 0,41 мг/кг, 0,42 мг/кг, 0,43 мг/кг, 0,44 мг/кг, 0,45 мг/кг, 0,46 мг/кг, 0,47 мг/кг, 0,48 мг/кг, 0,49 мг/кг, 0,50 мг/кг, 0,51 мг/кг, 0,52 мг/кг, 0,53 мг/кг, 0,54 мг/кг, 0,55 мг/кг, 0,56 мг/кг, 0,57 мг/кг, 0,58 мг/кг, 0,59 мг/кг, 0,60 мг/кг, 0,61 мг/кг, 0,62 мг/кг, 0,63 мг/кг,0,64 мг/кг, 0,65 мг/кг, 0,66 мг/кг, 0,67 мг/кг, 0,68 мг/кг, 0,69 мг/кг, 0,70 мг/кг, 0,71 мг/кг, 0,72 мг/кг, 0,73 мг/кг, 0,74 мг/кг, 0,75 мг/кг, 0,76 мг/кг, 0,77 мг/кг, 0,78 мг/кг, 0,79 мг/кг, 0,80 мг/кг, 0,81 мг/кг, 0,82 мг/кг, 0,83 мг/кг, 0,84 мг/кг, 0,85 мг/кг, 0,86 мг/кг, 0,87 мг/кг, 0,88 мг/кг, 0,89 мг/кг, 0,90 мг/кг, 0,91 мг/кг, 0,92 мг/кг, 0,93 мг/кг, 0,94 мг/кг, 0,95 мг/кг, 0,96 мг/кг, 0,97 мг/кг, 0,98 мг/кг, 0,90 мг/кг, 1,0 мг/кг, 1,01 мг/кг, 1,02 мг/кг, 1,03 мг/кг, 1,04 мг/кг, 1,05 мг/кг, 1,06 мг/кг, 1,07 мг/кг, 1,08 мг/кг, 1,09 мг/кг, 1,10 мг/кг, 1,11 мг/кг, 1,12 мг/кг, 1,13 мг/кг, 1,14 мг/кг, 1,15 мг/кг, 1,16 мг/кг, 1,17 мг/кг, 1,18 мг/кг, 1,19 мг/кг или 1,20 мг/кг уриказы.
Типичные дозы рапамицина для композиций, содержащих синтетические наноносители, содержащие рапамицин, могут составлять 0,050 мг/кг, 0,055 мг/кг, 0,060 мг/кг, 0,065 мг/кг, 0,070 мг/кг, 0,075 мг/кг, 0,080 мг/кг, 0,085 мг/кг, 0,090 мг/кг, 0,095 мг/кг, 0,100 мг/кг, 0,105 мг/кг, 0,110 мг/кг, 0,115 мг/кг, 0,120 мг/кг, 0,125 мг/кг, 0,130 мг/кг, 0,135 мг/кг, 0,140 мг/кг, 0,145 мг/кг, 0,150 мг/кг, 0,155 мг/кг, 0,160 мг/кг, 0,165 мг/кг, 0,170 мг/кг, 0,175 мг/кг, 0,180 мг/кг, 0,185 мг/кг, 0,190 мг/кг, 0,195 мг/кг, 0,200 мг/кг, 0,205 мг/кг, 0,210 мг/кг, 0,215 мг/кг, 0,220 мг/кг, 0,225 мг/кг, 0,230 мг/кг, 0,235 мг/кг, 0,240 мг/кг, 0,245 мг/кг, 0,250 мг/кг, 0,255 мг/кг, 0,260 мг/кг, 0,265 мг/кг, 0,270 мг/кг, 0,275 мг/кг, 0,280 мг/кг, 0,285 мг/кг, 0,290 мг/кг, 0,295 мг/кг, 0,300 мг/кг, 0,305 мг/кг, 0,310 мг/кг, 0,315 мг/кг, 0,320 мг/кг, 0,325 мг/кг, 0,330 мг/кг, 0,335 мг/кг, 0,340 мг/кг, 0,345 мг/кг, 0,350 мг/кг, 0,355 мг/кг, 0,360 мг/кг, 0,365 мг/кг, 0,370 мг/кг, 0,375 мг/кг, 0,380 мг/кг, 0,385 мг/кг, 0,390 мг/кг, 0,395 мг/кг, 0,400 мг/кг, 0,405 мг/кг, 0,410 мг/кг, 0,415 мг/кг, 0,420 мг/кг, 0,425 мг/кг, 0,430 мг/кг, 0,435 мг/кг, 0,440 мг/кг, 0,445 мг/кг, 0,450 мг/кг, 0,455 мг/кг, 0,460 мг/кг, 0,465 мг/кг, 0,470 мг/кг, 0,475 мг/кг, 0,480 мг/кг, 0,485 мг/кг, 0,490 мг/кг, 0,495 мг/кг, 0,500 мг/кг рапамицина.
Примерные дозы композиций, содержащих синтетические наноносители, содержащие рапамицин, как представлено в настоящем документе, могут составлять 0,55 мг/кг, 0,56 мг/кг, 0,57 мг/кг, 0,58 мг/кг, 0,59 мг/кг, 0,60 мг/кг, 0,61 мг/кг, 0,62 мг/кг, 0,63 мг/кг,0,64 мг/кг, 0,65 мг/кг, 0,66 мг/кг, 0,67 мг/кг, 0,68 мг/кг, 0,69 мг/кг, 0,70 мг/кг, 0,71 мг/кг, 0,72 мг/кг, 0,73 мг/кг, 0,74 мг/кг, 0,75 мг/кг, 0,76 мг/кг, 0,77 мг/кг, 0,78 мг/кг, 0,79 мг/кг, 0,80 мг/кг, 0,81 мг/кг, 0,82 мг/кг, 0,83 мг/кг, 0,84 мг/кг, 0,85 мг/кг, 0,86 мг/кг, 0,87 мг/кг, 0,88 мг/кг, 0,89 мг/кг, 0,90 мг/кг, 0,91 мг/кг, 0,92 мг/кг, 0,93 мг/кг, 0,94 мг/кг, 0,95 мг/кг, 0,96 мг/кг, 0,97 мг/кг, 0,98 мг/кг, 0,90 мг/кг, 1,0 мг/кг, 1,01 мг/кг, 1,02 мг/кг, 1,03 мг/кг, 1,04 мг/кг, 1,05 мг/кг, 1,06 мг/кг, 1,07 мг/кг, 1,08 мг/кг, 1,09 мг/кг, 1,10 мг/кг, 1,11 мг/кг, 1,12 мг/кг, 1,13 мг/кг, 1,14 мг/кг, 1,15 мг/кг, 1,16 мг/кг, 1,17 мг/кг, 1,18 мг/кг, 1,19 мг/кг, 1,20 мг/кг, 1,21 мг/кг, 1,22 мг/кг, 1,23 мг/кг, 1,24 мг/кг, 1,25 мг/кг, 1,26 мг/кг, 1,27 мг/кг, 1,28 мг/кг, 1,29 мг/кг, 1,30 мг/кг, 1,31 мг/кг, 1,32 мг/кг, 1,33 мг/кг, 1,34 мг/кг, 1,35 мг/кг, 1,36 мг/кг, 1,37 мг/кг, 1,38 мг/кг, 1,39 мг/кг, 1,40 мг/кг, 1,41 мг/кг, 1,42 мг/кг, 1,43 мг/кг, 1,44 мг/кг, 1,45 мг/кг, 1,46 мг/кг, 1,47 мг/кг, 1,48 мг/кг, 1,49 мг/кг, 1,50 мг/кг, 1,51 мг/кг, 1,52 мг/кг, 1,53 мг/кг, 1,54 мг/кг, 1,55 мг/кг, 1,56 мг/кг, 1,57 мг/кг, 1,58 мг/кг, 1,59 мг/кг, 1,60 мг/кг, 1,61 мг/кг, 1,62 мг/кг, 1,63 мг/кг, 1,64 мг/кг, 1,65 мг/кг, 1,66 мг/кг, 1,67 мг/кг, 1,68 мг/кг, 1,69 мг/кг, 1,70 мг/кг, 1,71 мг/кг, 1,72 мг/кг, 1,73 мг/кг, 1,74 мг/кг, 1,75 мг/кг, 1,76 мг/кг, 1,77 мг/кг, 1,78 мг/кг, 1,79 мг/кг, 1,80 мг/кг, 1,81 мг/кг, 1,82 мг/кг, 1,83 мг/кг, 1,84 мг/кг, 1,85 мг/кг, 1,86 мг/кг, 1,87 мг/кг, 1,88 мг/кг, 1,89 мг/кг, 1,90 мг/кг, 1,91 мг/кг, 1,92 мг/кг, 1,93 мг/кг, 1,94 мг/кг, 1,95 мг/кг, 1,96 мг/кг, 1,97 мг/кг, 1,98 мг/кг, 1,99 мг/кг, 2,00 мг/кг, 2,01 мг/кг, 2,02 мг/кг, 2,03 мг/кг, 2,04 мг/кг, 2,05 мг/кг, 2,06 мг/кг, 2,07 мг/кг, 2,08 мг/кг, 2,09 мг/кг, 2,10 мг/кг, 2,11 мг/кг, 2,12 мг/кг, 2,13 мг/кг, 2,14 мг/кг, 2,15 мг/кг, 2,16 мг/кг, 2,17 мг/кг, 2,18 мг/кг, 2,19 мг/кг, 2,20 мг/кг, 2,21 мг/кг, 2,22 мг/кг, 2,23 мг/кг, 2,24 мг/кг, 2,25 мг/кг, 2,26 мг/кг, 2,27 мг/кг, 2,28 мг/кг, 2,29 мг/кг, 2,30 мг/кг, 2,31 мг/кг, 2,32 мг/кг, 2,33 мг/кг, 2,34 мг/кг, 2,35 мг/кг, 2,36 мг/кг, 2,37 мг/кг, 2,38 мг/кг, 2,39 мг/кг, 2,40 мг/кг, 2,41 мг/кг, 2,42 мг/кг, 2,43 мг/кг, 2,44 мг/кг, 2,45 мг/кг, 2,46 мг/кг, 2,47 мг/кг, 2,48 мг/кг, 2,49 мг/кг, 2,50 мг/кг, 2,51 мг/кг, 2,52 мг/кг, 2,53 мг/кг, 2,54 мг/кг, 2,55 мг/кг, 2,56 мг/кг, 2,57 мг/кг, 2,58 мг/кг, 2,59 мг/кг, 2,60 мг/кг, 2,61 мг/кг, 2,62 мг/кг, 2,63 мг/кг, 2,64 мг/кг, 2,65 мг/кг, 2,66 мг/кг, 2,67 мг/кг, 2,68 мг/кг, 2,69 мг/кг, 2,70 мг/кг, 2,71 мг/кг, 2,72 мг/кг, 2,73 мг/кг, 2,74 мг/кг, 2,75 мг/кг, 2,76 мг/кг, 2,77 мг/кг, 2,78 мг/кг, 2,79 мг/кг, 2,80 мг/кг, 2,81 мг/кг, 2,82 мг/кг, 2,83 мг/кг, 2,84 мг/кг, 2,85 мг/кг, 2,86 мг/кг, 2,87 мг/кг, 2,88 мг/кг, 2,89 мг/кг, 2,90 мг/кг, 2,91 мг/кг, 2,92 мг/кг, 2,93 мг/кг, 2,94 мг/кг, 2,95 мг/кг, 2,96 мг/кг, 2,97 мг/кг, 2,98 мг/кг, 2,99 мг/кг, 3,00 мг/кг, 3,01 мг/кг, 3,02 мг/кг, 3,03 мг/кг, 3,04 мг/кг, 3,05 мг/кг, 3,06 мг/кг, 3,07 мг/кг, 3,08 мг/кг, 3,09 мг/кг, 3,10 мг/кг, 3,11 мг/кг, 3,12 мг/кг, 3,13 мг/кг, 3,14 мг/кг, 3,15 мг/кг, 3,16 мг/кг, 3,17 мг/кг, 3,18 мг/кг, 3,19 мг/кг, 3,20 мг/кг, 3,21 мг/кг, 3,22 мг/кг, 3,23 мг/кг, 3,24 мг/кг, 3,25 мг/кг, 3,26 мг/кг, 3,27 мг/кг, 3,28 мг/кг, 3,29 мг/кг, 3,30 мг/кг, 3,31 мг/кг, 3,32 мг/кг, 3,33 мг/кг, 3,34 мг/кг, 3,35 мг/кг, 3,36 мг/кг, 3,37 мг/кг, 3,38 мг/кг, 3,39 мг/кг, 3,40 мг/кг, 3,41 мг/кг, 3,42 мг/кг, 3,43 мг/кг, 3,44 мг/кг, 3,45 мг/кг, 3,46 мг/кг, 3,47 мг/кг, 3,48 мг/кг, 3,49 мг/кг, 3,50 мг/кг, 3,51 мг/кг, 3,52 мг/кг, 3,53 мг/кг, 3,54 мг/кг, 3,55 мг/кг, 3,56 мг/кг, 3,57 мг/кг, 3,58 мг/кг, 3,59 мг/кг, 3,60 мг/кг, 3,61 мг/кг, 3,62 мг/кг, 3,63 мг/кг, 3,64 мг/кг, 3,65 мг/кг, 3,66 мг/кг, 3,67 мг/кг, 3,68 мг/кг, 3,69 мг/кг, 3,70 мг/кг, 3,71 мг/кг, 3,72 мг/кг, 3,73 мг/кг, 3,74 мг/кг, 3,75 мг/кг, 3,76 мг/кг, 3,77 мг/кг, 3,78 мг/кг, 3,79 мг/кг, 3,80 мг/кг, 3,81 мг/кг, 3,82 мг/кг, 3,83 мг/кг, 3,84 мг/кг, 3,85 мг/кг, 3,86 мг/кг, 3,87 мг/кг, 3,88 мг/кг, 3,89 мг/кг, 3,90 мг/кг, 3,91 мг/кг, 3,92 мг/кг, 3,93 мг/кг, 3,94 мг/кг, 3,95 мг/кг, 3,96 мг/кг, 3,97 мг/кг, 3,98 мг/кг, 3,99 мг/кг, 4,00 мг/кг, 4,01 мг/кг, 4,02 мг/кг, 4,03 мг/кг, 4,04 мг/кг, 4,05 мг/кг, 4,06 мг/кг, 4,07 мг/кг, 4,08 мг/кг, 4,09 мг/кг, 4,10 мг/кг, 4,11 мг/кг, 4,12 мг/кг, 4,13 мг/кг, 4,14 мг/кг, 4,15 мг/кг, 4,16 мг/кг, 4,17 мг/кг, 4,18 мг/кг, 4,19 мг/кг, 4,20 мг/кг, 4,21 мг/кг, 4,22 мг/кг, 4,23 мг/кг, 4,24 мг/кг, 4,25 мг/кг, 4,26 мг/кг, 4,27 мг/кг, 4,28 мг/кг, 4,29 мг/кг, 4,30 мг/кг, 4,31 мг/кг, 4,32 мг/кг, 4,33 мг/кг, 4,34 мг/кг, 4,35 мг/кг, 4,36 мг/кг, 4,37 мг/кг, 4,38 мг/кг, 4,39 мг/кг, 4,40 мг/кг, 4,41 мг/кг, 4,42 мг/кг, 4,43 мг/кг, 4,44 мг/кг, 4,45 мг/кг, 4,46 мг/кг, 4,47 мг/кг, 4,48 мг/кг, 4,49 мг/кг, 4,50 мг/кг, 4,51 мг/кг, 4,52 мг/кг, 4,53 мг/кг, 4,54 мг/кг, 4,55 мг/кг, 4,56 мг/кг, 4,57 мг/кг, 4,58 мг/кг, 4,59 мг/кг, 4,60 мг/кг, 4,61 мг/кг, 4,62 мг/кг, 4,63 мг/кг, 4,64 мг/кг, 4,65 мг/кг, 4,66 мг/кг, 4,67 мг/кг, 4,68 мг/кг, 4,69 мг/кг, 4,70 мг/кг, 4,71 мг/кг, 4,72 мг/кг, 4,73 мг/кг, 4,74 мг/кг, 4,75 мг/кг, 4,76 мг/кг, 4,77 мг/кг, 4,78 мг/кг, 4,79 мг/кг, 4,80 мг/кг, 4,81 мг/кг, 4,82 мг/кг, 4,83 мг/кг, 4,84 мг/кг, 4,85 мг/кг, 4,86 мг/кг, 4,87 мг/кг, 4,88 мг/кг, 4,89 мг/кг, 4,90 мг/кг, 4,91 мг/кг, 4,92 мг/кг, 4,93 мг/кг, 4,94 мг/кг, 4,95 мг/кг, 4,96 мг/кг, 4,97 мг/кг, 4,98 мг/кг, 4,99 мг/кг, 5,00 мг/кг, 5,01 мг/кг, 5,02 мг/кг, 5,03 мг/кг, 5,04 мг/кг, 5,05 мг/кг, 5,06 мг/кг, 5,07 мг/кг, 5,08 мг/кг, 5,09 мг/кг, 5,10 мг/кг, 5,11 мг/кг, 5,12 мг/кг, 5,13 мг/кг, 5,14 мг/кг, 5,15 мг/кг, 5,16 мг/кг, 5,17 мг/кг, 5,18 мг/кг, 5,19 мг/кг, 5,20 мг/кг, 5,21 мг/кг, 5,22 мг/кг, 5,23 мг/кг, 5,24 мг/кг, 5,25 мг/кг, 5,26 мг/кг, 5,27 мг/кг, 5,28 мг/кг, 5,29 мг/кг, 5,30 мг/кг, 5,31 мг/кг, 5,32 мг/кг, 5,33 мг/кг, 5,34 мг/кг, 5,35 мг/кг, 5,36 мг/кг, 5,37 мг/кг, 5,38 мг/кг, 5,39 мг/кг, 5,40 мг/кг, 5,41 мг/кг, 5,42 мг/кг, 5,43 мг/кг, 5,44 мг/кг, 5,45 мг/кг, 5,46 мг/кг, 5,47 мг/кг, 5,48 мг/кг, 5,49 мг/кг, 5,50 мг/кг, 5,51 мг/кг, 5,52 мг/кг, 5,53 мг/кг, 5,54 мг/кг, 5,55 мг/кг, 5,56 мг/кг, 5,57 мг/кг, 5,58 мг/кг, 5,59 мг/кг, 5,60 мг/кг, 5,61 мг/кг, 5,62 мг/кг, 5,63 мг/кг, 5,64 мг/кг, 5,65 мг/кг, 5,66 мг/кг, 5,67 мг/кг, 5,68 мг/кг, 5,69 мг/кг, 5,70 мг/кг, 5,71 мг/кг, 5,72 мг/кг, 5,73 мг/кг, 5,74 мг/кг, 5,75 мг/кг, 5,76 мг/кг, 5,77 мг/кг, 5,78 мг/кг, 5,79 мг/кг, 5,80 мг/кг, 5,81 мг/кг, 5,82 мг/кг, 5,83 мг/кг, 5,84 мг/кг, 5,85 мг/кг, 5,86 мг/кг, 5,87 мг/кг, 5,88 мг/кг, 5,89 мг/кг, 5,90 мг/кг, 5,91 мг/кг, 5,92 мг/кг, 5,93 мг/кг, 5,94 мг/кг, 5,95 мг/кг, 5,96 мг/кг, 5,97 мг/кг, 5,98 мг/кг, 5,99 мг/кг, 6,00 мг/кг, 6,01 мг/кг, 6,02 мг/кг, 6,03 мг/кг, 6,04 мг/кг, 6,05 мг/кг, 6,06 мг/кг, 6,07 мг/кг, 6,08 мг/кг, 6,09 мг/кг, 6,10 мг/кг, 6,11 мг/кг, 6,12 мг/кг, 6,13 мг/кг, 6,14 мг/кг, 6,15 мг/кг, 6,16 мг/кг, 6,17 мг/кг, 6,18 мг/кг, 6,19 мг/кг, 6,20 мг/кг, 6,21 мг/кг, 6,22 мг/кг, 6,23 мг/кг, 6,24 мг/кг, 6,25 мг/кг, 6,26 мг/кг, 6,27 мг/кг, 6,28 мг/кг, 6,29 мг/кг, 6,30 мг/кг, 6,31 мг/кг, 6,32 мг/кг, 6,33 мг/кг, 6,34 мг/кг, 6,35 мг/кг, 6,36 мг/кг, 6,37 мг/кг, 6,38 мг/кг, 6,39 мг/кг, 6,40 мг/кг, 6,41 мг/кг, 6,42 мг/кг, 6,43 мг/кг, 6,44 мг/кг, 6,45 мг/кг, 6,46 мг/кг, 6,47 мг/кг, 6,48 мг/кг, 6,49 мг/кг или 6,50 мг/кг, где доза дана в мг синтетических наноносителей, содержащих рапамицин.
Любая из доз, представленных в настоящем документе для композиции, содержащей уриказу, такую как пегситиказа, может использоваться в любом из способов, или композиций, или наборов, представленных в настоящем документе. Обычно, когда речь идет о дозе, вводимой субъекту, доза представляет собой указанную дозу. Любая из доз, представленных в настоящем документе, для композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, такой как рапамицин, может быть использована в любом из способов, или композиций, или наборов, представленных в настоящем документе. Обычно, когда речь идет о дозе, вводимой субъекту, доза представляет собой указанную дозу. Таким образом, в любом из способов, представленных в настоящем документе, дозы представляют собой указанные дозы.
В некоторых вариантах осуществления любого из способов, представленных в настоящем документе, дополнительный объем (основной объем) может быть использован для заполнения инфузионной линии для введения субъекту любой из композиций, представленных в настоящем документе.
В настоящем документе представлен ряд возможных схем введения доз. Соответственно, любой из субъектов, представленных в настоящем документе, может получить лечение в соответствии с любой из схем введения доз, приведенных в настоящем документе. В качестве примера, любой из субъектов, представленных в настоящем документе, может получать лечение композицией, содержащей уриказу, такую как пегилированная уриказа, и/или композицией, содержащей синтетические наноносители, содержащие иммуносупрессант, такой как рапамицин, в соответствии с любым из этих схем введения доз. Способом введения композиций любого из представленных способов лечения может быть внутривенное введение, такое как внутривенная инфузия, которая, например, может происходить в течение примерно 1 часа. Кроме того, любой из способов лечения, представленных в настоящем документе, может также включать введение дополнительного терапевтического средства, такого как терапевтическое средство, снижающее уровень мочевой кислоты, такое как уриказа, или профилактическое лечение против обострения подагры. Введение дополнительного терапевтического средства может осуществляться в соответствии с любой из применяемых схем лечения, представленных в настоящем документе.
Предпочтительно, в некоторых вариантах осуществления, лечение комбинацией композиции синтетического наноносителя, содержащей иммуносупрессант, такой как рапамицин, с композицией, содержащей уриказу, такую как пегилированная уриказа, может включать три дозы композиции синтетического наноносителя одновременно с композицией, содержащей уриказу, с последующими двумя дозами уриказы без сопутствующего введения композиции, содержащей иммуносупрессант, такой как композиция синтетического наноносителя, содержащая иммуносупрессант, или без сопутствующего введения дополнительного терапевтического средства. В таком варианте осуществления каждую дозу можно вводить каждые две-четыре недели. В одном варианте осуществления предоставляется способ, в соответствии с которым любому из субъектов, представленных в настоящем документе, сопутствующе вводят три дозы композиции синтетического наноносителя с композицией, содержащей уриказу, ежемесячно в течение трех месяцев. В другом варианте осуществления, этот способ дополнительно включает введение 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более ежемесячных доз композиции, содержащей уриказу, отдельно или без сопутствующего введения иммуносупрессанта, такого как композиция синтетического наноносителя, содержащая иммуносупрессант, или дополнительного терапевтического средства. В некоторых вариантах осуществления любого из способов, представленных в настоящем документе, уровень мочевой кислоты измеряют у субъекта в один или несколько моментов времени до, во время и/или после периода лечения.
Дополнительные терапевтические средства
Дополнительные терапевтические средства от повышенного уровня мочевой кислоты, подагры, обострения подагры или состояний, связанных с подагрой, могут быть назначены любому из субъектов, представленных в настоящем документе, например, для снижения уровня мочевой кислоты и/или лечения подагры и/или профилактики обострения подагры. Любой из способов, представленных в настоящем документе, может включать введение одного или нескольких из этих дополнительных терапевтических средств. В некоторых вариантах осуществления, любой из способов, представленных в настоящем документе, не включает сопутствующее введение дополнительного терапевтического средства. Примеры дополнительных терапевтических средств включают, но не ограничиваются ими, следующее. Другие примеры должны быть известны специалистам в данной области.
Дополнительные терапевтические средства включают противовоспалительные терапевтические средства (т.е. любые терапевтические средства, которые могут уменьшать воспаление). Противовоспалительные терапевтические средства включают, но не ограничиваются ими, кортикостероиды или производные кортизола (гидрокортизон). Кортикостероиды включают, но не ограничиваются ими, глюкокортикоиды и минералокортикоиды. Еще другие примеры кортикостероидов включают, но не ограничиваются ими, те, которые являются природными (например, 11-дегидрокортикостерон (11-оксокортикостерон, 17-дезоксикортизон)= 21-гидроксипрегн-4-ен-3,11,20-трион; 11-дезоксикортикостерон (дезоксикортикостерон, дезоксикортон; 21-гидроксипрогестерон)=21-гидроксипрегн-4-ен-3,20-дион; 11-дезоксикортизол (кортодоксон, кортексолон)=17α,21-дигидроксипрегн-4-ен-3,20-дион; 11-кетопрогестерон (11-оксопрогестерон; кетогестин)=прегн-4-ен-3,11,20-трион; 11β-Гидроксипрегненолон=3β,11β-дигидроксипрегн-5-ен-20-он; 11β-Гидроксипрогестерон (21-дезоксикортикостерон)=11β-гидроксипрегн-4-ен-3,20-дион; 11β,17α,21-тригидроксипрегненолон=3β,11β,17α,21-тетрагидроксипрегн-5-ен-20-он; 17α,21-дигидроксипрегненолон=3β,17α,21-тригидроксипрегн-5-ен-20-он; 17α-гидроксипрегненолон=3β,17α-дигидроксипрегн-5-ен-20-он; 17α-гидроксипрогестерон=17α-гидроксипрегн-4-ен-3,11,20-трион; 18-гидрокси-11-дезоксикортикостерон=18,21-дигидроксипрегн-4-ен-3,20-дион; 18-Гидроксикортикостерон=11β,18,21-тригидроксипрегн-4-ен-3,20-дион; 18-Гидроксипрогестерон=18-гидроксипрегн-4-ен-3,20-дион; 21-дезоксикортизол=11β,17α-дигидроксипрегн-4-ен-3,20-дион; 21-дезоксикортизон=17α-гидроксипрегн-4-ен-3,11,20-трион; 21-гидроксипрегненолон (пребедиолон)=3β,21-дигидроксипрегн-5-ен-20-он; альдостерон=11β,21-дигидроксипрегн-4-ен-3,18,20-трион; Кортикостерон (17-дезоксикортизол)=11β,21-дигидроксипрегн-4-ен-3,20-дион; кортизол (гидрокортизон)= 11β,17α,21-тригидроксипрегн-4-ен-3,20-дион; кортизон=17α,21-дигидроксипрегн-4-ен-3,11,20-трион; прегненолон=прегн-5-ен-3β-ол-20-он; и прогестерон=прегн-4-ен-3,20-дион); синтетические, такие как прогестероновый тип (например, флюгестон (флурогестон)=9α-фтор-11β,17α-дигидроксипрегн-4-ен-3,20-дион; Фторметолон=6α-метил-9α-фтор-11β,17α-дигидроксипрегна-1,4-диен-3,20-дион; медризон (гидроксиметилпрогестерон)=6α-метил-11β-гидроксипрегн-4-ен-3,20-дион; и пребедиолона ацетат (21-ацетоксипрегненолон)=3β,21-дигидроксипрегн-5-ен-20-он 21-ацетат) и производные прогестерона прогестины (например, хлормадинона ацетат, ципротерона ацетат, медрогестон, медроксипрогестерона ацетат, мегестрола ацетат и сегестерона ацетат); гидрокортизонового типа (например, хлоропреднизон=6α-хлор-17α,21-дигидроксипрегна-1,4-диен-3,11,20-трион; клопреднол=6-хлор-11β,17α,21-тригидроксипрегна-1,4,6-триен-3,20-дион; дифлупреднат=6α,9α-дифтор-11β,17α,21-тригидроксипрегна-1,4-диен-3,20-дион 17α-бутират 21-ацетат; флудрокортизон=9α-фтор-11β,17α,21-тригидроксипрегн-4-ен-3,20-дион; флуоцинолон=6α,9α-дифтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион; флуперолон=9α-фтор-11β,17α,21-тригидрокси-21-метилпрегна-1,4-диен-3,20-дион; флупреднизолон=6α-фтор-11β,17α,21-тригидроксипрегна-1,4-диен-3,20-дион; лотепреднол=11β,17α,дигидрокси-21-окса-21-хлорметилпрегна-1,4-диен-3,20-дион; метилпреднизолон=6α-метил-11β,17α,21-тригидроксипрегна-1,4-диен-3,20-дион; предникарбат=11β,17α,21-тригидроксипрегна-1,4-диен-3,20-дион 17α-этилкарбонат 21-пропионат; преднизолон=11β,17α,21-тригидроксипрегна-1,4-диен-3,20-дион; преднизон=17α,21-дигидроксипрегна-1,4-диен-3,11,20-трион; тиксокортол=11β,17α-дигидрокси-21-сульфанилпрегн-4-ен-3,20-дион; и триамцинолон=9α-фтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион); метазоновый тип (16-метилированный) (например, метазон; алклометазон=7α-хлор-11β,17α,21-тригидрокси-16α-метилпрегна-1,4-диен-3,20-дион; беклометазон=9α-хлор-11β,17α,21-тригидрокси-16β-метилпрегна-1,4-диен-3,20-дион; бетаметазон=9α-фтор-11β,17α,21-тригидрокси-16β-метилпрегна-1,4-диен-3,20-дион; клобетазол=9α-фтор-11β,17α-дигидрокси-16β-метил-21-хлорпрегна-1,4-диен-3,20-дион; клобетазон=9α-фтор-16β-метил-17α-гидрокси-21-хлорпрегна-1,4-диен-3,11,20-трион; клокортолон=6α-фтор-9α-хлор-11β,21-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион; дезоксиметазон=9α-фтор-11β,21-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион; дексаметазон=9α-фтор-11β,17α,21-тригидрокси-16α-метилпрегна-1,4-диен-3,20-дион; дифлоразон=6α,9α-дифтор-11β,17α,21-тригидрокси-16β-метилпрегна-1,4-диен-3,20-дион; дифлюокортолон=6α,9α-дифтор-11β,21-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион; флуклоролон=6α-фтор-9α,11β-дихлор-16α,17α,21-тригидроксипрегна-1,4-диен-3,20-дион; флуметазон=6α,9α-дифтор-11β,17α,21-тригидрокси-16α-метилпрегна-1,4-диен-3,20-дион; флуокортин=6α-фтор-11β,21-дигидрокси-16α-метилпрегна-1,4-диен-3,20,21-трион; флуокортолон=6α-фтор-11β,21-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион; флупредниден=9α-фтор-11β,17α,21-тригидрокси-16-метиленпрегна-1,4-диен-3,20-дион; флутиказон=6α,9α-дифтор-11β,17α-дигидрокси-16α-метил-21-тиа-21-фторметилпрегна-1,4-диен-3,20-дион; флутиказона фуроат=6α,9α-дифтор-11β,17α-дигидрокси-16α-метил-21-тиа-21-фторметилпрегна-1,4-диен-3,20-дион 17α-(2-фуроат); галометазон=2-хлор-6α,9α-дифтор-11β,17α,21-тригидрокси-16α-метилпрегна-1,4-диен-3,20-дион; мепреднизон=16β-метил-17α,21-дигидроксипрегна-1,4-диен-3,11,20-трион; мометазон=9α,21-дихлор-11β,17α-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион; мометазон фуроат=9α,21-дихлор-11β,17α-дигидрокси-16α-метилпрегна-1,4-диен-3,20-дион 17α-(2-фуроат); параметазон=6α-фтор-11β,17α,21-тригидрокси-16α-метилпрегна-1,4-диен-3,20-дион; преднилиден=11β,17α,21-тригидрокси-16-метиленпрегна-1,4-диен-3,20-дион; римексолон=11β-гидрокси-16α,17α,21-триметилпрегна-1,4-диен-3,20-дион; и улобетазол (галобетазол)= 6α,9α-дифтор-11β,17α-дигидрокси-16β-метил-21-хлорпрегна-1,4-диен-3,20-дион); ацетониды и родственные им (например, амцинонид=9α-фтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с циклопентаноном, 21-ацетат; будесонид=11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с бутиральдегидом; циклесонид=11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с (R)-циклогексанкарбоксальдегидом, 21-изобутират; дефлазакорт=11β,21-дигидрокси-2'-метил-5'H-прегна-1,4-диено[17,16-d]оксазол-3,20-дион 21-ацетат; десонид=11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; формокортал (фторформилон)=3-(2-хлорэтокси)-9α-фтор-11β,16α,17α,21-тетрагидрокси-20-оксопрегна-3,5-диен-6-карбоксальдегид циклический 16α,17α-ацеталь с ацетоном, 21-ацетат; флуклоролона ацетонид (флуклонид)=6α-фтор-9α,11β-дихлор-16α,17α,21-тригидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; Флудроксикортид (флурандренолон, флурандренолид)=6α-фтор-11β,16α,17α,21-тетрагидроксипрегн-4-ен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; Флунизолид=6α-фтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; флуоцинолона ацетонид=6α,9α-дифтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; флуоцинонид=6α,9α-дифтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном, 21-ацетат; галцинонид=9α-фтор-11β,16α,17α-тригидрокси-21-хлорпрегн-4-ен-3,20-дион циклический 16α,17α-ацеталь с ацетоном; и триамцинолона ацетонид=9α-фтор-11β,16α,17α,21-тетрагидроксипрегна-1,4-диен-3,20-дион циклический 16α,17α-ацеталь с ацетоном); и другие (например, кортивазол=6,16α-диметил-11β,17α,21-тригидрокси-2'-фенил[3,2-c]пиразолопрегна-4,6-диен-20-он 21-ацетат; и RU-28362=6-метил-11β,17β-дигидрокси-17α-(1-пропинил)андроста-1,4,6-триен-3-он).
Кортикостероиды, особенно гликокортикоиды, обладают противовоспалительным и иммуносупрессивным эффектом, что может быть эффективным при лечении симптомов, включая боль и воспаление, связанные с подагрой, обострениями подагры и/или состояниями, связанными с подагрой. Введение кортикостероидов также может помочь в уменьшении аллергических реакций, связанных с одним или несколькими дополнительными терапиями, например заместительной терапией уриказой. Еще другие неограничивающие примеры кортикостероидов включают преднизон, преднизолон, медрол и метилпреднизолон.
Дополнительные терапевтические средства включают кратковременные терапии обострения подагры или боли и воспаления, связанных с любым из симптомов, связанных с подагрой, или состояния, связанного с подагрой, включая нестероидные противовоспалительные препараты (НПВП), колхицин, пероральные кортикостероиды. Не ограничивающие Примеры НПВП включают как отпускаемое без рецепта НПВП, такие как ибупрофен, аспирин и напроксен, так и НПВП, отпускаемые по рецепту, такие как целекоксиб, диклофенак, дифлунизал, этодолак, индометацин, кетопрофен, кеторолак, набуметон, оксапрозин, пироксикам салсалат, сулиндак и толметин.
Колхицин представляет собой противовоспалительное средство, которое обычно рассматривается как альтернатива НПВП для лечения симптомов, включая боль и воспаление, связанные с подагрой, обострением подагры и/или состояниями, связанными с подагрой.
Дополнительные примеры дополнительных терапевтических средств включают ингибиторы ксантиноксидазы, которые представляют собой молекулы, которые ингибируют ксанитиноксидазу, уменьшая или предотвращая окисление ксантина до мочевой кислоты, тем самым снижая выработку мочевой кислоты. Ингибиторы ксантиноксидазы обычно классифицируются как аналоги пурина и другие типы ингибиторов ксантиноксидазы. Примеры ингибиторов ксантиноксидазы включают аллопуринол, оксипуринол, тизопурин, фебуксостат, топироксостат, инозиты (например, фитиновая кислота и мио-инозитол), флавоноиды (например, кемпферол, мирицетин, кверцетин), кофейная кислота и 3,4-дигидрокси-5-нитробензальдегид (DHNB).
Еще другие примеры дополнительных терапевтических средств включают урикозурические средства. Урикозурические средства направлены на увеличение выведения мочевой кислоты с целью снижения уровней мочевой кислоты в сыворотке крови путем модуляции реабсорбции почечных канальцев. Например, некоторые урикозурические средства модулируют активность почечных переносчиков мочевой кислоты (например, ингибиторы URAT1/SLC22A12). Неограничивающие примеры урикозурических средств включают пробенецид, бензбромарон, лесинурад, сульфинпиразон. Другие дополнительные терапевтические средства также могут обладать урикозурической активностью, например, аспирин.
Дополнительные терапевтические средства также включают другие методы лечения на основе уриказы, которые включают пегилированную уриказу. Было показано, что такие способы лечения, например, при введении людям, снижают уровень мочевой кислоты в крови и улучшают симптомы подагры. Расбуриказа (Elitek®), непегилированная рекомбинантная уриказа, клонированная из Aspergillus flavus, одобрена для контроля уровня мочевой кислоты у пациентов с синдромом лизиса опухоли (Elitek®). KRYSTEXXA® (пеглотиказа) представляет собой рекомбинантную уриказу (в основном свиную с последовательностью на карбоксильном конце от павиана), связанную несколькими молекулами PEG 10 кДа, одобренную для лечения хронической рефрактерной подагры. Однако, как упоминалось в другом месте, клинический опыт применения KRYSTEXXA® показал, что у значительного числа пациентов будут развиваться антитела к лекарственным средствам, которые ограничивают долгосрочную эффективность препарата. Таким образом, предварительное введение KRYSTEXXA® может быть противопоказанием для использования способов, представленных в настоящем документе.
Способы лечения, предоставленные в настоящем документе, могут позволить пациентам перейти на пероральную терапию подагры, такую как ингибиторы ксантиноксидазы, если и до тех пор, пока у таких пациентов не возникнет последующее проявление отложений мочевой кислоты, после чего будет проведен новый курс лечения, представленный в настоящем документе, в соответствии с любым из представленных способов. Таким образом, любой из способов, представленных в настоящем документе, может включать последующее введение перорального терапевтического средства от подагры в качестве дополнительного терапевтического средства после осуществления схемы лечения согласно любому из представленных способов. Считается, что пероральная терапия не может полностью предотвратить накопление кристаллов мочевой кислоты с течением времени у пациентов с хронической тофусной подагрой в анамнезе. В результате ожидается, что лечение, представленное в настоящем документе, вероятно, будет требоваться периодически у таких пациентов. Таким образом, у таких субъектов, субъекту также дополнительно вводят одну или несколько композиций в соответствии с любым из способов, представленных в настоящем документе.
Терапии, представленные в настоящем документе, могут позволить пациентам впоследствии лечиться терапевтическим средством, снижающим уровень мочевой кислоты, таким как уриказа. В некоторых вариантах осуществления, без иммуносупрессанта. В некоторых вариантах осуществления, без синтетических наноносителей, содержащих иммуносупрессант.
Терапия в соответствии с любым из способов, представленных в настоящем документе, может также включать предварительное лечение лекарственным средством против обострения подагры, например, колхицин или НПВП. Соответственно, любой из способов, представленных в настоящем документе, может дополнительно включать такое лекарственное средство против обострения подагры, при котором лекарственное средство против обострения подагры вводится одновременно с композицией, содержащей уриказу, и композицией, содержащей синтетические наноносители, включающие иммуносупрессант.
Идентификация или мониторинг субъекта, например, при измерении уровней мочевой кислоты в сыворотке и/или ADA, может быть стадией, включенной в любой из способов, представленных в настоящем документе. Способы, представленные в настоящем документе, могут включать стадию определения или получения уровня антител к уриказе (такого как титр) у субъекта, например, в образце от субъекта, и этот уровень может использоваться для идентификации субъекта для лечения или мониторинга субъекта, получающего лечение. В одном варианте осуществления лечение может быть любым из способов лечения, представленных в настоящем документе. Например, если уровень антител к уриказе ниже порогового значения (например, 1080), лечение может быть показано или не нуждается в корректировке. Если уровень антител к уриказе превышает пороговое значение (например, 1080), может быть показана корректировка лечения или дальнейший мониторинг или оценка.
В некоторых вариантах осуществления, если у такого субъекта развивается нежелательный иммунный ответ, субъекту дополнительно вводят одну или несколько композиций в соответствии с любым из способов, представленных в настоящем документе. В некоторых вариантах осуществления любого из способов, представленных в настоящем документе, субъекта наблюдают с помощью двухэнергетической компьютерной томографии (DECT), которая может использоваться для визуализации отложений мочевой кислоты в суставах и тканях. Визуализацию, такую как DECT, можно использовать для оценки эффективности лечения любым из способов или композиций, представленных в настоящем документе. В результате любой из способов, представленных в настоящем документе, может дополнительно включать стадию визуализации, например, с помощью DECT. В некоторых вариантах осуществления любого из способов, представленных в настоящем документе, субъект является субъектом, у которого подагра, такая как хроническая тофусная подагра, или состояние, связанное с подагрой, было диагностировано с помощью такой визуализации, например, с помощью DECT.
Субъекты
Субъекты, представленные в настоящем документе, могут нуждаться в лечении в соответствии с любым из способов, или композиций, или наборов, представленных в настоящем документе. К таким субъектам относятся субъекты с повышенными уровнями мочевой кислоты в сыворотке или отложениями мочевой кислоты. К таким субъектам относятся субъекты с гиперурикемией. Лечаший врач может определить субъектов, нуждающихся в лечении, как представленно в настоящем документе.
В некоторых вариантах осуществления любой из субъектов, подлежащих лечению, как представлено в любом из способов, представленных в настоящем документе, имеет подагру или состояние, связанное с подагрой, или другое состояние, как представлено в настоящем документе. В некоторых вариантах осуществления, любой из субъектов для лечения, как предусмотрено в любом из способов, при условии, что у субъекта было или ожидается обострение подагры.
В некоторых вариантах осуществления субъект страдает или имеет риск развития эрозивного заболевания костей, связанного с подагрой, циррозом или стеатогепатитом, связанным с подагрой, или висцеральной подагрой.
В некоторых вариантах осуществления субъект имеет повышенный уровень мочевой кислоты или имеет риск повышенного уровня мочевой кислоты, например, повышенный уровень мочевой кислоты в плазме или сыворотке. Когда уровень мочевой кислоты в крови может превышать физиологический предел растворимости, мочевая кислота может кристаллизоваться в тканях, включая суставы, и вызывать подагру и состояния, связанные с подагрой.
В некоторых вариантах осуществления, уровни мочевой кислоты в сыворотке ≥5 мг/дл, ≥6 мг/дл или ≥7 мг/дл указывают на то, что субъект может быть кандидатом на лечение любым из способов, или композиций или наборов, описанных в настоящем документе. В некоторых вариантах осуществления, такой субъект имеет уровень мочевой кислоты в сыворотке ≥6 мг/дл, например, между 6,1 мг/дл - 15 мг/дл, между 6,1 мг/дл - 10 мг/дл, 7 мг/дл - 15 мг/дл, 7 мг/дл - 10 мг/дл, 8 мг/дл - 15 мг/дл, 8 мг/дл - 10 мг/дл, 9 мг/дл -15 мг/дл, 9 мг/дл - 10 мг/дл, 10 мг/дл-15 мг/дл или 11 мг/дл- 14 мг/дл. В некоторых вариантах осуществления, субъект имеет уровень мочевой кислоты в сыворотке примерно 6,1 мг/дл, 6,2 мг/дл, 6,3 мг/дл, 6,4 мг/дл, 6,5 мг/дл, 6,7 мг/дл, 6,8 мг/дл, 6,9 мг/дл, 7,0 мг/дл, 7,1 мг/дл, 7,2 мг/дл, 7,3 мг/дл, 7,4 мг/дл, 7,5 мг/дл,7,6 мг/дл 7,7 мг/дл, 7,8 мг/дл, 7,9 мг/дл, 8,0 мг/дл, 8,1 мг/дл, 8,2 мг/дл, 8,3 мг/дл, 8,4 мг/дл, 8,5 мг/дл, 8,6 мг/дл, 8,7 мг/дл, 8,8 мг/дл, 8,9 мг/дл, 9,0 мг/дл, 9,1 мг/дл, 9,2 мг/дл, 9,3 мг/дл, 9,4 мг/дл, 9,5 мг/дл, 9,6 мг/дл, 9,7 мг/дл, 9,8 мг/дл, 9,9 мг/дл, 10,0 мг/дл, 10,1 мг/дл, 10,2 мг/дл, 10,3 мг/дл, 10,4 мг/дл, 10,5 мг/дл, 10,6 мг/дл, 10,7 мг/дл, 10,8 мг/дл, 10,9 мг/дл, 11,0 мг/дл, 11,1 мг/дл, 11,2 мг/дл, 11,3 мг/дл, 11,4 мг/дл, 11,5 мг/дл, 11,6 мг/дл, 11,7 мг/дл, 11,8 мг/дл, 11,9 мг/дл, 12,0 мг/дл, 12,1 мг/дл, 12,2 мг/дл, 12,3 мг/дл, 12,4 мг/дл, 12,5 мг/дл, 12,6 мг/дл, 12,7 мг/дл, 12,8 мг/дл, 12,9 мг/дл, 13,0 мг/дл, 13,1 мг/дл, 13,2 мг/дл, 13,3 мг/дл, 13,4 мг/дл, 13,5 мг/дл, 13,6 мг/дл, 13,7 мг/дл, 13,8 мг/дл, 13,9 мг/дл, 14,0 мг/дл, 14,1 мг/дл, 14,2 мг/дл, 14,3 мг/дл, 14,4 мг/дл, 14,5 мг/дл, 14,6 мг/дл, 14,7 мг/дл, 14,8 мг/дл, 14,9 мг/дл, 15,0 мг/дл или выше. В некоторых вариантах осуществления субъект имеет уровень мочевой кислоты в плазме или сыворотке 5,0 мг/дл, 5,1 мг/дл, 5,2 мг/дл, 5,3 мг/дл, 5,4 мг/дл, 5,5 мг/дл, 5,6 мг/дл, 5,7 мг/дл, 5,8 мг/дл, 5,9 мг/дл, 6,0 мг/дл, 6,1 мг/дл, 6,2 мг/дл, 6,3 мг/дл, 6,4 мг/дл, 6,5 мг/дл, 6,6 мг/дл, 6,7 мг/дл, 6,8 мг/дл, 6,9 мг/дл или 7,0 мг/дл. В некоторых вариантах осуществления субъект имеет уровень мочевой кислоты в плазме или сыворотке больше или равный 5,0 мг/дл, 5,1 мг/дл, 5,2 мг/дл, 5,3 мг/дл, 5,4 мг/дл, 5,5 мг/дл, 5,6 мг/дл, 5,7 мг/дл, 5,8 мг/дл, 5,9 мг/дл, 6,0 мг/дл, 6,1 мг/дл, 6,2 мг/дл, 6,3 мг/дл, 6,4 мг/дл, 6,5 мг/дл, 6,6 мг/дл, 6,7 мг/дл, 6,8 мг/дл, 6,9 мг/дл или 7,0 мг/дл.
В некоторых вариантах осуществления, субъект имеет гиперурикемию или существует риск ее развития. В некоторых вариантах осуществления, субъект имеет или у него существует риск развития, подагры, острой подагры, острой перемежающейся подагры, подагрического артрита, острого подагрического артрита, острой подагрической артропатии, острой полиартикулярной подагры, рецидивирующего подагрического артрита, хронической подагры (с тофусами или без), тофусной подагры, хронической тофусной подагры, хронической прогрессирующей подагры (с тофусами или без), хронической полиартикулярной подагры (с тофусами или без), хронической подагрической артропатии (с тофусами или без), идиопатической подагры, идиопатической хронической подагры (с тофусами или без), первичной подагры, хронической первичной подагры (с тофусами или без), рефрактерной подагры, такой как хроническая рефрактерная подагра, аксиальной подагрической артропатия, приступа подагры, обострение подагры, подагры (т.е. монартикулярного артрита большого пальца ноги), хирагры (т.е. моноартикулярного артрита кисти), подагрического бурсита, подагрического спондилита, подагрического синовита, подагрического тендосиновита, подагры, поражающей сухожилия и связки, свинец-индуцированной подагры (например, свинцовой подагры), подагры, индуцированой лекарственным средством, подагры из-за почечной недостаточности, подагры из-за болезни почек, хронической подагры из-за почечной недостаточности (с тофусами или без), хронической подагры из-за болезни почек (с тофусами или без), эрозивного заболевания костей, связанного с подагрой, инсульта, связанного с подагрой, сосудистых бляшек, связанных с подагрой, цирроза или стеатогепатита, связанного с подагрой, подагры, связанной с печенью, эпизодической и рецидивирующей подагры, диабета, связанного с повреждением поджелудочной железы при подагре, общего воспалительного процесса заболевания, усугубляемого подагрой, другой вторичной подагры или неуточненной подагры.
В некоторых вариантах осуществления субъект имеет или у него существует риск развития состояния, связанного с почечной системой, например, камни мочевыводящих путей вследствие подагры, мочекислый уролитиаз, мочекислый нефролитиаз, мочекислая мочекаменная болезнь, подагрическая нефропатия, острая подагрическая нефропатия, хроническая подагрическая нефропатия, уратная нефропатия, мочекислая нефропатия и подагрическая интерстициальная нефропатия.
В некоторых вариантах осуществления субъект имеет или у него существует риск развития состояния, связанного с нервной системой, например, периферическая автономная нейропатия вследствие подагры, подагрическая нейропатия, подагрическая периферическая нейропатия, подагрическая туннельная нейропатия или подагрический неврит.
В некоторых вариантах осуществления субъект имеет или у него существует риск развития состояния, связанного с сердечно-сосудистой системой, например, метаболического синдрома, гипертензии, ожирения, диабета, инфаркта миокарда, инсульта, дислипидеми, гипертриглицеридемии, инсулинорезистентности/гипергликемии, заболевания коронарной артерии/ишемической болезни сердца, заболевания коронарной артерии или закупорки, связанной с подагрой или гиперурикемией, сердечной недостаточности, заболевания периферических артерий, инсульта/цереброваскулярного заболевания, заболевания периферических сосудов и кардиомиопатии вследствие подагры.
В некоторых вариантах осуществления субъект имеет или у него существует риск развития состояния, связанного с глазной системой, включая, например, подагрический ирит, воспалительное заболевание глаза, вызванное подагрой, синдром сухого глаза, красный глаз, увеит, внутриглазная гипертензия, глаукома и катаракта.
В некоторых вариантах осуществления субъект имеет или у него существует риск развития состояния, связанного с кожей, включая, например, подагра наружного уха, подагрический дерматит, подагрическая экзема, подагрический панникулит и милиариальная подагра.
Композиции и наборы
Композиции, представленные в настоящем документе, могут включать неорганические или органические буферы (например, натриевые или калиевые соли фосфата, карбоната, ацетата или цитрата) и агенты регулирования pH (например, хлористоводродная кислота, гидроксид натрия или калия, соли цитрата или ацетата, аминокислоты и их соли) антиоксиданты (например, аскорбиновая кислота, альфа-токоферол), поверхностно-активные вещества (например, полисорбат 20, полисорбат 80, полиоксиэтилен9-10 нонилфенол, дезоксихолат натрия), растворы и/или крио/лио стабилизаторы (например, сахароза, лактоза, маннит, трегалоза), средства регулирования осмотического давления (например, соли или сахара), антибактериальные средства (например, бензойная кислота, фенол, гентамицин), противовспенивающие агенты (например, полидиметилсилозон), консерванты (например, тимеросал, 2-феноксиэтанол, EDTA), полимерные стабилизаторы и агенты регулирования вязкости (например, поливинилпирролидон, полоксамер 488, карбоксиметилцеллюлоза) и сорастворители (например, глицерин, полиэтиленгликоль, этанол).
Композиции согласно изобретению могут включать фармацевтически приемлемые эксципиенты. Композиции могут быть получены с использованием обычных методов фармацевтического производства и компаундирования для получения полезных лекарственных форм. Методы, подходящие для использования на практике настоящего изобретения, можно найти в Handbook of Industrial Mixing: Science and Practice, Edited by Edward L. Paul, Victor A. Atiemo-Obeng, and Suzanne M. Kresta, 2004 John Wiley & Sons, Inc.; and Pharmaceutics: The Science of Dosage Form Design, 2nd Ed. Edited by M. E. Auten, 2001, Churchill Livingstone. В варианте осуществления композиции суспендируют в стерильном физиологическом растворе для инъекций вместе с консервантом.
Следует понимать, что композиции изобретения могут быть получены любым подходящим способом, и изобретение никоим образом не ограничивается композициями, которые могут быть получены с использованием способов, описанных в настоящем документе. Выбор подходящего способа получения может потребовать внимания к свойствам конкретных связанных элементов.
В некоторых вариантах осуществления композиции получают в стерильных условиях или подвергают начальной или заключительной стерилизации. Это может гарантировать, что полученные композиции будут стерильными и неинфекционными, что повысит безопасность по сравнению с нестерильными композициями. Это обеспечивает значительную меру безопасности, особенно когда субъекты, получающие композиции, имеют дефекты иммунитета, страдают от инфекции и/или подвержены инфекции. В некоторых вариантах осуществления композиции могут быть лиофилизированы и храниться в суспензии или в виде лиофилизированного порошка в зависимости от выбора формулирования в течение продолжительных периодов времени без потери активности.
Введение согласно настоящему изобретению может осуществляться различными путями, включая, но не ограничиваясь этим, внутривенный путь. Композиции, упомянутые в настоящем документе, могут быть изготовлены и получены для введения обычными способами.
Композиции по настоящему изобретению можно вводить в эффективных количествах, таких как эффективные количества, описанные в настоящем документе в другом месте. Дозы композиций, как представлено в настоящем документе, могут включать различные количества элементов в соответствии с изобретением. Количество элементов, присутствующих в композициях для дозирования, может варьироваться в зависимости от их природы, достигаемого терапевтического эффекта и других подобных параметров. Композиции для дозирования можно вводить в соответствии с любой из частот, приведенных в настоящем документе.
Другой аспект раскрытия относится к наборам. В некоторых вариантах осуществления набор включает любую одну или несколько композиций, представленных в настоящем документе. В некоторых вариантах осуществления любого из представленных наборов, набор включает любую одну или несколько композиций, содержащих уриказу, как представлено в настоящем документе. Предпочтительно композиции, содержащие уриказу, находятся в количестве, обеспечивающем любую одну или несколько доз, как представлено в настоящем документе. Композиции, содержащие уриказу, могут находиться в одном контейнере или в более чем одном контейнере в наборе. В некоторых вариантах осуществления любого из представленных наборов, набор дополнительно включает любую одну или несколько композиций синтетических наноносителей, представленных в настоящем документе. Предпочтительно композиции синтетического наноносителя находятся в количестве, обеспечивающем одну или несколько доз синтетических наноносителей, представленных в настоящем документе. Композиции синтетического наноносителя могут находиться в одном контейнере или в более чем одном контейнере в наборе. В некоторых вариантах осуществления любого из представленных наборов контейнер представляет собой флакон или ампулу. В некоторых вариантах осуществления любого из представленных наборов, композиции находится в лиофилизированной форме, каждая в отдельном контейнере или в одном и том же контейнере, так что они могут быть восстановлены в последующее время. В некоторых вариантах осуществления любого из наборов, лиофилизированная композиция дополнительно включает сахар, такой как маннит. В некоторых вариантах осуществления любого из представленных наборов, композиции находятся в форме замороженной суспензии, каждая в отдельном контейнере или в том же контейнере, так что они могут быть восстановлены в последующее время. В некоторых вариантах осуществления любого из наборов, замороженная суспензия дополнительно включает PBS. В некоторых вариантах осуществления любого из наборов, набор дополнительно включает PBS и/или 0,9% хлорид натрия, USP. В некоторых вариантах осуществления любого из представленных наборов, набор дополнительно включает инструкции по восстановлению, смешиванию, введению и т.п. В некоторых вариантах осуществления любого из представленных наборов, инструкции включают описание любого из способов, описанных в настоящем документе. Инструкции могут быть в любой подходящей форме, например, в виде печатного вкладыша или этикетки. В некоторых вариантах осуществления любого из наборов, представленных в настоящем документе, набор дополнительно включает один или несколько шприцев или другие устройства, которое может доставлять композиции in vivo субъекту.
Примеры
Пример 1: Результаты клинических исследований SEL 212, не человека
Доклиническая разработка
SEL 212 использовали для лечения мышей с дефицитом уриказы и мышей дикого типа, крыс и нечеловеческих приматов для оценки эффективности, схем введения доз и безопасности.
Ранняя стадия клинического исследования на мышах с дефицитом уриказы
Фармакологическое исследование проводили на мышах с генетическим дефицитом эндогенной уриказы. В исследовании оценивали эффективность схемы введения доз, состоящего из трех иммунизаций с SEL 212 с последующими дозами только пегситиказы для предотвращения формирования ADA к пегситиказе. Период лечения составлял первые 14 дней исследования. В ходе исследования мышей разделяли на три группы лечения. В течение периода лечения:
• первая группа, называемая группа без лечения, не получала лечения;
• вторая группа, называемая группа пегситиказы, получала лечение только пегситиказой; и
• третья группа, называемая SVP рапамицин+группа пегситиказы, получала лечение SVP рапамицин совместно с пегситиказой.
Группа пегситиказы и SVP рапамицин+группа пегситиказы получали лечение в нулевой, седьмой и 14 дни периода лечения. Затем каждая группа получала лечение только пегситиказой на 35 и 42 дни исследования или в период заражения. Уровни уриказа-специфических ADA регистрировали для определения образования ADA к пегситиказе. Уровни мочевой кислоты измеряли для определения эффективности SVP рапамицин, вводимого совместно с пегситиказой, в снижении уровня мочевой кислоты ниже 6 мг/дл, что является целью лечения пациентов с подагрой.
Образование антител. Группа пегситиказы выработала уриказа-специфические ADA при воздействии пегситиказы в период лечения. Группа без лечения также выработала уриказа-специфические ADA, как только они получали пегситиказу. Несмотря на воздействие пегситиказы как в период лечения, так и в период заражения, группа SVP рапамицин+пегситиказы не вырабатывала уриказа-специфических ADA ни в один из этих периодов.
Уровни мочевой кислоты. После первоначального воздействия пегситиказы группа без лечения сохраняла высокий уровень мочевой кислоты примерно 10 мг/дл. В группе пегситиказы регистрировали уровни мочевой кислоты ниже 6 мг/дл после первой дозы в период лечения. Однако во время последующих доз в период лечения и в период заражения уровни мочевой кислоты возвращались к уровням, значительно превышающим 6 мг/дл. Напротив, в группе SVP рапамицин+пегситиказа поддерживались уровни мочевой кислоты, близкие к нулю на протяжении всего исследования.
Ранняя стадия клинического исследования на нечеловеческих приматах
Также проводили доклиническое исследование для оценки способности SVP рапамицин снижать образование уриказа-специфических ADA у нечеловеческих приматов. Как показано на фиг. 3, во время исследования:
• пегситиказу вводили отдельно, называемых группа пустых наночастиц, или
• вводили совместно с одним из двух уровней дозы SVP рапамицин, называемых группы SVP рапамицин 0,1X и SVP рапамицин 1X, соответственно. Группа SVP рапамицин 0,1X получила уровень дозы SVP рапамицин 0,3 мг/кг и группа SVP рапамицин 1X получила уровень дозы SVP рапамицин 3 мг/кг.
Группа пустых наночастиц получала три ежемесячные дозы пегситиказы, и каждая группа SVP рапамицина 0,1Х и группа SVP рапамицин 1X получали три ежемесячные дозы пегситиказы, совместно вводимой с SVP рапамицином. Затем все группы получали две ежемесячные дозы только пегситиказы. Группа SVP рапамицин 0,1X получила одну десятую дозы, введенной в группе SVP рапамицин 1X.
Образование антител. Было отмечено, что группа пустых наночастиц вырабатывала высокие уровни уриказа-специфических ADA к концу исследования. В группе SVP рапамицин 0,1X и группе SVP рапамицин 1X смогли значительно снизить уровни уриказа-специфических ADA по сравнению с группой пустых наночастиц и, в случае группы SVP рапамицин 1X, ингибировали образование антител. Наблюдения в этом исследовании подтвердили у нечеловеческих приматов уменьшение уриказа-специфических ADA, которое наблюдали у мышей.
Уровни мочевой кислоты. Как и ожидалось, влияние пегситиказы, вводимой отдельно, или пегситиказы, вводимой совместно с SVP рапамицином, на уровни мочевой кислоты у нечеловеческих приматов не могло быть определено из-за активности естественной уриказы у этих животных.
Основываясь на этих доклинических исследованиях, а также токсикологических исследованиях, проведенных в соответствии с нормативными документами, именуемыми современной надлежащей лабораторной практикой или GLP, считается, что SEL 212 продемонстрировал достаточную эффективность и безопасность на доклинических моделях на животных, чтобы подтвердить переход к клиническим исследованиям.
Пример 2: Результаты клинических исследований SEL 212, человек
Фаза 1а клинических исследований
Фаза 1а клинических исследований для SEL 212 представляла собой исследование нарастающей дозы одной пегситиказы с участием 22 субъектов с повышенным уровнем мочевой кислоты в сыворотке более 6 мг/дл, которых разделяли на пять когорт. Каждая когорта получала однократную внутривенную инфузию пегситиказы при следующих уровнях доз 0,1 мг/кг для когорты #1, 0,2 мг/кг для когорты #2, 0,4 мг/кг для когорты #3, 0,8 мг/кг для когорты #4 и 1,2 мг/кг для когорты #5. Введение доз начинали с самой низкой дозы, и только после того, как всей когорте безопасно вводили дозы, начинали следующую когорту. За субъектами наблюдали в течение 30-дневного периода после инфузии с визитами, происходящими на 7, 14, 21 день, и в конце визитов исследования на день 30. Кровь и сыворотку каждого пациента оценивали на содержание мочевой кислоты в сыворотке, ADA (в частности, анти-пег, анти-уриказа и анти-пегситиказа) и параметры безопасности. Было отмечено, что пегситиказа не продемонстрировала серьезных побочных эффектов и хорошо переносилась при пяти испытанных уровнях доз. Кроме того, было отмечено, что пегситиказа быстро снижала (в течение нескольких часов) и поддерживала средние уровни мочевой кислоты в сыворотке ниже 6 мг/дл для каждой когорты в течение 14-30 дней, в зависимости от уровня дозы. В соответствии с доклиническими исследованиями на животных, пегситиказа индуцировала уриказа-специфические ADA у всех субъектов с различными уровнями в этой фазе 1a исследования.
На фиг. 4 показаны средние уровни мочевой кислоты в сыворотке пяти когорт фазы 1a клинических исследований, протестированных с различными интервалами измерения (день 7, 14, 21 и 30) в течение 30-дневного периода после однократной внутривенной инфузии пегситиказы в начале исследования.
Уровни мочевой кислоты в сыворотке измеряли на исходном уровне и на седьмой, 14, 21 и 30 дни, а уровни уриказа-специфических ADA, на исходном уровне и на седьмой, 14 и 30 дни после однократной внутривенной инъекции пегситиказы. Уровни уриказа-специфических ADA на 21 день в фазе 1a клинических исследований не измеряли. Основываясь на результатах фазы 1a клинических исследований, было отмечено, что пегситиказа в переносимой дозе способна достичь и поддерживать снижение уровня мочевой кислоты в сыворотке ниже целевого уровня 6 мг/дл в течение 30-дневного периода в отсутствие ингибирующих уриказа-специфических ADA.
Фаза 1b клинических исследований
В фазу 1b клинических исследований было включено 63 пациента с уровнем мочевой кислоты в сыворотке более 6 мг/дл, разделенных на 11 когорт. Однократную внутривенную инфузию одного SVP рапамицина в следующих нарастающих дозах вводили четырем группам в нарастающем порядке. Каждая когорта состояла из семи пациентов и была обозначена следующим образом: когорта #1 (0,03 мг/кг), когорта #3 (0,1 мг/кг), когорта #5 (0,3 мг/кг) и когорта #7 (0,5 мг/кг), в совокупности, когорты SVP рапамицин. После успешного и безопасного введения когорте одного SVP рапамицина соответствующий уровень дозы SVP рапамицина объединяли с фиксированной дозой пегсициказы (0,4 мг/кг). Комбинацию вводили совместно последовательно в виде однократной внутривенной инфузии, причем инфузия SVP рапамицина предшествовала инфузии пегситиказы. Обозначение когорт является следующим для шести когорт (5 пациентов на когорту), которые представляли собой когорту #2 (SVP рапамицин 0,03 мг/кг+0,4 мг/кг пегситиказы), когорту #4 (SVP рапамицин 0,1 мг/кг+0,4 мг/кг пегситиказы), когорту #6 (SVP рапамицин 0,3 мг/кг+0,4 мг/кг пегситиказы), когорту #10 (0,4 мг/кг пегситиказы+0,03 мг/кг SVP рапамицин, разделенные 48 часами), когорту #12 (SVP рапамицин 0,15 мг/кг+0,4 мг/кг пегситиказы) и когорту #14 (SVP рапамицин 0,1 мг/кг+0,4 мг/кг пегситиказы) в совокупности когорты SEL 212. В когорте #9 фиксированное количество только пегситиказы при уровне дозы 0,4 мг/кг вводили пяти пациентам, которая называется когорта пегситиказы. Также представлены способы такого лечения. За субъектами наблюдали в течение 30-дневного периода после инфузии с визитами, происходящими на 7, 14, 21 день, и в конце визитов исследования на день 30. Кровь и сыворотку каждого пациента оценивали на содержание мочевой кислоты в сыворотке, ADA (в частности, анти-пег, анти-уриказа и анти-пегситиказа) и параметры безопасности. Основная цель фазы 1b клинического исследования заключалась в оценке безопасности и переносимости SVP рапамицина в отдельности и в комбинации с фиксированной дозой пегситиказы. Вторичной клинической целью было оценить способность SVP рапамицина, вводимого совместно с пегситиказой, снижать уровни мочевой кислоты в сыворотке и уменьшать образование уриказа-специфических ADA по сравнению с введением только пегситиказы.
На фиг. 5 показаны уровни мочевой кислоты в сыворотке когорты #3 из фазы 1а клинического исследования, в котором субъекты получали фиксированное количество только пегситиказы (при том же 0,4 мг/кг пегситиказы. Также на первом графике представлены данные когорты #9 (пегситиказа 0,4 мг/кг) фазы 1а клинического исследования. Этот график представляет воспроизводимость данных в двух отдельных исследованиях. В обеих когортах наблюдается начальный контроль мочевой кислоты в сыворотке (уровни поддерживаются ниже 6 мг/дл), но после 14 дня индивидуумы теряют активность фермента. Также на фиг. 5 показаны данные по когортам только SVP рапамицин. Все значения остаются практически неизменными в течение 30 дней исследования, что указывает на то, что SVP рапамицин сам по себе не влияет на уровень мочевой кислоты в сыворотке. Для когорты #2 из фазы 1b клинического исследования, которая получала самую низкую дозу SVP рапамицина, вводимого совместно с пегситиказой, было отмечено, что у четырех из пяти испытуемых субъектов сохранялся уровень мочевой кислоты в сыворотке ниже 6 мг/дл на 21 день исследования. Также было отмечено, что у четырех из пяти субъектов в когорте #4 из фазы 1b клинического исследования, которые получили вторую самую низкую дозу SVP рапамицина, вводимого совместно с пегситиказой, поддерживались уровни мочевой кислоты в сыворотке менее 0,1 мг/дл вплоть до дня 30. Для когорты #6 (SEL 212 когорта), было отмечено, что у четырех (из запланированных пяти) субъектов поддерживались уровни мочевой кислоты в сыворотке менее 0,1 мг/дл вплоть до дня 21 и у двоих (из запланированных пяти) субъектов поддерживались уровни мочевой кислоты в сыворотке менее 0,1 мг/дл вплоть до дня 30. Для сравнения, в когорте #9 (когорта пегситиказы) четыре из пяти субъектов вернулись к исходному уровню мочевой кислоты в сыворотке к 30-му дню.
На фиг. 5 показаны уровни мочевой кислоты в сыворотке и уровни уриказа-специфических ADA для каждого субъекта в когорте #3 фазы 1a клинического исследования и когорте #9 (когорта пегситиказы) фазы 1b клинического исследования для сравнения с уровнями мочевой кислоты в сыворотке и уровнями уриказа-специфических ADA для каждого субъекта в когорте # 4 (когорта SEL 212) фазы 1b клинического исследования. Когорта #3 из фазы 1а клинического исследования изображена вместе с когортой #9 из фазы 1b клинического исследования для целей сравнения с когортой #4 из фазы 1b клинического исследования, поскольку субъекты в этих когортах получали одинаковую фиксированную дозу пегситиказы. Кроме того, когорта #4 из фазы 1b клинического исследования изображена на фиг. 5, потому что субъекты в когорте #4 из фазы 1b клинического исследования получили более высокую дозу SVP рапамицина, чем субъекты в когорте #2 в фазе 1b клинического исследования, другой когорте SEL 212, для которой были доступны данные за 30-дневный период наблюдения из фазы 1b клинического исследования.
Как показано на фиг. 5, в когорте #3 из фазы 1a клинического исследования и когорте #9 из фазы 1b клинического исследования наблюдали образование уриказа-специфических ADA на день 14, что приводило к возврату к исходным уровням мочевой кислоты в сыворотке. Для сравнения, для когорты #4 из фазы 1b клинического исследования было отмечено минимальное образование уриказа-специфических ADA у четырех из пяти исследуемых субъектов с соответствующим поддержанием контроля уровней мочевой кислоты в сыворотке вплоть до дня 30. В фазе 1а клинического исследования уровни уриказа-специфических ADA на 21 день не измеряли. Однако в ходе проведения клинического исследования фазы 1а стало известно, что было бы полезно измерить уровни уриказа-специфических ADA на 21-й день, чтобы более полно понять любые изменения таких уровней между днем 14 и днем 30. В результате для фазы 1b клинического исследования проверяли уровни уриказа-специфических ADA на день 21.
Дополнительные данные сывороточной мочевой кислоты и уриказа-специфических ADA после дня 30 собирали для трех субъектов в когорте #4 (SEL 212 когорта), у которых на день 30 уровни мочевой кислоты в сыворотке и уриказа-специфических ADA были очень низким или отсутствовали. Данные на день 37 собирали для всех трех из этих субъектов и снова на день 42 или день 44 для двух из трех субъектов. У каждого из этих трех субъектов отсутствовали или были очень низкие уровни уриказа-специфических ADA на день 37, день 42 или день 44, в зависимости от ситуации. Уровни мочевой кислоты в сыворотке оставались ниже исходного уровня на день 37 у всех трех субъектов. Что касается двух субъектов, для которых были доступны данные на день 42 или день 44, уровни мочевой кислоты в сыворотке приблизились или превысили исходный уровень на последнем контрольном моменте времени. По данным наблюдений из фазы 1b клинических исследований, SEL 212 способен контролировать уровень мочевой кислоты в течение по меньшей мере 30 дней у большинства субъектов в когорте # 4.
На комбинированной основе в общей сложности 85 субъектов получали дозу либо SEL 212 (SVP рапамицин и пегситиказа), либо только SVP рапамицина или только пегситиказы в связи с клиническими исследованиями фазы 1a и фазы 1b. В целом было отмечено, что SEAL 212 и его компоненты, SVP рапамицин и пегситиказа, хорошо переносятся. В обоих клинических испытаниях фазы 1 было в общей сложности четыре серьезных нежелательных явления, или SAE. Все SAE полностью устранены.
На фиг.6 показаны уровни мочевой кислоты в сыворотке и уровни уриказа-специфических ADA для каждого субъекта в когорте #3 фазы 1a клинического исследования и когорте #9 (когорта пегситиказы) фазы 1b клинического исследования для сравнения с уровнями мочевой кислоты в сыворотке и уровнями уриказа-специфических ADA для каждого субъекта в когорте #4 (когорта SEL-212) и когорте #6 (когорта SEL-212) в фазе 1b клинического исследования. Когорта #3 из фазы 1a клинического исследования также изображена вместе с когортой #9 из фазы 1b клинического исследования для целей сравнения с когортой #4 и когортой #6 из фазы 1b клинического исследования, потому что субъекты в этих когортах получали одинаковую фиксированную дозу пегситиказы. Кроме того, изображена когорта #4 из фазы 1b клинического исследования, поскольку субъекты в когорте #4 из фазы 1b клинического исследования получили более высокую дозу SVP-рапамицина, чем субъекты в когорте #2 фазы 1b клинического исследования. Также включена когорта #6 из фазы 1b клинического исследования, поскольку эти субъекты получили самую высокую дозу SVP-рапамицина, протестированную на сегодняшний день-выше, чем в обеих когортах #2 и #4.
На фиг. 7 представлено непрямое сравнение эффективности SEL-212 в когорте #6 фазы 1b клинического исследования с когортой #5 фазы 1b клинического исследования и данные двух повторных, рандомизированных, двойных слепых, плацебо-контролируемых клинических исследований KRYSTEXXA®, как описано в the Journal of the American Medical Association in 2011. Эти два клинических исследования KRYSTEXXA® включали 85 пациентов, которые получали дозы KRYSTEXXA® раз в две недели, 84 пациента, которые получали ежемесячные дозы KRYSTEXXA® и 43 пациента, которые получали плацебо.
KRYSTEXXA® был одобрен для лечения рефрактерной подагры в режиме приема раз в две недели, тогда как режим ежемесячного приема KRYSTEXXA® не был одобрен для маркетинга. На графике слева внизу представлены данные за четырехнедельный период после введения первой дозы Krystexxa® от когорт субъектов в клинических испытаниях KRYSTEXXA®, которые получали ежемесячные дозы.
У субъектов, получавших контроль-плацебо, обозначенных незакрашенными кружками на фиг.7, уровни мочевой кислоты превышали 6 мг/дл в течение всех четырех недель. Субъекты, получавшие KRYSTEXXA®, которые в дальнейшем ответили на терапию, как определено поддержанием уровней мочевой кислоты ниже 6 мг/дл в течение 80% времени трех и шести месяцев, отмечены черными кружками. Субъекты, получавшие KRYSTEXXA®, которые впоследствии перестали отвечать на терапию, что определялось неспособностью поддерживать уровень мочевой кислоты ниже 6 мг/дл в течение 80% времени на третьем и шестом месяцах, обозначены черными треугольниками. Только 35% субъектов, получавших KRYSTEXXA® в когортах с ежемесячным дозированием, были классифицированы как пациенты, ответившие на лечение. Примечательно, что даже через четыре недели средние уровни мочевой кислоты были выше 6 мг/дл у не ответивших на лечение, что составляет 65% субъектов, и были выше 4 мг/дл у пациентов, ответившие на лечение. У 89% всех субъектов, получавших лечение KRYSTEXXA®, выработались ADA. Для сравнения, график справа на фиг. 7 отображает данные когорты #5 фазы 1b клинического испытания, которая получала однократную дозу только SVP-рапамицина, и когорты #6 фазы 1b клинического испытания, которая получала однократную дозу SEL-212. Все пять субъектов в когорте #6 фазы 1b клинического исследования, получавших SEL-212, поддерживали уровни мочевой кислоты в сыворотке менее 0,1 мг/дл в течение 30 дней. Субъекты в когорте #5 фазы 1b клинического исследования, получавшие только SVP-рапамицин, не испытали значительного снижения уровней мочевой кислоты, поскольку такие уровни оставались относительно постоянными в течение 30-дневного периода. Также показано сравнение данных когорты #5 фазы 1b клинического исследования, которая получала однократную дозу SVP-рапамицина, с когортой #9 фазы 1b клинического исследования, которая получала только пегститиказу.
Хотя считается, что приведенное выше сравнение полезно для оценки результатов когорты #6 фазы 1b клинического исследования, фаза 1b клинического исследования и клинические исследования KRYSTEXXA® были отдельными исследованиями, проведенными разными исследователями в разных местах. Кроме того, имелись существенные различия, в том числе, например, то, что клинические исследования KRYSTEXXA® были двойными слепыми исследованиями с участием значительного числа пациентов с рефрактерной подагрой, в то время как фаза 1b клинического исследования оценивала SEL-212 в неизмененном виде у небольшого числа субъектов с повышенными уровнями мочевой кислоты. Более того, можно было сравнить только эффективность SEL-212 в течение четырехнедельного периода после первой инъекции KRYSTEXXA®, поскольку SEL-212 еще не оценивался в многодозовом клиническом исследовании.
Дополнительные данные по мочевой кислоте в сыворотке и уриказа-специфических ADA собирали после 30 дня для трех субъектов в когорте #4 (когорта SEL-212), у которых на день 30 уровни мочевой кислоты в сыворотке и уриказа-специфических ADA были очень низкими или отсутствовали. Данные собирали на день 37 для всех трех из этих субъектов и снова на день 42 или день 44 для двух из трех субъектов. У каждого из этих трех субъектов отсутствовали или были очень низкие уровни уриказа-специфических ADA на день 37, день 42 или день 44, в зависимости от ситуации. Уровни мочевой кислоты в сыворотке оставались ниже исходного уровня на день 37 у всех трех субъектов. Что касается двух субъектов, для которых были доступны данные на день 42 или день 44, уровни мочевой кислоты в сыворотке приблизились или превысили исходный уровень на последнем контрольном моменте времени.
Пример 3 - Фаза 2 клинических исследований
Здесь представлена фаза 2 клинических исследований SEL-212. Исследование состоит из многократных доз SEL-212, вводимых одновременно с дозами SEL-037. SEL-212 представляет собой комбинацию SEL-037 и SEL-110. SEL-037 включает пегситиказу (рекомбинантную пегилированную уратоксидазу Candida). SEL-110 представляет собой наночастицу, содержащую PLA (поли(D, L-лактид)) и PLA-PEG (поли(D, L-лактид)-блок-поли(этилен-гликоль)), инкапсулирующую рапамицин.
SEL-037 может включать фосфатный буфер и маннит в качестве эксципиентов. Перед введением 6 мг, измеренный как белок уриказы, лиофилизированный SEL-037 может быть восстановлен 1,1 мл стерильной воды для инъекций, USP (United States Pharmacopeia), которая образует концентрированный раствор 6 мг/мл. Достаточный объем восстановленного SEL-037 при 0,2 мг/кг или 0,4 мг/кг, измеренные как белок уриказы, разводили в 100 мл 0,9% хлорида натрия для инъекций, USP, и вводили дозы в виде однократной внутривенной инфузии с помощью инфузионного насоса в течение 60 минут.
SEL-110 предоставляется в виде суспензии 2 мг/мл, в зависимости от содержания рапамицина, в PBS. Соответствующее количество SEL-110 из расчета на мг/кг набирают в шприц или шприцы и вводят в виде внутривенной инфузии с помощью шприцевого инфузионного насоса. Если субъект входит в когорты 3, 4, 5, 6, 7 и 8, то SEL-110 вводится до SEL-037. SEL-110 доставляется с помощью шприцевого инфузионного насоса с одной постоянной скоростью, достаточной для доставки объема дозы в течение 55 минут одновременно с 60-минутной инфузией 125 мл физиологического раствора, и затем начинается на 60-минутной отметке инфузия SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8).
48 субъектов разделяли на 8 когорт для дозирования. Каждая когорта состояла из 6 пациентов. Когорта 3 получала SEL-212 (с 0,05 мг/кг SEL-110+0,2 мг/кг пегситиказы), когорта 4 получала SEL-212 (с 0,05 мг/кг SEL-110+0,4 мг/кг пегситиказы), когорта 5 получала SEL-212 (с 0,08 мг/кг SEL-110+0,2 мг/кг пегситиказы), когорта 6 получала SEL-212 (с 0,08 мг/кг SEL-110+0,4 мг/кг пегситиказы), когорта 7 получала SEL-212 (с 0,1 мг/кг SEL-110+0,2 мг/кг пегситиказы) и когорта 8 получала SEL-212 (с 0,1 мг/кг SEL-110+0,4 мг/кг пегситиказы).
Распределение субъектов
Все включенные субъекты были изначально рандомизированы на 4 когорты таким образом, что по достижении 12 субъектов в общей сложности для всех 4 когорт, каждая когорта включала 3 субъектов. После завершения по меньшей мере одного цикла лечения состояние субъекта оценивали перед открытием включения в исследование для всех когорт. Будущее включение в исследование является рандомизированным между всеми открытыми когортами.
Премедикация при лечении исследуемыми препаратами
Все субъекты получали 180 мг фексофенадина перорально в ночь до приема исследуемого препарата (12 ч ± 2 ч) и снова за 2 ± 1 час до приема исследуемого препарата (т.е. SEL-110 для когорт 3, 4, 5, 6. 7 и 8). Кроме того, они также получали метилпреднизолон 40 мг (или эквивалентное лекарство, например, преднизон 50 мг внутривенно или дексаметазон 8 мг внутривенно) внутривенно за 1 ± 0,5 часа до приема исследуемого препарата (т.е. предшествующий SEL-110 для когорт 3, 4, 5, 6, 7 и 8). Это происходит для каждой лечебной дозы исследуемого препарата (часть А, периоды лечения 1-3 и для части В, периоды лечения 4 и 5). Когорты 3-6 получали первую и вторую дозы.
Премедикация на случай обострения подагры
Всем субъектам, отвечающим всем критериям включения и исключения, назначается премедикация для профилактики обострения подагры. Схема начинают за 1 неделю до первого приема исследуемого препарата и продолжают до тех пор, пока субъект участвует в клиническом исследовании. Субъект получает колхицин 1,2 мг в виде однократной ударной дозы. Затем они продолжают принимать колхицин в дозе 0,6 мг QD (один раз в день) до конца своего участия в исследовании. Если есть противопоказания к колхицину, субъект получает 600 мг ибупрофена TID (3 раза в день) или эквивалентную дозу НПВП. При наличии противопоказаний к колхицину и НПВП субъект не получает премедикации от обострения подагры. Прием препаратов для профилактики обострения подагры продолжается до тех пор, пока субъект участвует в клиническом исследовании. Субъекты, которые начали получать НПВП в качестве лекарства для профилактики обострения подагры из-за противопоказаний к колхицину, продолжают получать НПВП, пока субъект включен в исследование.
Продолжительность лечения для когорты 3, когорты 4, когорты 5, когорты 6, когорты 7 и когорты 8
Период лечения 1 - Часть А
Субъектов обследовали в период 45 дней после введения доз. Как только они соответствовали критериям включения/исключения и все оценки были признаны приемлемыми, их инструктировали о том, когда начать премедикацию (дата и лекарства, День -7) для профилактики обострения подагры. День первоначального введения исследуемого лекарственного средства обозначали как День 0. Пациенты, соответствующие критериям участия, которые были отнесены к когортам 3, 4. 5, 6, 7 и 8, получили однократную внутривенную инфузию SEL-110 (доза в расчете на мг/кг). SEL110 доставляли шприцевым инфузионным насосом с одной постоянной скоростью, достаточной для доставки объема дозы в течение периода 55 минут. Одновременно с введением SEL-110 субъект получил 125 мл физиологического раствора в течение 60 минут. Затем (± 3 минуты) инфузией с помощью инфузионного насоса вводили SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8), разведенный в 100 мл физиологического раствора, доставляемый в течение 60 минут. Субъекты оставались в клинике в течение 9 часов после начала инфузии SEL-110 для оценки безопасности и ФК анализа крови. Субъекты возвращались для анализов крови на ФК и ФД в период лечения 1, дни 1,7, 14, 21 и оценки безопасности и анализов крови на антитела в период лечения 1, дни 7, 14, 21.
Период лечения 2 - часть A
Утром периода лечения 2, день 0, субъекты прибывали в клинику для введения доз исследуемого препарата. Пациенты, соответствующие критериям участия, которые были отнесены к когортам 3, 4, 5, 6, 7 и 8, получили однократную внутривенную инфузию SEL-110 (доза в расчете на мг/кг). SEL-110 доставляли шприцевым инфузионным насосом с одной постоянной скоростью, достаточной для доставки объема дозы в течение периода 55 минут. Одновременно с введением SEL-110 субъект получил 125 мл физиологического раствора в течение 60 минут. Затем (± 3 минуты) инфузией с помощью инфузионного насоса вводили SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8), разведенный в 100 мл физиологического раствора, доставляемый в течение 60 минут. Субъекты оставались в клинике в течение 9 часов после начала инфузии SEL-110 для оценки безопасности и ФК анализа крови. Субъекты возвращались для анализов крови на ФК и ФД в период лечения 2, дни 1, 7, 14, 21 и оценки безопасности и анализов крови на антитела в период лечения 2, дни 7, 14, 21.
Период лечения 3 - часть A
Утром периода лечения 3, день 0, субъекты прибывают в клинику для введения доз исследуемого препарата. Пациенты, соответствующие критериям участия, которые были отнесены к когортам 3, 4, 5, 6, 7 и 8, получают однократную внутривенную инфузию SEL-110 (доза в расчете на мг/кг). SEL-110 доставляют шприцевым инфузионным насосом с одной постоянной скоростью, достаточной для доставки объема дозы в течение периода 55 минут. Одновременно с введением SEL-110 субъект получает 125 мл физиологического раствора в течение 60 минут. Затем (± 3 минуты) инфузией с помощью инфузионного насоса вводят SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8), разведенный в 100 мл физиологического раствора, доставляемый в течение 60 минут. Субъекты остаются в клинике в течение 9 часов после начала инфузии SEL-110 для оценки безопасности и ФК анализа крови. Субъекты возвращаются для анализов крови на ФК и ФД в период лечения 3, дни 1, 7, 14 и 21 и оценки безопасности и анализов крови на антитела в период лечения 3, дни 7, 14, 21.
Период лечения 4 - часть B
Утром периода лечения 4, день 0, субъекты прибывают в клинику для введения доз исследуемого препарата. Субъекты получат однократную внутривенную инфузию SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8), разведенного в 100 мл физиологического раствора, в течение 60 минут с помощью инфузионного насоса. Субъекты остаются в клинике в течение 9 часов после начала инфузии SEL-037 для оценки безопасности и ФК анализа крови. Субъекты возвращаются для анализов крови на ФК и ФД в период лечения 4, дни 1, 7, 14, 21 и оценки безопасности и анализов крови на антитела в период лечения 4, дни 7, 14, 21.
Период лечения 5 - часть B
Утром периода лечения 5, день 0, субъекты прибывают в клинику для введения доз исследуемого препарата. Субъекты получат однократную внутривенную инфузию SEL-037 (0,2 мг/кг для когорт 3, 5 и 7; 0,4 мг/кг для когорт 4, 6 и 8), разведенного в 100 мл физиологического раствора, в течение 60 минут с помощью инфузионного насоса. Субъекты остаются в клинике в течение 9 часов после начала инфузии SEL-037 для оценки безопасности и ФК анализа крови. Субъекты возвращаются для анализов крови на ФК и ФД в период лечения 5, дни 1, 7, 14, 21 и оценки безопасности и анализов крови на антитела в период лечения 5, дни 7, 14, 21.
Результаты
Когда пегситиказу вводили отдельно в фазе 1, описанной в примере 2, 57% (4 из 7 пациентов) пациентов с подагрой в анамнезе имели признаки обострения подагры в первый месяц после приема исследуемого лекарственного средства (таблица 1). Однако, в отличие от этого, когда синтетические наноносители PLA/PLA-PEG, содержащие рапамицин, одновременно вводили с пегситиказой в фазе 2 исследования, описанном в примере 3, только одно обострение подагры было зарегистрировано у субъектов, которые имели подагру в анамнезе (16 из 63 включенных в исследование пациентов) (Таблица 2). Этот субъект находился в когорте, получавшей только наноноситель, содержащий рапамицин (без уриказы). Поскольку этот субъект не получал уриказную терапию, уровень мочевой кислоты в сыворотке у этого субъекта существенно не снизился. Таким образом, обострение не было связано с изменением уровня мочевой кислоты в сыворотке крови. Еще один субъект, у которого не было предварительного диагноза подагры, сообщил об обострении после лечения. Уровень мочевой кислоты в сыворотке этого пациента снизился с 8,8 мг/дл до 0,1 мг/дл в течение 90 минут после введения препарата. Таким образом, хотя у этого субъекта до исследования был поставлен диагноз бессимптомной гиперурикемии, обострение, похоже, совпало с падением уровня мочевой кислоты в сыворотке.
Таблица 1. Обострения у субъектов с подагрой в анамнезе
Таблица 2. Обострения у субъектов SEL-212
Была проведена фаза 2 исследования (Пример 3). Это исследование включало введение нескольких внутривенных вливаний синтетических наноносителей PLA/PLA-PEG, содержащих рапамицин вместе с пегситиказой, для оценки его безопасности и переносимости. Тридцать восемь субъектов рандомизировали и вводили дозы, причем 8 субъектов сообщили, что страдают от обострения подагры (таблица 3).
Таблица 3. Субъекты, перенесшие обострение подагры после лечения
Частоту обострения у вышеуказанных субъектов сравнивали с частотой обострения в исследованиях пеглотиказы. Те субъекты, которые получали профилактику обострения подагры (только колхицином или НПВП), были выбраны в соответствии с условиями субъекта пеглотиказа. Частота обострений (количество обострений на пациента в месяц) была выбрана в качестве меры для сравнения частоты обострений. Этот показатель был выбран на основании того факта, что данные исследования охватывают 2 месяца или 2 цикла лечения; в то время как исследования пеглотиказы варьировались по продолжительности от 35 дней (Sundy et al., Pharmacokinetics and pharmacodynamics of intravenous PEGylated recombinant mammalian urate oxidase in patients with refractory gout. Arthritis and Rheumatism. Vol. 56, No. 3, March 2007, pp 1021-1028) до 6 месяцев (John S. Sundy, MD, PhD; Herbert S. B. Baraf, MD; Robert A. Yood, MD; et al. Efficacy and Tolerability of pegloticase for the Treatment of Chronic Gout in Patients Refractory to Conventional TreatmentTwo Randomized Controlled Trials. JAMA. 2011;306(7):711-720). Месячные показатели пациентов были выбраны для сравнения между исследованиями.
Когорты 3 и 4 объединяли вместе для этого анализа, так как им вводили одинаковую дозу синтетических наноносителей, содержащих рапамицин (0,05 мг/кг), и аналогично когорты 5 и 6 объединяли вместе (с синтетическим наноносителем, содержащим дозу рапамицина 0,08 мг/кг). В когортах 3 и 4 19 субъектов получили дозу в течение 24 циклов лечения. Не все субъекты получали все виды лечения, поскольку некоторые субъекты досрочно выбывали из исследования после изменений протокола. К настоящему времени в когортах 5 и 6 13 субъектов получили в общей сложности 24 цикла лечения. Это означает, что у субъектов, получавших профилактику обострения подагры, в общей сложности произошло 2 обострения в течение 48 циклов лечения. Это можно приравнять к 0,04 обострениям на цикл лечения; другими словами, частота обострения составляет 0,04 обострения на пациента в месяц.
Напротив, в фазе 3 исследований пеглотиказы (John S. Sundy, MD, PhD; Herbert S. B. Baraf, MD; Robert A. Yood, MD; et al. Efficacy and Tolerability of Pegloticase for the Treatment of Chronic Gout in Patients Refractory to Conventional TreatmentTwo Randomized Controlled Trials. JAMA. 2011;306(7):711-720) сообщалось о следующем: 2,3 обострения на пациента в течение первых 3 месяцев у 85 пациентов, получавших пеглотиказу раз в две недели, и 2,7 обострения на пациента в течение первых 3 месяцев у 84 пациентов, получавших пеглотиказу ежемесячно. Эти цифры соответствуют частоте обострения 0,77 и 0,9 обострения на пациента в месяц, соответственно.
Дальнейшие сравнения можно провести с двумя основными фирменными пероральными препаратами, снижающими уровень мочевой кислоты, фебуксостатом и лесинурадом. В фазе 3 рандомизированного двойного слепого многоцентрового исследования безопасность и эффективность фебуксостата изучали в течение 52 недель (Michael A. Becker, M.D., H. Ralph Schumacher, Jr., M.D., Robert L. Wortmann, M.D., Patricia A. MacDonald, B.S.N., N.P., Denise Eustace, B.A., William A. Palo, M.S., Janet Streit, M.S., and Nancy Joseph-Ridge, M.D. Febuxostat Compared with Allopurinol in Patients with Hyperuricemia and Gout. N Engl J Med 2005; 353:2450-2461December 8, 2005). Период сравнения для этого анализа включал только первые 8 недель этого исследования, когда проводили профилактику обострения подагры. При дозе 80 мг/день 55 из 255 субъектов потребовалось лечение по меньшей мере одного обострения подагры. Это было бы эквивалентно частоте обострения по меньшей мере 0,22 обострений на пациента в месяц, а возможно и больше. При дозе 120 мг/день 90 из 250 субъектов нуждались в лечении по меньшей мере одного обострения подагры, что соответствует, по меньшей мере, частоте обострения 0,36 обострений на пациента в месяц, а возможно и более.
В фазе 2 рандомизированного двойного слепого исследования для оценки эффективности и переносимости лесинурада субъектам давали колхицин для профилактики обострения подагры и лечили лесинурадом в различных дозах в течение 1 месяца (Perez -Ruiz F, Sundy JS, Miner JN for the RDEA594-203 Study Group, et al. Lesinurad in combination with allopurinol: results of a phase 2, randomised, double-blind study in patients with gout with an inadequate response to allopurinol, Annals of the Rheumatic Diseases 2016;75:1074-1080). В течение этого периода лечения обострения подагры, требующие лечения, были зарегистрированы у 10 из 46 пациентов в месяц при дозе 200 мг в день, у 13 из 42 пациентов в месяц при дозе 400 мг в день и у 15 из 48 пациентов в месяц при дозе 600 мг в день. Это соответствует частоте обострения 0,22, 0,31 и 0,31 обострений на пациента в месяц, соответственно.
Табличные данные, в которых приводится сравнение частоты обострений между различными лекарствами наряду с их эффективностью в снижении уровня мочевой кислоты в сыворотке (sUA), собраны в таблице 4.
Таблица 4. Обострения на пациента в месяц по сравнению с другими видами лечения, снижающими уровень мочевой кислоты.
пациенты, не ответившие на лечение - 84,35
пациенты, не ответившие на лечение -99,75
80 мг/день
* Показатель эффективности.
Частота обострения явно снижается у субъектов, получавших рапамицин-содержащий наноноситель, одновременно вводимый с пегситиказой, по сравнению со всеми другими лекарствами. Этот неожиданный результат значительно лучше, чем при использовании других методов лечения. Это также имеет преимущество для приверженности пациентов к терапии, снижающей уровень мочевой кислоты, такой как уриказа, поскольку приверженность значительно снижается, когда после начала терапии возникают повторные обострения (Treatment of chronic gouty arthritis: it is not just about urate-lowering therapy. Schlesinger N - Semin. Arthritis Rheum. - October 1, 2012; 42 (2); 155-65).
Пример 4- Ежемесячный прием рапамицин-содержащих наноносителей в сочетании с пегилированной уриказой снижает образование антител к лекарственным средствам, что приводит к устойчивой активности уриказы у пациентов с симптомами подагры.
Предпосылки: Подагра вызывается отложением кристаллов мононатрия урата (MSU) в суставах из-за хронической гиперурикемии. Долгосрочное лечение направлено на снижение уровней sUA, что позволяет кристаллам MSU растворяться.
Пегилированные уриказы представляют собой препараты для лечения тяжелой хронической подагры. Однако уриказы ограничены индукцией антител к лекарственным средствам (ADA), что может поставить под угрозу эффективность и безопасность. SEL-212 представляет собой новый комбинированный продукт, состоящий из пегилированной уриказы, вводимой совместно с рапамицин-содержащими наноносителями, состоящими из PLA и PLA-PEG (SEL-110). SEL-110 был разработан для уменьшения образования ADA путем индукции толерогенных дендритных клеток и антиген-специфических регуляторных Т-клеток. Пролонгированная терапевтическая активность туриказы играет роль в поддержании устойчивого контроля уровней мочевой кислоты в сыворотке (SUA) у пациентов.
Способы: Пациенты с симптоматической подагрой (≥1 тофус, обострение подагры в течение 6 месяцев или подагрическая артропатия) и повышенным уровнем SUA ≥6 мг/дл лечились фиксированными дозами пегилированной уриказы (0,2 мг/кг) в сочетании с SEL-110 (0,1 и 0,15 мг/кг) или только пегилированной уриказой (0,2 или 0,4 мг/кг) в качестве контроля. Пациенты получали инфузию 28-дневными циклами до 5 раз. Контролировали безопасность, переносимость, sUA, ADA и активность уриказы.
В этом примере 2ответивший на лечение» указывает на индивида со значениями мочевой кислоты в сыворотке <6 мг/Ддл и мочевой кислотой в сыворотке ≤1 мг/дл на 21-й день (правило прекращения лечения). В этом примере «не ответивший на лечение» представляет собой субъекта, имеющего уровни мочевой кислоты в сыворотке ≥6 мг/дл в любое время в течение 28-дневного цикла введения доз. «Максимальный титр» представляет собой максимальный титр, наблюдаемый в течение 28-дневного цикла введения доз.
Антитела к уриказе определяли с помощью сэндвич-ELISA. Уриказу наносили на планшет, и анти-уриказа IgG определяли с использованием анти-человеческих IgG вторичных антител. Активность уриказы определяли флуорометрическим методом. Когда уриказа превращает мочевую кислоту в аллантоин и H2O2, добавляют пероксидазу хрена и достигают с помощью H2O2 и флуоресцентного зонда для получения количественного сигнала.
Результаты: Демографические данные 46 пациентов, получавших лечение 28-дневными циклами x5 комбинированных доз SEL-110 и пегилированной уриказы, по сравнению с 6 пациентами, получавшими только пегилированную уриказу, составляли 23-70 лет vs. 41-64 годами (среднее значение 53,6 vs. 51,8 года), 97,8% мужчин vs. 100% и 73,9% белой рассы vs. 33,3%. Средний ИМТ на исходном уровне составлял 34,5 vs. 38,9 кг/м2. 71,7% vs. 100% пациентов страдали ожирением со средней продолжительностью устойчивой или симптоматической подагры 12,5 vs. 12,8 лет. 43 пациента SEL-212 были оценены для этого анализа.
Большинство периодов лечения SEL-212 имели максимальные титры антител <1080 (83,4%, 111/133), в то время как 14,3% (1/7) периодов лечения только пегилированной уриказой имели максимальные титры антител <1080.
Для пациентов, включенных в когорты, получавшие 5 комбинированных доз рапамицинсодержащих наноносителей и пегилированной уриказы, средний максимальный титр антител к уриказе, наблюдаемый в течение периода лечения, был нанесен на график для ответивших на лечение и не ответивших на лечение (фиг. 10). Все не ответившие на периоды лечение имели титры ≥1080 (11/11). Средний максимальный титр антител к уриказе у пациентов, не ответивших на лечение, снижался в последующие периоды лечения, и впоследствии ни у одного пациента титры не превышали 1080 в периоды лечения 4 и 5.
7 циклов лечения только с пегилированной уриказой имели среднюю AUC активности уриказы 3437 мЕд/дл*нед. (фиг. 11). Для когорт, получавших 5 месячных доз SEL-212, AUC уриказной активности была разделена на отдельные циклы лечения с максимальными титрами антител к уриказе выше или ниже титра 1:1080. Для циклов лечения, в которых максимальные титры антител к уриказе превышали 1:1080, средняя AUC активности уриказы составляла 6776 мЕд/дл*нед. Для периодов лечения с титрами антител к уриказе менее 1:1080 средняя AUC активности уриказы была значительно выше (p=0,0029) при 8924 мЕд/дл*нед. Данные показывают, что AUC активности уриказы коррелирует с титром антител к уриказе и, наряду с фиг.10, подтверждает, что титр антител к уриказе 1:1080 является клинически значимым.
У пациентов, получавших только пегилированную уриказу, вырабатывался высокий титр антител, и они были исключены из исследования в течение первых двух месяцев. Комбинация пегилированной уриказы со все более высокими дозами рапамицин-содержащих наноносителей приводило к улучшению титров антител к уриказе через 3 месяца, при этом 78% пациентов имели титры ≤1:1080 при 0,15 мг/кг рапамицин-содержащих наноносителей. Однако введение только пегилированной уриказы через 4 и 5 месяцев привело к снижению пациентов с титрами ≤1:1080 на 5-м месяце (фиг. 12A). Пять ежемесячных доз пегилированной уриказы и рапамицин-содержащих наноносителей привели к более высокому проценту (~66%) пациентов с титрами ≤ 1:1080 на 5-м месяце (фиг. 12B).
Данные всех когорт использовали для построения графика максимального титра антител к уриказе, достигнутого во время цикла лечения, в зависимости от AUC активности уриказы (фиг. 13A-13B). На фиг. 13A показаны 0,2 мг/кг дозы пегилированной уриказы и на фиг. 13B показаны 0,4 мг/кг дозы пегилированной уриказы. Графики показывают, что по мере увеличения титра антител к уриказе, AUC активности уриказы, соответственно, уменьшается.
Используя данные всех когорт, AUC активности уриказы показала зависимость от дозы рапамицин-содержащих наноносителей, причем более высокая AUC была связана с более высокой дозой рапамицин-содержащих наноносителей. На фиг. 13C показаны 0,2 мг/кг дозы пегилированной уриказы и на фиг. 13D показаны 0,4 мг/кг дозы пегилированной уриказы. Связь между AUC уриказы и дозой рапамицин-содержащего наноносителя оказалась сильнее при дозе 0,4 мг/кг пегилированной уриказы.
Заключение: Снижая образование ADA, ежемесячное дозирование рапамицин-содержащих наноносителей в сочетании с пегилированной уриказой увеличивает активность уриказы у пациентов с симптомами подагры по сравнению с одной пегилированной уриказой. Когда титры антител к уриказе составляют <1080, пациенты демонстрируют устойчивую активность уриказы, что обеспечивает интервалы лечения в 28 дней.
ДРУГИЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Все признаки, раскрытые в данном описании, могут быть объединены в любом сочетании. Каждый признак, раскрытый в настоящем описании, может быть заменен альтернативным признаком, служащими той же, эквивалентной или аналогичной цели. Таким образом, если явно не указано иное, то каждый раскрытый признак является только примером из общего ряда эквивалентных или аналогичных признаков.
Из приведенного выше описания специалист в данной области может легко установить основные характеристики настоящего изобретения и, не выходя за рамки его сущности и объема, может внести различные изменения и модификации по изобретению, чтобы адаптировать его к различным применениям и условиям. Таким образом, другие варианты осуществления также находятся в пределах формулы изобретения.
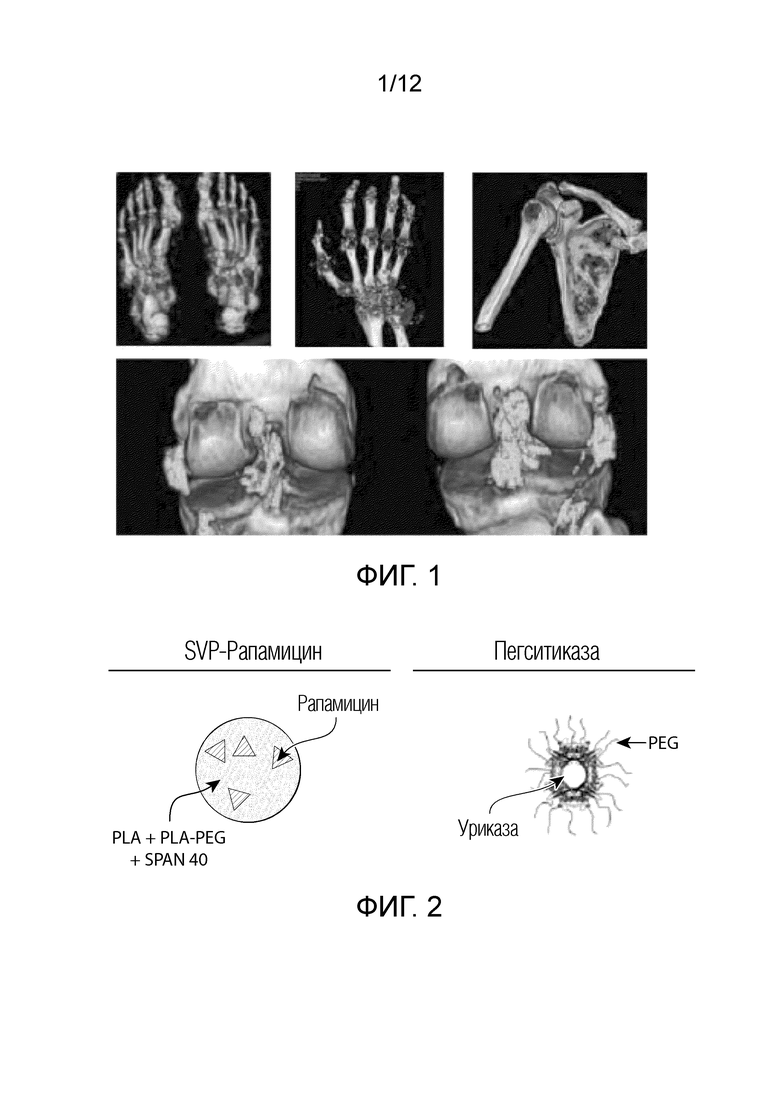
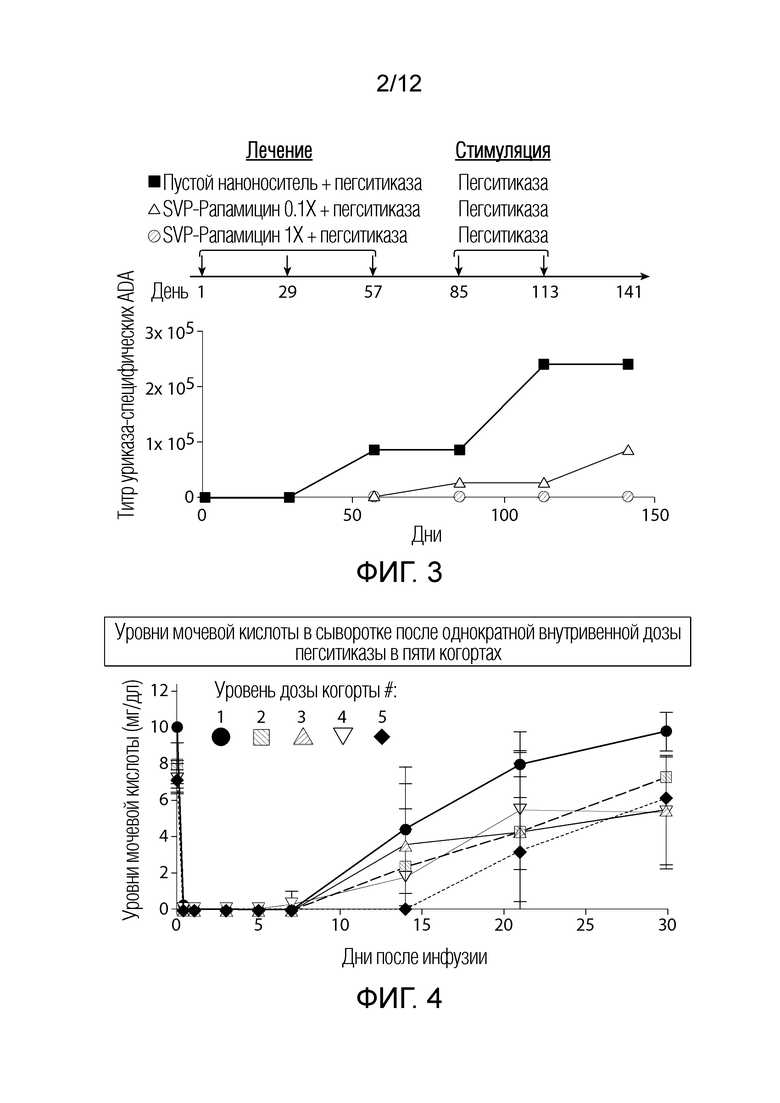
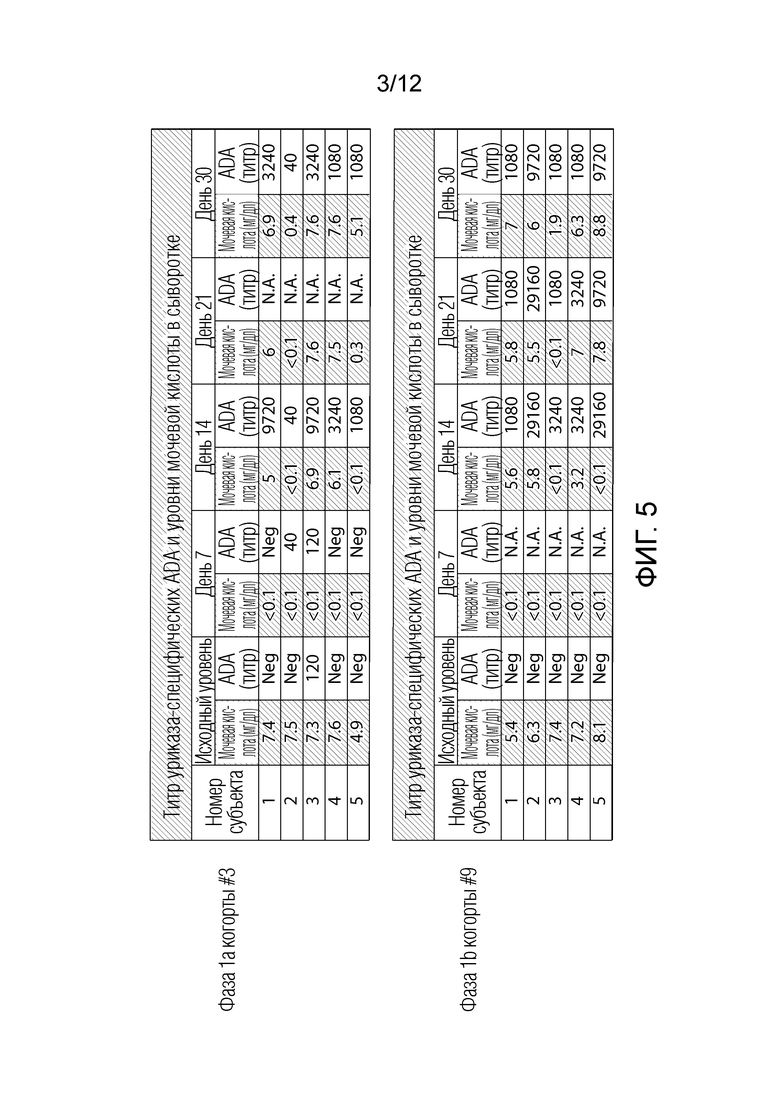
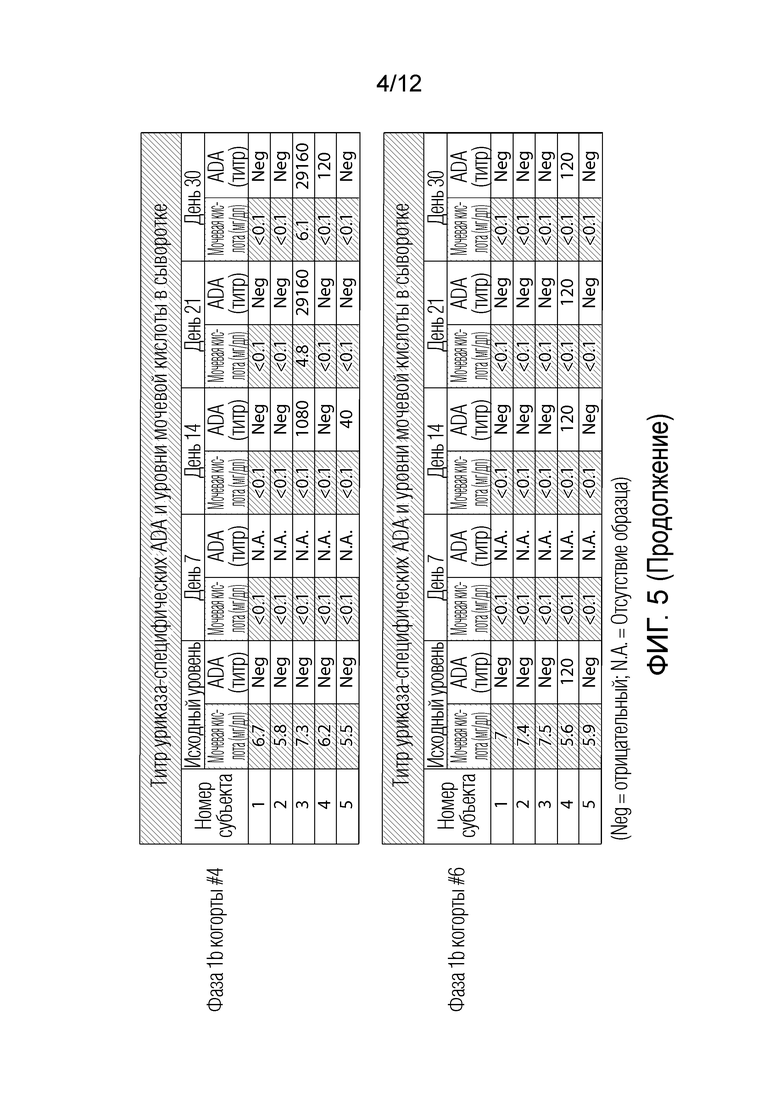
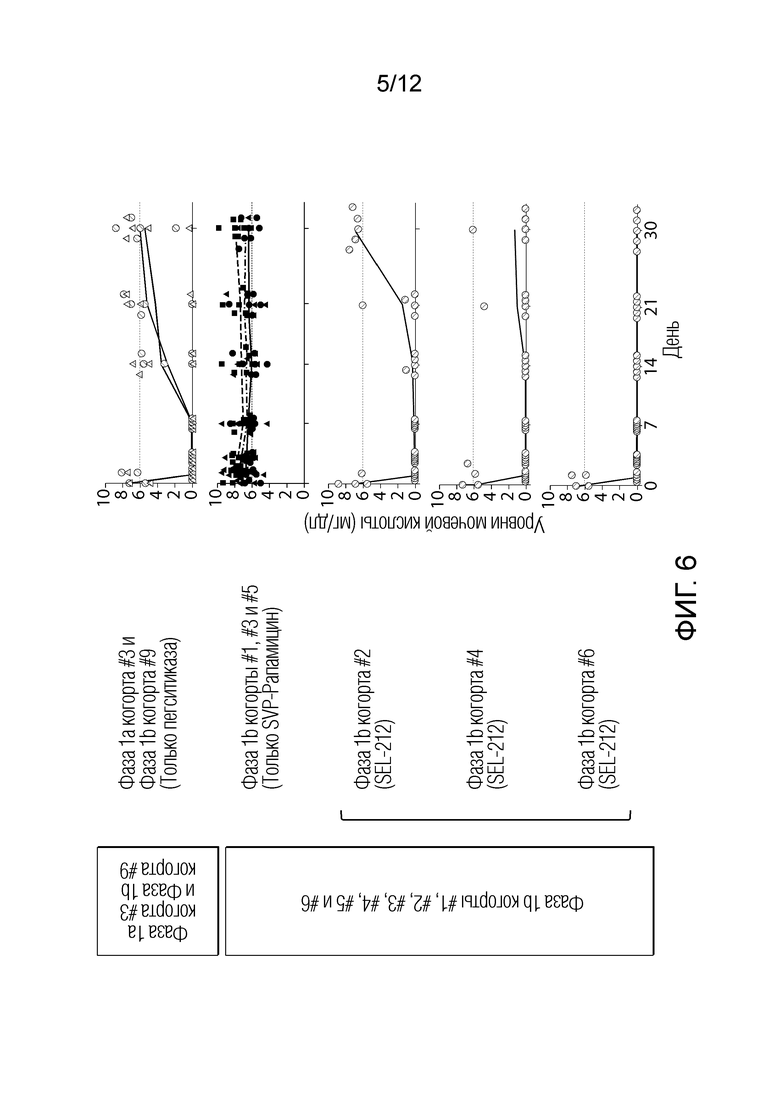
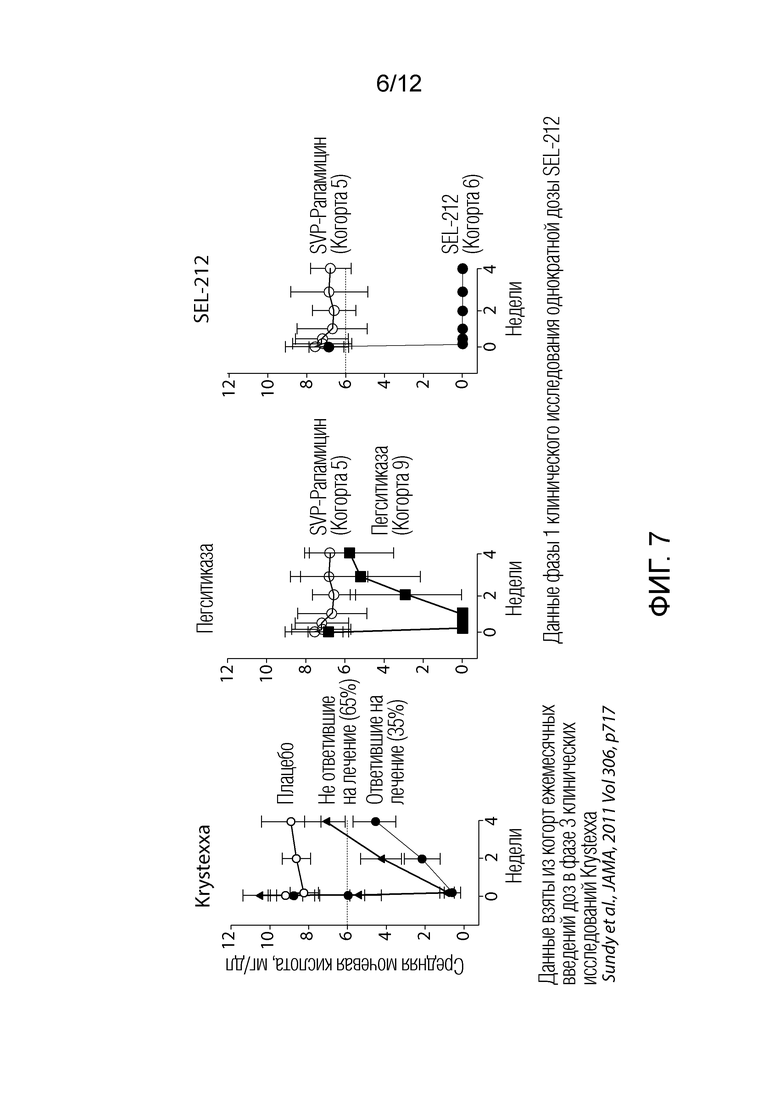
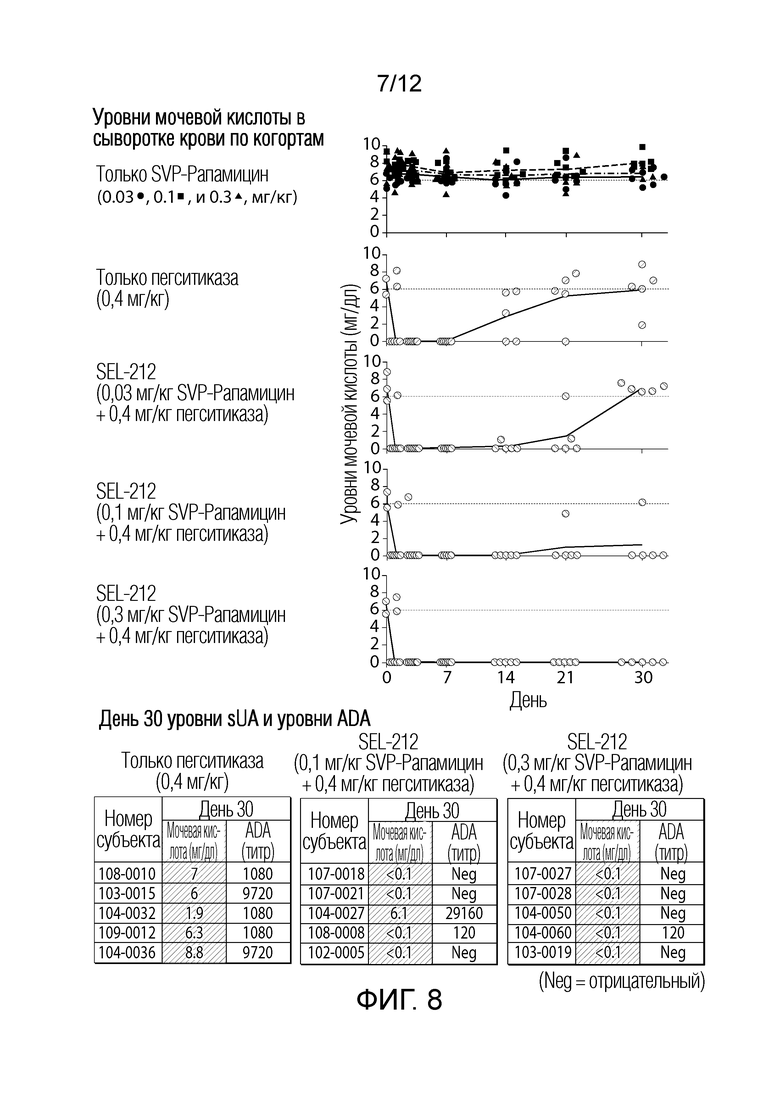

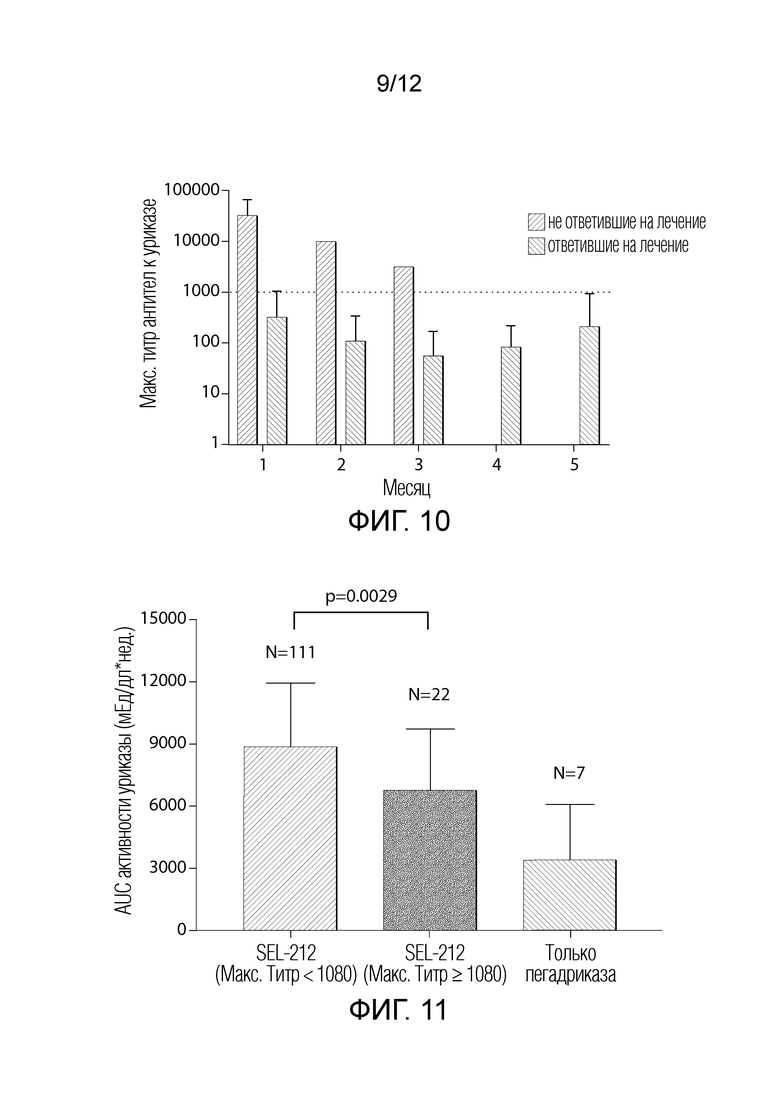
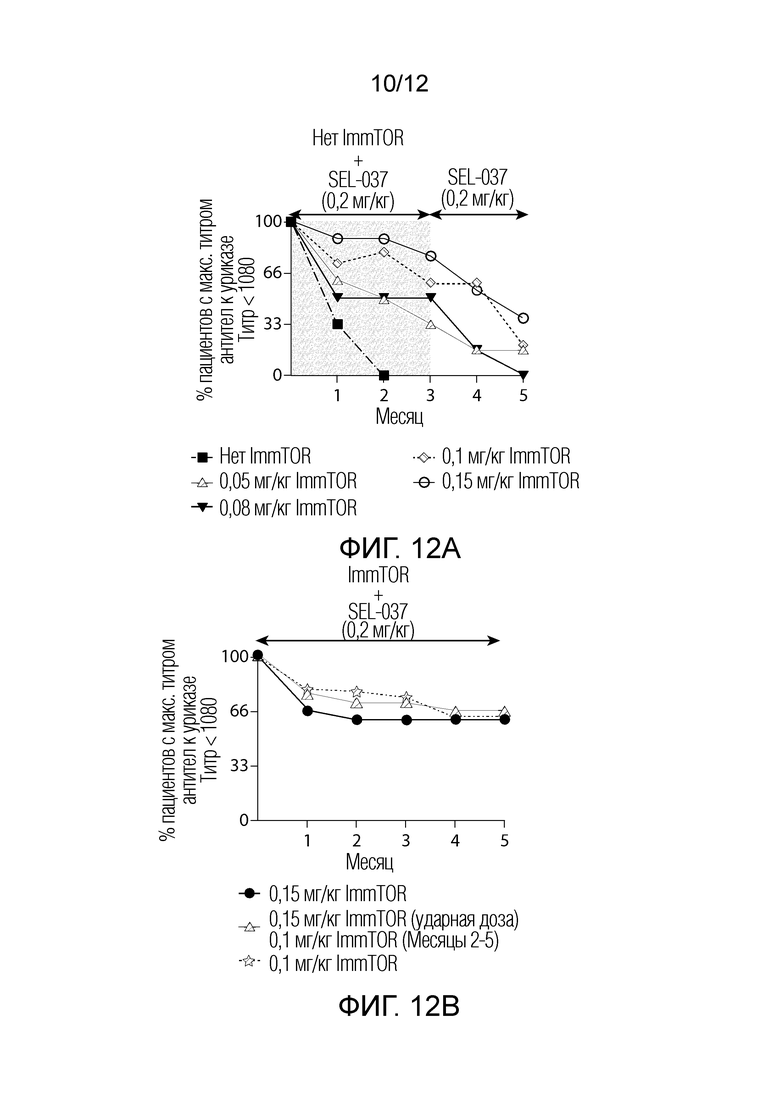
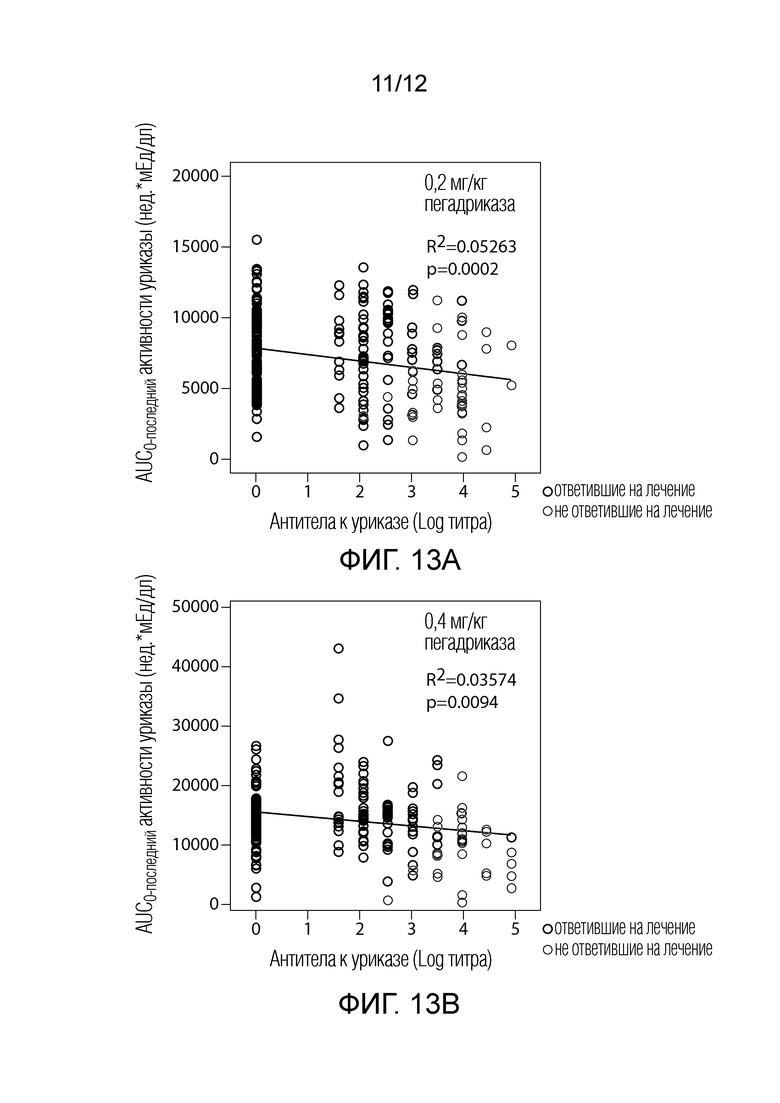
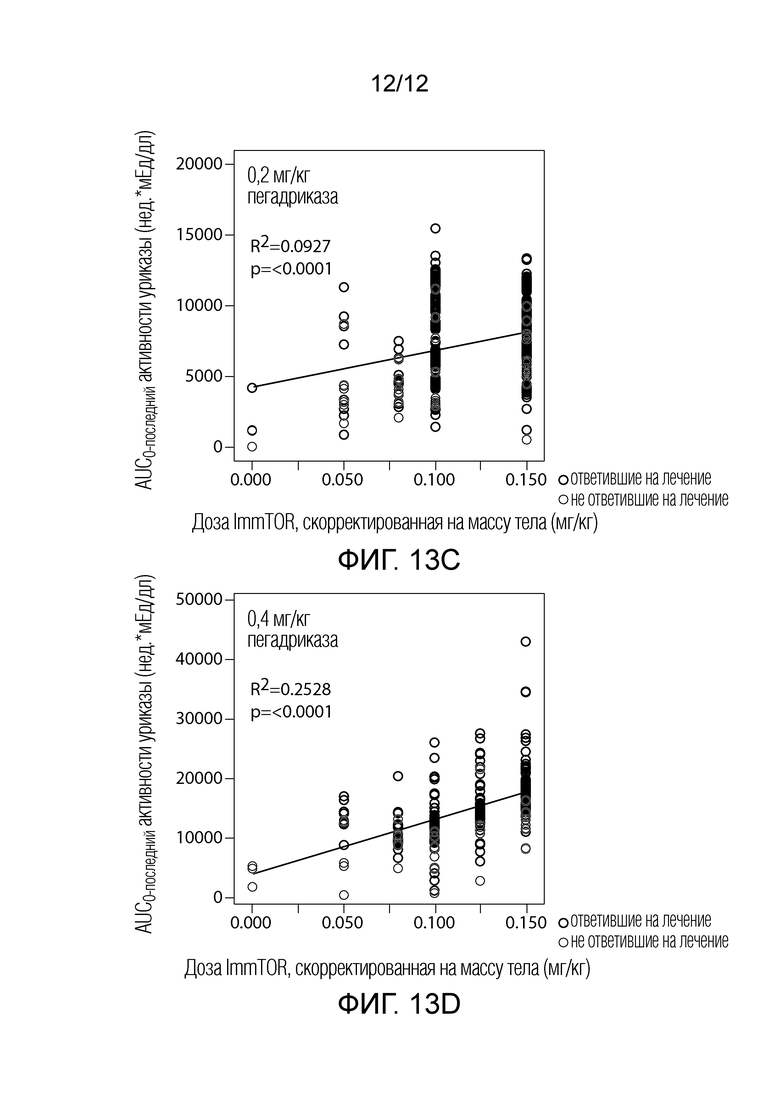
Группа изобретений относится к лечению субъектов с гиперурикемией, подагрой и состоянием, связанным с подагрой. Раскрыт способ оценки субъекта для лечения гиперурикемии, подагры или состояния, связанного с подагрой или для предотвращения обострения подагры, где способ включает получение титра антител к уриказе в образце от субъекта; сравнение титра антител к уриказе в образце от субъекта с пороговым значением, где пороговым значением является титр антител к уриказе, равный 1080; и оценку субъекта, где когда уровень антител к уриказе ниже порогового значения, показано лечение или нет необходимости в корректировке, а когда уровень антител к уриказе выше порогового значения, показан дополнительный мониторинг или оценка. Также раскрыты способ лечения гиперурикемии, подагры или состояния, связанного с подагрой, или для предотвращения обострения подагры у субъекта, а также способ предотвращения обострения подагры. Группа изобретений обеспечивает оценку и лечение субъекта с гиперурикемией, подагрой и состоянием, связанным с подагрой. 3 н. и 9 з.п. ф-лы, 18 ил., 4 табл., 4 пр.
1. Способ оценки субъекта для лечения гиперурикемии, подагры или состояния, связанного с подагрой или для предотвращения обострения подагры, где способ включает:
получение титра антител к уриказе в образце от субъекта;
сравнение титра антител к уриказе в образце от субъекта с пороговым значением, где пороговым значением является титр антител к уриказе, равный 1080; и
оценку субъекта, где когда уровень антител к уриказе ниже порогового значения, показано лечение или нет необходимости в корректировке, а когда уровень антител к уриказе выше порогового значения, показан дополнительный мониторинг или оценка.
2. Способ по п. 1, дополнительно включающий получение титра антител к уриказе в образце от субъекта в последующий момент времени и оценку субъекта.
3. Способ лечения гиперурикемии, подагры или состояния, связанного с подагрой, или для предотвращения обострения подагры у субъекта, где способ включает сопутствующее введение композиции, включающей синтетические наноносители, включающие иммунодепрессант и композицию, включающую уриказу субъекту, имеющему титр антител к уриказе ниже порогового значения, где пороговым значением является титр антител к уриказе, равный 1080, и где когда уровень антител к уриказе ниже порогового значения, показано лечение или не требуется корректировки, а когда уровень антител к уриказе выше порогового значения, показана корректировка лечения или дальнейший мониторинг или оценка.
4. Способ по п. 3, дополнительно включающий корректировку лечебной дозы и/или частоты лечения на основании идентификации или мониторинга субъекта; и/или способ дополнительно включает одну или несколько стадий для идентификации или мониторинга субъекта для получения титра антител к уриказе.
5. Способ предотвращения обострения подагры, включающий совместное введение субъекту, имеющему титр антител к уриказе ниже порогового значения, 1) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и 2) композиции, содержащей уриказу, где субъекту не вводят дополнительное терапевтическое средство для предотвращения обострения подагры совместно с сопутствующим введением, где пороговым значением является титр антител к уриказе, равный 1080, где когда уровень антител к уриказе ниже порогового значения, показано лечение или нет необходимости в корректировке, а когда уровень антител к уриказе выше порогового значения, показан дополнительный мониторинг или оценка; и где:
(a) лечебные дозы и/или частоту корректируют на основании идентификации или мониторинга субъекта; и/или
(b) способ дополнительно включает одну или несколько стадий для идентификации или мониторинга субъекта для получения титра антител к уриказе; и/или
(c) идентифицируют субъекта, как уже имевшего или у которого ожидается обострение подагры в результате лечения с помощью терапии подагры без сопутствующего введения дополнительного терапевтического средства для предотвращения обострения подагры.
6. Способ по любому из предшествующих пунктов, где субъект: (а) является субъектом, который в этом нуждается, например субъектом с повышенным уровнем мочевой кислоты в сыворотке и/или нежелательными отложениями мочевой кислоты или субъектом, имеющим гиперурикемию; и/или (b) имеет подагру или состояние, связанное с подагрой; и/или (c) не вводится дополнительное терапевтическое средство для предотвращения обострения подагры совместно с каждым сопутствующим введением.
7. Способ по любому из пп. 3-6, где введение:
(a) является сопутствующим и происходит у субъекта один или несколько раз, например, по меньшей мере дважды, по меньшей мере трижды, по меньшей мере четыре раза, по меньшей мере пять раз, по меньшей мере шесть раз, по меньшей мере семь раз, по меньшей мере восемь раз, по меньшей мере девять раз или по меньшей мере десять раз; и/или
(b) является сопутствующим и происходит каждые две-четыре недели; и/или
(c) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и композиции, содержащей уриказу, проводят ежемесячно, например, где композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, и композицию, содержащую уриказу, вводят ежемесячно в течение по меньшей мере трех месяцев, четырех месяцев, пяти месяцев, шести месяцев, семи месяцев, восьми месяцев, девяти месяцев, десяти месяцев или более; и/или
(d) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, проводят в дозе 0,05-0,5 мг/кг иммуносупрессанта при каждом введении, например, где композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в дозе 0,05 мг/кг, 0,08 мг/кг, 0,1 мг/кг, 0,125 мг/кг, 0,15 мг/кг, 0,2 мг/кг, 0,25 мг/кг, 0,3 мг/кг, 0,35 мг/кг, 0,4 мг/кг, 0,45 мг/кг или 0,5 мг/кг иммуносупрессанта при каждом введении; и/или
(e) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, проводят в дозе 0,55-6,5 мг/кг при каждом введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант, например, где композицию, содержащую синтетические наноносители, содержащие иммуносупрессант, вводят в дозе 0,55 мг/кг, 0,65 мг/кг, 0,7 мг/кг, 0,8 мг/кг, 0,9 мг/кг, 1,0 мг/кг, 1,1 мг/кг, 1,25 мг/кг, 1,5 мг/кг, 2,0 мг/кг, 2,5 мг/кг, 3,0 мг/кг, 3,5 мг/кг, 4,0 мг/кг, 4,5 мг/кг, 5,0 мг/кг, 5,5 мг/кг, 6,0 мг/кг или 6,5 мг/кг при каждом введении, где доза указана в мг синтетических наноносителей, содержащих иммуносупрессант; и/или
(f) композиции, содержащей уриказу, проводят: (i) в дозе 0,1-1,2 мг/кг уриказы при каждом введении, например, в дозе 0,1 мг/кг, 0,2 мг/кг, 0,3 мг/кг, 0,4 мг/кг, 0,5 мг/кг, 0,6 мг/кг, 0,7 мг/кг, 0,8 мг/кг, 0,9 мг/кг, 1,0 мг/кг, 1,1 мг/кг, 1,2 мг/кг уриказы при каждом введении; и/или (ii) по меньшей мере один раз после одного или нескольких сопутствующих введений без иммуносупрессанта; и/или (iii) по меньшей мере один раз после одного или нескольких сопутствующих введений без синтетических наноносителей, содержащих иммуносупрессант; и/или (iv) по меньшей мере один раз после одного или нескольких сопутствующих введений без иммуносупрессанта, или по меньшей мере один раз после одного или нескольких сопутствующих введений без синтетических наноносителей, содержащих иммуносупрессант, и: (A) композицию, содержащую уриказу, вводят, по меньшей мере, дважды после одного или нескольких сопутствующих введений, например, где композицию, содержащую уриказу, вводят по меньшей мере трижды или четыре, пять или более раз после одного или нескольких сопутствующих введений; или (B) композицию, содержащую уриказу, вводят ежемесячно в течение двух месяцев после одного или нескольких сопутствующих введений; и/или (v) в дозе 0,1-1,2 мг/кг уриказы при каждом введении после одного или нескольких сопутствующих введений без иммуносупрессанта, например, где композицию, содержащую уриказу, вводят в дозе 0,1 мг/кг, 0,2 мг/кг, 0,3 мг/кг, 0,4 мг/кг, 0,5 мг/кг, 0,6 мг/кг, 0,7 мг/кг, 0,8 мг/кг, 0,9 мг/кг, 1,0 мг/кг, 1,1 мг/кг, 1,2 мг/кг уриказы при каждом введении после одного или нескольких сопутствующих введений без иммуносупрессанта; и/или
(g) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, проводят до композиции, содержащей уриказу, при каждом сопутствующем введении; и/или
(h) композиции, содержащей синтетические наноносители, содержащие иммуносупрессант, и композиции, содержащей уриказу, проводят в пределах часа друг от друга при каждом сопутствующем введении.
8. Способ по любому из пп. 3-7, где:
(a) субъект имеет острую подагру; хроническую подагру с тофусами или без них; идиопатическую подагру; рефрактерную подагру, такую как хроническая рефрактерная подагра; вторичную подагру; неуточненную подагру; подагру, связанную с сердечно-сосудистым заболеванием, заболеванием почек, заболеванием легких, неврологическим заболеванием, заболеванием глаз, дерматологическим заболеванием или заболеванием печени; или у него был приступ подагры или обострение подагры; и/или
(b) уриказа представляет собой пегилированную уриказу; и/или
(c) иммуносупрессант представляет собой ингибитор mTOR; и/или
(d) иммуносупрессант инкапсулирован в синтетических наноносителях.
9. Способ по любому из пп. 3-8, где синтетические наноносители представляют собой полимерные синтетические наноносители, и где: (a) полимерные синтетические наноносители содержат гидрофобный полиэфир, например, где гидрофобный полиэфир включает PLA, PLG, PLGA или поликапролактон; и/или (b) полимерные синтетические наноносители дополнительно включают PEG, например, где PEG конъюгирован с PLA, PLG, PLGA или поликапролактоном и/или (c) полимерные синтетические наноносители включают PLA, PLG, PLGA или поликапролактон и PEG, конъюгированный с PLA, PLG, PLGA или поликапролактоном, и/или (d) полимерные синтетические наноносители включают PLA и PLA-PEG; и/или (e) среднее значение распределения частиц по размерам, полученное с применением динамического рассеяния света синтетических наноносителей, представляет собой диаметр более 120 нм, более 150 нм, более 200 нм, или более 250 нм, (f) диаметр составляет менее 300 нм, менее 250 нм или менее 200 нм; и/или (g) нагрузка иммуносупрессанта синтетических наноносителей составляет 7-12% или 8-12%, или 7-10% или 8-10%; или 7%, или 8%, или 9%, или 10%, или 11% или 12% масс.
10. Способ по любому из пп. 3-9, где каждое введение каждой композиции представляет собой внутривенное введение.
11. Способ по любому из пп. 3-10, где способ дополнительно включает введение субъекту дополнительного терапевтического средства, где: (a) дополнительное терапевтическое средство представляет собой пероральное терапевтическое средство для лечения подагры; и/или (b) дополнительное терапевтическое средство вводят: (i) по меньшей мере один раз после одного или нескольких сопутствующих введений без иммуносупрессанта, или (ii) по меньшей мере один раз после одного или нескольких сопутствующих введений без синтетических наноносителей, содержащих иммуносупрессант или (iii) по меньшей мере дважды, по меньшей мере трижды, четыре раза, пять раз или более; и/или (c) дополнительная терапия представляет собой терапию против обострения подагры, например, где терапия против обострения подагры представляет собой профилактическое лечение, применяемое совместно, но до введения каждой композиции уриказы, и/или терапия против обострения подагры представляет собой колхицин или НПВП и/или (d) каждое введение каждой композиции представляет собой внутривенную инфузию.
12. Способ по любому из пп. 3-11, где
(a) по меньшей мере одно введение или каждое введение осуществляется не внутримышечным способом введения; и/или
(b) уриказа представляет собой пегситиказу или пеглотиказу; и/или
(c) по меньшей мере, одно введение или каждое введение представляет собой внутривенное введение, например, где внутривенное введение представляет собой внутривенную инфузию; и/или
(d) композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят субъекту по меньшей мере дважды, по меньшей мере трижды, четыре раза, пять раз или более; и/или
(e) композицию, содержащую уриказу и фармацевтически приемлемый носитель, вводят каждые две-четыре недели, например ежемесячно; и/или
(f) композицию, содержащую уриказу дополнительно содержащую фармацевтически приемлемый носитель, вводят совместно с композицией, содержащей иммуносупрессант.
| SANDS E.E | |||
| et al | |||
| An Open Label Phase II Multiple Dose Safety, Pharmacokinetic and Pharmacodynamics Study of SEL-212 Followed by Open Label Administration of SEL-037 in Subjects with Symptomatic Gout and Elevated Blood Uric Acid // SELECTA BIOSCIENCES CLINICAL STUDY PROTOCOL, 2018, pp.1-120 | |||
| US 20180289776 A1, 11.10.2018 | |||
| US 20120301454 A1, |
Авторы
Даты
2024-12-02—Публикация
2020-06-04—Подача