Изобретение относится к области органической химии, а именно к применению индивидуальных соединений класса спиро[пиррол-оксадиазолопиразинов], которые могут быть использованы в фармакологии в качестве средств, обладающих противомикробной активностью в отношении S. aureus и С. albicans.
Заявленные соединения 3-ароил-4-гидрокси-1-(2-гидроксиэтил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дионы и способ их синтеза известны из уровня техники. Заявленные соединения являются продуктами взаимодействия 8-ароил-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-трионов с 3,4-диаминофуразаном («Синтез спиро[пиррол-2,5'-оксадиазолопиразинов] реакцией пирролооксазинтрионов с диаминофуразаном», Третьяков Н.А., Масливец А.Н., ЖОрХ, 2021, 57, №12, 1793-1796. [Synthesis of Spiro[[1,2,5]oxadiazolo[3,4-b]pyrazine-5,2'-pyrroles] by Reaction of Pyrrolooxazinetriones with Diaminofurazan. Tretyakov N.A., Maslivets A.N. Russ. JOC, 2021, 57(12), 2074-2076. doi: 10.1134/S1070428021120277]), образующихся по следующей схеме:
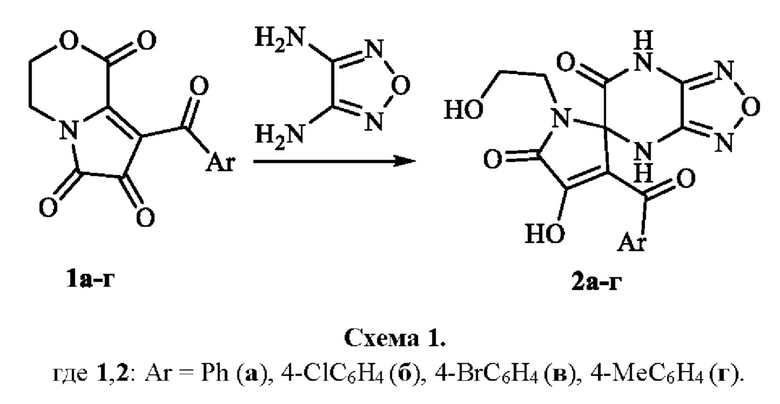
Противогрибковая активность 3-ароил-4-гидрокси-1-(2-гидроксиэтил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дионов ранее не была исследована.
Задачей изобретения является изыскание новых соединений, обладающих противомикробной активностью, и расширение арсенала средств воздействия на живой организм.
Поставленная задача решается тем, что соединения 3-ароил-4-гидрокси-1-(2-гидроксиэтил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дионы проявляют высокую противомикробную активность в концентрации в 1000 мкг/мл.
Синтезируют заявляемые соединения путем взаимодействия 8-ароил-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-трионов с 3,4-диаминофуразаном в среде растворителя с последующим выделением целевых продуктов, по следующей схеме:
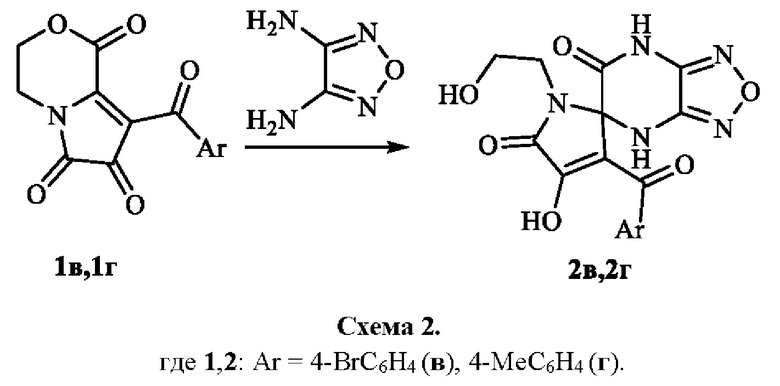
Процесс ведут при температуре 78-80°С, а в качестве растворителя используют безводный этилацетат.
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-(4-Бромбензоил)-4-гидрокси-1-(2-гидроксиэтил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дион (2в).
К раствору 1.0 ммоль 8-(4-бромбензоил)-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-триона (1в) в 10 мл безводного этилацетата добавляли 1.0 ммоль 3,4-диаминофуразана, кипятили 1 ч, охлаждали, образовавшийся осадок отфильтровывали. Выход 71%, т.пл. 202-204°С (этилацетат).
Соединение (2в) C16H12BrN5O6.
Найдено, %: С 42.85; Н 2.53; N 15.41
Вычислено, %: С 42.69; Н 2.69; N 15.56. Соединение (2в) - бесцветное кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, труднорастворимое в ацетоне, этилацетате, хлороформе, 1,4-диоксане, нерастворимое в ароматических углеводородах, алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (2в), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы ОН в виде узкого пика при 3446 см-1, енольной группы ОН в виде широкой полосы при 3279 см-1, NH-групп при 3149 и при 3087 см-1, двух лактамных карбонильных групп при 1717 см-1 и при 1703 см-1 и ароильной карбонильной группы при 1634 см-1.
В спектре ЯМР 1Н соединения (2в), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют группа из 4 метиленовых протонов гидроксиэтильного заместителя при 3.22-3.32 м.д. (м, 1H), 3.39-3.59 м.д. (м, 3Н), уширенный синглет протона группы ОН гидроксиэтильного заместителя при 6.33 м.д., и два синглета NH-групп при 8.52 м.д. и 12.48 м.д.
Пример 2. 4-Гидрокси-1-(2-гидроксиэтил)-3-(4-метилбензоил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дион (2 г).
К раствору 1.0 ммоль 8-(4-метилбензоил)-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-триона (1 г) в 10 мл безводного этилацетата добавляли 1.0 ммоль 3,4-диаминофуразана, кипятили 1 ч, охлаждали, образовавшийся осадок отфильтровывали. Выход 80%, т.пл. 193-195°С (этилацетат).
Соединение (2 г) C17H15N5O6.
Найдено, %: С 53.18; Н 3.76; N 18.01
Вычислено, %: С 52.99; Н 3.92; N 18.18. Соединение (2 г) - бесцветное кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, труднорастворимое в ацетоне, этилацетате, хлороформе, 1,4-диоксане, нерастворимое в ароматических углеводородах, алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (2 г), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы ОН в виде узкого пика при 3426 см-1, енольной группы ОН в виде широкой полосы при 3281 см-1, NH-групп при 3161 и при 3096 см-1, двух лактамных карбонильных групп при 1720 см-1 и при 1707 см-1 и ароильной карбонильной группы при 1630 см-1.
В спектре ЯМР 1Н соединения (2 г), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствуют группа из 4 метиленовых протонов гидроксиэтильного заместителя при 3.21-3.31 м.д. (м, 1H), 3.39-3.58 м.д. (м, 3Н), уширенный синглет протона группы ОН гидроксиэтильного заместителя при 4.40 м.д., и два синглета NH-групп при 8.53 м.д. и 12.46 м.д.
Пример 3. Фармакологическое исследование соединений (2в, 2г) на наличие противомикробной активности.
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ - М.: И-во Медицина, 2005]. Готовили исходные разведения микроорганизмов в физиологическом растворе из суточной агаровой культуры по оптическому стандарту мутности (ОСО) на 5 ME с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
Противомикробные свойства химического вещества изучали на 3-х коллекционных условно-патогенных штаммах микроорганизмов: Staphylococcus aureus (АТСС 25923), Escherichia coli (АТСС 25922), Candida albicans (РКПГУ 1353/1277), полученных в ФГБУ «Научный центр экспертизы средств медицинского применения» Минздравсоцразвития России. Факт ингибирования (торможения роста) микробных клеток в разведениях препаратов отмечали после 20-ти часового термостатирования при 37°С. Окончательные результаты фиксировали через 7 суток после высева на скошенный агар РПА. Максимально испытанная концентрация соединений соответствовала 1000,0 мкг/мл. Противомикробную (ингибирующую, бактерицидную) активность оценивали по минимально действующей концентрации.
Анализ полученных данных показал:
• соединения 2в и 2г обладают ингибирующим действием в отношении культуры S. aureus в концентрации 1000.0 мкг/мл, а также обладают ингибирующим действием в отношении культуры С. albicans в концентрации 1000.0 мкг/мл.
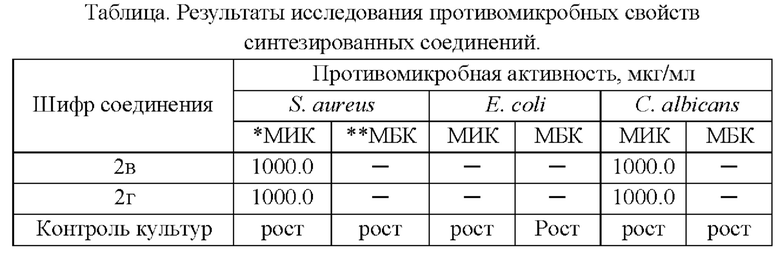
Примечание: "-" - отсутствие противомикробного действия в испытанных концентрациях; *МИК - минимальная ингибирующая концентрация; **МБК - минимальная бактерицидная концентрация.
Предлагаемые вещества 3-ароил-4-гидрокси-1-(2-гидроксиэтил)-4'H-спиро[пиррол-2,5'-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6'(1H,7'H)-дионы (2в,г) обладают противомикробной активностью, и могут найти применение в фармакологии в качестве потенциального лекарственного средства.
Изобретение относится к области органической химии, а именно к применению индивидуальных соединений класса спиро[пиррол-оксадиазолопиразинов] формул 2в, 2г в качестве средств, обладающих противомикробной активностью. Технический результат – выраженное ингибирующее действие соединений 2в, 2г в отношении культур S. aureus, C. albicans. 1 табл., 3 пр.
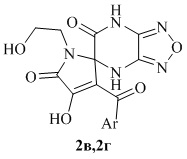 , где Ar = 4-BrC6H4 (в), 4-MeC6H4 (г)
, где Ar = 4-BrC6H4 (в), 4-MeC6H4 (г)
Применение 3-ароил-4-гидрокси-1-(2-гидроксиэтил)-4′H-спиро[пиррол-2,5′-[1,2,5]оксадиазоло[3,4-b]пиразин]-5,6′(1H,7′H)-дионов:
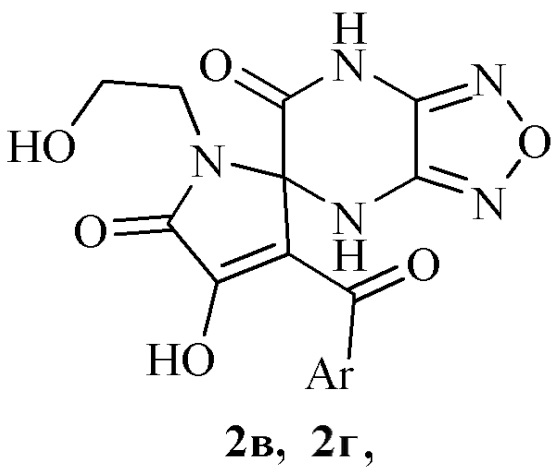
где 2: Ar = 4-BrC6H4 (в), 4-MeC6H4 (г),
в качестве средств, обладающих противомикробной активностью.
| 2'-Амино-2,5'-диоксо-5-фенил-1,2,5',6',7',8'-гексагидро-1'Н-спиро[пиррол-3,4'-хинолины] | 2020 |
|
RU2743922C1 |
| Третьяков Н.А | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Журнал органической химии, 2021, том 57, N 12, с.1793-1796 | |||
| 2'-Оксо-1',2'-дигидро-9аН-спиро[пиридо[2,1-b][1,3]оксазин-2,3'-пиррол] | 2021 |
|
RU2776064C1 |
| WO 2014191109 A1, 04.12.2014. | |||
Авторы
Даты
2024-12-03—Публикация
2024-03-27—Подача