Группа изобретений относится к области органической химии, а именно к структуре, анальгетической активности и способу получения новых индивидуальных соединений класса триазаспиро[4,4]нонентрионов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Известен способ синтеза структурных аналогов заявленных соединений -8-гидрокси-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионов, являющихся продуктами взаимодействия 4-ароил-5-(этоксикарбонил)-1H-пиррол-2,3-дионов с мочевиной («Синтез спиро[имидазол-2,2'-пирролов] при взаимодействии 5-(алкоксикарбонил)-1H-пиррол-2,3-дионов с мочевиной», Дубовцев А.Ю., Силайчев П.С., Железнова М.А., Алиев З.Г., Масливец А.Н., ЖОрХ, 2016, 52, №12, 1779), образующихся по следующей схеме:
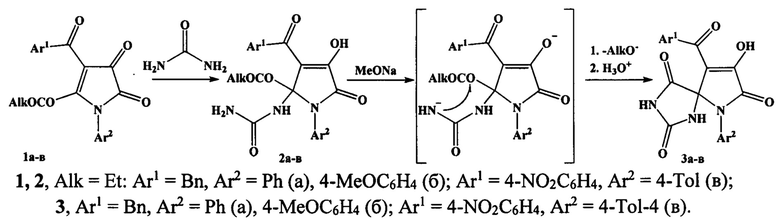
К недостаткам данного способа относится невозможность получить 9-ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионы, обладающие анальгетической активностью.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 9-ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионов и расширение арсенала средств воздействия на живой организм.
Поставленная задача осуществляется путем взаимодействия 8-ароил-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-трионов с мочевиной в среде растворителя с последующим выделением целевых продуктов, по следующей схеме:
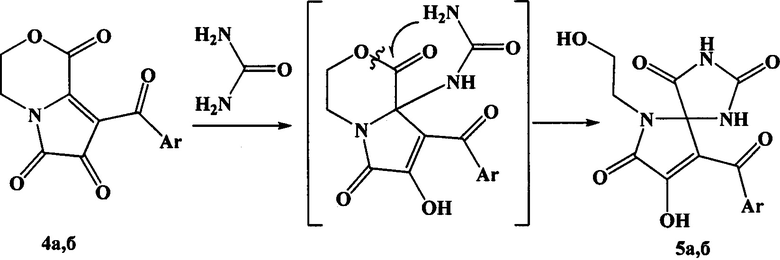
4,5, Ar=Ph (а), 4-ClC6H4 (б).
Процесс ведут при температуре 76-78°С, а в качестве растворителя используют безводный этилацетат.
Из патентной и технической литературы не были выявлены способы получения 9-ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионов, имеющие сходные признаки с заявляемым способом, а именно, не использовались исходные продукты, растворители, в которых проходит реакция, и интервал температур.
Изобретение иллюстрируется следующими примерами.
Пример 1. 9-Бензоил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трион (5а).
К 1,2 ммоль 8-бензоил-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-триона (4а) добавляли 1,2 ммоль мочевины, добавляли растворитель: 15 мл безводного этилацетата, кипятили 1-2 часа до изменения окраски, охлаждали, образовавшийся осадок отфильтровывали. Выход 92%, т.пл. 220-222°С. Соединение (5а) C15H13N3O6.
Найдено, %: С 54.36; Н 3.97; N 12.69
Вычислено, %: С 54.38; Н 3.96; N 12.68.
Соединение (5а) - бесцветное кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в менее полярных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (5а), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы ОН в виде узкого пика при 3318 см-1, енольной группы ОН в виде широкой полосы при 3145 см-1, двух лактамных карбонильных групп при 1728 см-1, ароильной карбонильной группы при 1684 см-1 и кетонной карбонильной группы при 1634 см-1.
В спектре ЯМР 1Н соединения (5а), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствует группа из 4 метиленовых протонов этоксильного заместителя при 3.10-3.16 м.д. (м, 1Н), 3.36-3.57 (м, 3Н) соответственно, уширенный синглет протона спиртовой группы ОН при 4.72 м.д., синглеты протонов групп NH при 8.43 м.д. и 11.27 м.д.
Пример 2. 8-Гидрокси-6-(2-гидроксиэтил)-9-(4-хлорбензоил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трион (5б).
К 0,9 ммоль 8-(4-хлорбензоил)-3,4-дигидро-1H-пирроло[2,1-с][1,4]-оксазин-1,6,7-триона (4б) добавляли 0,9 ммоль мочевины, добавляли растворитель: 15 мл безводного этилацетата, кипятили 1-2 часа до изменения окраски, охлаждали, образовавшийся осадок отфильтровывали. Выход 83%, т.пл. 250-252°С. Соединение (5б) C15H12N3O6.
Найдено, %: С 49.26; Н 3.31; N 11.50
Вычислено, %: С 49.26; Н 3.31; N 11.49.
Соединение (5б) - бесцветное кристаллическое вещество, легкорастворимое в ДМСО и ДМФА, трудно растворимое в менее полярных органических растворителях, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (5б), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы ОН в виде узкого пика при 3316 см-1, енольной группы ОН в виде широкой полосы при 3160 см-1, двух лактамных карбонильных групп при 1719 см-1, ароильной карбонильной группы при 1680 см-1 и кетонной карбонильной группы при 1639 см-1.
В спектре ЯМР 1Н соединения (5а), записанном в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец, присутствует группа из 4 метиленовых протонов этоксильного заместителя при 3.09-3.16 м.д. (м, 1Н), 3.35-3.56 (м, 3Н) соответственно, уширенный синглет протона спиртовой группы ОН при 5.91 м.д., синглеты протонов групп NH при 8.41 м.д. и 11.28 м.д.
Пример 3. Фармакологическое исследование соединений (5а и 5б) на наличие анальгетической активности.
Оценку анальгетических свойств соединений (5а и 5б) изучали на беспородных мышах массой 18-22 грамм методом термического раздражения «горячая пластинка» по Эдди и Леймбах (Eddy N.B., Leimbarh D.J. - Pharmacol and Exper. Gher., 1953, 385-393). В качестве препарата сравнения использовали метамизол натрия (М.Д. Машковский, «Лекарственные средства», т. 1, стр. 184, М., Медицина, 1978).
Проведенные исследования показали (см. табл.), что соединения (5а и 5б) обладают анальгетической активностью. Данные о фармакологической активности структурных аналогов заявляемых соединений в доступной литературе отсутствуют.

Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить неописанные в литературе 9-ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионы (5а, 5б) с хорошими выходами, которые могут найти применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств.
Группа изобретений относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса триазаспиро[4,4]нонентрионов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии. Предложены 9-ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триаза-спиро[4,4]нон-8-ен-2,4,7-трионы, обладающие анальгетической активностью, а также способ их получения. 2 з.п. ф-лы, 1 табл., 3 пр.
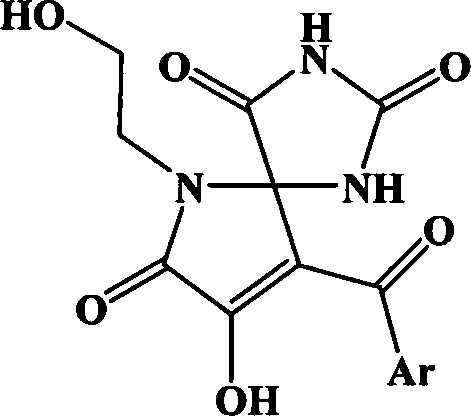 Ar = Ph (а), 4-ClC6H4 (б)
Ar = Ph (а), 4-ClC6H4 (б)
1. 9-Ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионы общей формулы
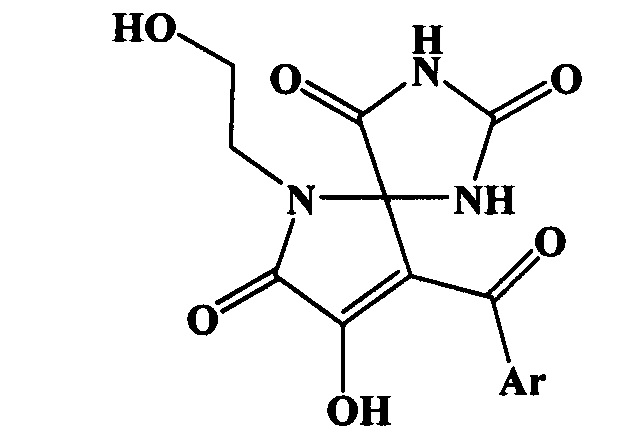
где Ar = Ph (а), 4-ClC6H4 (б),
обладающие анальгетической активностью.
2. Способ получения 9-Ароил-8-гидрокси-6-(2-гидроксиэтил)-1,3,6-триазаспиро[4,4]нон-8-ен-2,4,7-трионов по п. 1, отличающийся тем, что 8-ароил-3,4-дигидро-1H-пирроло[2,1-с][1,4]оксазин-1,6,7-трионы подвергают взаимодействию с мочевиной в среде растворителя при температуре 76-78°С в течение 1-2 ч, по следующей схеме:
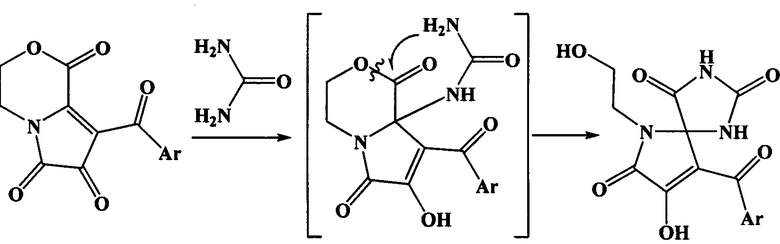
где Ar = Ph (а), 4-ClC6H4 (б),
с последующим выделением целевых продуктов.
3. Способ по п. 2, отличающийся тем, что в качестве растворителя используют безводный этилацетат.
Авторы
Даты
2019-11-25—Публикация
2019-06-24—Подача