Изобретение относится к медицине, а именно к онкологии, к лучевой диагностике – мультиспиральной компьютерной томографии (МСКТ) и магнитной резонансной томографии (МРТ), к способам полуавтоматического подсчета интенсивности сигнала в структуре опухолей надпочечников с целью дифференциальной диагностики между различными гистологическими типами новообразований, преимущественно между злокачественными.
Классификация новообразований надпочечников
Злокачественные опухоли надпочечников по данным различных авторов составляют 0,02–0,06% от всех злокачественных опухолей.
Образования надпочечников могут носить посттравматический геморрагический характер, возникать вследствие инфекционного поражения, встречаются кистозные образования доброкачественной природы. Также существует большое разнообразие первичных опухолей надпочечников. Вторичное неопластическое поражение надпочечников также не редкость, например, при раке лёгкого. Случайно обнаруженные образования надпочечников называют инциденталомами, которые делят на гормонально-активные и гормонально-неактивные, в дальнейшем необходимо отнести выявленное образование к более конкретной категории.
Существует большое количество различных классификаций первичных опухолей надпочечников. Впервые проблему создания клинической классификации рака коры надпочечников по стадиям пытались решить D.A.Macfarlan et al. в 1958 г. Ими были выделены 4 стадии на основе TNM классификации. Позже TNM классификация была доработана M. Sullivan. Также одной из наиболее удобных является клинико-морфологическая классификация, предложенная Micali и соавторами в 1985г. В 1963г О.В. Николаевым было предложено разделение всех опухолей коры надпочечников в соответствии с преобладанием секреции тех или иных гормонов: адьдостеромы, глюкостеромы, кортикоэстромы, андростеромы и смешанные опухоли.
Известен метод полуколичественной оценки изменений, основанный на обработке одного среза с наибольшим количеством гипоинтенсивных включений (Nicola Schieda , Abdulmohsen Alrashed , Trevor A Flood , et al. Comparison of Quantitative MRI and CT Washout Analysis for Differentiation of Adrenal Pheochromocytoma From Adrenal Adenoma AJR Am J Roentgenol. 2016 Jun;206(6):1141-8. doi: 10.2214/AJR.15.15318. Epub 2016 Mar 24).
Его недостатком является то, что выявленные на одном срезе изменения экстраполируются на весь опухолевый объем, что может приводить к искажению реальной картины. Подавляющее число новообразований надпочечников на аксиальных срезах имеет неправильную форму.
В настоящее время другие методы оценки и подсчета микрокровоизлияний и микрососудов, и наличия включений в структуре новообразований надпочечников в отечественной литературе отсутствуют.
В зарубежной литературе встречаются схожие методики измерения новообразований, но не во всём предлагаемом протоколе и нет предложений по выведенной формуле злокачественности (Nicola Schieda , Abdulmohsen Alrashed , Trevor A Flood , et al. Comparison of Quantitative MRI and CT Washout Analysis for Differentiation of Adrenal Pheochromocytoma From Adrenal Adenoma AJR Am J Roentgenol. 2016 Jun;206(6):1141-8. doi: 10.2214/AJR.15.15318. Epub 2016 Mar 24; Rosalind Gerson , Wendy Tu , Jorge Abreu-Gomez , et al. Evaluation of the T2-weighted (T2W) adrenal MRI calculator to differentiate adrenal pheochromocytoma from lipid-poor adrenal adenoma Eur Radiol. 2022 Dec;32(12):8247-8255. doi: 10.1007/s00330-022-08867-4. Epub 2022 Jun 9.)
Задачей изобретения является создание более эффективного способа определения гистологической принадлежности опухоли надпочечников с использованием МСКТ и МРТ в режиме статических изображений c целью дифференциальной диагностики опухолей.
Технический результат
Технический результат заявленного способа состоит в разработке объективного способа оценки внутренней структуры опухолей надпочечников и улучшении дифференциально-диагностических возможностей совместного применения МСКТ и МРТ между опухолями надпочечников различной гистологической принадлежности.
Заявляемый способ осуществляется следующим образом:
Мультиспиральная компьютерная томография выполнялась на рентгеновском компьютерном томографе SIEMENS «SOMATOM Emotion» и Phillips «Brillians».
МСКТ включает два этапа: на первом этапе производят исследование брюшной полости и забрюшинного пространства по стандартной методике; Исследование производят в положении пациента лежа на спине с руками вытянутыми над головой (для предотвращения возможных артефактов от костей верхних конечностей). В качестве центра исследуемой области выбирают точку пересечения срединной сагиттальной линии тела с горизонтальной линией, проведенной через мечевидный отросток грудины. Для получения пристрелочного изображения (топограммы) использовался режим «Abdomen», при этом брюшная полость визуализировались в корональной плоскости сканирования. По топограмме планируют аксиальные срезы, необходимые для выполнения первого этапа исследования. Положение срезов программируют с таким расчетом, чтобы в зону сканирования попало пространство от диафрагмальной поверхности печени, до бифуркации аорты и нижней полой вены. Толщина среза составляет 6 мм, размер поля зрения - 25-30 см. Первый этап исследования позволяет оценить состояние всех органов брюшной полости и забрюшинного пространства, определить локализацию надпочечников, выявить патологическое образование в одной или обеих железах.
Получение тонких срезов и уменьшение поля сканирования позволяет детально изучить структуру, контуры надпочечников, измерить размеры всех отделов железы (тело, латеральная и медиальная ножки). В случае выявления патологического образования, детально изучают его структуру, оценивают денситометрические характеристики разных отделов опухоли, определяют взаимоотношение патологического образования с прилежащими паренхиматозными органами и крупными сосудами. Для более точной пространственной ориентации в месторасположении опухоли, из серии аксиальных срезов реконструируют изображения в коронарной и сагиттальной плоскостях сканирования.
С целью уточнения характера выявленных изменений, производилось введение контрастного вещества. Использовались контрастные препараты: «Ультравист-240» фирмы SCHERING; «Омнипак-240» фирмы NYCOMED IM¬AGING из расчета 0,5-1 мл/кг массы тела. Исследование в условиях контрастного усиления производят по полученным на втором этапе аксиальными срезам сразу же после инъекции.
Нативная фаза с захватом грудной клетки.
Артериальная фаза 1 сек, первое постконтрастное изображение получают через 20 сек, затем на 4 минуте исследования.
Венозная фаза 20 сек
Поственозная (выделительная) фаза 240 сек
Для анализа данных нормировку сигнала не проводили.
Интенсивность сигнала - насколько яркой или темной кажется структура на фоне окружающих тканей или при количественном анализе среднее значение интенсивности сигнала (ИС) в области интереса.
Неоднородность сигнала - наличие и степень выраженности неравномерности распределения сигнала структуры на фоне окружающих тканей или при количественном анализе, разброс значений интенсивности сигнала внутри изучаемой области, который может быть оценен как абсолютное значение стандартного отклонения интенсивности сигнала (СО ИС) или отношение СО ИС к самой величине ИС в области интереса.
Данные характеристики доступны для простого визуального анализа, однако их можно оценить и количественно, используя стандартный интерфейс рабочей станции, что позволяет установить конкретные количественные референсные значения этих показателей.
ИС в заявляемом способе оценивали и по абсолютному значению.
В программе Радиант-просмотровщик 64 бит в аксиальной плоскости выбирается зона интереса, включающая точечные (микрокровоизлияния, кальцинация) и линейные (микрососуды, фиброз) структуры.
Далее программное обеспечение автоматически рассчитывает площадь и показывает максимальные и минимальные значения плотности и стандартное отклонение неоднородности.
Способ иллюстрируется Фиг. 1-7:
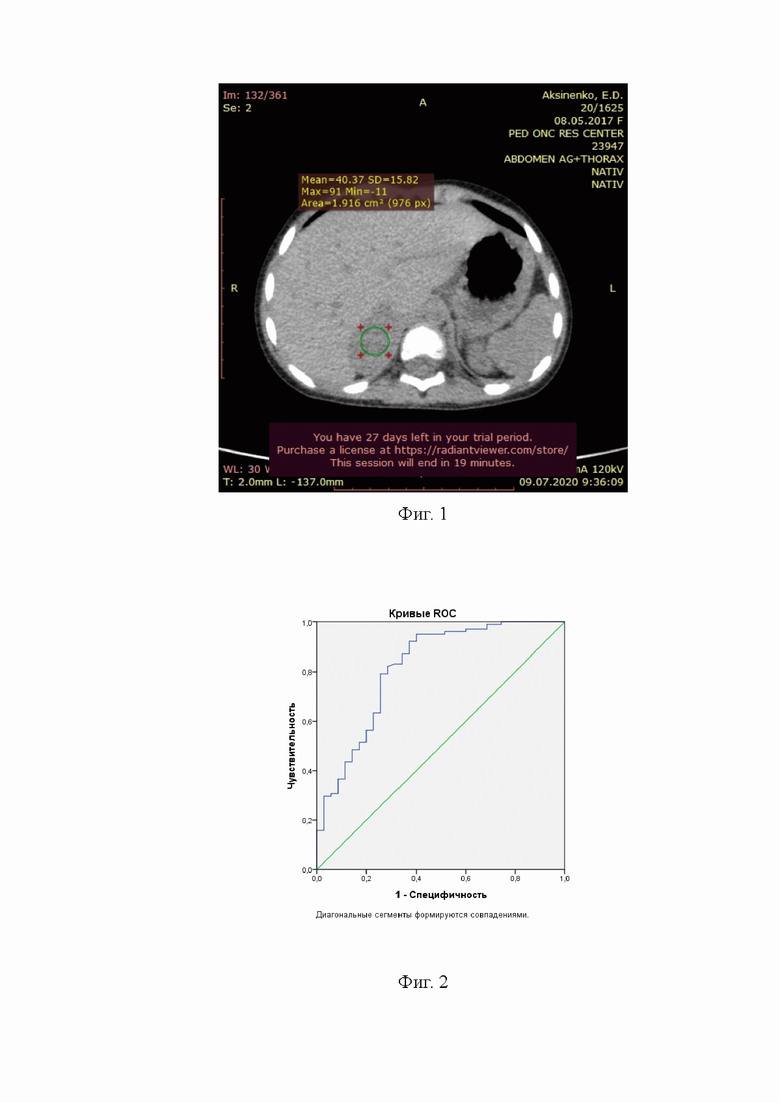
Фиг. 1 - Изображён КТ скан в поперечной проекции в нативную фазу. (С помощью программы радиант просмотровщик 64 бит при измерении элепсом определяется максимальное, среднее и минимальное значение плотности образования (опухоли) надпочечника);
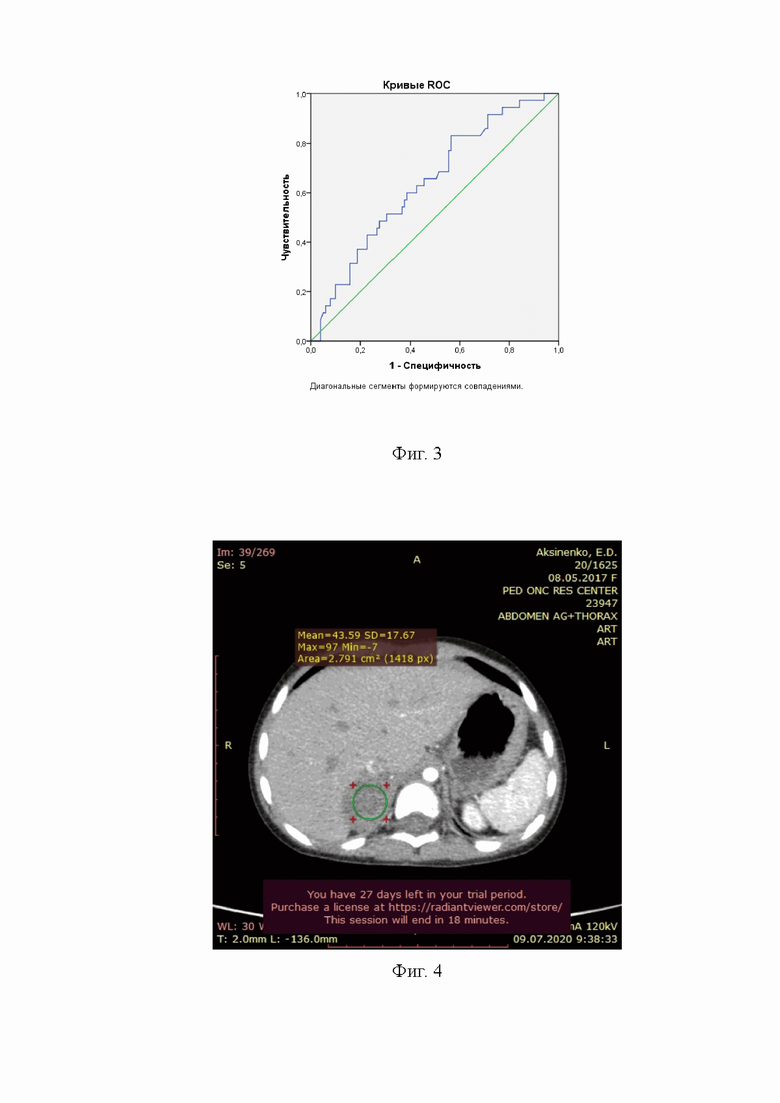
Фиг.2 - ROC-кривая для определения точки разделения показателей КТ на злокачественные и не злокачественные образования. (Плотность КТ преартериальная (нативная) фаза: с помощью ROC-кривой (Площадь под кривой составила 0,817 (95% ДИ 0,727-0,906, р=0,001) определили критическую точку по Юдену– значение плотности 31 НU(хаунсфилду), чувствительность в которой составила 95,0% при специфичности 60,0%. При плотности менее этого значения вероятность злокачественного характера образования низкая (6/27=22,2%), а выше- высокая (95/109=87,2%, р=0,0001). На графике можно выбрать другую критическую точку, где специфичность выше – 33,5…, чувствительность в которой составила 79,2% при специфичности 71,4%. При плотности ≤33,5… вероятность злокачественного характера образования низкая (21/47=44,7%), а >33,5- высокая (80/89=89,9%, р=0,0001);
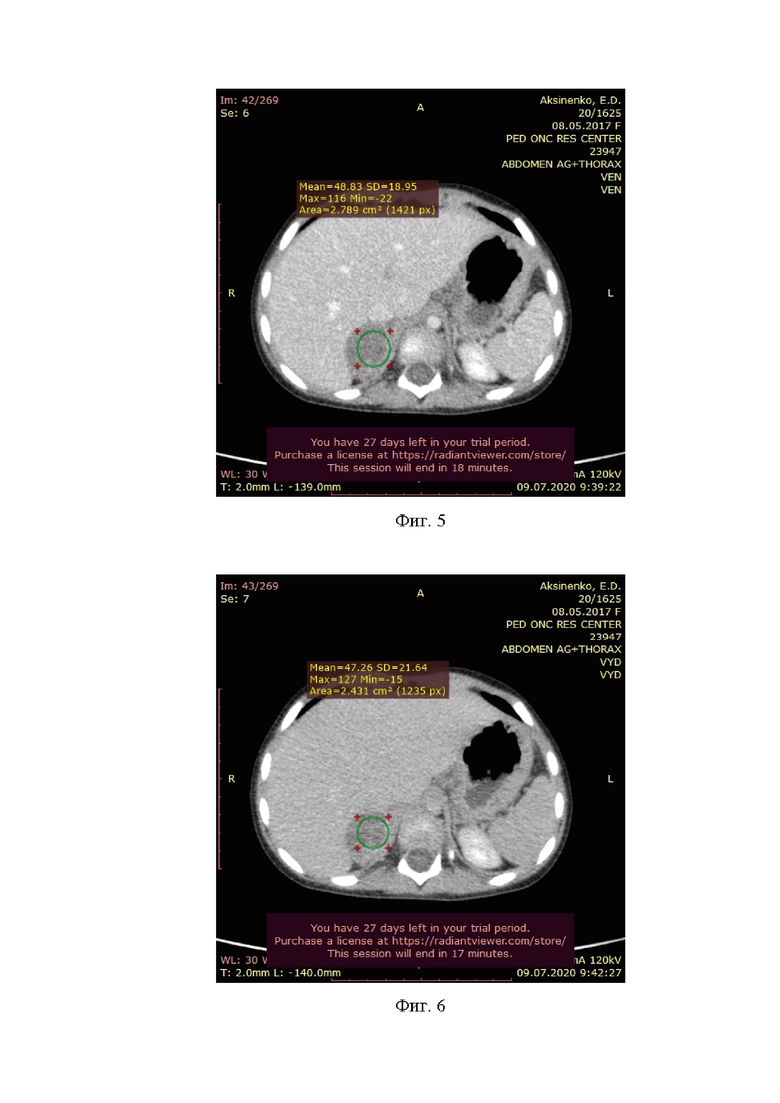
Фиг.3 - ROC-кривая для определения точки разделения показателей КТ на злокачественные и не злокачественные образования. (СД КТ преартериальна (нативная) фаза: с помощью ROC-кривой (Площадь под кривой составила 0,639 (95% ДИ 0,536-0,741), р=0,015) определили критическую точку по Юдену– значение СД 10,0 чувствительность в которой составила 82,9% при специфичности 45,4%. При индексе менее этого значения вероятность злокачественного характера образования высокая (44/51=86,3%), а выше- низкая (57/85=67,1%, р=0,015));
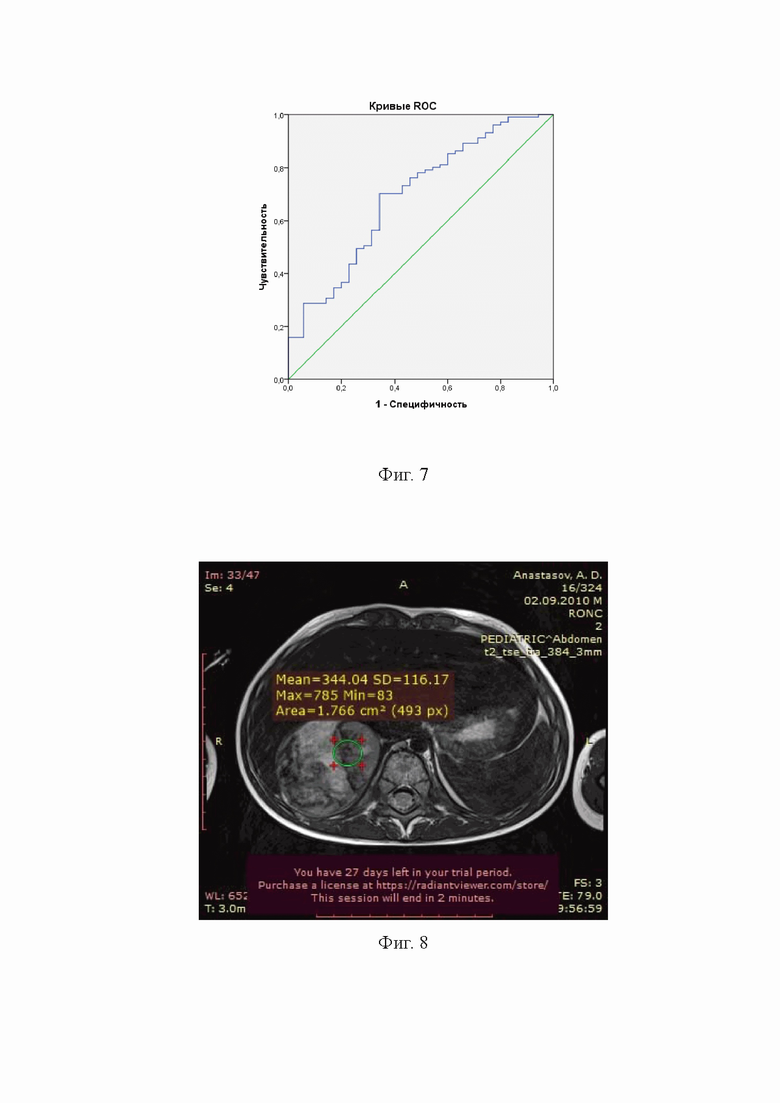
Фиг.4. - Изображён КТ скан в поперечной проекции в артериальную фазу. (С помощью программы радиант просмотровщик 64 бит при измерении элепсом определяется максимальное, среднее и минимальное значение плотности образования (опухоли) надпочечника);
Фиг.5 - Изображён КТ скан в поперечной проекции в венозную фазу. (С помощью программы радиант просмотровщик 64 бит при измерении элепсом определяется максимальное, среднее и минимальное значение плотности образования (опухоли) надпочечника);
Фиг.6 - Изображён КТ скан в поперечной проекции в выделительную фазу. (С помощью программы радиант просмотровщик 64 бит при измерении элепсом определяется максимальное, среднее и минимальное значение плотности образования (опухоли) надпочечника;
Фиг.7 - ROC-кривая для определения точки разделения показателей КТ на злокачественные и не злокачественные образования. (Плотность КТ поственозная фаза: с помощью ROC-кривой (Площадь под кривой составила 0,692 (95% ДИ 0,589-0,794, р=0,001) определили критическую точку по Юдену - значение плотности 67,4 HU, чувствительность в которой составила 70,3% при специфичности 65,7%. При плотности менее этого значения вероятность злокачественного характера образования низкая (30/53=56,6%), а выше- высокая (71/83=85,5%, р=0,0002)).
Таким образом, статистически значимым явились показатели:
Таблица 1
Для составления индивидуального прогноза наличия злокачественного образования необходимо вычислить индекс злокачественности по формуле
ИЗ=0,014* КТ натив -0,030* СД КТ натив +0,007* КТ поственозная,
Если полученная сумма более 0,5 - можно прогнозировать злокачественный характер образования. Если же сумма меньше 0,5, наличие злокачественного роста маловероятно.
МРТ выполняли на высокопольном МР-томографе Skyra (3T) Siemens (Germany).
Исследование проводят с использованием нательной катушки, которая укладывалась на живот пациента, затем фиксировалась к столу с помощью специальных креплений для уменьшения артефактов и предотвращения непроизвольного смещения катушки во время исследования. Для лучшей визуализации одновременно подключают сегменты встроенной в стол пациента матричной катушки. Сочетанное использование катушек улучшало качество используемых изображений. Исследование проводят в положении пациента на столе лежа на спине - головой в сторону изоцентра магнита, руки расположены вдоль туловища.
Пациенты младше 3-х лет проходят исследование под глубокой седацией. Специальную подготовку остальных пациентов не проводят, однако, рекомендовалось по возможности воздержаться от приема пищи за 2 часа до исследования.
Первичное центрирование пациента проводят с помощью световой метки по срединной линии живота на уровне мечевидного отростка, или на 5-10 см ниже (в зависимости от размеров пациента). Для получения топограммы использовали быструю поисковую программу Abdomen – localizer, в основе которой – импульсная последовательность градиентного эха длительностью 18с без задержки дыхания. Полученные изображения в трех взаимно перпендикулярных плоскостях использовали для дальнейшего позиционирования срезов. Стандартный протокол исследования предполагает получение Т2 и Т1 взвешенных изображений в коронарной и аксиальной плоскостях, с подавлением МР-сигнала от жировой ткани и без него.
Исследования были проведены на аппарате Magnetom Skyra® 3.0T (Siemens, ФРГ) с использованием гибкой радиочастотной 8-канальной приемной катушки «для тела», которую укладывали на область живота, размещенных в приборе в положении «supine» (на спине), центрация на область мечевидного отростка. При анализе данных настоящего исследования были использованы следующие последовательности:
1. Т2 взвешенные изображения (Т2ВИ) на основе импульсной последовательности (ИП) Turbo Spin Echo (Т2ВИ TSE), без и с частотным подавлением сигнала жировой ткани в двух ортогональных проекциях (коронарной и аксиальной проекциях), со следующими параметрами: поле обзора 300-320 мм, матрица изображения 320, толщина среза 3 мм, межсрезовое расстояние – 0,6 мм, TR(время повтора)/TE(время эхо) = 1500 мс / 75 мс.
2. Диффузионно взвешенные изображения (ДВИ) на основе эхопланарной ИП с подавлением сигнала жировой ткани частотно селективным инвертирующим импульсом и построением карт измеряемого коэфициента диффузии (ИКД), со следующими параметрами: поле обзора 380 мм, матрица изображения 320, толщина среза 5 мм, межсрезовое расстояние – 0,6 мм, TR/TE = 1500 мс / 50 мс, b-фактор = 50, 400, 800.
3. Т1 взвешенные изображения (Т1ВИ) на основе градиентного эха в аксиальной со следующими параметрами: поле обзора 380 мм, матрица изображения 320, толщина среза 3 мм, межсрезовое расстояние - 0,6 мм, TR/TE = 4,3 мс / 1,89 мс.
Введение контрастного препарата проводилось при расчете дозы 0,2 мл/кг для 0,5 молярных препаратов гадолиния и 0,1 мл/кг для 1,0 молярных препаратов гадолиния. Скорость введения 3 мл/сек
Т1 ВИ преартериальная (нативная) фаза
Т1ВИ артериальная фаза 1 сек первое постконтрастное изображение получали через 30 сек, затем на 50 сек и на 90 секунде исследования.
Т1 ВИ венозная фаза 30 сек
Т1 ВИ поственозная (выделительная) фаза 50 сек
Т1 ВИ отсроченная фаза 90 сек
Для анализа проводили нормировку измеренной интенсивности МРТ- сигнала от опухоли по сигналу от поясничной мышцы на каждой последовательности исследования.
Интенсивность сигнала - насколько яркой или темной кажется структура на фоне окружающих тканей или при количественном анализе среднее значение интенсивности сигнала (ИС) в области интереса.
Неоднородность сигнала - наличие и степень выраженности неравномерности распределения сигнала структуры на фоне окружающих тканей или при количественном анализе разброс значений интенсивности сигнала внутри изучаемой области, который может быть оценен как абсолютное значение стандартного отклонения интенсивности сигнала (СО ИС) или отношение СО ИС к самой величине ИС в области интереса.
Данные характеристики доступны для простого визуального анализа, однако их можно оценить и количественно, используя стандартный интерфейс рабочей станции, что позволяет установить конкретные количественные референсные значения этих показателей.
ИС согласно заявляемому способу оценивали и по абсолютному значению. Для анализа проводили нормировку измеренной интенсивности МРТ- сигнала от опухоли по сигналу от поясничной мышцы.
В программе Радиант-просмотровщик 64 бит в аксиальной плоскости выбирали зону интереса, включающую точечные (микрокровоизлияния, кальцинация) и линейные (микрососуды, фиброз) структуры.
Затем при помощи ручной сегментации при измерении участка образования определяют среднее значение плотности в указанной зоне при этом максимальные и минимальные значения в расчет не берутся, четких требований к площади фигуры не предъявляется (лучше более 0,1 см2), проводится нормирование сигнала к плотности поясничной мышцы.
Далее программное обеспечение автоматически рассчитывает площадь сегментированных структур на срезе в выбранном объеме в миллиметрах показывает максимальные и минимальные значения интенсивности сигнала и стандартное отклонение неоднородности сигнала.
Способ иллюстрируется фигурами 8 – 22:
На Фиг.8 представлен МРТ срез в режиме Т2 ВИ в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
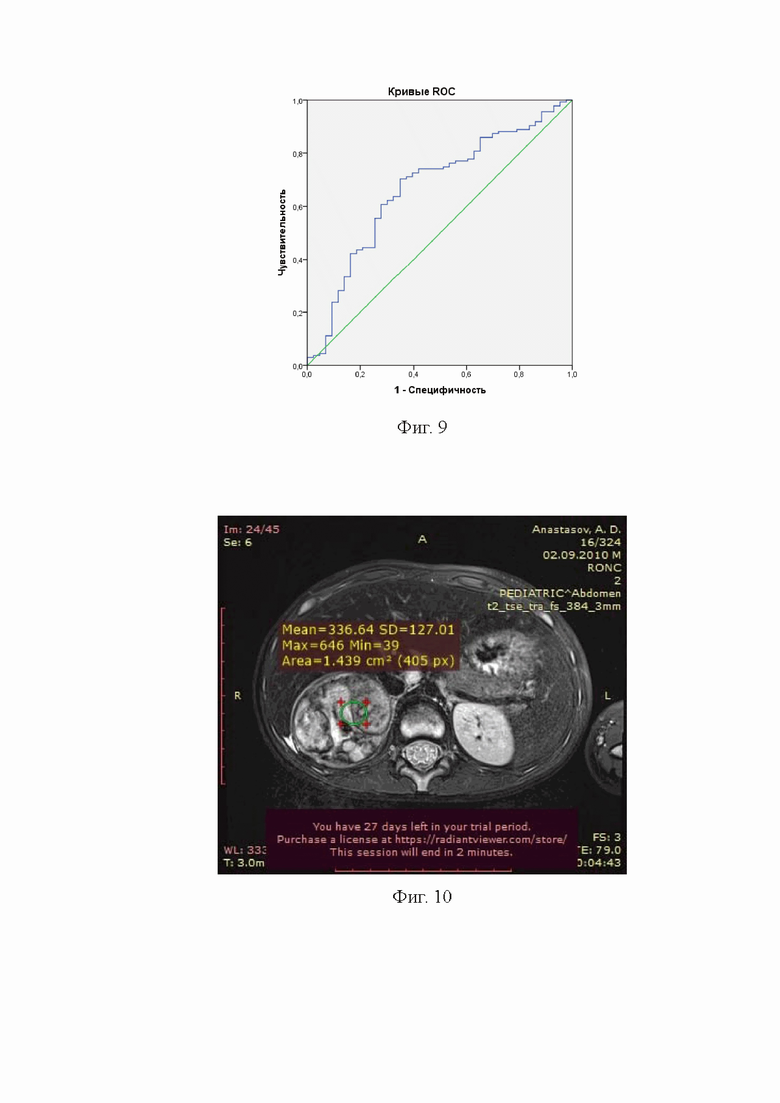
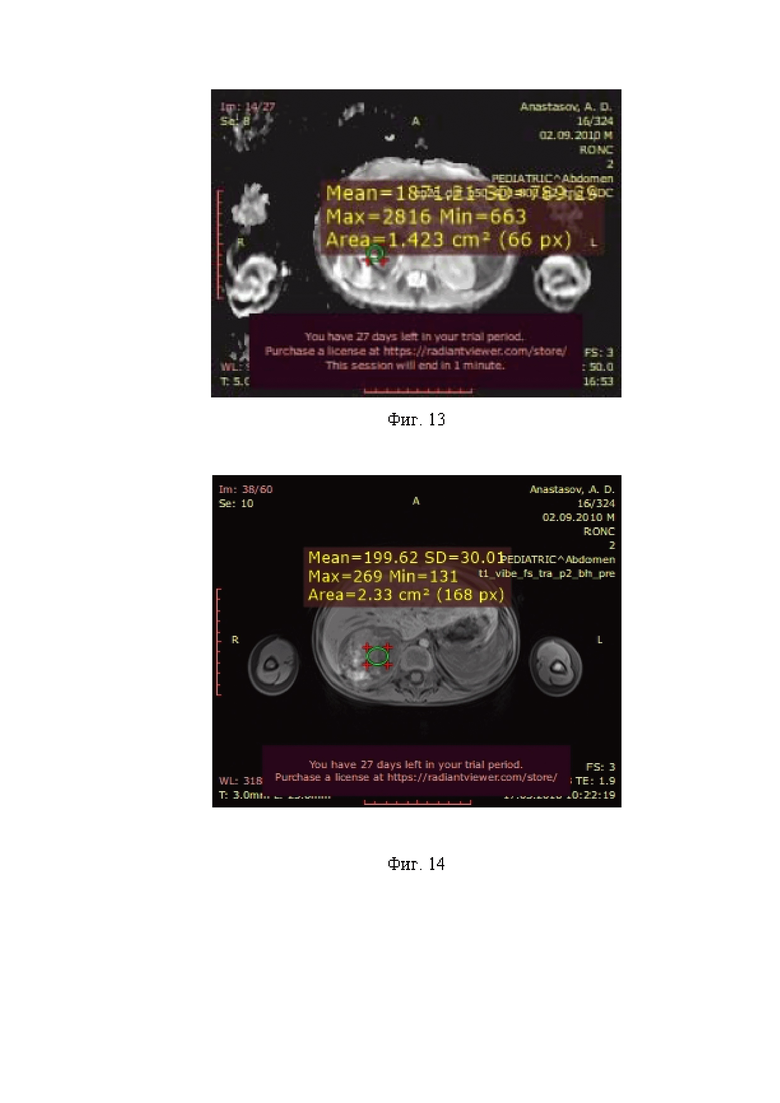
С помощью ROC- кривых (Фиг.9, Фиг.11, Фиг.15, Фиг.18, Фиг.20, Фиг.22) выявили точку разделения показателей нормированной интенсивности сигнала МРТ на злокачественные и доброкачественные образования.
Интенсивность сигнала Т2 взвешенные изображения
С помощью ROC-кривой (Фиг.9), площадь под кривой составила 0,668 (95% ДИ 0,573-0,762), р=0,001, определили критическую точку по Юдену– значение нормированной интенсивности сигнала Т2 ВИ 2,22, чувствительность в которой составила 70,4% при специфичности 65,1%. При нормированной интенсивности сигнала менее этого значения вероятность злокачественного характера образования низкая (40/68=58,8%), а выше- высокая (95/110=86,4%, р=0,00001).
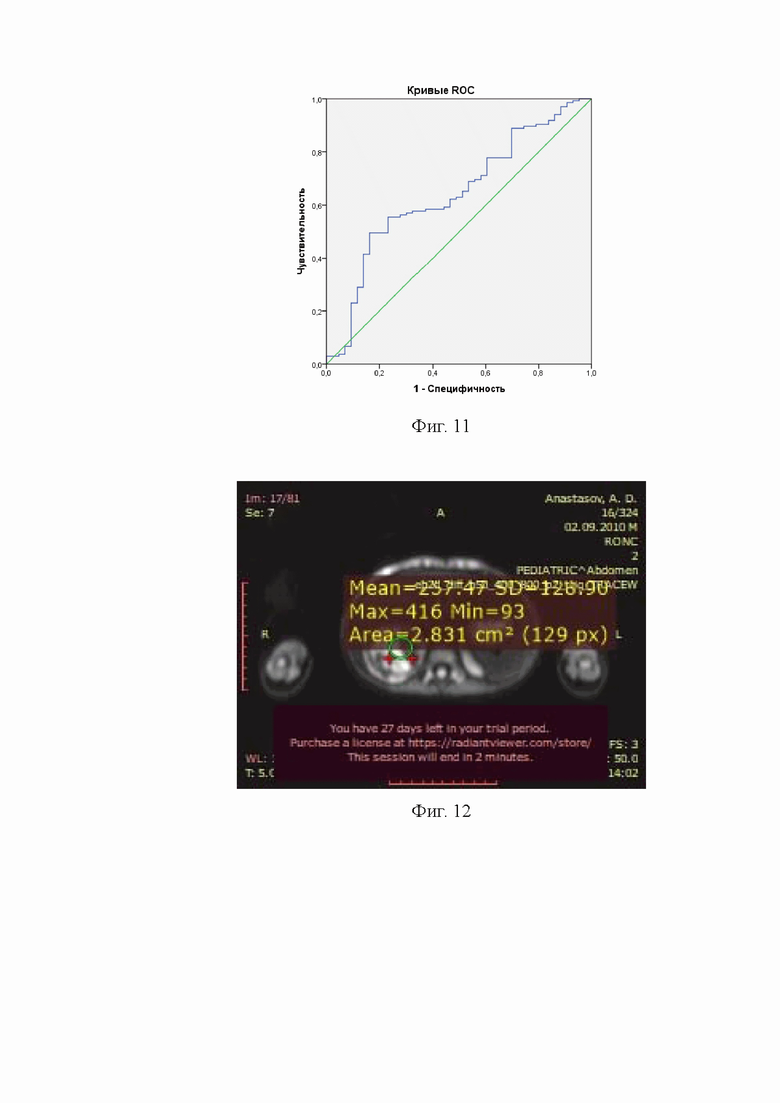
На Фиг. 10 представлен МРТ срез в режиме Т2 ВИ с жироподавлением в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
Интенсивность сигнала Т2 взвешенные изображения с жироподавлением
С помощью ROC-кривой (Фиг.11), площадь под кривой составила 0,643 (95% ДИ 0,548-0,737), р=0,005, определили критическую точку по Юдену значение нормированной интенсивности сигнала Т2 ВИ фс 2,43, чувствительность в которой составила 49,6% при специфичности 83,7%. При нормированной интенсивности сигнала менее этого значения вероятность злокачественного характера образования низкая (68/103=66,0%), а выше- высокая (67/75=89,3%, р=0,0002).
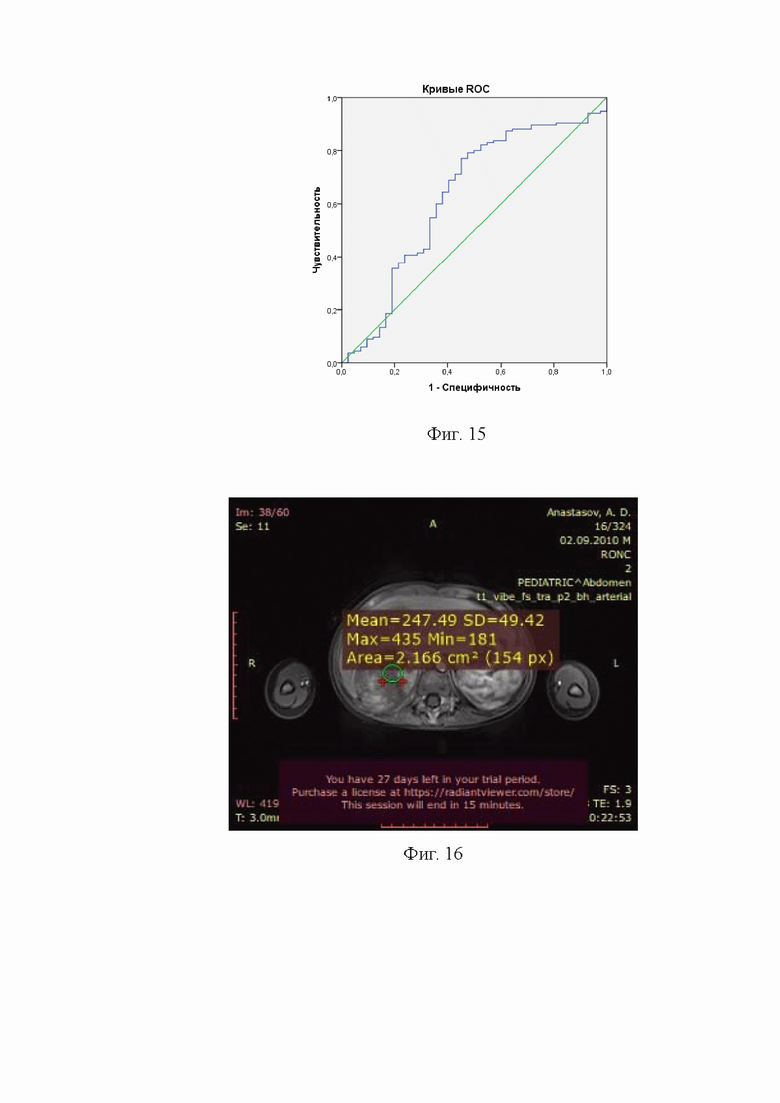
На Фиг. 12 представлен МРТ срез в режиме ИКД в аксиальной проекции. В программе Радиант- просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
На Фиг. 13 представлен МРТ срез в режиме ДВИ в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
На Фиг. 14 представлен МРТ срез в режиме Т1 ВИ преартериальная (нативная) фаза в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
Интенсивность сигнала Т1 взвешенные изображения преартериальная фаза
С помощью ROC-кривой (Фиг.15), площадь под кривой составила 0,628 (95% ДИ 0,523-0,733), р=0,012, определили критическую точку по Юдену–значение нормированной интенсивности сигнала Т1 ВИ пре 0,77, чувствительность в которой составила 77,0% при специфичности 54,8%. При нормированной интенсивности сигнала менее этого значения вероятность злокачественного характера образования низкая (31/53=58,5%), а выше- высокая (104/124=83,9%, р=0,0004).
На Фиг. 16 представлен МРТ срез в режиме Т1 ВИ артериальная фаза в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
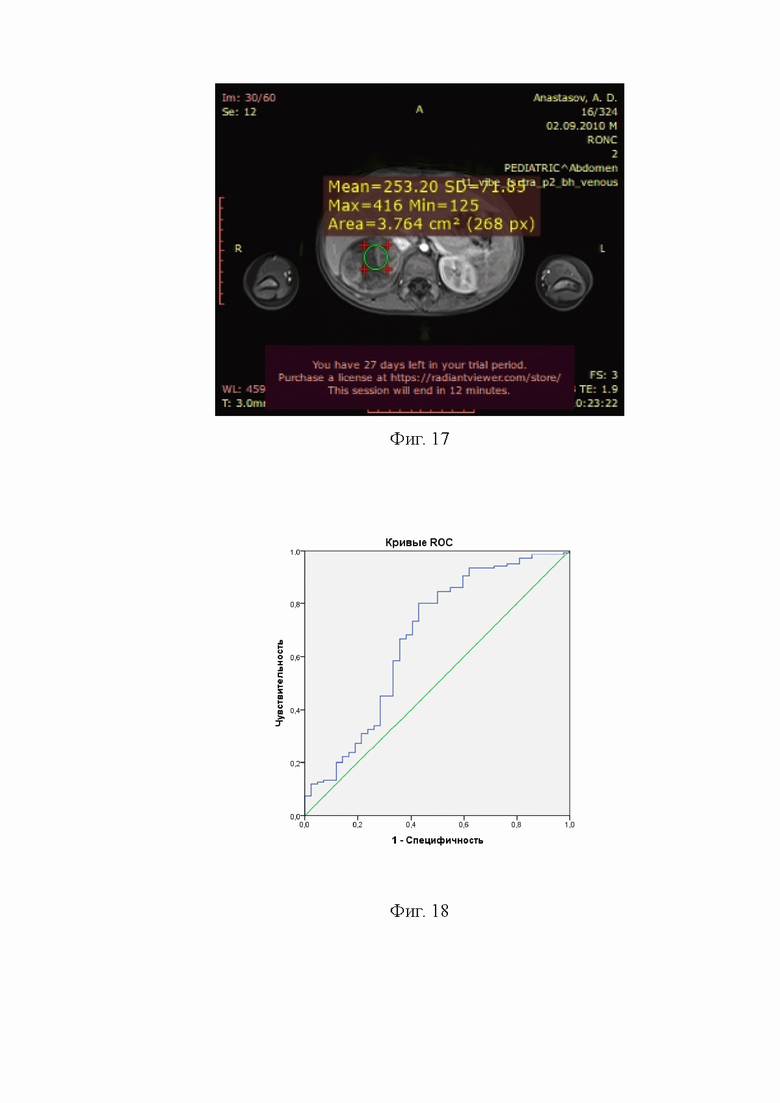
На Фиг.17 представлен МРТ срез в режиме Т1 ВИ венозная фаза в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
Интенсивность сигнала Т1 взвешенные изображения в венозную фазу.
С помощью ROC-кривой (Фиг.18), площадь под кривой составила 0,670 (95% ДИ 0,566-0,774), р=0,001), определили критическую точку по Юдену – значение нормированной интенсивности сигнала 1,20, чувствительность в которой составила 80,0% при специфичности 42,9%. При нормированной интенсивности сигнала менее этого значения вероятность злокачественного характера образования низкая (12/29=41,4%), а выше- высокая (123/148=83,1%, р=0,00001).
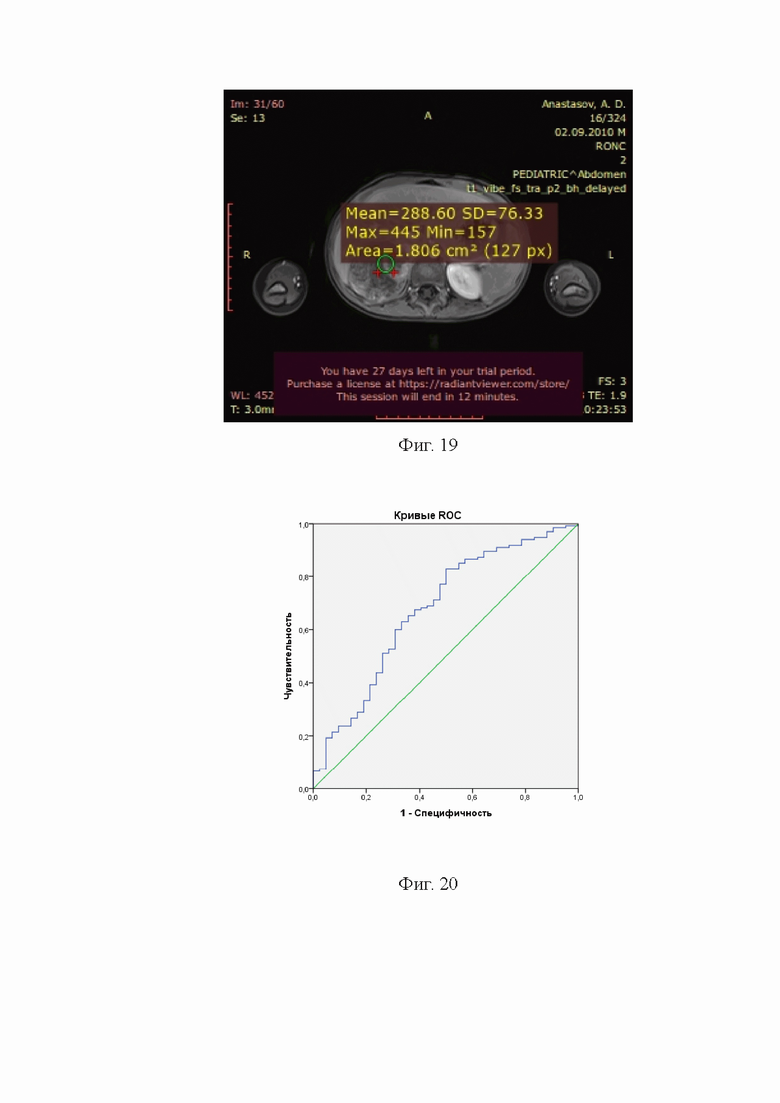
На Фиг. 19. представлен МРТ срез в режиме Т1 ВИ выделительная фаза в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
Интенсивность сигнала Т1 взвешенные изображения поственозная фаза.
С помощью ROC-кривой (Фиг. 20), площадь под кривой составила 0,678 (95% ДИ 0,581-0,774), р=0,001, определили критическую точку по Юдену– значение нормированной интенсивности сигнала Т1 ВИ пост 1,24, чувствительность в которой составила 83,0% при специфичности 50,0%. При нормированной интенсивности сигнала менее этого значения вероятность
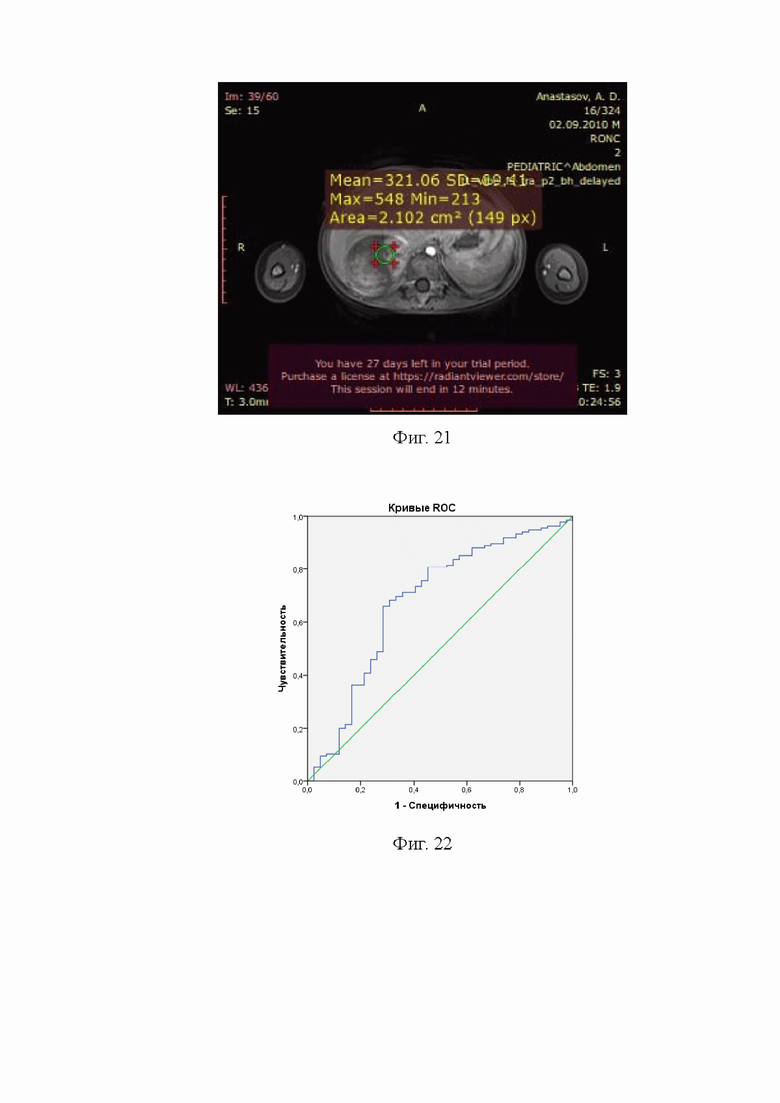
На Фиг.21 представлен МРТ срез в режиме Т1 ВИ, отсроченная фаза в аксиальной проекции. В программе Радиант просмотровщик 64 бит при измерении эллипсом выявлен участок образования надпочечника, определена максимальная средняя и минимальное значение интенсивности сигнала и степень неоднородности сигнала.
Интенсивность сигнала Т1 взвешенные изображения отсроченная фаза.
С помощью ROC-кривой (Фиг 22), площадь под кривой составила 0,678 (95% ДИ 0,578-0,778), р=0,001, определили критическую точку по Юдену– значение нормированной интенсивности сигнала Т1 ВИ отсроченной 1,45, чувствительность в которой составила 65,9% при специфичности 71,4%. При нормированной интенсивности сигнала менее этого значения вероятность злокачественного характера образования низкая (44/76=57,9%), а выше- высокая (91/101=90,1%, р=0,00001).
Таким образом, статистически значимым явились показатели:
Таблица 2
Показатели нормированной интенсивности сигнала выше данных пограничных значений с разной вероятностью свидетельствуют о злокачественном характере образования. При нормированной интенсивности сигнала менее данного значения вероятность злокачественного характера образования низкая.
Для выявления прогностических факторов среди показателей, для которых найдены пороговые значения, проведен однофакторный регрессионный анализ.
Результаты однофакторного регрессионного анализа.
Таблица 3
Как видно из таблицы, все показатели статистически значимы.
На втором этапе проводят многофакторный регрессионный анализ. Регрессионная модель, простроенная методом пошагового исключения, имела коэффициент детерминации 0,78 при р=0,0001, что позволяет использовать ее на практике. Получены коэффициенты для вычисления индекса злокачественности.(таблица 4)
Результаты многофакторного регрессионного анализа.
Таблица 4
Для составления индивидуального прогноза наличия злокачественного образования необходимо вычислить индекс злокачественности по формуле:
ИЗ=0,074*Т2ВИ+0,090*Т2ВИфс+0,192*Т1ВИпост,
где ИЗ – индекс злокачественности.
Если полученная сумма более 0,5, прогнозируют злокачественный характер образования. Если же сумма меньше 0,5, наличие злокачественного роста маловероятно.
Чувствительность данной модели составила 91,1%, специфичность – 20,9%, точность – 74,2%. прогностическая ценность положительного результата – 78,3%, прогностическая ценность отрицательного результата – 42,9%. Т.е. при данной границе разбиения получаем высокий процент ложно – положительных результатов и низкую специфичность (гипердиагностика злокачественности).
С помощью построения ROC-кривой (Площадь под кривой составила 0,727 (95% ДИ 0,645-0,809), р=0,0001) для суммы показателей найдено пороговое значение - критическая точка по Юдену – 0,77. С применением данной точки чувствительность модели составила 51,9%, специфичность – 85,7%, точность – 59,9%. прогностическая ценность положительного результата – 92,1%, прогностическая ценность отрицательного результата – 35,6%. Т.е. при данной границе разбиения получаем высокий процент ложно – отрицательных результатов (пропускаем злокачественные образования), но растет число истинно- отрицательных (точно определяем доброкачественные образования).
По данным гистологии всего злокачественных образований - 135, доброкачественных – 42
Данные гистологии
Таблица 5
Так как на практике важно не пропустить злокачественные образования, лучше пользоваться границей 0,5.
Одновременно (последовательное) исследование МСКТ и МРТ было выполнено 134 больным – 101 пациент со злокачественным поражением и 33 – с доброкачественным. С помощью вычисления индексов по ранее приведенным формулам выставлен диагноз по результатам МСКТ и МРТ и соотнесен с результатами гистологического исследования (Таблица 6)
Сопоставление результатов МСКТ и МРТ с данными гистологического исследования для оценки информативности для выявления злокачественной природы образований (n=134)
Таблица 6
Результаты МСКТ и МРТ совпадают в 104/134 (77,6%) случаях. При МСКТ диагноз установлен правильно у 109 (81,3%) пациентов, что статистически значимо чаще (р=0,031), чем при МРТ – у 95(70,9%).
Для выбора дальнейшей тактики лечения важно не пропустить злокачественное образование, поэтому при наличии результатов 2 методов диагностики (МСКТ и МРТ) – при выявлении злокачественности процесса хотя бы одним из методов, мы считали опухоль злокачественной (Таблица 7, Таблица 8)
Информативность совместного использования КТ и МРТ (n=134)
Таблица 7
При данном подходе чувствительность увеличивается до 98%, но специфичность снижается до 15,2%.
Показатели информативности МСКТ, МРТ и совместно (n=134)
Таблица 8
Таким образом, заявленный способ повышает диагностические возможности для определения опухолей надпочечников, что способствует выбору оптимальной тактики ведения пациентов с опухолями надпочечников.
Клинический пример №1.
Девочка 2,4 года (И/Б 11/1201) с диагнозом по данным гистологического исследования ганглионеврома левого надпочечника 1 стадии. Выполнены оба исследования.
ИЗ (МРТ) =0,074* 2,065+0,090* 2,132 фс+0,192* 0,728=0,485
По данным МРТ – 0,485 т.о. по данным обследования можно сделать заключение о незлокачественном характере образования.
ИЗ (КТ) =0,014* 23,68 -0,030* 10,19 +0,007* 48,42=0,365
По данным КТ Индекс злокачественности составил 0,365, т.о. по данным обследования можно сделать заключение о незлокачественном характере образования.
Клинический пример №2.
Девочка 2,5 лет (И/Б 15/2354) с диагнозом по данным гистологического исследования нейробластома правого надпочечника 1 стадии. Выполнены оба исследования.
ИЗ (МРТ)=0,074* 2,963+0,090* 2,881+0,192* 2,732=1,004
По данным МРТ – 1,004 т.о. по данным обследования можно сделать заключение о злокачественности образования.
ИЗ (КТ)=0,014* 31,51 -0,030* 5,2 +0,007* 68,73=0,766
По данным КТ Индекс злокачественности составил 0,766, т.о. по данным обследования можно сделать заключение о злокачественности образования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛУЧЕВОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕЙ НАДПОЧЕЧНИКОВ У ДЕТЕЙ С ИСПОЛЬЗОВАНИЕМ МАГНИТНОЙ РЕЗОНАНСНОЙ ТОМОГРАФИИ | 2023 |
|
RU2814782C1 |
| СПОСОБ ЛУЧЕВОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕЙ НАДПОЧЕЧНИКОВ У ДЕТЕЙ С ИСПОЛЬЗОВАНИЕМ МУЛЬТИСПИРАЛЬНОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ С ВНУТРИВЕННЫМ КОНТРАСТИРОВАНИЕМ | 2023 |
|
RU2815158C1 |
| Способ дифференциальной диагностики доброкачественных и злокачественных образований в печени у детей | 2020 |
|
RU2748530C1 |
| Способ выполнения кинематической магнитно-резонансной томографии височно-нижнечелюстных суставов у пациентов с металлоконструкциями | 2022 |
|
RU2816449C2 |
| Способ диагностики огнестрельных ранений позвоночника с помощью магнитно-резонансной и рентгеновской компьютерной томографии | 2019 |
|
RU2714082C1 |
| СПОСОБ ДИАГНОСТИКИ ОЗЛОКАЧЕСТВЛЕНИЯ ХОНДРОМ | 2004 |
|
RU2275851C1 |
| СПОСОБ ДИНАМИЧЕСКОЙ МАГНИТНО-РЕЗОНАНСНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЯИЧНИКОВ | 2015 |
|
RU2578184C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2571708C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ ИНТРАОПЕРАЦИОННЫХ И РАННИХ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ПРИ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЯХ ПРИ ОПУХОЛЯХ ПАРЕНХИМЫ ПОЧЕК | 2019 |
|
RU2709837C1 |
| Способ прогнозирования эффективности химиотерапии при раке мочевого пузыря по данным магнитно-резонансной томографии | 2022 |
|
RU2800817C1 |
Изобретение относится к медицине, а именно к онкологии, лучевой диагностике, и может быть использовано для лучевой дифференциальной диагностики опухолей надпочечников у детей. Проводят магнитно-резонансную томографию (МРТ) и получают Т1 и Т2 взвешенных изображений (ВИ) в коронарной и аксиальной плоскостях с подавлением МР-сигнала от жировой ткани и без него. Далее, вводят контрастный препарат гадолиния и получают Т1 ВИ поственозную фазу 50 сек. Проводят мультиспиральную компьютерную томографию (МСКТ) с внутривенным контрастированием. Вычисляют индекс злокачественности для МРТ (ИЗ1) и индекс злокачественности для МСКТ (ИЗ2). Если одно из ИЗ1 и ИЗ2 более 0,5, то прогнозируют злокачественный характер образования. Если сумма ИЗ1 и ИЗ2 меньше 0,5, то наличие злокачественного роста маловероятно. Способ обеспечивает выбор наиболее эффективной тактики ведения пациентов за счет объединения двух методик определения индекса злокачественности новообразований надпочечников – МРТ и КТ. 22 ил., 8 табл., 2 пр.
Способ лучевой дифференциальной диагностики опухолей надпочечников у детей, заключающийся в том, что проводят магнитно-резонансную томографию (МРТ) и получают Т1 и Т2 взвешенных изображений (ВИ) в коронарной и аксиальной плоскостях с подавлением МР-сигнала от жировой ткани и без него, после чего вводят контрастный препарат гадолиния и получают Т1 ВИ поственозную фазу 50 сек, проводят мультиспиральную компьютерную томографию (МСКТ) с внутривенным контрастированием, вычисляют индекс злокачественности для МРТ (ИЗ1) и индекс злокачественности для МСКТ (ИЗ2) по формулам
ИЗ1=0,074*Т2ВИ+0,090*Т2ВИфс+0,192*Т1ВИпост,
где Т2ВИ - значение интенсивности сигнала опухоли в режиме Т2ВИ,
Т2ВИфс - значение интенсивности сигнала опухоли в режиме Т2ВИ с жироподавлением,
Т1ВИпост - значение интенсивности сигнала опухоли в режиме Т1ВИ в поственозную фазу;
ИЗ2=0,014*КТнатив-0,030*СД КТнатив+0,007* КТпост,
где КТ натив – среднее значение интенсивности сигнала надпочечника в нативную фазу;
СД КТнатив - абсолютное значение стандартного отклонения интенсивности сигнала надпочечника в нативную фазу;
КТпост - среднее значение интенсивности сигнала надпочечника в поственозную фазу; если одно из ИЗ1 и ИЗ2 более 0,5, то прогнозируют злокачественный характер образования, если сумма ИЗ1 и ИЗ2 меньше 0,5, то наличие злокачественного роста маловероятно.
| СПОСОБ ЛУЧЕВОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕЙ НАДПОЧЕЧНИКОВ У ДЕТЕЙ С ИСПОЛЬЗОВАНИЕМ МУЛЬТИСПИРАЛЬНОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ С ВНУТРИВЕННЫМ КОНТРАСТИРОВАНИЕМ | 2023 |
|
RU2815158C1 |
| СПОСОБ ЛУЧЕВОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕЙ НАДПОЧЕЧНИКОВ У ДЕТЕЙ С ИСПОЛЬЗОВАНИЕМ МАГНИТНОЙ РЕЗОНАНСНОЙ ТОМОГРАФИИ | 2023 |
|
RU2814782C1 |
| ПЫКОВ М | |||
| И | |||
| и др | |||
| Диагностика злокачественных опухолей надпочечников у детей | |||
| Вестник Российского научного центра рентгенорадиологии | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| ABDELRAHMAN K | |||
| H | |||
| et al | |||
| Imaging features of adrenal gland masses in the pediatric population | |||
| Abdominal Radiology | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
Авторы
Даты
2024-12-04—Публикация
2024-04-26—Подача