Область техники, к которой относится изобретение
Настоящее изобретение относится к производному платины и, в частности, к карбоплатиновому комплексу, полученному путем образования водородных связей на основе молекул карбоплатина, а также к фармацевтическому препарату на основе платины, полученному из этого карбоплатинового комплекса.
Предпосылки
Открытие противоопухолевой эффективности цис-дихлородиамминплатины дало начало исследованиям и применению противоопухолевых препаратов на основе платины, а также сделало исследования противоопухолевых препаратов на основе платины одной из актуальных задач в области терапии опухолей в последние годы. Цисплатин (Cisplatin), содержащий цис-дихлородиамминплатину в качестве активного компонента, является первым противоопухолевым препаратом на основе платины для человека, и не является клеточно-специфическим препаратом. Исследования показывают, что цисплатин может связываться с ДНК и вызывать перекрестную сшивку, тем самым разрушая функцию ДНК и подавляя репликацию ДНК клеток. В клиническом применении цисплатин обладает широким противоопухолевым спектром и применяется при плоскоклеточном раке головы и шеи, раке яичников, эмбриональной карциноме, семиноме, раке легких, раке щитовидной железы, лимфосаркоме, ретикулосаркоме и так далее. Статистика больших данных показывает, что цисплатин обладает хорошим эффектом при лечении опухолей, но в клинической практике он также демонстрирует серьезные токсические и побочные эффекты. С другой стороны, учитывая лекарственную устойчивость химиотерапевтических препаратов, по-прежнему существует потребность в поиске альтернативных лекарственных средств.
Карбоплатин представляет собой противораковый препарат на основе платины второго поколения, полученный путем молекулярной модификации цисплатина, и представляет собой новое соединение платины, полученное путем одновременной замены двух атомов хлора в молекуле цисплатина на 1,1-циклобутандикарбоновую кислоту. Он частично преодолевает токсическое и побочное действие цисплатина и при этом сохраняет противоопухолевые свойства. Клиническое применение показывает, что биохимические и физические характеристики карбоплатина аналогичны характеристикам цисплатина, но его нефротоксичность, ототоксичность и нейротоксичность, особенно желудочно-кишечные реакции, значительно ниже, чем у цисплатина, и, таким образом, карбоплатин стал противоопухолевым препаратом широкого спектра действия, который уже более десяти лет привлекает к себе пристальное внимание. Как и цисплатин, карбоплатин является препаратом, неспецифическим в отношении клеточного цикла, он в основном действует на атомы N7 и O6 гуанина в ДНК, вызывая тем самым межцепочечную и внутрицепочечную сшивку ДНК, нарушая репликацию молекул ДНК, и приводя к апоптозу опухолевых клеток.

Цисплатин Карбоплатин
В дополнение к цисплатину и карбоплатину, различные противораковые препараты на основе платины находятся на стадии исследований и клинических испытаний. Помимо проблемы токсических реакций, стабильность этих препаратов, особенно в водных растворах, стала фатальным недостатком для их клинического применения. Поэтому постоянно осуществляются попытки усовершенствования и модификации препаратов с уже имеющимися структурами.
С другой стороны, проблема резистентности к химиотерапевтическим препаратам также является критическим фактором, влияющим на лечение опухолей, так как после многократного контакта опухолевых клеток с лекарством чувствительность к лекарству уменьшается или даже исчезает, что приводит к снижению эффективности или полной неэффективности препарата. Когда возникает лекарственная устойчивость, химиотерапевтический эффект препарата значительно снижается, и дальнейшее введение препарата приводит к неэффективному лечению. В то же время, когда опухолевые клетки становятся устойчивыми к одному противоопухолевому препарату, у них также может развиться перекрестная устойчивость к другим противоопухолевым препаратам с отличающейся структурой и механизмами действия, и такая множественная лекарственная устойчивость (МЛУ) или перекрестная резистентность является наиболее важной причиной неэффективности химиотерапии опухолей, и для этого до сих пор нет хорошей стратегии в клинической практике. С развитием трансляционной медицины было обнаружено, что мутации генов, стимулирующие опухоли, облегчают возникновение и развитие опухолей посредством различных сигнальных путей и механизмов, что проложило путь для таргетированной терапии опухолей. Однако лекарственная устойчивость неизбежно возникает и при таргетированной терапии через 8-14 месяцев лечения, и решение вопроса лекарственной устойчивости по-прежнему остается проблемой для успешного лечения опухолей.
Продолжающиеся исследования, разработка и регистрация новых лекарств, безусловно, являются целью всей фармацевтической отрасли, и модернизация классических противораковых, противовирусных и антибактериальных препаратов также является важной идеей и направлением для улучшения терапевтической эффективности и расширения показаний.
Сущность изобретения
Настоящее изобретение относится к комплексу карбоплатина, где молекулы 1,1-циклобутандикарбоновой кислоты введены в молекулу карбоплатина посредством образования водородных связей, улучшена растворимость в воде, стабильность, биодоступность и другие функции карбоплатина, в результате чего получается фармацевтический препарат на основе платины с пониженной токсичностью.
Кроме того, настоящее изобретение обеспечивает фармацевтический препарат, содержащий указанный выше карбоплатиновый комплекс в качестве активного компонента, который обладает не только хорошей стабильностью, но также явной эффективностью.
Настоящее изобретение дополнительно обеспечивает способы получения вышеуказанного карбоплатинового комплекса и фармацевтического препарата. Контролируя и оптимизируя процесс очистки, получают устойчивый комплекс, образованный карбоплатином и 1,1-циклобутандикарбоновой кислотой за счет нековалентных связей, который в качестве целевого продукта имеет очень высокую чистоту.
Настоящее изобретение также обеспечивает применение вышеуказанного карбоплатинового комплекса в приготовлении противоопухолевого, антибактериального, противогрибкового или противовирусного лекарственного средства, тем самым улучшая направленную доставку лекарства и уменьшая токсические и побочные эффекты лекарственного средства.
Настоящее изобретение также обеспечивает способ контроля качества вышеуказанного карбоплатинового комплекса в виде нерасфасованного лекарственного средства, который позволяет контролировать качество и безопасность карбоплатинового комплекса, используемого в производстве фармацевтических препаратов.
Первый аспект настоящего изобретения относится к карбоплатиновому комплексу, который представляет собой комплекс, сформированный путем объединения карбоплатина и 1,1-циклобутандикарбоновой кислоты посредством двух водородных связей, где каждая из двух водородных связей образована между карбонильным кислородом молекулы карбоплатина и карбоксильным водородом молекулы 1,1-циклобутандикарбоновой кислоты.
В частности, указанный выше карбоплатиновый комплекс может быть комплексом, образованным из одной молекулы карбоплатина и одной молекулы 1,1-циклобутандикарбоновой кислоты посредством межмолекулярных водородных связей. Структура карбоплатинового комплекса по настоящему изобретению может быть представлена следующим образом:
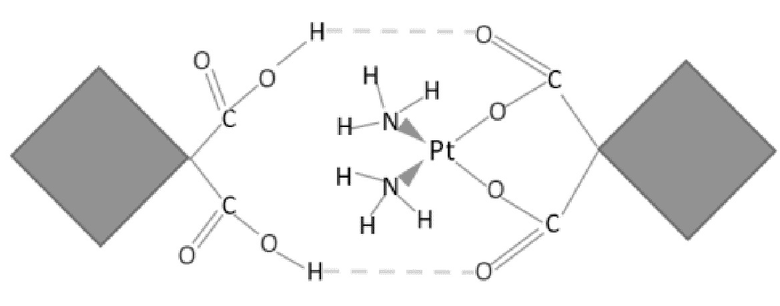
Эта структура иллюстрирует основной продукт, образованный путем комбинации карбоплатина и 1,1-циклобутандикарбоновой кислоты, его молекулярная формула может быть представлена как C6H12N2O4Pt·C6H6O4, а его молекулярная масса может составлять 515,0917.
Как описано выше, карбоплатин представляет собой продукт, полученный реакцией замещения между цисплатином и 1,1-циклобутандикарбоновой кислотой, где два атома хлора в молекуле цисплатина замещены 1,1-циклобутандикарбоновой кислотой. В смеси, образующейся при синтезе карбоплатина, кроме свободного мономолекулярного цисплатина, карбоплатина и 1,1-циклобутандикарбоновой кислоты, будут также компоненты с относительно большой молекулярной массой. Дальнейшее исследование состава этих примесей заставило изобретателя сосредоточить внимание на конкретных продуктах, образующихся в результате дальнейшей самосборки карбоплатина с 1,1-циклобутандикарбоновой кислотой посредством водородных связей. Дополнительный анализ и исследование показали, что «примесь» на самом деле представляет собой комплекс, образованный карбоплатином и свободной 1,1-циклобутандикарбоновой кислотой в молярном соотношении 1:1 за счет водородных связей и геометрического пространства. Исследования также показали, что этот комплекс чрезвычайно неупорядочен и нестабилен как «химическое лекарство», очень чувствителен к кислоте и щелочи, температуре, оптическому спектру, хроматографии, электромагнитному полю и т.д., и легко разлагается на карбоплатин и свободную 1,1-циклобутандикарбоновую кислоту. Однако в мягких условиях (при температуре ниже 80°С, рН 2-7,5, в темноте и т.д.) комплекс полностью стабилен. Кроме того, исследования автора изобретения также показали, что структура комплекса аналогична структуре пар оснований ДНК, где карбоплатин и 1,1-циклобутандикарбоновая кислота также собраны вместе посредством двух водородных связей и геометрической пространственной структуры, и многие особенности комплекса также аналогичны характеристикам пар оснований ДНК. В подходящей среде, например, когда фермент (хеликаза) активен, водородные связи могут быть разорваны, и активность карбоплатина высвобождается.
Для дальнейшего изучения связывания карбоплатина с 1,1-циклобутандикарбоновой кислотой в настоящем изобретении используют метод ядерного магнитного резонанса (1H-ЯМР) с использованием дейтерированного диметилсульфоксида (ДМСО) в качестве растворителя (общепризнано, что он эквивалентен влиянию водной среды на объект испытаний) для изучения химических сдвигов водорода карбоплатина и 1,1-циклобутандикарбоновой кислоты в смешанном состоянии. Результаты показывают, что при постоянном количестве 1,1-циклобутандикарбоновой кислоты с увеличением количества карбоплатина в результатах титрования смеси двух компонентов происходит лишь изменение химического сдвига карбоксильного водорода, в то время химического сдвига амино водорода не отмечается. Можно сделать вывод, что самосборка между карбоплатином и 1,1-циклобутандикарбоновой кислотой достигается посредством карбоксильного водорода.
Токсичность препаратов платины обусловлена координационными связями платины, активная координационная связь атома платины может связываться с G-N7 в ДНК с образованием более сильного аддукта. Уменьшение побочных эффектов препаратов платины заключается в замедлении скорости и эффективности формирования аддукта. Когда карбоплатин и 1,1-циклобутандикарбоновая кислота образуют комплекс, то есть комплексный субстрат, имеющий структуру, аналогичную паре оснований ДНК A-T/G-C, молекула карбоплатина является хозяином, а молекула 1,1-циклобутандикарбоновой кислоты – гостевой молекулой для обеспечения водородных связей, и лекарственная активность хозяина эффективно блокируется гостевой молекулой с образованием комплекса с нулевой или очень низкой токсичностью в отношении ДНК, таким образом, не наблюдается токсичности для нормальных нереплицирующихся клеток.
В другом варианте осуществления настоящего изобретения карбоплатиновый комплекс получают из самособирающегося продукта карбоплатина и 1,1-циклобутандикарбоновой кислоты, и массовое содержание карбоплатинового комплекса составляет 95% или более.
Самособирающийся продукт высокой чистоты может быть получен посредством соответствующего управления технологическим процессом, тем самым предоставляя идеи и направления для создания препаратов платины с лучшими свойствами, такими как стабильность при растворении в воде, противоопухолевый спектр, токсические и побочные эффекты, и механизм действия на основе карбоплатина. Для того чтобы отличить его от карбоплатина, этот тип карбоплатинового комплекса в настоящем изобретении обозначают аббревиатурой «карбоплатин 4.0». Иными словами, карбоплатин 4.0 по настоящему изобретению содержит продукт самосборки карбоплатина и 1,1-циклобутандикарбоновой кислоты в качестве основного компонента, где уровень самосборки составляет 95% или более. За счет контроля соответствующего процесса приготовления, уровень самосборки может достигать 96% или более, или 98% или более, или даже до 99% или более.
Структура карбоплатинового комплекса, предложенная в настоящем изобретении, включает карбоплатин и 1,1-циклобутандикарбоновую кислоту, объединенные водородной связью. Что касается карбоплатинового комплекса, пик фазового перехода начинает формироваться (т.е. начинается плавление и разложение, обычно образуя острый пик фазового перехода) примерно при 197,8±2°C в результатах, измеренных с помощью дифференциальной сканирующей калориметрии (ДСК), и/или не отмечается дифракционного пика при 2θ примерно 11,55 ± 0,2º в результатах, полученных в анализе с применением рентгеновской порошковой дифрактометрии (XRPD).
В частности, в приведенных выше результатах измерения XRPD дифракционный пик при 2θ примерно 11,55±0,2° является характеристическим пиком карбоплатина. Понятно, что из-за влияния образцов, условий детекции и т.д., приведенные выше результаты детекции могут иметь определенные отклонения, и все дифракционные пики, появляющиеся около 11,55° (например, 11,55±0,2°), обычно можно считать характеристическими пиками карбоплатина. Согласно результатам исследований по настоящему изобретению при анализе посредством XRPD карбоплатинового комплекса обычно присутствуют дифракционные пики при 7,55°; 10,51°; 14,63°; 15,10°; 15,66°; 16,78°; 18,55°; 20,83°; 22,86°; 23,67°; 24,02° и т.д.; эти дифракционные пики могут быть использованы в качестве характеристических пиков указанного выше карбоплатинового комплекса, и все их отклонения могут находиться в диапазоне ±0,2° (например, указанный выше дифракционный пик при 2θ 7,55º может быть пиком дифракции при 7,55±0,2º).
Кроме того, настоящее изобретение относится к фармацевтическому препарату, содержащему карбоплатиновый комплекс в качестве активного компонента.
Согласно классификации в области фармацевтики, фармацевтический препарат, предлагаемый настоящим изобретением, в основном используется в качестве противоопухолевого препарата, антибактериального препарата, противогрибкового препарата или противовирусного препарата.
В частности, фармацевтический препарат находится в форме жидкости для инъекций, лиофилизированного порошка для инъекций, перорального твердого препарата, гелеобразного препарата или спрея.
В фармацевтическом препарате по настоящему изобретению карбоплатиновый комплекс (т.е. карбоплатин 4.0) является активным компонентом, где 1,1-циклобутандикарбоновая кислота фактически играет роль фармацевтических вспомогательных веществ. Исследование по настоящему изобретению показывает, что 1,1-циклобутандикарбоновая кислота применима в качестве фармацевтического вспомогательного вещества для карбоплатина 4.0 благодаря особенности ее молекулярной структуры. Во-первых, сама 1,1-циклобутандикарбоновая кислота является важным сырьем для производства карбоплатина; во-вторых, 1,1-циклобутандикарбоновая кислота и карбоплатин могут формировать наиболее подходящий стабильный комплексный субстрат за счет водородных связей; кроме того, благодаря эффекту вспомогательного вещества 1,1-циклобутандикарбоновой кислоты изменяются и улучшаются такие свойства, как растворимость в воде, стабильность, биодоступность, таргетинг в отношении хеликазы и другие функции карбоплатина. Кроме того, 1,1-циклобутандикарбоновая кислота также образуется, когда карбоплатин связывается с ДНК, демонстрируя, что 1,1-циклобутандикарбоновая кислота имеет четкую структуру, контролируемое качество и химическую стабильность и, соответственно, следовые количества 1,1-циклобутандикарбоновой кислоты также безопасны для организмов.
На основании исследований свойств и эффективности вышеуказанного карбоплатинового комплекса, настоящее изобретение дополнительно обеспечивает применение карбоплатинового комплекса в производстве лекарственного средства, такого как противоопухолевое средство, антибактериальное средство, противогрибковое средство или противовирусное средство.
Основываясь на детальных исследованиях структуры и характеристик вышеуказанного карбоплатинового комплекса, автор настоящей заявки полагает, что карбоплатиновый комплекс с признаками, описанными в настоящем изобретении, является, если быть точным, новым препаратом карбоплатина, который можно понимать как фармацевтический препарат, аналогичный липосомной ловушке (liposome entrapment). С учетом того, что противоопухолевая эффективность карбоплатина уже не вызывает сомнений, экспериментально может быть подтвержден следующий механизм действия: комплекс структуры хозяин/гость, полученный из карбоплатина и 1,1-циклобутандикарбоновой кислоты за счет водородной связи, готовят в виде нового фармацевтического препарата, который в условиях хеликазной активности может разрушаться и высвобождать одну молекулу карбоплатина и одну молекулу 1,1-циклобутандикарбоновой кислоты, другими словами, водородная связь комплекса является мишенью для хеликазы, и комплекс (карбоплатин 4.0) можно рассматривать как комплексообразующий субстрат для хеликазы.
Таким образом, в сочетании с вышеуказанными исследованиями механизма можно полагать, что лекарственное средство по настоящему изобретению относится к лекарственной системе направленного действия, в которой водородные связи в молекуле активного компонента служат мишенью для хеликазы. Лекарство для направленного действия может включать противоопухолевое средство, противовирусное средство, антибактериальное средство, противогрибковое средство и так далее.
Настоящее изобретение дополнительно предлагает способ получения вышеуказанного карбоплатинового комплекса, в частности, за счет оптимизации и целенаправленного контроля рабочих условий достигается самосборка карбоплатина и 1,1-циклобутандикарбоновой кислоты, при этом получают целевой продукт с как можно более высокими показателями чистоты или содержания, что соответствует вышеуказанным характеристикам.
Способ приготовления включает следующие рабочие процессы (условия самосборки):
смешивание карбоплатина и 1,1-циклобутандикарбоновой кислоты в молярном соотношении 1:(1,5-3) при 65°С±10°С в течение не менее 0,5 часов с получением пересыщенного водного раствора; и
сбор кристаллов карбоплатинового комплекса (т.е. самособирающегося продукта).
Вышеупомянутый перенасыщенный водный раствор относится к перенасыщенному водному раствору комплекса, образованного карбоплатином и 1,1-циклобутандикарбоновой кислотой. Как правило, сначала может быть приготовлен водный раствор карбоплатина определенной концентрации, а затем к водному раствору карбоплатина может быть добавлена 1,1-циклобутандикарбоновая кислота, где в указанных выше условиях самосборки концентрация каждого сырьевого материала максимально высока, насколько это возможно без осаждения кристаллов, и можно считать, что приготовленный раствор является перенасыщенным водным раствором.
Исследования автора настоящей заявки показали, что водный раствор смеси карбоплатина и 1,1-циклобутандикарбоновой кислоты также может естественным образом образовывать нестабильный комплекс, и различные количества комплекса также могут формироваться в различных условиях, даже физическая порошковая смесь карбоплатина и 1,1-циклобутандикарбоновой кислоты может давать молекулярную информацию о небольшом количестве комплекса. В этом случае способ получения, предусмотренный в настоящем изобретении, оптимизирует условия системы растворов, образованных карбоплатином и 1,1-циклобутандикарбоновой кислотой, так что получается система смешанных растворов, в которой имеется значительный избыток 1,1-циклобутандикарбоновой кислоты, и каждый из двух реакционных исходных материалов имеет максимально возможную концентрацию, позволяющую полученному комплексу находиться в перенасыщенном состоянии. Кроме того, поддержание соответствующей контролируемой температуры в течение определенного периода времени (обычно достаточно более 1 часа, например, ее можно поддерживать в течение 3 или 4 часов) благоприятно для образования упорядоченного и стабильного комплекса между молекулой карбоплатина и молекулой 1,1-циклобутандикарбоновой кислоты посредством нековалентных связей, то есть получают высокий выход карбоплатинового комплекса. В то же время свободный мономолекулярный карбоплатин и 1,1-циклобутандикарбоновая кислота рассматриваются как примеси и их уровни снижаются до крайне низких (следовых) количеств. Самособирающийся продукт находится в кристаллическом состоянии. Реакционную систему охлаждают до комнатной температуры или ниже для осаждения кристаллов, которые отделяют с получением продукта относительно высокой чистоты, представляющего собой почти бесцветные кристаллы. После разделения можно провести более одной перекристаллизации, чтобы улучшить чистоту продукта. Понятно, что использование сырья высокой чистоты также является эффективным средством для повышения чистоты и выхода продукта.
В описанном выше процессе сборки за счет оптимизации отношения смешивания (молярного отношения) карбоплатина и 1,1-циклобутандикарбоновой кислоты в водном растворе, а также таких факторов, как температура и время сборки, два компонента собираются в стабильный комплекс в водном растворе, а после разделения и очистки кристаллизацией образуется карбоплатиновый комплекс с высоким уровнем самосборки. В одном варианте осуществления настоящего изобретения, при необходимости, приготовленный перенасыщенный раствор может быть отфильтрован для сбора фильтрата, который помещают в темноту при комнатной температуре (обычно 20°С±5°С), обычно не менее чем на 7 дней, чтобы облегчить осаждение кристаллов комплекса, так что чистота и выход карбоплатинового комплекса дополнительно улучшаются.
Если не указано иное, выход карбоплатинового комплекса, содержание карбоплатинового комплекса в системе продуктов самосборки и уровень самосборки, упомянутые в настоящем изобретении, имеют одинаковое значение.
На основе процесса получения вышеуказанного карбоплатинового комплекса дополнительно получают фармацевтический препарат с карбоплатиновым комплексом в качестве активного компонента, где способ получения фармацевтического препарата включает:
приготовление кристаллов карбоплатинового комплекса в соответствии с ранее описанным способом, измельчение и сушку с получением порошка карбоплатинового комплекса; и
приготовление порошка карбоплатинового комплекса в виде препарата.
В частности, карбоплатиновый комплекс можно сначала приготовить в виде маточной жидкости, а затем в виде жидкости для инъекций или лиофилизированного порошка для инъекций и т.п. следующим образом:
растворение порошка карбоплатинового комплекса в стерилизованной воде, перемешивание и растворение при 45°С±5°С и выдерживание при комнатной температуре в течение 1 часа или более с получением маточной жидкости;
фильтрация и стерилизация маточной жидкости при комнатной температуре, а затем упаковка с получением жидкости для инъекций; или
приготовление из маточной жидкости лиофилизированного порошка для инъекций, твердого препарата для перорального применения, препарата в виде геля или препарата в виде спрея и т.д.
В настоящем изобретении 1,1-циклобутандикарбоновую кислоту используют в качестве вспомогательного вещества для нового препарата карбоплатина, тем самым превращая препарат порошка карбоплатинового комплекса в очень стабильную жидкость для инъекций, что аналогично технологии липосомной ловушки. Конкретный пример приготовления жидкости для инъекций может включать растворение 500 г порошка карбоплатинового комплекса в стерильной воде и нормирование стерильной водой до 500 литров; перемешивание и растворение до однородного состояния при 45°С±5°С, выдерживание при комнатной температуре не менее 1 часа для получения маточной жидкости для препарата, и проведение анализа содержания; когда показатели анализа содержания соответствуют стандарту, проводят фильтрацию приготовленной маточной жидкости и стерилизацию при комнатной температуре, а также упаковку для получения жидкости для инъекций с концентрацией 5 мг/5 мл и хранение при низкой температуре (4°C-10°C) в темноте.
В вариантах осуществления настоящего изобретения после получения ожидаемого карбоплатинового комплекса (который можно обозначить как карбоплатин 4.0) комплекс может быть приготовлен в виде соответствующих фармацевтических лекарственных форм на основе обычных методов в области фармацевтики. В дополнение к препарату для инъекций он также может иметь форму препарата для перорального применения или препарата для местного применения, такого как препарат в виде геля и препарат в виде спрея.
Другой аспект настоящего изобретения относится к способу контроля качества указанного выше карбоплатинового комплекса.
Исследования автора настоящего изобретения показывают, что, хотя анализ посредством хроматографии и масс-спектрометрии (ЖХ-МС) является предпочтительным методом определения содержания большинства синтетических продуктов, ввиду того, что две молекулы в карбоплатиновом комплексе связаны лишь водородными связями, хроматографическое разделение нарушает эти водородные связи, что может привести к искажению результатов испытаний из-за высвобождения карбоплатина и 1,1-циклобутандикарбоновой кислоты. Точная молекулярная масса карбоплатина 4.0 может быть получена в режиме определения отрицательных ионов с помощью прямого масс-спектрометрического анализа после дозирования образцов методом инжектирования в поток, но физическая смесь карбоплатина и 1,1-циклобутандикарбоновой кислоты (далее именуемая двухкомпонентной физической смесью) также может давать те же самые ионы в аналогичном режиме; следовательно, даже если молекулярная масса и может быть измерена точно, ее нельзя использовать в качестве основного метода определения содержания карбоплатина 4,0.
Анализ методом капиллярного электрофореза показывает, что карбоплатин 4.0, карбоплатин, 1,1-циклобутандикарбоновая кислота и другие образцы можно идентифицировать тремя способами, которые представляют собой капиллярно-зональный электрофорез в водной среде (CZE), капиллярно-зональный электрофорез в неводной среде (NACZE) и мицеллярную электрокинетическую капиллярную хроматографию (МЭКХ). При указанных выше различных оптимизированных условиях идентификации ни один из приведенных выше образцов не демонстрирует феномена разделения, и времена появления пиков карбоплатина 4.0 и карбоплатина совпадают. В сочетании с результатами анализа 1H-ЯМР и ЖХ-МС дополнительно продемонстрировано, что карбоплатин 4.0 диссоциирует на карбоплатин и 1,1-циклобутандикарбоновую кислоту под действием энергии электрического поля из-за наличия внутримолекулярных водородных связей, которые относительно слабее ковалентных связей.
Кроме того, нет очевидной разницы между карбоплатином 4.0 (или его лиофилизированным порошком, образовавшимся после растворения в воде и последующей лиофилизации) и вышеуказанной двухкомпонентной физической смесью и в инфракрасных спектрах, и анализ инфракрасного спектра также не подходит для количественного и качественного анализа карбоплатина 4.0.
С другой стороны, когда используют анализ с помощью рентгеновской порошковой дифрактометрии (XRPD), наблюдаются очевидные различия в характеристиках дифракционных пиков между вышеуказанным карбоплатиновым комплексом с водородной связью и карбоплатином в диаграмме XRPD. Другими словами, характеристический пик карбоплатина появляется около угла дифракции 11,55±0,2°, в то время как карбоплатин 4.0 почти не имеет дифракционного пика в этом положении, а его основные характеристические пики появляются в положениях, где угол 2θ составляет 7,55°; 10,51°; 14,63°; 15,10°; 15,66°; 16,78°; 18,55°; 20,83°; 22,86°; 23,67°; 24,02° и т.д. (все отклонения могут быть в пределах ±0,2°). Безусловно, дополнительная детекция пиков поглощения карбоплатина и 1,1-циклобутандикарбоновой кислоты с помощью хроматографии и масс-спектрометрии также является необходимым этапом контроля качества продукта.
Согласно результатам исследований по настоящему изобретению, хотя содержание карбоплатина 4.0 не может быть напрямую установлено с помощью некоторых из существующих аналитических методов, содержание карбоплатина 4.0 может быть определено косвенно путем измерения содержания карбоплатина и 1,1-циклобутандикарбоновой кислоты. Таким образом, для карбоплатина 4.0 могут быть установлены следующие методы контроля качества: (1) на основе различий между характеристическими дифракционными пиками карбоплатина 4.0, карбоплатина и 1,1-циклобутандикарбоновой кислоты метод XRPD используется для контроля предельного содержания свободного карбоплатина в карбоплатине 4,0; (2) поскольку карбоплатин 4.0 образован одной молекулой карбоплатина и одной молекулой 1,1-циклобутандикарбоновой кислоты посредством водородных связей и легко диссоциирует в условиях полярного растворителя с образованием карбоплатина и 1,1-циклобутандикарбоновой кислоты, молярное отношение карбоплатина и 1,1-циклобутандикарбоновой кислоты и содержание обоих из них может быть определено с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) и включено в стандарт контроля качества для карбоплатина 4.0.
Соответственно, настоящее изобретение предлагает способ контроля качества карбоплатинового комплекса, включающий исследование испытуемого образца с помощью рентгеновской порошковой дифрактометрии и определение того, что испытуемый образец не имеет дифракционного пика при 2θ приблизительно 11,55±0,2°; испытуемый образец в таком случае может включать указанный выше карбоплатиновый комплекс, или указанный выше фармацевтический препарат, содержащий карбоплатиновый комплекс в качестве активного компонента.
Понятно, что способ контроля качества по настоящему изобретению нацелен на карбоплатиновый комплекс (карбоплатин 4.0), и этот способ также можно использовать для контроля качества чистоты нерасфасованного лекарственного средства из карбоплатина 4.0. Как правило, содержание свободного карбоплатина в нерасфасованном препарате должно быть не более 2%, а в более предпочтительных случаях может быть не более 1%.
Согласно результатам анализа карбоплатина 4.0 посредством XRPD, карбоплатин 4.0 не имеет характеристического пика при 2θ примерно 11,55±0,2º и имеет дифракционные пики в положениях, где 2θ составляет примерно 7,55°; 10,51°; 14,63°; 15,10°; 15,66°; 16,78°; 18,55°; 20,83°; 22,86°; 23,67°; 24,02° и т.д. (все их отклонения могут быть в пределах ±0,2°), где дифракционный пик при 2θ около 15,10±0,2º можно рассматривать как полуколичественный характеристический пик карбоплатина 4,0. Исходя из этого, относительная интегральная площадь характеристического пика при 2θ примерно 15,10±0,2° и характеристический пик карбоплатина (дифракционный пик при 2θ примерно 11,55±0,2°) могут быть использованы в качестве количественных стандартов для получения анализа предельного содержания свободного карбоплатина.
В частности, в результатах измерения XRPD испытуемого образца, который представляет собой карбоплатин 4.0, если обнаруживается дифракционный пик при 2θ примерно 11,55±0,2°, интегральная площадь дифракционного пика при 2θ примерно 11,55±0,2° будет зарегистрирована как A1, а интегральная площадь дифракционного пика при 2θ примерно 15,10±0,2º будет зарегистрирована как A2, так что содержание свободного карбоплатина в карбоплатине 4.0 может быть определено значением A1/A2. Например, в одном варианте осуществления настоящего изобретения для достижения эффективного контроля содержания свободного карбоплатина в нерасфасованном лекарственном средстве карбоплатина 4.0 (испытуемом образце карбоплатина 4.0) на основании результатов измерения XRPD испытуемого образца карбоплатина 4.0 значение A1/A2 не должно быть больше соответствующего отношения интегральной площади смешанного образца (или смешанного эталона), приготовленного из карбоплатина 4,0 и карбоплатина, с учетом x% карбоплатина 4,0 по массе, чтобы гарантировать, что содержание свободного карбоплатина не превышает x%. В одном конкретном варианте осуществления x% может составлять, например, 1%, 0,5%, 0,1% и т.д. Карбоплатин 4.0, использованный для приготовления вышеупомянутого смешанного образца, практически не имеет дифракционного пика, выявляемого при 2θ примерно 11,55±0,2°, и поэтому его в целом можно считать чистым карбоплатином 4.0.
В одном конкретном варианте осуществления настоящего изобретения готовят смешанный образец карбоплатина 4.0 и карбоплатина, где карбоплатин составляет 1% по массе карбоплатина 4.0 (т.е. x%=1%); смешанный эталон и нерасфасованное лекарственное средство карбоплатин 4.0 анализируют с помощью XRPD, где значение A1/A2, измеренное для вышеупомянутого смешанного эталона, составляет примерно 0,67, поэтому значение A1/A2, измеренное для нерасфасованного лекарственного средства карбоплатина 4.0, не должно превышать 0,67, что гарантирует, что содержание свободного карбоплатина в нерасфасованном препарате не превышает 1%. В другом варианте осуществления указанное выше значение x% может составлять конкретно 0,5%, где значение A1/A2, измеренное для смешанного эталона, составляет примерно 0,55, поэтому значение A1/A2, измеренное для нерасфасованного лекарственного средства карбоплатина 4,0, не должно превышать 0,55, что гарантирует, что содержание свободного карбоплатина в нерасфасованном препарате не превышает 0,5%. В еще одном варианте осуществления указанная выше величина x% может составлять конкретно 0,1%, где значение A1/A2, измеренное для смешанного эталона, составляет примерно 0,5, поэтому значение A1/A2, измеренное для нерасфасованного лекарственного средства карбоплатина 4,0, не должно превышать 0,5, что гарантирует, что содержание свободного карбоплатина в нерасфасованном лекарственном средстве не превышает 0,1%.
В качестве альтернативы, в другом варианте осуществления может быть предусмотрен другой метод испытаний на предельное содержание: интенсивность (или интегральная площадь) дифракционного пика нерасфасованного лекарственного средства карбоплатина 4,0 при 2θ 11,55±0,2º не должна превышать интенсивность (или интегральную площадь) дифракционного пика смешанного образца при том же значении 2θ, где смешанный образец приготовлен из карбоплатина 4,0 и карбоплатина с учетом x% по массе карбоплатина; где, как описано выше, x% может составлять, например, 1%, 0,5%, 0,1% и т.д.
Способ контроля качества, предусмотренный настоящим изобретением, дополнительно включает исследование испытуемого образца карбоплатина 4.0 методом ВЭЖХ и определение того, что содержание карбоплатина и 1,1-циклобутандикарбоновой кислоты в испытуемом образце составляет 97%-103% для каждого из них, а молярное отношение карбоплатина и 1,1-циклобутандикарбоновой кислоты составляет 0,95-1,05. Иными словами, согласно способу контроля качества по настоящему изобретению, кроме определения характеристик дифракционных пиков методом XRPD, требуется проводить исследование методом ВЭЖХ в отношении карбоплатина и 1,1-циклобутандикарбоновой кислоты, которые высвобождаются после разрыва водородной связи. Результаты детектирования должны составлять 97%-103% от их собственных теоретических количеств в комбинированном состоянии, соответственно, и карбоплатин и 1,1-циклобутандикарбоновая кислота обычно присутствуют в молярном отношении 1:1, а контрольный стандарт должен быть в пределах ±0,05 (т.е. молярное отношение этих двух компонентов составляет примерно 0,95-1,05).
Исследования автора настоящего изобретения позволили установить, что при анализе методом ВЭЖХ концентрация карбоплатина показывает хорошую линейную зависимость и интегральное значение площади хроматографического пика карбоплатина в диапазоне 0,025-0,999 мг/мл, где уравнение линейной регрессии представляет собой Y=40169+8,62E6X, а коэффициент корреляции r=0,999; концентрация 1,1-циклобутандикарбоновой кислоты показывает хорошую линейную связь с интегральным значением площади хроматографического пика 1,1-циклобутандикарбоновой кислоты в диапазоне 0,101-3,99 ммоль/л, где уравнение линейной регрессии представляет собой Y=7407+962202X, а коэффициент корреляции r=0,999. Исходя из этого, в одном варианте осуществления настоящего изобретения ВЭЖХ детекция может быть выполнена на испытуемом образце карбоплатина 4.0 и смешанном эталонном образце карбоплатина и 1,1-циклобутандикарбоновой кислоты; по результатам измерений определяют содержание и соотношение молярных концентраций (молярное соотношение) карбоплатина и 1,1-циклобутандикарбоновой кислоты в испытуемом образце карбоплатина 4,0 по площади пика в сравнении с внешним стандартом.
В одном варианте осуществления настоящего изобретения при определении содержания/молярного отношения испытуемый образец карбоплатина 4.0 готовят с подвижной фазой для испытания в растворе испытуемого образца с концентрацией карбоплатина 4,0 примерно 1,0 мг/мл (в расчете на теоретическое количество), а эталонное вещество карбоплатин и эталонное вещество 1,1-циклобутандикарбоновую кислоту используют для приготовления смешанного эталонного аналитического раствора, где концентрации обоих веществ составляют примерно 0,7 мг/мл и 0,3 мг/мл, соответственно, для ВЭЖХ детекции.
Настоящее изобретение не только обеспечивает карбоплатиновый комплекс (карбоплатин 4.0), образованный специфической водородной связи, но также обеспечивает фармацевтический препарат, изготовленный на основе этого карбоплатинового комплекса, и, в частности, обеспечивает лекарство направленного действия, которое служит мишенью для хеликазы, и которое, как ожидается, станет усовершенствованной версией лекарственного средства карбоплатина. Настоящее изобретение дополнительно обеспечивает возможный способ контроля качества приготовленного карбоплатина 4.0 в виде нерасфасованного лекарственного средства, и исследует активность и фармакокинетику карбоплатина 4.0 с использованием карбоплатина в качестве контроля.
Согласно результатам исследования настоящего изобретения, поскольку карбоплатин 4.0 диссоциирует с высвобождением карбоплатина, можно вполне обоснованно ожидать, что его клинические показания включают все показания для лекарственного средства карбоплатина в нерасфасованном виде. В настоящее время карбоплатин в основном используется клинически для лечения мелкоклеточного рака легкого, рака яичников, рака яичка, герминогенной опухоли, рака щитовидной железы и рака носоглотки, а также может быть использован для таких лечения злокачественных опухолей, как рак шейки матки, немелкоклеточный рак легкого, рак пищевода, семинома, рак мочевого пузыря, мезотелиома, педиатрическая опухоль головного мозга и другие виды рака головы и шеи. Пациенты, которые не переносят цисплатин из-за почечной недостаточности, рефрактерной рвоты, потери слуха или нейротоксичности, с большей вероятностью выберут карбоплатин 4.0 в качестве улучшенного препарата. Показания, скорее всего, будут расширены на опухоли головного мозга или метастазы в головной мозг, опухоли костей или метастазы в кости, рак предстательной железы, рак поджелудочной железы, рак желчных протоков и т.д., другими словами, имеет место более широкий спектр показаний. В то же время карбоплатин 4.0 также подходит для лечения других резистентных к платине пациентов и в сочетании с таргетной лекарственной терапией; он не имеет клинической перекрестной резистентности с другими химиотерапевтическими препаратами и может применяться индивидуально или в комбинации с другими химиотерапевтическими препаратами, а также может применяться в сочетании с хирургическим вмешательством и лучевой терапией для улучшения терапевтического эффекта.
В одном конкретном варианте осуществления карбоплатин 4.0 используют для изучения химиочувствительности восьми видов устойчивых к оксалиплатину или иринотекану раковых клеток толстой кишки и их первичных клеток. Результаты показывают, что карбоплатин 4.0 не вызывает реакции перекрестной резистентности с оксалиплатином и иринотеканом, и, таким образом, карбоплатин 4.0 можно рассматривать как еще один вариант химиотерапии для пациентов с клинически резистентным раком толстой кишки.
С другой стороны, поскольку атом платины карбоплатина заблокирован другой молекулой, 1,1-циклобутандикарбоновой кислотой, это будет препятствовать связыванию атома платины с ДНК, что значительно снижает токсическую активность карбоплатина 4.0 по отношению к ДНК.
В соответствии с исследованиями автора настоящего изобретения, каждый из карбоплатина 4.0 и карбоплатина подвергали анализу связывания с линейной ДНК, и результаты показывают, что в определенный период времени карбоплатин быстро образует поперечно-сшитый аддукт с ДНК, и линейная ДНК деформируется, сжимается и уплотняется; но реакции сшивки между карбоплатином 4.0 и линейной ДНК не происходит, и форма линейной ДНК в основном не изменяется. Кроме того, каждый из карбоплатина 4.0 и карбоплатина смешивали с суперспиральной плазмидной ДНК, и через некоторое время результаты электрофореза показали, что карбоплатин сшивается с суперспиральной плазмидной ДНК с образованием аддукта, в то время как карбоплатин 4.0 не образует сшивки с суперспиральной плазмидной ДНК, и скорость ее движения согласуется с суперспиральной плазмидной ДНК контрольной группы без добавления какого-либо платинового препарата. Приведенные выше результаты исследований показывают, что в структуре карбоплатина 4.0 атом платины карбоплатина заблокирован и закрыт другой молекулой 1,1-циклобутандикарбоновой кислоты, и именно такая блокировка и закрытие препятствует связыванию атома платины с ДНК, что значительно снижает токсическую активность карбоплатина 4.0 по отношению к ДНК.
Результаты фармакокинетического исследования показывают, что по сравнению с карбоплатином период полувыведения (t1/2) при клиренсе лекарственного средства карбоплатина 4.0 значительно сокращен. Поскольку карбоплатин 4.0 обладает лучшей растворимостью и неполярностью, чем карбоплатин, он имеет короткий период полувыведения из органов организма, более высокую скорость клиренса и значительно сниженные токсические и побочные эффекты, особенно частоту нефротоксичности. Абсолютная биодоступность карбоплатина 4.0 и карбоплатина, в основном, одинакова, однако по сравнению с карбоплатином карбоплатин 4.0 имеет преимущества низкого связывания с белками плазмы, быстрого трансмембранного транспорта, отсутствия повреждения нереплицирующихся клеток и т.д., и таким образом, также проявляет более высокую биодоступность. Кроме того, с точки зрения кажущегося объема распределения (Vd), по сравнению с карбоплатином, карбоплатин 4.0 более широко распределяется, особенно в тканях и органах с барьерами, такими как ткань головного мозга, костный мозг и предстательная железа, что указывает на то, что карбоплатин 4.0 обладает более широкими клиническими показаниями.
Исследования в настоящем изобретении также показывают, что в дополнение к тому, что карбоплатин 4.0 превосходит карбоплатин по противоопухолевым свойствам, ожидается, что карбоплатин 4.0 станет усовершенствованным противоопухолевым препаратом карбоплатина. Карбоплатин 4.0 также обладает отличными противовирусными, противогрибковыми и антибактериальными свойствами, поэтому он указывает на более широкий спектр показаний, включая очевидное ингибирующее действие на вирус пузырчатки полости рта и конечностей (вирус EV71), вирус гриппа (H3N2), вирус HSV-1, вирус Эпштейна-Барр, вирус ВПЧ, бактериофаги, индикаторные бактерии, Candida albicans и др.
Кроме того, авторы настоящего изобретения оценили применение карбоплатина 4.0 и карбоплатина в противовирусном аспекте посредством данных, полученных в экспериментах по цитотоксичности; и результаты показывают, что цитотоксичность карбоплатина препятствует его применению в противовирусном аспекте. Карбоплатин 4.0 прошел оценку влияния лекарственной эффективности, лекарственной токсичности, лекарственной устойчивости и влияния лекарств на апоптоз и пролиферацию клеток в испытании на цитотоксичность.
Другой аспект настоящего изобретения дополнительно относится к способу лечения злокачественного опухолевого заболевания, включающему введение пациенту лекарственного средства, содержащего указанный выше карбоплатиновый комплекс в качестве активного компонента, или введение указанного выше фармацевтического препарата.
Другой аспект настоящего изобретения дополнительно относится к способу лечения бактериальной или грибковой инфекции, включающему введение пациенту лекарственного средства, содержащего указанный выше карбоплатиновый комплекс в качестве активного компонента, или введение указанного выше фармацевтического препарата.
Другой аспект настоящего изобретения дополнительно относится к способу лечения вирусной инфекции, включающему введение пациенту лекарственного средства, содержащего указанный выше карбоплатиновый комплекс в качестве активного компонента, или введение указанного выше фармацевтического препарата.
Карбоплатиновый комплекс по настоящему изобретению образован путем объединения карбоплатина и 1,1-циклобутандикарбоновой кислоты через две водородные связи, где межмолекулярные водородные связи улучшают растворимость в воде, стабильность, биодоступность и другие функции карбоплатина, и, в сравнении с карбоплатином, карбоплатиновый комплекс имеет значительно более низкие токсические и побочные эффекты и чрезвычайно низкую лекарственную устойчивость/перекрестную устойчивость, а также имеет более широкий спектр показаний в противоопухолевых, противовирусных, противогрибковых и антибактериальных аспектах.
Краткое описание чертежей
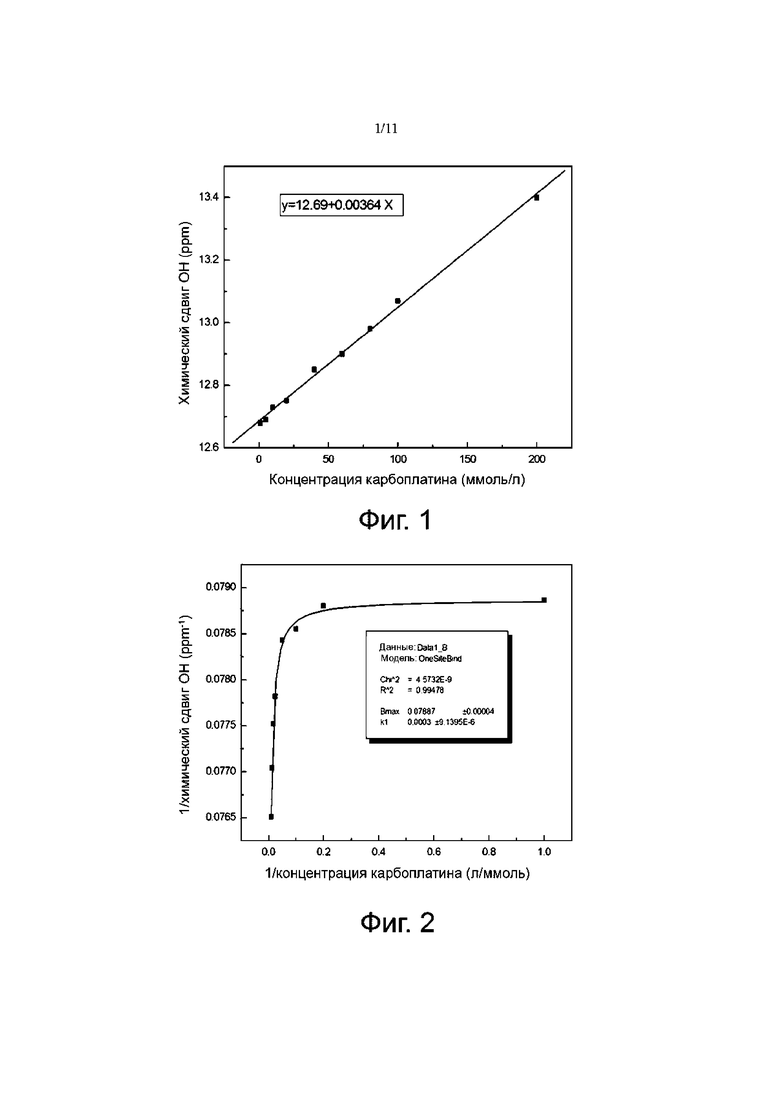
Фиг. 1 представляет собой диаграмму, показывающую изменение химического сдвига карбоксильного водорода (ОН) с увеличением концентрации карбоплатина.
Фиг. 2 представляет собой нелинейную аппроксимирующую диаграмму обратной величины химического сдвига карбоксильного водорода (1/Химический сдвиг) и обратной величины молярной концентрации карбоплатина (1/С карбоплатина).
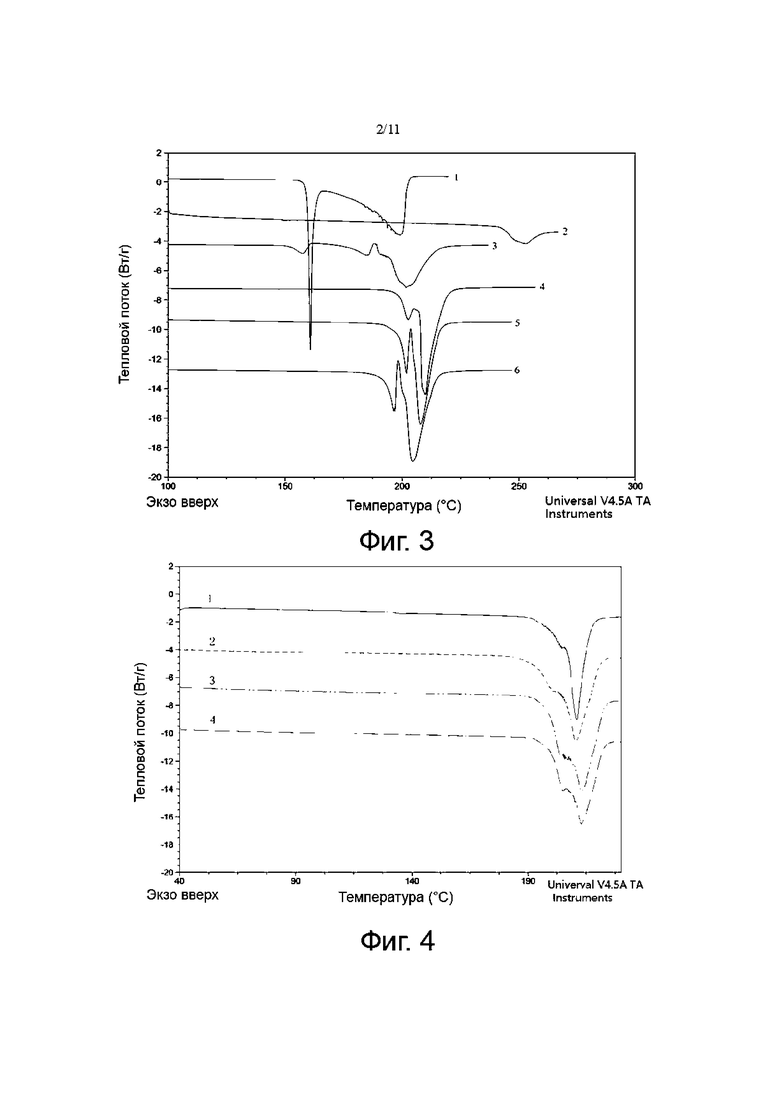
Фиг. 3 представляет собой диаграмму измерения ДСК 1,1-циклобутандикарбоновой кислоты, карбоплатина, смешанного порошка «с», лиофилизированного порошка «b», нерасфасованного лекарственного средства карбоплатина 4,0 и лиофилизированного порошка «а».
Фиг. 4 представляет собой диаграмму измерения ДСК четырех серий нерасфасованного лекарственного средства карбоплатина 4.0.
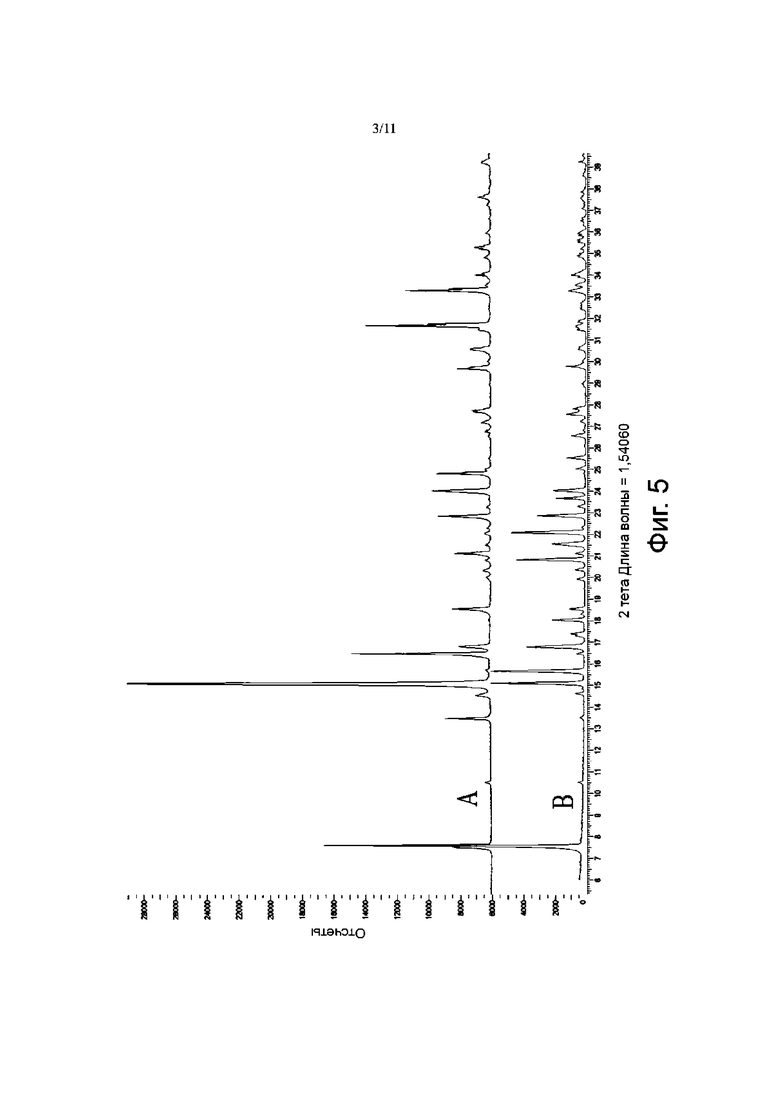
Фиг. 5 представляет собой диаграмму XRPD нерасфасованного лекарственного средства карбоплатина 4.0, где A представляет собой диаграмму XRPD, измеренную методом отражения, а B представляет собой диаграмму XRPD, измеренную методом пропускания.
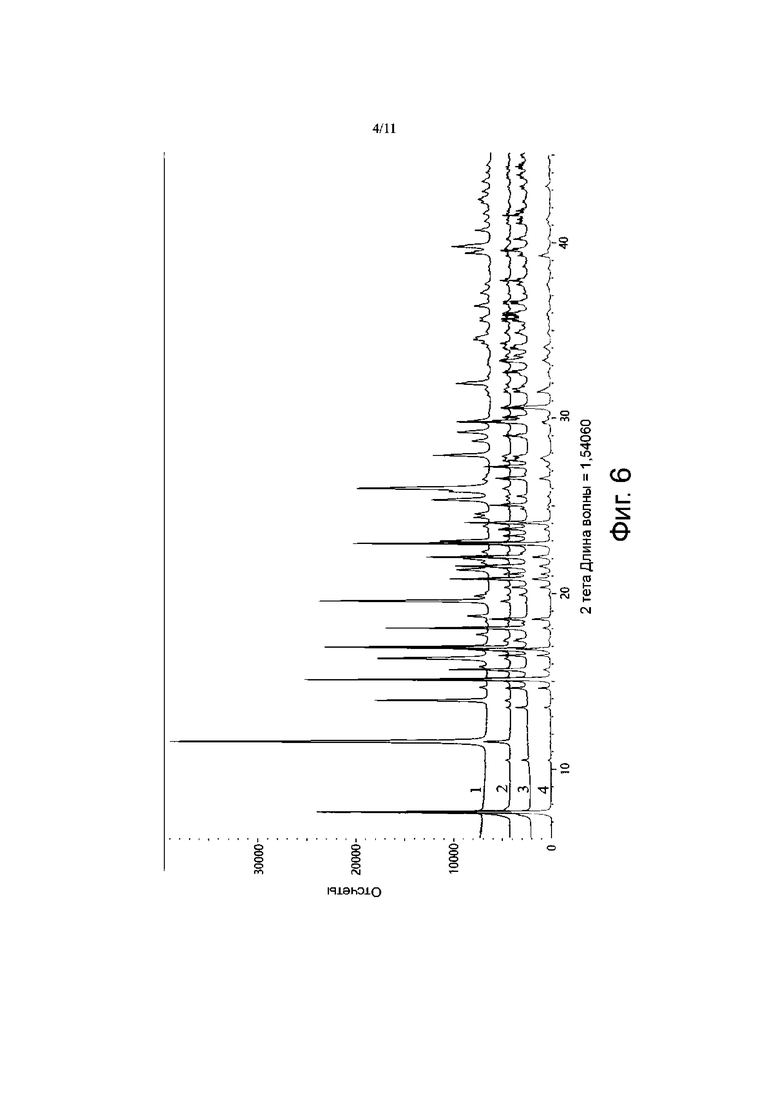
Фиг. 6 представляет собой диаграмму XRPD смешанного порошка «с», лиофилизированного порошка «b», нерасфасованного лекарственного средства карбоплатина 4.0 и лиофилизированного порошка «а».
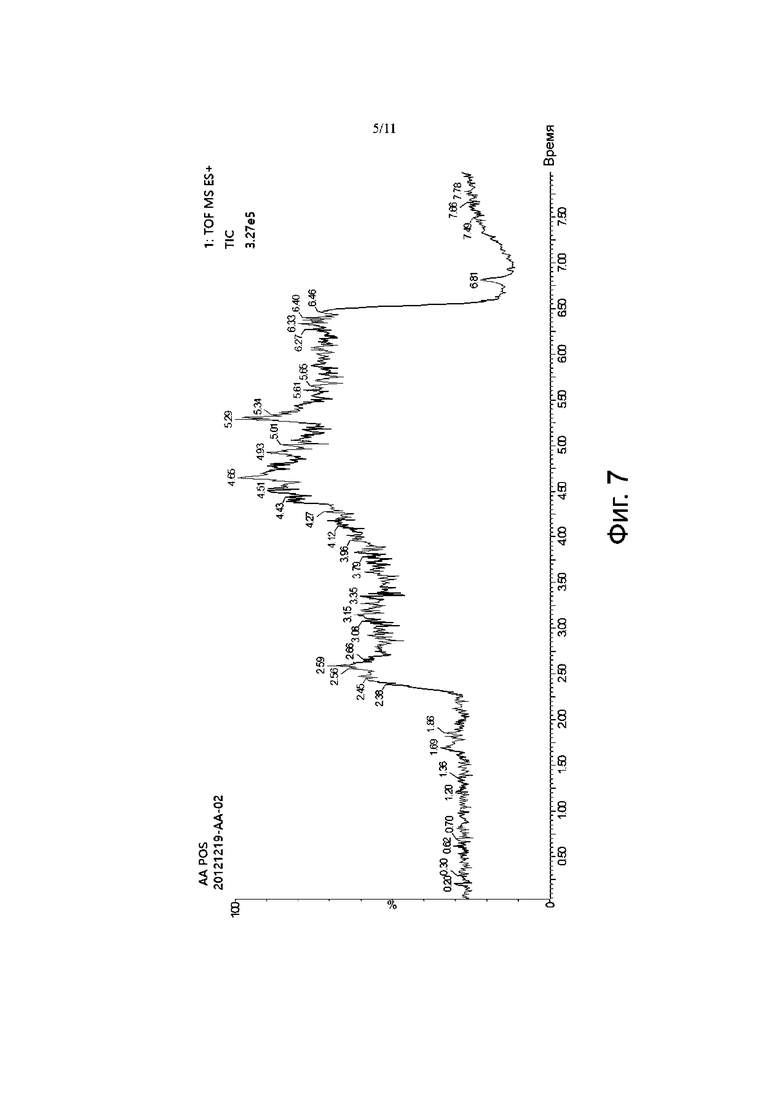
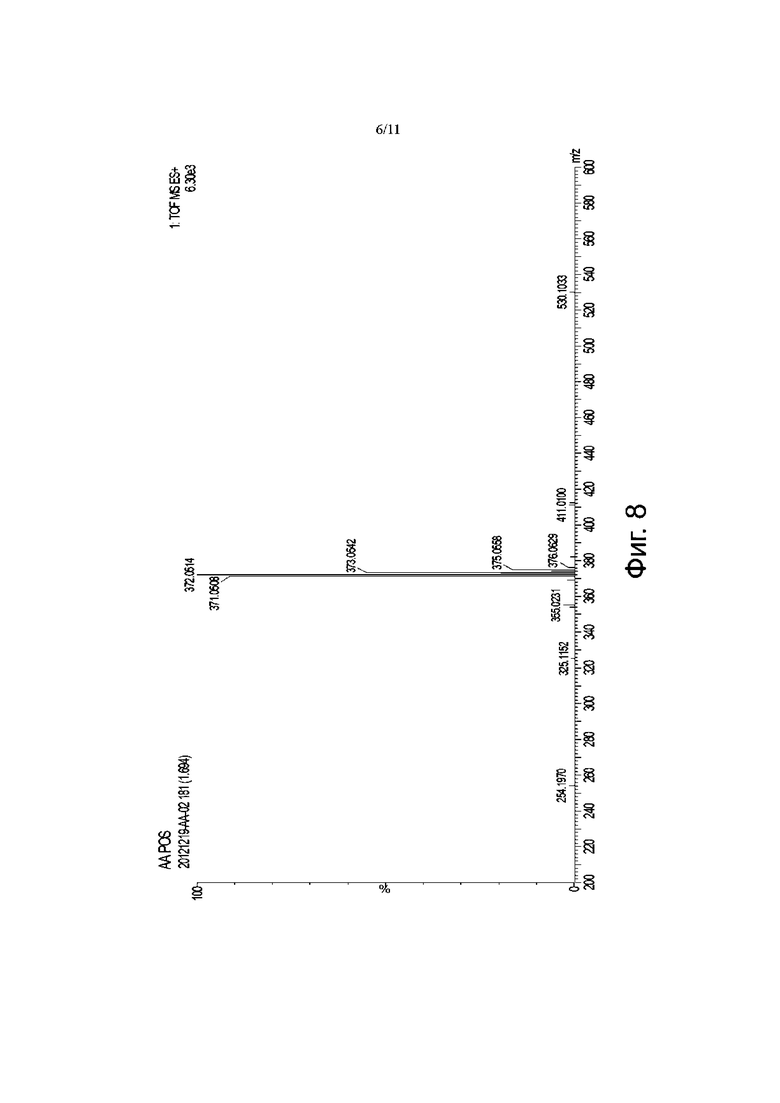
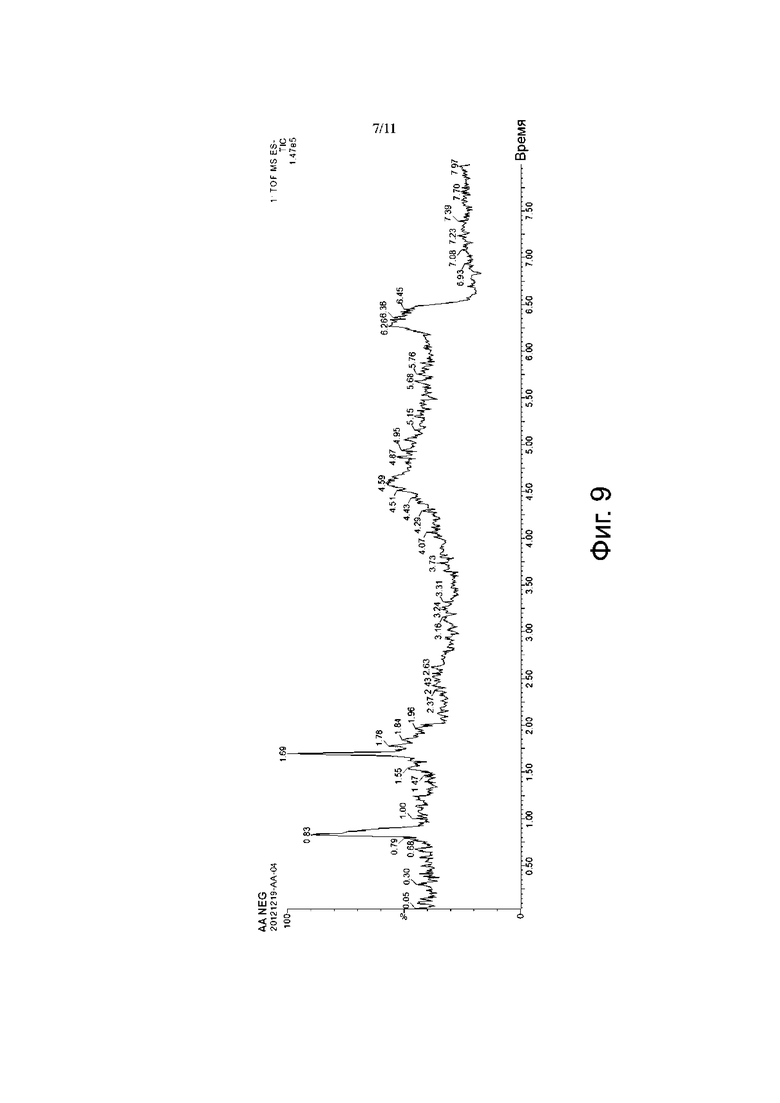
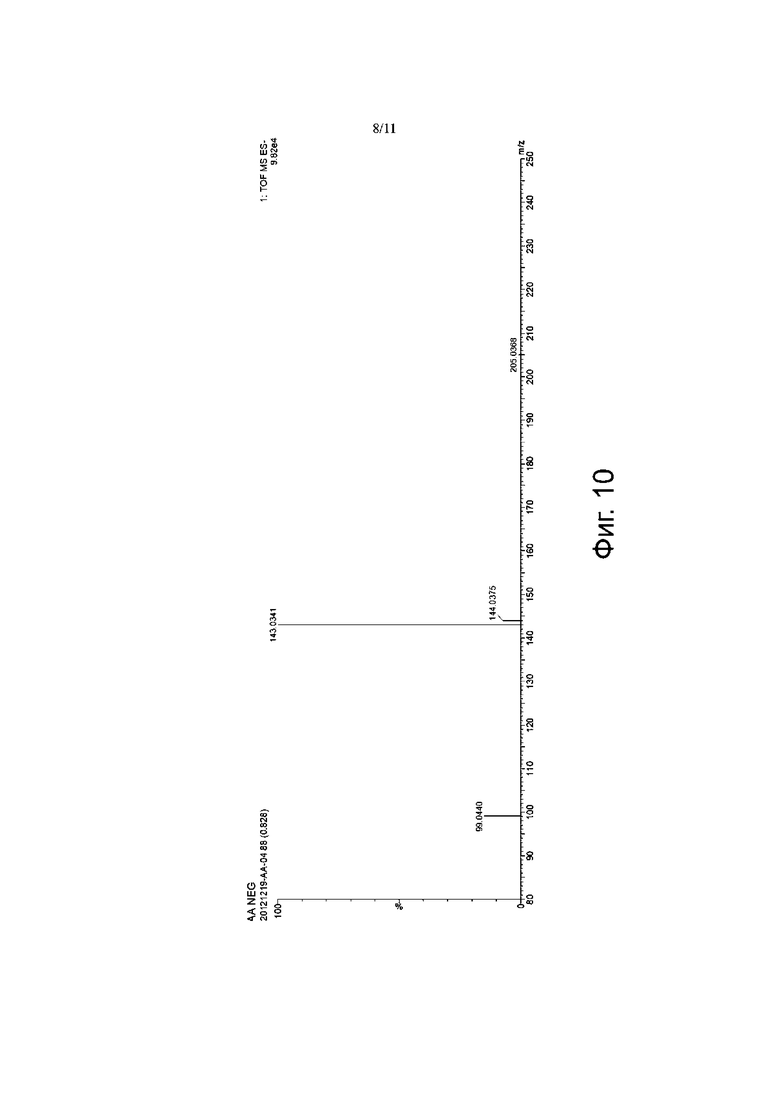
Фиг. 7-10 представляют собой спектрограммы анализа ЖХ-МС для карбоплатина 4.0, где Фиг. 7 и Фиг. 8 представляют собой хроматограмму и масс-спектрограмму полных ионных токов карбоплатина в режиме определения положительных ионов, соответственно (время удерживания RT = 0,83 мин); Фиг. 9 и Фиг. 10 представляют собой хроматограмму и масс-спектрограмму полных ионных токов 1,1-циклобутандикарбоновой кислоты в режиме определения отрицательных ионов, соответственно (время удерживания RT =1,7 мин).
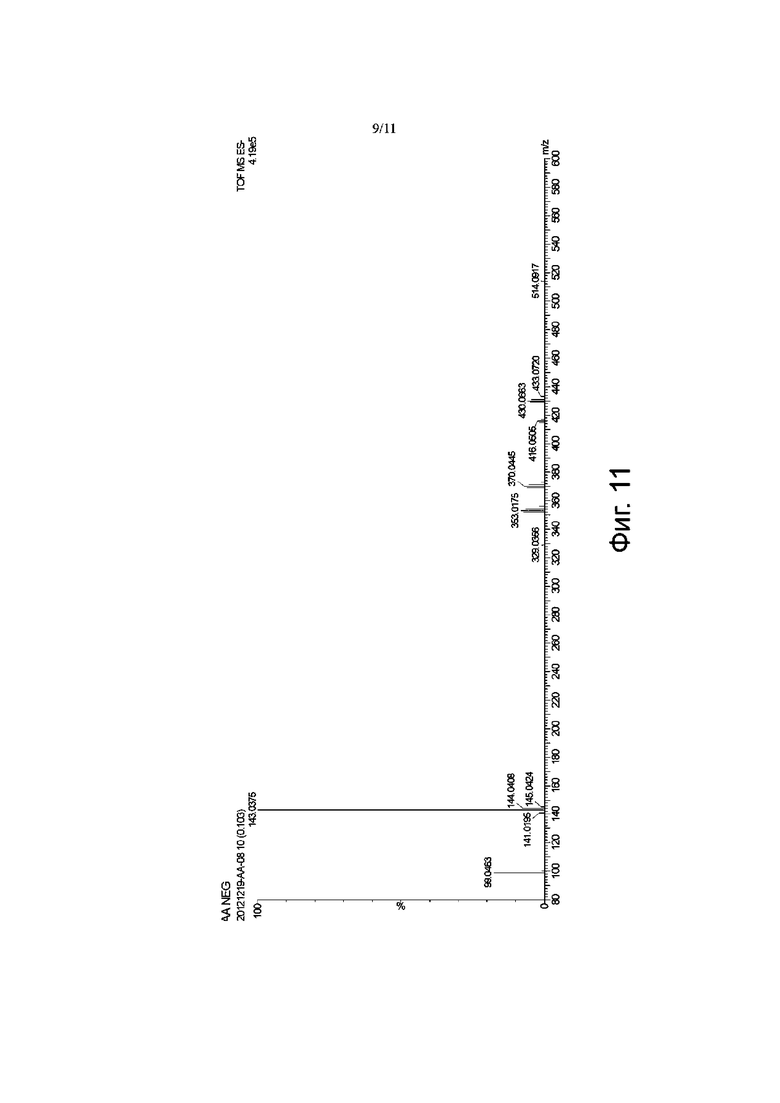
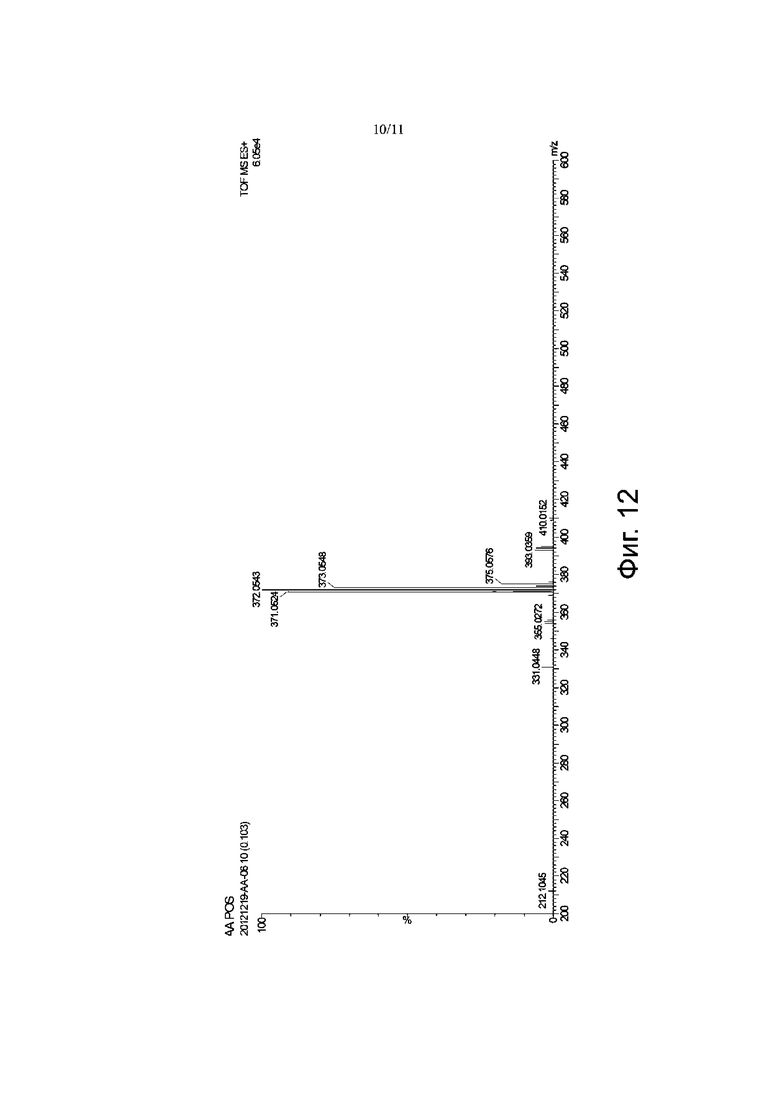
Фиг. 11 и Фиг. 12 представляют собой спектрограммы карбоплатина 4.0, полученные методом проточно-инжекционной масс-спектрометрии, где Фиг. 11 представляет собой масс-спектрограмму образца карбоплатина 4.0 в режиме определения отрицательных ионов, а Фиг. 12 представляет собой масс-спектрограмму образца карбоплатина 4.0 в режиме определения положительных ионов.
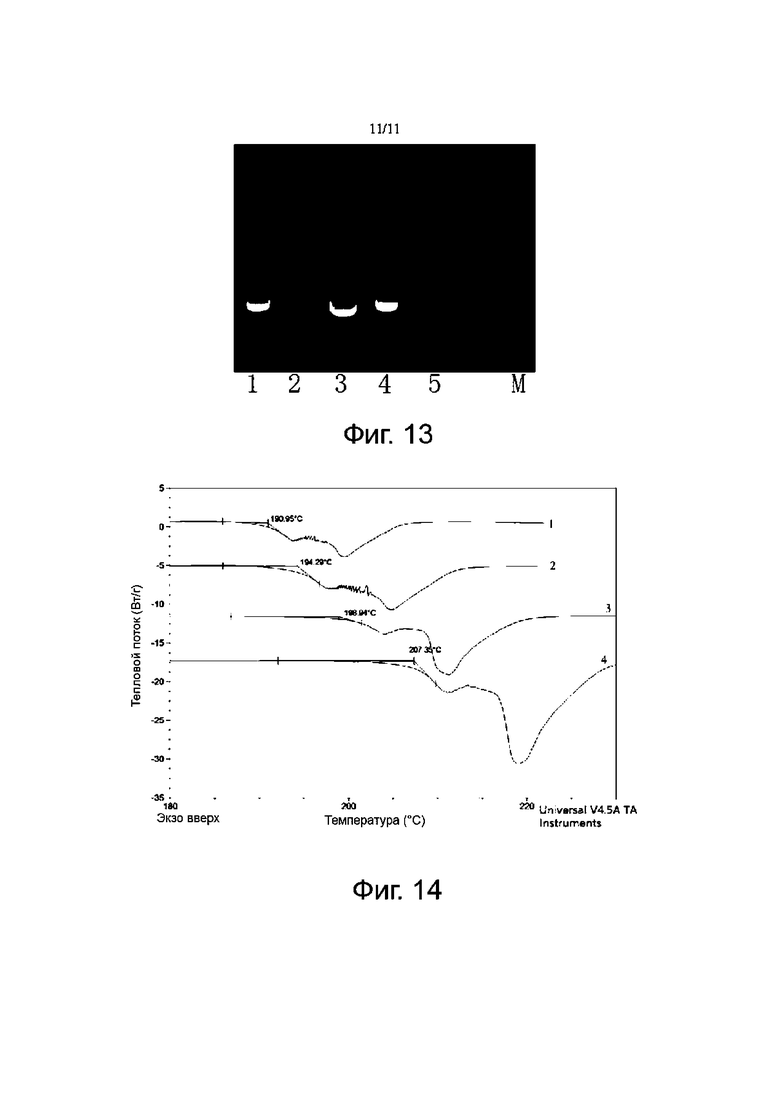
Фиг. 13 представляет собой электрофореграмму экспериментов по связыванию ДНК для карбоплатина 4.0 и карбоплатина с участием хеликазы.
Фиг. 14 представляет собой диаграмму измерения ДСК нерасфасованного лекарственного средства карбоплатина 4.0 при различных условиях скорости нагревания.
Описание вариантов осуществления изобретения
В сочетании с примерами содержание настоящего изобретения будет описано ниже более подробно. Следует понимать, что осуществление настоящего изобретения не ограничивается следующими примерами, и любые модификации и/или изменения формы настоящего изобретения будут подпадать под объем охраны настоящего изобретения.
В следующих примерах, если не указано иное, во всех задействованных процессах (таких как регуляция температуры, повышение температуры, измерение, сбор, приготовление жидкости для детектирования с целью тестирования, процесс детектирования и т.д.) можно использовать обычные средства обработки, известные в данной области техники, например, использование обычных инструментов, методов и т.д. для соответствующего лечения.
В следующих примерах используемые инструменты и соответствующие условия испытаний являются такими, как описано далее:
1) Метод титрования с использованием ядерного магнитного резонанса (1H-ЯМР).
Спектрометр ядерного магнитного резонанса с преобразованием Фурье типа JEOL ECA-400, оснащенный селективным импульсным ламинальным генератором сигналов и 5-мм многоядерными зондами с градиентными импульсами по оси z. Рабочая частота 1Н составляла 400 МГц, в качестве растворителя использовали ДМСО-d6, в качестве внутреннего стандарта - ТМС, температура эксперимента - комнатная, использовали многоядерные зонды Ф5 мм. Ширина спектра 1H-ЯМР составляет 9,18 кГц, точка данных 32768, ширина импульса 90° составляет 11 мкс, а задержка релаксации составляет 1,2 с.
2) Дифференциальная сканирующая калориметрия (ДСК). Аналитический прибор представляет собой American TA Q2000, где алюминиевая пластина представляет собой эталонную пластину, а пластина для образцов представляет собой алюминиевую пластину; и скорость нагревания составляет 10º/мин, и диапазон нагревания - 40ºC-240ºC.
3) Порошковая рентгеновская дифракция (XRPD).
Порошковый рентгеновский дифрактометр (Bruker D8-advance, оснащенный вращающимся предметным столиком для образцов на отражение-пропускание);
Пропускание: CuKα-излучение, фокусирующий монохроматор, с фокусировкой оптического пути зеркалом Гёбеля, напряжение трубки: 40 кВ и ток трубки: 40 мА;
Режим сканирования: θ/2θ сканирование; щель расходимости DS: 1,2 мм, щель Соллера: 2,5 мм;
Диапазон сканирования 2θ: 6-50°; скорость сканирования: 0,4 с/шаг; размер шага: 0,015º/шаг.
4) Жидкостная хроматография-масс-спектрометрия (ЖХ-МС).
Прибор: Shimadzu LCMS-8040
Капиллярное напряжение: 3 кВ (или -2,6 кВ).
Напряжение экстрактора: 4 В (или -4 В);
Напряжение конуса образца: 15 В (или -20 В);
Температура источника: 300°C;
Диапазон сканирования: 80-1000 атомных единиц массы;
Хроматографическая колонка: XDB-C18, 4,6×50 мм, 1,8 мкм;
Подвижная фаза А: 0,1% водный раствор муравьиной кислоты;
Подвижная фаза B: метанол;
Градиент: 0 мин, 99% А и 1% В; 1 мин, 99% А и 1% В; 3,5 мин, 40% А и 60% В; 5,5 мин, 40% А и 60% В;
Скорость потока: 0,5 мл/мин;
Объем введения: 2 мкл.
В следующих примерах карбоплатин получали от Qilu Pharmaceutical Co., Ltd., а 1,1-циклобутандикарбоновая кислота является продуктом компании MERCK в Германии.
Пример 1. Процесс самосборки карбоплатина 4.0 и получение из него жидкости для инъекций
1. Процесс самосборки карбоплатина 4.0.
1) карбоплатин и 1,1-циклобутандикарбоновую кислоту с соответствующей чистотой не менее 99% смешивали в молярном отношении 1:2 с получением перенасыщенного водного раствора (концентрация каждого компонента была как можно более высокой, и поддерживались условия без кристаллизации); причем такую операцию смешивания и приготовления осуществляли при 65°C±5°C в течение примерно 4 часов для завершения реакции самосборки;
2) реакционную систему фильтровали, фильтрат выдерживали при комнатной температуре (20±5°С) в течение 10 дней в темноте, при этом можно было наблюдать образование кристаллов;
3) раствор извлекали и собирали кристаллы комплекса, который был продуктом кристаллизации карбоплатина 4.0; чистоту продукта устанавливали путем XRPD анализа, при этом содержание карбоплатина 4.0 в продукте составляло до 99% или более.
2. Приготовление жидкого препарата карбоплатина 4.0 для инъекций:
1) Соответствующее количество указанного выше кристаллического продукта карбоплатина 4.0 (или измененного состава) измельчали в порошок с последующей вакуумной сушкой и удалением кристаллизационной воды, и получали порошок карбоплатина 4.0;
2) 500 г вышеуказанного порошка карбоплатина 4.0 растворяли в стерилизованной воде и доводили количество до 500 литров с получением водного раствора. Полученный водный раствор перемешивали и растворяли до однородного состояния при 45°С±5°С, оставляя при комнатной температуре не менее чем на 1 час для приготовления маточной жидкости, после чего проверяли содержание карбоплатина;
3) если содержание вышеуказанной маточной жидкости соответствовало стандарту при испытании маточной жидкости, маточную жидкость фильтровали и стерилизовали при комнатной температуре и фасовали в виде раствора для инъекций 5 мг/5 мл, который хранили при 4°C в темноте.
3. Сравнительный пример
1) карбоплатин и 1,1-циклобутандикарбоновую кислоту с их соответствующей чистотой не менее 99% смешивали в молярном соотношении 1:1,1 с получением перенасыщенного водного раствора; где такие операции смешивания и приготовления осуществляли при температуре примерно 40°С в течение приблизительно 4 часов для завершения реакции;
2) реакционную систему фильтровали, фильтрат выдерживали при комнатной температуре (20±5°С) в темноте в течение 10 дней, при этом можно было наблюдать образование кристаллов;
3) раствор извлекали, кристаллический продукт собирали, и чистоту кристаллического продукта определяли анализом XRPD, при этом содержание карбоплатина 4,0 в продукте составляло менее 88%.
В следующих Примерах 2-3 исследовали структуру и физико-химические свойства карбоплатина 4.0; если не указано иное, нерасфасованное лекарственное средство карбоплатин 4.0 (т.е. кристаллический продукт карбоплатина 4.0) для использования готовили в соответствии с процессом самосборки из Примера 1. Кроме того, лиофилизированный порошок, полученный из нерасфасованного лекарственного средства карбоплатина 4.0, растворяли в воде (в дальнейшем лиофилизированный порошок «а»), лиофилизированный порошок, полученный из физически смешанных и растворенных в воде карбоплатина и 1,1-циклобутандикарбоновой кислоты (в дальнейшем именуемый лиофилизированный порошок «b»), и измельченный порошок, полученный из физически смешанного карбоплатина и 1,1-циклобутандикарбоновой кислоты (далее называемый лиофилизированным порошком «с») получали следующим образом:
1) Готовили точную навеску 100 мг нерасфасованного лекарственного средства карбоплатина 4,0, растворяли в 5,0 мл деионизированной воды с получением водного раствора; после выдерживания при комнатной температуре в течение 2 часов водный раствор замораживали в холодильнике при -70°С в течение 4 часов, а затем переносили в лиофилизатор (German Christ Lyophilizer Alpha2-4LD PLUS, где температура охлаждающей ловушки составляет -69°С, а вакуум 10 Па) для лиофилизации в течение 12 часов, и слегка растирали в ступке с получением белого лиофилизированного порошка, а именно лиофилизированного порошка «а»;
2) получали точную навеску смешанного образца, содержащего 100 мг карбоплатина и 38 мг 1,1-циклобутандикарбоновой кислоты (молярное соотношение составляет примерно 1:1), и готовили в виде лиофилизированного порошка «b» в соответствии с описанным выше процессом приготовления, в частности, лиофилизированного порошка «а»;
3) готовили точную навеску 100 мг карбоплатина и 38 мг 1,1-циклобутандикарбоновой кислоты, смешивали и затем слегка растирали в ступке с получением порошка, а именно лиофилизированного порошка «c».
Пример 2. Анализ структуры и физико-химических свойств карбоплатина 4.0
1. 1H ЯМР-анализ.
Определенные количества 1,1-циклобутандикарбоновой кислоты и карбоплатина растворяли в 0,5 мл дейтерированного ДМСО (ДМСО-d6) с получением смешанного испытуемого раствора 1,1-циклобутандикарбоновой кислоты и карбоплатина. После выдерживания в течение ночи смешанный испытуемый раствор анализировали с помощью 1H-ЯМР.
В соответствии с вышеописанным способом было приготовлено 9 групп вышеуказанных смешанных испытуемых растворов, пронумерованных 0-8, концентрации 1,1-циклобутандикарбоновой кислоты и карбоплатина в каждой группе смешанных испытуемых растворов приведены в Таблице 1 (добавленное количество 1,1-циклобутандикарбоновой кислоты поддерживали постоянным, а количество добавляемого карбоплатина меняли), и анализ 1Н-ЯМР проводили для 9 групп смешанных испытуемых растворов, соответственно, и результаты представлены в Таблице 1 и на Фиг. 1 и 2.
Результаты показали, что, за исключением двух карбоксильных атомов водорода в молекуле 1,1-циклобутандикарбоновой кислоты, химические сдвиги всех остальных атомов водорода не менялись с увеличением добавляемого количества карбоплатина. Химические сдвиги карбоксильных атомов водорода 1,1-циклобутандикарбоновой кислоты значительно изменились с увеличением добавляемого количества/концентрации карбоплатина (как показано на Фиг. 1 и в Таблице 1, где взаимосвязь между химическим сдвигом карбоксильного атома водорода и концентрацией карбоплатина может быть примерно следующей: y=12,69+0,00364x), переходя от сильного поля к слабому (12,681→13,422 ppm), что указывает на наличие взаимодействия двух водородных связей между 1,1-циклобутандикарбоновой кислотой и карбоплатином. Неожиданно оказалось, что в процессе титрования химический сдвиг амино водорода (NH3) в молекуле карбоплатина существенно не изменился, что указывает на то, что на амино водород (NH3) в молекуле карбоплатина мало повлияло добавление 1,1-циклобутандикарбоновой кислоты, другими словами, амино водород (NH3) в молекуле карбоплатина не образует водородной связи с 1,1-циклобутандикарбоновой кислотой.
Как показано на Фиг. 2, константа диссоциации k1, равная 0,3 ммоль/л, между карбоплатином и 1,1-циклобутандикарбоновой кислотой была рассчитана с помощью нелинейного подбора на основе значений химического сдвига карбоксильного водорода при различных количествах добавления карбоплатина. На основании обратной величины химического сдвига карбоксильного водорода и обратной величины молярной концентрации карбоплатина была рассчитана константа связывания между 1,1-циклобутандикарбоновой кислотой и карбоплатином, которая составила 4,22×104 л/моль. Это также указывало на то, что действительно имело место взаимодействие двух водородных связей между двумя компонентами карбоплатина 4.0 (т.е. карбоплатином и 1,1-циклобутандикарбоновой кислотой), но сила связывания между двумя компонентами относительно слабее, чем ковалентная связь.
Таблица 1 Добавленное количество карбоплатина и 1,1-циклобутандикарбоновой кислоты и химический сдвиг карбоксильного водорода
(Молярное отношение)
(ppm)
2. Анализ методом ДСК
1) ДСК анализ
(1) Готовили точную навеску соответствующего количества нерасфасованного лекарственного средства карбоплатина 4.0, лиофилизированного порошка «а», лиофилизированного порошка «b», смешанного порошка «с», карбоплатина и 1,1-циклобутандикарбоновой кислоты, и измеряли их термогравиметрические параметры (т.е. процесс плавления) с помощью анализатора ДСК, и результаты показаны на Фиг. 3.
Результаты показали, что кривые ДСК трех образцов, которые представляли собой нерасфасованное лекарственное средство Карбоплатин 4.0 (кривая 5 на Фиг. 3), лиофилизированный порошок «а» (кривая 4 на Фиг. 3) и лиофилизированный порошок «b» (кривая 6 на Фиг. 3), были относительно схожими, при этом их эндотермические пики начинали появляться при 198,94°С, 198,68°С и 193,06°С, соответственно. Условно говоря, эндотермический процесс (или кривая) лиофилизированного порошка «а» был ближе к таковому для нерасфасованного лекарственного средства карбоплатина 4.0, в то время как эндотермический процесс лиофилизированного порошка «b» немного отличался от такового для нерасфасованного лекарственного средства карбоплатина 4.0. В дополнение к эндотермическому пику при 198°С смешанный порошок «с» также имел очевидный эндотермический пик при 153,05°С (см. кривую 3 на Фиг. 3), и этот пик был близок к эндотермическому пику 1,1-циклобутандикарбоксилата. кислоты (см. кривую 1 на Фиг. 3), и можно подтвердить, что этот пик был эндотермическим пиком 1,1-циклобутандикарбоновой кислоты. Можно видеть, что физическая смесь карбоплатина и 1,1-циклобутандикарбоновой кислоты проявляет характеристики своего состава. Карбоплатин не проявлял никакого эндотермического пика около 153°С и 198°С, и имел пик разложения при повышении температуры до 252°С (см. кривую 2 на Фиг. 3).
(2) Чтобы проверить, является ли пик примерно 198°C пиком плавления карбоплатина 4.0, температуру плавления карбоплатина 4.0 дополнительно проверили, изменив скорость нагревания, и результаты были показаны на Фиг. 14. При этом скорости нагревания, соответствующие кривым 1-4 на Фиг. 14, составили 3°С/мин, 5°С/мин, 10°С/мин и 20°С/мин, соответственно.
Как показано на Фиг. 14, с увеличением скорости нагревания пик плавления смещается вправо, поэтому можно определить, что карбоплатин 4.0 не имеет постоянной температуры плавления, а пик, отображаемый ДСК, представляет собой пик разложения при плавлении.
(3) были приготовлены 4 серии нерасфасованного препарата карбоплатина 4.0, пронумерованные как 1-4; брали соответствующее количество каждой из 1-4 серий нерасфасованного препарата карбоплатин 4.0, измеряли их термогравиметрические параметры с помощью анализатора ДСК, и результаты были показаны на Фиг. 4. Как можно видеть, все 4 разные серии нерасфасованного лекарственного средства карбоплатина 4.0 также демонстрировали эндотермические пики только около 198°C, и эндотермический пик не появлялся при температурах примерно 153°C и 252°C.
2) Результат и обсуждение
(1) Кривые ДСК карбоплатина 4.0, лиофилизированного порошка «а» и смешанного порошка «с» показали большие различия, где не только положение и форма пика термоабсорбции (или эндотермического пика) показали значительные изменения, но также различалось количество пиков поглощения;
(2) нерасфасованное лекарственное средство карбоплатин 4.0 и лиофилизированный порошок «а» начинали демонстрировать резкий пик фазового перехода примерно при 198°С, в то время как лиофилизированный порошок «b» имел пик фазового перехода примерно при 193°С, что указывает, что два компонента карбоплатина 4.0 (карбоплатин и 1,1-циклобутандикарбоновая кислота) находились в кристаллическом состоянии, в то время как два компонента лиофилизированного порошка «b» находились в полукристаллическом или аморфном состоянии.
(3) Имелись различия между лиофилизированным порошком «b» и смешанным порошком «c», в то время как кривая ДСК лиофилизированного порошка «b» была аналогична кривой для карбоплатина 4.0, и не было эндотермического пика растворения 1,1-циклобутандикарбоновой кислоты около 153°C, что указывает на то, что после растворения в воде и лиофилизации карбоплатин и 1,1-циклобутандикарбоновая кислота образуют аналог карбоплатина 4.0, благодаря силе водородной связи, однако его кристаллическое состояние значительно отличается от карбоплатина 4.0, собранного и приготовленного с помощью специального способа из этого примера.
(4) Сравнивая кривые ДСК нерасфасованного лекарственного средства карбоплатина 4.0 и лиофилизированного порошка «а», можно видеть, что кривые ДСК этих двух препаратов были относительно схожими; после того, как карбоплатин 4.0 был лиофилизирован с получением лиофилизированного порошка «а», его пик поглощения немного сместился, но не было эндотермического пика около 153°С, что указывает на то, что процесс лиофилизации мало влиял на связывание между двумя компонентами карбоплатина 4.0.
Приведенные выше результаты испытаний ДСК показывают, что нерасфасованное лекарственное средство карбоплатин 4.0 (твердое состояние) действительно значительно отличается от физической смеси (такой как вышеупомянутый лиофилизированный порошок «b» и смешанный порошок «c») карбоплатина и 1,1-циклобутандикарбоновой кислоты, поскольку карбоплатин 4.0 образован из двух компонентов посредством водородных связей и не является простой физической смесью. Это дополнительно иллюстрирует то, что в процессе самосборки по настоящему изобретению два компонента карбоплатин и 1,1-циклобутандикарбоновая кислота действительно образуют новое химическое соединение (то есть карбоплатин 4.0), благодаря силе водородной связи, которая может стабильно существовать при более мягких условиях.
3. Анализ методом XRPD
Этот тест показал, что, поскольку нерасфасованное лекарственное средство карбоплатин 4.0 представляло собой игольчатые кристаллы и имелась серьезная предпочтительная ориентация, использование обычного метода отражения не может точно отражать структурную информацию образца, в то время как использование метода пропускания ослабляло предпочтительную ориентацию, которая может более реалистично отражать информацию о структуре образца и быть более точной для количественного анализа (результаты пропускания и отражения нерасфасованного лекарственного средства карбоплатина 4.0 показаны на Фиг. 5). Поэтому в следующих экспериментах для анализа XRPD использовали метод пропускания.
XRPD анализ:
100 мг нерасфасованного лекарственного средства карбоплатина 4.0, образцы лиофилизированного порошка «а», лиофилизированного порошка «b», смешанного порошка «с», карбоплатина и 1,1-циклобутандикарбоновой кислоты загружали в держатель образца для пропускания, соответственно; такие же экспериментальные условия использовали для определения XRPD, и результаты показаны на Фиг. 6.
Результаты показали, что существуют значительные различия между спектрами XRPD нерасфасованного препарата карбоплатина 4.0 (спектр 4 на Фиг. 6), лиофилизированного порошка «а» (спектр 3 на Фиг. 6), лиофилизированного порошка «b» (спектр 2 на Фиг. 6) и смешанного порошка «с» (спектр 1 на Фиг. 6), как описано далее:
(1) Как лиофилизированный порошок «b», так и смешанный порошок «c» имели дифракционные пики при 2θ примерно 11,55±0,2°, которые были характеристическими пиками карбоплатина; и спектры XRPD нерасфасованного лекарственного средства карбоплатина 4.0 и лиофилизированного порошка «а» были сходными, и их основные характерные пики находились в положениях, где значение 2θ составляло примерно 7,55°, 10,51°, 14,63°, 15,10°, 15,66°, 16,78°, 18,55°, 20,83°, 22,86°, 23,67°, 24,02° и т.д., но они не имели дифракционного пика при 2θ примерно 11,55±0,2°. Это продемонстрировало, что нерасфасованное лекарственное средство карбоплатин 4.0 и лиофилизированный порошок «а» отличались от физической смеси карбоплатина и 1,1-циклобутандикарбоновой кислоты (т.е. от лиофилизированного порошка «b» и смешанного порошка «с»), что также указывает, что в процессе самосборки по настоящему изобретению два компонента карбоплатин и 1,1-циклобутандикарбоновая кислота действительно образовали новое химическое соединение (т.е. карбоплатин 4.0), благодаря силе водородных связей, которая может стабильно существовать в более мягких условиях.
В сочетании с вышеприведенным сравнительным анализом показано, что характеристический пик дифракции примерно при 11,55±0,2º можно использовать в качестве пика контроля качества карбоплатина 4.0. Другими словами, метод анализа XRPD можно использовать в качестве метода контроля качества чистоты нерасфасованного лекарственного средства карбоплатина 4.0, а также можно использовать в качестве метода определения содержания карбоплатина 4.0 в нерасфасованном лекарственном средстве карбоплатине 4.0.
4. Анализ методом ЖХ-МС
1) ЖХ-МС анализ
ЖХ-МС-анализ кристаллического продукта карбоплатина 4.0 в этом примере выполняли в соответствии с обычным методом.
Анализ ЖХ-МС проводили на карбоплатине 4.0, и диссоциированный карбоплатин и 1,1-циклобутандикарбоновую кислоту определяли в режиме положительных ионов и в режиме отрицательных ионов, соответственно (см. Фиг. 7 – Фиг. 10), где пик молекулярного иона карбоплатина [M+H]+ имел m/z 372,0514, а пик молекулярного иона 1,1-циклобутандикарбоновой кислоты [M+H]- имел m/z 143,0341, что указывает на то, что карбоплатин 4,0 диссоциирует на карбоплатин и 1,1-циклобутандикарбоновую кислоту в условиях разделения жидкостной хроматографией.
2) Проточно-инжекционная масс-спектрометрия
Принимая во внимание, что разделение с помощью жидкостной хроматографии разрушает внутримолекулярные водородные связи карбоплатина 4.0, для введения образца использовали проточную инжекцию, чтобы непосредственно анализировать водный раствор карбоплатина 4.0. Пики молекулярных ионов карбоплатина 4.0 [m/z 514,0917] и 1,1-циклобутандикарбоновой кислоты [m/z 143,0375] наблюдались в режиме отрицательных ионов (см. Фиг. 11), и только пик молекулярных ионов карбоплатина [m/z 372,0543] был обнаружен в режиме положительных ионов (см. Фиг. 12).
3) Описанную выше проточно-инжекционную масс-спектрометрию проводили на физически смешанном образце карбоплатина и 1,1-циклобутандикарбоновой кислоты (молярное соотношение 1:1), и было обнаружено, что те же ионы, что и карбоплатин 4.0, также генерируется в режиме отрицательных ионов.
Приведенные выше результаты анализа показали, что хроматографическое разделение разрушило бы водородные связи в карбоплатине 4.0, поэтому метод жидкостной хроматографии-масс-спектрометрии не соответствовал стандарту испытания качества карбоплатина 4.0. Использование введения в поток для образца позволяет напрямую проводить масс-спектрометрию и получать точную молекулярную массу карбоплатина 4.0 в режиме отрицательных ионов. Однако, поскольку физически смешанный образец карбоплатина и 1,1-циклобутандикарбоновой кислоты также продуцировал в этом режиме те же ионы, что и карбоплатин 4.0, масс-спектрометрия не позволяет отличить карбоплатин 4.0 от физической смеси карбоплатина и 1,1-циклобутандикарбоновой кислоты, но ее можно использовать только для точного определения молекулярной массы карбоплатина 4.0.
Пример 3. Способ оценки хеликазы
В этом эксперименте влияние хеликазы на карбоплатин 4.0 было подтверждено тестом на связывание ДНК с участием хеликазы, включая использование суперспиральной и линейной плазмидной ДНК (Hr. pcDNA, которую можно экстрагировать обычным способом) в качестве матрицы, изменяя конформацию ДНК посредством реакций путем объединения с различными противоопухолевыми препаратами на основе платины, с последующим определением разных препаратов платины по различиям в гель-электрофореграммах.
На связывание препаратов платины с плазмидной ДНК влияли многие факторы, такие как концентрация препарата (концентрация карбоплатина или карбоплатина 4,0), время реакции, размер плазмиды, хлорид-ион в растворе, ЭДТА, кислотность и щелочность (pH), температура и т.д.; авторы изобретения провели большое количество сравнительных экспериментов и окончательно выбрали следующие условия, включая концентрацию препарата 0,05-0,2 ммоль/л, размер плазмиды около 6000 п.н., время реакции 1 час, pH 6,5-7,3, буфер без ЭДТА и ионов Cl, и температуру 37°C, при которых наблюдались значительные различия в связывании с ДНК карбоплатина и карбоплатина 4,0 (см. Фиг. 13).
Детали эксперимента были следующими:
В этом эксперименте использовали ДНК-хеликазу T4 GP41 (далее именуемую как T4), которая была получена от iCloning Biotech Co., Ltd.
Условия эксперимента: гель-электрофорез на 0,8% агарозе (упаковка от фирмы Promega), рН 6,5-7,3; 37°С, время реакции 1 час, концентрация препарата 0,1 ммоль/л; 5 В, Hr. pcDNA: 6000 п.н., 1 ммоль/л АТФ (упаковка от Promega).
Следующие образцы (номера испытаний 1-5 и М) были проанализированы в описанных выше экспериментальных условиях, и добавление pcDNA, лекарств и хеликаз в каждый образец было показано следующим образом:
Тест 1: pcDNA + Карбоплатин + T4
Тест 2: pcDNA + Карбоплатин 4.0 + T4
Тест 3: pcDNA + Карбоплатин 4.0
Тест 4: pcDNA + Карбоплатин
Тест 5: pcDNA
Тест М: Маркер (контрольный стандарт)
Результаты испытаний представлены на Фиг. 13, где цифры 1-5 и М на Фиг. 13 соответствовали вышеуказанным номерам испытания, соответственно.
Результаты показали, что картины электрофореза плазмид в Тесте 1 и Тесте 4 были примерно одинаковыми, что указывает на то, что хеликаза не оказывала очевидного влияния на карбоплатин; но карбоплатин 4.0 был совершенно другим, картины электрофореза плазмид в тесте 3 и тесте 5 были в основном одинаковыми, что указывает на то, что сам карбоплатин 4.0 в основном не был связан с суперспиральной плазмидой (pcDNA); и скорость электрофореза плазмиды в Тесте 2 была самой низкой, что указывает на то, что хеликаза разрушила водородную связь карбоплатина 4.0 и высвободила карбоплатин, а высвобожденный карбоплатин объединился с плазмидой с образованием аддукта ДНК, что уменьшило скорость электрофореза.
Изобретение относится к способу получения карбоплатинового комплекса, который представляет собой комплекс, образованный объединением карбоплатина и 1,1-циклобутандикарбоновой кислоты посредством двух водородных связей, причем каждая из двух водородных связей образуется между карбонильным кислородом молекулы карбоплатина и карбоксильным водородом молекулы 1,1-циклобутандикарбоновой кислоты, где структура указанного карбоплатинового комплекса приведена ниже. Предложенный способ включает смешивание карбоплатина и 1,1-циклобутандикарбоновой кислоты в молярном соотношении 1:1,5-3 при 65°С±10°С в течение не менее 0,5 ч с получением пересыщенного водного раствора и сбор кристаллов карбоплатинового комплекса. Также предложены способ получения фармацевтического препарата и способ контроля качества карбоплатинового комплекса. Изобретение позволяет получить устойчивый комплекс, образованный карбоплатином и 1,1-циклобутандикарбоновой кислотой за счет нековалентных связей, который в качестве целевого продукта имеет очень высокую чистоту. 3 н. и 4 з.п. ф-лы, 14 ил., 1 табл., 3 пр.
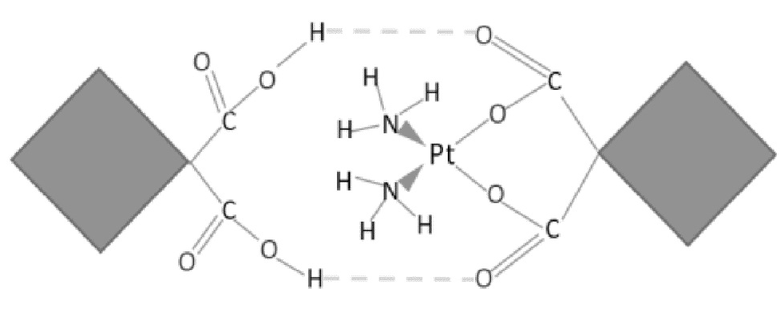
1. Способ получения карбоплатинового комплекса, который представляет собой комплекс, образованный объединением карбоплатина и 1,1-циклобутандикарбоновой кислоты посредством двух водородных связей, причем каждая из двух водородных связей образуется между карбонильным кислородом молекулы карбоплатина и карбоксильным водородом молекулы 1,1-циклобутандикарбоновой кислоты, и структура указанного карбоплатинового комплекса является следующей:
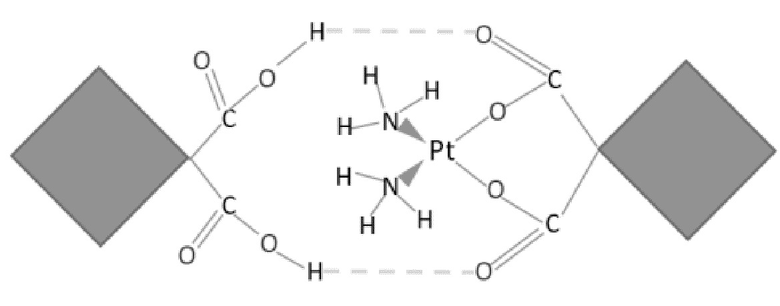 ,
,
и причем способ включает:
смешивание карбоплатина и 1,1-циклобутандикарбоновой кислоты в молярном соотношении 1:1,5-3 при 65±10°С в течение не менее 0,5 ч с получением пересыщенного водного раствора; и
сбор кристаллов карбоплатинового комплекса.
2. Способ получения по п. 1, в котором карбоплатиновый комплекс происходит из продукта самосборки карбоплатина и 1,1-циклобутандикарбоновой кислоты и имеет массовое содержание 95% или более.
3. Способ получения по п. 1, в котором карбоплатиновый комплекс начинает демонстрировать пик фазового перехода при 197,8±2°C по результатам, измеренным методом дифференциальной сканирующей калориметрии, и/или не имеющий при 2θ дифракционного пика примерно 11,55±0,2° по результатам, измеренным методом рентгеновской порошковой дифрактометрии.
4. Способ получения фармацевтического препарата, содержащего карбоплатиновый комплекс, полученный способом получения по любому из пп. 1-3, в качестве активного компонента, включающий:
- получение кристаллов карбоплатинового комплекса в соответствии со способом по п. 1, а также измельчение и сушку с получением порошка карбоплатинового комплекса; и
- приготовление препарата из этого порошка карбоплатинового комплекса.
5. Способ получения по п. 4, дополнительно включающий:
- растворение порошка карбоплатинового комплекса в стерилизованной воде, перемешивание и растворение при 45±5°С и выдерживание при комнатной температуре в течение 1 часа или более с получением маточной жидкости;
- фильтрование и стерилизацию маточной жидкости при комнатной температуре, а затем упаковку с получением жидкости для инъекций или
- получение из маточной жидкости лиофилизированного порошка для инъекций, твердого препарата для перорального применения, препарата в виде геля или препарата в виде спрея.
6. Способ контроля качества карбоплатинового комплекса, включающий:
- детекцию испытуемого образца с использованием рентгеновской порошковой дифрактометрии и определение того, что испытуемый образец не имеет при 2θ дифракционного пика примерно 11,55±0,2°; где испытуемый образец представляет собой карбоплатиновый комплекс, полученный способом получения по любому из пп. 1-3.
7. Способ контроля качества по п. 6, дополнительно включающий:
- детекцию испытуемого образца с использованием ВЭЖХ и определение того, что содержание карбоплатина и 1,1-циклобутандикарбоновой кислоты в испытуемом продукте составляет 97-103% для каждого вещества, а молярное отношение карбоплатина и 1,1-циклобутандикарбоновой кислоты составляет 0,95-1,05.
| YANG XuQing et al | |||
| Structural studies of dicycloplatin, an antitumor supramolecule, SCIENCE CHINA, 2010, vol | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Аппарат для обогащения руд флотацией | 1923 |
|
SU1346A1 |
| CN 109053808 A, 21.12.2018 | |||
| US 6699901 B1, 02.03.2004 | |||
| CN 104127402 A, 05.11.2014 | |||
| CN 104693245 A, 10.06.2015 | |||
| СПОСОБ ПОЛУЧЕНИЯ ДИЦИКЛОПЛАТИНА | 2015 |
|
RU2676269C1 |
Авторы
Даты
2024-12-12—Публикация
2020-08-26—Подача