ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к области лечения рубцов на коже.
УРОВЕНЬ ТЕХНИКИ
[0002] Введение кондиционированной среды из мезенхимальных стволовых клеток (SCs) показало, что секретируемые факторы, а не сами SCs, оказывают благоприятное паракринное действие и объясняют большую часть первоначальных результатов. Ранее было показано, что подвергнутые стрессу мононуклеарные клетки периферической крови (PBMCs) представляют собой легкодоступный и богатый источник клеточных секретов с сильной регенеративной активностью (APOSEC). Недавно было выявлено несколько способов действия и уже были описаны различные клинические показания для применения APOSEC, в том числе заживление ран, острый инфаркт миокарда, аутоиммунный миокардит, ишемия головного мозга и повреждение спинного мозга.
[0003] 0бразование патологических рубцов является сложной медицинской проблемой, которая встречается по всему миру. В западных странах у более чем 100 миллионов человек ежегодно образуются рубцы, при этом согласно оценкам у 11 миллионов человек развиваются келоидные рубцы. Риск развития гипертрофических рубцов после операции или ожоговой травмы превышает 30%. В отличие от обычных рубцов, гипертрофические рубцы характеризуются процессами чрезмерного образования фиброзных тканей в поврежденной области. Напротив, келоидные рубцы представляют собой прогрессирующие фибропролиферативные мальформации, которые образуются в рубцовой ткани и разрастаются за границы первоначального повреждения. Молекулярные механизмы, приводящие к образованию гипертрофических рубцов или келоидных рубцов, не до конца понятны. Гипертрофические рубцы и келоидные рубцы не только создают серьезные психологические проблемы, но и вызывают боль, зуд и приводят к ограничению движений. Терапевтические возможности по-прежнему ограничены, и золотого стандарта для лечения патологических рубцов не существует. Возможными вариантами являются 1) введение стероидов, подавляющих пролиферацию фибробластов, 2) радиационно-индуцированная остановка клеточного цикла и гибель клеток фибробластов, 3) прессотерапия с воздействием на натяжение в области раны и 4) хирургическое удаление рубцовых тканей, которое, однако, демонстрирует чрезвычайно высокую частоту рецидивов. Кроме того, применялись химиотерапевтические средства и другие вещества, однако без заметной эффективности. Наиболее перспективным вариантом лечения на сегодняшний день является комбинация хирургического удаления и последующего лечения стероидами.
[0004] Таким образом, задача настоящего изобретения заключается в обеспечении способов удаления/лечения рубцов на коже, которые не требуют хирургического вмешательства и/или применения лекарственного средства, имеющего нежелательные побочные эффекты.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] Настоящее изобретение относится к композиции, содержащей супернатант клеточной культуры моно нуклеарных клеток периферической крови (РВМС) для применения при лечении рубцов на коже.
[0006] Неожиданно оказалось, что супернатанты клеточных культур РВМС можно применять для лечения рубцов на коже. Как известно, супернатанты клеточных культур РВМС применяют для лечения поврежденных тканей, таких как раны на коже (см., например, ЕР 2379085). Однако в заживлении ран участвуют совершенно другие биологические процессы и типы клеток по сравнению со зрелыми рубцами на коже.
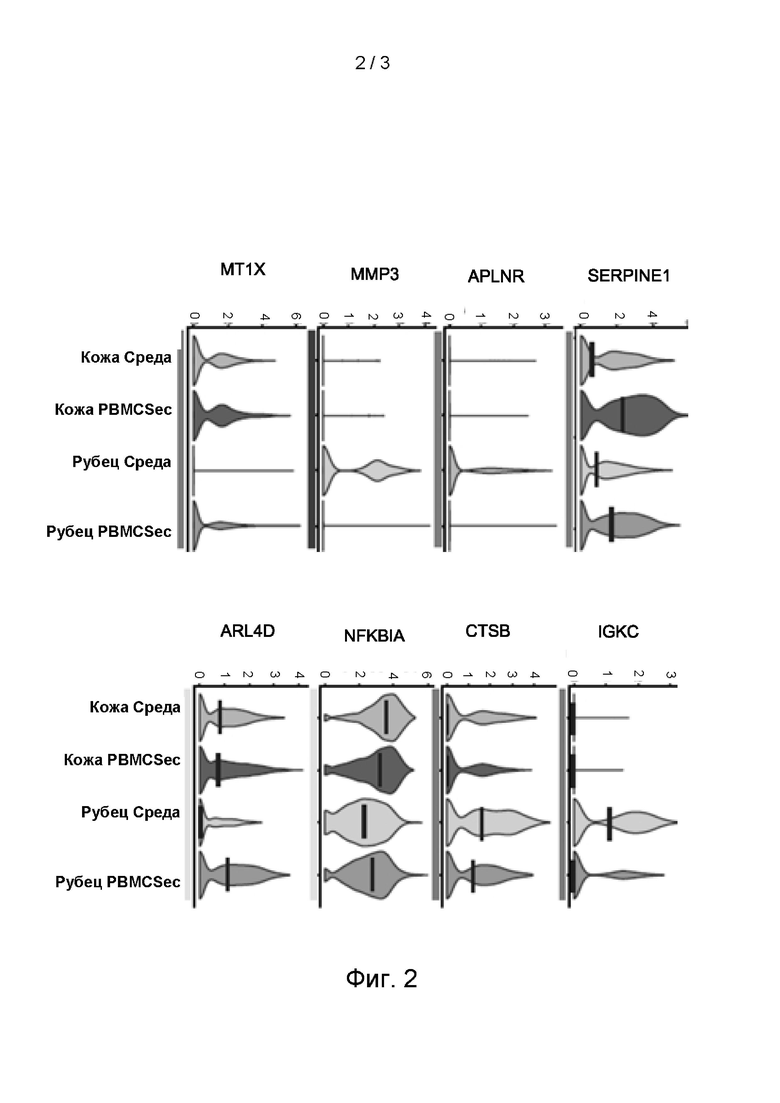
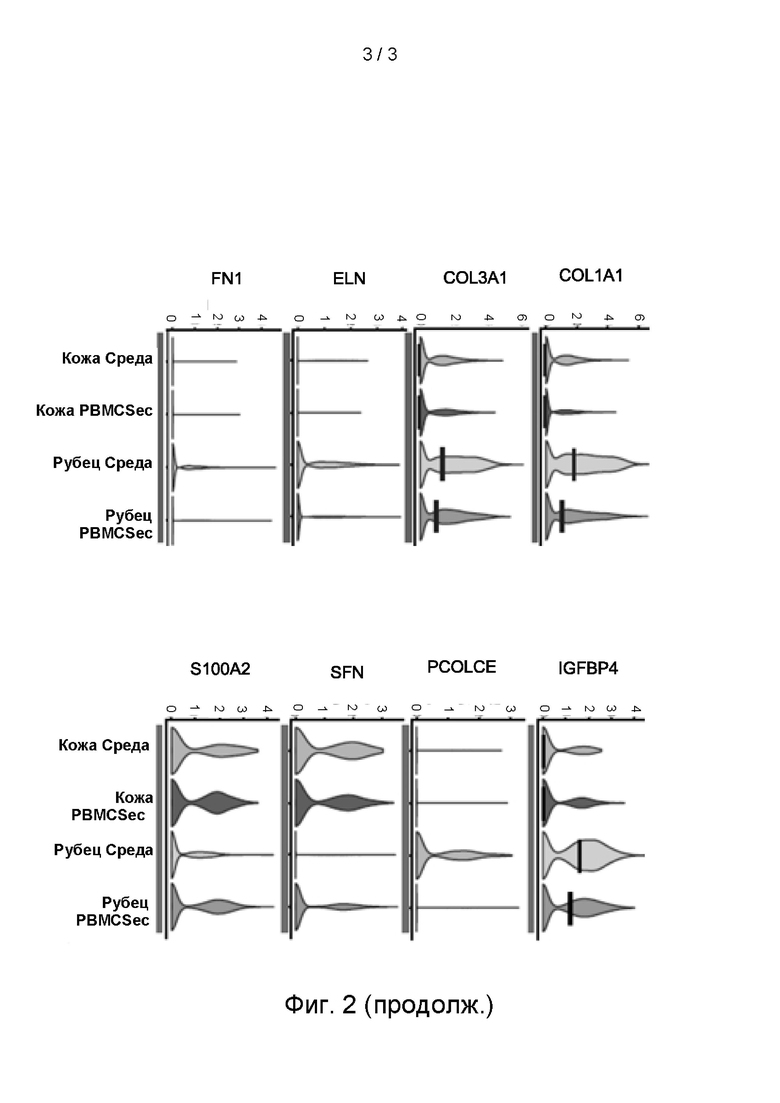
[0007] Заживление ран представляет собой сложный процесс, состоящий из 4 фаз: фазы гемостаза, фазы воспаления, пролиферативной фазы и фазы созревания. В то время как основной функцией заживления раны является быстрое закрытие поврежденного участка и создание нового защитного барьера от окружающей среды, рубец представляет собой фиброзную ткань, остающуюся после заживления раны, которая заменяет нормальную кожу. В отличие от нормальной кожи, рубцовая ткань главным образом характеризуется избыточным продуцированием внеклеточного матрикса, такого как коллагены COL1A1 и COL3A1, эластин (ELN), фибронектин 1 (FN1) и проколлаген (PCOLCE) (фиг. 2). Кроме того, в рубцовой ткани значительно дерегулированы несколько факторов, модифицирующих внеклеточный матрикс, в том числе цитокин (например, белок 4, связывающий инсулиноподобный фактор роста (IGFBP4)), протеазы (например, матриксная металлопротеиназа-3 (ММР3)) и ингибиторы протеазы (например, член 1 семейства Е серпинов (SERPINE1)) (Фиг. 2). Кроме того, миофибробласты обладают высокой активностью, что приводит к стягиванию кожи. Поэтому основной целью лечения рубцов является уменьшение количества миофибробластов и чрезмерного продуцирования компонентов внеклеточного матрикса, а также нормализация дерегулированного продуцирования и дерегулированных факторов, модифицирующих матрикс.
[0008] Другой аспект настоящего изобретения относится к способу косметического лечения рубцов на коже, включающему стадию введения в рубцы на коже эффективного количества композиции, содержащей супернатант клеточной культуры моно- нуклеарных клеток периферической крови (РВМС).
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
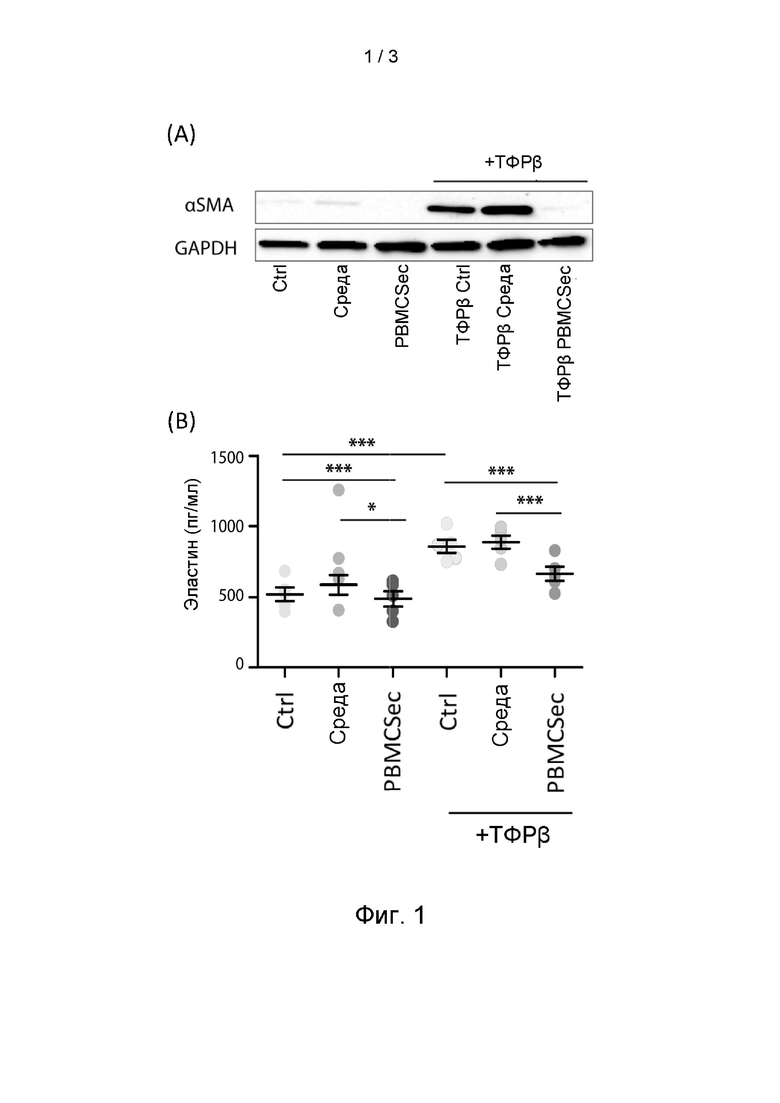
[0009] На фиг. 1 показано, что APOSEC блокирует ТФР-опосредованную (ТФР - тромбоцитарный фактор роста) дифференцировку в миофибробласты. А) Вестерн-блот первичного фибробласта человеческой кожи, стимулированного с помощью среды или APOSEC, в отсутствие или в присутствии ТФР-бета. APOSEC предотвращал ТФР-бета-индуцированную дифференцировку фибробластов в миофибробласты, как показано на основе экспрессии альфа-SMA. Твердофазный иммуноферментный анализ (ELISA) супернатантов фибробластов, стимулированных ТФР-бета, показал повышенное продуцирование эластина. Добавление APOSEC снижало повышенную секрецию эластина.
[0010] На фиг. 2 показано scPHК-секвенирование (сРНК - малые цитоплазматические РНК) (scRNAseq) биопсий гипертрофических рубцов и нормальной кожи человека, обработанных ex vivo с помощью среды или APOSEC. Показаны гены, связанные с фиброзом кожи. Лечение с помощью APOSEC нормализовало экспрессию указанных генов до значений, наблюдаемых в нормальной коже.
ОПИСАНИЕ ВАРИАНТОВ РЕАЛИЗАЦИИ
[0011] Настоящее изобретение относится к композиции, содержащей супернатант клеточной культуры РВМС, для применения при лечении рубцов на коже.
[0012] Известно, что клетки, в частности клетки млекопитающих, секретируют многочисленные вещества во время культивирования в среде для культивирования клеток. Полученные таким образом кондиционированные культуральные среды можно применять для лечения и/или предотвращения различных заболеваний и расстройств. Например, в WO 2010/070105 и WO 2010/079086 описаны кондиционированные культуральные среды («супернатанты»), которые получены путем культивирования PBMCs и которые можно использовать для лечения различных воспалительных состояний. Соответственно, в контексте настоящего документа «супернатант клеточной культуры мононуклеарных клеток периферической крови (PBMCs)» относится к любому супернатанту, получаемому путем культивирования PBMCs in vitro в культуральной среде. После стадии культивирования культивированные PBMCs удаляют из культуральной среды с получением по существу бесклеточного, предпочтительно полностью бесклеточного супернатанта. Супернатант культуры РВМС содержит, наряду с компонентами среды для культивирования, вещества, продуцируемые и секретируемые посредством PBMCs и/или даже лизированных PBMCs. Термин «супернатант» можно использовать взаимозаменяемо с кондиционированной культуральной средой, получаемой путем культивирования PBMCs.
[0013] Супернатант согласно настоящему изобретению можно получить путем культивирования PBMCs, которые подвергаются ионизирующему излучению до или во время культивирования. Ионизирующее излучение предпочтительно представляет собой гамма-излучение.
[0014] В контексте настоящего документа «рубец на коже» относится к фиброзной ткани, которая заменяет нормальную ткань кожи после повреждения кожи. Рубцы на коже являются результатом биологического процесса заживления раны на коже. Рубцовая ткань обычно состоит из того же белка (т.е. коллагена), что и ткань, которую она заменяет. Однако состав волокон в рубцовой ткани значительно отличается от состава ткани, не содержащей рубцов. В нормальной ткани коллаген образует случайное переплетение, тогда как в рубцовой ткани коллаген подвергается сшиванию и характеризуется упорядочиванием в одном направлении. Вследствие такого упорядочивания коллагена в рубцовой ткани кожа рубца обычно имеет более низкое функциональное качество по сравнению с нормальным рандомизированным упорядочиванием коллагена, поэтому такая кожа будет, например, менее устойчивой к ультрафиолетовому излучению, при этом потовые железы и волосяные фолликулы в рубцовых тканях не вырастают вновь. Согласно настоящему изобретению «рубец на коже» относится к любому типу рубцов на коже и, в частности, к гипертрофическим рубцам, келоидным рубцам и растяжкам.
[0015] Гипертрофический рубец является результатом избыточного продуцирования коллагена, которое приводит к тому, что рубец увеличивается в размерах, однако в границах первоначальных ран. Такие рубцы обычно возникают в течение от 4 до 8 недель после инфицирования раны или закрытия раны.
[0016] Келоидные рубцы являются более серьезной формой чрезмерного рубцевания, поскольку они могут неограниченно расти с образованием крупных опухолевых (хотя и доброкачественных) новообразований. Келоидные рубцы обычно разрастаются за пределы первоначальной области раны. Такие рубцы могут быть зудящими или болезненными, при этом их хирургическое удаление может ухудшить состояние и привести к прогрессированию келоида.
[0017] Растяжки, также известные как стрии, также являются формой рубцевания. Они возникают, когда кожа быстро растягивается (например, во время беременности, значительного увеличения веса или скачков роста у детей и подростков) или когда кожа находится в состоянии натяжения во время процесса заживления.
[0018] В контексте настоящего документа термины «лечить» и «лечение» рубцов на коже относятся к уменьшению объема рубца и/или размера рубца на по меньшей мере 20%, предпочтительно на по меньшей мере 40%, более предпочтительно на по меньшей мере 50%, более предпочтительно на по меньшей мере 60%, более предпочтительно на по меньшей мере 70%, более предпочтительно на по меньшей мере 80%, более предпочтительно на по меньшей мере 90%, более предпочтительно на по меньшей мере 95% и/или, в идеале, к восстановлению исходной ткани. Введение композиции согласно настоящему изобретению должно приводить к частичной или даже полной трансформации рубцовой ткани в нормальную ткань.
[0019] Еще один аспект настоящего изобретения относится к способу косметического лечения рубцов на коже, включающему стадию введения в рубцы на коже эффективного количества композиции, содержащей супернатант клеточной культуры моно-нуклеарных клеток периферической крови (PBMCs).
[0020] Согласно предпочтительному варианту реализации настоящего изобретения композицию, предложенную в настоящем изобретении, наносят на рубец на коже или вводят в рубец на коже путем инъекции.
[0021] Композицию согласно настоящему изобретению можно наносить местно или вводить в рубец на коже путем инъекции. Оказалось, что для небольших рубцов на коже достаточно местного введения на рубец композиции согласно настоящему изобретению. В частности, растяжки можно обрабатывать местно. Если рубец характеризуется чрезмерным накоплением коллагена, предпочтительно вводить композицию согласно настоящему изобретению в рубец и/или ткань, окружающую рубец, путем инъекции.
[0022] Если композицию согласно настоящему изобретению вводят местно, указанная композиция может быть предоставлена в виде геля, предпочтительно гидрогеля, в виде мази, в виде пасты, в виде крема, в виде порошка, в виде линимента или в виде лосьона. Для приготовления указанных лекарственных форм для местного применения можно использовать маслянистые основы, абсорбирующие мазевые основы, эмульсионные основы типа вода в масле, эмульсионные основы типа масло в воде, водорастворимые или смешивающиеся с водой основы, которые также могут содержать антиоксиданты, такие как витамин С и другие вещества.
[0023] Согласно еще одному предпочтительному варианту реализации настоящего изобретения композицию вводят в рубец на коже путем инъекции с помощью иглы или узла микроигл, содержащего множество микроигл.
[0024] Композицию согласно настоящему изобретению можно инъецировать в рубец на коже с помощью игл. В зависимости от размера рубца композицию инъецируют в рубец в одно или более мест инъекции. Особенно предпочтительным является применение узлов микроигл, содержащих множество микроигл. Применение таких узлов микроигл позволяет инъецировать композицию согласно настоящему изобретению одновременно в более чем одно место инъекции. Кроме того, узел микроигл особенно подходит для введения композиции согласно настоящему изобретению в рубец на коже путем проникновения в рубец, который ранее был покрыт указанной композицией. В таком случае узел микроигл несколько раз вводят в кожу и выводят из кожи.
[0025] Узел микроигл также может быть частью трансдермального пластыря, содержащего композицию согласно настоящему изобретению, которую наносят на рубец на коже. Такой трансдермальный пластырь является особенно подходящим, поскольку он позволяет непрерывно вводить композицию согласно настоящему изобретению в течение длительного периода времени.
[0026] Согласно еще одному предпочтительному варианту реализации настоящего изобретения композицию по меньшей мере частично инъецируют в рубец на коже во время удаления иглы или микроигл.
[0027] Для более однородного распределения композиции согласно настоящему изобретению внутри рубца на коже предпочтительно вводить указанную композицию во время удаления иглы или игл из рубца на коже.
[0028] Рубец на коже предпочтительно представляет собой гипертрофический рубец, келоидный рубец или растяжку.
[0029] Согласно еще одному предпочтительному варианту реализации настоящего изобретения клеточная культура PBMCs содержит моноциты, Т-клетки, В-клетки и/или NK-клетки.
[0030] Согласно дополнительному предпочтительному варианту реализации настоящего изобретения клетки PBMCs культивируют в среде для культивирования клеток, выбранной из группы, состоящей из среды для роста клеток, предпочтительно среды CellGro, более предпочтительно среды Cellgro GMP DC, RPMI, DMEM (минимальная эссенциальная среда Игла, модифицированная по способу Дульбекко), X-vivo и Ultraculture.
[0031] PBMCs клеточной культуры РВМС подвергают ионизирующему излучению до или во время культивирования. Наряду с перечисленными вызывающими стресс условиям PBMCs можно подвергать дополнительному стрессу. Следовательно, согласно предпочтительному варианту реализации настоящего изобретения PBMCs подвергают одному или более дополнительным вызывающим стресс условиям до или во время культивирования.
[0032] В контексте настоящего документа термин «в вызывающих стресс условиях» относится к условиям культивирования, приводящим к появлению клеток, подвергнутых стрессу. Условия, вызывающие стресс у клеток, включают, среди прочего, нагревание, химические вещества, излучение, гипоксию, осмотическое давление и т.д.
[0033] Дополнительный стресс у клеток согласно настоящему изобретению приводит к дополнительному увеличению экспрессии и секреции веществ, полезных для лечения воспалительных заболевания кожи, в частности, заболеваний кожи, связанных с ишемией.
[0034] Согласно предпочтительному варианту реализации настоящего изобретения вызывающие стресс условия включают гипоксию, озон, нагревание (например, выше оптимальной температуры культивирования PBMCs, т.е. 37°C, на более чем 2°C, предпочтительно на более чем 5°C, более предпочтительно на более чем 10°C), излучение (например, УФ-излучение, гамма-излучение), химические вещества, осмотическое давление (т.е. осмотические условия, повышенные на по меньшей мере 10% по сравнению с осмотическими условиями, обычно возникающими в биологической жидкости, в частности, в крови) или их комбинации.
[0035] Следовательно, согласно дополнительному предпочтительному варианту реализации настоящего изобретения вызывающее стресс условие выбрано из группы, состоящей из излучения, в частности, ионизирующего излучения или УФ-излучения, гипоксии, озона, нагревания, осмотического давления и сдвига pH.
[0036] Согласно еще одному предпочтительному варианту реализации настоящего изобретения PMCs подвергают действию ионизирующего излучения, предпочтительно гамма-излучения, в дозе по меньшей мере 10 Гр, предпочтительно по меньшей мере 20 Гр, более предпочтительно по меньшей мере 40 Гр, более предпочтительно по меньшей мере 50 Гр.
[0037 ]Согласно предпочтительному варианту реализации настоящего изобретения перед выделением супернатанта PBMCs культивируют в течение по меньшей мере 4 часов, предпочтительно в течение по меньшей мере 6 часов, более предпочтительно в течение по меньшей мере 12 часов.
[0038] Согласно предпочтительному варианту реализации настоящего изобретения клеточная культура РСВМС содержит от 1×105 до 1×108 PBMCs/мл, предпочтительно от 1×106 до 1×107 PBMCs/мл, более предпочтительно от 2×106 до 5×106 PBMCs/мл.
[0039] Композиция согласно настоящему изобретению может содержать фармацевтически приемлемые вспомогательные вещества, такие как разбавители (например, буферы, такие как фосфатно-солевой буфер (PBS), растворы NaCl или сбалансированный солевой раствор Хэнка (HBSS)), стабилизаторы (например, бутилированный гидрокситолуол (ВНТ), бутилированный гидроксианизол (ВНА), витамин С, витамин Е), носители и т.д. Способы получения таких вспомогательных веществ хорошо известны специалисту в данной области техники.
[0040] Для увеличения срока годности композиции согласно настоящему изобретению супернатант можно лиофилизировать. Способы лиофилизации таких препаратов хорошо известны специалистам в данной области техники.
[0041] Перед применением лиофилизированный препарат можно привести в контакт с водой или водным раствором, содержащим буферы, стабилизаторы, соли и т.д.
[0042] Согласно еще одному предпочтительному варианту реализации настоящего изобретения композицию, предложенную в настоящем изобретении, можно использовать для лечения рубцов на коже людей и всех видов млекопитающих, таких как лошади, собаки, кошки и верблюды.
[0043] Настоящее изобретение дополнительно проиллюстрировано с помощью следующих примеров, но без ограничения ими.
ПРИМЕР
[0044] Материал и способы
[0045] Материал пациента
[0046] Резецированную рубцовую ткань получали от трех пациентов, перенесших плановую операцию по резекции рубца. Рубцы были предварительно классифицированы пластическим хирургом как гипертрофические, патологические рубцы в соответствии с POSAS (Fearmonti RM et al. Plastic and reconstructive surgery 127, 242 (2011)). Все рубцы представляли собой зрелые рубцы, то есть в возрасте по меньшей мере двух лет, не были прооперированы и ранее не подвергались лечению с применением кортикостероидов, 5-FU (5-фторурацил), облучения или аналогичных способов. Все образцы рубцов получали от пациентов мужского и женского пола моложе 45 лет, не имеющих хронических заболеваний или не принимающих лекарственных препаратов на постоянной основе. Здоровую кожу получали от трех здоровых доноров женского пола в возрасте от 25 до 45 лет из излишней кожи брюшной стенки, удаленной во время плановой абдоминопластики.
[0047] Животные:
[0048] Во всех экспериментах на животных использовали самок мышей Balb/c в возрасте от 8 до 12 недель (Центр разведения животных Венского медицинского университета, Австрия). Мышей содержали в соответствии с улучшенными стандартными условиями содержания животных при 12/12-часовом цикле дня и ночи в выбранной не содержащей патогенов среде со свободным доступом к пище и воде.
[0049] Модель глубокой раны и рубцевания у мышей
[0050] Для модели глубокой раны на коже и рубцевания мышей подвергали глубокой анестезии путем внутрибрюшинного введения кетамина в количестве от 80 до 100 мг/кг, ксилазина в количестве от 10 до 12,5 мг/кг и использовали послеоперационное обезболивание путем подкожной инъекции 0,1 мл/10 мг бупренофина и добавления 7,5 мг/мл пиритрамида в питьевую воду. На спине отмечали квадратный участок размером 9×9 мм и вырезали его острыми ножницами. Раны оставляли заживать непокрытыми без какого-либо дополнительного вмешательства в течение 4 недель, а затем исследовали образовавшуюся рубцовую ткань и документировали результаты.
[0051] Получение APOSEC
[0052] Секретомы PBMCs получали в соответствии с Правилами надлежащей производственной практики (GMP), установленными Австрийским Красным Крестом, Службой переливания крови Верхней Австрии (Австрия), как описано (Wagner Т et al. Sci Rep 8, 18016 (2018); Laggner M et al. Stem cell research & therapy 11,9 (2020)). PBMCs получали путем центрифугирования в градиенте плотности с применением среды фиколл-пак Плюс (GE Healthcare. США), доводили до концентрации 25×106 клеток/мл (25 Ед/мл, 1 Ед=секретом 1 миллиона клеток) и подвергали воздействию гамма-облучения цезием 137 с дозой 60 Гр (IBL 437С, Isotopen Diagnostik CIS GmbH, Германия). Клетки культивировали в среде CellGenix GMP DC, не содержащей феноловый красный (CellGenix GmbH, Германия) в течение 24±2 часов. Клетки и клеточный дебрис удаляли посредством центрифугирования и пропускали супернатанты через фильтр с размером пор 0,2 мкм. Для клиренса вируса проводили обработку метиленовым синим, как описано (Gugurell A et al, Blood Transfus 18(2020):30-39). Секретом лиофилизировали, окончательно стерилизовали посредством высоких доз гамма-облучения и хранили при -80°C. Все эксперименты проводили с применением полученных в соответствии с GMP секретом следующих партий: А000918399086, А000918399095 и А000918399098, А000918399101, А000918399102 и А000918399105. Непосредственно перед проведением экспериментов лиофилизат повторно суспендировали в 0,9% NaCl до обеспечения исходной концентрации 25 Ед/мл.
[0053] Стимулирование рубцов у мышей с помощью APOSEC
[0054] Начиная с дня 29 после ранения кожи, мышам вводили путем инъекции 100 мкл 0,9% NaCl, среду (среду CellGenix GMP DC, не содержащую феноловый красный) или APOSEC, полученный, как описано выше, через день в течение двух недель. Затем половину мышей из каждой группы умерщвляли и направляли на анализ, другую половину оставляли еще на две недели без дополнительного вмешательства, а затем умерщвляли.
[0055] Стимулирование кожи и рубцов ex vivo
[0056] Из кожи и рубцовой ткани человека брали панч-биопсии размером 6 мм, удаляли подкожную жировую ткань и помещали биопсии в 12-луночные планшеты, в которые в качестве добавок были введены 400 мкл DMEM (Gibco, Thermo Fisher, США, с 10% фетальной бычьей сывороткой и 1% пенициллином/стрептомицином) и 100 мкл среды CellGenix или 100 мкл APOSEC. Кроме того, в верхнюю часть дермы в середине биопсии инъецировали 100 мкл среды или APOSEC. Биопсии инкубировали в течение 24 часов, а затем собирали для анализа scRNAseq.
[0057] Стимулирование кожи и рубца с помощью APOSEC, выделение клеток и капельное scRNAseq
[0058] Рубцы у мышей и образцы стимулированной кожи и рубцов человека расщепляли в наборе для диссоциации цельной кожи Miltenyi (Miltenyi Biotec, Германия) в течение 2,5 часов в соответствии с протоколом производителя и обрабатывали на GentleMACS OctoDissociator (Miltenyi). Суспензию клеток обрабатывали с применением 100 мкм и 40 мкм фильтра, центрифугировали в течение 10 минут со скоростью 1500 об/мин, дважды промывали и повторно суспендировали в 0,04% FBS в фосфатно-солевом буфере (PBS). В течение 30 секунд добавляли DAPI (4',6-диамидин-2-фенилиндол) в количестве 1 мкл/1 миллион клеток, клетки снова дважды промывали и сортировали в отношении жизнеспособности на высокоскоростном устройстве для сортировки клеток MoFlo Astrios (Beckman-Coulter, США) и для дальнейшей обработки использовали только явно DAPI-отрицательные клетки. Сразу после сортировки жизнеспособные клетки загружали в прибор 10X-chromium (экспрессия гена в одной клетке 3'v 2/3, 10Х Genomics, USA) с получением гель-шарика в эмульсии (GEM). Получение GEM, приготовление библиотеки, секвенирование РНК, демультиплексирование и подсчет осуществляли в профильном биомедицинском центре секвенирования Центра молекулярной медицины (СеММ, Австрия). Секвенирование проводили 2×75 п.о., спаренный конец на Illumina HiSeq 3000/4000 (Illumina, США).
[0059] Результаты
[0060] APOSEC предотвращает опосредованное ТФР-бета разрушение эластичных волокон кожи
[0061] В биопсии ex vivo инъецировали ТФР-бета1, ТФР-бета1 и среду, а также ТФР-бета1 и APOSEC. В биопсии нормальной кожи человека вводили путем инъекции ТФР-бета1 для индуцирования ремоделирования ткани, подобной рубцу. Через два дня после инъекции ТФР-бета1 наблюдали плотный внеклеточный матрикс (ЕСМ) и распад эластичных волокон. Аналогичные морфологические изменения наблюдались при введении в кожу путем инъекции ТФР-бета1 и среды. Комбинация ТФР-бета1 с APOSEC ингибировала осаждение ЕСМ и деградацию эластичных волокон.
[0062] APOSEC предотвращает индуцированное ТФР-бета накопление ЕСМ в коже мыши
[0063] Далее исследовали, наблюдались ли аналогичные эффекты при инъецировании APOSEC в кожу мыши in vivo. Анализ показал, что APOSEC значительно снижал продуцирование и отложение коллагена после инъекции ТФР-бета1. Кроме того, наблюдалась пониженная экспрессия альфа-гладкомышечного актина, представляющего собой миофибробласты.
[0064] APOSEC предотвращает ТФР-бета-индуцированную дифференцировку фибробластов в миофибробласты.
[0065] Для дальнейшего исследования влияния на дифференцировку фибробластов в сокращающиеся миофибробласты первичные фибробласты человека стимулировали in vitro с помощью ТФР-бета. Стимулирование с применением ТФР-бета сильно индуцировало экспрессию альфа-гладкомышечного актина (альфа-SMA), белкового маркера для миофибробластов. Хотя добавление среды самой по себе не влияло на экспрессию альфа-SMA, добавление APOSEC полностью устраняло индуцированную ТФР-бета дифференцировку фибробластов в миофибробласты (фиг. 1А). Кроме того, белковая экспрессия эластина была в значительной степени индуцирована посредством ТФР-бета и ингибирована посредством APOSEC (фиг. 1В).
[0066] Внутрикожная инъекция APOSEC в рубцы человека ex vivo регулирует РНК-экспрессию генов, ассоциированных с рубцом
[0067] APOSEC или контрольную среду инъецировали внутрикожно в панч-биопсии кожи и рубцовой ткани человека. Через 24 часа биопсии подвергали диссоциации под воздействием ферментов и анализировали одиночные клетки путем секвенирования РНК одиночных клеток (фиг. 2). Несколько мРНК, связанных с образованием рубца, показали значительную регуляцию после инъекции APOSEC. Введение APOSEC в рубцовую ткань явно изменяло профиль мРНК до тех уровней, которые наблюдаются в здоровой коже (т.е. на коже без рубцов).
[0068] Вывод
[0069] Указанные анализы продемонстрировали, что введение, в частности внутрикожная инъекция, APOSEC способно улучшать качество рубца за счет ингибирования дифференцировки в мио фибробласты и продуцирования и отложения компонентов внеклеточного матрикса. APOSEC явным образом улучшает уже существующие зрелые рубцы (в отличие от новых формирующихся рубцов).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ АЛЛЕРГИИ ИЛИ АЛЛЕРГИЧЕСКОЙ РЕАКЦИИ | 2020 |
|
RU2827897C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ГИПЕРТРОФИЧЕСКОГО РУБЦА ПОСЛЕ МАММОПЛАСТИКИ | 2006 |
|
RU2320995C1 |
| АНАЛИЗ АКТИВНОСТИ СЕКРЕТОМОВ | 2018 |
|
RU2790567C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯИЛИ ЛЕЧЕНИЯ РАНЫ ИЛИ РУБЦА, ВКЛЮЧАЮЩАЯ БЕНЗБРОМАРОН | 2021 |
|
RU2816016C1 |
| Способ устранения рубцовых изменений кожи | 2020 |
|
RU2731527C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ РУБЦОВЫХ ДЕФОРМАЦИЙ КОЖИ | 2015 |
|
RU2599868C1 |
| КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ КОЖНЫХ РУБЦОВ | 2013 |
|
RU2705211C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 2009 |
|
RU2542512C2 |
| ГЕЛЬ ДЛЯ ЛЕЧЕНИЯ, ПРОФИЛАКТИКИ ОБРАЗОВАНИЯ КЕЛОИДНЫХ И ГИПЕРТРОФИЧЕСКИХ РУБЦОВ КОЖИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2377975C2 |
| СПОСОБ ЛЕЧЕНИЯ ГИПЕРТРОФИЧЕСКИХ ИЛИ КЕЛОИДНЫХ РУБЦОВ КОЖИ | 2006 |
|
RU2335307C1 |
Группа изобретений относится к лечению рубцов на коже. Раскрыто применение композиции, содержащей эффективное количество супернатанта клеточной культуры мононуклеарных клеток периферической крови (PBMC) для лечения рубца на коже, при этом указанный рубец на коже представляет собой гипертрофический рубец или келоидный рубец, при этом клеточная культура PBMC содержит от 1*105 до 1*108 PBMCs/мл, и PBMCs подвергнуты действию ионизирующего излучения в дозе по меньшей мере 10 Гр до или во время культивирования, при этом указанная клеточная культура PBMC содержит моноциты, Т-клетки, В-клетки и NK-клетки. Также раскрыт способ косметического лечения рубцов на коже. Группа изобретений обеспечивает удаление/лечение рубцов на коже, которое не требует хирургического вмешательства. 2 н. и 8 з.п. ф-лы, 2 ил., 1 пр.
1. Применение композиции, содержащей эффективное количество супернатанта клеточной культуры мононуклеарных клеток периферической крови (PBMC) для лечения рубца на коже, при этом указанный рубец на коже представляет собой гипертрофический рубец или келоидный рубец, при этом клеточная культура PBMC содержит от 1*105 до 1*108 PBMCs/мл, и PBMCs подвергнуты действию ионизирующего излучения в дозе по меньшей мере 10 Гр до или во время культивирования, при этом указанная клеточная культура PBMC содержит моноциты, Т-клетки, В-клетки и NK-клетки.
2. Способ косметического лечения рубцов на коже, включающий стадию введения в рубцы на коже эффективного количества композиции, содержащей супернатант клеточной культуры мононуклеарных клеток периферической крови (PBMC), при этом клеточная культура PBMC содержит от 1*105 до 1*108 PBMCs/мл, и PBMCs подвергнуты действию ионизирующего излучения в дозе по меньшей мере 10 Гр до или во время культивирования, при этом указанная клеточная культура PBMC содержит моноциты, Т-клетки, В-клетки и NK-клетки.
3. Применение композиции по п. 1 или способ по п. 2, отличающиеся тем, что указанную композицию наносят на рубец на коже или вводят в рубец на коже путем инъекции.
4. Применение композиции по п. 3 или способ по п. 3, отличающиеся тем, что указанную композицию вводят в рубец на коже путем инъекции с помощью иглы или узла микроигл, содержащего множество микроигл.
5. Применение композиции по п. 4 или способ по п. 4, отличающиеся тем, что указанную композицию по меньшей мере частично инъецируют в рубец на коже во время удаления иглы или микроигл.
6. Способ по любому из пп. 2-5, отличающийся тем, что рубец на коже представляет собой растяжку.
7. Применение композиции по любому из пп. 1 или 3-5 или способ по любому из пп. 2-6, отличающиеся тем, что PBMCs культивируют в среде для культивирования клеток, выбранной из группы, состоящей из среды для роста клеток, предпочтительно среды CellGro, более предпочтительно среды DC Cellgro GMP, RPMI, DMEM, X-vivo и Ultraculture.
8. Применение композиции по любому из пп. 1, 3-5 или 7 или способ по любому из пп. 2-7, отличающиеся тем, что PBMCs подвергают действию ионизирующего излучения в дозе по меньшей мере 20 Гр, предпочтительно по меньшей мере 40 Гр, более предпочтительно по меньшей мере 50 Гр.
9. Применение композиции по любому из пп. 1, 3-5, 7 или 8 или способ по любому из пп. 2-8, отличающиеся тем, что перед выделением супернатанта PBMCs культивируют в течение по меньшей мере 4 часов, предпочтительно в течение по меньшей мере 6 часов, более предпочтительно в течение по меньшей мере 12 часов.
10. Применение композиции по любому из пп. 1, 3-5 или 7-9 или способ по любому из пп. 2-9, отличающиеся тем, что клеточная культура PBMC содержит от 1*106 до 1*107 PBMCs/мл, предпочтительно от 2*106 до 5*106 PBMCs/мл.
| KR 102215667 B1, 16.02.2021 | |||
| СПОСОБ ЛЕЧЕНИЯ КОЖНЫХ СТРИЙ | 2009 |
|
RU2407555C1 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 2009 |
|
RU2542512C2 |
| SHIN-ICHIRO YOKOYAMA et al | |||
| A strategy of retrograde injection of bone marrow mononuclear cells into the myocardium for the treatment of ischemic heart disease // Journal of Molecular and Cellular Cardiology, v | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
Авторы
Даты
2024-12-19—Публикация
2022-04-13—Подача