Область техники, к которой относится изобретение
Группа изобретений относится к области медицины, а именно к онкологии и генетике, и может быть использована для выявления наследственной формы рака молочной железы (РМЖ) при первичном генетическом тестировании.
Одним из наиболее распространенных наследственных опухолевых синдромов является наследственный рак молочной железы и яичников. Случаи РМЖ в России составляют 22,1% в структуре всех злокачественных новообразований (ЗНО) и являются ведущей онкологической патологией у женщин. В структуре смертности женщин РМЖ имеет наибольший удельный вес и составляет 15,8% (Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2021 году (заболеваемость и смертность) – М.: МНИОИ им. П.А. Герцена − филиал ФГБУ «НМИЦ радиологии» Минздрава России, − 2022. − илл. − 252 с. ISBN 978-5-85502-280-3).
Приблизительно 80-95% опухолей молочной железы являются спорадическими, тогда как остальные 5-20% классифицируются как семейные или наследственные. В группе наследственных опухолей только 20-25% случаев РМЖ обусловлены наличием патогенных вариантов в высокопенетрантных генах предрасположенности к РМЖ – BRCA1 и BRCA2(Nielsen, F.C.; van Overeem Hansen, T.; Sørensen, C.S. Hereditary breast and ovarian cancer: New genes in confined pathways. Nat. Rev. Cancer 2016, 16, 599–612).
Наследственные опухолевые синдромы (НОС) представляют собой генетическую предрасположенность к определенным типам рака, обусловленную патогенными генетическими вариантами (мутациями) в одном или нескольких генах [Garber J, Offit K. Hereditary cancer predisposition syndromes. J Clin Oncol. 2005;23(2):276−292. doi: 10.1200/jco.2005.10.042; Hereditary Cancer Syndromes and Risk Assessment: ACOG COMMITTEE OPINION, Number 793. Obstet Gynecol. 2019 Dec;134(6):e143-e149. doi: 10.1097/AOG.0000000000003562. PMID: 31764758; Баранова Е.Е., Бодунова Н.А., Воронцова М.В., Захарова Г.С., Макарова М.В., Румянцев П.О., Хатьков И.Е. Наследственные опухолевые синдромы: современная парадигма. Проблемы Эндокринологии. 2020;66(4):24-34. https://doi.org/10.14341/probl12366]. Зачастую эти мутации приводят к развитию злокачественного новообразования (ЗНО) в молодом возрасте и первично-множественным опухолям. По данным мировой научной литературы в среднем 10% ЗНО обусловлены НОС. Наиболее известные НОС – наследственный рак молочной железы и яичника, синдром Линча, синдром Ли-Фраумени, синдром Коудена, синдром Пейтца-Егерса, синдром Хиппеля-Линдау (Гиппеля-Линдау) множественная эндокринная неоплазия, нейрофиброматоз. Большинство НОС наследуются по аутосомно-доминантному типу, то есть для развития заболевания необходима всего одна поврежденная копия гена (гетерозиготная генная мутация/вариант нуклеотидной последовательности в гетерозиготном состоянии). Носителем гетерозиготной мутации может быть один из родителей и, соответственно, вероятность передачи ее потомству составляет 50%.
Уровень техники
В настоящее время установлено, что НОС вызваны герминальными генетическими вариантами, которые пациент получает от родителей, либо эти мутации возникают впервые (варианты нуклеотидной последовательности de novo). Наиболее известным и распространенным НОС является наследственный рак молочной железы и яичника, ассоциированный с генами BRCA1 и BRCA2 (Petrucelli N., Daly M.B., Pal T. BRCA1- and BRCA2-Associated Hereditary Breast and Ovarian Cancer. In: Adam M.P., Ardinger H.H., Pagon R.A., editors. Gene Reviews. University of Washington; Seattle, WA, USA: 1998. https://www.ncbi.nlm.nih.gov/books/NBK1247). Патогенные герминальные варианты в этих генах выявляются примерно в 50% случаев наследственного рака молочной железы.
Ген BRCA1 расположен на длинном плече 17 хромосомы (цитогенетическая локация: 17q21) и относится к генам-супрессорам опухоли, то есть защищает клетку от злокачественной трансформации, кодируя белки, участвующие в регуляции клеточного цикла, репарации ДНК (OMIMEntry - * 113705 - BRCA1 DNAREPAIR-ASSOCIATEDPROTEIN; BRCA1. Omim.org. https://www.omim.org/entry/113705?search=brca&highlight=brca. Published 2022. Accessed June 22, 2022.). Ген BRCA2 расположен на длинном плече 13 хромосомы (цитогенетическая локация: 13q12.3) и также относится к опухолевым супрессорам (OMIMEntry - * 600185 - BRCA2 DNAREPAIR-ASSOCIATEDPROTEIN; BRCA2. Omim.org. https://www.omim.org/entry/600185?search=brca&highlight=brca. Published 2022. Accessed June 22, 2022.). Мутации в генах BRCA1/2вызывают развитие рака молочной железы с вероятностью выше 70% (OMIM Entry - # 604370 - BREAST-OVARIAN CANCER, FAMILIAL, SUSCEPTIBILITY TO, 1; BROVCA1 [Электронный ресурс]. URL: https://www.omim.org/entry/604370). У носителей-женщин в разы увеличивается также риск развития рака яичников. Опасность мутации представляют и для мужчин в виде высокого риска рака простаты, молочной (грудной) железы. Ген BRCA2, патогенные варианты которого также ассоциированы с высоким риском развития рака молочной железы, открыт в 1994 г. (Narod S, Foulkes W. BRCA1 and BRCA2: 1994 and beyond. Nature Reviews Cancer. 2004;4(9):665-676. doi:10.1038/nrc1431.).
Помимо генов BRCA1/2, вклад в развитие наследственных форм рака молочной железы вносят гены CHEK2, TP53, PTEN, PALB2, ATM, RAD50, BLM,BRIP, NBN, MSH2, MLH1, MSH6 и PMS2 и другие (HosteG, D'HooreP, LegiusEetal. Abstract P5-09-05: Hereditary breast cancer beyond BRCA: Clinical and histopathological characteristics in patients with germline CHEK2, ATM, PALB2 and TP53-mutations. Poster Session Abstracts. 2019. doi:10.1158/1538-7445.sabcs18-p5-09-05; Laura Keren Urbina-Jara, et al. Landscape of Germline Mutations in DNA Repair Genes for Breast Cancer in Latin America: Opportunities for PARP-Like Inhibitors and Immunotherapy. Genes (Basel).2019 Oct; 10(10): 786, doi: 10.3390/genes10100786).
Еще одно исследование показало, что при наследственной форме РМЖ наиболее часто встречаются мутации в генах: BRCA1 (27,4%), BRCA2 (20,3%), TP53 (10,5%), MUTYH (9,9%), ATM (8,8%), CHEK2 (6,2%) и PALB2 (5,1%) (Guindalini RSC etal. Detection of germline variants in Brazilian breast cancer patients using multigene panel testing. SciRep. 2022 Mar 9;12(1):4190. doi: 10.1038/s41598-022-07383-1).
НаданныймоментизвестнаассоциацияпатогенныхгерминальныхвариантовнесколькихдесятковгеновсрискомразвитиянаследственныхформРМЖ (Breast Cancer Association Consortium; Breast Cancer Risk Genes - Association Analysis in More than 113,000 Women. N Engl J Med. 2021 Feb 4;384(5):428-439. doi: 10.1056/NEJMoa1913948; NCCN Guidelines. Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic. Version 3.2024 — February 12, 2024. https://www.nccn.org/professionals/physician_gls/pdf/genetics_bop.pdf.).
Благодаря развитию технологий высокопроизводительного секвенирования (NGS) стало возможным анализировать и изучать одновременно десятки и даже сотни генов в рамках одного анализа. Несмотря на преимущества NGS-панелей, не существует единой панели для диагностики наследственных форм РМЖ: в мире используется большое количество панелей, содержащих различные онкоассоциированные гены. Ввиду разного состава таких панелей и различные группы пациентов, для которых они применяются, сопоставлять результаты различных научных исследований с применением NGS-панелей достаточно затруднительно. Одним из подходов к генетическому тестированию наследственных форм РМЖ является применение полногеномных и полноэкзомных методов исследования. Их использование позволяет провести поиск потенциально всех патогенных вариантов во всех онкоассоциированных генах. Однако полногеномные методы тестирования трудно массовоприменять в клинической практике из-за большого объема получаемых данных, сложностей интерпретации, временных затрат. В настоящее время тестирование герминальных мутаций при РМЖ, как правило, начинается с определения наиболее частых мутаций, а затем, если причинного варианта не выявлено, производится расширенное тестирование с использованием таргетных NGS-панелей, включающих гены BRCA1/BRCA2.
Более 10 лет в России в качестве тестирования первой линии при подозрении на наследственный РМЖ применяется ПЦР-панель, состоящая из 8 патогенных вариантов генов BRCA1/2, которые считались наиболее распространенными у пациентов с наследственными формами РМЖ (Карпухин А.В., Логинова А.Н., Хомич Е.А., Поспехова Н.И. Наследственная предрасположенность к раку молочной железы. Медицинская генетика. 2002;1(6):254–261. Karpukhin A.V., Loginova A.N., Khomich E.A., Pospekhova N.I. Hereditary predisposition to breast cancer. Medical genetics. 2002; 1 (6):254–261 (in Russ.); Поспехова Н.И., Логинова А.Н., Любченко Л.Н. и др. Гетерогенность семей с наследственной предрасположенностью к раку молочной железы по встречаемости мутаций в гене BRCA1. Медицинская генетика. 2003; 2 (11):459–463. Pospekhova N.I., Loginova A.N., Lyubchenko L.N. et al. Heterogeneity of families with a hereditary predisposition to breast cancer by the occurrence of mutations in the BRCA1 gene. Medical genetics. 2003;2(11):459–463 (in Russ.); Loginova A., Pospekhova N., Lyubchenko L. et al. Spectrum of mutations in BRCA1 gene in hereditary forms of breast and ovarian cancer in Russian families. Bull Exp Biol Med. 2003;136(3):276–278. DOI: 10.1023/b:bebm.0000008982.21806.9b; Savkova A., Gulyaeva L., Gerasimov A., Krasil’nikov S. Genetic Analysis of Multiple Primary Malignant Tumorsin Women with Breast and Ovarian Cancer. Int J Mol Sci. 2023 Apr; 24(7): 6705, doi:10.3390/ijms24076705), таблица 1.
Таблица 1
В настоящее время в клинической практике диагностическим тестированием первой линии на наследственные формы РМЖ по-прежнему является ПЦР-панель на 8 «частых мутаций BRCA1/2» (наиболее близкий аналог - Клинические рекомендации «Рак молочной железы». Ассоциация онкологов России, Общероссийская общественная организация «Российское общество клинической онкологии», Общероссийская общественная организация «Российское общество онкомаммологов»; 2021; [Электронный ресурс]. URL: https://cr.minzdrav.gov.ru/recomend/379_4.). При получении отрицательного результата ПЦР-анализа «мутаций не выявлено», дальнейшее NGS-тестирования, как правило, назначается по ограниченным показаниям или не назначается вовсе, что может приводить к пропущенным случаям наследственного РМЖ. Известная ПЦР-панель включает мутации, которые встречаются в 50% случаев BRCA-ассоциированного рака. Однако, при первичном скрининге важно выявить риск развития РМЖ у максимально возможного количества обследуемых пациентов в процессе выполнения одного обследования, не расширяя список различных диагностических процедур.
Таким образом, решаемой в настоящем изобретении технической проблемой явилась разработка диагностической панели первой линии, позволяющей выявить с высокой точностью наследственную форму РМЖ в рамках первичного генетического тестирования.
Раскрытие сущности изобретения
Достигаемым техническим результатом является повышение точности выявления наследственной формы РМЖ за счет включения в панель наиболее распространенных по данным полногеномных исследований клинически значимых (патогенных) вариантов генов, ассоциированных с повышенным или высоким риском развития РМЖ. Созданная панель позволяет в рамках одного диагностического обследования в рамках первичного генетического тестирования выявить до 80-90% случаев наследственных форм РМЖ.
В панель не включены генетические варианты, связь которых с развитием наследственных форм РМЖ сомнительна, либо риск развития наследственных РМЖ незначительно превышает общепопуляционный: низкопенетрантные генетические варианты, варианты с неопределенной клинической значимостью, доброкачественные или вероятно доброкачественные полиморфизмы, переклассифицированные генетические варианты (утратившие свою клиническую значимость).
Указанный результат достигается благодаря следующей совокупности существенных признаков.
Созданная панель для выявления при первичном генетическом тестировании наследственной формы рака молочной железы, включает средства для обнаружения в образце крови пациента следующих патогенных вариантов, представленных в таблице 2:
Таблица 2
Способ выявления наследственной формы рака молочной железы, путем использования описанной выше панели. Выявление у пациента хотя бы одного из патогенных вариантов, определяемых с помощью указанной панели, свидетельствует о наличии наследственной формы рака молочной железы.
Осуществление изобретения
Разработанная нами диагностическая ПЦР-панель включает 48 онкоассоциированных вариантов, подобранных в результате анализа результатов полногеномных исследований (секвенирование ДНК пациентов с диагностированным раком молочной железы, как изолированным, так и в составе первично-множественных злокачественных новообразований).
Нами проанализированы 2707результатов полногеномного секвенирования, проведенного женщинам старше 18 лет с диагностированным РМЖ и подозрением на наследственную форму рака.
Возраст обследованных пациентов от 19 до 88 лет, средний возраст 50,04 ± 8,47 лет.
Критерии включения для проведения полногеномного секвенирования:
Первичная опухоль и не менее одного из нижеперечисленных критериев:
- возраст пациентки до 60 лет на момент диагностики злокачественного новообразования;
- билатеральный рак молочной железы;
- рак молочной железы диагностирован в сочетании с злокачественным новообразованием яичников;
- у пациентки диагностирован рак молочной железы и имеется отягощенный семейный анамнез: 2 и более родственников I или II степени родства с новообразованиями следующих локализаций (как минимум одним): колоректальный рак, рак эндометрия, рак желудка, рак яичника, рак поджелудочной железы, рак почки, ЗНО билиарного тракта, ЗНО головного мозга, множественные полипы толстой кишки;
- у пациентки диагностирован рак молочной железы и имеется отягощенный семейный анамнез: выявлен случай рака молочной железы у кровных родственников мужского пола I и/или II степени родства.
Все выявленные по результатам полногеномного секвенирования клинически значимые варианты валидированы методом секвенирования по Сэнгеру.
Важным является то, что критерием исключения из исследования не был факт ранее проведенных генетических исследований, что не отбраковывает генетические варианты, выявленные ранее с помощью ПЦР-панели, и позволяет наиболее достоверно оценить структуру всех клинически значимых генетических вариантов.
По результатам полногеномных исследований в 532 из 2707 случаев (19,7%) выявлен хотя бы 1 патогенный (влияющий на функцию гена) герминальный (наследственный) вариант в гене, изменения которого каким-либо образом ассоциированы с развитием онкологического заболевания по данным научной литературы.
В свою очередь, из числа патогенных вариантов выделена группа каузативных, т.е. непосредственно ассоциированных с фенотипом – являющихся причиной конкретного онкологического заболевания (значимым или основным фактором риска его развития). При выявлении герминального патогенного каузативного варианта можно делать вывод об установлении наследственной формы рака молочной железы. В нашем исследовании к каузативным можно отнести 401 варианта из 532 патогенных, что составляет 14,8% (401/2707) от всей обследованной выборки.
На варианты генов BRCA1/2приходится 285 случаев, что составляет 71,1% (285/401) всех выявленных случаев наследственного рака и 10,5% (285/2707) от всей обследованной выборки.
На 8 вариантов BRCA1/2 (таблица 1) пришлось суммарно 147 случаев, что составляет36,7% (147/401) всех выявленных случаев наследственного рака, 51,6% (147/285)всех случаев BRCA-ассоциированного рака и 5,4% (147/2707)от всей обследованной выборки.
Таким образом, нами отмечено, что 8 вариантов BRCA1/2, традиционно считающиеся наиболее распространенными и обуславливающими большую часть наследственных форм рака, составляют только чуть более половины случаев BRCA-ассоциированного рака и чуть более трети от всех установленных наследственных форм.
По результатам полногеномных исследований, которые позволили наиболее полно оценить структуру генетических вариантов у пациентов с диагностированным РМЖ, нами установлено, что некоторые каузативные генетические варианты повторяются 2 и более раза, что позволяет выделить наиболее частые варианты у пациентов с диагностированным РМЖ и разработать новую диагностическую ПЦР-панель первой линии, включающую наиболее частые герминальные патогенные варианты при РМЖ. Это варианты в определенных позициях генов BRCA1, BRCA2,ATM, BARD1, CHEK2, MLH1, NF1, PALB2, TP53(таблица 3).
По данным полногеномных исследований генетические варианты, включенные в нашу ПЦР-панель, суммарно встречаются у 299 из 2707 пациентов (11%), что составляет 299/401 (74,6%) всех выявленных по результатам полногеномного исследования наследственных случаев РМЖ. При этом наша ПЦР-панель включает суммарно 209/285 (73,3%) всех выявленных по результатам полногеномных исследований патогенных вариантов генов BRCA1 и BRCA2.
Таким образом, диагностическая ПЦР-панель первой линии, включающая наиболее частые герминальные патогенные варианты при РМЖ, позволяющая выявить более 70% случаев наследственного РМЖ, включая BRCA-ассоциированный рак, выглядит следующим образом (таблица 3).
Таблица 3
Исследование пациентов осуществляется следующим образом:
Предлагаемая ПЦР-панель универсальна для пациентов мужского и женского пола.
Исследование ограничено указанными генетическими вариантами.
Ограничения метода. Предлагаемая ПЦР-панель не предназначена для анализа полной последовательности включенных в нее генов, а также для выявления следующих типов генетических вариантов: структурные изменения хромосом (инверсии, транслокации, протяженные делеции или вставки), полиплоидия, анеуплоидия, протяженные участки триплетных и (или) других повторов; варианты в генах, имеющих псевдогены; эпигенетические изменения.
Подготовка биоматериала к исследованию. Для проведения ПЦР-панели рекомендовано получить образец венозной крови объемом 12 мл в 3 пробирках объемом 4 мл с ЭДТА; кровь следует тщательно перемешать, осторожно перевернув пробирки 4-6 раз, не встряхивать.
Все пробирки должны быть промаркированы и содержать следующую информацию: штрих-код; фамилия, имя, отчество пациента; дата рождения пациента; дата взятия биоматериала.
Полученные образцы крови не замораживать, хранить и транспортировать при температуре +2 - +8 (холодильник; термосумка с хладоэлементом).
С момента получения образца крови пациента до отправки в лабораторию-исполнитель должно пройти не более 3 календарных дней.
Перед отправкой биоматериала в лабораторию-исполнитель пациент вместе с врачом заполняет и подписывает документы:
согласие на обработку персональных данных;
направление на молекулярно-генетическое исследование (ПЦР-панель);
добровольное информированное согласие на молекулярно-генетическое исследование (ПЦР-панель).
Примечание: пациентам с диагностированными злокачественными новообразованиями при наличии клинических признаков наследственного опухолевого синдрома, отрицательными результатами данного ПЦР-тестирования может быть рекомендовано проведение расширенной NGS-панели, полноэкзомного или полногеномного секвенирования.
При положительном результате ПЦР-тестирования в зависимости от конкретного выявленного варианта можно сделать заключение о наследственной форме РМЖ, а также других ассоциированных рисках, обусловленных данным генетическим вариантом (таблица 4).
Таблица 4
В основе предложенного изобретения лежит молекулярно-генетическое исследование образцов венозной крови пациентов с диагностированным злокачественным новообразованием молочной железы вне зависимости от стадии заболевания, гистологических и иммуногистохимических особенностей опухоли.
В качестве неограничивающего примера приведено исследование образца периферической крови пациентов в возрасте18 лети старшена наличие одного или нескольких вариантов в генах ATM, BARD1, BRCA1, BRCA2, CHEK2, MLH1, NF1, PALB2, TP53 (таблица 3).
Процедура молекулярно-генетического исследования осуществляется следующим образом (указанные конкретные варианты использованных приборов, реактивов, представлены лишь в качестве примеров и могут быть заменены на аналогичные).
1. Выделение ДНК. Для проведения генотипирования используется ДНК, выделенная из лейкоцитарных клеток цельной крови человека. Для выделения ДНК используется любые доступные и валидированные наборы реагентов (пример набора: «ПРОБА-ГС-ГЕНЕТИКА» (ДНК-технология, Россия)) или другой набор), обеспечивающие выделение ДНК с концентрацией выше 5 нг/мкл из периферической крови. Процедура выделения ДНК производится по протоколу производителя этого набора.
2. Проведение полимеразной цепной реакции в режиме реального времени (ПЦР-РВ). В качестве реактивов для постановки ПЦР-РВ используется предназначенные для такого вида исследований реактивы (пример набора: набор «5X qPCRmix-HS» (Евроген, Россия)). Для обеспечения детекции сигнала при проведении ПЦР-РВ используются зонды (пример, зонды типа TaqMan). Подбор олигонуклеотидов (праймеров, зондов) осуществлялся путем использования одной из предназначенной для проведения такого рода деятельности программ (пример программного обеспечения: PrimerExpress v3 (Thermo, США)).
Синтез олигонуклеотидов производится на олигонуклеотидном анализаторе отечественного или импортного производства (пример синтезатора, Applied Biosistems 3900 (Thermo, США)). Для проведения ПЦР-РВ используется амплификатор, работающий в режиме реального времени (пример, амплификатор CFX96 c1000 Touch (Bio Rad, США) с детекцией продуктов амплификации в режиме реального времени). Для проведения ПЦР-РВ используется плашечный, пробирочный или матричный формат. В случае использования плашечного и пробирочного формата в каждую лунку или пробирку вносится реакционная смесь при постановке реакции. При использовании матричного формата при изготовлении матриц в узлах матриц иммобилизуются ПЦР-смеси, содержащие реагенты (праймеры, зонды, полимеразу, олигонуклеотиды), необходимые для проведения ПЦР-РВ. Суть молекулярно-генетической диагностики заключается в детекции наличия аллелей, содержащих патологический генотип, являющийся фактором риска развития патологии.
3. Формирование и выдача заключения по результатам молекулярно-генетического исследования.
Пример 1.
Пациентка L, 42 года. Диагностировано злокачественное новообразование молочной железы: C50.4 Рак правой молочной железы T2NxM0, IIa ст., ЭР 7б., ПР 3 б., HER2/neu 2+. Инфильтративный рак.
Ранее проведен анализ на 8 «частых мутаций» методом ПЦР с целью выявления генетической причины заболевания, который не выявил клинически значимых генетических вариантов.
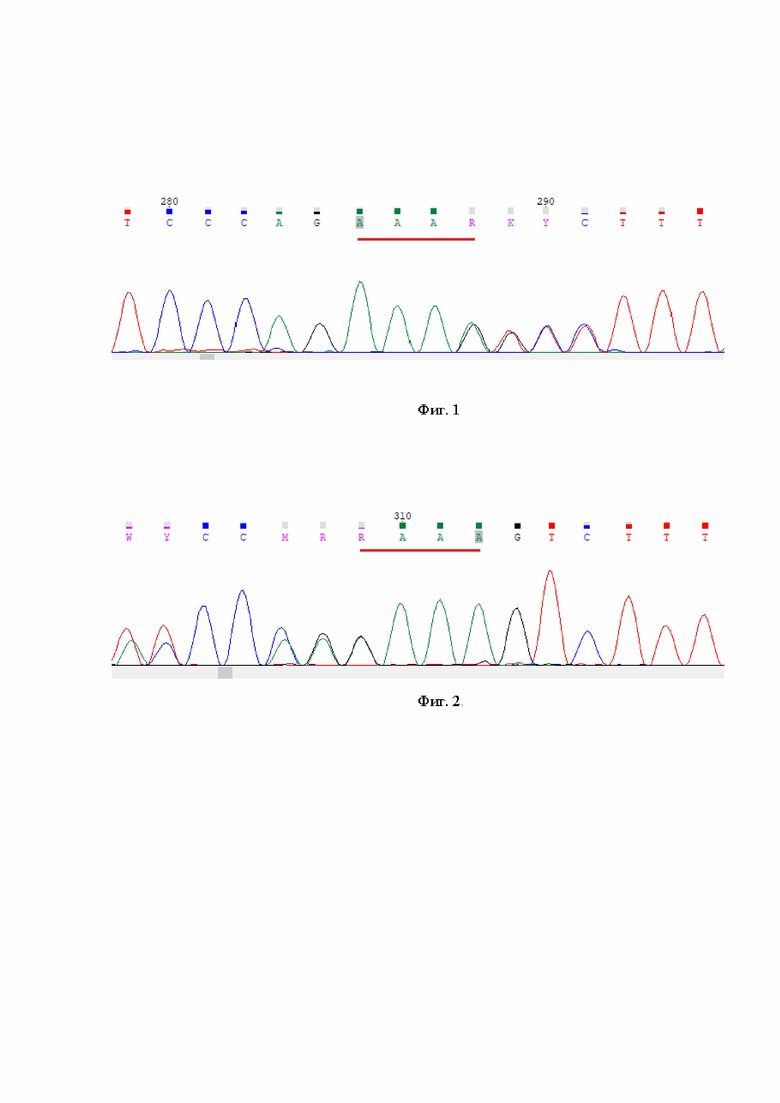
Нами проведено расширенное молекулярно-генетическое исследование согласно разработанному нами методу. Результат: выявлен ранее описанный патогенный вариант нуклеотидной последовательности гена BRCA2 chr13:g.32336627delA, (NM_000059.4):c.2272del (p.Ser758ValfsTer14), rs886040420 в гетерозиготном состоянии. Выявленный генетический вариант описан как ассоциированный с наследственным опухолевым синдромом (наследственный рак молочной железы и яичников, OMIM 612555) и высоким риском развития злокачественных новообразований молочной железы.
Выявленный генетический вариант валидирован референсным методом (секвенирование по Сэнгеру) (фиг. 1. Вариант гена BRCA2 chr13:g.32336627delA, (NM_000059.4):c.2272del, соответствующий rs886040420, выявлен в гетерозиготном состоянии, и фиг. 2. Результат подтвержден на реверс-последовательности.).
Таким образом, у пациентки диагностирован BRCA2-ассоциированный наследственный рак молочной железы.
Пример 2.
Пациентка B, 48 лет. Диагностировано злокачественное новообразование молочной железы: C50.8 Рак правой молочной железы T1mN0M0, Инфильтрирующая протоковая карцинома, G2.
Ранее проведен анализ на 8 «частых мутаций» методом ПЦР с целью выявления генетической причины заболевания, который не выявил клинически значимых генетических вариантов.
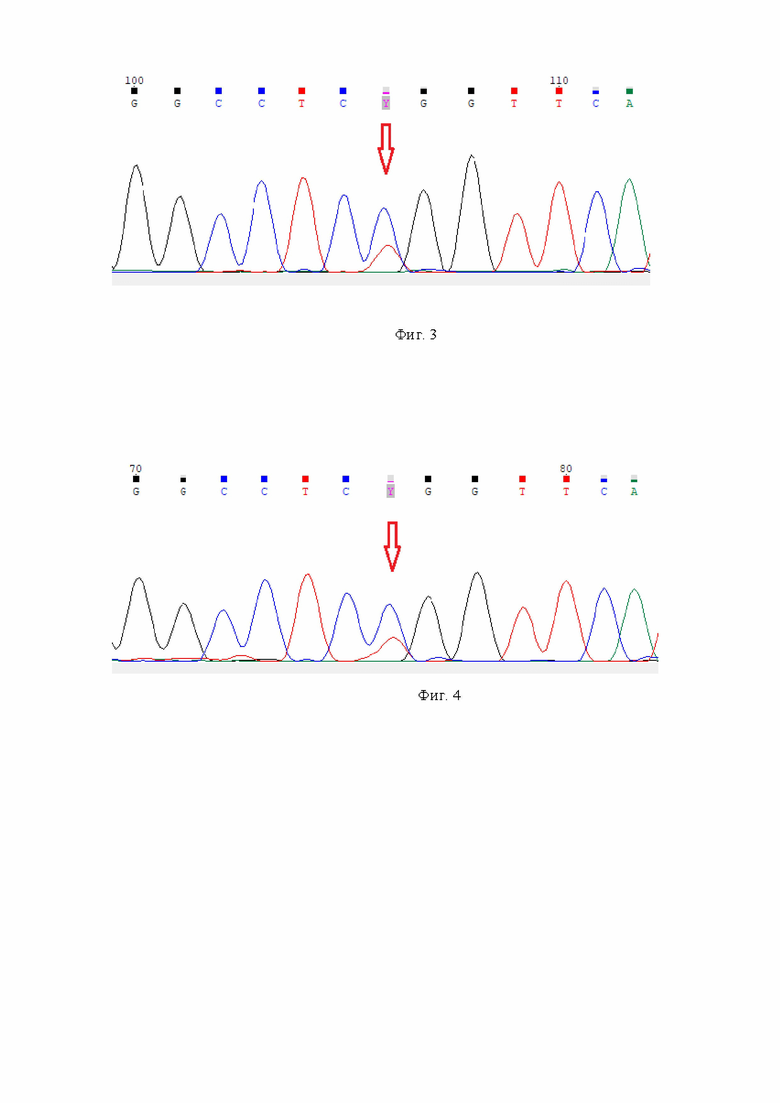
Нами проведено расширенное молекулярно-генетическое исследование согласно разработанному нами методу. Результат: выявлен патогенный вариант нуклеотидной последовательности гена TP53chr17:g.7674220C>T, (NM_000546.6):c.743G>A (p.Arg248Gln), rs11540652 в гетерозиготном состоянии. Патогенные гетерозиготные варианты гена TP53 ассоциированы с наследственным опухолевым синдромом (Ли-Фраумени, OMIM 151623) и повышенным риском развития злокачественных новообразований, в том числе молочной железы. Выявленный генетический вариант валидирован референсным методом (секвенирование по Сэнгеру) (фиг. 3. Вариант гена TP53chr17:g.7675070C>T, (NM_000546.6):c.542G>A, соответствующий rs11540652, выявлен в гетерозиготном состоянии и фиг. 4. Результат подтвержден на реверс-последовательности).
Таким образом, у пациентки диагностирован TP53-ассоциированный наследственный рак молочной железы (наследственный рак молочной железы в составе синдрома Ли-Фраумени).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫЯВЛЕНИЯ РЕЦЕССИВНЫХ ФАКТОРОВ НАСЛЕДСТВЕННОЙ ПРЕДРАСПОЛОЖЕННОСТИ К РАКУ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2013 |
|
RU2535157C1 |
| Способ молекулярно-генетической диагностики наследственных форм рака молочной железы | 2019 |
|
RU2702755C1 |
| Способ прогнозирования низкого риска развития рака молочной железы у женщин с высокопенетратными мутациями в генах BRCA1 и CHEK2 | 2022 |
|
RU2798666C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАСЛЕДСТВЕННОЙ ПРЕДРАСПОЛОЖЕННОСТИ К РАКУ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2012 |
|
RU2522501C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ЗЛОКАЧЕСТВЕННЫХ ЗАБОЛЕВАНИЙ МОЛОЧНОЙ ЖЕЛЕЗЫ И/ИЛИ ЯИЧНИКОВ У ПАЦИЕНТОВ ПОСЛЕ ТРАНСПЛАНТАЦИИ ПОЧКИ | 2023 |
|
RU2821583C1 |
| СПОСОБ ДИФФЕРЕНЦИРОВАННОГО ПРИМЕНЕНИЯ ДАННЫХ СЕКВЕНИРОВАНИЯ ДНК ДЛЯ ПАЦИЕНТОВ ПОСЛЕ ТРАНСПЛАНТАЦИИ ПОЧКИ | 2022 |
|
RU2803796C1 |
| Способ определения генетических маркеров для оценки полигенного риска развития рака молочной железы (гормон-негативного и гормон-позитивного подтипов) | 2020 |
|
RU2749465C1 |
| СПОСОБ АНАЛИЗА НАРУШЕНИЙ, СВЯЗАННЫХ С РАКОМ ЯИЧНИКОВ | 2008 |
|
RU2511408C2 |
| ОПРЕДЕЛЕНИЕ ПРЕДРАСПОЛОЖЕННОСТИ К РАКУ ПУТЕМ ИДЕНТИФИКАЦИИ ГЕНОТИПИЧЕСКИХ КОМБИНАЦИЙ СПЕЦИФИЧНЫХ ВАРИАНТОВ ГЕНОВ CYP1B1, BRCA2 И СНЕК2 | 2006 |
|
RU2470998C2 |
| Способ определения генетических маркеров для оценки полигенного риска развития гормон-позитивного подтипа рака молочной железы | 2020 |
|
RU2753002C1 |
Изобретение относится к биотехнологии. Группа изобретений относится к области медицины, а именно к онкологии и генетике, и может быть использована для выявления наследственной формы рака молочной железы (РМЖ) при первичном генетическом тестировании. Описана панель для определения наследственной формы рака молочной железы при первичном генетическом тестировании, которая включает 48 патогенных вариантов генов. Также описан способ выявления наследственной формы рака молочной железы, реализуется за счет использования созданной панели. Выявление у пациента хотя бы одного из патогенных вариантов, определяемых с помощью указанной панели, свидетельствует о наличии наследственной формы рака молочной железы. Благодаря созданной диагностической панели повышается точность выявления наследственной формы РМЖ при первичном генетическом тестировании за счет включения в панель наиболее распространенных по данным полногеномных исследований клинически значимых (патогенных) вариантов генов, ассоциированных с повышенным или высоким риском развития РМЖ. Созданная панель позволяет в рамках одного диагностического обследования в рамках первичного генетического тестирования выявить до 80-90% случаев наследственных форм РМЖ. 2 н.п. ф-лы, 4 ил., 4 табл., 2 пр.
1. Панель для определения наследственной формы рака молочной железы при первичном генетическом тестировании, включающая средства для обнаружения в образце крови пациента следующих патогенных вариантов:
2. Способ определения наследственной формы рака молочной железы, включающий использование панели по п. 1, где наличие у пациента хотя бы одного из патогенных вариантов, определяемых с помощью указанной панели, свидетельствует о наличии наследственной формы рака молочной железы.
| Е | |||
| И | |||
| Новикова, Е | |||
| А | |||
| Кудинова и др., ХАРАКТЕРИСТИКА BRCA-АССОЦИИРОВАННОГО РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ В РОССИЙСКОЙ ПОПУЛЯЦИИ, ВЕСТНИК РГМУ, 2021, номер 1, страницы 24-28 | |||
| И.С | |||
| Абрамов, Т.С | |||
| Лисица и др., ДИАГНОСТИКА НАСЛЕДСТВЕННЫХ ОПУХОЛЕВЫХ СИНДРОМОВ МЕТОДОМ ВЫСОКОПРОИЗВОДИТЕЛЬНОГО СЕКВЕНИРОВАНИЯ | |||
| ОПЫТ СОЗДАНИЯ БАЗЫ ДАННЫХ, Клиническая практика, 2021, |
Авторы
Даты
2025-01-14—Публикация
2024-08-28—Подача