Изобретение относится к медицине, а именно к хирургии грыж передней брюшной стенки.
До настоящего времени лечение послеоперационных вентральных грыж является одной из сложных проблем абдоминальной хирургии. Несмотря на внедрение в хирургическую практику новых способов реконструктивных операций с эндопротезированием дефекта брюшной стенки, рецидивы заболевания остаются еще пока на достаточно высоком уровне (Ермолов А.С., Благовестнов Д.А., Алексеев А.К., Упырев А.В., Ярцев П.А., Шляховский И.А., Корошвили В.Т., Бурбу А.В. Хирургическое лечение пациентов с большими и гигантскими послеоперационными вентральными грыжами // Хирургия. - 2019. - №9. - С. 38-43). Так, количество рецидивов при onlay - пластике достигает 41,4%, а при подапоневротическом расположении протеза - 22,4% (Тарасова Н.К., Дыньков С.М., Поздеев В.Н., Тетерин А.Ю., Османова Г.Ш. Анализ причин рецидива послеоперационных вентральных грыж / Хирургия. - 2019. - №10. - С. 36-42).
Одними из главных причин развития рецидива заболевания является инфекция области хирургического вмешательства, излишняя неконтролируемая интраоперационная травматичность операции при разделении анатомических компонентов в условиях деформируемых соединительнотканных структур брюшной стенки, нарушение процессов регенерации соединительной ткани, вызывающее атрофию и дряблость мышц, истончение апоневроза и, как следствие, нарушение функции как брюшной стенки, так и брюшной полости (Логинов В.И., Паршиков В.В., Касимов P.P., Бабурин А.Б. Современные механические способы интраоперационной профилактики инфекций области хирургического вмешательства // Новости хирургии. - 2015. - №.5. - С. 559-565; Суковатых Б.С, Валуйская Н.М., Праведникова Н.В., Герасимчук Е.В., Мутова Т.В. Профилактика послеоперационных вентральных грыж: современное состояние проблемы // Хирургия. - 2016. - №3. - С. 76-80; Паршиков В.В., Логинов В.И., Бабурин А.Б., Касимов P.P. Полувековой путь развития профилактики инфекционных осложнений в послеоперационных ранах // Медицинский вестник Башкорстана. - 2017. - Том 12, №1(67). - С. 82-92; Берещенко В.В., Надыров Э.А., Лызиков А.Н., Петренев Д.Р., Кондрачук А.Н. Модифицированный полипропиленовый эндо-протез для герниопластики: экспериментальная оценка эффективности его применения // Проблемы здоровья и экологии. - 2019. - №1(59). - С. 107-112; Паршиков В.В. Воспалительные осложнения протезирующей пластики брюшной стенки: диагностика, лечение и профилактика // Современные технологии в медицине. - 2019. - Том 11, №3. - С. 158-178; Basoglu М., Yildirgan M.I., Yilmaz I., Balik A., et al. Late complications of incisional hernias following prosthetic mesh repair. Acta Chir Belg. 2004; 104(4): 425-428). Это вызвало повышенный интерес к изучению количественных и качественных показателей строения и обмена соединительной ткани, формирующей полноценный рубец в области фасциальных слоев брюшной стенки (Кубышкин В.А., Агапов М.А., Давлятов М.Р., Какоткин В.В. Вентральные грыжи и экстрацеллюлярный матрикс соединительной ткани // Хирургия. - 2020. - №2. - С. 62-67).
Основными причинами уменьшения упруго-эластических и прочностных свойств соединительной ткани фасциальных слоев брюшной стенки являются следующие: 1) снижение соотношения между коллагенами I и III типов, приводящее к уменьшению диаметра коллагеновых волокон и снижению их механической устойчивости к разрыву (Henriksen N.A., Mortensen J.H., Lorentzen L., Agren M.S., Bay-Jensen A.C., Jorgensen L.N., Karsdal M.A. Abdominal wall hernias - A local manifestation of systemically impaired quality of the extracellular matrix. Surgery. 2016 July; 160(1): 220-227. https://doi.org/10.1016/i.surg.2016.02; Henriksen N.A., Ya-dete D.H., Sorensen L.T., Agren M.S., Jorgensen L.N. Connective tissue alteration in abdominal wall hernia. Br J Surg. 2011 Feb; 98(2): 210-219. https://doi.org/10.1002/bis.7339; Rosch R., Klinge U., Si Z., Junge K., Klosterhalfen B., Schumpelick V. A role for the collagen I/III and MMP-1/-13 genes in primary inguinal hernia? BMC Med Genet. 2002; 3:2; Иванов С.В., Иванов В.П., Иванов И.С., Барт И.И. Критерии прогнозирования грыжевой болезни // Вестник Национального медико-хирургического центра им. Н.И. Пирогова. - 2013 - №8(1). - С. 77-81); 2) снижение гидроксилирования остатков пролена и лизина, меди, а также нарушения активности фермента лизилоксидазы, принимающих участие в стабилизации формирования коллагеновых фибрилл и образовании дефектного коллагена (Henriksen N.A., Yadete D.H., Sorensen L.T., Agren M.S., Jorgensen L.N. Connective tissue alteration in abdominal wall hernia. Br J Surg. 2011 Feb; 98(2):210-219. https://doi.org/10.1002/bjs.7339; Kayaoglu H.A., Hazinedaroglu S.M., Bulent Erkek A., Kocaturk P.A., Kavas G.O., Aribal D. Comparison of the Plasma and Hernia Sac Tissue Copper Levels in Direct and Indirect Inguinal Hernia Patients. Biol Trace Elem Res. 2005; 108(1-3):53-59); 3) повышенная активность матриксных металлопротеиназ (ММР), участвующих в деградации коллагена (Henriksen N.A., Yadete D.H., Sorensen L.T., Agren M.S., Jorgensen L.N. Connective tissue alteration in abdominal wall hernia. Br J Surg. 2011 Feb; 98(2): 210-219. https://doi.org/10.1002/bjs.7339; Aren A. Gokce A.H., Gokce F.S., Dursun N. Roles of matrix metalloproteinases in the etiology of inguinal hernia. Hernia. 2011 Dec; 15(6):667-671. https://doi.org/10.1007/s10029-011-0846-5).
Убедительно показано, что прочность сформированного рубца в процессе заживления раны увеличивается параллельно повышению коллагена I типа, уменьшению концентрации фибронектина и коллагена III типа (Кубышкин В.А., Агапов М.А., Давлятов М.Р., Какоткин В.В. Вентральные грыжи и экстрацеллю-лярный матрикс соединительной ткани // Хирургия. - 2020. - №2. - С. 62-67). Решение данных проблем видится многими авторами в использовании сетчатых эндопротезов, изготовленных из монофиламентной полипропиленовой или политетрафторэтиленовой нити; применением фармакологических средств, стимулирующих ангиогенез или пролиферацию фибробластов и формирующие тем самым плотную соединительную ткань (Берещенко В.В., Надыров Э.А., Лызиков A.Н., Петренев Д.Р., Кондрачук А.Н. Модифицированный полипропиленовый эндопротез для герниопластики: экспериментальная оценка эффективности его применения // Проблемы здоровья и экологии. - 2019. - №1(59). - С. 107-112); в оптимизации технологии рассечения, отделения и соединения тканей в области хирургического вмешательства с оценкой критического сближения краев грыжевых ворот (снижение артериального давления на 15%, учащение пульса, увеличение давления сопротивления на вдохе, снижение сатурации свыше 10%, повышение уровня внутрибрюшного давления свыше 12 мм рт.ст.) (Кубышкин B.А., Агапов М.А., Давлятов М.Р., Какоткин В.В. Вентральные грыжи и экстра-целлюлярный матрикс соединительной ткани // Хирургия. - 2020. - №2. - С. 62-67; Черных А.В., Белянский К.Д., Закурдаев Е.И., Налетова Д.М. Клинико-анатомическое исследование нового способа уменьшения внутрибрюшного давления при протезирующей пластике срединных послеоперационных вентральных грыж передней брюшной стенки // Морфологические ведомости. - 2017. - Том 25. - №3. - С. 26-31; Ермолов А.С, Благовестнов Д.А., Алексеев А.К., Упырев А.В., Ярцев П.А., Шляховский И.А., Корошвили В.Т., Бурбу А.В. Хирургическое лечение пациентов с большими и гигантскими послеоперационными вентральными грыжами // Хирургия. - 2019. - №9. - С. 38-43; Логинов В.И., Паршиков В.В., Касимов P.P., Бабурин А.Б. Современные механические способы интраопераци-онной профилактики инфекций области хирургического вмешательства // Новости хирургии. - 2015. - №.5. - С. 559-565; Самарцев В.А., Гаврилов В.А., Паршаков А.А., Кузнецова М.В. Задняя сепарационная герниопластика TAR при послеоперационных вентральных грыжах W3 // Пермский медицинский журнал. - 2017. - Том XXXIV. - №1. - 2017. - С. 35-42).
Известен способ стимуляции процессов репаративной регенерации мягких тканей брюшной стенки и улучшения прочностных характеристик рубца за счет более интенсивной пролиферации и дифференцировки соединительнотканных структур и эпителия путем назначения в до- и послеоперационном периоде фармакологических препаратов пиримидинового ряда, например метилурацила, взятого нами за прототип (Г.Л. Билич. Стимуляция регенерации и защитных механизмов в детской хирургии. М.: Медицина, 1976. - 223 с; В.И. Русаков. Регуляция воспаления и регенерации в хирургии. Ташкент, 1971. - 376 с.; Машковский М.Д. Лекарственные средства: В 2-томах.-М.: Медицина, 1988. - Том 2. - С. 138-139). Метилурацил в плановой хирургии назначается за 2-3 дня до операции и в течение 6 дней после оперативного вмешательства по 0,5 гр. 3 раза в день.
К основным недостаткам прототипа относятся: крайне низкий регенеративный эффект, о чем свидетельствуют многолетние собственные наблюдения и литературные данные (Горбунов С.М. Анаболические препараты / В кн.: Аутодермопластика в клинической практике. - Казань: Полиграфиздат. - 1980. - С. 48-51; Ксимедон (научный сборник материалов экспериментальных и клинических исследований) Под ред. Г.А. Измайлова. - Казань: Изд-во ИОФХ им. А.Е. Арбузова КФАН СССР. - 1986. - 114 с.); отсутствие данных по влиянию препарата на повышение толерантности тканей к растяжению и деформационно-прочностных свойств послеоперационного рубца в фазе текучести и разрыва. Кроме этого, недостатком их применения являются возможные побочные явления, противопоказания к их назначению (Справочник Видаль 2009 [Электронный ресурс] - Режим доступа: http//www.webvidal.ru/2019/AV_1947.htm 6; Медицинский справочник лекарств [Электронный ресурс] / Мединфа. Медицинская энциклопедия. - Режим доступа: http//medinfa.ru/drug/11/1499/).
Целью изобретения является новое средство, повышающее деформационно--прочностные характеристики фасциальных слоев брюшной стенки, их толерантность к растяжению и эластичность., что позволяет повысить эффективность лечения.
Поставленная цель достигается путем применения в качестве фармакологического средства, повышающего деформационно-прочностные характеристики тканей брюшной стенки, их толерантность к растяжению и эластичность при достижении площадки текучести препарат пиримидинового ряда гидроксиэтилдиметилдигидропиримидин.
Выбор гидроксиэтилдиметилдигидропиримидина (Ксимедона) в качестве лекарственного средства, повышающего деформационно-прочностные характеристики тканей брюшной стенки и их толерантность к растяжению объясняется нами тем, что данный препарат по своему лечебному эффекту значительно превышает другие пиримидиновые производные, такие как метилурацил.
(Ксимедон. Под ред. Г.А. Измайлова. Казань: Изд-во ИОФХ им. А.Е. Арбузова КФАН СССР; 1986. - 114 с.; Измайлов С.Г., Измайлов Г.А., Аверьянов М.Ю., Резник B.C. Ксимедон в клинической практике. Н. Новгород: Изд-во НГМА, 2001.- 188 с.).
Интересной особенностью воздействия препарата является его способность регулировать коллагеногенез, препятствуя образованию келоидных рубцов (Измайлов Г.А., Шафиков И.З., Эвранова Г.Б. и др. Результаты клинических испытаний у взрослых в качестве противоожогового средства препарата Ксимедон в лекарственной форме - таблетки по 0,25 г в сравнении с метилурацилом. В кн.: Ксимедон. Казань: Изд-во ИОФХ им. А.Е. Арбузова КФАН СССР; 1986; с. 78-105). Доказана целесообразность использования гидроксиэтилдиметилдигидропиримидина в таблетированном виде как средства, стимулирующего процессы репаративной регенерации в тканях раны и повышающего неспецифическую резистентность организма к инфекции путем повышения функциональной активности нейтрофилов и их резервного потенциала. Выявленный эффект объясняется мембраностабилизирующим действием гидроксиэтилдиметилдигидропиримидина на лейкоциты (Измайлов С.Г. Профилактика гнойно-воспалительных осложнений послеоперационных ран в неотложной абдоминальной хирургии. Автореф. дис… докт. мед. наук: М; 1994). При этом нами установлено, что энтеральное применение гидроксиэтилдиметилдигидропиримидина выравнивает концентрацию плазменного фибронектина до нормы, что очень важно для созревания коллагеновых волокон, повышения их механической резистентности и прочности фасциальных слоев брюшной стенки (В.А. Кубышкин, М.А. Агапов, М.Р. Давлятов, В.В. Какоткин. Вентральные грыжи и экстрацеллюлярный матрикс соединительной ткани // Хирургия. - 2020. - №2. - С. 62-67).
В связи с этим нами высказана гипотеза, что энтеральное применение гидроксиэтилдиметилдигидропиримидина до- и после операции герниопластики вентральных грыж эндопротезированием позволит повысить деформационно-прочностные характеристики тканей области оперативного вмешательства, их толерантность к растяжению и эластичность в момент достижения ими не только площадки разрыва (предела прочности), но и площадки текучести (предел текучести), т.е. когда не наступает еще полного разрушения коллагеновых и эластических волокон, а происходит их частичная обратимая деформация. Такая превентивная подготовка ткани до операции к предстоящим нагрузкам при ее растяжении уменьшит ее разрушение и позволит закрыть грыжевой дефект максимально собственными тканями с минимальным разделением компонентов брюшного пресса и тем самым снизить травматичность операции, предупредив в последующем анатомо-функциональную недостаточность брюшной стенки и брюшной полости.
Гипотеза подтверждается проведенными экспериментальными исследованиями на животных на модели заживления линейных кожных ран (I) и ран желудка (II), ткань которого более чувствительна и подвержена к растяжению на различных участках. Кроме этого, учитывая замкнутую полость органа, методом пневмопрессии можно изучить влияние препарата на деформационные характеристики ткани не только в области формирующегося рубца, но и интактного участка органа.
I. Эксперимент выполнен на белых крысах самцах массой 0,15-0,18 кг, которые были распределены по группам в зависимости от решения поставленных задач. Каждое животное как до, так и после операции находилось в индивидуальной клетке в виварии при равных условиях.
Под эфирным наркозом животным удаляли шерстяной покров и после этого переходили к основному этапу операции - нанесению стандартных линейных кожных ран длиной 50 мм, осуществляемому разработанным нами устройством, выполненным в виде эластичного хирургического зажима, в губках которого сделаны продольные, сквозные совмещенные прорези. Перед нанесением разреза кожа обрабатывалась спиртом, йодом и покрывалась стерильной салфеткой. Весь этап операции проходил в асептических условиях. Для исключения негативного влияния на заживление раны затупленной режущей кромки инструмента нами использовались бритвенные лезвия "Нева", выпускаемые отечественной промышленностью. С помощью одной стороны лезвия разрез наносился однократно (Измайлов С.Г. Профилактика гнойно-воспалительных осложнений послеоперационных ран в неотложной абдоминальной хирургии: Дисс… докт. мед. наук. - Москва, 1994). Нанесение кожного разреза заключалось в следующем. Отступя на 60 мм от лопатки к хвосту, параллельно средней линии спины скальпелем наносилась резаная рана длиной 5-6 мм на всю глубину кожи. Затем через нанесенную рану проводили одну из плоских губок устройства и кожа фиксировалась путем сцепления рукояток за один из зубьев кремальер. После этого бритвенным лезвием "Нева" через сквозные совмещенные прорези наносили разрез и затем на расстоянии 10 мм друг от друга на образованную рану накладывали капроновые узловые швы. Во всех сериях опыта повязка на рану не применялась и усилие натяжения нити было одинаковым. Одному животному наносились две раны параллельно друг другу.
Животных умерщвляли под эфирным наркозом на 14-й и 21-й дни после операции, после чего производили забор тканей из области рубца для проведения тензиометрии, гистологического и гистохимического исследования. После эвтаназии выкраивался полнослойный кожный лоскут с полным захватом рубца. Затем с помощью острого лезвия перпендикулярно линии рубца по трафарету иссекались лоскуты кожи шириной 6-7 мм, длиной 40 мм (по 20 мм с каждой стороны рубца). Лоскуты кожи иссекались таким образом, чтобы в исследуемую ткань не попали участки швов. Измерение толщины лоскута по линии рубца выполнялось на микроскопе МБС-9 с ценой деления шкалы окуляра 0,05 мм.
Тензиометрия выполнялась на устройстве, изготовленном на базе силоизмерительного стенда для измерения усилий УИС К 80.47.00, позволяющем получить больше информации о течении раневого процесса путем оценки прочностных параметров с изученных диаграмм растяжения лоскута кожи с рубцом.
Для выявления различий в диаграммах растяжения тканей нами проведены для сравнения тензиометрические исследования деформации лоскутов здоровой кожи.
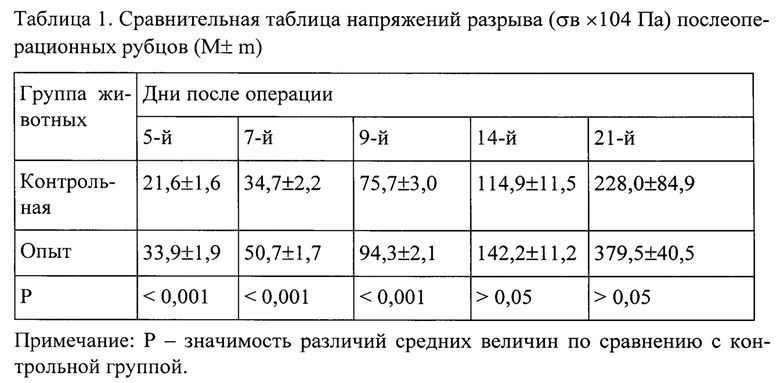
На фиг. 1. представлены диаграмма I растяжения лоскута здоровой кожи и диаграмма II растяжения кожного лоскута с рубцом. Анализ полученных диаграмм позволил выявить следующее.
Для тензиометрии здоровой кожи характерны два линейных участка 1 и 2, соединенных криволинейным участком 3. Участок 1 объясняется деформацией эластических и коллагеновых волокон, а более крутой участок 2 - деформацией преимущественно коллагеновых фибрилл вплоть до их разрушения (Kenedi R.M. The mechanical characteristics of skin and other soft tissue and their modelling. Aero-speice Medical Research Laboratory. Ohio Symposium on Biodynamic Models and their Applications Dayton (Ohio), 1970, Proceedings Paper №12, p. 383-402). Очевидно, что в начальной фазе деформации происходит в основном распрямление коллагеновой архитектоники - спиральной, ромбовидной и другой, напоминающее распрямление пружины. Дальнейшая деформация может быть иллюстрирована как растяжение уже выпрямленных коллагеновых волокон, составляющих основу кожи и являющихся наиболее прочными и менее растяжимыми.
На диаграмме рубцовой ткани выделяются три характерных прямолинейных участка 4, 5 и 6 с переходным криволинейным участком 7, а также площадки текучести 8 (промежуточный) и разрыва 9. Образование площадки текучести 8 объясняется тем, что после распрямления коллагеновых волокон происходит разрыв наиболее слабых вновь образованных коллагеновых волокон, а также разрыв менее прочных поперечных связей. На диаграмме растяжения это проявляется спадом кривой и появлением площадки текучести. Однако, оставшиеся распрямленные зрелые коллагеновые структуры вновь дают усилие, что проявляется на диаграмме в виде прямолинейного участка 6. Поэтому определение величины прочности рубца при достижении его площадки текучести указывает на зрелость соединительнотканной структуры новообразованной ткани. Таким образом, измерение напряжения рубца при текучести является более чувствительным и достоверным показателем, чем при разрыве, так как свидетельствует о полноценности и совершенстве коллагеногенеза, а также его равномерности по всей длине раны. Показатели упругости и эластичности ткани также целесообразнее определять при деформациях, меньших разрывных.
Основными показателями деформационно-прочностных свойств рубца являются:
σ - напряжение, характеризующее прочностные свойства и получаемое делением усилия Р на площадь поперечного сечения рубца;
ε - относительное удлинение, характеризующее эластичность и определяемое как результат деления разности растянутого лоскута 1 и начальной длины 10 к начальной длине 10, определяемое в процентах;
Е - модуль деформации (модуль упругости), определяемый как напряжение, необходимое для растяжения лоскута на единицу длины.
Наиболее информативным показателем, как по данным наших исследований, так и по результатам работ других авторов, является модуль упругости, который определяет сопротивление ткани деформированию без ее разрушения (Мишарев О.С., Абаев Ю.К., Прокопчук Н.Р. Изучение биомеханики заживления инфицированной раны в эксперименте // Клин. хир., 1985. - №1. - С. 48-49).
При анализе диаграмм растяжения лоскутов кожи констатировано, что гидроксиэтилдиметилдигидропиримидин оказывает заметное положительное влияние на ускорение заживления кожных ран, выражающееся в повышении прочности и упругости послеоперационных рубцов (табл.1).
Из табл. 1 видно, что напряжение разрыва в опытной группе на 5-й, 7-й и 9-й дни после операции по сравнению с контролем больше, соответственно, на 57, 31,6 и 19,7%. На 5-й день после операции прочность рубца у животных, получавших гидроксиэтилдиметилдигидропиримидин, была значительно выше, чем у контрольных. Обращает на себя внимание то, что начиная с 7-9-го дня после нанесения разреза происходило постепенное сглаживание прочности сращения краев раны между сопоставляемыми группами животных и на 14-й, 21-й дни различие в напряжении разрыва рубца было статистически не достоверным. Мы объясняем это тем, что гидроксиэтилдиметилдигидропиримидин проявляет свое действие на ранних сроках заживления раны, ускоряя процессы репаративной регенерации. Проведенные гистологические исследования и изучение упругости послеоперационного рубца, величина которой находится в прямой зависимости от интенсивности коллагеногенеза, подтверждали положительный эффект гидроксиэтилдиметилдигидропиримидина.
Модуль упругости в момент текучести послеоперационного рубца (Е2) в опытной группе (0,9±0,006)×103 Па выше на 33,3% по сравнению с контрольной (0,6±0,005)×103 Па), что указывает на более совершенную архитектонику вновь образованных коллагеновых волокон и прочность их поперечных связей. Модуль упругости при разрыве рубца (E1) в опытной группе (3,3±0,4)×103 Па по сравнению с контрольной (1,9±0,2)×103 Па больше на 42,1% (р<0,01), что свидетельствует о большем количестве организованных коллагеновых волокон, синтезированных под действием гидроксиэтилдиметилдигидропиримидина.
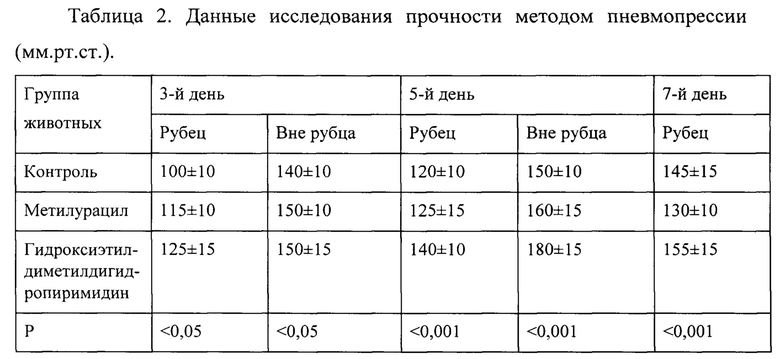
Из анализа диаграмм растяжения кожного лоскута с рубцом на 5-й день после операции выявлено (фиг. 2), что напряжение рубца у животных опытной группы при деформациях, меньших деформаций разрушения, σт составило (19,2±2,5)×104 Па, а в контрольной группе (11,4±1,6)×104 Па. Разница статистически значима в пользу гидроксиэтилдиметилдигидропиримидина (р<0,05). Это еще раз подтверждало, что у животных, получавших гидроксиэтилдиметилди-гидропиримидин, наблюдалось раннее образование коллагена в ране по сравнению с контрольной группой и процессы репаративной регенерации проходили равномерно по всей площади рубцовой ткани.
В группе животных с применением метилурацил а на 5-й день после операции напряжение разрыва рубца σв составило (26,6±2,0)×104 Па, а напряжение рубца при текучести σт=(12,2±1,7)×104 Па. Таким образом, по сравнению с метилурацилом напряжение рубца под действием гидроксиэтилдиметилдигидропиримидина при текучести больше на 36,5% (р<0,05), а при разрыве на 21,5% (р<0,05). Это свидетельствует о том, что гидроксиэтилдиметилдигидропиримидин по своим стимулирующим свойствам на процессы репаративной регенерации превосходит свой аналог - метилурацил.
Из приведенных результатов можно сделать вывод, что процессы репарации наиболее равномерно распределяются по всей длине раны в основной группе животных. Это подтверждается и характером разрыва послеоперационного рубца. Если в основной группе животных симметричность разрыва рубца наблюдали в более чем 92%, то в контроле (как с метилурацилом, так и без него) симметричность разрыва рубца наблюдалась лишь в 42% случаях. Это является немаловажным признаком, характеризующим качество репаративных процессов. Данные тензиометрии согласовывались с результатами гистологических исследований.
В контрольной группе животных на 5-й день раневого процесса происходило стягивание краев раны имелась в небольшом объеме грануляционная ткань. По ходу раневого канала отмечалась лейкоцитарная инфильтрация. На 9-й день эпидермальный регенерат разрастался. Грануляционная ткань становилась волокнисто-клеточной, выявлялись тонкие фуксинофильные коллагеновые волокна, располагающиеся в основном параллельно поверхности кожи. К 14-му дню втянутость рубца с поверхности оставалась. Коллагеновые волокна в дерме утолщались и сплетались в пучки. В область дефекта дермы продвигались волосяные луковицы и железы. В клеточном составе соединительнотканного регенерата начинали преобладать фибробласты и фиброциты. К 21-му дню рубец с поверхности оставался втянутым. Под эпидермисом формировался соединительнотканный каркас с преобладанием достаточно зрелых волокон, окрашивающихся фуксином, которые сплетались в пучки и образовывали сложную архитектонику. В глубине бывшего дефекта вновь образованные волокна переплетались с соседними коллагеновыми волокнами, образуя тесную связь.
В опытной группе животных, получавших гидроксиэтилдиметилдигидропиримидин, на 5-й день после операции в линейной ране отмечалось меньшее количество грануляционной ткани по сравнению с контрольной группой, где рана еще имела вид клеточно-волокнистой. Начинали образовываться нежные коллагеновые волокна. К 7-му дню коллагеновые волокна приобретали горизонтальную ориентацию. В клеточном составе имелись макрофаги и молодые фибробласты. К 9-му дню поверхность линейной раны покрывалась мощным эпителиальным пластом с погружными выростами. Грануляционная ткань становилась волокнисто-клеточной, коллагеновые волокна начинали сплетаться в пучки, рубец становился малозаметным. На 14-й день область бывшего разреза была трудно различима, волоконная часть дермы оставалась несколько разреженной и имелось довольно много кровеносных сосудов.
Морфологическое исследование кожных ран позволяет сделать вывод об ускорении репаративного процесс при введении гидроксиэтилдиметилдигидропиримидина, что проявляется в линейной ране уменьшением разрастания грануляционной ткани и ускорением коллагеногенеза. По нашим данным, гидроксиэтилдиметилдигидропиримидин оказывал заметное стимулирующее влияние на образование коллагена в послеоперационной ране, объясняющее повышение прочностных и упругих характеристик рубцовой ткани.
Итак, по данным экспериментальных исследований, гидроксиэтилдиметилдигидропиримидин существенно способствует не только увеличению упруго-прочностных характеристик сращения краев кожной раны при энтеральном способе введения, но и повышает растяжимость (эластичность) ткани, что подтверждают исследования тканевой структуры в фазе текучести препарата. Выраженность стимулирующего действия гидроксиэтилдиметилдигидропиримидина на заживление ран максимально проявлялась в первые 5-7 дней после повреждения. Проведенные исследования также подтвердились данными, полученными на модели обширной плоскостной раны, где наблюдалось ускорение коллагеногенеза (Измайлов С.Г., Горбунов С.М., Измайлов Г.А. и соавт. Доклиническое исследование ксимедона // Антибиотики и химиотерапия. - 1999. - №8. - С. 12-17).
II С целью изучения влияния гидроксиэтилдиметилдигидропиримидина на деформационно-прочностные характеристики тканей и их растяжимость проведены исследования на модели заживления ран пищеварительного тракта 116 кроликах самцах массой 2-3,5 кг. Под внутривенным гексеналовым наркозом моделировались повреждения желудка и двенадцатиперстной кишки в одинаковых условиях. В послеоперационном периоде с первого дня животным внутрижелудочно через зонд вводился гидроксиэтилдиметилдигидропиримидин в виде 10% водного раствора из расчета 100 мг/кг в сутки (1-я подгруппа опытной группы, 45 животных). Вторая подгруппа опытной группы (38 животных) в послеоперационном периоде получала 0,9% водный раствор метилурацила в таких же дозировках. Контрольную группу составили 33 кролика, получавших в послеоперационном периоде физиологический раствор хлорида натрия.
На 3, 5 и 7-е сутки после эвтаназии животных проводилось исследование деформационно-прочностных параметров тканей желудка и двенадцатиперстной кишки в зоне ушитых повреждений методом пневмопрессии.
После применения гидроксиэтилдиметилдигидропиримидина на 5-е сутки разрывы стенки желудка и двенадцатиперстной кишки в зоне рубца получены у 83% животных при пневмопрессии до 180 мм рт. ст. В подгруппе, получавшей метилурацил, у 57,1% животных на 5-е сутки рубец выдержал пневмопрессию в среднем 125±15 мм рт.ст. В контрольной группе животных данные показатели были заметно меньшими, чем во второй и особенно в первой подгруппах опытной группы. На 7-е сутки показатели пневмопрессии распределились следующим образом. В группе животных, получавших метилурацил, разрывы желудка и двенадцатиперстной кишки в области рубца получены у 80%) животных при пневмопрессии до 130±10 мм рт.ст., а в группе, получавшей гидроксиэтилдиметилдигидропиримидина - у 76,6% при давлении до 155±15 мм рт.ст. (р<0,001).
Представляют интерес данные, полученные при анализе разрывов желудка и двенадцатиперстной кишки вне ранее нанесенного повреждения, полученные при различном давлении. На 5-е сутки в группе животных, получавших гидроксиэтилдиметилдигидропиримидина, разрывы вне рубца наблюдались в среднем при пневмопрессии 180±15 мм рт.ст., на 7-е сутки эти цифры колебались в пределах от 170 до 240 мм рт. ст. (в среднем 200±10 мм рт.ст.).
В группе животных, получавших метилурацил, в большинстве случаев разрывы вне рубца получены на 5-е сутки при пневмопрессии 160±15 мм рт.ст., а на 7-е сутки эти показатели составили в среднем 180±10 мм рт. ст. (табл. 2). Данные, полученные при анализе этого явления в контрольной группе животных, получавших физиологический раствор хлорида натрия, практически не отличались от результатов применения метилурацила (табл. 2).
На основании результатов проведенных экспериментальных исследований установлено, что ушитые повреждения желудочно-кишечного тракта после применения гидроксиэтилдиметилдигидропиримидина имеют гораздо большую прочность, чем после применения метилурацила. Данное положение убедительно доказывается тем, что рубец после применения гидроксиэтилдиметилдигидропиримидина разрывается в большем проценте случаев при давлении, существенно превышающем таковое при применении метилурацила, как на 5-е, так и на 7-е сутки.
Устойчивость тканей желудка и двенадцатиперстной кишки к пневмопрессии после использования гидроксиэтилдиметилдигидропиримидина в большей степени проявлялась на более ранних сроках, чем после применения метилурацила. Данные, полученные при анализе результатов на 7-е сутки, показывают, что различия между группами, получавшими гидроксиэтилдиметилдигидропи-римидин и метилурацил, начинают постепенно нивелироваться.
Данные, полученные при анализе разрывов вне рубца, свидетельствуют о том, что гидроксиэтилдиметилдигидропиримидин в большей степени, чем метилурацил увеличивает упруго-прочностные и эластические параметры здоровых участков стенки желудка, значительно повышая ее толерантность к растяжению при деформациях, меньших разрывных. Положительное влияние гидроксиэтилдиметилдигидропиримидина на заживление ран желудка подтвердилось проведенными гистологическими исследованиями.
Полученные результаты в I и II серии эксперимента на животных в полной мере подтвердили высказанную нами гипотезу и явились основанием для назначения гидроксиэтилдиметилдигидропиримидина до- и после операции у больных с послеоперационными вентральными грыжами в качестве лекарственного средства, повышающего деформационно-прочностные характеристики тканей брюшной стенки, их толерантность к растяжению, увеличивая при этом коэффициент эластичности ткани при достижении ими предела текучести.
Применение средства осуществляют следующим образом:
С целью повышения деформационно-прочностных характеристик послеоперационного рубца и паравульнарных тканей к разрывным нагрузкам, а также их толерантности к растяжению в фазе текучести за 10 дней до операции - грыжесечения по поводу послеоперационной вентральной грыжи, больному назначают энтерально гидроксиэтилдиметилдигидропиримидин. После предоперационной подготовки больному выполняют оперативное вмешательство.
Обследовано 20 пациентов с большими срединными послеоперационными вентральными грыжами, которые были разделены на основную и контрольную группу. Больные по полу, возрасту, размерам грыжевого дефекта, выраженности подкожной жировой клетчатки и сопутствующим заболеваниям были репрезентативны. Во всех случаях планировалось выполнение протезирующей герниопластики методом «Sublay». В основной группе использовали предложенное средство. В контрольной группе применяли классическую методику, взятую нами за прототип, с назначением в до- и послеоперационном периоде метилурацила. Сроки назначения изучаемых препаратов в группах исследования не отличались друг от друга.
Клиническое применение предложенного средства у 10 больных с большими послеоперационными вентральными грыжами позволило во всех случаях выполнить аппаратно-фармакологическую сепарацию компонентов брюшной стенки под контролем показателей критического сближения краев раны и сблизить края грыжевого дефекта «встык» без повышения внутрибрюшного давления, закончив операцию по методике «Sublay». Послеоперационное осложнение наблюдали у 1 больного в виде серомы.
Выполнение операций у 10 больных по классической методике закончили в 6 случаях по способу «Inlay» и только в 4 - по методике «Sublay». В послеоперационном периоде серомы встретили у 3 больных, гематомы - у 2 пациентов. Клинико-экспериментальные исследования предлагаемого средства при хирургическом лечении послеоперационных вентральных грыж убедительно свидетельствуют о значительных преимуществах перед прототипом, которые сводятся к следующим отличиям от известного:
- выполнение разделения компонентов брюшной стенки в условиях аппаратной тракции, а также естественной противотракции под синхронным контролем изменения внутрибрюшного давления и повышения деформационно-прочностных характеристик фасциальных слоев брюшной стенки, их толерантности к растяжению и эластичности с помощью гидроксиэтилдиметилдигидропиримидина, позволяет закрыть грыжевой дефект максимально собственными тканями с минимальным разделением компонентов брюшного пресса, снизить травматичность операции и добиться более высокого лечебного эффекта;
- энтеральное применение гидроксиэтилдиметилдигидропиримидина до- и после операции повышает упруго-прочностные характеристики и эластичность тканей брюшной стенки, их толерантность к растяжению при деформациях, меньших деформаций разрушения (предел текучести), что позволяет подготовить компоненты брюшной стенки к предстоящим механическим нагрузкам как во время сепарации тканевых структур, так и после оперативного вмешательства, сопровождающееся повышением внутрибрюшного давления;
- гидроксиэтилдиметилдигидропиримидин, обладая выраженным стимулирующим влиянием на процессы физиологической регенерации и репарации, повышая деформационно-прочностные свойства поврежденных и не поврежденных тканей, их толерантность к растяжению и эластичность, позволяет максимально закрыть грыжевой дефект собственными тканями, что является профилактикой анатомо-функциональной недостаточности брюшной стенки и брюшной полости.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1. Диаграмма растяжения кожных лоскутов: I - здоровой кожи, II - кожи с рубцом.
Фиг. 2. Диаграммы растяжения кожных лоскутов с рубцом на 5-й день после операции: I - контрольной группы, II - опытной группы (с применением ксимедона). По оси абсцисс - относительное удлинение е, по оси ординат - напряжение (σт - предел текучести, σв - предел прочности).
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО И СПОСОБ ДЛЯ КОМБИНИРОВАННОГО АППАРАТНО-ФАРМАКОЛОГИЧЕСКОГО РАЗДЕЛЕНИЯ МЫШЕЧНО-ФАСЦИАЛЬНЫХ КОМПОНЕНТОВ БРЮШНОЙ СТЕНКИ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПОСЛЕОПЕРАЦИОННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ | 2021 |
|
RU2824801C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ ПРИЖИВЛЕНИЯ СЕТЧАТОГО ИМПЛАНТАТА ПОСЛЕ ПЛАСТИКИ ВЕНТРАЛЬНЫХ ГРЫЖ | 2019 |
|
RU2712210C1 |
| Способ оптимизации регенерационных процессов в послеоперационной ране после секторальной резекции молочной железы | 2022 |
|
RU2792555C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ОПТИМИЗАЦИИ ПРИЖИВЛЕНИЯ СИЛИКОНОВОГО ИМПЛАНТА ПОСЛЕ РЕКОНСТРУКТИВНО-ВОССТАНОВИТЕЛЬНОЙ ОПЕРАЦИИ НА МОЛОЧНОЙ ЖЕЛЕЗЕ | 2022 |
|
RU2788259C1 |
| СПОСОБ СТИМУЛИРОВАНИЯ ЗАЖИВЛЕНИЯ РАН | 1993 |
|
RU2082402C1 |
| СПОСОБ НАЛОЖЕНИЯ КИШЕЧНОГО ШВА ПРИ ФОРМИРОВАНИИ АНАСТОМОЗОВ НА ОРГАНАХ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2005 |
|
RU2321363C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ ВЕНТРАЛЬНЫХ ГРЫЖ | 2002 |
|
RU2215484C2 |
| УСТРОЙСТВО ДЛЯ ДРЕНИРОВАНИЯ ПОЛОСТИ РАНЫ ПРИ ПЛАСТИКЕ ГРЫЖЕВОГО ДЕФЕКТА БРЮШНОЙ СТЕНКИ | 2020 |
|
RU2749546C1 |
| Способ оптимизации регенерационных процессов и профилактики затяжного плеврального выпота после анатомической резекции легкого | 2024 |
|
RU2831662C1 |
| Способ профилактики осложнений надапоневротической пластики послеоперационной вентральной грыжи | 2017 |
|
RU2645245C1 |
Изобретение относится к медицине, а именно к хирургии, герниопластике. Применяют гидроксиэтилдиметилдигидропиримидин в качестве фармакологического средства, повышающего деформационно-прочностные характеристики фасциальных слоев брюшной стенки, их толерантность к растяжению и эластичность в до- и послеоперационном периоде. Применение указанного препарата при лечении грыж передней брюшной стенки позволяет снизить травматичность операции и повысить эффективность лечения. 2 ил., 2 табл., 2 пр.
Применение в до- и послеоперационном периоде гидроксиэтилдиметилдигидропиримидина в качестве средства, повышающего деформационно-прочностные характеристики фасциальных слоев брюшной стенки, их толерантность к растяжению и эластичность.
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ ПРИЖИВЛЕНИЯ СЕТЧАТОГО ИМПЛАНТАТА ПОСЛЕ ПЛАСТИКИ ВЕНТРАЛЬНЫХ ГРЫЖ | 2019 |
|
RU2712210C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНЫХ ПРОЦЕССОВ ПРИ ИМПЛАНТАЦИИ СВЕРХЛЕГКОГО ПОЛИПРОПИЛЕНОВОГО ЭНДОПРОТЕЗА В БРЮШНУЮ СТЕНКУ | 2018 |
|
RU2681109C1 |
| CN 105228555 B, 25.08.2017 | |||
| ЛУКОЯНЫЧЕВ Е.Е | |||
| и др | |||
| Фармакологическое сопровождение периоперационного периода имплантации сетчатого полипропиленового протеза (экспериментальное исследование) | |||
| Исследования и практика в медицине | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| ПАРШИКОВ В.В | |||
| и др | |||
| Прочностные характеристики | |||
Авторы
Даты
2025-01-21—Публикация
2023-08-01—Подача