Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно к хирургии трахеи и бронхов, и может быть использовано для восстановления проходимости дыхательных путей при лечении стенозирующих злокачественных опухолей трахеи и бронхов, включая опухолевые стенозы области бифуркации трахеи с вовлечением главных бронхов и бронхов 1-3 порядков.
Уровень техники
Злокачественные заболевания легких являются одной из наиболее часто встречающихся проблем среди пациентов с заболеваниями бронхолегочной системы (18,4%). Первичные и метастатические злокачественные новообразования центральных дыхательных путей являются не только часто диагностируемым видом (11,6%), но и основной причиной смертности от онкологических заболеваний, продолжительность которых оценивается до 5-ти лет (18,4%). При этом прорастание опухоли в просвет дыхательных путей в 20-30% случаев осложняется формированием стеноза трахеи и главных бронхов и приводит к дыхательной недостаточности, которая является причиной летальных исходов в 40% случаев. [1) Bray F., Ferlay J., Soerjomataram I., Siegel R.L., Torre L.A., Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424; 2) Umar Z., Haseeb Ul Rasool M., Hosna A.U., Parikh A., Ariyaratnam J., Sandhu J.K., Ashfaq S., Ahmed N., Khan J., Trandafirescu T. Malignant Airway Obstruction and Endobronchial Stent Placement: A Systematic Review on the Efficacy and Safety. Cureus. 2023;15(6):e40912; 3) Guibert N., Mazieres J., Marquette C.H., Rouviere D., Didier A., Hermant C. Integration of interventional bronchoscopy in the management of lung cancer. Eur Respir Rev. 2015;24(137):378-391]. В 75-85% случаев опухолевый стеноз располагается в трахее, в области карины, в главных и промежуточных бронхах, реже (15-25%) встречается мультифокальный характер (сложный стеноз) [Saxena P., Ram B., Dhooria S., Prasad K.T., Muthu V., Aggarwal A.N., Agarwal R., Sehgal I.S. Central airway obstruction due to endoluminal tumors: Experience from a tertiary care center in North India. Lung India. 2022;39(5):481-483]. Медиана выживаемости пациентов со злокачественной обструкцией дыхательных путей составляет 3,5 месяца (диапазон от 0 до 21)[ 1)Okiror L., Jiang L., Oswald N., Bille A., Rajesh P., Bishay E., Steyn R., Naidu B., Kalkat M. Bronchoscopic Management of Patients With Symptomatic Airway Stenosis and Prognostic Factors for Survival. Ann Thorac Surg. 2015;99(Issue 5):1725-1730 2)Li Y., Zhu M., Chen J., Ren K., Wan L., Lu H., Ren J., Han X. Single Y-shaped tracheal self-expandable metallic stent for emergent carinal stenosis combined with stenosis of the right main and intermediate bronchi. Medicine. 2020;99(22):e20498 3)Saxena P., Ram B., Dhooria S., Prasad K.T., Muthu V., Aggarwal A.N., Agarwal R., Sehgal I.S. Central airway obstruction due to endoluminal tumors: Experience from a tertiary care center in North India. Lung India. 2022;39(5):481-483].
У резектабельных пациентов с локализованной опухолью легкого или бронхов преимущественным выбором метода оперативного лечения остается резекция опухоли, тогда как лучевая и химио терапия используется для неоперабельных пациентов и в послеоперационном периоде для пациентов с неполной резекцией. Однако при прорастании опухоли в просвет трахеи и бронхов преимущественным методом остается эндоскопическое лечение: реканализация просвета дыхательных путей и установка трахеального или бронхиального стента для поддержания проходимости дыхательных путей. В последние годы спектр эндоскопического лечения при злокачественных стенозах трахеи и бронхов значительно расширился. Существуют различные методы реканализации просвета: механическая, лазерная, криодеструкция, эндоскопическая баллонная дилатация. Независимо от метода восстановления проходимости дыхательных путей на заключительном этапе лечения проводят эндоскопическое эндопротезирование с использованием различных стентов, которые отличаются конструктивным выполнением, включая форму, материал, размеры, наличие или отсутствие покрытий, и др. Таким образом, на сегодняшний день существуют различные средства и методы реканализации и стентирования области бифуркации трахеи и бронхов, однако до настоящего времени остается высоким процент осложнений после проведенного лечения, что связано с анатомическими особенностями взаимоотношения бронхов с окружающими тканями. Особую сложность при лечении вызывают опухолевые стенозы бронхов, локализованные в бронхах 1-3 порядков или имеющие мультифокальный характер, что связано с затруднением подбора стентов, которые обеспечили бы адекватную вентиляцию интактных бронхов при перекрытии их стентом, а также технические трудности установки стентов в бронхи мелкого калибра (2-3-го порядка). В связи с этим актуальным является дифференциальный подход к лечению больных с опухолевыми стенозами трахеи и бронхов, исходя из полученных данных комплексного предоперационного обследования, и определение тактики эндоскопического лечения, эффективность которого зависит от многих факторов, включая локализацию и протяженность опухолевого стеноза.
Из уровня техники известен способ билатерального стентирования нижних дыхательных путей при бифуркационном стенозе, основанный на доставке и установке саморасширяющихся металлических стентов в дыхательные пути в области бифуркации трахеи [Takeda T, Itano H, Fukita S, Saitoh M, Takeda S. Bilateral self-expandable metallic stents for lung cancer involving the carina. Respirol Case Rep. 2013;1(2):48-51.]. Билатеральное стентирование может быть осуществлено с использованием, так называемой, «the kissing-stents» техники. При выполнении гибкой бронхоскопии размещают кожные маркеры на уровне бифуркации трахеи и на 3 см краниальнее. Поочередно вводят две 0,035-дюймовые струны-проводники в правый и левый главные бронхи. После удаления бронхоскопа доставочные устройства продвигают по струнам-проводникам поочередно в правый и левый главный бронх под рентгеноскопическим контролем, подгоняя проксимальные и дистальные концы доставочных устройств. Поочередно производят установку стента в правом главном бронхе под рентгеноскопическим контролем и, после полного его раскрытия, устанавливают стент в левом главном бронхе, ориентируя его проксимальный конец на одном уровне с проксимальным концом установленного стента в правом главном бронхе. Однако данный способ доставки, осуществляемый без жесткой бронхоскопии, сопряжен с воздействием на голосовые связки, что сопровождается неприятными ощущениями у пациента, приводит к высокому риску развития дыхательной недостаточности. Кроме того, в способе установку и раскрытие стентов производят поочередно, сначала в главном бронхе одного легкого, затем другого, что усложняет возможность коррекции положения стентов при неудовлетворительном их раскрытии по отношению друг к другу. Кроме того, данный способ предполагает установку металлических саморасширяющихся стентов, имеющих сплошное покрытие полимерной пленкой с внешней или внутренней стороны. При такой конструкции раскрытие каудального края стента в промежуточном бронхе сопровождается перекрытием устья правого верхнедолевого бронха и вызывает нарушение проходимости потока воздуха в легочную ткань.
Из уровня техники также известно стентирование нижних дыхательных путей при опухолевом стенозе саморасширяющимися стентами (Ultraflex). Данные стенты снабжены полимерным покрытием в центральной части (Zaryab Umar, Muhammad Haseeb Ul Rasool, Asma U Hosna, Avish Parikh, Jonathan Ariyaratnam, Jasmine K Sandhu, Salman Ashfaq, Nazaakat Ahmed , Jawad Khan, Theo Trandafirescu. Malignant Airway Obstruction and Endobronchial Stent Placement: A Systematic Review on the Efficacy and Safety [Journal List Cureus v.15(6); 2023 Jun]). Данные стенты подходят для стентирования бифуркационного стеноза и при распространении на бронхи 1-2 порядка. Данные стенты легко адаптируются под анатомию бронха и могут быть установлены без жесткой бронхоскопии. Однако при эндоскопическом лечении пациентов с опухолевым стенозом трахеи и бронхов с использованием данных стентов возможен повторный стеноз за счет прорастания опухолевой тканью непокрытых концов стента, вызывая при этом сложности с их удалением. Кроме того, при использовании данных стентов существуют риски перекрытия интактных бронхов покрытой частью стента и нарушения вентиляции здоровых сегментов легкого, что в последующем приводит к ателектазу данных участков.
Из уровня техники известны различные критерии распространенности бронхиальных анастомотических стенозов, используемые при выборе конкретного способа лечения. В частности, известны критерии, предложенные P. Thistlethwaite (2008) [А.М. Гасанов, М.Ш. Хубутия, Е.А. Тарабрин, Ш.Н. Даниелян, Т.Э. Каллагов, И.У. Ибавов, В.Г. Котанджян. Эндоскопическое лечение бронхиальных осложнений после трансплантации легких. Хирургия. Журнал имени Н.И. Пирогова, 2021, №9 с. 12-18], которые включают в себя 4 типа стенозов: 1-тип характеризуется коротким сегментом стеноза, локализованным в пределах 1 см от линии шва анастомоза; 2-тип - стеноз, охватывающий анастомоз и более 1 см бронха от линии шва; 3 тип - неанастомотическое расположение бронхиальных стенозов; 4 тип - диффузный стеноз бронхов. Однако данные критерии не предусматривают злокачественную этиологию стеноза и локализацию стеноза, поэтому не могут быть положены в основу выбора тактики эндоскопического лечения пациентов с опухолевым стенозом бифуркации трахеи и бронхов 1-3 порядка.
Наиболее близким к заявленному способу является способ билатерального эндопротезирования нижних дыхательных путей при бифуркационном стенозе (RU 2784980 C1), включающий проведение через канал эндоскопа двух струн-проводников в главные бронхи правого и левого легкого, заведение по струнам-проводникам под рентгеноскопическим контролем двух металлических саморасширяющихся стентов, содержащих покрытия из полимерной пленки, и снабженных рентгеноконтрастными метками, с последующим раскрытием стентов. При этом в способе используют стент, предназначенный для установки в главном бронхе правого легкого, с отверстиями, расположенными, по меньшей мере, на участке сопряжения данного стента с устьем правого верхнего долевого бронха. При размещении кожных маркеров дополнительно определяют уровни каудального края стенозов и локализации устья правого верхнего долевого бронха с последующим совмещением рентгеноконтрастных меток с упомянутыми маркерами при заведении стентов по струнам-проводникам. Раскрытие двух стентов производят одновременно с совмещением краниальных краев двух стентов в трахее на одном уровне и размещением отверстий стента в устье правого верхнего долевого бронха. Способ позволяет обеспечить расширение, восстановление и поддержание проходимости дыхательных путей, вентиляцию дистальных отделов бронхов обоих легких, предотвратить сужение дыхательных путей и угрозу асфиксии, восстановить и поддержать дренажную функцию бронхов обоих легких. Однако данный способ предназначен для использования при бифуркационном стенозе и не может быть экстраполирован на стенозы, вызванные опухолевым процессом и имеющие другую локализацию.
Технической проблемой, решаемой заявленным изобретением, является выбор тактики эндоскопического лечения злокачественного стеноза в зависимости от локализации опухоли в просвете бронха, включая область бифуркации трахеи с вовлечением главных бронхов и локального стеноза бронхов 1-3 порядков.
Раскрытие изобретения
Технический результат, достигаемый при использовании заявленного изобретения, заключается в повышении эффективности эндоскопического лечения пациентов с опухолевыми стенозами области трахеи и бронхов, включая стенозы области бифуркации трахеи с вовлечением главных бронхов и бронхов 1-3 порядков, с использованием саморасширяющегося металлического стента с покрытием с внешней и/или внутренней стороны, снабженного перфорацией (отверстиями), при сокращении времени, затрачиваемом на установку стентов.
Технический результат достигается выбором тактики лечения в зависимости от локализации и протяженности опухолевого стеноза, а именно,
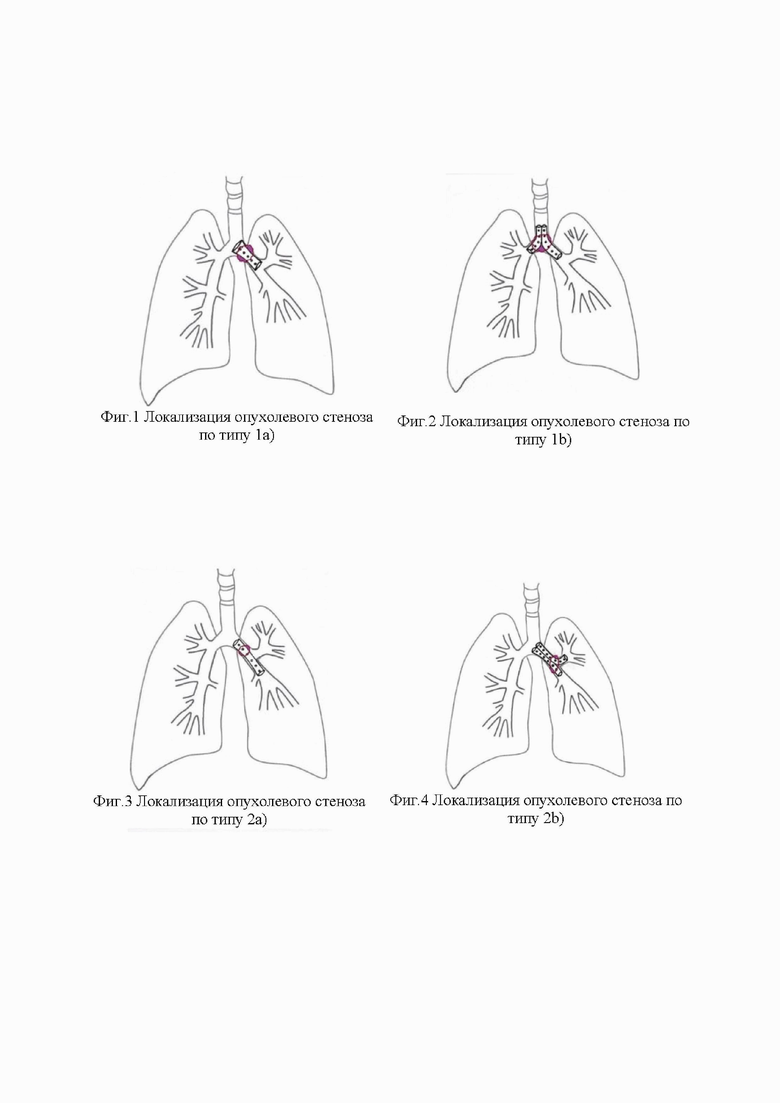
- при локализации опухолевого стеноза в области бифуркации трахеи (1-й тип) на уровне бифуркации трахеи с распространением на один (правый или левый) главный бронх (1а тип), проводят стентирование пораженного главного бронха одним стентом, не перекрывая интактные главный и долевой бронхи; в случае распространения опухолевого стеноза на оба (правый и левый) главные бронхи (1b тип) проводят билатеральное стентирование двумя стентами с расположением проксимальных концов стентов в просвете интактной части трахеи на одном уровне, дистальных концов стента в левом и правом главных бронхах на уровне междолевых шпор, и последующим одновременным раскрытием стентов;
- при локализации опухолевого стеноза в главном бронхе (2-й тип), в случае, когда опухоль не затрагивает междолевую шпору бронха (слева) или шпору верхнедолевого бронха (справа) (2а тип) проводят стентирование пораженного бронха одним стентом, который устанавливают с расположением дистального конца стента в просвете долевого бронха, а проксимального конца - на уровне карины, при этом вентиляция интактного долевого бронха осуществляется через перфоративные отверстия в стенте; в случае расположения опухоли с вовлечением междолевой шпоры бронхов (слева) или шпоры верхнедолевого верхнедолевого бронха (справа) (2b тип) проводят билобарное стентирование с одновременным заведением в пораженный бронх двух стентов с расположением проксимальных концов стентов в просвете главного бронха на одном уровне; и последующим одновременным раскрытием стентов;
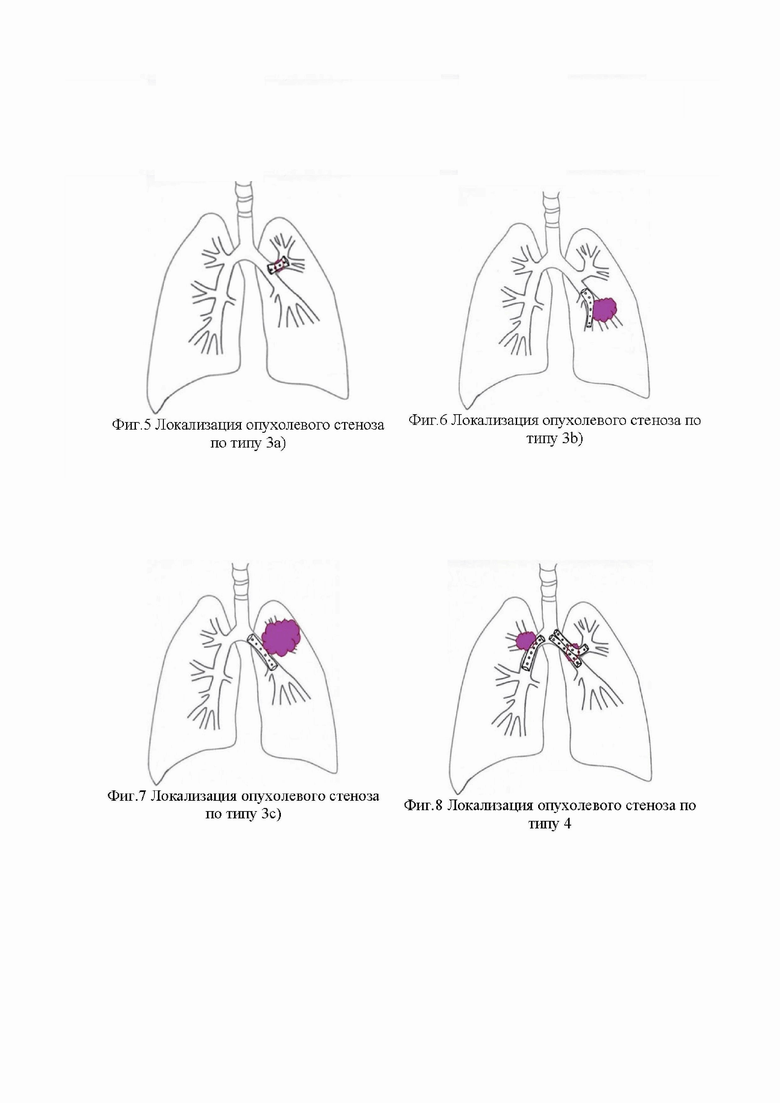
- при локализации опухолевого стеноза в долевом бронхе (3-й тип) в одном долевом бронхе без вовлечения сегментарных бронхов (справа) (3а тип) проводят стентирование одним стентом с расположением его дистального конца, не перекрывая сегментарные бронхи, или перекрывая 1 сегментарный бронх, и установкой проксимального конца на уровне междолевой шпоры, не перекрывая интактный долевой бронх; при локализации опухоли в долевом бронхе с распространением на два и боле сегментарных бронха (3b тип) проводят стентирование одним стентом с расположением его дистального конца в интактном сегментарном бронхе с перекрытием пораженных сегментарных бронхов, и проксимального конца на уровне междолевой шпоры, при перекрытии интактных сегментарных бронхов их вентиляция осуществляется через перфоративные отверстия в стенте; в случае распространения опухолевого стеноза на все сегментарные бронхи и на междолевую шпору бронха (3c тип) проводят стентирование интактного долевого бронха с перекрытием пораженного долевого бронха;
- в случае мультифокальной локализации опухоли, когда опухолевый стеноз расположен в просвете разных бронхов (1-3 порядка), с вовлечением или без области бифуркации трахеи (4-й тип) стентируют все интактные бронхи с перекрытием пораженных бронхов.
Во всех перечисленных вариантах расположения опухолевого стеноза (1 - 4 типов) для эндопротезирования используют саморасширяющийся металлический стент с покрытием с внешней и/или внутренней стороны, снабженный перфорацией (отверстиями), при этом содержащий отверстия на участке сопряжения данного стента с устьями сегментарных бронхов при билобарном стентировании двух и более долей одного легкого для разрешения дыхательной недостаточности; или содержащего отверстия на участке сопряжения данного стента с устьями сегментарных бронхов при стентировании локально одного долевого бронха, с перекрытием сегментарных бронхов или без перекрытия, с сохранением их вентиляции.
Заявленный способ основан на использовании новой совокупности признаков, в числе которых выявленные критерии, связанные с локализацией и распространением опухолевого стеноза, и связанные с ними приемы по установке стентов, обеспечивающие достижение наилучшего лечебного эффекта. При этом предложены новые приемы в лечении опухолевого стеноза при выполнении эндоскопических операций при сложных стенозах бронхов с вовлечением и обструкцией более одного бронха 1-3 порядка (4 тип), а также при локализации опухоли в главном бронхе с вовлечением междолевой шпоры бронхов (слева) или шпору верхнедолевого бронха (справа) (2b тип), которые направлены на одномоментное стентирование двух и более долевых бронхов или главного и долевого бронха одного легкого. При использовании разработанной тактики лечения возможно выполнение одномоментного селективного стентирования бронхов 1-3 порядков, селективное стентирование одного бронха 3 порядка без нарушения вентиляции интактных сегментов этой же доли легкого; при стентировании бронхов 1-3 порядков одного легкого, сохраняется возможность вентиляции интактного легкого; одномоментное раскрытие стентов обеспечивает одинаковую проходимость при полном раскрытии.
Краткое описание чертежей
Изобретение поясняется чертежами, где на фигурах 1 - 8 представлены варианты стентирования бифуркации трахеи и бронхов 1-3 порядка в зависимости от локализации и распространенности опухолевого стеноза.
Осуществление изобретения
Заявляемое решение предназначено для эндоскопического лечения опухолевых стенозов бифуркации трахеи, главных и промежуточного бронхов.
При выявлении у пациента опухолевого стеноза в области бифуркации трахеи с вовлечением главных бронхов и бронхов 1-3 порядков определяют его локализацию.
Операцию проводят под эндотрахеальным наркозом с помощью высокочастотной искусственной вентиляции легких (ВЧ ИВЛ). Для интубации трахеи используют тубус ригидного бронхоскопа KARL STORZ №12. Манипуляции выполняют с помощью видеоэндоскопической системы, например, Olympus EXERA III, видеобронхоскопа Olympus BF-Н 190 с диаметром рабочего канала 2.8, рентгеновской установки ZiehmImaging.
Всем пациентам с кровотечением или высоким риском кровотечения предварительно выполняют эндоваскулярную эмболизацию бронхиальных артерий микроэмболами.
При невозможности провести эндоскоп за зону сужения первым этапом выполняют бронхографию, при которой определяют интактные бронхи, оценивают протяженность стеноза и степень сужения просвета бронхов, а также расстояние между дистальным краем стеноза и шпорой интактного долевого бронха. Для этого через канал эндоскопа проводят катетер за зону стеноза дыхательных путей, далее поочередно выполняют бронхографию, определяют уровни каудального края стенозов и локализацию сегментарных бронхиальных, размещают кожные маркеры в этих зонах.
Вторым этапом после бронхографии и визуальной оценки состояния бронхов, селективно под рентгенологическим контролем в выбранные бронхи через катетер заводят одну или несколько струн-проводников диаметром 0,25 инч в зависимости от локализиации опухоли, которые фиксируют снаружи, при этом каждую струну отмечают меткой для определения в каком бронхе она расположена, при этом метки устанавливают на коже для определения локализации и границ распространения опухоли в трахее и бронхах.
Для восстановления проходимости бронхов может быть использован гибридный саморасширяющийся покрытый металлический стент с дополнительными перфоративными отверстиями по типу Multi-Hole, с помощью которых обеспечивается проходимость интактных сегментарных бронхов. Кроме того, они обеспечивают антимиграционную функцию, а диаметр доставочного устройства позволяет провести эндопротез через канал эндоскопа. В заявленном способе может быть использован саморасширяющийся покрытый металлический стент с дополнительными перфоративными отверстиями, выполненный в соответствии с патентом на полезную модель RU218278.
Третьим этапом по струне-проводнику и под рентгенологическим контролем через канал гибкого эндоскопа заводят доставочное устройство стента. По каналу бронхоскопа эндопротез заводят по струне-проводнику в главный, сегментарный или долевой бронх в зависимости от данных, полученных при бронхографии. Установку и раскрытие стента проводят под рентгенологическим и эндоскопическим контролем.
После установки стентов производят контроль их положения с помощью бронхоскопа. При необходимости положение стентов может быть скорректировано с помощью биопсионных щипцов при ригидной либо гибкой бронхоскопии. При неполном раскрытии стента после эндопротезирования, для оценки интактных бронхов бронхоскопия может быть выполнена с помощью SpyScope диаметром 3.3 мм фирмы Boston Scientific, который позволяет выполнить диагностику в бронхах мелкого калибра с одномоментной санацией.
После раскрытия стента выполняют санацию стерильным физиологическим раствором бронхов, расположенных дистальнее стеноза. При перекрытии интактных бронхов, оценивают наличие перфоративных отверстий в стенте в проекции устья бронха.
Тактику установки стента и их количество определяют в зависимости от данных бронхографии и локализации стеноза в просвете бронха. Варианты стентирования в зависимости от локализации опухолевого стеноза представлены на фигурах 1 - 8, а именно:
при локализации опухоли в области карины с вовлечением одного главного бронха, выполняют селективное стентирование главного бронха (фиг.1);
при локализации опухоли в области карины с вовлечением обоих главных бронхов, выполняют билатеральное стентирование главных бронхов (фиг.2);
при локализации опухоли в главном бронхе без вовлечения междолевой шпоры, выполняют селективное стентирование главного бронха, дистальный край устанавливают в один из интактных долевых бронхов (фиг.3);
при локализации опухоли в главном бронхе без вовлечения междолевой шпоры, выполняют билобарное стентирование долевых бронхов, основанное на заведении в область стеноза двух металлических саморасширяющихся стентов с полимерным покрытием и отверстиями, с последующим их одновременным раскрытием (фиг.4);
при локализации опухоли в долевом бронхе, без вовлечения сегментарных бронхов, селективно выполняют стентирование долевого бронха, дистальный край стента устанавливают на уровне слияния сегментанных бронхов (фиг.5);
при локализации опухоли в долевом бронхе с вовлечением на один и более сегментарных бронхов селективно выполняют стентирование долевого бронха, дистальный край стента устанавливают в один из интактных сегментарных бронхов (фиг.6);
при локализации опухоли в долевом бронхе, с вовлечением всех сегментарных бронхов и междолевую шпору выполняют стентирование интактного долевого бронха с перекрытием пораженного бронха (фиг.7);
при локализации опухоли мультифокально в разных бронхах выполняют стентирование двумя и более стентами (фиг.8).
Стенты используют длиной, позволяющей не выходить за пределы пораженных бронхов, при этом вентиляцию здорового легкого осуществляют путем высокочастотной подачи воздуха насыщенным кислородом с частотой 120 вдохов в минуту.
Стентирование проводят с визуализацией интактных бронхов до полного раскрытия стентов для оценки адекватности вентиляции и санации бронхов, при этом бронхоскопию выполняют с помощью Spy-Scope Discover диаметром эндоскопа 3,3 мм.
На третьи сутки после проведения операции выполняют контрольную КТ ОГК и трахеобронхоскопию для оценки разрешения ателектаза, стояния и раскрытия стентов.
В частности, при билобарном стентировании долевых бронхов одного легкого селективную бронхографию каждого долевого бронха одного легкого выполняют через просвет катетера, заведенного за зону стеноза по струне-проводнику. По данным бронхографии выявляют наиболее крупный сегментарный бронх с прямым ходом для позиционирования дистального края стента по выбранной траектории. Установка стента в сегментарный бронх не вызывает нарушения вентиляции перекрытых стентом интактных сегментарных бронхов, за счет наличия в нем перфоративных отверстий. Для селективного введения доставочных устройств стентов осуществляют маркировку струн (используют либо струны разного цвета, либо маркировку кожуха, в которой располагается струна-проводник). При билобарном стентировании проксимальные края стентов позиционируют на одном уровне в проекции устья главного бронха пораженного легкого, не перекрывая второй главный бронх или просвет трахеи.
Заявленный способ апробирован в условиях отделения эндоскопии и внутрипросветной хирургии и торакального отделения Научно-исследовательского института скорой помощи им. Н.В. Склифосовского г. Москва. На основании проведенных исследований выявлены критерии, связанные с локализацией опухолевого стеноза бронхов, и оказывающие существенное влияние на выбор тактики лечения.
За период с сентября 2022 по настоящее время эндоскопическое эндопротезирование при опухолевом стенозе бифуркации трахеи и бронхов 1-3 порядка выполнено 15 (100%) пациентам. Результаты эндоскопического стентирования представлены в Таблице 1.
На момент поступления у пациентов с дыхательной недостаточностью одышка по шкале mMRC 1 степени отмечалась у 3 пациентов (20%), 2 степени- у 3 (20%), 3 степени- у 6 (40%), 4 степени- у 3 (20%).
У 9 (60%) пациентов по КТ ОГК при поступлении отмечался ателектаз легких с развитием постобтурационной пневмонии: долевой - 7 (46,6%), сегментарный - 1 (6,7%), тотальный- 1 (6.7%). У 3 (20%) пациентов отмечался гидроторакс, объем жидкости варьировал от 500 до 1500 мл.
Таблица 1. Результаты стентирования
пациентов
операции
Наиболее часто (46.6%) выполнялось билобарное стентирование пациентам с локализацией опухолевого стеноза в главном бронхе с распространением на междолевую шпору. Интраоперационных осложнений не отмечалось. Наиболее длительным по времени было эндопротезирование при мультифокальном расположении опухолевого стеноза.
После эндоскопического стентирования у всех пациентов из исследуемой группы отмечалось разрешения дыхательной недостаточности или снижение одышки до 1 степени «по шкале mMRC». На 1-3 сутки после операции ателектаз легких полностью разрешился у 8 (53.6%) пациентов. В одном случае у пациента с локализацией опухоли в области бифуркации трахеи, с полным ателектазом легкого и прорастанием опухоли в паренхиму всех сегментов доли легкого, после стентирования сохраняется долевой ателектаз, но при этом выраженность одышки снизилась с 4 до 1 степени.
При анализе результатов проведенного исследования было выявлено, что локализация опухолевого стеноза в бронхах имеет огромное значение для выбора правильной тактики эндоскопического лечения. Выбор правильной тактики лечения с установкой в зону стеноза саморасширяющегося покрытого стента с перфорацией является важным аспектом при лечении пациентов с опухолевым стенозом, который позволяет снизить риск развития таких послеоперационных осложнений как ателектаз интактных сегментов легкого и миграция стента.
Клинический пример 1. Лечение опухолевого стеноза по типу 1а).
Пациент Л. 50 лет, после перенесенной коронавирусной инфекции в течение года отмечал жалобы на одышку при минимальной физической нагрузке и кашель с трудноотделяемой мокротой. По данным из анамнеза у пациента хроническая обструктивная болезнь легких. Стаж курения более 40 лет по 1-2 пачка/день.
При поступлении: общее состояние пациента удовлетворительное, сознание ясное. Дыхание самостоятельное, через естественные дыхательные пути, частота дыхательных движений (ЧДД) 19 в мин; АД 124\75 мм.рт.ст.; ЧСС 70 в мин; Сатурация 89%.
При компьютерной томографии (КТ) органов грудной клетки (ОГК) выявлено объемное образование корня правого легкого обтурирующее верхнедолевой и среднедолевой бронхи, с сужением просвета нижнедолевого бронха и левой легочной артерии и с прорастанием в клетчатку средостения.
При трахеобронхоскопии опухоль локализована на уровне бифуркации трахеи, с распространением на правый главный бронх. Во время исследования была выполнена щипцовая биопсия. По результатам морфологического исследования в полученном материале признаки хронического бронхита с плоскоклеточной метаплазией эпителия.
Пациенту выполнено эндоскопическое оперативное вмешательство. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, выполнена ригидная трахеоскопия тубусом ригидного бронхоскопа №12: в проекции правого главного бронха с переходом на карину определяется экзофитная опухоль, суживающая просвет до 2-3 мм. Первым этапом была выполнена бронхография: под рентген контролем по струне-проводнику, в просвет правого главного бронха заведен катетер и выполнено контрастирование. При контрастировании определяется полный блок на уровне средней трети главного бронха правого легкого с расширенными сегментарными бронхами нижней и средней долей. Вторым этапом на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения. Следующим этапом по каналу бронхоскопа по ранее установленной струне-проводнику в просвет промежуточного бронха заведено доставочное устройство и установлен бронхиальный саморасширяющийся покрытый металлический стент HANAROCTENT Multi-Hole диаметром 10 мм, длиной 60 мм. Дистальный край стента определяется на 0,5-1,0 см выше бифуркации правого легкого. После раскрытия стента, была выполнена санация бронхов стерильным физиологическим раствором в объеме 10 мл.
После стентирования жалобы на одышку исчезли, дыхание самостоятельное. Физикальные данные при выписке: АД 124\75 мм.рт.ст.; ЧСС 75 в мин.; ЧДД 18 в мин.; Сатурация 97-98%. При КТ ОГК и трахеобронхоскопии, выполненной на третьи сутки после операции состояние стента - удовлетворительное.
Пациент был выписан на 4-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства с контрольным эндоскопическим осмотром через 1 месяц.
Клинический пример 2. Лечение опухолевого стеноза по типу 1б).
Пациент С. 64 лет госпитализирован в хирургическое отделение НИИ СП им Н. В. Склифосовского, с жалобами на нарушение проходимости твердой пищи по пищеводу, умеренную боль в эпигастрии и одышку в покое. По данным из анамнеза у пациента дыхательная недостаточность 2 степени, хроническая обструктивная болезнь легких, в связи с этим длительно принимает будесонид вместе с сальметеролом и тиотропия бромид. Стаж курения более 50 лет по 1-2 пачка/день. Также наблюдается по поводу гипертонической болезни с максимальным уровнем САД 170 мм. рт. ст. Амбулаторно принимает лизиноприл и верапамил.
При поступлении: общее состояние пациента средней тяжести, сознание ясное. Дыхание самостоятельное, через естественные дыхательные пути, частота дыхательных движений (ЧДД) 18 в мин: АД 160\100 мм.рт.ст.; ЧСС 90 в мин; сатурация 96%.
По данным КТ ОГК выявлено образования заднего средостения с вовлечением в процесс прикорневых отделов правого легкого, верхней и средней доли с признаками ателектазирования.
При эзофагогастродуоденоскопия (ЭГДС): просвет грудного отдела пищевода на расстоянии 27,0 см от резцов сужен более 2\3 за счет сдавления извне, протяженностью 7,0 см.
При трахеобронхоскопии: в области карины по передней стенке определяется экзофитная опухоль, переходящая на правый и левый главные бронхи с сужением их просвета. Во время исследования была выполнена щипцовая биопсия. По результатам морфологического исследования в полученном материале мелкоклеточный рак.
Пациенту с новообразованием заднего средостения, с прорастанием образования в главные бронхи и сдавлением пищевода, с целью проведения энтерального питания, была выполнена чрескожная эндоскопическая гастростомия (ЧЭГ).
Пациенту выполнено эндоскопическое стентирование бронхов. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12: Первым этапом была выполнена бронхография: под рентген контролем по струне-проводнику, в просвет правого главного бронха заведен катетер и выполнено контрастирование. Далее на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения трахеи и бронхов. Под рентген контролем по струне-проводнику поочередно в просвет главных бронхов заведены доставочные устройства и установлены саморасширяющиеся полностью покрытые стенты HANAROCTENT Multi-Hole диаметром 10 мм, длиной 80 мм. При осмотре через стенты, определяются интактные устья сегментарных бронхов. Дистальные края стентов ориентированы в просвет нижнедолевых бронхов. Проксимальные края стентов расположены на 1,5 см дистальнее карины. Последним этапом выполнялась санация бронхов стерильным физиологическим раствором в объеме 10 мл.
В послеоперационном периоде лечение пациента осложнилось развитием средне-долевой пневмонии. Проводилась антибактериальная, ингаляционная, симптоматическая терапия с положительным эффектом.
При контрольной трахеобронхоскопии положение бронхиальных стентов - удовлетворительное.
При КТ ОГК после стентирования долевой ателектаз сохраняется, но при этом выраженность одышки снизилась с 4 до 1 степени. Физикальные данные при выписке: АД 132\80 мм.рт.ст.; ЧСС 82 в мин.; ЧДД 18 в мин.; Сатурация 96%.
Пациент выписан на 11 сутки после операции с рекомендациями дальнейшего динамического наблюдения, контрольной бронхоскопией через месяц и приема пищи через гастростому.
Клинический пример 3. Лечение опухолевого стеноза по типу 2а).
Пациент К. 69 лет с опухолью средне-грудного отдела пищевода, был госпитализирован в НИИ скорой помощи им. Н. В. Склифосовского с жалобами на затруднение прохождения твердой пищи по пищеводу, одышку при умеренной физической нагрузке и кровохарканье.
Из анамнеза известно, что пациент длительное время страдает гипертонической болезнью и хронической обструктивной болезнью легких.
Перенесенные заболевания: рак нижней трети пищевода сT3N0M0, аденома простаты.
При поступлении общее состояние: удовлетворительное. Дыхание самостоятельное, через естественные дыхательные пути, частота дыхательных движений (ЧДД) 19 в мин: АД 115\75 мм.рт.ст.; ЧСС 71 в мин; сатурация 91%.
При КТ признаки объемного образования средне-грудного отдела пищевода с прорастание в левый главный бронх с сужением их просвета.
При трахеобронхоскопии просвет левого главного бронха сужен до 0,4 см, за счет полуциркулярного разрастания экзофитной опухоли. Из образования взята биопсия, после биопсии определяется выраженная кровоточивость и с целью остановки кровотечения была выполнена инстилляция раствора адреналина, с положительным эффектом. По результатам морфологического исследования в полученном материале плоскоклеточный рак (неороговевающий).
При ЭГДС определяется протяженный субкомпенсированнный опухолевый стеноз грудного отдела пищевода.
Пациенту выполнено эндоскопическое оперативное вмешательство. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12. Первым этапом была выполнена бронхография: под рентген-контролем по струне-проводнику, в просвет верхне- и нижнедолевого бронхов левого легкого заведен катетер и выполнено контрастирование: контрастируются расширенные сегментарные бронхи нижней и верхней доли. Далее на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения трахеи и бронхов. Под рентген контролем по струне-проводнику в просвет главного бронха заведен и установлен саморасширяющийся полностью покрытый стент HANAROCTENT Multi-Hole диаметром 10 мм, длиной 60 мм. При осмотре через стент определяются интактные устья сегментарных бронхов. В проекции устья верхнедолевого бронха левого легкого проецируются 3-4 перфоративных отверстия для вентиляции верхне-долевых бронхов. Проксимальный край стента расположен на уровне карины. Последним этапом была выполнена санация бронхов стерильным физиологическим раствором.
На 2 сутки после стентирования пациенту с прогрессивным сужением просвета пищевода из-за прорастания опухоли пищевода, с целью проведения энтерального питания, была выполнена чрескожная эндоскопическая гастростомия (ЧЭГ).
После стентирования жалобы на одышку исчезли. Физикальные данные при выписке: АД 115\75 мм.рт.ст.; ЧСС 71 в мин.; ЧДД 18 в мин.; Сатурация 98%. При контрольном КТ ОГК и трахеобронхоскопии состояние стентов удовлетворительное.
Пациент был выписан на 8-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц, и рекомендациями по уходу за гастростомой.
Клинический пример 4. Лечение опухолевого стеноза по типу 2б).
Пациентка Ф. 51 года, ранее находившаяся на лечении в другом учебным учреждении с диагнозом: острая инфекция верхних дыхательных путей, средней тяжести, осложнившаяся левосторонней полисегментарной пневмонией, была госпитализирована в НИИ скорой помощи им. Н. В. Склифосовского, с жалобами на одышку при умеренной физической нагрузке.
Из анамнеза у пациентки центральное образование левого легкого, обтурирующее просвет левого главного бронха с ателектазом левого легкого.
При поступлении: общее состояние пациента средней тяжести, сознание ясное. Дыхание самостоятельное, через естественные дыхательные пути, ослаблено в левых отделах, частота дыхательных движений (ЧДД) 19 в мин; АД 124\70 мм.рт.ст.; ЧСС 88 в мин; сатурация 93%.
При дообследовании: на КТ ОГК картина объемного образования в прикорневом отделе левого легкого, с распространением в средостение и в верхнюю и нижнюю долю левого легкого с признаками ателектазирования, левосторонний гидроторакс (объемом около 500см3), эмфизема легких и гидроперикард.
При трахеобронхоскопии определяется экзофитная опухоль обтурирующий просвет левого главного бронха. Во время исследования была выполнена щипцовая биопсия. По результатам морфологического исследования в полученном материале мелкоклеточный рак.
Пациенту выполнено эндоскопическое стентирование бронхов. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12. Просвет дистальной части левого главного бронха, в области бронхиальной шпоры полностью обтурирован экзофитной опухолью. Первым этапом под рентген-контролем по струне-проводнику в просвет верхне- и нижнедолевого бронхов заведен катетер и выполнено контрастирование: контрастируются расширенные сегментарные бронхи нижней и верхней доли. Далее на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения. Под рентген-контролем по струне-проводнику поочередно в просвет нижне- и верхнедолевого бронхов заведены доставочные устройства и установлены саморасширяющиеся полностью покрытые стенты HANAROCTENT Multi-Hole диаметром 8 мм, длиной 60 мм. При осмотре через стенты, определяются интактные устья сегментарных бронхов. Проксимальные края стенты расположены на 1,5 см дистальнее карины. Последним этапом была выполнена санация бронхов стерильным физиологическим раствором.
После стентирования жалобы на одышку исчезли, дыхание самостоятельное. Физикальные данные при выписке: АД 115\89 мм.рт.ст.; ЧСС 76 в мин.; ЧДД 18 в мин.; Сатурация 97-98%. При контрольном КТ ОГК и трахеобронхоскопии ателектаз полностью разрешился, состояние стентов - удовлетворительное.
Пациентка была выписана на 3-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц.
Клинический пример 5. Лечение опухолевого стеноза по типу 3а).
Пациент Ю. 62 лет, поступил с диагнозом легочное кровотечение и с жалобами на одышку при физической нагрузке, которая беспокоит его в течение последнего месяца.
При поступлении: общее состояние пациента средней тяжести, сознание ясное. Дыхание самостоятельное, через естественные дыхательные пути, частота дыхательных движений (ЧДД) 18 в мин: АД 120\80 мм.рт.ст.; ЧСС 78 в мин; Сатурация 90%.
При трахеобронхоскопии просвет нижнедолевого бронха левого легкого обтурирован экзофитным опухолевым образованием с признаками состоявшегося легочного кровотечения.
При КТ ОГК определяется образование в нижней доле левого легкого с полостью распада.
В экстренном порядке пациенту на 1-е сутки после госпитализации выполнена эмболизация левой бронхиальной артерии микроэмболами Bearing nsPVA 500-710 мкм.
После эмболизации левой бронхиальной артерии пациенту выполнено эндоскопическое стентирование. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12: выполнено контрастирование сегментарных бронхов нижней доли левого легкого. При контрастировании определяются расширенные сегментарные бронхи нижней доли левого легкого, и связь бронха В8 с полостью деструкции. Размер полости при бронхоскопии составляет 3.0х2.5 см. Далее на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения. По струне-проводнику под рентген-контролем по каналу эндоскопа в проекцию устьев бронхов В9 и В10, с перекрытием бронха В8 доставлен саморасширяющийся металлический полностью покрытый стент HANAROCTENT Multi-Hole диаметром 8 мм, длиной 30 мм. Проксимальный край стента расположен на 1,0 см дистальнее устья бронха В6. По стенту отмечается поступление гнойного содержимого. Выполнена санация бронхов стерильным физиологическим раствором в объеме 60 мл.
Интраоперационно была выполнена резекция экзофитной порции опухолевого образования и отправлена на гистологическое исследование, после резекции отмечается выраженная кровоточивость, которая остановилась после инстилляции гемостатическим раствором адреналина. По данным гистологического исследования в пределах полученного материала морфологическая картина соответствует ороговевающей плоскоклеточной карциноме с участками изъязвления.
После стентирования жалобы на одышку исчезли, дыхание самостоятельное. Физикальные данные при выписке: АД 130\80 мм.рт.ст.; ЧСС 83 в мин.; ЧДД 18 в мин.; Сатурация 97-98%. При КТ ОГК и трахеобронхоскопии, выполненной на третьи сутки после операции, состояние стента - удовлетворительное.
Пациент выписан на 3-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц.
Клинический пример 6. Лечение опухолевого стеноза по типу 3б).
Пациент Ш 72 лет, переведен в НИИ СП им. Н. В. Склифосовского из другого лечебного учреждения, где он находился на лечении по поводу правостороннего пневмоторакса, там ему неоднократно выполнялось дренирование правой плевральной полости с эвакуацией воздуха.
При поступлении пациент предъявлял жалобы на боли в правой половине грудной клетки и одышку при умеренной физической нагрузке. Объективно: общее состояние средней тяжести, сознание ясное. Дыхание самостоятельное, везикулярное, через естественные дыхательные пути, аускультативно определяется ослабление дыхания справа, частота дыхательных движений (ЧДД) 18 в мин: АД 120\75 мм.рт.ст.; ЧСС 80 в мин; Сатурация 94%.
В анамнезе: верифицированный центральный рак правого легкого T3N1M0 стадия IIIА, хроническая обструктивная болезнь легких по эмфизематозному типу, гипертоническая болезнь 3 степени. Ранее лечился по поводу туберкулеза легких и двухсторонней полисегментарной вирусной пневмония среднетяжелой степени тяжести после перенесенного COVID-19.
Из вредных привычек: курение сигарет более 60 лет - 1 пачка/день.
По данным КТ ОГК: выявлено объемное образования в корне правого легкого, вызывающего сужение просвета промежуточного бронха; ателектаз средней и нижней долей правого легкого; посттуберкулезные изменения легких; правосторонний пневмоторакс; парасептальная и центрилобулярная эмфизема обоих легких с наличием булл и перифокальной инфильтрацией справа.
При трахеобронхоскопии просвет промежуточного бронха правого легкого ниже шпоры верхнедолевого бронха сужен до 0,1 см за счет циркулярной экзофитной опухоли.
Пациенту с правостороним пневмотораксом по данным КТ было выполнено дренирование правой плевральной полости, по дренажу эвакуировано большое количество воздуха и около 100 мл серозной жидкости.
На 5-е сутки после дренирование плевральной полости пациенту была выполнена ангиография с эмболизацией правой бронхиальной артерии цилиндрическими эмболами Эмбокс-Ц 600 мкм.
После дренирования и эмболизации правой бронхиальной артерии пациенту в условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, было выполнено эндоскопическое оперативное вмешательство: произведена интубация трахеи тубусом ригидного бронхоскопа №12. Первым этапом была выполнена бронхография: контрастированы расширенные сегментарные бронхи нижней доли; среднедолевой бронх контрастируется в виде культи, протяженностью 1,0-2,0 см, сегментарные бронхи средней доли не контрастируются, протяженность опухолевого стеноза 2,0 см. Далее на коже установлены метки (рентгенпозитивные) для определения границ опухолевого поражения. Вторым этапом по струне-проводнику в область опухолевого стеноза заведен биполярный электрод и выполнена реканализация просвета бронха посредством деструкции опухоли, после чего просвет бронха был восстановлен до 0,5 см. В целях визуализиации за опухолевый стеноз в проекцию средне-долевого бронха заведен SpayScope системы SpyGlass. Визуализирован слепо заканчивающийся средне-долевой бронх, сегментарные бронхи полностью вовлечены в опухолевый процесс, просвет их не определяется, нижнедолевой и сегментарный бронхи нижней доли интактные.
Третьим этапом под рентген контролем по каналу бронхоскопа, по струне-проводнику в просвет нижнедолевого бронха заведено доставочное устройство и установлен саморасширяющийся полностью покрытый стент HANAROCTENT Multi-Hole диаметром 10 мм, длиной 60 мм. Проксимальный край стента расположен на уровне шпоры верхнедолевого бронха правого легкого. Далее выполнена санация бронхов стерильным физиологическим раствором в объеме 30 мл.
Интраоперационно была взята биопсия образования и отправлена на гистологическое исследование. По данным морфологического исследования в пределах полученного материала морфологическая картина соответствует ороговевающей плоскоклеточной карциноме.
После стентирования жалобы на одышку исчезли, дыхание самостоятельное. Физикальные данные при выписке: АД 110\75 мм.рт.ст.; ЧСС 80 в мин.; ЧДД 18 в мин.; Сатурация 97-98%. При контрольном КТ ОГК ателектаз полностью разрешился, при трахеобронхоскопии определяется удовлетворительное состояние стента.
Пациент был выписан на 14-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц.
Клинический пример 7. Лечение опухолевого стеноза по типу 3с).
Пациент М. 58 лет, госпитализирован в НИИ им. Н.В. Склифосовского с инструментальной картиной низкоинтенсивного легочного кровотечения на фоне центрального рака правого легкого и одышкой 3 степени (по шкале mMRC).
Из анамнеза известно, что в течение последних 3-х месяцев больной отмечает нарастание одышки, кашель и повышение температуры тела до 38,0С. Ранее находился на стационарном лечении в отделении пульмонологии с диагнозом внебольничная правосторонняя долевая пневмония. При дообследовании (КТ, ФБС) выявлено образование верхнедолевого бронха с нарушением его проходимости, гистологически был выявлен мелкоклеточный рак. На фоне лечения отметил некоторое кратковременное улучшение. При ПЭТ КТ выявлен опухолевый стеноз верхнедолевого бронха.
В экстренном порядке пациенту на 1-е сутки после госпитализации выполнена ангиография бронхиальных артерий. По данным ангиографии отмечается гиперваскуляризация и перекалибровка дистального русла правой бронхиальной артерии, после чего выполнена ее эмболизация микроэмболами.
В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12. Просвет верхнедолевого бронха правого легкого циркулярно сужен до 0,1 см, опухоль затрагивает все сегментарные бронхи и шпору верхнедолевого бронха. По катетеру, под рентгенологическим контролем, в просвет суженного верхнедолевого бронха проведена струна проводник с атравматическим концом. Далее по струне в просвет нижнедолевых бронхов проведен катетер и выполнено контрастирование бронхов. При контрастировании протяженность опухолевого сужения около 6 см.
По струне проводнику в просвет опухолевого стеноза проведен катетер для РЧА аббляции ELRA 7-4B18L. Выполнено 2 сеанса РЧА на всем протяжении, длительность 2 минуты, мощность 10 Ватт, темп 75 градусов. После РЧА кровоточивости нет, просвет верхнедолевого бронха расширен до до 0,4 см в диаметре. В просвет стеноза проведено доставочное устройство саморасширяющегося полностью покрытого стента HANAROCTENT Multi-Hole диаметром 8мм, длиной 80 мм. При контрольном осмотре проксимальный край стента расположен на уровне шпоры верхнедолевого бронха, дистальный край стента расположен на уровне межсегментаной шпоры верхнедолевых бронхов.
После стентирования жалобы на одышку исчезли. Физикальные данные при выписке: АД 125\85 мм.рт.ст.; ЧСС 77 в мин.; ЧДД 18 в мин.; Сатурация 97-98%. При контрольном КТ ОГК и трахеобронхоскопии состояние стента удовлетворительное.
Пациент был выписан на 4-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц.
Клинический пример 8. Лечение опухолевого стеноза по типу 4.
Пациентка Е 51 года, поступила с жалобами на одышку при минимальной физической нагрузке и кашель с трудноотделяемой мокротой.
Из анамнеза: ретроперитонеосокопическая адреналэктомия слева по поводу адренокортикального рака; метостазы в легкие и л/у средостения. Проведено 8 курсов химиотерапии. В связи с массивным опухолевым поражением правого главного бронха со стенозированием и ателектазом нижней доли пациентке проводились многократные процедуры ФБС с комбинированным восстановлением проходимости бронхов.
По данным КТ ОГК и трахеобронхоскопии выявлено центральное образование со стенозированием просвета главного и промежуточного бронхов правого легкого, и проксимального отдела главного и нижнедолевого бронхов левого легкого.
Пациенту выполнено эндоскопическое оперативное вмешательство. В условиях операционной под тотальной внутривенной анестезией с применением релаксантов, с высокочастотной вентиляцией, произведена интубация трахеи тубусом ригидного бронхоскопа №12. При трахеобронхоскопии: карина представлена опухолевым инфильтратом и резко расширена. Просвет правого главного бронха практически полностью перекрыт опухолью исходящей из медиальной полуокружности правого главного и промежуточного бронхов. Дистальнее просвет нижнедолевых бронхов резко сужен до 0,2-0,3 см в диаметре за счет перибронхиальной инфильтрации. Первым этапом выполнена РЧА зондом, проведенным через канал эндоскопа. После аббляции просвет правого главного и промежуточного бронхов удалось расширить до 0,6-0,7 см в диаметре. Отмечается умеренная контактная кровоточивость. Экзофитная порция новообразования в зоне бифуркации также коагулирована аргоноплазменным катетером до образования коагуляционого струпа.
Просвет левого главного бронха на 0,5 см дистальнее карины сужен на 1\2 за счет инфильтративной опухоли по латеральной полуокружности. Протяженность сужения около 1,5 см., дистальнее по передней стенке левого главного бронха, на 0,5 см выше междолевой шпоры определяется участок инфильтративной опухоли с экзофитной порцией до 0,6 см в диаметре. Выполнена электроэксцизия экзофитной порции образования полипэктомической петлей в режиме коагуляции. Просвет нижнедолевого бронха левого легкого полностью обтурирован экзофитной опухолью, которая имеет широкое основание по задней стенке бронха.
Выполнена АПК аббляция инфильтративной части опухоли левого главного бронха и экзофитной порции опухоли нижнедолевого бронха. Вторым и третьим этапом выполнено контрастирование и установлением меток на коже для определения границ опухолевого поражения. Далее в просвет бронхов поочередно проведена струна, по струне-проводнику в просвет левого главного бронха проведено доставочное устройство стента, под рентгенологическим контролем выполнена установка и позиционирование стента HANAROCTENT Multi-Hole длиной 40 мм, диаметром 16 мм. Далее по струне проводнику в просвет правого главного и промежуточного бронхов установлен саморасширящийся металлический полностью покрытый стент HANAROCTENT Multi-Hole длиной 40 мм, диаметром 16 мм. После раскрытия стентов, была выполнена санация бронхов стерильным физиологическим раствором в объеме 10 мл.
При контрольном осмотре проксимальные края стентов расположены на уровне бифуркации, дистальный край стента правого главного бронха расположен в просвете нижнедолевого бронха. Дистальный край стента левого главного бронха расположен на 0,5 см выше междолевой шпоры.
Интраоперационно была взята биопсия образования. По данным морфологического исследования в пределах полученного материала морфологическая картина соответствует нейроэндокринной опухоли.
После стентирования жалобы на одышку исчезли. Физикальные данные при выписке: АД 120\80 мм.рт.ст.; ЧСС 80 в мин.; ЧДД 18 в мин.; Сатурация 98%. При контрольном КТ ОГК и трахеобронхоскопии состояние стентов удовлетворительное.
Пациент был выписан на 3-е сутки после оперативного вмешательства с положительной динамикой и рекомендациями наблюдения у врача терапевта и онколога по месту жительства, с контрольным эндоскопическим осмотром через 1 месяц.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ БИЛАТЕРАЛЬНОГО ЭНДОПРОТЕЗИРОВАНИЯ НИЖНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ ПРИ БИФУРКАЦИОННОМ СТЕНОЗЕ | 2022 |
|
RU2784980C1 |
| КОМПЛЕКТ СТЕНТОВ ДЛЯ БИЛАТЕРАЛЬНОГО ЭНДОПРОТЕЗИРОВАНИЯ НИЖНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ ПРИ БИФУРКАЦИОННОМ СТЕНОЗЕ | 2022 |
|
RU2796867C1 |
| УСТРОЙСТВО ДЛЯ РЕКАНАЛИЗАЦИИ СТЕНОЗОВ ТРАХЕИ И БРОНХОВ | 2021 |
|
RU2770280C1 |
| СПОСОБ ЛЕЧЕНИЯ ЦЕНТРАЛЬНЫХ СТЕНОЗИРУЮЩИХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ТРАХЕИ И БРОНХОВ | 2013 |
|
RU2533979C1 |
| СПОСОБ СТЕНТИРОВАНИЯ БИФУРКАЦИИ ТРАХЕИ | 2011 |
|
RU2465850C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ ПАТОЛОГИЕЙ ОРГАНОВ ДЫХАНИЯ, ОСЛОЖНЕННОЙ ЛЕГОЧНЫМИ КРОВОТЕЧЕНИЯМИ | 1998 |
|
RU2140211C1 |
| Способ лечения рубцовых и компрессионных стенозов трахеи | 2021 |
|
RU2771934C1 |
| СПОСОБ Y-ОБРАЗНОЙ РЕКОНСТРУКЦИИ БИФУРКАЦИИ ТРАХЕИ ПОСЛЕ ВЕРХНЕЙ ЛОБЭКТОМИИ С РЕЗЕКЦИЕЙ S6 СЛЕВА | 2021 |
|
RU2759340C1 |
| Устройство для реканализации стенозов трахеи и бронхов | 2021 |
|
RU2754739C1 |
| СПОСОБ ПРОТЕЗИРОВАНИЯ ПРОТЯЖЕННЫХ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ ТРАХЕИ | 2021 |
|
RU2783694C1 |
Изобретение относится к медицине, а именно к хирургии. При локализации опухоли в области карины с вовлечением одного главного бронха выполняют селективное стентирование главного бронха под рентгеноскопическим контролем саморасширяющимся металлическим покрытым стентом, снабженным перфорацией. При локализации опухоли в области карины с вовлечением обоих главных бронхов выполняют билатеральное стентирование главных бронхов. При локализации опухоли в главном бронхе без вовлечения междолевой шпоры выполняют селективное стентирование главного бронха. При этом дистальный край устанавливают в один из интактных долевых бронхов. При локализации опухоли в главном бронхе без вовлечения междолевой шпоры выполняют билобарное стентирование долевых бронхов. При этом в область стеноза заводят два металлических саморасширяющихся стента с полимерным покрытием и отверстиями с последующим их одновременным раскрытием. При локализации опухоли в долевом бронхе без вовлечения сегментарных бронхов селективно выполняют стентирование долевого бронха. При этом дистальный край стента устанавливают на уровне слияния сегментарных бронхов. При локализации опухоли в долевом бронхе с вовлечением на один и более сегментарных бронхов селективно выполняют стентирование долевого бронха. При этом дистальный край стента устанавливают в один из интактных сегментарных бронхов. При локализации опухоли в долевом бронхе с вовлечением всех сегментарных бронхов и междолевую шпору выполняют стентирование интактного долевого бронха с перекрытием пораженного бронха. При локализации опухоли мультифокально в разных бронхах выполняют стентирование двумя и более стентами. Способ позволяет повысить эффективность эндоскопического лечения пациентов с опухолевыми стенозами бифуркации трахеи и бронхов 1-3 порядка, сократить время, затрачиваемое на установку стентов. 8 ил., 1 табл., 8 пр.
Способ выбора тактики эндоскопического лечения пациентов с опухолевыми стенозами бифуркации трахеи и бронхов 1-3 порядка, основанного на доставке и установке под рентгеноскопическим контролем саморасширяющихся металлических покрытых стентов, снабженных перфорацией, характеризующийся тем, что
при локализации опухолевого стеноза в области бифуркации трахеи на уровне бифуркации трахеи с распространением на один - правый или левый - главный бронх проводят стентирование пораженного главного бронха одним стентом, не перекрывая интактные главный и долевой бронхи; в случае распространения опухолевого стеноза на оба главных бронха проводят билатеральное стентирование двумя стентами с расположением проксимальных концов стентов в просвете интактной части трахеи на одном уровне, дистальных концов стента в левом и правом главных бронхах на уровне междолевых шпор и последующим одновременным раскрытием стентов;
при локализации опухолевого стеноза в главном бронхе, в случае, когда опухоль не затрагивает междолевую шпору бронха или шпору верхнедолевого бронха, проводят стентирование пораженного бронха одним стентом, который устанавливают с расположением дистального конца стента в просвете долевого бронха, а проксимального конца - на уровне карины, с обеспечением вентиляции интактного долевого бронха через перфоративные отверстия в стенте; в случае расположения опухоли с вовлечением междолевой шпоры бронхов или шпоры верхнедолевого бронха проводят билобарное стентирование с одновременным заведением в пораженный бронх двух стентов с расположением проксимальных концов стентов в просвете главного бронха на одном уровне и последующим одновременным раскрытием стентов;
при локализации опухолевого стеноза в долевом бронхе в одном долевом бронхе без вовлечения сегментарных бронхов проводят стентирование одним стентом с расположением его дистального конца, не перекрывая сегментарные бронхи или перекрывая 1 сегментарный бронх, и установкой проксимального конца на уровне междолевой шпоры, не перекрывая интактный долевой бронх; при локализации опухоли в долевом бронхе с распространением на два и боле сегментарных бронха проводят стентирование одним стентом с расположением его дистального конца в интактном сегментарном бронхе с перекрытием пораженных сегментарных бронхов и проксимального конца на уровне междолевой шпоры, при перекрытии интактных сегментарных бронхов с обеспечением их вентиляции через перфоративные отверстия в стенте; в случае распространения опухолевого стеноза на все сегментарные бронхи и на междолевую шпору бронха проводят стентирование интактного долевого бронха с перекрытием пораженного долевого бронха;
в случае мультифокальной локализации опухоли, когда опухолевый стеноз расположен в просвете разных бронхов с вовлечением или без области бифуркации трахеи, стентируют все интактные бронхи с перекрытием пораженных бронхов.
| СПОСОБ БИЛАТЕРАЛЬНОГО ЭНДОПРОТЕЗИРОВАНИЯ НИЖНИХ ДЫХАТЕЛЬНЫХ ПУТЕЙ ПРИ БИФУРКАЦИОННОМ СТЕНОЗЕ | 2022 |
|
RU2784980C1 |
| US 4586505 A, 06.05.1986 | |||
| Гасанов А.М | |||
| и др | |||
| Первый опыт применения саморасширяющегося металлического Y-стента у пациента с декомпенсированным опухолевым стенозом трахеи и главных бронхов | |||
| Эндоскопическая хирургия | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| Пантелеев В.С | |||
| и др | |||
| Клинические случаи успешного эндоскопического стентирования | |||
Авторы
Даты
2025-03-03—Публикация
2024-10-24—Подача